从采出水去除钡和NORM的方法与流程
本申请根据35 U.S.C. §119(e)要求2014年3月7日提交的美国临时申请序列号61/949,364的优先权,所述申请全文通过引用结合到本文中。
关于联邦资助的研究和开发的声明
本发明在政府支持产生,根据美国能源安全研究合作组织(RPSEA)的分包合同10122-07,RPSEA根据原合同DE-AC-07NT42677为美国能源部的承包方。政府拥有本发明的某些权利。
发明领域
本发明的实施方案总体上涉及处理水的方法,更具体地讲,涉及从采出水去除钡和天然存在的放射性物质(NORM)(例如,镭)的方法。
发明背景
从非常规气源(例如页岩气生产)对美国能源供应的贡献正显著增长。水在页岩气生产中广泛用于钻探和水力破碎过程,因此,水管理是关键问题。采矿、钻探和水力破碎分别需要考虑过程后水处理。例如,水力破碎产生采出水,采出水可包含显著量天然存在的放射性物质(“NORM”)(包括镭),与很高盐度水平和高水平硬度离子(包括镁、钙、锶和钡)结合。此外,也经常存在铁和锰。可溶钡有毒性,并且可能沉淀,导致在处理设备上结垢。镭则致癌。
一些采出水可通过深井注入处置。然而,在某些地方,包括宾夕法尼亚,通过深井注入处置采出水的能力可能受到限制。因此,至少在这些地方,用允许其它用途和/或处置的经济方法处理采出水是必要的。
以前尝试已用硫酸盐沉淀处理采出水和去除放射性物质和钡,允许以后再用或处置水。在此过程中,大体积固体和硫酸盐沉淀产生,并从水分离。硫酸盐沉淀对高盐度水是有效处理,但形成很细的颗粒分散体(粒径小于100微米),它难以从水分离。颗粒沉降速率太慢,以致于不允许重力分离。
过滤,例如压滤,可用于帮助从水分离硫酸盐沉淀,但滤器昂贵,且由于分散体的小粒径并非完全有效。
因此,需要一种从采出水去除NORM和钡的方法,该方法利用硫酸盐沉淀,而且提供快速且成本有效的方法。另外,也需要产生固体盐产物以实现较高水回收的方法。
发明概述
在一个实施方案中,本发明为一种从采出水去除钡和天然存在的放射性物质的方法。方法包括用硫酸盐源预处理具有约4.0至约10.0范围pH的采出水,以形成硫酸钡、硫酸镭或其组合的悬浮体;用阴离子絮凝剂处理经预处理的采出水;并从硫酸钡、硫酸镭或其组合重力分离经处理的采出水。
在另一个实施方案中,本发明为一种从采出水制备回收盐产物的方法。方法包括,从采出水去除钡和天然存在的放射性物质;使经分离的水蒸发,以形成蒸馏水和浓盐水;从浓盐水结晶出盐晶体;并洗涤盐晶体,以制备回收盐产物。从采出水去除钡和天然存在的放射性物质包括:用硫酸盐源预处理具有约4.0至约10.0范围pH的采出水,以形成硫酸钡、硫酸镭或其组合的悬浮体;用阴离子絮凝剂处理经预处理的采出水;并从硫酸钡、硫酸镭或其组合重力分离经处理的采出水。
在另一个实施方案中,本发明为一种从采出水制备具有低浓度钡和NORM的回收盐产物的系统。系统包括,钡和NORM处理装置;重力分离单元;从经分离的水产生蒸馏水和浓盐水的蒸发单元;构造成从浓盐水产生盐晶体的结晶单元;和构造成洗涤盐晶体以制备回收盐产物的结晶处理单元。钡和NORM处理装置构造成用硫酸盐源预处理具有约4.0至约10.0范围pH的采出水,以形成硫酸钡、硫酸镭或其组合的悬浮体;并用阴离子絮凝剂处理经预处理的采出水。重力分离单元构造成从硫酸钡、硫酸镭或其组合分离经处理的水。
不同实施方案提供处理采出水以去除钡和NORM(例如,镭)的快速经济方法。在其它实施方案中,制备具有低水平钡和NORM的盐产物和蒸馏水。
附图简述
从以下本发明实施方案的说明,可推断本发明的另外的特征、使用可能性和优点。在这样做时,本发明的目的由各个所描述或所说明的实施例单独或以任何组合代表,而不依赖概述或引用或说明书或附图中的图解。在附图中:
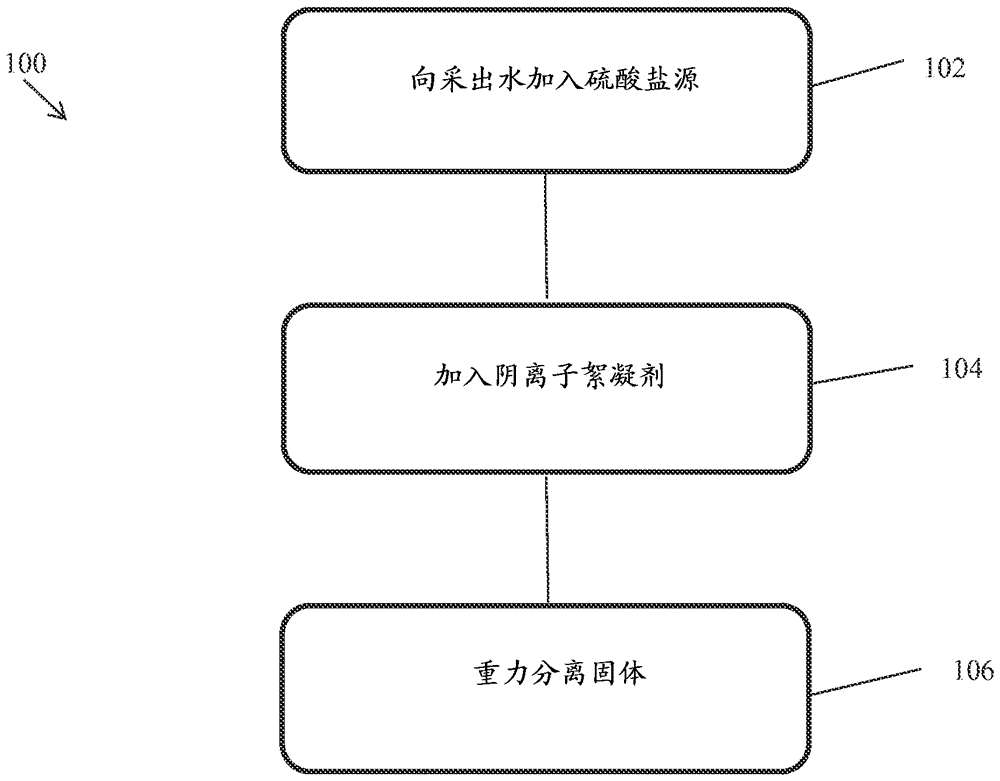
图1为根据本发明的一个实施方案,钡和NORM去除方法的示意流程图;
图2为根据本发明的一个实施方案,从采出水制备具有低浓度钡和天然存在的放射性物质的回收盐产物的方法的示意流程图;并且
图3为描绘制备回收盐产物的系统的示例性实施方案的示意图。
发明详述
除非本文另外清楚地指明,单数形式“一”和“所述”包括复数对象。叙述相同特征的所有范围的端点可独立组合,并且包含所述端点在内。
本文所述的任何数值包括以1单位增量从较低值到较高值的所有值,其条件为在任何较低值和任何较高值之间隔离至少2个单位。例如,如果陈述组分的量或工艺变量(例如,温度、压力、时间等)的数值为例如1至90,则在本说明书中旨在明确列举例如15至85、22至68、43至51、30至32等的数值。对于小于1的数值,则适当将1单位认为是0.0001、0.001、0.01或0.1。这些只是明确预期的实例,在所列举的最低值和最高值之间的数值的所有可能组合均应认为是在本申请中以类似方式明确陈述。
与量相关使用的修饰词“约”包含所述值在内,并且具有由上下文确定的意义(例如,包括与具体量测量相关的容许范围)。
本发明的一个方面为从采出水去除钡和NORM的方法。方法包括:用硫酸盐源预处理具有约4.0至约10.0范围pH的采出水,以形成硫酸钡、硫酸镭或其组合的悬浮体;用阴离子絮凝剂处理经预处理的采出水;并从硫酸钡、硫酸镭或其组合重力分离经处理的采出水。
本文所用采出水应指作为采矿、钻探、水力破碎或其它资源提取过程的副产物的水,包括水力破碎回流水、井完成水、地层水和“压裂水”。然而,应了解,如果希望从样品去除钡或NORM(例如镭),可对任何液体样品利用水处理方法。采出水通常有很高的盐度,并且可包含高水平钡或NORM,例如镭。例如,一些采出水包含大于200mg/L钡。在另一个实例中,采出水包含1000mg/L或更多钡。在另一个实例中,采出水包含2,000mg/L或更多钡。在另一个实例中,钡可以约300mg/L至约30,000mg/L或更多的范围存在于采出水中。采出水可包含大于500pCi/L镭。在一个实例中,钡可以约500pCi/L至约18,000pCi/L或更多的范围存在于采出水中。采出水可具有超过20,000mg/L的总溶解固体。在本发明的一个实施方案中,采出水包含大于70,000mg/L总溶解固体(TDS)。在另一个实例中,采出水包含约20,000mg/L至约400,000mg/L或更多量的总溶解固体。在另一个实例中,采出水包含约50,000至约300,000mg/L TDS或更多量的总溶解固体。在关注的采出水中,大部分离子一般为钠和氯。
在采出水中发现的污染物的实例显示于表1中,表1显示在马赛勒斯页岩气采出水中发现的数个类型污染物的分析。分析来自宾夕法尼亚,马赛勒斯页岩气点的九个采出水样品。表1提供在样品中发现的范围上限和下限和中值的污染物列表。
表1. 马赛勒斯采出水组成
在一个实施方案中,方法包括调节采出水的pH,如果需要或者如果希望将水调节到特定pH或范围。通过在本领域已知的任何常规方法调节pH,例如,加入至少一种酸和/或碱。在一个实施方案中,可利用加入石灰、氢氧化钠、氢氧化钾、氢氧化铵、盐酸、硫酸、硝酸、苏打灰、碳酸氢钠、二氧化碳或其任何组合调节pH。在本发明的一个实施方案中,通过加入石灰、氢氧化钠或其组合调节pH。
本发明的实施方案通过用硫酸盐处理在宽pH范围有效去除钡和镭。例如,用硫酸盐源预处理的水可具有约4.0至约10.0的pH。在另一个实施方案中,pH在约5.0至约10.0的范围内。或者,pH可在约5.0至约9.0,约5.0至约9.5,约7.0至约10.0,约8.0至约10.0,约7.0至约9.5,约9.0至约9.5或约9.0至约10.0的范围内。在一个实施方案中,碳酸盐预处理在pH 9.0进行,这特别有效地从采出水去除钡和镭。相比之下,过高pH,例如11.0,使阴离子絮凝剂不太有效地产生絮凝物,同时增加大量废物流。
采出水的pH可在硫酸盐沉淀之前调节,或者可与硫酸盐沉淀同时调节。在另一个实施方案中,可进一步在硫酸盐沉淀后调节pH。氧化动力学在较高pH较快,使得金属离子(例如Fe2+和Mn2+)的氧化需要较小的容器和/或停留时间,如下更详细讨论。
硫酸盐源可以为提供硫酸根离子到采出水且适合与采出水中存在的钡和NORM反应的任何类型化合物。在一个实施方案中,硫酸盐源不引入需要危险物质处置或另外去除技术的另外元素。在一个实施方案中,硫酸盐源为硫酸钠、硫酸钾、硫酸镁、硫酸钙、硫酸锶或其组合。在另一个实施方案中,硫酸盐源为硫酸钠,因为它是廉价的硫酸盐源,不含需要危险物质处置的元素。虽然硫酸镁、硫酸钙和硫酸锶可以是硫酸盐源,但它们具有低于硫酸钠的溶解性,因此,在去除钡和镭中低效。
硫酸盐源可以有效从采出水沉淀钡或NORM的任何量(剂量)加入。所加硫酸盐源的量可基于采出水中硫酸根与溶解的钡的摩尔比。在一些实施方案中,加入硫酸盐源达到约0.90至约1.20的硫酸根:钡比率。在另一个实施方案中,硫酸根:钡比率为约1.00至约1.15。在另一个实施方案中,硫酸根:钡比率为约1.10至约1.13。
硫酸盐源加到采出水导致钡和镭分别沉淀成硫酸钡和硫酸镭。根据过程条件、采出水组成和硫酸根:钡摩尔比,钙和锶沉淀也可分别作为硫酸钙和硫酸锶出现。在一些实施方案中,用硫酸盐源预处理采出水包括以下至少之一:(1)硫酸盐源递增加到采出水;(2)硫酸盐源以一批加到采出水;和(3)在加硫酸盐源期间和/或之后和用阴离子絮凝剂处理经预处理水之前搅动或搅拌采出水。
搅动或搅拌硫酸盐源与采出水可进行约0.25分钟至约30分钟。在另一个实施方案中,搅动或搅拌可进行约1分钟至约15分钟。在另一个实施方案中,搅拌混合物约3分钟至约10分钟。在另一个实施方案中,搅拌混合物约5分钟至约10分钟。在其它实施方案中,可搅拌混合物,经过以下范围之一:约0.25分钟至约15分钟,约0.25分钟至约10分钟,约0.25分钟至约5分钟,约1分钟至约30分钟,约1分钟至约3分钟,或约1分钟至约5分钟。
在一个实施方案中,阴离子絮凝剂为聚电解质。阴离子絮凝剂以充分从经预处理水絮凝硫酸盐沉淀的量(剂量)加入。例如,所得经处理水中阴离子絮凝剂的浓度可在约1.0至约150mg/L的范围内。或者,可加入阴离子絮凝剂,以得到落在以下范围之一内的阴离子絮凝剂浓度:1.25mg/L至约125mg/L,约1.25mg/L至约12.50mg/L,约6.25mg/L至约12.50mg/L,约6.25mg/L至约25.0mg/L,约1.25mg/L至约50.0mg/L,约1.25mg/L至约125.0mg/L,或约6.25mg/L至约50.0mg/L。
阴离子絮凝剂具有在约1,000,000至约50,000,000道尔顿范围的分子量。在一个实施方案中,阴离子絮凝剂具有例如在约15,000,000道尔顿至约50,000,000道尔顿范围的高分子量。在另一个实施方案中,阴离子絮凝剂具有在约1,000,000道尔顿至约10,000,000道尔顿范围的低分子量。或者,阴离子絮凝剂的分子量可在以下范围之一:约15,000,000至约50,000,000道尔顿,约1,000,000至约30,000,000道尔顿,约1,000,000至约25,000,000道尔顿,约15,000,000至约30,000,000道尔顿,约12,000,000至约25,000,000道尔顿,和约15,000,000至约25,000,000道尔顿。在一个实施方案中,阴离子絮凝剂具有约23,000,000道尔顿的分子量。
在加入阴离子聚电解质絮凝剂后,可搅拌(或搅动)经处理水足够量时间,以有效絮凝在经预处理水中生成的沉淀。在一个实施方案中,搅拌经处理水约1至约10分钟。在另一个实施方案中,搅拌水约1至约5分钟。在一个实施方案中,随着絮凝物形成逐渐减小搅拌、搅动或混合强度(即,变得更缓和),以避免絮凝物破裂。在一个实施方案中,搅拌或搅动可在开始时剧烈,强度渐进性或逐渐减小。
在一个实施方案中,阴离子絮凝剂具有约5%至约50%的阴离子度。或者,阴离子絮凝剂的阴离子度可在约5%至约30%或约5%至约15%的范围内。在另一个实施方案中,阴离子絮凝剂的阴离子度最高约15%。在另一个实施方案中,阴离子絮凝剂具有小于25%的阴离子度。在一个实施方案中,阴离子絮凝剂具有约0.05mEq/g至约10.0mEq/g的电荷密度。在一个供选实施方案中,阴离子絮凝剂可具有约0.08mEq/g至约7.0mEq/g的电荷密度。
在一个实施方案中,阴离子絮凝剂为线型聚合物。在一个实施方案中,阴离子絮凝剂包括阴离子丙烯酰胺共聚物。阴离子丙烯酰胺共聚物可以为丙烯酰胺和丙烯酸的共聚物。共聚物可关于电荷和位置随机排列。在一个实施方案中,阴离子絮凝剂具有约50至约90%mol丙烯酰胺残基。或者,阴离子絮凝剂具有约70至约90%mol或约80至约90%mol丙烯酰胺残基,其中后者是特别有效的絮凝剂。阴离子聚电解质絮凝剂的实例为PolyFloc®
AE1115、AE1125、AE1700、AE1701和AE1702,均由GE-Betz售出。其中AE1700系列(即,AE1700-1703)具有极高分子量,即,大于15,000,000道尔顿。絮凝剂AE1125和1125具有低分子量,即,小于15,000,000道尔顿,具体地讲,小于11,000,000道尔顿。
在加入阴离子絮凝剂后,重力分离经处理的水。重力分离经处理水的澄清产物(clarate)和絮凝物可通过在本领域已知的任何常规方法进行。在一个实施方案中,重力分离可在澄清器、重力分离器、沉降槽或离心分离器中进行。絮凝物朝向水的顶部生成,并且可从经处理水的底部去除任何污泥。产生的絮凝物包含来自采出水的作为硫酸钡和硫酸镭沉淀的钡和镭。
絮凝物快速生成,从而使絮凝的沉淀从水快速容易地去除。在一个实施方案中,絮凝物在小于约15分钟内沉降。在另一个实施方案中,絮凝物在小于约10分钟内沉降。在另一个实施方案中,絮凝物在小于约5分钟内沉降。在另一个实施方案中,絮凝物在小于约3分钟内沉降。在一个实施方案中,在约1分钟至约15分钟范围内从溶液沉降出沉淀。在另一个实施方案中,该范围为约1分钟至约10分钟。在另一个实施方案中,该范围为约1分钟至约5分钟。在另一个实施方案中,该范围为约1分钟至约3分钟。在一个实施方案中,沉淀在约2分钟内沉降,在另一个实施方案中,沉淀在约1分钟内沉降。所得澄清产物具有大大减少的固体。
钡和NORM去除方法100的一个实施方案显示于图1中。方法100包括:将硫酸盐源加到具有约4.0至约10.0范围pH的采出水102,以形成硫酸钡、硫酸镭或其组合的悬浮体;将阴离子絮凝剂加到经硫酸盐处理的采出水104;并从硫酸钡、硫酸镭或其组合重力分离经处理水106。如上讨论,钡和NORM去除方法也可包括在硫酸盐处理之前或之后调节水的pH。钡和NORM去除方法也可包括在硫酸盐处理之前或之后对水通气,并去除从钡/NORM污泥分离的金属-氢氧化物污泥(在图1中未显示),这将在以下讨论。在一个实施方案中,离开从采出水去除钡和/或NORM的过程的重力分离水的钡浓度小于200mg Ba/升,这得到包含小于5mg/L钡的回收盐产物,例如氯化钠。在一些实施方案中,离开预处理过程的重力分离水也为pH中性。
为了再利用或处置,可用另外的预处理和处理步骤制备采出水。在一个实施方案中,可从水分离和去除水中的大体积固体,例如,在平衡池中。可在预处理采出水之前、在预处理和处理步骤之间或在重力分离经处理水期间分离大体积固体。
在另一个实施方案中,可从采出水去除铁和锰。铁和锰可存在于采出水中。在一个实施方案中,锰可以大于1mg/L的量存在。在另一个实施方案中,锰可以约1mg/L至50mg/L或更大存在。铁可以大于10mg/L的量存在。在另一个实施方案中,铁可以约10mg/L至约200mg/L或更大存在。
为了去除铁、镁、钙、锰或其组合,如果需要,用碱或酸调节水的pH,以达到约9.0至约10.0范围的pH。pH调节如上所述。采出水的pH调节到约9.0至约10.0,具体地讲,约9.0至约9.5,导致产生金属-氢氧化物污泥。金属-氢氧化物污泥可包含悬浮固体、有机物、铁、锰或其组合。具体地讲,铁和锰分别沉淀成三价铁固体(Fe(OH)3)和二氧化锰(MnO2)。镁沉淀成氢氧化镁。金属-氢氧化物的沉淀可在用硫酸盐源预处理采出水之前、同时或之后进行。即,加硫酸盐源在加碱之前、与加碱同时或在加碱之后进行。
在一个实施方案中,方法进一步包括在用硫酸盐源预处理之前从水分离由调节pH到约9.0至约10.0或约9.0至约9.5产生的金属-氢氧化物污泥。这允许在加入硫酸盐源之前处置金属-氢氧化物污泥。在此实施方案中,在分离金属-氢氧化物污泥后产生含硫酸盐的污泥。这允许分别处理金属-氢氧化物污泥和含硫酸盐的污泥。
或者,可在用硫酸盐源预处理采出水之后使铁、锰和镁沉淀。即,在加酸或碱源和分离所得金属-氢氧化物污泥之前加入硫酸盐源和分离其含硫酸盐的污泥。这也允许分别处置污泥,而不需要容纳随后产生的污泥。在分别处理时,可根据其具体废物流需要来处置掉金属-氢氧化物污泥和含硫酸盐的污泥。另外,单独地分别处理污泥防止污泥中废物的污染和积累,所述废物可另外在其它地方更容易或有效地处置。
在一个实施方案中,加入硫酸盐源和用于调节pH的酸或碱及何时分离生产的污泥的次序取决于:
(a)采出水中的干燥TSS(总悬浮固体)(mg/L)与采出水中的钡浓度(mg/L)之比,其中<0.1为低比率,≥0.1为高比率;
(b)干燥悬浮固体中的镭放射性,其中<1,400pCi/g为低放射性,≥1,400pCi/g为高放射性;和
(c)采出水中的镭放射性(pCi/L)与钡浓度(mg/L)之比,其中<0.85 pCi Ra/mg Ba2+为低比率,≥0.85 pCi Ra/mg Ba2+为高比率。
在此实施方案中,用这些参数确定加入硫酸盐源及碱和污泥处理的次序,如表2中所示。
表2.
例如且参照表2,在所有三个参数低或高时,加入碱源和硫酸盐源可以任何顺序或同时进行,并且可在加入两种源后分离产生的污泥。作为另一个实例,在干燥悬浮固体中的镭-226放射性高时,虽然两个比率低,但加入碱和硫酸盐可以任何顺序或同时进行,并且在已加入碱和硫酸盐源后分离产生的污泥,或者在加碱后分离铁-锰污泥,随后加入硫酸盐源,并分离含硫酸钡和/或硫酸镭的污泥。
在另一个实施方案中,方法进一步包括在调节pH到约9.0至约9.5后对采出水通气。通气帮助氧化采出水中的溶解铁、锰和镁。通气可用室内空气完成,并且应进行足以氧化pH采出水中存在的铁和锰的时间。相信室内空气中的CO2帮助Ca+2离子沉淀成CaCO3。在一个实施方案中,施加通气约60分钟。在另一个实施方案中,通气可进行约30分钟至约120分钟。
在一个实施方案中,在硫酸盐源加到采出水之前对采出水通气。可在从采出水分离大体积固体之后但在从采出水分离硫酸盐沉淀之前进行通气。或者,可在分离大体积固体或硫酸盐沉淀步骤之前进行通气。在另一个实施方案中,在分离任何大体积固体和硫酸盐沉淀步骤之后进行通气。
在一个实施方案中,方法进一步包括加入凝固剂。凝固剂可以为在本领域已知的任何常规凝固剂。可使用的凝固剂的一些实例包括氯化铁、硫酸铁、聚氯化铝、聚胺、聚氯化二烯丙基二甲基铵(polyDADMAC)、单宁、硫酸铝、硫酸亚铁或其组合。在一个实施方案中,凝固剂包括聚氯化铝、聚胺和丙烯酰胺的混合物。凝固剂以有效促进絮凝物生成的量加入。在一个实施方案中,凝固剂可以约0.1mg/L至约100mg/L的量加入。在另一个实施方案中,凝固剂可以约1mg/L至约50mg/L的量加入。在另一个实施方案中,凝固剂可以约10mg/L至约30mg/L的量加入。凝固剂可与阴离子絮凝剂一起加入,或在加阴离子絮凝剂后加入。在一个实施方案中,在仅用硫酸盐源和阴离子絮凝剂处理产生混浊的澄清产物时,例如,澄清产物具有大于20mg/L TSS、大于40mg/L TSS或大于100mg/L TSS,则加入凝固剂。在另一个实施方案中,在使用低分子量阴离子絮凝剂时,例如,小于15,000,000道尔顿,具体地讲,小于11,000,000道尔顿,则可加入凝固剂。
本发明的另一个方面为一种从采出水制备具有低浓度钡和天然存在的放射性物质的回收盐产物的方法。方法包括,从采出水去除钡和天然存在的放射性物质;使经分离的水蒸发,以形成蒸馏水和浓盐水;从浓盐水结晶出盐晶体,例如氯化钠;并洗涤盐晶体,以制备回收盐产物。去除钡和天然存在的放射性物质包括:用硫酸盐源预处理具有约4.0至约10.0范围pH的采出水,以形成硫酸钡、硫酸镭或其组合的悬浮体;用阴离子聚电解质絮凝剂处理经预处理的采出水;并从硫酸钡、硫酸镭或其组合重力分离经处理采出水。
在一个实施方案中,经分离的采出水具有200mg/L或更小的钡浓度。通过具有在经分离的水中200mg/L或更小的钡浓度,回收盐产物包含小于5mg/L钡。回收盐产物为从总过程回收的盐,总过程包括去除钡和镭,蒸发,结晶,和洗涤盐晶体。在一个实施方案中,经分离的采出水具有100mg/L或更小钡浓度,这提供相对于回收盐产物内钡和镭含量的安全限度。在经分离的采出水中的钡浓度为100mg/L或更小时,回收盐产物具有约0.002pCi/g的估计镭放射性,这是低于岩盐典型值的数量级。在另一个实施方案中,经分离的采出水具有80pCi/L或更小的镭浓度,使得回收盐产物具有约0.002pCi/g的估计镭放射性。
可根据在本领域已知的任何常规方法蒸发经分离的水。例如,可利用包含构造成驱动桨叶的发动机的容器,并且底部排放去除结晶浆料。蒸发可例如在大气压进行,直至固体重量分数为例如经分离的水的两倍。
在一个实施方案中,蒸发的程度和蒸发的蒸馏水的量取决于数个因素,包括浓缩多少样品,表示为质量浓度系数。质量浓度系数可如式(1)中所示计算:
两个质量浓度系数可如式(2)和(3)中所示计算:
y1 = -0.00001446x + 2.046 (2)
y2 = -2.359ln(x) + 25.846 (3)
其中x为进料钡浓度(mg/L),y为质量浓度系数。
应控制蒸发,使得最终质量得到高于第一计算浓度(y1)且低于第二浓度系数(y2)的质量浓度系数y。即,在一些实施方案中,浓度系数在y1和y2(分别为式(2)和(3)的质量浓度系数)之间。以此方式控制蒸发防止氯化钡和氯化钠共结晶,使氯化钠晶体不含氯化钡固体,并能够通过简单处理方法去除。在进料钡浓度为约27,000mg/L(在此以上变得难以避免共结晶)时,式(2)和(3)的计算浓度系数趋于一致。因此,在一个实施方案中,进料钡浓度<27,000mg/L。
结晶导致产生盐晶体,包括例如氯化钠。可通过在本领域已知的任何常规方法并在本领域常用的任何温度进行结晶。例如,可在约106℃至约114℃范围进行浓盐水结晶。在一个实施方案中,蒸发和结晶在蒸发器-结晶器中以分批方式进行。
在一个实施方案中,可由真空过滤使盐晶体脱水,这可通过在本领域已知的常规方法进行。例如,在真空过滤期间可使用1μm滤器。在一个实施方案中,1μm滤器为玻璃纤维滤器。在另一个实施方案中,可通过在本领域已知的任何常规方法真空干燥脱水的晶体。例如,可在95℃真空干燥脱水晶体过夜。在另一个实施方案中,进一步处理脱水晶体,以通过在本领域已知的任何常规方法,例如洗涤,从晶体表面去除夹带的母液,以使盐晶体中的钡和其它杂质最大限度地减少。
这种方法的一个实施方案显示于图2中,总称为250。方法250包括,从采出水100, 200去除钡和NORM,如图1中所述;使分离水202蒸发;结晶出盐晶体204;并洗涤盐晶体206。方法250导致产生回收盐产物,例如氯化钠。经分离的水蒸发产生蒸馏水和浓盐水,使浓盐水晶体,并处理以形成回收盐产物。洗涤盐晶体可包括脱水和干燥,且结晶器浓缩物在脱水步骤作为系统排放物去除。
图3图示说明根据本发明的一个实施方案可执行从采出水250制备具有低浓度钡和NORM的回收盐产物的方法的系统350。系统350包括,钡和NORM处理装置10;重力分离单元20;蒸发单元30;结晶单元40;和结晶处理单元50。然而,应了解,蒸发单元30和结晶单元40可以为完成两种单元功能的单一单元。
钡和NORM处理装置包括供应采出水的采出水供应线路12;供应硫酸盐源到装置的硫酸盐源供应线路14;供应阴离子絮凝剂的阴离子絮凝剂供应线路16;供应酸和/或碱以调节水的pH的酸和/或碱供应线路18,如上讨论。应理解,一些供应线路可合并成单一供应线路,例如硫酸盐源供应线路14和阴离子絮凝剂供应线路16例如作为处理供应线路(未显示)。在钡和NORM处理装置中产生的浆料通过分离单元20经线路22分离。在此,重力分离单元20从污泥(通过污泥线路24去除)分离澄清产物,即,经分离水。澄清产物从重力分离单元20经线路26送到蒸发单元30。蒸馏水从蒸发单元30通过线路32去除,而产生的浓盐水经线路34送到结晶单元40。结晶单元40使浓盐水结晶产生盐晶体,盐晶体通过线路42转移到结晶处理单元50。进一步处理和/或洗涤盐晶体,如上讨论,以制备回收盐产物。
如上讨论,在一个实施方案中,钡和NORM处理装置可包括调节pH和/或通气(在图3中未显示),以产生金属-氢氧化物污泥。可在硫酸盐源加到采出水之前、之后或同时进行pH改变物质加入和通气。另外,可包括另外分离步骤(在图3中未显示),以使金属-氢氧化物污泥和硫酸盐沉淀污泥分别去除,从而允许分别处理污泥。
为了使本领域的技术人员能够更好实施本发明,给出以下实施例,这些实施例作为说明,而不作为限制。
实施例
实施例1-6和比较性实施例1-5
向2升锥形瓶加入采出水(1130g),并按BaCl2·2H2O补加6.2g/L Ba。用NaOH调节pH至9.0,并通过鼓泡器通空气60分钟。下一步,采出水中的每mol钡加入1.1mol Na2SO4,作为180mL的2.8M NaSO4,搅拌15分钟,并将20mL混合物等分到各个20mL瓶。向各瓶加入絮凝剂作为0.5%vol溶液,以达到1.25mg/L、12.5mg/L或125mg/L浓度。絮凝剂由它们的GE-Betz产品号确定,例如AE1700。将各瓶在200RPM(转/分钟)搅拌2分钟,在60RPM搅拌2分钟,然后重力分离2分钟。通过Hach DR 3900仪器测定澄清产物总悬浮固体水平。表3显示,阴离子絮凝剂(即,AE1115、AE1125、AE1700、AE1701、AE1702和AE1703)表现得在数量级上优于比较性实施例CE-1所示的没有絮凝剂和比较性实施例CE-2至CE-5的阳离子絮凝剂(即,PolyFloc®CP1154、CP1156、CP1158和CP1160,各阳离子絮凝剂购自GE-Betz),如2分钟沉降时间后澄清产物中剩余的测定悬浮固体所示。
表3
实施例7-12和比较性实施例6
实施例7-12和比较性实施例6在与实施例1-6和比较性实施例1-5相同的规程下进行,不同之处在于调节pH到4.0,且总悬浮固体水平通过目视检查确定。目视检查等级从最澄清的澄清产物(由4表示)到最混浊的澄清产物(由1表示)。如表4中所示,与阳离子絮凝剂比较性实施例6(CE-6)比较,阴离子絮凝剂在pH 4.0表现好,参见实施例7至12。即,与CE-6比较,大部分阴离子絮凝剂能够以1.25mg/L或12.5mg/L浓度在目视检查时达到3或4,对于检验的所有3个浓度,CE-6从未达到高于最混浊分级1的目视检查得分。
表4
实施例13-15
进行2升瓶试验,以进一步评定阴离子絮凝剂AE1125、AE1700和AE1702促进分离钡和/或NORM(镭)的硫酸盐诱导沉淀的能力。用1.4升采出水填充各Phillips & Bird PG-700系列标准瓶检验器系统,水已预先用NaOH处理,并经空气注入。各瓶得到248mL的0.28M Na2SO4,并在150RPM搅拌5分钟。根据表5、6和7中所示最终浓度加入絮凝剂。在300RPM搅拌混合物10秒,在100RPM搅拌2分钟,在60RPM搅拌3分钟,然后在20RPM搅拌15分钟。这些混合条件模拟水处理(具体地讲,絮凝过程)期间的常规混合操作,其中随着絮凝物生成混合变得更缓和,以避免絮凝物在送到澄清器之前破坏。然后,根据样品,重力分离样品1分钟或10分钟。目视检查各2升瓶,并用Hach DR3900便携仪器测定总悬浮固体。目视检查与总悬浮固体测定一致,因而在此未报告。
应注意到,在絮凝剂加入后在水表面上生成膜,它具有与絮凝物相似的颜色。这表明,膜可以是阴离子絮凝剂和硫酸钡沉淀的组合。这种膜未在没有絮凝剂的对照样品中观察到。另外,膜倾向于在样品期间重新分散,因此,可具有受影响的估计总悬浮固体。
可从表5、6和7看到,阴离子絮凝剂AE1125、AE1700和AE1702的测定总悬浮固体(mg/L)分别基本上低于对照,对照在1分钟和10分钟沉降后都具有高总悬浮固体。在12.5mg/L和25mg/L较低浓度比较时,AE1700和AE1702具有低于AE1125的测定总悬浮固体。AE1700在6.25mg/L特别有效地降低总悬浮固体测定值,而AE1702在12.5mg/L更有效地降低总悬浮固体测定值。
表5. 实施例13:阴离子絮凝剂AE1125
表6. 实施例14:阴离子絮凝剂AE1700
表7. 实施例15:阴离子絮凝剂AE1702
表8显示实施例13C(25mg/L AE1125)、14C(12.5mg/L AE1700)和15B(6.25mg/L AE1702)的分析结果,除非另外指明,否则以mg/L表示。即,对未处理进料和干固体污泥及经处理过滤的澄清产物测定钡、锶、钙、镁、锰、铁、钠和/或硫的浓度。例如,实施例14C(12.5mg/L AE1700)和15B(6.25mg/L AE1702)的澄清产物中的钡含量为47mg/L和37mg/L。相比之下,实施例13C(25mg/L AE1125)的澄清产物钡含量为450mg/L。
表8
实施例16-18
在30升容器中对絮凝剂AE1125、AE1700和AE1702进一步评价沉降性能。采出水掺加BaCl2·2H2O,以达到6,200mg钡/升采出水。用20%重量NaOH溶液调节掺加钡的采出水的pH,以达到pH 9.0,并通气至少60分钟,以使Fe+2氧化成Fe+3,Mn+2氧化成Mn+4。用1.064升1.4M Na2SO4溶液处理该浆料,以达到1.10的硫酸根:钡摩尔比。向经硫酸盐处理的水加入絮凝剂AE1125、AE1700和AE1702,以分别达到25mg/L, 6.25mg/L和12.5mg/L。含AE1125的瓶也接收25mg/L凝固剂GE-Betz KlarAidTM CDP1336,以确定是否可去除在实施例1和12期间从该低分子量阴离子絮凝剂剩余的颗粒。然后将经絮凝剂处理的水用顶部搅拌器在110RPM搅拌10秒,在45RPM搅拌2分钟,在30RPM搅拌3分钟,最后在10RPM搅拌15分钟。设计搅拌规程,以通过使用本领域的技术人员已知的常规混合方程使所用规程与上述2升瓶实施例匹配。搅拌后,重力分离絮凝物。在沉降1分钟和10分钟后,从30升容器顶部抽出澄清产物。通过Hach DR 3900悬浮固体方法测定澄清产物总悬浮固体。另外,抽1升澄清产物用于重力悬浮固体测定,在分析前通过1μm玻璃纤维滤器过滤。在沉降15分钟后从容器排出经处理污泥。重力分离污泥1-3天,同时定期去除澄清产物,直到不再形成澄清产物。将污泥称湿重,并在真空烘箱中在95℃干燥,以得到干重。通过使用电感耦合等离子体(ICP)和利用γ光谱的镭-226,二者均根据本领域的技术人员已知的常规方法,分析采出水、经处理澄清产物和经处理污泥的钡、锶、钙、镁、锰、铁、硫和钠。
如表9所示,来自实施例16、17和18的10分钟澄清产物样品没有可见颗粒存在。在封盖搁置4小时后,样品有可见颗粒。在采样后4-24小时进行的重力悬浮固体测定反映固体增加。不受任何特别理论限制,相信颗粒是由于硫酸盐不断沉淀,具体地讲,硫酸钡。
表9
进一步分析实施例16-18,以测定未处理采出水、干固体污泥和经处理过滤的澄清产物中存在的226-镭、钡、锶、钙、镁、锰、铁、硫和/或钠的量。在通过0.45μm滤器过滤后,通过ICP分析所有液体样品。未处理采出水在通过γ光谱法的镭-226分析前不过滤。如上讨论进行ICP和γ光谱法。通过酸化溶解经干燥的固体污泥样品,过滤,并通过ICP分析。
不受任何理论限制,相信对未处理采出水中铁和锰观察到的可变性可能是由于在处理前暴露于空气的变化,这导致在任何处理前铁和锰氧化和沉淀程度的变化。另外,相信采出水中钡、锶、钙和镁的可变性反映总体采出水制备、采样和分析过程的再现性。未处理采出水样品的镭-226放射性可变性最可能是由于在采出水样品之间悬浮固体量的变化。
可在表10中看到,与实施例16、17和18的未处理、经过滤采出水比较,在干固体污泥和经处理过滤的澄清产物中钡浓度和镭-226放射性大大降低。除非另外说明,否则所有测定结果以mg/L表示。
表10
虽然已关于某些实施方案描述了本发明,但本领域的技术人员应理解,可在不脱离本发明的范围下进行各种变化,并且可用等效要素代替。另外,可在不脱离本发明的范围下作出很多修改,以使具体情况或材料适应本发明的教导。因此,预期本发明不限于所公开的具体实施方案,但本发明应包括落在所附权利要求范围内的所有实施方案。
- 还没有人留言评论。精彩留言会获得点赞!