用于从甲烷和氨催化制备氰化氢的方法与流程
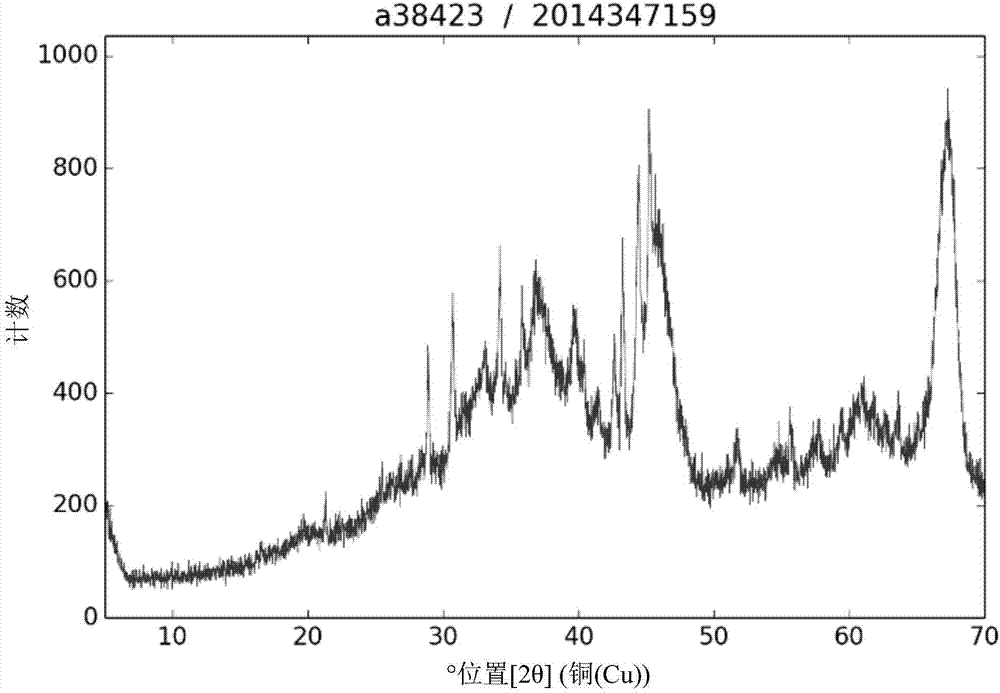
由甲烷和氨制备氰化氢的已知方法包括氧化andrussow法和非氧化甲烷-氨(degussa/bma)法和shawinigan法。andrussow法使用pt-rh或pt-ir网纱(gauze)催化剂;甲烷-氨(bma)法使用pt网纱催化剂。这两种方法都需要高温:andrussow法需要大于1000℃的温度,甲烷-氨(bma)法需要大于1200℃的温度。shawinigan法不使用催化剂,并且需要将过程温度保持在大于1500℃。ullmann’senclyopediaofindustrialchemistry;cyanocompounds,inorganic,2012p676。已知方法所需的高温是由于过程的吸热性质。然而,在较高温度下,氨分解为氮和氢的竞争性副反应也是热力学有利的。angew.chem.int.ed.(2011),50,4601-4605。为了降低生产成本和竞争性副反应,降低反应过程所需的温度是有利的。为了降低过程的温度,可以选择放热的氧化方法如andrussow方法而非吸热的非氧化方法。然而,andrussow方法仍然需要大于1000℃的温度,并且比吸热的非氧化方法的操作更不安全。更安全的方法是优选的。为了降低生产成本的另一个优点是降低所使用的材料的成本。期望使用替代性的、较便宜的催化剂金属,例如基础金属fe、co、ni,而不是贵金属如pt。关于研究替代性的催化金属的使用,angew.chem.int.ed.(2011),50,4601-4605提供了基于描述符的(descriptor-based)对于各种催化剂金属用于从甲烷和氨制备氰化氢的活性和选择性的倾向的了解。所分析的信息是模拟碳和氮在过渡金属表面上的吸附能量的结果。应该注意,所分析的结果是理论模型而不是实际例子。该文章涉及pt催化剂,并且提出除了其他金属之外,钴(co)在1100℃的温度下对于氨的吸附是活性金属。氨吸附是氰化氢生产和氮生产的竞争性副反应的前体步骤。理论反应条件表明,包含co的催化剂会产生显著量的氮,因此对于氰化氢生产不会具有选择性。因此,还期望提供一种方法,其使用更便宜的催化剂金属并且对于氰化氢的生产具有选择性。所描述的现有技术提供了用包含pt的网纱催化剂在高于1000℃的温度下从甲烷和氨制备氰化氢的方法。本发明提供了包含更便宜的金属即fe、co或ni的催化剂,其中催化剂对于氰化氢的生产是选择性的,且优选在低于1000℃的温度下进行。本发明的催化剂提供了另外的优点,例如使用催化剂的更便宜形式如颗粒和挤出物的能力。技术实现要素::本发明提供了一种催化剂材料,其包含载体、在所述载体上的第一金属和第二金属,其中所述第一和第二金属为化合物的形式,其中所述第一金属为fe、co或ni,并且其中所述第二金属选自sn,zn和in。第一和第二金属形成化合物,使得在载体上不存在大量游离的第一金属即fe、co或ni,并且不存在大量游离的sn、zn或in。相反,fe、co或ni在载体上与sn、zn或in形成合金。应当注意,术语“化合物(chemicalcompound)”涵盖单一化合物以及多于一种化合物。因此,催化剂材料可以包括两种或更多种化合物或相,例如化合物的混合物。该催化剂对于优选在低于1000℃的温度下从甲烷(ch4)和氨(nh3)选择性地制备氰化氢(hcn)的过程是有活性的。本发明的催化剂包含fe、co或ni、氧化铝和选自sn、zn和in的金属。例如,载体包括氧化铝、氧化铝的尖晶石、氧化物、碳化物、氮化物或碳氮化物。在一个实施方案中,第一和第二金属与碳或氮形成三元化合物。这种三元化合物例如描述在以下文献中:“ternarycarbidesofthetransitionmetalsnickel,cobalt,iron,manganesewithzincandtin”,h.h.stadelmaierandl.j.huetter,actametallurgica,vol.7,june1959,page415-419。催化剂的第一金属可以优选包含co。在一个实施方案中,第一金属包含co,第二金属包含sn。例如,第一金属是co,第二金属是sn。sn和co可以是二元合金的形式或是在图1所示的co-sn合金的稳定区域内的相的紧密混合物的形式。氧化铝意指任何形式的氧化铝,包括勃姆石、α-氧化铝和γ-氧化铝。优选形成α-氧化铝。任何其它高温稳定的催化剂载体是可能的,例如氧化铝的尖晶石,如znal2o4或mgal2o4;氧化物,如ceo2、zro2;碳化物和氮化物。本发明的催化剂可以是用于改变的或改性的催化剂的前体。在活化和/或操作期间,氧化物可以被还原成金属状态,例如变成碳化物或氮化物。该第三相或三元化合物可以作为氮化物和/或碳化物产生。co和金属的重量百分数的比率为约5:1至约1:5、5:1至1:5、约3:1至约1:3、3:1至1:3,为约1:2.4,为1:2.4。在一个实施方案中,催化剂的载体是铁磁性载体。载体可以包含co,并且第二金属可以涂覆到载体上。当载体是铁磁性时,在本发明的催化剂存在下进行的吸热化学反应的热量可以通过改变围绕催化剂的电磁场来快速提供。本发明还涉及从甲烷(ch4)和氨(nh3)制备氰化氢(hcn)的方法,其中使甲烷和氨与本发明的催化剂接触,并且该方法的温度优选小于1000℃。该方法可以在低于1000℃的温度下进行,例如700℃至低于1000℃,750℃至950℃,800℃至850℃。该方法在惰性气氛中,例如在氮气气氛中进行。当载体是在方法中用作感应加热元件的铁磁性载体时,可以通过感应加热来提供用于该方法的热量。例如,载体包含co,并且第二金属涂覆在载体上。因此,催化剂易于诱导加热,其可以通过改变围绕催化剂的电磁场来产生。在一个实施方案中,催化剂的载体是在由甲烷和氨制备氰化氢的方法中用作感应加热元件的铁磁性载体。载体可以包含co,且第二金属可以涂覆在载体上。本发明的其它方面涉及:一种用于由甲烷(ch4)和氨(nh3)制备氰化氢(hcn)的催化剂,其包含fe、co或ni、氧化铝和选自sn、zn和in的金属。催化剂可以包含co。催化剂可以包含co、氧化铝和sn。在一个实例中,fe、co或ni与sn、zn或in的重量百分数的比率为约5:1至1:5。作为实例,fe、co或ni与sn、zn或in的重量百分数的比率为约1:2.4。图1是co-sn相图,且图2a-2d是根据本发明的废催化剂的xrd图。图1是如从landolt-“numericaldataandfunctionalrelationshipsinscienceandtechnology”,“groupiv:macroscopicpropertiesofmatter”,volume5,“phaseequilibria,crystallographicandthermodynamicdataofbinaryalloys”,subvolumec,ca-cd…co-zr,b.predel的第370页图1所看到的co-sn相图。图1示出了钴(co)和锡(sn)在400至2000k的温度下的相平衡;此外表明了curie温度tc。因此,图1是显示sn和co的不同相的存在的合金图。cosn合金可以包含这些离散相或不同相中的一种或多种。这种离散相(或离散相的混合物)也称为“化合物”。图2a-2d是根据本发明的废催化剂的xrd图。在图2a中,主相是给出高背景的eta/γ-al2o3。结晶相是co3sn2。在图2b中,主相是给出高背景的eta/γ-al2o3和无定形碳。结晶相是co3sn2、γ-co1.5sn、cosn、β-cosn3、cosn2。在图2c中,主相是给出高背景的eta/γ-al2o3和一些无定形碳。结晶相是co3sn2、γ-co1.5sn、cosn、cosn2、一些co3snc。在图2d中,主相是给出高背景的eta/γ-al2o3和无定形碳。结晶相是co3sn2、γ-co1.5sn、cosn、cosn2、一些co3snc。对于所有四个图2a-2d,适用以下参考代码表:在参考代码表中表示为b、d和k的化合物属于具有六方晶格几何形状的相同空间群(p6/mmm,191)。然而,表示为b、d和k的化合物的晶格常数略有不同:b:d:k:对于图2a,适用以下xrd图的对应表:对于图2b,适用以下xrd图的对应表:对于图2c,适用以下xrd图的对应表:对于图2d,适用以下xrd图的对应表:编号位置[°2θ]匹配119,6306k;a;g228,8349k330,6535e;c433,0501g;f534,1283k635,7544g;f737,1051c;f839,5928k;c;a940,3438f1041,3497l1142,6181f1243,2328e;k;c;f1343,8319g;f1444,4379e;c1545,162c;g1645,9434c;a;f1747,9066k;c;l;f1854,3276c;l;f1955,5601c2057,6956c;g2159,4596e;c2260,7162c;a;f2362,6767c;g;f2463,5352e;c2567,2371c;f实施例:一般催化剂制备:本发明的催化剂可以通过将第一金属如co和第二金属的盐溶液浸渍到载体上来制备。catalystpreparationscienceandengineering,editedbyjohnregalbuto,crcpress,2007,page341和preparationofcatalystsi:scientificbasesforthepreparationofheterogeneouscatalystseditedbyg.poncelet,p.a.jacobs,b.delmon,pages430-440公开了通过浸渍方法的示例性催化剂制备。盐溶液可以是硝酸盐、氯化物、硫化物或有机络合物。在浸渍之后,将催化剂在80℃至150℃干燥并在500℃至700℃煅烧。在反应之前,通过在600℃至900℃的温度下使催化剂暴露于h2而使其还原。也可以通过相关化合物前体的共沉淀来制备催化剂混合物。可以将催化剂成型为粒料、挤出物或在干燥步骤之后粉碎成颗粒。在还原期间,本发明的催化剂形成一种或多种双金属混合物形式的合金(或合金的混合物)。在反应期间,催化剂可以与碳形成三元合金例如co3snc或与氮形成三元合金例如cosnn。一般氰化氢(hcn)的制备:通过在h2气氛下的还原来制备催化剂。将预热的ch4和nh3的流混合并送至含有催化剂的温度为750℃至1000℃的反应器,该催化剂包含载体或支撑物以及双金属化合物或组分。在反应器的出口处,出口流出物被冷却以冷凝氰化氢(hcn)。可以处理或再循环残余气体。可以通过o2气氛下的氧化来使催化剂再生。实施例1-8:将催化剂在850℃下在10%h2在n2的流中(使用约900nml/min的流速)还原4小时。载体是煅烧氧化铝,双金属化合物或组分是co和sn。将cosn/al2o3催化剂压制成粒料(直径13mm,高度3.5mm),然后将粒料分成1/6至1/2的原始尺寸的碎片。用1000nml/min的21%的o2在n2的流使催化剂再生,同时以5℃/分钟的速率将温度从100℃升至850℃。在实验期间,通过装备有hayesepq柱和tcd检测器的气相色谱仪来分析气体产物的h2、ch4和hcn含量。通过一个单独的gc程序来测量ch4浓度,而通过另一个来测量hcn。表1:在包含co、sn和氧化铝的催化剂存在下由甲烷和氨制备氰化氢ch4:nh3vol%/vol%为10:10。表2:在包含co、sn和氧化铝的催化剂存在下由甲烷和氨制备氰化氢在实施例9-12中,ch4:nh3vol%/vol%为70:30。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1
- 一种1‑氨基异喹啉‑6‑甲醇的制备方法与流程
- 3‑羟基氮杂环丁烷盐酸盐及N‑Boc‑3‑羟基氮杂环丁烷的制备方法与流程
- 一种多羟基双酮类葫芦烷型三萜及其制法和用途的制作方法与工艺
- 一种五羟基二酮类葫芦烷型三萜及其制法和用途的制作方法与工艺
- 具有氨基烷氧基取代的抗菌碱性双芳族衍生物的制作方法与工艺
- 基于乳剂状载体及三(羟甲基)氨基甲烷,至少一种氨基酸和氧化染料的组合的永久染发剂的制作方法与工艺
- 布渣叶黄烷酮‑2‑羟基化酶及其编码基因与应用的制作方法与工艺
- 利用Mannich反应制备2‑甲基‑4‑氨基‑5‑氰基嘧啶的方法与流程
- 采用水溶法得到的MAA结晶生产COS安乃近的方法与流程
- 采用酒溶法得到的MAA结晶生产COS安乃近的方法与流程