架构紧凑的六通道肿瘤标志物联检用微流控芯片装置的制作方法
本发明涉及一种架构紧凑的六通道肿瘤标志物联检用微流控芯片装置,属于分析测试领域。
背景技术:
肿瘤标志物(tumormarker,tm)是指在肿瘤的发生和增殖过程中,由肿瘤细胞本身所产生的或者是由机体对肿瘤细胞反应而产生的,反映肿瘤存在和生长的一类物质,包括蛋白质、激素、酶(同工酶)及癌基因产物等。化验患者血液或体液中的肿瘤标志物,可在肿瘤普查中早期发现肿瘤,并观察肿瘤治疗的疗效以及判断患者预后。目前临床上常用的肿瘤标志物有:(1)甲胎蛋白(afp)为原发性肝癌、睾丸癌、卵巢癌等肿瘤的标志物;(2)癌胚抗原(cea)为消化系统肿瘤、肺癌、乳腺癌等肿瘤的标志物;(3)糖类抗原125(ca125)为卵巢癌等肿瘤的标志物;(4)糖类抗原153(ca153)为乳腺癌等肿瘤的标志物;(5)糖类抗原19-9(ca19-9)为消化系统肿瘤的标志物;(6)糖类抗原724(ca724)为胃癌、卵巢癌等肿瘤的标志物;(7)糖类抗原242(ca242)为消化系统肿瘤的标志物;(8)糖类抗原50(ca50)为消化系统肿瘤、乳癌、肺癌等肿瘤的标志物;(9)cyfra21-1(cy211)为非小细胞肺癌等肿瘤的标志物;(10)神经元特异性烯醇化酶(nse)为小细胞肺癌、神经内分泌肿瘤等肿瘤的标志物;(11)前列腺特异性抗原(psa)为前列腺癌的肿瘤标志物;(12)人绒毛膜促性腺激素(hcg)为胚胎细胞癌、滋养层肿瘤(绒癌、葡萄胎)等肿瘤的标志物;(13)甲状腺球蛋白(tg)为甲状腺癌的标志物;(14)铁蛋白(sf)为消化系统肿瘤、肝癌、乳腺癌、肺癌等肿瘤的标志物;(15)β2-微球蛋白(β2-mg)在慢性淋巴细胞白血病、淋巴瘤、骨髓瘤、肺癌、甲状腺癌、鼻咽癌等患者体液中升高;(16)鳞状细胞抗原(scc)为宫颈癌、肺鳞癌、食管癌等肿瘤标志物。目前临床上检测的肿瘤标志物绝大多数不仅存在于恶性肿瘤中,也存在于良性肿瘤、胚胎组织、甚至正常组织中。因此,肿瘤标志物有动态检查和多项联合检查更有价值。那么对于众多的肿瘤标志物,临床上如何选择呢?不同的肿瘤会一些相对特异的肿瘤标志物,如ca153常出现在乳腺癌;cea常出现在肠癌、胃癌;ca19-9常出现在肠癌、胰腺癌;ca125常出现在卵巢癌等等。临床医生会根据不同的肿瘤检查不同的标志物。同一种肿瘤或不同类型的肿瘤可有一种或几种肿瘤标志物异常;同一种肿瘤标志物可在不同的肿瘤中出现。为提高肿瘤标志物的辅助诊断价值和确定何种标志物可作为治疗后的随访监测指标,可进行肿瘤标志物联合检测,合理选择几项灵敏度、特异性能互补的肿瘤标志物组成最佳组合,进行联合检测。一般来说肿瘤标志物的联合检测可提高对肿瘤诊断的正确率。
仅就多种肿瘤标志物其联合检测的相关技术背景其本身的概貌或总览而言,可以参见以下中国发明专利申请案:cn200410041175.3、cn200510026780.8、cn200610040051.2、 cn200910064647.x。
仅就微流控芯片技术其本身的整体概貌而言,可以参见著名微流控专家林炳承先生不久前出的专著“图解微流控芯片实验室”,该专著已经由科学出版社出版,该专著对于微流控技术的过去、现在,以及,未来展望等等方面,都有着详尽的、深入到具体细节的长篇论述。
那么,下面要谈谈本案特别关注的焦点问题。
微流控芯片的基本架构,包括刻蚀有微小液流通道的基片以及与之贴合在一起的盖片,所述基片上的微小液流通道,在装配上盖片之前,表观上看就是一些微槽道,要等到在其上覆盖了盖片之后,才真正闭合形成所述微小液流通道,该微槽道的槽道内表面连同包绕着该微槽道的那部分盖片一起构成所述的微小液流通道;那么,显然,装配完成了之后的该微小液流通道,它的内表面面积的主要部分是那个微槽道的内表面面积,换句话说,该微槽道内表面的状态或性质基本上决定了该微小液流通道的整体状态或性质;因此说,这个构建在基片上的微槽道的内表面状态或内表面性质是关键因素;原则上讲,任何的能够保持或基本保持其固体形态的材料,都能够用来制作基片及盖片,比如,能够用作基片及盖片的材料可以是单晶硅片、石英片、玻璃片、高聚物如聚二甲基硅氧烷、聚甲基丙烯酸甲酯、聚碳酸酯等等;当然,基片的选材和盖片的选材可以相同,也可以不相同;从材料耗费、制作难度以及应用普及前景等等方面来看,这些材料之间存在不小差异,尤其是那个基片的选材,影响较大。
在各种基片制作材料中,聚二甲基硅氧烷,即pdms,相对而言十分容易成型,在这样的基片上制作微槽道极其简单,并且该材料成本低廉,以该聚二甲基硅氧烷材料制作基片,在其上压制或刻蚀微槽道,并与玻璃或聚丙烯或其它塑料片等廉价材料制作的盖片相配合,貌似是一种比较理想的选择;当然,盖片材料也可以选择使用廉价的聚二甲基硅氧烷材料:那么,这种基片选材为聚二甲基硅氧烷材料的方案,材料极便宜,制作极简易,看似也应当极易于普及、推广。
但是,事情并非如此简单。
其一,这个聚二甲基硅氧烷材料,即缩写字母pdms所指代的材料,其本身是一种强烈疏水的材料,在这一材料上构建微槽道,如果不进行针对该微槽道表面的改性操作,那么,整体装配完成之后,即盖上盖片后,因结构中的所述微槽道其内表面占据了大部分的液流通道的内表面,那么,该pdms微槽道内表面其强烈的疏水特性,是决定性因素,它会使得类似于水溶液的极性液体微细液流的通过变得十分困难,其流动阻力之大,甚至一般的微泵都难以推动,当然,如果盖片也选择使用该pdms材料,那么,问题基本上一样,大同小异;因此,在现有技术之中,特别针对该pdms材料上的微槽道内表面进行改性修饰,是必须的操作;那么,这个针对pdms微槽道内表面的改性操作很麻烦吗?那倒也不是这个问题,构成严重技术困扰的,是另一个问题:这个pdms材料基片其体相内部的pdms聚合物分子具有自动向表面扩散、迁移的特性,这种基片体相内部pdms聚合物分子自动向表面扩散、迁 移的特性,将使得经过表面改性修饰的那个微槽道其内表面的改性之后的状态并不能维持足够长的时间,那个经表面改性之后的微槽道其内表面状态的维持时间大致仅够完成实验室内部测试实验的时间需要;换句话说,经过表面改性或表面修饰的该pdms微槽道内表面,其改性之后或曰修饰之后所形成的表面状态并不能持久,而是很快地自动趋于或曰变回表面改性之前的表面状态,在较短的时间里就回到那种原本的强烈疏水的表面状态,那么,试想,这样的微流控芯片能够大量制作、大量储存、广泛推广吗,答案很明显,那就是,不可能。这个pdms材料上的微槽道,不做表面修饰的话,类似于水溶液的极性溶液微细液流无法泵送通过,芯片也就没法使用;而如果做了表面修饰,又无法持久保持其修饰之后的状态,还是同样无法推广应用。
那么,如何做到既能够利用廉价的pdms材料来制作基片,而又能够解除所述微槽道内表面修饰状态无法持久、芯片无法大量制作、大量储备进而广泛推广这样一个令本领域众多专业人员长期纠结的困扰,就是一个明摆着的其技术障碍不可小觑的高难度问题。
该高难度问题已经存在很多个年头了,迄今为止,尚未得到妥善解决。
其二,未经表面修饰的pdms材料,上文已经述及,其表面强烈疏水,这种强烈疏水的材料表面并且还有另一个问题,那就是,这种强烈疏水的pdms表面会吸附生物大分子,并且,这些被吸附的生物大分子还会进一步地在pdms表面上更深一步的沉陷,渐陷渐深,直至沉陷入到pdms基片的体相之内,其实,这种过程,部分地也是由于pdms材料体相内部聚合物分子具有向表面扩散、迁移运动所导致;这种情况,也可以从另一个角度来解释,即,持续不断地由pdms体相内部向其表面扩散、迁移的那些聚合物分子,其运动的结果,是逐渐地将那些已经被表面吸附的生物大分子卷入pdms基片的体相之内,简单地说,这些被吸附的生物大分子就是被pdms基片体相吞没了;那么,这种pdms基片体相吞没生物大分子的现象,其所造成的影响,必然是导致涉及生物大分子的各类实验测试数据的严重偏差。
如上所述,pdms基片的问题是,它不但表面吸附生物大分子,而且吞没生物大分子,这样一来,作为实验测试对象的生物大分子其消失不会因为表面饱和吸附而停止,而是,不断被吸附,还不断地被吞没。
关于pdms基片在相关实验测试过程中其体相不断吞没测试相关生物大分子的现象,另一种解释是说,pdms体相内存在大量的微小气孔,相关生物大分子被表面吸附之后,沉陷进入这些微小气孔,进而被吞没;然而,本案发明人认为,那些能够容许微小尺度的空气分子挤入其间的所述微小气孔,不等于说它们也能直接容许相对大尺度的生物大分子进入,两者在尺度上差别巨大,不可一概而论。撇开解释,无论怎样,作为相关测试分析对象的生物大分子被pdms基片微槽道内表面吸附,进而不断被pdms基片体相所吞没,这是已知客观存在的现象。
为了阻止这种pdms基片体相对于生物大分子的吞没作用,可以从遏制pdms表面对生物大分子的吸附来着手解决,办法就是针对该pdms材料表面进行化学修饰改性,对于以 pdms为基片材料的情况来讲,就是对所述的微槽道部分的表面进行化学修饰改性,经过化学修饰改性的所述微槽道内表面,能够遏制其对生物大分子的吸附,进而避免生物大分子被pdms基片体相所吞没;但是,还是那个老问题,那就是,pdms材料表面上的化学修饰改性之后的表面状态无法持久保持,该pdms基片体相内部的聚合物分子其自动向表面扩散、迁移的过程,会很快地将那个经过表面化学修饰改性的微槽道内表面状态变回原本的强烈疏水并且强烈吸附生物大分子的状态,换句话说,无论该领域专业人员们怎样折腾,该pdms基片其微槽道内表面总是快速地向强烈疏水表面状态演变。
那么,如何既能够获得pdms材料价格极其低廉、基片制作极其简易的好处,又能够达成长期遏制该pdms基片微槽道内表面对生物大分子的吸附进程,进而阻止pdms基片体相对生物大分子的吞没作用,使得相关芯片制成品能够维持一个足够长时间的、合理的保质期,就是一个十分棘手的难题。该难题如同上文述及的另一个难题一样,同样令本领域众多专业人员长期纠结、困扰,该难题同样是一个明摆着的其技术障碍不可小觑的高难度问题。该难题也已经存在很多个年头了,迄今为止,也尚未得到妥善解决。
其三,如上所述,该pdms微槽道内表面强烈疏水,而针对性的表面化学改性或表面化学修饰又难于持久,因此,实际只能在其表面改性或表面修饰之后的表面状态尚属有效的短期之内使用它;倘若已经过了那个比较短暂的有效期限,而仍然强行使用的话,由于表面状态已然重新靠近疏水的状态,使用惯常的微泵驱动试样液流则必然存在比较大的流动阻力,这样,就只能靠加大微泵泵送功率及泵送压力来迫使试样液流向目标方向流动,如上所述,这种pdms材料比较柔软,以过高的、机械的泵送压力来泵送试样液流,将导致该基片其进样端包括进样端附近区域的所述微槽道发生鼓泡、膨化、扭曲、变形,并且,这种高压情况下,处于该进样端及其附近区域的微槽道及其周边也容易发生基片与盖片之间的剥离,此情形下,试样溶液将进入所述剥离之后形成的基片与盖片之间的出现的裂隙而四处横流,这实际导致该微流控芯片的毁损;当然,如果该表面改性或表面修饰原本就不到位,也会导致在短暂的惯常的有效期之内出现上述情形;在单纯采用外加微泵进行液流驱动的情况下,上述该问题始终存在。如上所述,如果完全没有做过任何所述表面改性或表面修饰等前置操作,那么,上述该问题将更为严重,即便没有发生进样端及其附近区域所述微槽道鼓泡、膨化、扭曲、变形以及基片与盖片之间剥离等问题,仅仅因为该流动阻力过大,采用高压微泵也未必能够驱动试样液流朝终端方向前进。
技术实现要素:
本发明所要解决的技术问题是,提供一个一揽子的解决方案,同时解决上文述及的三个方面的实际上相互牵扯在一起的一系列的难题,并且,将该解决方案应用于构建一种新型的能够针对六种比较典型的主要肿瘤标志物进行同时筛查、同时检测的微流控芯片装置。
本发明通过如下方案解决所述技术问题,该方案提供的装置是一种架构紧凑的六通道肿瘤标志物联检用微流控芯片装置,该方案其特点是,该装置的结构包括微流控芯片,该微 流控芯片的结构包括相互贴合装设在一起的基片和盖片,所述基片和盖片均为板状物或片状物,该基片的面向该盖片的那个面含有经由模压工艺或刻蚀工艺形成的槽道结构,相互贴合安装在一起的该基片与该盖片共同构建成了含有管道结构的微流控芯片,该管道的结构位置位于该基片与该盖片相互贴合的交界区域,该管道的两端分别与该微流控芯片的进样端以及终端连接,该进样端是该微流控芯片试样溶液的注入端,该终端是该微流控芯片实际进样测试时其芯片内试样溶液流动的终端,该终端与该进样端相互远离,该终端与该进样端之间的距离介于3厘米与10厘米之间,在该管道内不同位置上依顺序或逆序装设有工作电极以及对电极以及参比电极,所述顺序指的是所述参比电极其结构位置更靠近所述终端位置,所述逆序指的是所述参比电极结构位置更靠近所述进样端位置,所述工作电极由导电性电极以及贴附在该导电性电极上的包埋了肿瘤标志物抗体的金胶敏感膜构成,该管道的构造呈现并联构造,所述呈并联构造的管道由六条分支管道并联构成,所述呈现并联构造的所述管道其外形轮廓近似于并联电路的轮廓,所述工作电极的数量是六个,该六个工作电极的装设位置分别位于所述六条分支管道内,以及,该六个工作电极其表层金胶敏感膜结构中的肿瘤标志物抗体分别是对肿瘤标志物抗原能特异性结合的六种肿瘤标志物抗体物质,该六种抗体物质分别是肿瘤标志物抗体afp、cea、psa、ca125、ca19-9及ca15-3,所述抗原是广义的抗原,所述抗体是广义的抗体,所述工作电极其材质是金属银材质、黄金材质、碳素材质或热分解导电高分子材质,所述工作电极其形貌呈现柱状、片状或丝状,该基片其材质是聚二甲基硅氧烷材质,该基片其表面是原生形态的表面,该原生形态的表面其意思指的是没有经过任何表面化学修饰或任何表面化学改性的该材质的原生形态的表面,该装置的结构还包括链环式电磁夹具,该链环式电磁夹具其结构中共有六个环节,所述环节均呈条状、杆状或棒状,各相邻环节相互铰接形成链环,该链环其外形轮廓呈六边形环状结构,该六边形环状结构的每个顶角其结构位置均为铰接结构位置,该六边形环状结构其中的两个处于对边位置的环节其材质是导磁性材质,该六边形环状结构的余下四个环节其材质均是非磁性材质,所述非磁性材质指的是对外加磁场没有强烈响应的材质,该导磁性材质的两个环节之中的一个环节上缠绕有励磁线圈,该缠绕有励磁线圈的环节在其励磁线圈的两侧近邻位置上各装设有一个导磁性材质的极靴,共有两个所述极靴,该两个极靴均指向另一个导磁性材质的环节,该另一个导磁性材质的环节其表面上贴附固定装设有微型超声波换能器,依托电磁吸合力量的该链环式电磁夹具套接定位在该微流控芯片其所述终端的邻近位置,以及,高频振荡电讯号传输电缆,该高频振荡电讯号传输电缆的一端与该微型超声波换能器连接在一起;该链环式电磁夹具提供了一个方便该装置拆解的功能;该微型超声波换能器其主要功能是在微流控芯片实际进样测试时,利用其所发射的超声波来降低试样溶液与该微流控芯片其内部通道的内壁之间的界面张力,使其能够相容,并且,利用所述进样端以及所述终端与该微型超声波换能器装设位置之间的距离差异以及其所感受到的超声波强度上的差异,诱导形成所述进样端其界面张力与所述终端其界面张力之间的差异,该微流控芯片该两端之间的界面张力差异会在该微 流控芯片的该两端之间形成压力差异,该压力差异会驱动试样溶液向所述终端流动;该微型超声波换能器其功能还包括以其所发射的超声波遏止试样中所含有的生物大分子其在该微流控芯片其内部通道内表面上的吸附,进而遏止该聚二甲基硅氧烷材质的基片其体相对该生物大分子的吞没作用;柔软并具弹性的该聚二甲基硅氧烷材质的基片其功能包括以其对超声波强烈吸收的性质,对超声波进行强烈吸收,并藉此在该微流控芯片该终端到该进样端之间的有限的短距离之内实现超声波强度的快速递减;以及,微泵,该微泵与该进样端连接;该微泵的功能是,在该试样溶液与该微流控芯片其内部通道的内壁之间的界面张力受该超声波作用而降低、相间相容性增加的前提条件下,以该微泵的机械性泵送力量来与该超声波诱导的所述两端之间的界面张力差异其所带来的驱动力量互相支持、互相调适、互相耦合,以协同运作的方式汇聚成一股驱动试样液流向所述终端方向流动的力量。
所述肿瘤标志物抗体是广义的抗体,该广义的抗体指的是具备抗体功能或功能上类似于抗体的能够与各种相对应的临床所涉肿瘤标志物发生结合并形成免疫复合物或免疫复合物的类似物的物质;所述肿瘤标志物抗原是广义的抗原,该广义的抗原指的是能够利用相应抗体或功能上类似于抗体的物质进行酶标检测的各种临床所涉的需要鉴别、检测的肿瘤标志物。
所述励磁线圈一词其本身的技术含义是公知的。
所述导磁性材质一词其本身的技术含义是公知的;属于导磁性材质的材料例如纯铁、硅钢、软磁铁氧体等等。
本案所述非磁性材质指的是对外加磁场没有强烈响应的材质,属于所述非磁性材质的材料例如金属铜、金属锌、铜锌合金、金属铝、铝镁合金等等。
所述铰接一词其本身的技术含义在机械设计里领域是公知的。
所述微泵一词其本身的技术含义对于微流控芯片领域的专业人员来说是公知的。
所述微泵既可以是外置形式的微泵;该微泵也可以是做进或曰嵌入该微流控芯片内部其进样端结构位置或该进样端近邻结构位置的内置形式的微泵。
所述微泵例如微型的压电泵、微型的蠕动泵或微型的气动泵。
所述金胶敏感膜是将壳聚糖金胶溶液与肿瘤标志物抗体溶液充分混合均匀,用点样仪点样或涂布于指定结构位置,并使其干燥成膜而成。所述金胶敏感膜中的肿瘤标志物抗体均为辣根过氧化物酶或者葡糖糖氧化酶标记的肿瘤标志物抗体,所述金胶敏感膜已包含为固定上述各肿瘤标志物抗体而引入其中的辅助性介质,所述辅助性介质例如壳聚糖、醋酸纤维素、明胶其中的一种或它们的混合物。
所述微流控芯片结构中的所述管道包括所述分支管道,其内径尺寸均可以是任意选定的尺寸,但是,出于尽量少用待测液样以及降低试剂损耗等方面的考虑,所述管道包括所述分支管道优选毛细管级的通道,所述毛细管级的通道意即其内径与通常意义上的毛细管的内径相当的通道。所述毛细管其内部通道的横截面形状可以是任意的形状,所述横截面形状例 如圆形、椭圆形、方形、矩形、条形,当然也可以是任意的存在弯曲的线形,并且,所述毛细管的内部形状随着管道的延伸,不同部位的横截面形状也可以允许是不同的形状。仅就毛细管一词而言,其技术含义是公知的。
结构中涉及的对电极以及参比电极均为微小尺寸的电极,其电极形状均可以是任意选定的形状,所述任意选定的形状例如柱状、片状、条状或丝状等等。所述对电极以及所述参比电极其本身的词汇的技术含义是公知的。
仅就超声波换能器一词其本身的技术含义对于超声波技术领域的专业人员来说,是公知的。
各种尺寸、各种形状的超声波换能器均有市售;市售的微型超声波换能器其尺寸可以小到仅以毫米计算的量级。
仅就微型超声波换能器其在一般工业应用对象固态物体表面上的固定技术其本身而言,对于超声波技术领域的专业人员来说,是已知的一般技术。本案不对此展开赘言。
仅就裸的pdms基片其本身的微槽道模压或刻蚀技术来说,是极简单的已知的技术。
所涉高频振荡电讯号传输电缆其各种规格的工业产品市场均有售。
该装置的结构还可以包括高频振荡电讯号发生器;所述高频振荡电讯号传输电缆其另一端可以与该高频振荡电讯号发生器连接。
所涉高频振荡电讯号发生器其本身的技术,对于超声波技术领域的专业人员来说,是简单的和公知的;所述高频振荡电讯号发生器可以向超声波仪器专业厂家定制。
该微型超声波换能器其额定超声波发射功率的优选范围是介于5毫瓦与5000毫瓦之间;该微型超声波换能器其在运行时所发射的超声波的频率的优选范围是介于100khz与12mhz之间。
本案装置当然还可以进一步包括一些附件,所述附件例如多道电化学工作站等等,所述多道电化学工作站的技术含义是公知的。本案微流控芯片结构中涉及的各个工作电极以及对电极以及参比电极等,可以分别经由相应的专用串线与所述多道电化学工作站的相应接口进行联接。所述专用串线是用来将各所述电极与所述多道电化学工作站的各相应接口进行相互联接的专用电缆。本案装置中的所述微流控芯片,其结构也可以包括微阀,所述微阀的数量不限,根据实际需要,所述微阀可以装设在该微流控芯片结构中的任何需要安装的部位;该微阀一词对于微流控芯片技术领域的专业人员来说,其本身的技术含义是公知的;该微阀其本身的制作技术及使用技术亦是公知的;该微阀不是必需的构件。
所述工作电极的直径可以允许是任意设定的便于安装使用的适宜的直径,但是,推荐的或曰优选的所述直径其范围介于0.1微米至2000微米之间;所述工作电极的长度可以允许是任意设定的便于安装使用的长度,但是,推荐的或曰优选的所述长度其范围是在1微米至15000微米个之间。
通过喷涂或点样仪点样或其它合适工艺涂布装设于所述工作电极表面层的所述金胶敏感膜,其膜层厚度可以允许是任意设定的可对待测样液发生电性信号响应的厚度,但是,推荐的厚度或者说是优选的厚度是介于10纳米与200纳米之间。
芯片结构中的所述盖片,其材质可以允许是任何的电绝缘性材质,例如:聚丙烯、玻璃、聚甲基丙烯酸甲酯、聚二甲基硅氧烷,等等,为了做出更小尺寸的微流控芯片,比如做成长度仅2.0厘米到3.0厘米的超小尺寸的微流控芯片,并在该极短的距离内实现对超声波的极快速衰减,可以优选聚二甲基硅氧烷来作为盖片。当然,在大尺寸的微流控芯片上选择使用聚二甲基硅氧烷来作为所述盖片,也是本案技术方案所允许的。
所述盖片及基片其厚度可以允许是任意设定的便于装配的厚度,推荐的厚度或曰优选的厚度是介于1.0毫米与5.0毫米之间。较小的厚度有利于节省材料。
本案微流控芯片的使用方法:
本案以所述双驱动耦合运作模式驱动液流在该六通道微流控芯片的毛细管通道中流动,利用多通道电化学分析仪器分别对六种典型肿瘤标志物抗原进行联合检测。
本案微流控芯片的具体检测使用步骤如下:
1、在微管路中加入血清样品液,在所述双驱动耦合运作模式驱动下,各种肿瘤标志物抗原分子被各通道中电极表面上金胶敏感膜包埋的相应的辣根过氧化物酶标记的肿瘤标志物抗体捕获。
2、辣根过氧化物酶标记的肿瘤标志物抗体与血清样品中的肿瘤标志物抗原形成免疫复合物。
3、采用多通道电化学分析仪,加入邻苯二酚等电子媒介体,采用安培法检测上述反应引起的电流变化,由此获得各种分析物的种类和含量。
4、将结果进行综合分析,对肿瘤标志物抗原进行综合诊断。
本发明的优点是,在所述微流控芯片的所述终端其邻近位置依托电磁吸合力量套接定位所述的链环式电磁夹具,以该链环式电磁夹具其一个导磁性环节上所贴附安装的微型超声波换能器,利用其所发射的低功率、高频频段的超声波,使得未经过表面化学改性或表面化学修饰的强烈疏水的该微流控芯片内部管道其管壁与测试对象水溶液之间的相容性大幅增加,这为试样液流的通过提供了一个现实可能性;同时,利用聚二甲基硅氧烷基片其对超声波的强烈吸收能力,在比较短的距离内,也就是,从所述终端到所述进样端之间的仅数厘米尺度的很短的距离内,达成超声波强度的快速递减,藉此在该微流控芯片的所述两端造成所述界面张力的差异,该两端之间的界面张力的差异会导致一种驱动力量,该种因界面张力差异而导致的驱动力量其功能是驱赶试样液流在原本强烈疏水的毛细管通道内向所述终端方向流动;而结构中同时存在的所述微泵,其功能是,在该试样溶液与该微流控芯片其内部通道的内壁之间的界面张力受该超声波作用而降低、相间相容性增加的前提条件下,以该微泵的机械性泵送力量来与该超声波诱导的所述两端之间的界面张力差异其所带来的驱动力量 互相支持、互相调适、互相耦合,以协同运作的方式汇聚成一股驱动试样液流向所述终端方向流动的力量;该微泵的存在,使得该微型超声波换能器其超声波发射强度能够被允许适度降低,这对于检测对象中含有超声波敏感成分的情形尤其适宜;而由于该超声波换能器及其所辐射超声波的存在,能够提高相间相容性,降低界面张力,并提供该两端界面张力差异其所带来的特别的驱动力量,那么,在该情形下,试样液流其在该微槽道内的流动阻力大幅降低,相应地,该微泵其运行阻力大幅降低,这样,该微泵就能够以比较低的泵送压力来进行针对所述试样溶液的泵送工作,由于机械性的泵送压力大幅降低,因此,在这样一种情形下,就不易发生因进样端机械泵送压力过大而导致的所述进样端及其附近区域的所述微槽道鼓泡、膨胀、变形、扭曲以及该区域基片与盖片之间剥离等等问题;本案该双驱动耦合运作的方案并且增加了针对该试样液流流动动作的操控性,能够允许使用超声波强度、超声波频率、微泵泵送功率、微泵泵送压强等等多个指标来针对该流动的流动速率、流动动作包括向前流动或暂停流动或加速流动等等流动动作进行多参数精确操控;藉由本案该双驱动耦合运作的方案,完全无须对该聚二甲基硅氧烷材质的基片其微槽道等等相关表面进行任何的表面化学修饰或表面化学改性,完全免除了该表面化学修饰或表面化学改性的麻烦程序;另一方面,该低功率、高频频段的超声波,还能够遏制试样中的生物大分子在该无修饰的裸的聚二甲基硅氧烷基片其管道内表面上的吸附,进而遏制该聚二甲基硅氧烷基片其体相对所述生物大分子的吞没作用;所述抗原、抗体以及抗原与抗体的可逆结合物当然都是属于所述的生物大分子的类型;由于所述的吸附作用以及所述的吞没作用被有效地遏制,因此,相关测试结果将更加能够客观地反映实际情况;该低功率、高频频段超声波的作用,当然还包括促成抗原、抗体之间的可逆结合反应的快速达成,这使得相关测试操作能够以比较快的速度完成。
如上所述,该微泵的存在,使得该微型超声波换能器其超声波发射强度能够被允许适度降低,那么,该特点有助于保护所述工作电极其敏感覆层,使之免受超声损伤。
基于本案方案,完全不需要进行针对该聚二甲基硅氧烷基片其相关表面的表面化学修饰或表面化学改性操作,因此,这个表面化学修饰层或表面化学改性层根本就不需要存在,那么,该聚二甲基硅氧烷基片其体相内部聚合物分子不断自动向表面扩散、迁移其所导致的对所述表面化学修饰层或表面化学改性层的破坏性影响也就不存在了。
本案的技术方案一揽子地化解了上文述及的与聚二甲基硅氧烷基片其应用相关的一系列技术难题。基于本案方案,该种十分廉价并且极易加工制作的聚二甲基硅氧烷材料便有可能在该微流控芯片其制备、生产、应用等等领域发挥更大的作用。
本案结构中的该链环式电磁夹具其一个导磁性环节上贴附固定装设了所述微型超声波换能器,该结构提供了一个方便该装置拆解的功能,如此,该链环式电磁夹具连同其一个导磁性环节上所贴附的该微型超声波换能器便能够方便地与该微流控芯片相互脱离,那么,该部分可自由脱离的构件便能够良性循环地重复使用许多次;该结构特征有利于节约该装置的使用成本。
本案该微流控芯片其大规模集成的架构,决定了其在实际测试应用之中,对血清试样的需要量较小,这有助于降低相关受检人员的身心损伤。
附图说明
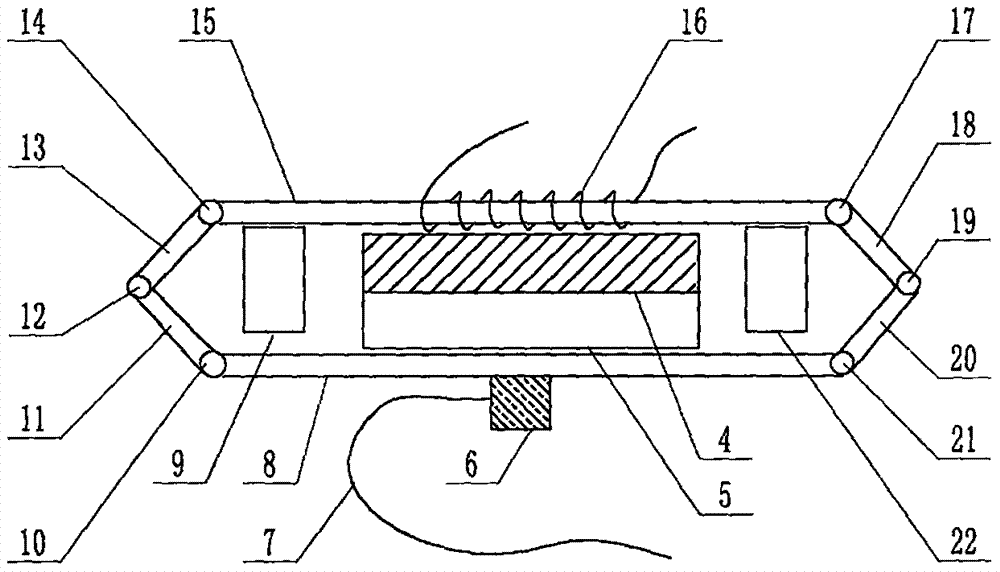
图1是本案该装置该链环式电磁夹具其与该微流控芯片套接状态下大略的外观侧视图,该图例并且指示该套接状态下各构件之间的相对位置关系。
图2是本案该装置的另一个观察角度之下的外观侧视图;图2的观察角度与图1的观察角度相互垂直;图2中没有绘出输液软管以及微泵等构件。
图中,1是链环式电磁夹具,2是该微流控芯片的所述终端,3是该微流控芯片的所述进样端,4是聚二甲基硅氧烷材质的基片,5是盖片,6是微型超声波换能器,7是高频振荡电讯号传输电缆,8、15分别是位于不同结构位置的两个导磁性材质的环节,该两个导磁性材质的环节在该结构中互为对边关系,9、22分别是位于不同结构位置的两个极靴,10、12、14、17、19、21分别是处于六个不同位置的六个铰接点,11、13、18、20分别是处于四个不同位置的四个非磁性材质的环节,16是励磁线圈,23是输液软管,24是微泵;图例中的该链环式电磁夹具结构仅是示意的图例结构,实际该链环式电磁夹具结构不限于该图例链环式电磁夹具结构;图例中的箭头符号标示该微流控芯片其在实际运行时,受两端压力差驱动,其试样液流的流动方向。
具体实施方式
在图1及图2所展示的本案该实施例中,该例其要点是,该装置的结构包括微流控芯片,该微流控芯片的结构包括相互贴合装设在一起的基片4和盖片5,所述基片4和盖片5均为板状物或片状物,该基片4的面向该盖片5的那个面含有经由模压工艺或刻蚀工艺形成的槽道结构,相互贴合安装在一起的该基片4与该盖片5共同构建成了含有管道结构的微流控芯片,该管道的结构位置位于该基片4与该盖片5相互贴合的交界区域,该管道的两端分别与该微流控芯片的进样端3以及终端2连接,该进样端3是该微流控芯片试样溶液的注入端,该终端2是该微流控芯片实际进样测试时其芯片内试样溶液流动的终端,该终端2与该进样端3相互远离,该终端2与该进样端3之间的距离介于3厘米与10厘米之间,在该管道内不同位置上依顺序或逆序装设有工作电极以及对电极以及参比电极,所述顺序指的是所述参比电极其结构位置更靠近所述终端2位置,所述逆序指的是所述参比电极结构位置更靠近所述进样端3位置,所述工作电极由导电性电极以及贴附在该导电性电极上的包埋了肿瘤标志物抗体的金胶敏感膜构成,该管道的构造呈现并联构造,所述呈并联构造的管道由六条分支管道并联构成,所述呈现并联构造的所述管道其外形轮廓近似于并联电路的轮廓,所述工作电极的数量是六个,该六个工作电极的装设位置分别位于所述六条分支管道内,以及,该六个工作电极其表层金胶敏感膜结构中的肿瘤标志物抗体分别是对肿瘤标志物抗原能特异性结合的六种肿瘤标志物抗体物质,该六种抗体物质分别是肿瘤标志物抗体afp、cea、psa、ca125、ca19-9及ca15-3,所述抗原是广义的抗原,所述抗体是广义的抗体,所述工 作电极其材质是金属银材质、黄金材质、碳素材质或热分解导电高分子材质,所述工作电极其形貌呈现柱状、片状或丝状,该基片4其材质是聚二甲基硅氧烷材质,该基片4其表面是原生形态的表面,该原生形态的表面其意思指的是没有经过任何表面化学修饰或任何表面化学改性的该材质的原生形态的表面,该装置的结构还包括链环式电磁夹具1,该链环式电磁夹具1其结构中共有六个环节8、11、13、15、18、20,所述环节8、11、13、15、18、20均呈条状、杆状或棒状,各相邻环节相互铰接形成链环,该链环其外形轮廓呈六边形环状结构,该六边形环状结构的每个顶角10、12、14、17、19、21其结构位置均为铰接结构位置,该六边形环状结构其中的两个处于对边位置的环节8、15其材质是导磁性材质,该六边形环状结构的余下四个环节11、13、18、20其材质均是非磁性材质,所述非磁性材质指的是对外加磁场没有强烈响应的材质,该导磁性材质的两个环节之中的一个环节15上缠绕有励磁线圈16,该缠绕有励磁线圈16的环节15在其励磁线圈16的两侧近邻位置上各装设有一个导磁性材质的极靴,共有两个所述极靴9、22,该两个极靴9、22均指向另一个导磁性材质的环节8,该另一个导磁性材质的环节8其表面上贴附固定装设有微型超声波换能器6,依托电磁吸合力量的该链环式电磁夹具1套接定位在该微流控芯片其所述终端2的邻近位置,以及,高频振荡电讯号传输电缆7,该高频振荡电讯号传输电缆7的一端与该微型超声波换能器6连接在一起;该链环式电磁夹具1提供了一个方便该装置拆解的功能;该微型超声波换能器6其主要功能是在微流控芯片实际进样测试时,利用其所发射的超声波来降低试样溶液与该微流控芯片其内部通道的内壁之间的界面张力,使其能够相容,并且,利用所述进样端3以及所述终端2与该微型超声波换能器6装设位置之间的距离差异以及其所感受到的超声波强度上的差异,诱导形成所述进样端3其界面张力与所述终端2其界面张力之间的差异,该微流控芯片该两端2、3之间的界面张力差异会在该微流控芯片的该两端2、3之间形成压力差异,该压力差异会驱动试样溶液向所述终端2方向流动;该微型超声波换能器6其功能还包括以其所发射的超声波遏止试样中所含有的生物大分子其在该微流控芯片其内部通道内表面上的吸附,进而遏止该聚二甲基硅氧烷材质的基片4其体相对该生物大分子的吞没作用;柔软并具弹性的该聚二甲基硅氧烷材质的基片4其功能包括以其对超声波强烈吸收的性质,对超声波进行强烈吸收,并藉此在该微流控芯片该终端2到该进样端3之间的有限的短距离之内实现超声波强度的快速递减;以及,微泵24,该微泵24与该进样端3连接;该微泵24的功能是,在该试样溶液与该微流控芯片其内部通道的内壁之间的界面张力受该超声波作用而降低、相间相容性增加的前提条件下,以该微泵24的机械性泵送力量来与该超声波诱导的所述两端2、3之间的界面张力差异其所带来的驱动力量互相支持、互相调适、互相耦合,以协同运作的方式汇聚成一股驱动试样液流向所述终端2方向流动的力量。
图例中的箭头符号标示该微流控芯片其在实际运行时,受两端2、3压力差驱动,其试样液流的流动方向。
图1及图2中均没有绘出所述高频振荡电讯号发生器等附属件。
所涉导磁性材料及所涉非磁性材料市场均有售。
所涉微型超声波换能器6市场有售;也可以向超声波换能器厂家定制。
所述微泵24可以向专业厂家定制。
所涉高频振荡电讯号传输电缆7市场有售;也可以向超声波换能器厂家或电缆专业厂家定制。
所涉高频振荡电讯号发生器市场有接近需要的产品可购;也可以向相关厂家定制
本案所涉该微流控芯片其内部通道是疏水的毛细管形态的管道。
所述微泵一词其本身的技术含义对于微流控芯片领域的专业人员来说是公知的。
所述微泵例如微型的压电泵、微型的蠕动泵、微型的气动泵,等等。
所述微泵既可以是外置形式的微泵;该微泵也可以是做进或曰嵌入该微流控芯片内部其进样端结构位置或该进样端近邻结构位置的内置形式的微泵。图例中的微泵是外置形式的微泵;该微泵当然也可以是做进或曰嵌入该微流控芯片结构内部进样端或其近邻结构位置的所述内置形式的微泵,其基本结构要素与外置形式的微泵相同。
所述多道电化学工作站市场有售;该多道电化学工作站也可以根据具体需要向相关专业厂家定制。
鉴于本案上文相关文字表达其所描绘的所述呈现并联构造的管道其形态已经足够清晰,本案实施例中不再具体图示本案该种微流控芯片内所述管道的具体形态。
本案所述抗体指的是广义的抗体;本案所述抗原指的是广义的抗原;本案所述免疫复合物指的是广义的免疫复合物。
- 还没有人留言评论。精彩留言会获得点赞!
- 普适型用于同时检测多种肿瘤标志物的微流控芯片装置的制造方法
- 男性适用的典型肿瘤标志物联合检测用微流控芯片装置的制造方法
- 女性适用的典型肿瘤标志物联合检测用微流控芯片装置的制造方法
- 一种检测口腔癌的标志物及其试剂盒的制造方法与工艺
- microRNA 标志物组及其在制备检测胃癌淋巴结转移试剂盒中的应用的制造方法与工艺
- 基于弹性蛋白酶荧光底物检测乳腺癌肿瘤标志物CA153的酶联免疫试剂盒制备方法与制造工艺
- 检测和评价力量训练效果的miRNA标志物或其组合及其应用的制造方法与工艺
- 一种最优超平面的构建方法、动态优化系统和构建装置与制造工艺
- 癌症标志物及癌症的判定方法与制造工艺
- 检测尿液中单羟酚类代谢物的试剂盒及其制备方法与制造工艺