一种复合催化体系和一种反应体系及其使用方法与流程
本申请涉及但不限于一种复合催化体系和一种反应体系及其使用方法。
背景技术:
在油气田开采过程中,经常遇到由于地层温度不高,导致地层及井筒结蜡、原油无法流动的现象,造成开采成本提高,开采效果差。为解决此问题曾采用注蒸汽、热洗、电加热等来解决这方面的问题,这些方法相比化学热存在诸多不足。化学自生热体系利用一到两种化学剂注入地层,反应生成大量热量,使地层温度升高,将蜡溶解,同时生成的气体又可以起到一定的解堵、驱油作用,在油田开采中应用最为广泛。
目前油田生产中应用最广泛的自生热体系为亚硝酸钠/氯化铵配方。亚硝酸纳/氯化铵自生热体系的反应产物有氮气、高温热水和氯化钠盐水。其中盐水对大多数地层无损害,大量的氮气可以提高局部地层压力,并在较大压力冲击作用下冲洗储层,把堵塞物和溶解垢一起举升到地面。从产物看体系的危害性较小。
亚硝酸钠/氯化铵作为化学生热体系,在实际应用时,为降低单井成本,常将两种液体在地面混合后注入井内,而不采用将两种液体分别注入井下混合。许多油井地层温度都在60℃以上,此温度下,达到峰值温度的时间只有4分钟左右。若使用剂量大,体系在井筒会发生剧烈反应,放出大量气体和热量,热量在井筒散失很多而不能全部作用在地层,大量的气体使井筒压力升高,注入压力难以控制。
技术实现要素:
目前应用于海上油田热解堵作业的化学生热体系,在传统的工艺过程中,多采用段塞式交替注入方式。这种方式不能充分混合生热体系,导致药剂浪费并降低生热效率。比较理想的注入工艺要满足“地面混合地下反应”的目的。因此,为合理控制反应时间,充分利用反应放出的热能,使两液体注入井下的过程中尽量不反应,抵达油层反应,找到一种延缓反应的方法非常有必要。
本申请的发明人在实践经验的基础上经过大量研究分析后研发出能够控制放热反应进程的抑制剂,并以温度作为控制手段。由此可实现在地面温度条件下将掺复合催化体系的生热体系混合后使其不发生或极其缓慢发生反应,而在井底温度条件下抑制剂失效而使放热反应迅速发生以达到作业目的。以此可以实现地面合注工艺,有效利用生热体系,提高生热效率,增强工艺效果。
本申请提供了一种复合催化体系,所述复合催化体系包括酸性引发剂和碱性抑制剂;其中,所述酸性引发剂选自甲酸、苯甲酸、乙酸、草酸、邻苯二甲酸和柠檬酸中的一种或多种,所述碱性抑制剂选自甲胺、三乙醇胺、二甲胺、二乙胺和乙二胺中的一种或多种,所述酸性引发剂与所述碱性抑制剂的摩尔比为1:1-4。
在一个实施方案中,所述酸性引发剂可以为柠檬酸,所述碱性抑制剂可以为三乙醇胺。
在一个实施方案中,所述酸性引发剂与所述碱性抑制剂的摩尔比可以为1:2。
本申请还提供了一种能够控制放热反应进程的反应体系,所述反应体系包括亚硝酸钠/氯化铵化学生热体系,以及如上所述的复合催化体系,所述复合催化体系中所述酸性引发剂的含量为使得与所述化学生热体系等体积的水的pH为1.7-3.5。
在一个实施方案中,所述酸性引发剂的含量可以为使得与所述化学生热体系等体积的水的pH约为2.5。
在一个实施方案中,亚硝酸钠与氯化铵的摩尔比可以为1:1。
本申请还提供了一种使用如上所述的能够控制放热反应进程的反应体系控制放热反应进程的方法,其中,所述复合催化体系的组分和所述化学生热体系的组分在低于50℃的温度下混合抑制放热反应进行;所述复合催化体系的组分和所述化学生热体系的组分混合后在50℃-60℃的温度下促进放热反应进行。
本申请还提供了一种如上所述的能够控制放热反应进程的反应体系用于油水井解堵、驱油的方法,该方法包括在0℃-50℃(可选地,在0℃-45℃)下将所述复合催化体系的所述酸性引发剂与所述化学生热体系的氯化铵的水溶液混合,将所述复合催化体系的所述碱性抑制剂与所述化学生热体系的亚硝酸钠的水溶液混合,将两种混合后的混合物间隔或同时注入油田井筒及地层中。
本申请提供的复合催化体系,弱酸中加入弱碱后,封闭了H+的自由电离,H+浓度减小,体现在溶液pH值升高;当溶液温度升高时,弱碱的封闭效果减弱,弱酸解离增多,pH值会相应降低,此时H+浓度促使反应进行。在应用于生热体系时,注入油井的同时加入适当的弱酸弱碱,抑制弱酸电离,使放热反应不能顺利进行。当到达油层后,由于周围温度的上升,体系温度上升,弱酸电离度变大,溶液pH值降低,变为利于反应引发的酸性环境,促进放热反应进行,从而实现控制放热反应进程的目的。
附图说明
附图用来提供对本申请技术方案的进一步理解,并且构成说明书的一部分,与本申请的实施例一起用于解释本申请的技术方案,并不构成对本申请技术方案的限制。
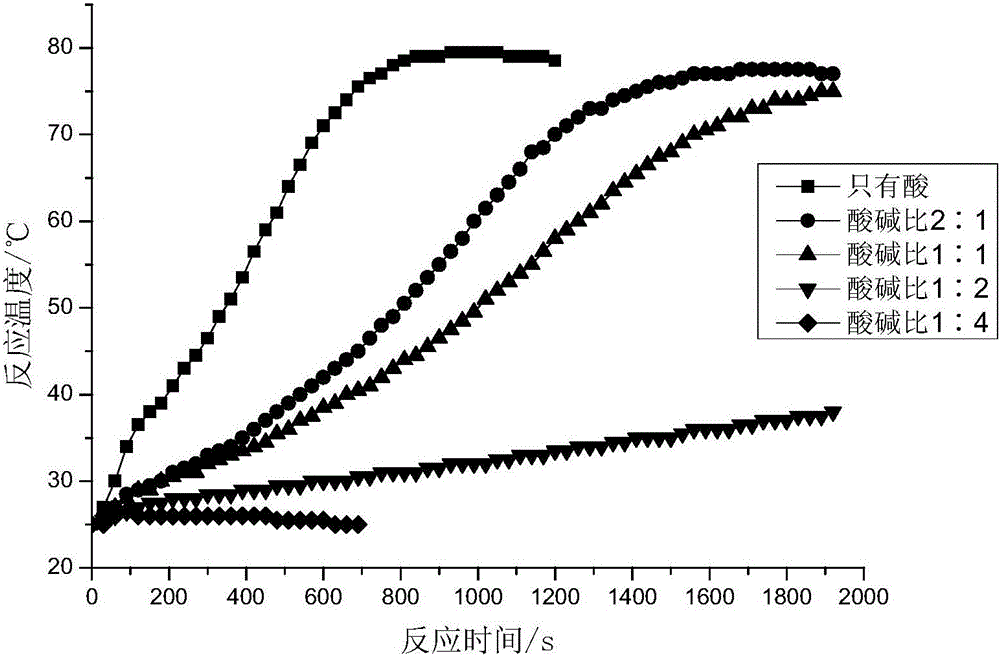
图1为实施例1和对比例1的反应液的温度随时间的变化曲线。
图2为实施例2和对比例2的反应液的温度随时间的变化曲线。
图3为实施例3和对比例3的反应液的温度随时间的变化曲线。
图4为实施例4和对比例4的反应液的温度随时间的变化曲线。
图5为实施例5和对比例5的反应液的温度随时间的变化曲线。
图6为实施例6和对比例6的反应液的温度随时间的变化曲线。
图7为对比例7的反应液的温度随时间的变化曲线。
图8为对比例8的反应液的温度随时间的变化曲线。
图9为对比例9的反应液的温度随时间的变化曲线。
具体实施方式
下面通过实施例来描述本申请的实施方式,本领域的技术人员应当认识到,这些具体的实施例仅表明为了达到本申请的目的而选择的实施技术方案,并不是对技术方案的限制。根据本申请的教导,结合现有技术对本申请技术方案的改进是显然的,均属于本申请保护的范围。
本申请提供了一种复合催化体系,所述复合催化体系包括酸性引发剂和碱性抑制剂;其中,所述酸性引发剂选自甲酸、苯甲酸、乙酸、草酸、邻苯二甲酸和柠檬酸中的一种或多种,所述碱性抑制剂选自甲胺、三乙醇胺、二甲胺、二乙胺和乙二胺中的一种或多种,所述碱性抑制剂与所述酸性引发剂的摩尔比为1:1-4。
所述酸性引发剂与所述碱性抑制剂的摩尔比在上述范围内可以较好的实现放热反应的抑制效果。在本申请实施方式中,所述碱性抑制剂与所述酸性引发剂的摩尔比可以为1:2。
在本申请实施方式中,所述酸性引发剂可以为柠檬酸,所述碱性抑制剂可以为三乙醇胺。
本申请还提供了一种能够控制放热反应进程的反应体系,所述反应体系包括亚硝酸钠/氯化铵化学生热体系,以及如上所述的复合催化体系,所述复合催化体系中所述酸性引发剂的含量为使得与所述化学生热体系等体积的水的pH为1.7-3.5。需要说明的是,测量与所述化学生热体系等体积的水的pH是在与所述化学生热体系相同的温度下进行的。
在本申请实施方式中,可以通过将上述复合催化体系用于自生热的反应体系来控制放热反应进程。影响放热反应进程的因素有很多,例如反应物浓度、催化剂浓度、反应温度、反应物pH值等。在本申请实施方式中,所述复合催化体系利用控制反应物pH值来控制放热反应进程。
本申请的发明人经过大量实验后发现,在用所述复合催化体系控制所述化学生热体系的放热反应进程时,当所述复合催化体系中酸性引发剂的含量为使得与所述化学生热体系等体积的水的pH为1.7-3.5时,能够有效控制放热反应进程。
在本申请实施方式中,所述酸性引发剂的含量为使得与所述化学生热体系等体积的水的pH约为2.5。
在本申请中,亚硝酸钠与氯化铵的摩尔比可以为本领域技术人员已知的范围。在本申请实施方式中,亚硝酸钠与氯化铵的摩尔比可以为1:1。
在本申请实施方式中,所述亚硝酸钠和所述氯化铵的化学生热体系在使用时通常为亚硝酸钠水溶液和氯化铵水溶液的混合体系。亚硝酸钠水溶液和氯化铵水溶液的浓度可以根据实际需要进行选择。可选地,亚硝酸钠水溶液和氯化铵水溶液的浓度分别可以为3mol/L。
在本申请中,由于化学生热体系发生化学反应需要一定的条件,通常温度对化学反应的影响较大。在亚硝酸钠/氯化铵化学生热体系,在较低温度下,亚硝酸钠和氯化铵接触反应较慢,但是升高温度,将会促进亚硝酸钠和氯化铵的反应。因此,要控制放热反应的反应进程,需要抑制或者增强温度对放热反应的影响。
本申请还提供了一种使用如上所述的能够控制放热反应进程的反应体系控制放热反应进程的方法,其中,所述复合催化体系的组分和所述化学生热体系的组分在低于50℃的温度下混合抑制放热反应进行;所述复合催化体系的组分和所述化学生热体系的组分混合后在50℃-60℃的温度下促进放热反应进行。
在上述温度范围内,所述复合催化体系能够有效抑制或者增强温度对放热反应的影响。
本申请还提供了一种将如上所述的能够控制放热反应进程的反应体系用于油水井解堵、驱油的方法,该方法包括在0℃-50℃下将所述复合催化体系的所述酸性引发剂与所述化学生热体系的氯化铵的水溶液混合,将所述复合催化体系的所述碱性抑制剂与所述化学生热体系的亚硝酸钠的水溶液混合,将两种混合后的混合物间隔或同时注入油田井筒及地层中。
本申请提供的复合催化体系,在应用于生热体系时,注入油井的同时加入适当的弱酸弱碱,抑制弱酸电离,使放热反应不能顺利进行。当到达油层后,由于周围温度的上升,体系温度上升,弱酸电离度变大,溶液pH值降低,变为利于反应引发的酸性环境,促进放热反应进行,从而实现控制放热反应进程的目的。
本申请通过加入抑制剂的方式,以温度作为控制手段,与引发剂混合制备反应引发温度可控的复合型催化体系,控制化学生热体系反应的最佳发生温度和时机,有效利用放热量、降低热损失、提高工艺效果。通过复合催化体系使得放热反应任意可控,可根据不同的油田井筒及地层条件设计化学生热体系的用量;实现了化学生热体系的“同时注入”的工艺,提高反应效率及药剂的利用率。
以下实施例中所用试剂均来自国药集团化学试剂有限公司,相同的试剂来源相同。
反应液的温度通过热电偶温度传感器测量。
实施例1
在25℃下,将8.025g氯化铵溶于50mL水中,向氯化铵水溶液中加入0.105g柠檬酸形成混合液;将10.35g亚硝酸钠溶于50mL水中,向亚硝酸钠水溶液中加入与柠檬酸的摩尔比分别为1:1、1:2、1:4的三乙醇胺形成混合液;将两种混合液混合形成反应液。
其中,柠檬酸的添加量使得100mL水的pH值为2.64。通过观察,反应液的温度随时间的变化如图1所示。
从图1可以看出:当酸碱比例为1:1时,可有效推迟温度峰值达到的时间,约4000s左右。而当酸碱比例为1:2和1:4时,能够明显抑制反应的进行。
对比例1
采用实施例1的方法,不同的是,柠檬酸与三乙醇胺的摩尔比为2:1;或者不加入三乙醇胺,即,只有酸存在。反应液的温度随时间的变化如图1所示。
从图1可以看出,柠檬酸与三乙醇胺的摩尔比为2:1时,从1000s开始,温度与柠檬酸与三乙醇胺的摩尔比为1:1时相比,具有明显上升的趋势。说明酸含量较高的体系,不利于控制反应的进程。
实施例2
采用实施例1的方法,不同的是,柠檬酸的添加量使得100mL水的pH值为2.34。通过观察,反应液的温度随时间的变化如图2所示。
从图2可以看出:当酸碱比例为1:1时,可有效推迟温度峰值达到的时间,约2000s左右。而当酸碱比例为1:2时,能够明显推迟温度峰值达到的时间超过2000s;而当酸碱比例为1:4时,明显抑制反应的进行。
对比例2
采用实施例2的方法,不同的是,柠檬酸与三乙醇胺的摩尔比为2:1;或者不加入三乙醇胺。通过观察,反应液的温度随时间的变化如图2所示。
从图2可以看出,相比于只含有酸的体系,反应温度出现峰值的时间接近900s。而柠檬酸与三乙醇胺的摩尔比为2:1时,从400s开始,温度与柠檬酸与三乙醇胺的摩尔比为1:1时相比,具有明显上升的趋势。说明酸的浓度的升高,不利于控制反应的进程。
实施例3
采用实施例1的方法,不同的是,柠檬酸的添加量使得100mL水的pH值为2.22。通过观察,反应液的温度随时间的变化如图3所示。
从图3可以看出:当酸碱比例为1:1时,温度峰值达到的时间,约1800s左右,而当酸碱比例为1:2时,能够明显推迟温度峰值达到的时间超过1800s;当酸碱比例为1:4时,明显抑制反应的进行。
对比例3
采用实施例3的方法,不同的是,柠檬酸与三乙醇胺的摩尔比为2:1;或者不加入三乙醇胺。通过观察,反应液的温度随时间的变化如图3所示。
从图3可以看出,只含有酸的体系,反应温度出现峰值的时间接近600s。而柠檬酸与三乙醇胺的摩尔比为2:1时,从100s开始,温度与柠檬酸与三乙醇胺的摩尔比为1:1时相比,具有明显上升的趋势。与图2相比,说明酸的浓度的升高,不利于有效控制反应的进程。同时也说明,本申请的复合催化体系,能够有效的控制放热反应的进程。
实施例4
采用实施例1的方法,不同的是,初始温度为45℃。通过观察,反应液的温度随时间的变化如图4所示。
从图4可以看出,当酸碱比例为1:2时,在保证峰值温度的情况下可推迟峰值达到时间约1400s。当酸碱比例为1:1时,可有效推迟温度峰值达到的时间,约1000s左右。而当酸碱比例为1:4时,能够明显抑制反应的进行。
对比例4
采用实施例4的方法,不同的是,不加入三乙醇胺;或者柠檬酸与三乙醇胺的摩尔比为2:1。通过观察,反应液的温度随时间的变化如图4所示。
从图4可以看出,只含有酸的体系,和酸碱比为2:1的体系反应温度出现峰值的时间接近,在600s左右,说明酸含量较多不利于有效控制反应的进程。
实施例5
采用实施例4的方法,不同的是,柠檬酸的添加量使得100mL水的pH值为1.94。通过观察,反应液的温度随时间的变化如图5所示。
从图5可以看出,酸碱比例为1:1时,温度出现峰值的时间降低到500s左右,而当酸碱比例为1:2时,仍然能够有效起到延迟反应进行的效果。而酸碱为1:4时,仍然能够有效抑制反应的进行。
对比例5
采用实施例5的方法,不同的是,不加入三乙醇胺;或者柠檬酸与三乙醇胺的摩尔比为2:1。通过观察,反应液的温度随时间的变化如图5所示。
从图5可以看出,在较高的初始反应温度下,采用柠檬酸的质量浓度为0.3%时,酸碱比为2:1时,反应温度出现峰值的时间接近只含有酸的体系。说明较高的温度和较高的酸含量,不利于控制反应的进程。
实施例6
采用实施例5的方法,不同的是,柠檬酸的添加量使得100mL水的pH值为1.78。通过观察,反应液的温度随时间的变化如图6所示。
从图6可以看出:当酸碱比例为1:1时,仍然能够有效起到延迟反应进行的效果,峰值达到时间约700s;当酸碱比例为1:2时,峰值达到时间约1400s。而酸碱为1:4时,仍然能够有效抑制反应的进行。
对比例6
采用实施例6的方法,不同的是,不加入三乙醇胺;或者柠檬酸与三乙醇胺的摩尔比为2:1。通过观察,反应液的温度随时间的变化如图6所示。
从图6可以看出,只含有酸的体系,和酸碱比为2:1的体系反应温度出现峰值的时间接近,在200s左右,说明酸含量较多不利于控制反应的进程。
对比例7
采用实施例1的方法,不同的是,初始温度分别为25℃、45℃、60℃和75℃,不加入三乙醇胺。通过观察,反应液的温度随时间的变化如图7所示。
从图7可以看出,与45℃初始温度距离发生剧烈反应的600s相比,初始温度分别为60℃和75℃发生反应的时间几乎在100s内,说明,初始温度大于60℃,不利于控制反应进程。
对比例8
采用对比例7的方法,不同的是,柠檬酸的添加量使得100mL水的pH值分别为2.34、1.94、1.67、1.56。通过观察,反应液的温度随时间的变化如图8所示。
从图8可以看出,初始温度分别为60℃和75℃时,反应温度出现峰值的时间在100s内。并且与图7相比,反应温度出现峰值的时间明显延长。说明,随着酸性引发剂的浓度升高,不利于控制反应进程。
对比例9
采用对比例7的方法,不同的是,柠檬酸的添加量使得100mL水的pH值分别为2.22、1.78、1.54、1.33。通过观察,反应液的温度随时间的变化如图9所示。
从图9可以看出,初始温度分别为60℃和75℃时,反应温度出现峰值的时间在100s内。并且与图2相比,反应温度出现峰值的时间接近。说明,与酸性引发剂的浓度相比,初始温度对反应进程的影响更明显。
应用实施例1
将实施例1的反应体系用于渤海油田B5井。采用地面合注方式,在地面井口连接具有两条管线的三通管件,其中一条管线输送混配有柠檬酸和氯化铵水溶液的混合液,另一条管线输送混配有三乙醇胺和亚硝酸钠水溶液的混合液,两条管线输送的物料在三通管件处混合后注入井筒。地面温度18℃,地层温度62℃,氯化铵水溶液和亚硝酸钠水溶液的浓度分别为3mol/L;亚硝酸钠与氯化铵的摩尔比为1:1;柠檬酸与三乙醇胺摩尔配比为1:2。柠檬酸的用量为使得与氯化铵和亚硝酸钠体系等体积的水的pH为3.5。井筒内体积7m3,注入速度20m3/h(从地面至地层需20min),注入过程中井筒段内注入压力没有升高,说明抑制剂的存在延缓了反应的引发;在注入后期(大概260min)时出现了升压的现象,说明体系液进入地层后在地层温度下抑制剂失效引发了放热反应,伴生气量增加导致注入压力升高。
从以上实施例可以看出,本申请提供的复合催化体系,能够有效控制放热反应的进程,实现了在地面温度条件下掺复合催化体系的生热体系混合后使其不发生或极其缓慢发生反应,而在井底温度条件下抑制剂失效而使放热反应迅速发生以达到作业目的。从而实现地面合注工艺,有效利用生热体系,提高生热效率,增强工艺效果。
虽然本申请所揭露的实施方式如上,但所述的内容仅为便于理解本申请而采用的实施方式,并非用以限定本申请。任何本申请所属领域内的技术人员,在不脱离本申请所揭露的精神和范围的前提下,可以在实施的形式及细节上进行任何的修改与变化,但本申请的专利保护范围,仍须以所附的权利要求书所界定的范围为准。
- 还没有人留言评论。精彩留言会获得点赞!