一种锌钛复合金属氧化物及其制备和应用的制作方法
本发明属于氧化物催化剂制备及催化应用领域,具体涉及锌钛复合金属氧化物的制备及将其用于太阳光驱动的过氧化氢清洁生产过程。
背景技术:
传统的化学工业提供给人类所需的新物质,极大地丰富了人们的生活,但也逐渐暴露出很多弊端,如未能有效利用资源,造成资源浪费、环境污染等。发展可再生、清洁能源是解决这些问题的重要途径。过氧化氢(H2O2)被誉为“最清洁”的化学品,其应用于造纸、纺织、印染、电子、食品、环保和化学合成等领域,随着经济社会发展和人民生活水平的不断提高,其应用会更加广泛。
目前工业上生产H2O2的主要方法是蒽醌法,该方法具有装置易于大型化、产率较高等优点。不足之处是生产系统复杂,生产过程能耗大,H2O2与有机物质在反应体系里同时存在,易产生爆炸危险与高毒性。因此,人们发展了以H2和O2为原料的H2O2直接合成法(Science,2009,323,1037-1041.),这种方法通常是以贵金属Au、Pd或双金属AuPd作为催化剂,水为介质,通过H2和O2的反应,选择性生成H2O2。该法基本不使用有机溶剂,因此较蒽醌法更绿色、环保。但是,H2和O2的气体混合体系在很宽的浓度范围内具有爆炸风险,难以控制,在合成时需精细调节两者的比例,或加入稀释剂(例如:N2、Ar气),这会对反应产生影响,导致H2O2选择性不高,产率较低。
为了避免H2和O2两种气体的直接接触,研究者提出以质子氢(H+)代替分子氢(H2)制备H2O2。TiO2是一种广泛使用的光催化剂,在光激发下产生的光生电子能够还原氧,然后经过一系列自由基转化过程可以形成H2O2,但生成的H2O2会在TiO2表面快速分解,降低H2O2的产率。为了抑制H2O2在TiO2表面的分解,研究者设计了TiO2负载Au、Ag的氧化物为催化剂,通过贵金属将电子导出,使得H2O2在贵金属表面生成,从而抑制H2O2的分解,提高H2O2的产率(ACS Catal.,2012,2,599-603;J.Am.Chem.Soc.,2010,132,7850-7851.),但这种方法的催化剂需要使用贵金属,资源非常有限,价格昂贵,不适于工业生产与推广。利用氟离子(F-)改性TiO2,可以减少H2O2在TiO2表面的分解,提高产率(Chem.Commun.,2005,2627-2629.),但是所使用的氟化氢(HF)具有强腐蚀性,操作危险大,增加工业生产的成本与风险。因此,开发以质子氢和氧气为原料、在催化剂作用的温和条件下清洁生产H2O2的方法,将极具推广和工业生产前景。
技术实现要素:
本发明的目的是提供一种锌钛复合金属氧化物及其制备方法,及将其用做光合成H2O2的催化剂。
本发明提供的锌钛复合金属氧化物催化剂,表示为TiO2-ZnTiO3-(PO4)n,其中TiO2-ZnTiO3是由Zn、Ti、O组成的二元金属氧化物,Zn:Ti摩尔比为2~6:1,二元金属氧化物的晶粒尺寸为30~90nm,具有多孔特征;(PO4)n附着在TiO2-ZnTiO3表面,其中n=1~6;该催化剂用于常温、常压下、以水和氧气为原料,光合成H2O2的催化剂。
该催化剂的制备方法为:先制备锌钛复合金属氢氧化物(简写为ZnTi-LDH),然后将其在空气或惰性气氛下焙烧,转变为锌钛复合金属氧化物(简写为ZnTi-MMO),再在酸性溶液中、室温下将ZnTi-MMO中的ZnO溶蚀掉,得到TiO2-ZnTiO3复合氧化物,然后在磷酸缓冲溶液中处理,得到磷酸根改性TiO2-ZnTiO3复合氧化物表示为TiO2-ZnTiO3-(PO4)n催化剂。
上述锌钛复合金属氧化物的制备方法,具体步骤如下:
A.将锌盐、钛盐、脲、氟化铵溶于去离子水中配制混合液,其中,锌盐浓度是0.004~0.8mol/L,锌盐与钛盐的摩尔浓度比为3~6,脲的摩尔浓度是锌和钛盐摩尔浓度之和的2~8倍,氟化铵的摩尔浓度是锌和钛盐摩尔浓度之和的4~10倍;超声同时搅拌3~30min,将混合液在100~150℃条件下加热搅拌回流12~48小时,冷却至室温,抽滤洗涤至pH=7,60~80℃干燥6~12小时,得到水滑石,表示为[ZnxTi(OH)4]2x+(CO32-)x·nH2O,简单表示为ZnTi-LDH,x代表锌与钛的摩尔比,x=2~6,n表示水分子数,n=6~15。
所述的锌盐是硝酸锌、硫酸锌、氯化锌中的一种,钛盐是异丙醇钛、四氯化钛、硫酸钛中的一种。
B.将步骤A得到的水滑石置于马弗炉或管式炉中,在空气或氮气气氛中焙烧,焙烧条件为:以1~10℃/min的升温速率升至300~800℃,保温1~8小时,得到y(ZnO)-TiO2-ZnTiO3其中y=3~11;
C.向反应器中按0.5~3g/mL的比例加入上述y(ZnO)-TiO2-ZnTiO3和水,在室温、磁力搅拌,转速为200~800rpm的条件下滴加0.1~1mol/L的HClO4至pH=1.0~3.0,再在转速为300~1000rpm磁力搅拌条件下反应3~24小时,溶蚀ZnO,过滤、干燥,得到TiO2-ZnTiO3;
D.将K2HPO4·3H2O和KH2PO4溶于去离子水中配制0.1~1mol/L pH=5~8的磷酸缓冲液;按每0.5~3g/mL的比例加入TiO2-ZnTiO3到磷酸缓冲溶液中,在室温、磁力搅拌,转速为300~800rpm的条件下、光照反应1~10小时,得到磷酸改性的锌钛复合金属氧化物TiO2-ZnTiO3-(PO4)n,其中n=1~6。
图1是步骤A制备的ZnTi-LDH的X射线粉末衍射(XRD)图,图中出现水滑石(LDH)的(003)、(006)、(012)、(100)、(101)、(009)、(107)、(108)、(113)特征峰,证明产物是ZnTi-LDH。
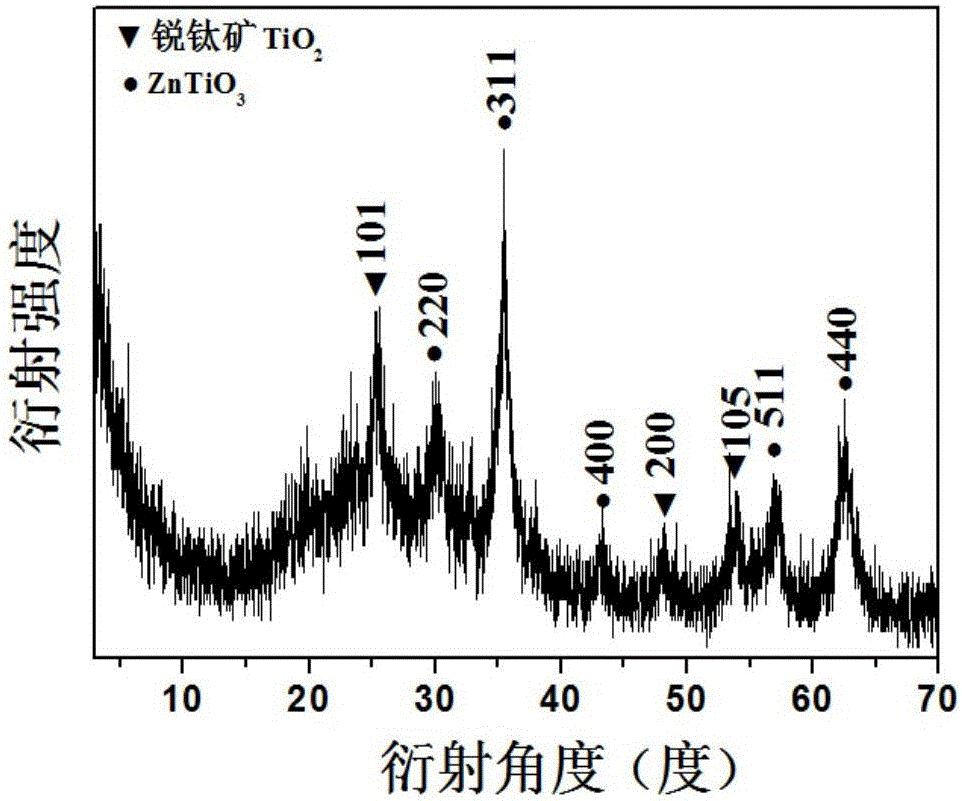
图2是步骤C制备的TiO2-ZnTiO3的X射线粉末衍射(XRD)图,图中出现对应于锐钛矿TiO2的(101)、(200)、(105)衍射峰,与锐钛矿TiO2的衍射峰(PDF 21-1272)一致。;对应于锌钛尖晶石ZnTiO3的(220)、(311)、(400)、(511)、(440)衍射峰,与锌钛尖晶石ZnTiO3的衍射峰(JCPDS:36-0190)一致。证明产物是TiO2-ZnTiO3复合氧化物。
图3是步骤D制备的TiO2-ZnTiO3-(PO4)n的X射线粉末衍射(XRD)图,图中出现对应于锐钛矿TiO2的(101)、(200)、(105)衍射峰,与锐钛矿TiO2的衍射峰(PDF 21-1272)一致。;对应于锌钛尖晶石ZnTiO3的(311)、(511)、(440)衍射峰,与锌钛尖晶石ZnTiO3的衍射峰(JCPDS:36-0190)一致,还有磷酸根对应的峰。证明产物是TiO2-ZnTiO3复合氧化物被磷酸根改性,即TiO2-ZnTiO3-(PO4)n。
将分别对TiO2-ZnTiO3-(PO4)n、对比例2的TiO2-ZnTiO3、对比例1的TiO2的样品进行光合成H2O2催化性能测试,结果反应3.5小时TiO2-ZnTiO3-(PO4)n合成H2O2产量达到180-232.3μmol/L;TiO2-ZnTiO3合成H2O2产量为79.7μmol/L,而纯TiO2催化剂合成H2O2产量仅有59.5μmol/L。说明TiO2-ZnTiO3-(PO4)5在光合成H2O2反应中的催化性能显著增强。
本发明具有如下的显著效果:
(1)以地球丰富、无毒性的元素:锌、钛为组成制备复合氧化物催化剂,并作为光合成H2O2的催化剂,具有绿色、可持续、低成本的特点,适合规模化制备。
(2)仅以水、氧气和少量醇为原料、利用太阳光作为能源供体生产大宗工业必需品H2O2,整个过程不使用任何有毒试剂、有毒溶剂、无碳排放,反应条件温和(常温、常压),是绿色、清洁的生产过程。
(3)催化剂制备工艺简单,不需要特殊设备与条件,适合于规模化生产。
附图说明
图1是实施例1步骤A得到的的[Zn3Ti(OH)4]6+(CO32-)3·12H2O的X射线粉末衍射(XRD)图。
图2是实施例1步骤C得到的TiO2-ZnTiO3的X射线粉末衍射(XRD)图。
图3是实施例1步骤D得到的TiO2-ZnTiO3-(PO4)n的X射线粉末衍射(XRD)图
具体实施方式
实施例1
A.称取5.9498g Zn(NO3)2·6H2O、2.842g Ti[OCH(CH3)2]4、6.005g脲于250mL的烧杯中,加入100mL去离子水,超声、搅拌至混合形成均一溶液,超声功率40W、时间为10min,温度20℃,配制混合盐溶液,其中锌钛摩尔浓度比为2/1。将混合液移至三口烧瓶中在100℃条件下加热搅拌回流48小时,冷却至室温,抽滤洗涤至pH=7,60℃干燥12小时,得到[Zn2Ti(OH)4]4+(CO32-)2·10H2O。
B.将步骤A中制备的水滑石置于马弗炉中,在空气气氛中焙烧,焙烧条件为:以5℃/min的升温速率升至600℃,保温2小时,得到3(ZnO)-TiO2-ZnTiO3。
C.向玻璃或石英反应器中加入0.5g 3(ZnO)-TiO2-ZnTiO3和500ml去离子水,在室温、磁力搅拌,转速为400rpm的条件下滴加1mol/L的HClO4至pH=2.9,再在转速为300rpm的磁力搅拌条件下,反应2小时,溶蚀ZnO,得到TiO2-ZnTiO3。
D.将K2HPO4·3H2O和KH2PO4溶于去离子水中配制0.1mol/L磷酸缓冲液;称取0.5g TiO2-ZnTiO3加入到磷酸缓冲溶液中,在室温、磁力搅拌,转速为350rpm的条件下、光照反应3小时,得到TiO2-ZnTiO3-(PO4)5。
将TiO2-ZnTiO3-(PO4)5用作光催化反应的催化剂的催化性能测试,具体方法如下:向烧杯中加入30mL醇/水混合液,其中醇的体积分数为5%,醇为异丙醇;称取30mg催化剂加入到烧杯中,在室温、磁力搅拌条件下滴加1mol/L的HClO4至pH=3.0,首先在磁力搅拌条件下通入纯度大于99%的氧气30min,气体流速50mL/min,使溶液达到溶解氧饱和状态,然后用光照强度为100mW/cm2)的氙灯光源照射,反应3.5小时,此过程定时取样测试溶液中H2O2浓度。结果反应3.5小时后,TiO2-ZnTiO3-(PO4)5溶液中H2O2浓度值为216.5μmol/L。
测试反应溶液中H2O2浓度值是参照文献[Jie Chen,Shaohua Shen,Penghui Guo,Po Wu and Liejin Guo.J.Mater.Chem.A,2014,2,4605-4612.]的方法测试的。
实施例2
A.称取8.922g Zn(NO3)2·6H2O、2.842g Ti[OCH(CH3)2]4、6.005g脲于250mL的烧杯中,加入100mL去离子水,超声、搅拌至混合形成均一溶液,超声功率40W、时间为10min,温度20℃,配制混合盐溶液,其中锌钛摩尔浓度比为3/1。将混合液移至三口烧瓶中在100℃条件下加热搅拌回流48小时,冷却至室温,抽滤洗涤至pH=7,60℃干燥12小时,得到[Zn3Ti(OH)4]6+(CO32-)3·12H2O。
B.将步骤A中制备的水滑石置于马弗炉中,在空气气氛中焙烧,焙烧条件为:以5℃/min的升温速率升至600℃,保温2小时,得到5(ZnO)-TiO2-ZnTiO3。
C.向玻璃或石英反应器中加入0.5g 5(ZnO)-TiO2-ZnTiO3和500ml去离子水,在室温、磁力搅拌,转速为300rpm的条件下滴加1mol/L的HClO4至pH=3.08,在磁力搅拌,转速为350rpm的条件下,反应2.5小时,溶蚀ZnO,得到TiO2-ZnTiO3。
D.将K2HPO4·3H2O和KH2PO4溶于去离子水中配制0.1mol/L磷酸缓冲液;称取0.5g TiO2-ZnTiO3加入到磷酸缓冲溶液中,在室温、磁力搅拌,转速为450rpm的条件下、光照反应3小时,得到TiO2-ZnTiO3-(PO4)5。
催化剂应用性能测试,具体方法同实施例1,反应3.5小时后,溶液中H2O2浓度值为232.3μmol/L。
实施例3
A.称取17.844g Zn(NO3)2·6H2O、2.842g Ti[OCH(CH3)2]4、6.005g脲于250mL的烧杯中,加入100mL去离子水,超声、搅拌至混合形成均一溶液,超声功率40W、时间为10min,温度20℃,配制混合盐溶液,其中锌钛摩尔浓度比为6/1。将混合液移至三口烧瓶中在100℃条件下加热搅拌回流48小时,冷却至室温,抽滤洗涤至pH=7,60℃干燥12小时,得到[Zn6Ti(OH)4]12+(CO32-)6·15H2O。
B.将步骤A中制备的水滑石置于马弗炉中,在空气气氛中焙烧,焙烧条件为:以5℃/min的升温速率升至600℃,保温2小时,得到11(ZnO)-TiO2-ZnTiO3。
C.向玻璃或石英反应器中加入0.5g 11(ZnO)-TiO2-ZnTiO3和500ml去离子水,在室温、磁力搅拌,转速为420rpm的条件下滴加1mol/L的HClO4至pH=3.10,在磁力搅拌,转速为480rpm的条件下,反应3小时,溶蚀ZnO,得到TiO2-ZnTiO3。
D.将K2HPO4·3H2O和KH2PO4溶于去离子水中配制0.1mol/L磷酸缓冲液;称取0.5g TiO2-ZnTiO3加入到磷酸缓冲溶液中,在室温、磁力搅拌条件,转速为500rpm的条件下、光照反应3小时,得到TiO2-ZnTiO3-(PO4)5。
H2O2催化剂应用性能测试,具体方法同实施例1,反应3.5小时后,溶液中H2O2浓度值为183.8μmol/L。
实施例4
A.称取8.922g Zn(NO3)2·6H2O、2.842g Ti[OCH(CH3)2]4、6.005g脲于250mL的烧杯中,加入100mL去离子水,超声、搅拌至混合形成均一溶液,超声功率40W、时间为10min,温度20℃,配制混合盐溶液,其中锌钛摩尔浓度比为3/1。将混合液移至三口烧瓶中在100℃条件下加热搅拌回流48小时,冷却至室温,抽滤洗涤至pH=7,60℃干燥12小时,得到[Zn32+Ti(OH)3]6+(CO32-)3·10H2O。
B.将步骤A中制备的水滑石置于马弗炉中,在空气气氛中焙烧,焙烧条件为:以5℃/min的升温速率升至450℃,保温2小时,得到5(ZnO)-TiO2-ZnTiO3。
C.向玻璃或石英反应器中加入0.5g 5(ZnO)-TiO2-ZnTiO3和500ml去离子水,在室温、磁力搅拌,转速为380rpm的条件下滴加1mol/L的HClO4至pH=2.98,在磁力搅拌,转速为450rpm的条件下,反应3.5小时,溶蚀ZnO,得到TiO2-ZnTiO3。
D.将K2HPO4·3H2O和KH2PO4溶于去离子水中配制0.1mol/L磷酸缓冲液;称取0.5g TiO2-ZnTiO3加入到磷酸缓冲溶液中,在室温、磁力搅拌、转速为500rpm的条件下、光照反应3小时,得到TiO2-ZnTiO3-(PO4)5。
催化剂性能测试,具体方法同实施例1,反应3.5小时后,溶液中H2O2浓度值为230.8μmol/L。
对比例1
按照实施例1步骤D的方法将TiO2-ZnTiO3换成目前常用的TiO2光催化剂用磷酸改性,得到磷酸改性的TiO2催化剂,表示为TiO2-(PO4)5。
采用实施例1的方法进行催化性能测试,反应3.5小时后,溶液中H2O2浓度值为59.5μmol/L。
对比例2
按照实施例1步骤C的方法得到的TiO2-ZnTiO3。
采用实施例1的方法进行催化性能测试,反应3.5小时后,溶液中H2O2浓度值为79.7μmol/L。
- 还没有人留言评论。精彩留言会获得点赞!