纳米孔组件及其用途的制作方法
纳米孔组件及其用途
[0001]
相关申请的交叉引用
[0002]
本申请根据35u.s.c.
§
119(e)要求2018年2月12日提交的美国临时专利申请号62/629,604的优先权,其公开内容通过引用以其整体并入本文。
技术领域
[0003]
本公开文本总体上涉及纳米孔,并且更具体地涉及使用用非膜蛋白组装的纳米孔用于检测分析物的系统和方法。
背景技术:
[0004]
生物纳米孔是嵌入在衬底(通常是脂膜)中的蛋白质通道。自然界中的各种各样的蛋白质复合物形成巧妙的类似通道的结构,其中的一些已经作为纳米孔加以探索,通过α-溶血素、mspa、气溶素、flua、omp f/g、csgg、clya和pa
63
来例示。例如,来自金黄色葡萄球菌(staphylococcus aureus)的生物蛋白纳米孔α-溶血素(αhl)已经用于单分子检测。
[0005]
最近,研究人员在单分子分析中采用了生物固态dna折纸术和复合纳米孔。与其合成对应物相比,生物纳米孔具有优点,主要是因为它们可以在人工纳米孔尚无法匹配的原子级精度下可重复地制造和修饰。然而,生物纳米孔的现有使用也具有缺点。例如,它们在提供不同的形状、大小和亲水/疏水特性以便以高灵敏度和特异性检测不同分析物方面并非是多功能的。
[0006]
因此,仍然非常需要一种适用于检测具有不同特性的分析物的稳健纳米孔系统。
技术实现要素:
[0007]
本公开文本通过提供一种用于检测分析物的纳米孔组件来满足本领域的这种需求。纳米孔组件包括由多个亚基形成的通道。每个所述亚基包含能够形成蛋白质通道的非膜蛋白。在一些实施方案中,每个所述亚基包含具有与选自seq id no:1-35的多肽序列至少75%相同的多肽序列的多肽。在一些实施方案中,所述多肽包含与seq id no:4-12至少75%相同的多肽序列。
[0008]
在一些实施方案中,所述多肽可以包含至少一个被半胱氨酸取代的残基。在一些实施方案中,所述多肽来源于phi29门户蛋白(portal protein)或尾蛋白(tail protein)。在一些实施方案中,phi29尾蛋白可以包含e595c、k321c和k358c取代中的一个或多个。在一些实施方案中,phi29尾蛋白可以包含k134i、d138l、d139l、d158l、e163v、e309v、d311v、k321v、k356a、k358a、d377a、d381v、n388l、r524i、r539a和e595v取代中的一个或多个。
[0009]
一方面,纳米孔组件还包括用于检测分析物的探针。所述探针可操作地连接到至少一个亚基。所述探针可以是化学物、碳水化合物、适体、核酸、肽、蛋白质、抗体和受体中的一种。在一些实施方案中,所述探针包含与选自seq id no:36-79的序列至少75%相同的序列。在一些实施方案中,所述探针是抗psa抗体。所述探针可以经由共价键可操作地连接到至少一个所述亚基。所述共价键包括二硫键、酯键或巯基键。在一些实施方案中,所述探针
可操作地连接到接近通道的入口的位置或在通道的内侧的位置。
[0010]
所述分析物可以是核酸、氨基酸、肽、蛋白质、聚合物和化学分子中的一种。在一些实施方案中,所述分析物是psa、cea、afp、vcam、mir-155、mir-22、mir-7、mir-92a、mir-122、mir-192、mir-223、mir-26a、mir-27a和mir-802中的一种。
[0011]
根据纳米孔组件的一些实施方案,所述通道被嵌入在聚合物囊泡中。在一些实施方案中,所述通道被插入在膜中。所述膜可以包括聚合物膜或脂膜。所述聚合物膜可以包括交替共聚物、周期共聚物、嵌段共聚物、二嵌段共聚物、三嵌段共聚物、三元共聚物或其组合。在一些实施方案中,聚合物膜包含pmoxa-pdms-pmoxa。在一些实施方案中,所述纳米孔组件还可以包括胆固醇和/或卟啉。
[0012]
另一方面,本公开文本还提供了一种用于检测分析物的设备。所述设备包括以上所述的纳米孔组件和任选地用于所述纳米孔组件的支撑物。所述设备还可以包括电极,所述纳米孔组件被栓系到所述电极。
[0013]
另一方面,本公开文本还提供了一种试剂盒,其包括以上所述的纳米孔组件和任选地用于使用所述纳米孔组件的说明书。
[0014]
另一方面,本公开文本提供了一种检测分析物的方法。所述方法包括:(1)使含有分析物的样品与所述的纳米孔组件接触;(2)施加跨过纳米孔组件的通道的电流;(3)以一个或多个时间间隔确定穿过通道的电流;以及(4)将以一个或多个时间间隔测量的电流与参考电流进行比较,其中相对于参考电流的电流变化指示样品中分析物的存在。所述分析物可以是核酸、氨基酸、肽、蛋白质、聚合物和化学分子中的任一种。在一些实施方案中,参考电流是用不含分析物的样品测量的。在一些实施方案中,纳米孔组件被放置在支撑物上。
[0015]
前述概述并非旨在限定本公开文本的每个方面,并且在其他部分,诸如以下详细描述中描述了另外的方面。整个文献旨在作为统一的公开内容相关联,并且应当理解,考虑本文所述的特征的所有组合,即使特征的组合并非在本文献的同一句子或段落或部分中一起被发现。本发明的其他特征和优点通过以下详细描述将变得清楚。然而,应当理解,尽管详细描述和具体实施例指示本公开文本的具体实施方案,但它们仅通过说明的方式给出,因为从此详细描述中,本公开文本的精神和范围内的各种改变和修改对于本领域技术人员来说将变得清楚。
附图说明
[0016]
图1a和图1b是示出了用作嵌入聚合物膜的纳米孔的典型非膜蛋白(作为截锥结构示出)的不同功能层的示意图。图1a示出了对于膜锚定重要的三个不同结构域。图1b示出了对于单分子感测的功能模块的缀合特别重要的两个区域。
[0017]
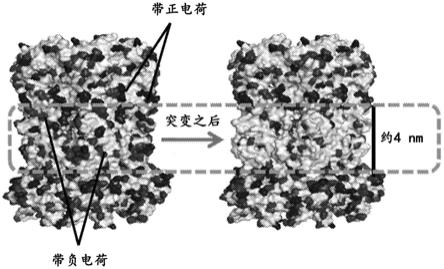
图2示出了在用于直接膜插入的膜锚定层中诱变的例子,其中以phi29gp9δloop尾蛋白作为例子示出。在中间层(加框)上进行一系列疏水性突变以增加其直接膜插入的能力之前和之后phi29 gp9δloop尾蛋白通道的结构。示例性突变位点包括:k134i、d138l、d139l、d158l、e163v、e309v、d311v、k321v、k356a、k358a、d377a、d381v、n388l、r524i、r539a和e595v。表达和纯化之后,突变体蛋白自发地插入到聚合物膜中。指示了代表性的带正电的残基(例如,r和k)和代表性的带负电的残基(例如,e、q、d和n)。
[0018]
图3示出了噬菌体蛋白表达和纯化的例子,其中显示了phi29 gp9尾蛋白的蛋白质
表达和纯化。考马斯蓝染色的sds-page凝胶显示具有70.33kda分子量的phi29 gp-9尾蛋白通道的表达。
[0019]
图4是示例性考马斯蓝染色的sds-page凝胶,其显示大部分gp-9尾蛋白通道在纯化和组装之后存在于100kda的柱中,从而指示所述通道是由其约70kda的单体单元组装而成的。
[0020]
图5是在非膜蛋白表面中靶位点选择的例子,如使用phi29 gp9尾蛋白所显示的。phi29 gp9尾蛋白结构显示三个可能的残基,用于诱变为半胱氨酸,以缀合疏水性膜锚定模块。
[0021]
图6示出了插入到聚合物膜中的非膜蛋白通道的例子,如使用phi29gp9δloop尾蛋白所显示的。单通道记录数据显示phi29 gp9δloop通道直接插入到组合物pmoxa
6-pdms
65-pmoxa6的聚合物膜中。导电缓冲液:1m nacl,5mm tris,ph 7.6。施加电压:75mv。
[0022]
图7a和图7b示出了噬菌体p22 gp1门户蛋白全长(图7a)和桶结构(barrel)缺失突变体(图7b)的结构。
[0023]
图8示出了在非膜蛋白中用于膜锚定的靶位点选择的例子,如使用p22gp1门户蛋白所显示的。在噬菌体p22 gp1门户蛋白的结构上显示了用于并入膜锚定结构域的代表性缀合位点(例如,可及的半胱氨酸残基,c283)。
[0024]
图9示出了用融合的肽探针功能化的非膜蛋白孔的例子,如使用与vcam1融合的p22 gp1门户蛋白所显示的。考马斯蓝染色的凝胶显示在c末端与vcam1探针融合的纯化的噬菌体p22 gp1门户蛋白全长和桶结构缺失突变体。
[0025]
图10示出了用融合的肽探针功能化的非膜蛋白孔的例子,如使用与psa融合的p22 gp1门户蛋白所显示的。考马斯蓝染色的凝胶显示在c末端与psa探针融合的纯化的噬菌体p22 gp1门户蛋白桶结构缺失突变体。
[0026]
图11示出了用用于单分子感测的融合的肽探针功能化的非膜蛋白孔的例子,如使用与用于检测psa的psa探针融合的p22 gp1门户蛋白所显示的。单通道记录数据显示携带融合psa探针的p22 gp1蛋白通道直接插入到组合物pmoxa6-pdms35-pmoxa6的聚合物膜中。在psa(10ng/ul)存在的情况下,探针与psa结合并导致特征性电流阻断事件。导电缓冲液:1m kcl,5mm tris,ph 7.6。施加电压:75mv。
[0027]
图12示出了在非膜蛋白中用于膜锚定的靶位点选择的例子,如使用t4gp20门户蛋白所显示的。在噬菌体t4 gp20门户蛋白的结构上指示了用于并入膜锚定结构域的代表性缀合位点(例如,经由可及的半胱氨酸残基c217、245、246)。
[0028]
图13示出了用胆固醇-peg-马来酰亚胺标记非膜蛋白通道用于膜锚定的例子,如使用t4 gp20门户蛋白所显示的。
[0029]
图14示出了插入在聚合物膜中的非膜蛋白通道的例子,如使用携带胆固醇的t4 gp20门户蛋白所显示的。在施加的电势下观察到蛋白质的逐步直接插入。导电缓冲液:1m kcl,5mm tris,ph 7.6。施加电压:100mv。膜:pmoxa6-pdms35-pmoxa6。
[0030]
图15示出了经由点击化学将探针缀合到非膜蛋白通道的例子,如使用phi29 gp10门户蛋白所显示的。将硫醇-mir-21探针用tco(反式-环辛烯)标记,接着将tco-mir-21探针缀合到甲基四嗪蛋白。sds-page凝胶验证了靶mir-21与缀合到蛋白质的mir-21探针的结合。
[0031]
图16示出了使用探针功能化的非膜蛋白孔进行分析物(例如,mirna)检测的例子,如使用t4 gp20门户蛋白所显示的。在靶mirna存在的情况下,观察到电流阻断事件,从而指示在单分子水平下检测到mirna。导电缓冲液:1m kcl,5mm tris,ph 7.6。施加电压:100mv。膜:pmoxa6-pdm s35-pmoxa6。
[0032]
图17a示出了用于插入作为纳米孔的非膜蛋白的基于聚噁唑啉的三嵌段共聚物的例子,如使用pmoxa
6-pdms
65-pmoxa6所显示的。
[0033]
图17b示出了平面膜在2天过程中的稳定性。膜没有显示膜泄漏的迹象。膜:pmoxa
6-pdms
35-pmoxa6。
[0034]
图17c和图17d示出了使用聚合物囊泡与平面聚合物膜的融合体插入非膜蛋白孔的例子,如使用phi29 gp9尾蛋白(图17c)和p22 gp1门户蛋白(图17d)所显示的。图17c中的平面膜和聚合物囊泡组合物:pmoxa
11-pdms
65-pmoxa
11
;图17d中的平面膜和聚合物囊泡组合物:pmoxa
5-pdms
13-pm oxa5;
[0035]
图18示出了具有用于并入分析物探针的spytag/spycatcher系统的非膜蛋白的例子,如使用phi29 gp10门户蛋白所显示的。考马斯蓝染色的sds-page凝胶显示并入在phi29 gp10门户蛋白中的spytag与psa-spycatcher蛋白结合形成复合物。然后,功能化的孔可以用于感测psa,如图19所示。
[0036]
图19示出了用于使用spytag-spycatcher系统进行分析物检测的非膜蛋白通道的例子,如使用phi29 gp10门户蛋白所显示的。直接插入之后,phi29gp10门户上的spytag/spycatcher(psa探针)能够检测溶液中的psa(10ng/ul),如作为电流阻断事件显示。导电缓冲液:1m kcl,5mm tris,ph 7.6。施加电压:100mv。膜:pmoxa
6-pdms
35-pmoxa6。
具体实施方式
[0037]
本公开文本提供了适用于检测不同分析物的稳健纳米孔系统和方法。它允许检测单个分子和与其他污染物一起存在的靶分子。所述系统提供无标记、无扩增的实时检测。它需要非常低的样品量并且可以用于高通量分析。所述系统可以适于以高灵敏度和特异性检测具有不同形状、大小和亲水/疏水特性的各种分析物(例如,小分子、聚合物、多肽和核苷酸)。
[0038]
本公开文本通过提供由非膜蛋白(例如来源于噬菌体的蛋白质)形成的纳米孔满足了本领域的需求。为了生成所公开的纳米孔,将噬菌体蛋白表达、纯化、自组装并插入在脂膜或聚合物膜中。然而,非膜蛋白通道更难直接插入到脂质双层或聚合物膜中。与膜蛋白通道不同,非膜蛋白通道通常缺少中间的疏水和两端的亲水层。本发明通过采用一系列方法克服了这一限制,所述方法用于将各种蛋白质通道直接或通过高效融合机制插入聚合物膜中。此外,在一些情况下,进行蛋白质工程化,诸如定点诱变、氨基酸的插入和缺失,以及功能模块的引入,以调谐纳米孔特性来满足不同的检测需求。
[0039]
所公开的纳米孔系统具有广泛的应用,包括但不限于单分子检测、dna/rna/肽测序、化学物、生物试剂和聚合物的感测,以及疾病诊断。如将在以下进一步描述的,采用所公开的纳米孔系统的方法、试剂盒和检测装置也在本公开文本的范围内。
[0040]
i.纳米孔组件
[0041]
本公开文本的一方面涉及由非膜蛋白形成的纳米孔。适用于形成纳米孔的非膜蛋
白可以来源于细胞dna转位酶、解旋酶、末端酶、atp酶及其片段。适用于形成纳米孔的非膜蛋白还可以包括dna修复、复制、重组、染色体分离、dna/rna运输、膜分选、细胞重组、细胞分裂、细菌二分分裂和其他过程中涉及的蛋白质。
[0042]
纳米孔可以包括多个亚基,每个亚基包含非膜蛋白。例如,纳米孔可以包括10至15个噬菌体门户蛋白的亚基或5至10个噬菌体尾蛋白的亚基。形成纳米孔的非膜蛋白通道可以来源于噬菌体门户蛋白,包括但不限于t3、t4、t5、t7、spp1、p22、p2、p3、λ、μ、hk97和c1。例如,形成纳米孔的非膜蛋白通道可以来源于噬菌体尾蛋白,包括但不限于phi29、c1、脑膜炎奈瑟球菌b血清群(neisseria meningitidis serogroup b)、t4、phix174、λ、spp1、t5、μ、f4-1、p2、沙雷氏菌噬菌体ksp90、肠杆菌噬菌体t7m、噬菌体hk97。
[0043]
与噬菌体蛋白(例如,噬菌体门户蛋白或尾蛋白)具有显著同一性的变体和同源物也在本公开文本的范围内,包括但不限于t3、t4、t5、t7、spp1、p22、p2、p3、λ、μ、hk97和c1。例如,此类变体和同源物可以具有与本文所述的噬菌体门户蛋白的序列具有至少约70%、约71%、约72%、约73%、约74%、约75%、约76%、约77%、约78%、约79%、约80%、约81%、约82%、约83%、约84%、约85%、约86%、约87%、约88%、约89%、约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%或约99%序列同一性的序列。
[0044]
生物孔诱变可以用于优化蛋白质孔,以用于组装或用于本文所述的组合物或方法中。例如,蛋白质工程化和诱变技术可以用于使生物孔突变并针对特定应用调整其特性。因此,纳米孔组件可以包括由多个亚基形成的通道。每个所述亚基包含具有与选自seq id no:1-35的多肽序列具有至少75%同一性的多肽序列的多肽。在一些实施方案中,所述多肽包含与seq id no:4-12至少75%相同的多肽序列。
[0045]
所述亚基可以包含一个或多个取代、缺失或插入,以促进纳米孔的功能化或插入膜中。例如,所述亚基可以包含至少一个被半胱氨酸取代的残基,使得官能团可以经由二硫键连接到所述亚基。例如,半胱氨酸残基可以用于将诸如卟啉的化学物缀合到纳米孔。在一些实施方案中,所述亚基可以包括具有e595c、k321c和k358c取代中的一个或多个的phi29 gp9蛋白。
[0046]
此外,所述亚基可以包括具有k134i、d138l、d139l、d158l、e163v、e309v、d311v、k321v、k356a、k358a、d377a、d381v、n388l、r524i、r539a和e595v取代中的一个或多个的phi29 gp9蛋白。用疏水性残基(例如,a、v、l)取代带电荷的残基(例如,k、r、d、e)局部和整体地增加了蛋白质的疏水性。
[0047]
在一些实施方案中,将蛋白质通道并入膜或纳米盘中的过程可以得益于蛋白质上的亲和标签(例如,聚组氨酸亲和标签),并且得益于亲和柱(例如,ni柱)上混合纳米孔群体的纯化。亲和标签和化学缀合技术(例如,以上所示的半胱氨酸的修饰)可以用于将系链连接到纳米孔,以用于本文所示的各种方法、组合物或装置。例如,所得的系链可以用于将纳米孔吸引或连接到固体支撑物或电极。
[0048]
表1.通道蛋白的氨基酸序列
[0049]
[0050]
[0051]
[0052]
[0053]
[0054]
[0055]
[0056]
[0057][0058]
表2.接头和探针的序列
[0059]
[0060]
[0061][0062]
表3.核酸序列
[0063]
[0064]
[0065]
[0066]
[0067]
[0068]
[0069]
[0070]
[0071]
[0072]
[0073]
[0074]
[0075]
[0076]
[0077]
[0078][0079]
如本文所用的术语多肽“变体”是通常与本文明确公开的多肽相差一个或多个取代、缺失、添加和/或插入的多肽。此类变体可以是天然存在的或可以是合成产生的,例如,通过修饰本公开文本的以上多肽序列中的一个或多个,和评估如本文所述的多肽的一种或多种生物活性,和/或使用本领域熟知的一些技术中的任一种。
[0080]
例如,某些氨基酸可以取代蛋白质结构中的其他氨基酸,而不会明显丧失所述蛋白质结合其他多肽或细胞的能力。由于决定蛋白质的生物功能活性的是该蛋白质的结合能力和性质,所以可以在蛋白质序列中并且因此在其基础dna编码序列中进行某些氨基酸序列取代,从而获得具有类似特性的蛋白质。因此,可以设想,可以在所公开的组合物的肽序列或编码所述肽的对应dna序列中进行各种变化,而不会明显丧失其生物实用性或活性。
[0081]
变体序列包括其中已经通过修饰编码本公开文本的多肽的多核苷酸而引入保守取代的那些。氨基酸可以根据物理特性以及对二级和三级蛋白质结构的贡献进行分类。此类保守修饰包括氨基酸取代、添加和缺失。保守氨基酸取代是其中氨基酸残基被具有相似侧链的氨基酸残基替代的氨基酸取代。本领域已经定义了具有相似侧链的氨基酸残基家族。这些家族包括具有以下侧链的氨基酸:碱性侧链(例如,赖氨酸、精氨酸、组氨酸)、酸性
侧链(例如,天冬氨酸、谷氨酸)、不带电荷的极性侧链(例如,甘氨酸、天冬酰胺、谷氨酰胺、丝氨酸、苏氨酸、酪氨酸、半胱氨酸、色氨酸)、非极性的侧链(例如,丙氨酸、缬氨酸、亮氨酸、异亮氨酸、脯氨酸、苯丙氨酸、甲硫氨酸)、β-分支侧链(例如,苏氨酸、缬氨酸、异亮氨酸)以及芳香族侧链(例如,酪氨酸、苯丙氨酸、色氨酸、组氨酸)。
[0082]“序列同一性”或“同源性”是指在比对序列并引入空位(如果需要的话)以实现最大同源性百分比之后,多核苷酸或多肽序列变体中与非变体序列相同的残基的百分比。在具体实施方案中,多核苷酸和多肽变体具有与本文所述的多核苷酸或多肽的至少约70%、至少约75%、至少约80%、至少约90%、至少约95%、至少约98%或至少约99%的多核苷酸或多肽同源性。
[0083]
多肽变体序列可以与本公开文本中列举的序列共享70%或更高(即80%、85%、90%、95%、97%、98%、99%或更高)的序列同一性。多肽变体还可以包括多肽片段,其包含本文公开的氨基酸序列的各种长度的连续延伸段。多肽变体序列包括本文公开的一个或多个序列的至少约5、10、15、20、30、40、50、75、100、150或更多个连续肽以及它们之间的所有中间长度。
[0084]
ii.用探针功能化的纳米孔组件
[0085]
一方面,纳米孔组件还包括用于检测分析物的探针。所述探针可操作地连接到至少一个亚基。这种探针缀合到纳米孔组件,以允许一种或多种分析物的选择性结合。探针可以以各种化学计量(探针与纳米孔组件之间的摩尔比)缀合到纳米孔组件。在一个例子中,探针可以缀合到每个亚基。在另一个例子中,仅一个探针缀合到纳米孔组件。还设想包括两种或更多种不同类型的探针的纳米孔组件。此类功能化的纳米孔组件可以用于检测分析物,诸如核酸、氨基酸、肽、蛋白质、聚合物和化学分子。在一些实施方案中,分析物是psa、cea、afp、vcam、mir-155、mir-22、mir-7、mir-92a、mir-122、mir-192、mir-223、mir-26a、mir-27a、mir-802或其片段中的一种。
[0086]
术语“特异性结合(specific binding)”、“选择性结合(selective binding)”、“选择性地结合(selectively binds)”和“特异性地结合(specifically binds)”是指纳米孔组件上的探针与样品中的分析物的结合强于与样品中存在的其他污染物的结合。例如,在通过结合测定(例如elisa、平衡透析或2000表面等离子体共振仪器中的表面等离子体共振(spr)技术)确定时,探针可以以大约小于10-6
m,诸如大约小于10-7
m、10-8
m、10-9
m或10-10
m或甚至更低的平衡解离常数(kd)结合分析物。
[0087]
所述探针可以是化学物、碳水化合物、适体、核酸、肽、蛋白质、抗体和受体中的一种。在一些实施方案中,探针可以包含与seq id no:36-79的序列至少75%相同的序列。在一些实施方案中,所述探针是抗psa抗体。探针经由共价键可操作地连接到至少一个亚基。探针可以经由亚基上的一个或多个功能位点连接到所述亚基。此类功能位点可以通过诱变,例如用半胱氨酸或其他非天然氨基酸取代来引入。探针也可以经由公认的化学方法连接到通道,包括但不限于酯键、点击化学和巯基键。在一些实施方案中,探针可操作地连接到接近通道的入口的位置或在通道的内侧的位置。
[0088]
iii.具有膜的纳米孔组件
[0089]
另一方面,本公开文本提供了一种纳米孔组件,其中通道被插入在膜中。根据应用,聚合物膜可以具有各种组成,呈独立形式或在微流体装置中。聚合物膜嵌入式通道展示
出稳健的电生理特性,这是基于纳米孔的单分子分析的首要特征。膜可以包括聚合物膜(例如,平面聚合物膜)或脂膜。聚合物膜的性质可以是对称的或不对称的。例如,聚合物膜是交替共聚物(例如,a-b-a-b
-…
)或周期共聚物(例如,aa-bb-aa-bb
…
)。在另一个例子中,聚合物膜可以是由通过共价键连接的两个或更多个均聚物亚基构成的嵌段共聚物。可替代地,聚合物膜可以是二嵌段或三嵌段共聚物(例如,pmoxa-pdms-pmoxa)。聚合物膜也可以是由三个不同单体组成的三元共聚物。
[0090]
在一些实施方案中,聚合物膜包含交替共聚物、周期共聚物、嵌段共聚物、二嵌段共聚物、三嵌段共聚物、三元共聚物或其组合。在一些实施方案中,聚合物膜包含pmoxa-pdms-pmoxa。
[0091]
在一些实施方案中,通道被嵌入在各种大小的聚合物囊泡中。在一些实施方案中,聚合物囊泡与平面聚合物膜融合以插入通道。聚合物囊泡由亲水-疏水嵌段共聚物构成,以具有中心水性核的双层囊泡系统布置。它们具有亲水性内核和亲脂性双层。它们与纳米颗粒的不同之处在于,它们含有亲水性核心,而不是纳米颗粒的情况中的亲脂性核心。尽管它们具有双层结构,但是由于存在厚且刚性的双层,它们比脂质体具有更高的稳定性。它们含有提供蛋白质亲和环境的亲水性核心。
[0092]
在一些实施方案中,在各种组成的任何洗涤剂(例如,基于ddm、doc、tween、sds和brij的洗涤剂)的存在下,将通道插入到聚合物膜中。在一些实施方案中,在存在不同量的甘油、cscl和/或蔗糖以供高效融合的情况下,将蛋白质通道重构到聚合物囊泡中。
[0093]
在一些实施方案中,通过诱变(例如,含有一个至若干个取代)将蛋白质通道重工程化,以有利于插入在(平面)聚合物膜中。此外,出于在聚合物膜中插入的目的,将蛋白质通道重工程化以引入功能性位点,用于用化学物或生物聚合物进行位点特异性标记。此类功能性位点包括用于缀合化学物(诸如卟啉)或生物分子(诸如胆固醇或任何疏水性脂质模块或各种长度的核酸)的半胱氨酸残基。功能性位点/基团还可以包括通过公认的化学方法产生的非天然氨基酸和连接,所述化学方法包括但不限于酯、点击化学和巯基。
[0094]
在一些实施方案中,缀合的位置在通道的膜锚定层中,例如t4 gp 20门户蛋白的残基70-80、110-140、155-245、300-340、410-435;p22 gp1门户蛋白的残基10-45、250-300;以及phi29 gp9尾蛋白的残基130-170、300-325、350-390、530-595。因此,为了增加或减少用于膜插入目的的带状区的疏水性,重工程化可以包括以下中的任一个的诱变(例如,取代、插入、缺失):t4 gp 20门户蛋白的残基70-80、110-140、155-245、300-340、410-435;p22 gp1门户蛋白的残基450-500、350-380;以及phi29 gp9尾蛋白的残基130-170、300-325、350-390、530-595。
[0095]
在一些实施方案中,缀合的位置在通道的顺式和反式亲水层中,诸如t4 gp 20门户蛋白的残基465-515、285-305;p22 gp1门户蛋白的残基450-500、350-380;以及phi29 gp9尾蛋白的残基20-50和250-300。因此,为了增加或减少用于膜插入目的的带状区的疏水性,重工程化可以包括诱变(例如,取代、插入、缺失),可以包括以下中的任一个:t4 gp 20门户蛋白的残基465-515、285-305;p22 gp1门户蛋白的残基450-500、350-380;以及phi29 gp9尾蛋白的残基20-50和250-300。
[0096]
iv.包含纳米孔组件的装置和试剂盒
[0097]
另一方面,本公开文本还提供了一种用于检测分析物的试剂盒和检测设备。所述
试剂盒可以包括所述的纳米孔组件、任选地缓冲液和任选地使用所述纳米孔组件的说明书。
[0098]
所述设备可以包括所述的纳米孔组件和用于所述纳米孔组件的支撑物。所述检测设备还可以包括嵌入在固体支撑物中的电极。电极可以用于监测蛋白质纳米孔组装到膜中。电极还可以用于分析物检测步骤期间的数据采集。用于监测和检测的电极不必嵌入在支撑物中,并且可以例如设置在单独的专用集成电路(asic)芯片中。
[0099]
如本文所用,术语“支撑物”是指不可溶于水性液体并且在没有孔口的情况下不能使液体穿过的刚性衬底。示例性固体支撑物包括但不限于玻璃和改性或功能化玻璃、塑料(包括丙烯酸树脂、聚苯乙烯以及苯乙烯与其他材料的共聚物、聚丙烯、聚乙烯、聚丁烯、聚氨酯、teflon
tm
、环烯烃、聚酰亚胺等)、尼龙、陶瓷、树脂、zeonor、二氧化硅或基于二氧化硅的材料(包括硅和改性硅)、碳、金属、无机玻璃、光纤束和聚合物。特别有用的支撑物包括改性硅,例如在si衬底上的sin膜。对于一些实施方案,支撑物位于流动池设备或其他容器内。
[0100]
在一些实施方案中,纳米孔在衬底诸如芯片、盘、块、板等上制造。此类衬底可以由各种材料制成,所述材料包括但不限于硅、玻璃、陶瓷、锗、聚合物(例如,聚苯乙烯)和/或砷化镓。衬底可以被蚀刻或可以不被蚀刻,例如芯片可以是半导体芯片。
[0101]
在具体实施方案中,检测设备可以包括与纳米孔阵列接触的储器。储器可以容纳电极,所述电极被定位以施加穿过由蛋白质纳米孔形成的孔口的电流。
[0102]
在一些实施方案中,本公开文本的检测设备可以包括(a)电极;(b)栓系到电极的纳米孔;以及(c)包围纳米孔的膜。还提供了多重实施方案。例如,检测设备可以包括(a)多个电极;(b)多个纳米孔,每个所述纳米孔栓系到所述多个电极中的一个电极;以及(c)包围每个所述纳米孔的膜。
[0103]
可以使用共价部分或非共价结合部分将纳米孔拴系到电极(例如,经由绝缘垫)。共价连接的一个例子是当核酸系链共价连接到纳米孔并共价连接到绝缘垫时。其他系链可以类似地用于共价连接,包括例如非核酸系链,诸如聚乙二醇或其他合成聚合物。非共价连接的一个例子是当纳米孔具有连接的亲和部分时,诸如聚组氨酸标签、strep-标签或其他氨基酸编码的亲和部分。亲和部分可以非共价结合到绝缘垫上的配体,所述配体诸如结合聚组氨酸的镍或其他二价阳离子,或结合strep-标签的生物素(或其类似物)。在一些实施方案中,不需要使用此类氨基酸亲和部分。
[0104]
如本文所述,纳米孔(无论是复合纳米孔还是栓系纳米孔)可以与检测电路耦合以记录本公开文本的方法中的电信号,所述检测电路包括例如膜片钳电路、隧穿电极电路或横向电导测量电路(诸如石墨烯纳米带,或石墨烯纳米间隙)。此外,孔还可以与光学传感器耦合,所述光学传感器检测多核苷酸上的标记,例如荧光部分或拉曼信号产生部分。
[0105]
本公开文本的检测设备可以用于检测各种分析物中的任一种,包括但不限于离子、核酸、核苷酸、多肽、生物活性小分子、脂质、糖等。因此,在本文所示的设备中,这些分析物中的一种或多种可以存在于蛋白质纳米孔的孔口中或穿过蛋白质纳米孔的孔口。
[0106]
可以应用于本文所示的设备的其他检测技术包括但不限于检测事件,诸如分子或此分子的一部分的运动,特别是在所述分子是dna或结合dna的酶诸如聚合酶的情况下。例如,通过引用并入本文的olsen等人,jacs 135:7855-7860(2013)披露了将dna聚合酶i的klenow片段(kf)的单分子生物缀合到电子纳米电路中,以便允许对酶功能和动态可变性进
行电子记录,且解析单独的核苷酸并入事件。或者,例如,通过引用并入本文的hurt等人,jacs 131:3772-3778(2009)披露了测量dna与kf的复合物在所施加电场中在纳米孔顶上的停留时间。或者,例如,通过引用并入本文的kim等人,sens.actuators b chem.177:1075-1082(2012)披露了在实验中使用电流测量传感器,所述实验涉及在α-溶血素纳米孔中捕获的dna。或者,例如,通过引用并入本文的garalde等人,j.biol.chem.286:14480-14492(2011)披露了当被捕获在α-溶血素孔顶上的电场中时,基于kf-dna复合物的特性来区分kf-dna复合物。披露涉及α-溶血素的测量的其他参考文献包括以下(全部属于howorka等人,通过引用并入本文):pnas 98:12996-13301(2001);biophysical journal 83:3202-3210(2002);以及nature biotechnology 19:636-639(2001)。
[0107]
在一些实施方案中,本发明涉及组装到脂质双层膜中的通道蛋白。通过以固定的施加电势穿过孔的离子电流来监测分析物的存在,其中电流的中断指示分析物与通道蛋白的相互作用。在一些实施方案中,稳定化的传感器芯片含有单个蛋白质纳米孔蛋白。蛋白质纳米孔传感器芯片可以应用于在单分子水平下进行的测量,即随机感测。通过监测以固定的施加电势穿过孔的离子电流,可以基于单独电流阻断事件的振幅和持续时间来区分各种分析物。
[0108]
v.用于使用纳米孔组件检测分析物的方法
[0109]
另一方面,本公开文本提供了一种检测/感测分析物的方法。所述方法包括:(1)使含有分析物的样品与所述的纳米孔组件接触;(2)施加跨过纳米孔组件的通道的电流;(3)以一个或多个时间间隔确定穿过通道的电流;以及(4)将以一个或多个时间间隔测量的电流与参考电流进行比较,其中相对于参考电流的电流变化指示样品中分析物的存在。在一些实施方案中,参考电流是用不含分析物的样品测量的。在一些实施方案中,纳米孔组件被放置在支撑物上。
[0110]
在一些实施方案中,所述方法可以包括测量由每单位分析物或聚合物穿过通道的转位诱导的离子电流和/或电流特征的变化。在一些实施方案中,所述方法可以包括测量由每单位分析物或聚合物与通道上耦合的探针的瞬时或永久结合诱导的离子电流和/或电流特征的变化,所述结合导致电流特征的变化。
[0111]
可以通过本公开文本公开的方法检测的分析物可以是核酸、氨基酸、肽、蛋白质、聚合物和化学分子中的任一种。所述方法中检测的核酸可以是单链的、双链的或含有单链和双链序列两者。核酸分子可以起源于双链形式(例如,dsdna)并且可以任选地转化为单链形式。核酸分子也可以起源于单链形式(例如,ssdna、ssrna),并且ssdna可以任选地转化为双链形式。
[0112]
vi.定义
[0113]
为了帮助理解根据本公开文本的组合物和方法的详细描述,提供一些明确的定义以有利于本公开文本的各个方面的无歧义公开。
[0114]
除非另外定义,否则本文所用的所有技术和科学术语具有与本公开文本所属领域的普通技术人员通常所理解相同的含义。
[0115]
应当注意,如在本说明书和所附权利要求书中所用的,单数形式的“一个/一种(a)”、“一个/一种(an)”和“所述”包括复数指示物,除非上下文清楚地另外指明。除非另外说明,否则术语“包括”、“包含”、“含有”或“具有”及其变型旨在涵盖其后列出的项目及其等
效物以及另外的主题。
[0116]
如本文所用,在关于项目的集合使用时,术语“每个”旨在标识集合中的单独项目,但不一定是指集合中的每个项目。如果明确的公开文本或上下文清楚地另外说明,则可能出现例外情况。
[0117]
除非另外声明,否则本文中提供的任何和所有例子或示例性语言(例如,“诸如”)的使用都仅旨在更好地说明本发明,并且不对本发明的范围施加任何限制。说明书中的语言不应当被解释为指示任何未要求保护的要素是实践本发明所必需的。
[0118]
如本文所用,术语“纳米孔”和“通道”用于是指具有离子电流可以流过的纳米级通路的结构。纳米孔的内径可以根据装置的预期用途而有极大地变化。通常,通道或纳米孔具有至少约0.5nm,通常至少约1nm并且更通常至少约1.5nm的内径,其中所述直径可以长达50nm或更长,但是在许多实施方案中,不会超过约10nm,并且通常不会超过约2nm。
[0119]
如本文所用,术语“分析物”是指正在进行分析或试图被检测的物质或化学成分。预期本发明不限于特定的分析物。代表性分析物包括离子、糖、蛋白质、核酸和核酸序列。
[0120]
如本文所用,术语“膜”是指防止电流或流体通过的片材或其他屏障。相比于本文所示的固体支撑物,膜通常是柔性的或可压缩的。膜可以由脂质材料制成,例如以形成脂质双层,或者膜可以由非脂质材料制成。膜可以呈例如由二嵌段聚合物或三嵌段聚合物形成的共聚物膜的形式,或者呈例如由勃拉脂质(bolalipid)形成的单层的形式。参见例如,rakhmatullina等人,langmuir:the acs journal of surfaces and colloids 24:6254-6261(2008),其通过引用并入本文。
[0121]
如本文所用,术语“脂膜”意指主要由包含饱和或不饱和、支链或无支链、芳族或非芳族烃基团的化合物制成的膜。膜可以由多种脂质构成。脂质的例子包括但不限于脂肪酸、甘油单酯、甘油二酯和甘油三酯、甘油磷脂、鞘脂、类固醇、脂蛋白和糖脂。
[0122]“核酸”或“核酸序列”或“核酸分子”是指单链或双链形式的脱氧核糖核苷酸或核糖核苷酸及其聚合物。术语核酸可与基因、互补dna(cdna)、信使rna(mrna)、寡核苷酸和多核苷酸互换使用。所述术语涵盖含有已知核苷酸类似物或经修饰的骨架残基或连接的核酸,其是合成的、天然存在的和非天然存在的,其具有与参考核酸类似的结合特性,并且其以与参考核苷酸类似的方式代谢。此类类似物的例子包括但不限于硫代磷酸酯、氨基磷酸酯、甲基膦酸酯、手性甲基膦酸酯、2-o-甲基核糖核苷酸、肽核酸(pna)。所述术语涵盖由dna和rna的任何已知碱基类似物形成的分子,诸如但不限于4-乙酰基胞嘧啶、8-羟基-n6-甲基腺嘌呤、氮丙啶基-胞嘧啶、假异胞嘧啶、5-(羧基羟甲基)尿嘧啶、5-氟尿嘧啶、5-溴尿嘧啶、5-羧甲基氨基甲基-2-硫尿嘧啶、5-羧基-甲基氨基甲基尿嘧啶、二氢尿嘧啶、肌苷、n6-异戊烯基腺嘌呤、1-甲基腺嘌呤、1-甲基假尿嘧啶、1-甲基鸟嘌呤、1-甲基肌苷、2,2-二甲基-鸟嘌呤、2-甲基腺嘌呤、2-甲基鸟嘌呤、3-甲基胞嘧啶、5-甲基胞嘧啶、n6-甲基腺嘌呤、7-甲基鸟嘌呤、5-甲基氨基甲基尿嘧啶、5-甲氧基氨基-甲基-2-硫尿嘧啶、β-d-甘露糖基辫苷(beta-d-mannosylqueosine)、5'-甲氧基羰基-甲基尿嘧啶、5-甲氧基尿嘧啶、2-甲硫基-n6-异戊烯基腺嘌呤、尿嘧啶-5-氧乙酸甲酯、尿嘧啶-5-氧乙酸、氧基丁氧基胸苷(oxybutoxosine)、假尿嘧啶、辫苷、2-硫胞嘧啶、5-甲基-2-硫尿嘧啶、2-硫尿嘧啶、4-硫尿嘧啶、5-甲基尿嘧啶、n-尿嘧啶-5-氧乙酸甲酯、尿嘧啶-5-氧乙酸、假尿嘧啶、辫苷、2-硫胞嘧啶和2,6-二氨基嘌呤。
[0123]
除非另外指示,否则特定核酸序列还暗示涵盖其保守修饰的变体(例如,简并密码子取代)和互补序列以及明确指示的序列。具体地,在一些方面,简并密码子取代通过生成其中一个或多个所选(或所有)密码子的第三位置经混合碱基和/或脱氧肌苷残基取代的序列来实现(batzer,nucleic acid res.19:5081,1991;ohtsuka等人,j.biol.chem.260:2605-8,1985;rossolini等人,mol.cell.probes 8:91-8,1994)。术语核酸可与基因、cdna、mrna、寡核苷酸和多核苷酸互换使用。
[0124]“多肽”以其常规含义使用,即作为氨基酸的序列使用。多肽不限于特定长度的产物。肽、多肽和蛋白质包括在多肽的定义内,并且除非另外明确指示,否则此类术语可以在本文中可互换使用。此术语还包括多肽的表达后修饰,例如糖基化、乙酰化、磷酸化等,以及本领域已知的其他修饰,可以是天然存在的和非天然存在的。多肽可以是完整蛋白质或其子序列。
[0125]
本领域已知的术语“相同的”或“同一性”百分比是指两个或更多个多肽分子或者两个或更多个核酸分子的序列之间的关系,如通过比较序列所确定。在本领域中,“同一性”还意指核酸分子或多肽(视情况而定)之间的序列相关性程度,如通过两个或更多个核苷酸序列或者两个或更多个氨基酸序列的串之间的匹配所确定。“同一性”测量具有空位比对(如果存在)的两个或更多个序列中较小的序列之间相同匹配的百分比,所述空位通过特定数学模型或计算机程序(即,“算法”)定址。“基本同一性”是指具有与指定序列的至少约70%、约71%、约72%、约73%、约74%、约75%、约76%、约77%、约78%、约79%、约80%、约81%、约82%、约83%、约84%、约85%、约86%、约87%、约88%、约89%、约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%或约99%序列同一性的序列。在一些方面,同一性存在于长度为至少约50-100个氨基酸或核苷酸的区域。在其他方面,同一性存在于长度为至少约100-200个氨基酸或核苷酸的区域。在其他方面,同一性存在于长度为至少约200-500个氨基酸或核苷酸的区域。在某些方面,使用选自gap、blastp、blastn、fasta、blasta、blastx、bestfit和smith-waterman算法的计算机程序确定序列同一性百分比。
[0126]
术语“相似性”是相关概念,但是相比于“同一性”,是指包括相同匹配和保守取代匹配两者的相似性的量度。如果两个多肽序列具有例如10/20个相同氨基酸,并且其余部分均为非保守取代,则同一性和相似性百分比均为50%。在同一例子中,如果还有五个位置存在保守取代,则同一性百分比仍为50%,但相似性百分比将为75%(15/20)。因此,在存在保守取代的情况下,两个多肽之间的相似性百分比程度将高于这两个多肽之间的同一性百分比。
[0127]
还应当特别理解的是,本文列举的任何数值包括从下限值到上限值的所有值,即,在所列举的最低值与最高值之间的数值的所有可能的组合被认为在本申请中明确声明。例如,如果声明浓度范围为约1%至50%,则预期诸如2%至40%、10%至30%或1%至3%等的值明确地列举在本说明书中。上面列出的值仅是特别预期的例子。
[0128]
在各个方面,范围在本文中表达为从“约”或“大约”一个具体值和/或到“约”或“大约”另一个具体值。当通过使用先行词“约”将值表达为近似值时,应当理解,一定量的变化也包括在范围内。
[0129]
术语“可操作地连接”是指核酸表达控制序列(诸如启动子或转录因子结合位点的阵列)与第二核酸序列之间的功能性连接,其中表达控制序列引导对应于第二序列的核酸
的转录。
[0130]
如本文所用,如本文所用的术语“纯化的”或“基本上纯化的”是指所需蛋白质富集至少20%,更优选地至少50%,甚至更优选地至少75%,并且最优选地至少90%或甚至95%。
[0131]
本文引用的每个出版物、专利申请、专利和其他参考文献均通过引用以其整体并入,并入程度使其与本公开文本一致。
[0132]
本文公开的出版物的提供仅针对其先于本发明的提交日期的公开内容。本文中的任何内容都不应视为承认本发明因在先发明而无权早于此类出版物。此外,所提供的出版日期可能与实际出版日期不同,这可能需要独立确认。
[0133]
除非本文另外指示,否则本文中列举的数值的范围仅旨在用作单独地提到落在所述范围内的每个单独值和每个终点的速记方法,并且每个单独值和终点纳入说明书中如同其在本文中单独列举一般。
[0134]
除非本文中另外指示或根据上下文另有明确矛盾,否则本文所述的所有方法都以任何合适的顺序来进行。关于所提供的任何方法,方法的步骤可以同时或顺序进行。当方法的步骤顺序进行时,除非另外说明,否则所述步骤可以按任何顺序进行。
[0135]
在方法包括步骤的组合的情况下,除非本文另外说明,否则步骤的每个和每一个组合或子组合都涵盖在本公开文本的范围内。
[0136]
如本文所用的章节标题仅用于组织目的,而不应解释为限制所描述的主题。
[0137]
应当理解,本文所述的实施例和实施方案仅用于说明目的,并且根据它们进行的各种修改或变化将为本领域技术人员知晓,并且应包括在本申请的精神和范围内以及所附权利要求书的范围内。
[0138]
vii.实施例
[0139]
实施例1
[0140]
本实施例描述了在后续实施例中使用的材料和方法。
[0141]
材料和方法
[0142]
非膜蛋白通道重构
[0143]
对于非膜蛋白通道,难以直接插入到脂质双层或聚合物膜中,因为与膜蛋白通道不同,非膜蛋白通道通常缺少中间的疏水层和两端的亲水层,因此需要进行广泛工程化。为了用于生物传感或测序,还需要使用不同的探针对非膜蛋白通道进行工程化和功能化。尽管非膜蛋白通道可能源自具有不同序列、形状、结构或特性的各种来源,但用于将其重工程化和使其能够用作纳米孔的策略和方法具有一些共同特征。如图1a和图1b所示,三个不同的结构域对于膜锚定是重要的,并且两个区域对于用于单分子感测的功能模块的缀合是特别重要的。为了将这些不同的结构域重工程化并改变疏水或亲水特性或功能化的缀合位点或探针,涉及一系列分子克隆工作。通常,出于各种工程化目的,采用通用的限制酶克隆方法。然而,也可以采用其他克隆方法,诸如重组克隆、克隆、等温组装反应或iis型组装。
[0144]
非膜蛋白的表达和纯化
[0145]
尽管非膜蛋白通道可能源自具有不同序列、形状、结构或特性的各种来源,但用于表达和纯化它们的策略和方法具有一些共同特征。
[0146]
首先,将重工程化的非膜蛋白通道基因克隆到在末端上具有或没有标签的表达载体中。然后将载体转化到合适的蛋白质表达宿主例如大肠杆菌(e.coli)系统中。在宿主中表达蛋白质通道之后,将宿主裂解,并采取一系列步骤来去除宿主碎片。最后,非膜蛋白可以通过以下方法之一或组合进行纯化,诸如亲和色谱法、交换色谱法、尺寸排阻色谱法或其他常用的纯化方法。
[0147]
例如,将非膜蛋白通道基因和变体基因克隆到在n末端具有his标签的pet23a载体中。在转化到bl21(de3)细胞中之后,将一个bl21(de3)菌落在抗生素存在的情况下接种在5ml新鲜lb培养基中,并在37℃下在振动器中培养若干小时,直至od达到0.8。然后将烧瓶保持在4℃下以冷却。然后将0.5mm iptg添加到烧瓶中以进行诱导。将细菌在振动器中在16℃下培养过夜。将细菌在8000rpm下收获10min,弃去上清液,并且然后用裂解缓冲液悬浮沉淀物。对细菌溶液进行超声处理,直至溶液变得透明且不粘稠。将溶液在超声处理之后在12000rpm下离心30min,弃去上清液并收集沉淀物。将10ml尿素(8m)添加到沉淀中并在振荡器上低速振荡,直至沉淀完全溶解在尿素中。将溶液在12000rpm下离心10min。将上清液添加到100ml蛋白质复性缓冲液中并搅拌过夜。将溶液在重折叠之后在12000rpm下离心30min,弃去沉淀物并收集上清液。将上清液穿过0.45um注射器过滤器以弃去变性的蛋白质。将上清液添加到透析袋中,并且将透析液更换三次。收集透析袋中的液体并在12000rpm下离心10分钟,弃去沉淀物并收集上清液。用裂解缓冲液平衡镍珠,并且将上清液添加到珠中。然后用洗涤缓冲液洗涤珠。使用7~10个柱体积的洗脱缓冲液洗脱蛋白质。收集洗脱液并浓缩至5ml。将洗脱液在12000rpm下离心10min,并且然后吸收上清液并用注射器注射到akta fplc中。在注射之前,用10ml裂解缓冲液洗涤样品环。在通过尺寸排阻柱之后收集蛋白质。在sec之后运行sds-page凝胶以检查蛋白质样品,并储存在-80℃下。
[0148]
缀合
[0149]
为了用不同的探针功能化或增强非膜蛋白通道的疏水性或亲水性,可以采用各种缀合方法。尽管非膜蛋白通道可能源自具有不同序列、形状、结构或特性的各种来源,但用于缀合的策略和方法具有一些共同特征。为了将疏水性部分缀合到非膜蛋白通道,可以在蛋白质通道上的半胱氨酸基团上进行反应。蛋白质通道的每个亚基含有一个或多个半胱氨酸,它们位于通道的中间层并且是环境可及的。在含有0.5m nacl、50mm tris、15%甘油的ph 6.8缓冲液中制备蛋白质溶液。将溶液脱气,并且将100倍过量的tcep添加到溶液中。在室温下孵育20min之后,将4μl的4mm胆固醇-peg-马来酰亚胺逐滴添加到蛋白质溶液中,并且将反应混合物在室温下在黑暗中孵育2小时。通过nanosep 100k旋转柱去除过量的胆固醇-peg-马来酰亚胺。用12%sds-page检查蛋白质的标记。
[0150]
为了将探针缀合到非膜蛋白通道,采用点击化学,诸如四嗪-烯烃连接或叠氮化物-炔烃点击化学。对于四嗪-烯烃连接,在含有0.5m nacl、50mm tris、15%甘油的ph 6.8缓冲液中制备蛋白质溶液。将溶液脱气,并且将100倍过量的tcep添加到溶液中。在孵育20min之后,将1.6μl的10mm甲基四嗪-peg4-马来酰亚胺逐滴添加到蛋白质溶液中,并且将混合物在室温下在黑暗中孵育1小时。通过使用脱盐旋转柱脱盐去除过量的甲基四嗪-peg4-马来酰亚胺。在含有0.5m nacl、50mm tris的ph 6.8缓冲液中制备50μl探针溶液。将溶液脱气,并且将100倍过量的tcep添加到溶液中。在孵育20min之后,将6μl的25mm tco-peg3-马来酰亚胺逐滴添加到寡聚物溶液中,并且将混合物在室温下孵育2小时。通过脱盐
柱去除过量的tco-peg3-马来酰亚胺。通过20%尿素-page凝胶验证探针的标记。
[0151]
对于叠氮化物-炔烃连接,将tco修饰的探针与甲基四嗪标记的蛋白质以不同的摩尔比混合,以实现最佳蛋白质标记效率。将混合物在室温下孵育1小时。用12%sds-page验证缀合。在含有0.5m nacl、50mm tris、15%甘油的ph 6.8缓冲液中制备40μl的20μm蛋白质溶液。将溶液脱气,并且将100倍过量的tcep添加到溶液中。在孵育20min之后,将1.6μl的10mm磺基dbco-peg4-马来酰亚胺逐滴添加到蛋白质溶液中,并且将混合物在室温下在黑暗中孵育1小时。通过使用脱盐旋转柱脱盐去除过量的马来酰亚胺试剂。将dbco修饰的蛋白质与叠氮化物修饰的探针以等摩尔浓度混合,并且将反应混合物在室温下孵育2小时。用12%sds-page凝胶验证缀合。
[0152]
纳米孔实验设置和数据记录
[0153]
尽管非膜蛋白通道可能源自具有不同序列、形状、结构或特性的各种来源,但所有非膜蛋白通道或变体都可以应用于相似的纳米孔设置或装置。通常,设置包括具有一个或多个孔口的传感器芯片或阵列。传感器芯片能够支持脂膜或聚合物膜的形成,从而可以将隔室分为顺式(顶部)和反式(底部)隔室。两个隔室均填充导电缓冲液。输入电极嵌入到一个隔室中,并且接地电极嵌入到另一个隔室中。此外,所述设置还可以与流体系统结合以使样品能够从一个容器流到传感器装置。为了将非膜蛋白通道插入到脂膜或聚合物膜中,将蛋白质通道悬浮在其相应的储存缓冲液中,在导电缓冲液(通常为1m kcl或1m nacl,5mm hepes或tris,ph 7.6)中稀释50-100倍,并添加到顶部隔室中。在施加的电势(恒定保持电压或斜坡电压)下且在具有或没有洗涤剂的情况下,可以观察到蛋白质通道直接插入在平面膜中。当没有分析物存在时,电流稳定且平整。当分析物存在时,与探针的相互作用会导致记录到电流变化。
[0154]
数据分析
[0155]
尽管非膜蛋白通道可能源自具有不同序列、形状、结构或特性的各种来源,但用于数据分析的策略和方法具有一些共同特征。通常,分析约10,000+个电流阻断事件(转位或单分子结合事件),以确保结果在统计学意义内。开发了基于matlab或python的自定义算法,以用于事件的定量快速处理。通常,使用两个参数:(1)当前阻断分数,表示为[(电流
未阻断-电流
分析物阻断之后
)/电流
未阻断
];和(2)停留时间:τ
中断
(事件的持续时间)和τ
连通
(连续事件之间的时间)。根据τ
连通
和τ
中断
,可以获得κ
缔合
(缔合速率常数)和κ
解离
(解离速率常数),并且最后获得k
d
(平衡解离常数)。构建校准曲线,显示捕获率随分析物浓度而变。在将未知浓度的分析物引入到纳米孔中之后,可以计算平均捕获率,并且可以根据校准曲线确定分析物浓度。临床样品的分析需要进一步调谐分析算法,以清楚地区分“污染性”或非特异性信号与真实的分析物诱导的事件。为了使分析物检测系统标准化,通常采用具有“加标”对照的“内源”归一化器。然后,使用诊断领域中常用的标准测定(诸如免疫测定和qrt-pcr)对平台数据进行交叉验证。最后,统计样本大小/检力分析是基于用于两组比较的两样品t检验,以及用于两种因素的组合的双向方差分析(anova)。
[0156]
实施例2
[0157]
phi29 gp-9尾蛋白的表达和纯化
[0158]
sds page中的纯化的phi29 gp-9尾蛋白及其变体在图3至图4中示出。表达和纯化步骤如下。将phi29 gp-9尾蛋白基因和变体基因克隆到在n末端具有his标签的载体pbdht
中。在转化到bl21(de3)中之后,将一个bl21菌落接种在内部具有抗生素的5ml新鲜lb培养基中,并在37℃下在振动器(220rpm)中培养若干小时,直至od达到0.8。然后将烧瓶保持在4℃下以冷却。然后将0.5mm iptg添加到烧瓶中以进行诱导。将细菌在振动器(180rpm)中在16℃下培养过夜。将细菌在8000rpm下收获10min,弃去上清液,并且然后将沉淀物重悬于裂解缓冲液(50mm tris ph 8.0,500mm nacl)中。对细菌溶液进行超声处理,直至溶液变得透明且不粘稠。将溶液在超声处理之后在12000rpm下离心30min,弃去上清液并收集沉淀物。将10ml尿素(8m)添加到沉淀中并在振荡器上低速振荡,直至沉淀完全溶解在尿素中。将溶液在12000rpm下离心10min。将上清液添加到100ml蛋白质复性缓冲液(15%甘油,500mm nacl,50mm tris,2m l-精氨酸,ph 8.0)中并搅拌过夜。将溶液在重折叠之后在12000rpm下离心30min,弃去沉淀物并收集上清液。将上清液穿过0.45um注射器过滤器以弃去变性的蛋白质。将上清液添加到透析袋中,并且将透析液(50mm nacl,5mm tris)更换三次。收集透析袋中的液体并在12000rpm下离心10分钟,弃去沉淀物并收集上清液。用裂解缓冲液平衡镍珠,并且将上清液添加到珠中。用50个柱体积的洗涤缓冲液(50mm tris ph 8.0,500mm nacl,25mm咪唑)洗涤珠。使用7~10个柱体积的洗脱缓冲液(50mm tris ph 8.0,500mm nacl,500mm咪唑)洗脱蛋白质。收集洗脱液并浓缩至5ml。将洗脱液在12000rpm下离心10min,并且然后吸收上清液并用注射器注射到aktafplc中。在注射之前,用10ml裂解缓冲液洗涤样品环。在通过尺寸排阻柱之后收集蛋白质。在sec之后运行sds-page凝胶以检查蛋白质样品,并储存在-80℃下。
[0159]
实施例3
[0160]
作为纳米孔的噬菌体尾蛋白
[0161]
许多噬菌体含有长的可收缩或不可收缩的尾部或者短的不可收缩尾部。尾部在宿主细胞识别、膜穿透和病毒基因组弹射过程中发挥关键作用。尾蛋白来源于(包括但不限于)phi29、t4、t3、t5、t7、spp1、p22、p2、p3、λ、μ、hk97和c1。
[0162]
本发明的这些蛋白质通道对于生物分子(诸如疾病相关生物标记物、多核苷酸和多肽序列)的生物感测和测序是理想的。具有改进的膜能力,修饰的蛋白质通道可以有效地插入到脂膜或聚合物膜中,并且充当用于生物感测和测序的纳米孔。通过与各种探针缀合,修饰的蛋白质通道具有以高灵敏度和特异性检测特定疾病相关的生物标记物的能力。本发明的孔可以存在于同源或异源孔中。
[0163]
代表性实施例:来自phi29的gp-9尾蛋白
[0164]
phi29噬菌体尾部(gp9)的晶体结构显示,六个gp9亚基形成了六聚体或圆柱状的管结构。在结构内部,在触发dna弹射之前,远端被六个柔性疏水环封阻。为了将基因组dsdna递送到宿主细胞的细胞质中,phi29尾部需要穿透细胞膜。管的长度为约12.5nm。管具有大约4nm的内径和大约9nm的外径。管壁主要由厚度为约2.5nm的β-折叠片构成。
[0165]
构建了全长gp9的克隆和一系列突变体(图2至图6),诸如gp9δloop[417-491],其中无序区(残基417-491)缺失。根据晶体结构,gp9δ417-491结构也是圆柱形管状均六聚体。通过研究尾蛋白的结构,氨基酸130-170、300-325、350-390、530-595位于中间通道的表面上,它们可以与膜的疏水层相互作用。因此,疏水性基团连接到这些位点或这些氨基酸突变为疏水性氨基酸可以改变通道的膜插入能力,所述水性氨基酸包括甘氨酸(gly)、丙氨酸(ala)、缬氨酸(val)、亮氨酸(leu)、异亮氨酸(ile)、脯氨酸(pro)、苯丙氨酸(phe)、甲硫氨
酸(met)和色氨酸(trp)。具体地,以下位点之一或任何组合的突变是关键的:k134i、d138l、d139l、d158l、e163v、e309v、d311v、k321v、k356a、k358a、d377a、d381v、n388l、r524i、r539a、e595v。为了将疏水性基团缀合到通道的中部,将以下位点突变为半胱氨酸是重要的:e595c、k321c和k358c。此外,氨基酸250-300和20-50位于通道的上部和下部的表面上,它们可以与亲水性环境相互作用。
[0166]
作为纳米孔的病毒门户蛋白
[0167]
门户蛋白不仅存在于噬菌体phi29、t3、t4、t5、t7、spp1和p22中,而且还存在于其他病毒系统中,诸如腺病毒和疱疹病毒。被称为连接体的门户通道是具有中央通道的孔状蛋白质结构,所述中央通道充当基因组dna在包装期间进入病毒衣壳和在感染期间离开的途径。尽管结构研究指示不同病毒连接体蛋白之间的序列同源性和大小存在显著差异,但它们在拓扑上都相似,具有截锥形状。来源于过表达的蛋白质的连接体的化学计量通常根据表达条件而变化。如果本发明的这些蛋白质通道可以直接插入到坚固的聚合物膜中,则所述蛋白质通道对于生物感测和测序应用而言可能是理想的。由于来自不同病毒门户蛋白的连接体的结构显示出相似的特征,因此上文概述的原理通过扩展也适用于它们全部。
[0168]
代表性实施例:p22门户通道
[0169]
p22是一种有尾噬菌体,其组装空的前体衣壳,随后通过强大的包装马达将所述前体衣壳与病毒dna包装在一起。p22门户蛋白形成用于病毒dna双向通过的通道状结构。短尾dsdna噬菌体的短尾病毒科(podoviridae)包括p22样亚组的成员,诸如sf6、cus-3、ε34和apse-1。门户桶结构是高度动态的,并且在溶液中易发生蛋白水解。p22门户蛋白由12个相同的亚基构成,所述亚基在中央通道周围对称排列。总高度为约30nm,具有约17nm直径的漏斗形的核心,所述核心连接到约20nm长的α螺旋管。在整个结构中,通道的平均内径在3.5nm至7.5nm之间变化。
[0170]
构建了一系列突变体(图7至图11),其包括以下限定特征:(1)门户核心(残基1-602)在拓扑上与其他病毒蛋白通道相似,但螺旋桶结构管的存在是p22独有的。门户核心与螺旋桶结构之间的连接可以易于通过溶液中的胰凝乳蛋白酶裂解,这指示两个结构域在本质上是柔性的。本发明包括去除桶结构残基603-725,并且用任何肽或核酸序列作为单独的识别结构域进行替换。(2)本发明包括内部柔性环残基464-492的改变(缺失、截短、突变),以改变电生理特性和/或检测能力。(3)本发明包括使用edta(60mm或更高)组装十二聚体复合物:对于十二聚体环的正确组装,非特异性地捕获在单体-单体界面处的螯合二价阳离子是必需的。(4)本发明包括通过改变残基glu70(其与glu423、glu414、glu406、glu393和glu396簇集在一起)的五个环来改变通道内部的整体电负性。(5)本发明包括改变在翼结构域下面形成带的任何疏水性氨基酸(phe 24、ile25、leu28、phe60、phe128、pro129和pro132),以改变表面的疏水性;(6)本发明包括在末端添加若干氨基酸(任何天然或非天然氨基酸),目的是使用这些氨基酸作为锚定点(诸如半胱氨酸或赖氨酸或精氨酸)用于增加功能性或针对膜插入和通道稳定性改变电生理特性(亲水或疏水标签);(7)本发明包括对疏水层和亲水层的诱变;中部:氨基酸250至300,10-45;上部:450-500;下部:350-380;arg 476或c末端至cys的突变用于缀合;中部thr240、val244、arg 273,用于cys诱变以缀合胆固醇。
[0171]
代表性实施例:t4门户通道
[0172]
t4门户主要作为12聚体(根据蛋白质表达条件,一些为11聚体或13聚体)环存在,长14nm,宽7nm,并且内部通道直径3nm。由于通道由12个亚基组装而成,因此改变一个单体中的一个或多个残基将触发整个通道中的效应,所述突变存在于分子的同一平面中。本发明包括(图12至图14和图16):(1)通过改变带电残基的环来改变通道内部的整体电负性;(2)改变内部通道入口处的两个碱性残基r338和k342(使用任何氨基酸来改变亲水性);(3)在末端添加若干氨基酸(任何天然或非天然氨基酸),目的是使用这些氨基酸作为锚定点(诸如半胱氨酸或赖氨酸或精氨酸)用于增加功能性或针对膜插入和通道稳定性改变电生理特性(亲水或疏水标签);以及(5)改变(缺失、截短、突变)内部柔性环残基374-398,以改变电生理特性和/或检测能力。
[0173]
实施例4
[0174]
纳米孔外壳的膜的组合物
[0175]
平面双层脂膜(blm)或聚合物膜是在(a)bch-1a水平blm池(eastern scientific)或(b)自制定制腔室中产生的。将具有100或200μm孔口的特氟隆(teflon)隔板放置在设备中,以将blm池分为顺式(顶部)和反式(底部)隔室。自制腔室已预先钻出100或200um的孔口,从而分隔顺式隔室与反式隔室。
[0176]
脂膜:通过以下方式形成具有变化组成的平面脂质双层:用己烷中的脂质(浓度:0.5mg/ml)预涂覆孔口,接着用正癸烷中的脂质(浓度:20-30mg/ml)涂覆。脂质组合物的例子包括:(i)两性离子脂质,诸如100%dphpc或dopc或popc;(ii)0%-50%的阴离子脂质,诸如dphpg/dopg/popg或dphps/dops/pops,所述阴离子脂质与组合物(i)按比例混合(最终比例总计达100%);(iii)0%-25%的胆固醇,所述胆固醇与组合物(i)和(ii)按比例混合。确切的脂质组合物取决于蛋白质的特性。使用的典型脂膜组合物包括:100%dphpc;100%dphpc;30%dphps;70%dphpc:28%dphpg:2%胆固醇。
[0177]
聚合物膜:通过使用悬浮在有机溶剂中的膜进行手工涂覆来形成具有变化组成的平面聚合物膜,所述有机溶剂诸如癸烷或硅油(基于聚苯基-甲基硅氧烷,或基于聚二甲基硅氧烷,粘度为20mpa.s)。膜组合物是基于聚噁唑啉的三嵌段共聚物(图17),诸如:
[0178]
(i)peoxa-peo-peoxa[聚(2-乙基噁唑啉)-b-聚(环氧乙烷)-b-聚(2-乙基噁唑啉)]peoxa-peo-peoxa;
[0179]
(ii)pmoxa-pdms-pmoxa[聚(2-甲基噁唑啉)-b-聚(二甲基硅氧烷)-b-聚(2-甲基噁唑啉)];(嵌段之间具有乙基-苄基或丙基或丙基-乙氧基连接)
[0180]
(iii)pmoxa-pb-pmoxa[聚(2-甲基噁唑啉)-b-聚(1,4-丁二烯)-b-聚(2-甲基噁唑啉)];
[0181]
(iv)pmoxa-pe-pmoxa[聚(2-甲基噁唑啉)-b-聚(乙烯)-b-聚(2-甲基噁唑啉)];
[0182]
(v)pmoxa-peo-pmoxa[聚(2-甲基噁唑啉)-b-聚(环氧乙烷)-b-聚(2-甲基噁唑啉)]
[0183]
使用的典型膜包括pmoxa6-pdms35-pmoxa6;pmoxa6-pdms65-pmoxa6;pmoxa11-pdms65-pmoxa11;pmoxa5-pdms13-pmoxa5;pmoxa3-pdms38-pmoxa3(图17)。嵌段长度(由pmoxax-pdmsy-pmoxax中的下标x和y表示)(其决定亲水或疏水嵌段的长度)可根据以下因素调谐:(1)为了稳定插入蛋白质孔,需要一定的膜厚度;(2)膜需要保持非常低的渗透性;(3)膜必须在不同的溶液条件下(包括极端ph(1-12)和高/低盐环境下)在延长时间段内在
机械和化学上是稳定的。
[0184]
实施例5
[0185]
蛋白质通道在膜中的插入
[0186]
通常,将悬浮在其相应的储存缓冲液中的蛋白质通道(尾蛋白或门户通道)在导电缓冲液(通常为1m kcl或1m nacl,5mm hepes或tris,ph 7.6)中稀释50-100倍,并添加到blm池的顶部隔室中。在施加的电势(恒定保持电压或斜坡电压)下,可以观察到蛋白质通道直接插入在平面膜中(图6、图11、图14、图16和图19)。
[0187]
如果需要,所述的膜组合物还可以用于产生具有变化的多分散性的泡状聚合物囊泡结构,以重构蛋白质通道。对于高插入效率,可以将变化量的甘油、cscl和/或蔗糖包封在聚合物囊泡内。然后,所得的蛋白质-聚合物囊泡可以以盐和电压依赖性方式与相同组成的平面双层融合。
[0188]
实施例6
[0189]
将疏水性部分经由与半胱氨酸残基反应缀合到非膜蛋白通道
[0190]
在此使用t4 gp20门户蛋白为例来说明如何将疏水性部分经由与半胱氨酸残基反应缀合到非膜通道。蛋白质通道的每个亚基含有三个半胱氨酸,它们位于通道的中间层并且是环境可及的(图13)。在含有0.5m nacl、50mm tris、15%甘油的ph 6.8缓冲液中制备40μl的20μm蛋白质溶液。将溶液脱气,并且将100倍过量的tcep添加到溶液中。在室温下孵育20min之后,将4μl的4mm胆固醇-peg-马来酰亚胺逐滴添加到蛋白质溶液中,并且将反应混合物在室温下在黑暗中孵育2小时。通过nanosep 100k旋转柱去除过量的胆固醇-peg-马来酰亚胺。用12%sds-page检查蛋白质的标记(图13)。
[0191]
实施例7
[0192]
将携带疏水性部分的非膜蛋白通道插入到脂膜或聚合物膜中
[0193]
产生了平面聚合物膜。在施加的电压(恒定保持电压或斜坡电压)下,在向顺式腔室添加蛋白质通道之后,观察到携带疏水性部分的非膜蛋白通道的直接插入(图14)。突变为疏水性氨基酸或将疏水性基团缀合到中间层phi29 gp-9尾蛋白可以显著增强插入过程及其稳定性。
[0194]
实施例8
[0195]
将探针经由点击反应缀合到非膜蛋白通道
[0196]
使用phi29 gp10门户蛋白作为代表性例子。
[0197]
策略1:经由四嗪-烯烃连接:在含有0.5m nacl、50mm tris、15%甘油的ph 6.8缓冲液中制备40μl的20μm蛋白质溶液。将溶液脱气,并且将100倍过量的tcep添加到溶液中。在孵育20min之后,将1.6μl的10mm甲基四嗪-peg4-马来酰亚胺逐滴添加到蛋白质溶液中,并且将混合物在室温下在黑暗中孵育1小时。通过使用脱盐旋转柱脱盐去除过量的甲基四嗪-peg4-马来酰亚胺。在含有0.5m nacl、50mm tris的ph 6.8缓冲液中制备50μl的30μm硫醇修饰的mirna探针溶液。将溶液脱气,并且将100倍过量的tcep添加到溶液中。在孵育20min之后,将6μl的25mm tco-peg3-马来酰亚胺逐滴添加到寡聚物溶液中,并且将混合物在室温下孵育2小时。通过脱盐柱去除过量的tco-peg3-马来酰亚胺。通过20%尿素-page凝胶验证mirna探针的标记。为了将mirna探针缀合到蛋白质,将tco修饰的mirna探针与甲基四嗪标记的蛋白质以不同的摩尔比混合,以实现最佳蛋白质标记效率。将混合物在室温下
孵育1小时。用12%sds-page验证缀合。
[0198]
策略2:经由叠氮化物-炔烃点击化学:在含有0.5m nacl、50mm tris、15%甘油的ph 6.8缓冲液中制备40μl的20μm蛋白质溶液。将溶液脱气,并且将100倍过量的tcep添加到溶液中。在孵育20min之后,将1.6μl的10mm磺基dbco-peg4-马来酰亚胺逐滴添加到蛋白质溶液中,并且将混合物在室温下在黑暗中孵育1小时。通过使用脱盐旋转柱脱盐去除过量的马来酰亚胺试剂。将dbco修饰的蛋白质与叠氮化物修饰的mirna探针以等摩尔浓度混合,并且将反应混合物在室温下孵育2小时。用12%sds-page验证缀合。
[0199]
实施例9
[0200]
缀合到蛋白质的dna探针的验证
[0201]
将蛋白质-mirna探针缀合物与靶mirna寡聚物在室温下以等摩尔浓度一起孵育30min。用12%sds-page验证蛋白质-mirna探针与靶mirna的结合(图15)。
[0202]
实施例10
[0203]
使用工程化的非膜蛋白通道进行的psa检测
[0204]
为了将蛋白质探针缀合到纳米孔通道,已经尝试并测试了各种方法,包括半胱氨酸残基与甲基四嗪-peg4-马来酰亚胺的反应以及随后与tco标记的探针的反应,以及spycatcher/spytag蛋白质缀合系统。显示了针对psa的单链抗体如何经由spycatcher/spytag缀合到phi29 gp10门户蛋白通道。构建并纯化具有c末端spytag肽的phi29 gp10蛋白通道。构建并纯化具有c末端spycatcher的针对psa的单链抗体。通过凝胶验证组装的蛋白质通道-psa单链抗体(图18)。然后将纯化的组装蛋白质通道-psa单链抗体插入到聚合物膜中,以测试其结合psa抗原的能力。先前描述了设置电生理实验的程序。在插入之后,将一系列不同浓度的psa抗原添加到腔室中,并观察到独特的结合事件(图19)。
[0205]
实施例11
[0206]
使用工程化的非膜蛋白通道进行的微小rna检测
[0207]
为了将核酸探针缀合到纳米孔通道,已经尝试并测试了各种不同的方法,如实施例6所概述。已经证明了mir-21探针可以与缀合到t4 gp20门户蛋白通道。将纯化的缀合复合物插入到聚合物膜中,以测试其结合对应的微小rna的能力。先前描述了设置电生理实验的程序。在插入之后,将一系列不同浓度的微小rna添加到腔室中,并观察到独特的结合事件(图16)。
[0208]
通过以下详细描述,本发明的其他目的、特征和优点将变得清楚。然而,应当理解,详细说明和实施例虽然指示了本发明的具体实施方案,但仅以说明的方式给出。另外,设想根据此详细描述,在本发明的精神和范围内的改变和修改对于本领域技术人员将变得清楚。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1