一种金属掺杂氮化碳材料及其制备方法和应用与流程
1.本技术属于半导体光催化技术领域,具体涉及一种金属掺杂氮化碳材料及其制备方法和应用。
背景技术:
2.在21世纪,全球能源需求大幅增长,工业大规模繁荣了几十年,导致了不可再生化石能源的减少甚至枯竭,人类的活动已经对可持续发展造成了严重的破坏,可持续已经成为一个影响学术和工业领域的热点问题。其中,太阳能被广泛认为是化石能源的理想替代品。利用太阳光将在苛刻的条件下发生的化学反应转化为在温和条件下进行的反应,它作为一门新兴的学科在很多领域发挥了很重要的作用,比如能源、环境、健康、生物质转化等。
3.通过半导体光催化将太阳能转化为清洁和无碳的氢(h2),半导体光催化在纯水中析氢时,利用光激发电子还原质子,生成氢气气体;而光激发空穴将水氧化而产生氧气(o2)。由于光激发电子-空穴对易重组、水氧化动力不足、水氧化过电位高,使得光催化在纯水中析氢的性能受到很大限制,导致了较低的太阳光-h2转化率。为了提高半导体光催化剂的效率和抑制光腐蚀,各种空穴清除剂充当了牺牲电子供体,但这种方法实际上是在增加成本。此外,生成的h2能量有时并不能抵消清除空穴所需的能量。因此,利用丰富的、廉价的原料作为清除剂析氢,同时也能产生其他有附加值的化学品是十分有必要的。
4.科研人员发现了成本低廉且光学性质较稳定的氮化碳,其还具有良好的热稳定性和化学稳定性,以及具有特殊的力学性能、化学性能、电学性能。它的共轭大π键结构是提高电子空穴分离效率的理想体系,利用太阳光可在催化剂石墨相氮化碳作用下产氢。因此,过去十年间氮化碳(c3n4)得到了科学家的广泛关注。但是由于石墨相氮化碳(g-c3n4)的光利用率仍旧比较低,而在半导体作为催化剂析氢中,主要考虑的是与其有关的合适的带隙和吸收范围,激发电子的生命周期,以及延迟重组的电荷迁移。g-c3n4的光催化性能在现实实践中不够理想,材料上的众多缺点制约了其在光催化制氢的应用。
技术实现要素:
5.有鉴于此,本技术提供一种金属掺杂氮化碳材料及其制备方法和应用,本发明提供的金属掺杂氮化碳材料具有优异的光催化性能,可提升光催化产氢的效率。
6.本发明提供一种金属掺杂氮化碳材料,所述金属掺杂氮化碳材料为掺杂有金属元素的石墨相氮化碳,所述金属元素为锂、钠、钾、镁或铝。
7.本发明提供如前所述的金属掺杂氮化碳材料的制备方法,包括以下步骤:
8.s1、将金属盐溶于尿素溶液,加热反应,得到前驱体;所述金属盐中金属元素为锂、钠、钾、镁或铝;
9.s2、将所述前驱体进行蒸发结晶,得到前驱体晶体;
10.s3、将所述前驱体晶体高温煅烧,得到金属掺杂氮化碳材料。
11.在本发明的实施例中,步骤s1中,所述加热反应的温度为70-85℃。
12.在本发明的实施例中,步骤s2中,所述蒸发结晶通过电热鼓风干燥机保持70-80℃,直至蒸发得到前驱体晶体。
13.在本发明的实施例中,步骤s3中,所述高温煅烧的温度为500-600℃,升温速率为12-18℃/min。
14.本发明提供如前所述的金属掺杂氮化碳材料在光催化产氢中的应用。
15.为了提高g-c3n4的光吸收和电荷分离效率等,人们开展了纳米结构工程、共聚、晶体结构工程和异质结构构建等方面的研究。
16.其中,材料上的缺陷可以根据其尺寸分为不同的类别,表现为点缺陷(空位、间隙缺陷、置换缺陷等)、线缺陷(位错)和体缺陷(杂质、空隙等)。虽然带有缺陷的材料普遍被认为是有害的纳米材料,但研究发现智能控制缺陷可以获得良好的光催化性能。
17.本发明主要在氮化碳中掺杂锂、钠、钾、镁或铝这些特定金属对其进行改性,所述的金属离子掺杂石墨相氮化碳(g-c3n4),不仅在晶格中引入了缺陷或改变了结晶度,而且可吸附导带的电子,同时还抑制光生电子和空穴的复合,从而提高材料光催化的效率。通过光催化产氢实验结果,表明本发明所述的掺杂金属于石墨相氮化碳中可以改善光催化活性,利于应用。
18.此外,本发明所述材料的制备方法简便,易于推广。
附图说明
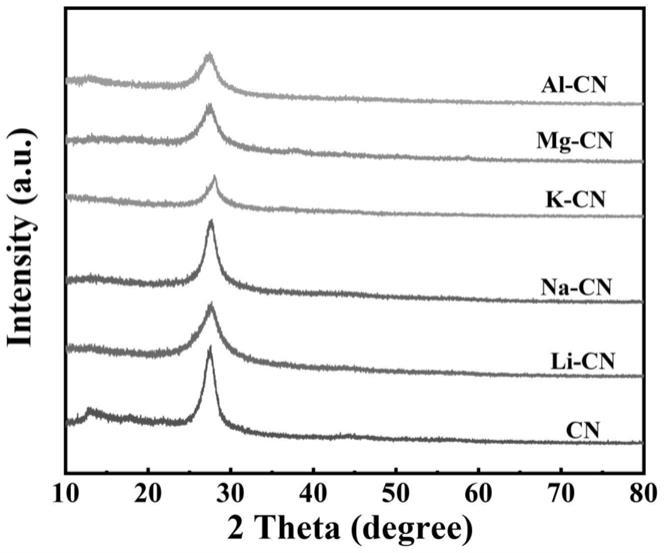
19.图1为本发明实施例1-5所述金属掺杂氮化碳材料的x射线衍射表征图;
20.图2为本发明实施例1-5所述金属掺杂氮化碳材料的光催化产氢量结果图;
21.图3为本发明实施例1-5所述金属掺杂氮化碳材料的光催化产氢率结果图。
具体实施方式
22.下面对本技术实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本技术一部分实施例,而不是全部的实施例。基于本技术中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本技术保护的范围。
23.本技术提供了一种金属掺杂氮化碳材料,所述金属掺杂氮化碳材料为掺杂有金属元素的石墨相氮化碳,所述金属元素为锂、钠、钾、镁或铝。
24.本发明提供的金属掺杂氮化碳材料具有优异的光催化性能,可提升光催化产氢的效率。
25.g-c3n4存在比表面积小、长波长处光吸收差、电荷迁移率低、光生电子-空穴对复合速率高等不足,为了克服所述问题,本发明实施例在g-c3n4中掺杂锂(li)、钠(na)、钾(k)、镁(mg)或铝(al)元素,得到所述的掺杂金属元素的g-c3n4。
26.在本发明的实施例中,所述的金属掺杂氮化碳材料可简称为al-cn、mg-cn、k-cn、na-cn、li-cn(锂元素掺杂的氮化碳),可通过x射线衍射获得物性相关内容。此外,还可利用扫描电子显微镜对掺杂金属(锂、钠、钾、镁、铝)的石墨相氮化碳的三维形貌分析和进行微区的成分分析;利用红外光谱确定其化学基团,紫外-可见光谱计算其掺杂后的禁带宽度。
27.本发明所述的金属离子掺杂石墨相氮化碳不仅在晶格中引入了缺陷或改变了结
晶度,而且可吸附导带的电子,同时还抑制光生电子和空穴的复合,从而提高材料光催化的效率。
28.本发明实施例提供了如前所述的金属掺杂氮化碳材料的制备方法,包括以下步骤:
29.s1、将金属盐溶于尿素溶液,加热反应,得到前驱体;所述金属盐中金属元素为锂、钠、钾、镁或铝;
30.s2、将所述前驱体进行蒸发结晶,得到前驱体晶体;
31.s3、将所述前驱体晶体高温煅烧,得到金属掺杂氮化碳材料。
32.本发明实施例以尿素(nh2conh2)作为制备的基础原料,可将准确称量好的尿素倒入装有去离子水的烧杯,然后放置在磁力搅拌器上搅拌使尿素完全溶解于去离子水,得到尿素(水)溶液。
33.本发明实施例溶解后加入准备好的金属盐,接着可使用集热式恒温加热磁力器加热,优选于70-85℃并保持搅拌进行反应,得到前驱体。在本发明中,所述金属盐中金属元素为锂、钠、钾、镁或铝,优选为钾元素;具体原料可为硝酸锂、碘化钠、溴化钾、硝酸镁、氯化铝等可溶性盐,采用分析纯市售产品即可。所述的加热反应温度进一步为80℃,搅拌时间优选为12-15小时,例如12小时、13小时。
34.得到前驱体后,本发明实施例将其装入蒸发皿中,优选放入电热鼓风干燥机中保持70-80℃,直至蒸发得到前驱体晶体再停止干燥。
35.等待干燥箱降温至室温,本发明实施例将蒸发所得结晶转移至坩埚中,然后在马弗炉中高温煅烧,得到相应金属掺杂的氮化碳。其中,所述高温煅烧的温度优选为500-600℃,更优选为550℃,升温速率优选为12-18℃/min,更优选为15℃/min。
36.烧结之后,本发明实施例可用去离子水溶解掺杂金属的氮化碳,接着离心、干燥,得到最终的金属元素掺杂的氮化碳。
37.此外,本发明提供了如前所述的金属掺杂氮化碳材料在光催化产氢中的应用。
38.最后,本发明实施例使用光催化产氢系统,对掺杂锂、钠、钾、镁或铝金属元素的石墨相氮化碳的光催化产氢性能进行测试。结果表明,本发明所述的掺杂金属于石墨相氮化碳中可以改善光催化活性,具有较高的光催化效率,利于其应用在光催化产氢等方面。此外,本发明所述材料的制备方法简便,易于推广。
39.为了更好理解本发明技术内容,下面提供具体实施例,对本发明做进一步的说明。本发明实施例采用市售原料。
40.实施例1
41.首先,用电子天平称量36g的尿素和1.08g的溴化钾(分析纯),并用量筒量取150ml的去离子水倒入烧杯,将称量好的尿素倒入装有去离子水的烧杯,然后放置在磁力搅拌器上搅拌。尿素溶解后加入准备好的1.08g的溴化钾,接着使用集热式恒温加热磁力器加热至80℃,并保持搅拌12小时得到8g前驱体。紧接着将其分装入3个蒸发皿中,放入电热鼓风干燥机中保持70℃,直至蒸发皿中出现前驱体结晶再停止干燥。等待干燥箱降温至室温,将蒸发所得结晶转移至坩埚中,然后在马弗炉中以550℃,15℃/min的升温速率,烧结4h,得到钾元素掺杂的氮化碳。
42.之后,用量筒称量150ml去离子水并将所述掺杂钾的氮化碳溶解于与此,放在磁力
搅拌器上搅拌60min完全溶解,接着分装入4个离心瓶中,使用高速离心机以8000rad离心3min,取出离心瓶并用去离子水冲洗离心瓶,再将其放入高速离心机以相同的条件离心4次,完成离心后将液体分装至蒸发皿,将该蒸发皿放入电热鼓风干燥机保持70℃干燥钾元素掺杂的氮化碳,等待干燥完成,得到2g最终的钾元素掺杂的氮化碳材料。
43.实施例2-5
44.使用电子天平,分别称量1.08g的硝酸锂、硝酸镁、碘化钠、氯化铝(均为分析纯),重复实施例1上述操作,分别得到锂、镁、钠、铝元素掺杂的氮化碳材料。
45.利用x射线衍射对得到的掺杂金属元素的石墨相氮化碳进行物性分析,结果如图1所示。图1中,cn代表未掺杂的石墨相氮化碳g-c3n4,其通过以尿素为基底在高温下制得。本发明实施例中掺杂锂、钠、钾、镁、铝元素,在石墨相氮化碳晶格中引入了缺陷或改变了结晶度,利于获得良好的光催化性能。
46.使用电子天平称量60mg的原始无掺杂氮化碳(g-c3n4),并使用量筒量取60ml的去离子水和1ml氯铂酸及10ml乳酸,然后将g-c3n4溶解于装有150ml去离子水的烧杯中,最后分别加入氯铂酸和乳酸。完全混合过后使用cel-sph2n系列光催化活性评价系统,每隔半小时转动进气阀门和出气阀门,并记录下氢气的峰面积、保留时间等。
47.对上述掺杂锂、钠、钾、镁、铝金属元素的石墨相氮化碳的光催化产氢性能进行测试;结果如图2、图3所示。
48.图2显示的产氢量结果中,未掺杂的石墨相氮化碳随着时间进展,150min内几乎没有产氢;而本发明掺杂金属元素后产氢量明显增加,其中以k-cn增量最多,150min处h2量在2500μmol以上,接着往下依次是al-cn、mg-cn、li-cn、na-cn。图3是相应的产氢率结果,其中,k-cn的产氢率最高。由此得出,本发明掺杂金属的石墨相氮化碳材料具有提升的光催化活性。
49.以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。
50.以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1