定量联合检测PA与CRP的方法、试剂盒及其制备方法和应用与流程
本发明属于医学检验技术领域,具体涉及一种定量联合检测PA与CRP的方法、试剂盒及其制备方法和应用。
背景技术:
住院和门诊病人的营养诊断率低是我国医疗服务中存在的一个普遍现象。据统计,我国每年近亿人次的住院病人中,营养诊断率不足1%。按公认的住院病人营养不良率40%计算,则每年有4千万患有营养不良的住院病人得不到合理有效的营养支持,影响了其临床结局。
营养不良与脏器功能损伤是一个渐进的过程,不同阶段的代谢特点不同,因此,营养与代谢状况评价和脏器功能评价必须采用多指标组合分析。例如,蛋白质/能量评价组合一般由前白蛋白(Prealbumin,PA)、转铁蛋白、视黄醇结合蛋白和C反应蛋白(C-reactive protein,CRP)组成,分别反映蛋白质的丢失及其程度、营养治疗后蛋白质合成速率以及蛋白质浓度下降是否为应激反应所致。然而,目前市场上使用的营养诊断体外诊断产品评价指标单一,临床接受程度很低。鉴于此,为了准确了解临床病人的营养状况,更好地使病人得到治疗,排除因营养支持方面的缺陷导致的临床新问题,有必要研究开发操作简便、临床接受程度高、检测效果好的营养诊断产品。
技术实现要素:
本发明的目的是为了准确了解临床病人的营养状况,更好地使病人得到治疗,排除因营养支持方面的缺陷导致的临床新问题,而提供一种操作简便、临床接受程度高、检测效果好的定量联合检测PA与CRP的方法、试剂盒及其制备方法和应用。
本发明提供的技术方案之一是:一种定量联合检测PA与CRP的试剂盒,其包括试纸条I和试纸条II,所述试纸条I用于定量检测PA,由底板I、样品垫I、结合垫I、硝酸纤维素膜I和吸水纸I构成,所述样品垫I、结合垫I、硝酸纤维素膜I和吸水纸I依次搭接地粘贴在底板I上且分别部分重合,在硝酸纤维素膜I上分布有检测线I和质控线I,所述检测线I靠近结合垫I端,所述质控线I靠近吸水纸I端,所述结合垫I上喷涂有荧光微球标记的抗PA抗体I,所述检测线I上包被有抗PA抗体II,所述质控线I上包被有驴抗鼠抗体;所述试纸条II用于检测CRP,由底板II、样品垫II、结合垫II、硝酸纤维素膜II和吸水纸II构成,所述样品垫II、结合垫II、硝酸纤维素膜II和吸水纸II依次搭接粘贴在底板II上且分别部分重合,在硝酸纤维素膜II上分布有检测线II和质控线II,所述检测线II靠近结合垫II端,所述质控线II靠近吸水纸II端,所述结合垫II上喷涂有荧光微球标记的抗CRP抗体I,所述检测线II上包被有抗CRP抗体II,所述质控线II上包被有驴抗鼠抗体;其中,所述抗PA抗体I和所述抗PA抗体II具有不同的抗原结合位点,所述抗CRP抗体I和所述抗CRP抗体II具有不同的抗原结合位点。
本发明中,所述PA指前白蛋白(Prealbumin,PA),所述CRP指C反应蛋白(C-reactive protein,CRP)。
本发明中,所述的荧光微球较佳地是直径为0.1~10μm的用聚合材料或二氧化硅包裹荧光物质制得的微球,其表面连接有活性基团或与链霉亲和素偶联;所述荧光物质为有机或无机的荧光物质或多种荧光物质的掺杂物以及量子点。
所述底板I和底板II的材料较佳地为PVC塑料胶板。
所述样品垫I和样品垫II的材料较佳地为玻璃纤维膜或聚酯纤维膜。
所述结合垫I和结合垫II的材料较佳地为玻璃纤维膜或聚酯纤维 膜。
所述试纸条I和所述试纸条II较佳地以平行方式排布于同一卡座上,以方便操作和读取数据。
本发明提供的技术方案之二是:前述定量联合检测PA与CRP的试剂盒的制备方法,其包括如下步骤:
(1)硝酸纤维素膜的制备:将抗PA抗体II和驴抗鼠抗体包被到硝酸纤维素膜I上,分别作为检测线I和质控线I,包被的量均为0.5~1.25μL/cm,干燥后备用;将抗CRP抗体II和驴抗鼠抗体包被到硝酸纤维素膜II上,分别作为检测线II和质控线II,包被的量均为0.5~1.25μL/cm,干燥后备用;
(2)结合垫的制备:以EDC为偶联剂,将荧光微球分别标记在抗PA抗体I和抗CRP抗体I上,将标记有荧光微球的抗PA抗体I喷涂至结合垫I上,将标记有荧光微球的抗CRP抗体I喷涂至结合垫II上,干燥后备用;
(3)试纸条的组装:将样品垫I、结合垫I、包被有抗PA抗体II作为检测线I与驴抗鼠抗体作为质控线I的硝酸纤维素膜I和吸水纸I依次搭接地粘贴在粘性底板I上且分别部分重合,得试纸条I;将样品垫II、结合垫II、包被有抗CRP抗体II作为检测线II与驴抗鼠抗体作为质控线II的硝酸纤维素膜II和吸水纸II依次搭接地粘贴在粘性底板II上且分别部分重合,得试纸条II。
本发明中,步骤(1)为硝酸纤维素膜的制备。
其中,优选地,所述的抗PA抗体II、所述的抗CRP抗体II和驴抗鼠抗体在包被前用抗体保护剂调节浓度。所述的抗体保护剂为本领域常规所述,如在PB缓冲溶液中加入适量的蔗糖、叠氮钠或BSA等均可以作为适用于本发明的抗体保护剂。所述的抗体保护剂的pH值优选7.2~7.4。所述调节浓度优选将所述的抗PA抗体II和所述的抗CRP抗体II的浓度调节至0.3~1.5mg/mL(最优选0.5mg/mL),将驴抗鼠抗体的 浓度调节至0.5~2.0mg/mL(最优选1.0mg/mL)。
所述检测线I和所述质控线I间的距离以及所述检测线II和所述质控线II间的距离均为本领域常规,一般检测试纸条的检测线和质控线之间的距离均适用于本发明,本发明优选所述检测线I和所述质控线I间的距离以及所述检测线II和所述质控线II间的距离均为4~8mm。
所述包被的量优选均为1.0μL/cm。
所述干燥优选环境的湿度低于40%。
本发明中,步骤(2)为结合垫I和结合垫II的制备。较佳地,步骤(2)为将荧光微球加入MES缓冲溶液,再加入EDC溶液混匀,然后加入用MES缓冲溶液稀释的抗PA抗体I或抗CRP抗体I,混匀后室温搅拌反应1~3h,加入BSA封闭1~2h,离心弃上清,沉淀用MES缓冲溶液复溶至起始体积,将制备好的荧光微球标记的抗PA抗体I和抗CRP抗体I分别喷涂至结合垫I和结合垫II上,干燥后备用即可。
其中,所述结合垫I或结合垫II优选经过缓冲液、表面活性剂、稳定剂、非离子表面活性剂和防腐剂中的一种或多种处理后再使用;所述缓冲液更优选磷酸盐缓冲液;所述表面活性剂更优选聚乙烯吡咯烷酮或TWEEN-20;所述稳定剂更优选蔗糖或牛血清白蛋白;所述非离子表面活性剂更优选聚乙二醇对异辛基苯基醚;所述防腐剂更优选叠氮化钠。
所述MES缓冲溶液为本领域常规所述,MES是4-Morpholine Ethane Sulfonic Acid的简称,即2(N-吗啉)乙磺酸,所述EMS缓冲溶液的pH值优选为5.0~7.0,更优选为5.5。
所述EDC溶液为本领域常规所述,EDC是1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐的英文字母简称,所述EDC溶液的浓度没有特殊要求,常规的浓度均适用。
步骤(2)中还可以EDC/NHS(Hydroxy-2,5-dioxopyrrolidine-3-s ulfonicacid sodium salt,N-羟基硫代琥珀酰亚胺)作为偶联剂;即, 在荧光微球中加入EDC和NHS混匀,活化羧基官能团,离心后再加入抗PA抗体I或抗CRP抗体I进行偶联。以此方法偶联能够使不同批次生产的试纸条产品的质量更稳定,数据指标均一性更优良。
所述抗PA抗体I或抗CRP抗体I在加入体系前优选用MES缓冲溶液稀释至0.3~0.8mg/mL,更优选稀释至0.5mg/mL。
所述抗PA抗体I或抗CRP抗体I的加入量优选为每mg荧光微球中加入20~80μg(更优选25~50μg)抗体。
所述干燥优选环境的湿度低于40%。
本发明中,步骤(3)为试纸条的组装。
其中,所述试纸条I和所述试纸条II在制得后切成宽度为3.5~4.5mm的条状。
较佳地,步骤(3)还包括将所述试纸条I和所述试纸条II安装于同一卡座上,以方便操作和读取数据。所述卡座起固定试纸条的作用,同时使样品垫上方形成易于操作的加样孔。
本发明的一较佳实例包括如下步骤:
(1)硝酸纤维素膜的制备:
用0.01M pH 7.2~7.4的抗体保护剂分别调节抗PA抗体II和抗CRP抗体II的浓度为0.5mg/mL、驴抗鼠抗体的浓度为1.0mg/mL,使用Bio-Dot XYZ3050型三维喷点平台(Bio-Dot,美国)将抗PA抗体II及驴抗鼠抗体包被到硝酸纤维素膜I上,分别作为检测线I和质控线I,两线相隔5mm,喷膜量均为1.0μL/cm,37℃条件下真空干燥2h,室温干燥的环境下保存备用,将抗CRP抗体II及驴抗鼠抗体包被到硝酸纤维素膜II上,分别作为检测线II和质控线II,两线相隔5mm,喷膜量均为1.0μL/cm,37℃条件下真空干燥2h,室温干燥的环境下保存备用;
(2)结合垫的制备:
以5mL体系计,取250μL10mg/mL的荧光微球加入5mL 0.05 M pH 5.5的MES缓冲溶液,再加入50μL 5.0mg/mL EDC溶液,搅拌混匀后,分别加入100~250μL 0.5mg/mL的用MES缓冲溶液稀释的抗PA抗体I或抗CRP抗体I,充分混匀后,室温搅拌反应2h,加入占反应体系体积1/10的浓度为10%的BSA封闭1h,在4℃条件下11000r/min离心20min,弃上清,沉淀用3mL 0.05M pH 5.5的MES缓冲溶液复溶,4℃条件下11000r/min离心20min,最后弃上清,沉淀用0.05M pH 5.5的MES缓冲溶液复溶至起始体积,将制备好的以荧光微球标记的抗PA抗体I和抗CRP抗体I用Bio-Dot XYZ3050型三维喷点平台分别喷涂至结合垫I和结合垫II上,37℃条件下真空干燥2h,室温干燥的环境下保存备用;
(3)试纸条的组装:将样品垫I、结合垫I、包被有抗PA抗体II作为检测线I与驴抗鼠抗体作为质控线I的硝酸纤维素膜I和吸水纸I依次搭接地粘贴在粘性底板I上且分别部分重合,得试纸条I;将样品垫II、结合垫II、包被有抗CRP抗体II作为检测线II与驴抗鼠抗体作为质控线II的硝酸纤维素膜II和吸水纸II依次搭接地粘贴在粘性底板II上且分别部分重合,得试纸条II;将所述试纸条I和所述试纸条II切成宽度为4.0mm的条状,安装于同一卡座上。
本发明提供的技术方案之三是:利用前述试剂盒定量联合检测PA与CRP的方法,其包括如下步骤:
(1)在样品垫I上加入含有不同已知浓度的PA标准物的溶液,在样品垫II上加入含有不同已知浓度的CRP标准物的溶液,反应10~25min后,将试纸条置于激发光源下,分别测定检测线I、质控线I上条带的荧光强度以及检测线II、质控线II上条带的荧光强度,分别根据检测线I与质控线I的荧光强度的比值以及检测线II与质控线II的荧光强度的比值绘制反映PA和CRP含量的标准曲线;
(2)在样品垫I和样品垫II上加入待测物溶液,反应10~25min后,将试纸条置于激发光源下,分别测定检测线I、质控线I上条带的荧光 强度以及检测线II、质控线II上条带的荧光强度,将检测线I与质控线I的荧光强度的比值以及检测线II与质控线II的荧光强度的比值对照步骤(1)得到的标准曲线,读取待测物溶液中的PA含量和CRP含量。
本发明中,所述的激发光源包含于检测本发明所述试纸条的荧光免疫读取仪内,所述荧光免疫读取仪包含激发光源模块、滤光模块、光电转换模块、控制分析模块和软件系统,所述的激发光源的波长较佳地为450~500nm,更优选470nm。
步骤(1)中所述反应的时间较佳地为15min。
步骤(2)中所述反应的时间较佳地为15min。
本发明的检测原理为:
按照检测步骤把样本溶液加入到试纸条的样品垫上,当检测样本中不含PA或者CRP时,荧光微球-抗体复合物只会被硝酸纤维素膜质控线上的驴抗鼠抗体捕获,在激发光源的激发作用下只有质控线出现荧光条带当检测样本中含有PA或CRP抗原时,荧光微球-抗体复合物就会和检测样本中的抗原结合形成荧光微球-抗体-抗原复合物,这种荧光微球-抗体-抗原复合物被硝酸纤维素膜检测线上的抗PA或CRP抗体捕获,未结合的荧光微球-抗体复合物在毛细作用下继续向吸水纸方向移动,被质控线上包被的驴抗鼠抗体捕获,在激发光源的激发作用下检测线和质控线均出现荧光条带;在一定范围内,随检测样本中PA或CRP抗原的浓度增加,硝酸纤维素膜上检测线的荧光亮度越强。
本发明提供的技术方案之五是:前述试剂盒在联合检测PA与CRP中的应用。
在符合本领域常识的基础上,上述各优选条件,可任意组合,即得本发明各较佳实例。
本发明所用试剂和原料均市售可得。
本发明的积极进步效果在于:
相比传统的检测方法,本发明的试纸条和检测方法有极大优势:
(1)灵敏度高,其灵敏度是用传统的染料和有色标记物质检测方法的10~1000倍,能达到pg/mL,可以与气质联用和HPLC等精密检测方法相媲美,使用双抗夹心提高了捕获效率,增强了灵敏度;
(2)微球表面携带活性化学基团,抗体标记使用的是化学偶联方法,形成的荧光微球-抗体复合物能稳固结合,标记稳定性好、非特异性低;
(3)操作方便耗时短,检测线性范围宽,本发明试纸条的检测范围是5-100ng/mL,只需10~20min就能得到检测结果;
(4)本发明实现了对PA和CRP的快速联合检测,所测指标能够更加有效地用于评价待测样本的营养状况。
附图说明
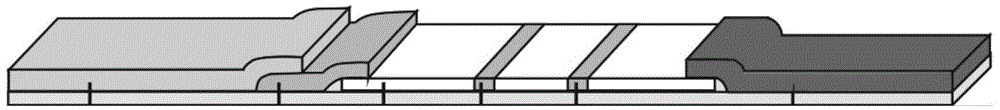
图1为实施例1中定量联合检测样本中PA和CRP的试剂盒的结构示意图。
图2为图1所示试剂盒中单一试剂条的细节结构图。
图3为实施例1中卡座的实拍图。
图4为实施例2中反映PA含量的标准曲线,其中,纵坐标为检测线I和质控线I上条带的荧光强度的比值,横坐标为PA的浓度。
图5为实施例2中反映CRP含量的标准曲线,其中,纵坐标为检测线II和质控线II上条带的荧光强度的比值,横坐标为CRP的浓度。
具体实施方式
以下实施例用于说明本发明,但并不用来限制本发明的范围。除特殊说明的之外,各实施例中所用的设备和试剂均常规市售可得。
实施例1定量联合检测样本中PA和CRP的试剂盒的制备
本实施例中,底板材料为PVC塑料胶板,材料购自余姚市富诚塑化有限公司;样品垫材料为玻璃纤维膜,材料购自上海金标生物科技有限公司;结合垫的材料为玻璃纤维膜,材料购自上海金标生物科技 有限公司公司。抗PA抗体I和抗PA抗体II具有不同的抗原结合位点,抗CRP抗体I和抗CRP抗体II具有不同的抗原结合位点。
(1)硝酸纤维素膜的制备
用pH 7.2~7.4的PB缓冲液(加入3%蔗糖)调节抗PA抗体II的浓度为0.5mg/mL、驴抗鼠抗体的浓度为1.0mg/mL,使用Bio-Dot XYZ3050型三维喷点平台将抗PA抗体II及驴抗鼠抗体包被到硝酸纤维素膜I上,分别作为检测线I和质控线I,喷膜量均为1μL/cm,37℃条件下真空干燥2h,室温干燥的环境下保存备用。所述干燥的环境湿度低于40%。
用pH 7.2~7.4的PB缓冲液(加入3%蔗糖)调节抗CRP抗体II的浓度为0.5mg/mL、驴抗鼠抗体的浓度为1.0mg/mL,使用Bio-Dot XYZ3050型三维喷点平台将抗CRP抗体II及驴抗鼠抗体包被到硝酸纤维素膜II上,分别作为检测线II和质控线II,喷膜量均为1μL/cm,37℃条件下真空干燥2h,室温干燥的环境下保存备用。所述干燥的环境湿度低于40%。
(2)荧光微球标记抗体及结合垫的制备
在两个含有5mL 0.05M pH 5.5的MES缓冲溶液的容器中加入250μL10mg/mL的荧光微球,再加入50μL 5.0mg/mL EDC溶液,搅拌混匀后,分别加入100-250μL 0.5mg/mL的抗PA抗体I与抗CRP抗体I,充分混匀后,室温搅拌反应2h,加入十分之一体积10%的BSA封闭1h,在4℃条件下11000r/min离心20min,弃上清,沉淀用5mL的0.05M pH 5.5的MES缓冲溶液清洗,用上述的离心条件再次离心,最后弃上清,沉淀用MES缓冲溶液复溶至起始体积。将制备好的标记有荧光微球的抗PA抗体I和抗CRP抗体I用Bio-Dot XYZ3050型三维喷点平台分别喷涂至检测PA的结合垫I和检测CRP的结合垫II上,37℃条件下真空干燥2h,室温干燥的环境下保存备用。所述干燥的环境湿度低于40%。
(3)试纸条的组装
如图1和图2所示,将样品垫I、结合垫I、包被有抗PA抗体II作为检测线I与驴抗鼠抗体作为质控线I的硝酸纤维素膜I和吸水纸I依次搭接地粘贴在粘性底板I上且分别部分重合,得试纸条I;将样品垫II、结合垫II、包被有抗CRP抗体II作为检测线II与驴抗鼠抗体作为质控线II的硝酸纤维素膜II和吸水纸II依次搭接地粘贴在粘性底板II上且分别部分重合,得试纸条II;将所述试纸条I和所述试纸条II切成宽度为4.0mm的长条状,安装于同一卡座上。图1中,6和7分别为卡座与样品垫间形成的加样孔,其中一个为检测PA所设,另一个为检测CRP所设。1为卡座底板,用于安装试纸条。2和3分别为检测PA/CRP和CRP/PA的试纸条,平行排列于卡座底板上,5和4分别对应检测线和质控线。图2为单个试纸条的细节图,其中,8为样品垫,9为结合垫,10为硝酸纤维素膜,11为检测线,12为质控线,13为吸水纸,从图中可以看出,样品垫、结合垫、包被有抗PA/CRP抗体作为检测线与驴抗鼠抗体作为质控线的硝酸纤维素膜和吸水纸依次搭接地粘贴在粘性底板上且分别部分重合。将试纸条I和试纸条II安装于同一卡座(如图3所示),样品垫I和样品垫II与卡座之间分别形成一个方便加样操作的加样孔,即得。
(5)将试纸条装入铝箔袋,加入干燥剂后,封口保存,于室温干燥的环境下至少可保存一年。
实施例2样本中PA和CRP的定量检测
使用实施例1制备的试纸条对样本中的PA和CRP进行检测,其步骤包括:
(1)在样品垫I的加样孔中加入含有不同已知浓度(具体为0.0、2.5、5.0、12.5、25.0、37.5、75.0、100、200μg/L)的PA标准物的溶液,在样品垫II的加样孔中加入含有不同已知浓度(具体为0.0、1.0、2.5、5.0、7.5、10.0、50.0、100.0、200.0、400.0μg/L)的CRP标准物 的溶液,反应15min后,将试纸条置于470nm激发光源下,分别测定检测线I、质控线I上条带的荧光强度以及检测线II、质控线II上条带的荧光强度,分别根据检测线I与质控线I的荧光强度的比值以及检测线II与质控线II的荧光强度的比值绘制反映前PA和CRP含量的标准曲线。以检测线I和质控线I上条带的荧光强度的比值为纵坐标,PA的浓度为横坐标绘制标准曲线,如图4所示,结果表明在PA浓度为5.0~100.0μg/L的范围内有很好的线性相关(R2=0.998),其灵敏度为2.5μg/L;以检测线II和质控线II上条带的荧光强度的比值为纵坐标,CRP的浓度为横坐标绘制标准曲线,如图5所示,结果表明在CRP浓度为5.0~100.0μg/L的范围内有很好的线性相关(R2=0.998),其灵敏度为1.0μg/L。
(2)在样品垫I的加样孔和样品垫II的加样孔中分别加入待测物溶液,反应15min后,将试纸条置于470nm激发光源下,分别测定检测线I、质控线I上条带的荧光强度以及检测线II、质控线II上条带的荧光强度,将检测线I与质控线I的荧光强度的比值以及检测线II与质控线II的荧光强度的比值对照步骤(1)得到的标准曲线,读取待测物溶液中的PA含量和CRP含量。
实施例3样本中前白蛋白和C-反应蛋白的定量检测
取实施例1制备的试纸条,打开铝箔袋取出试纸条,平放于桌面,取2μL血样于装有2mL 0.01M pH 7.4的磷酸盐缓冲溶液的CRP试剂瓶中,充分混匀后分别取100μL加入装有0.9mL 0.01M pH 7.4的磷酸盐缓冲溶液的CRP试剂瓶中,在试剂瓶中取100uL溶液加入试纸条对应检测PA和CRP的加样孔中,反应15min后将试纸条放入置于激发光源下,分别测定检测线I、质控线I上条带的荧光强度以及检测线II、质控线II上条带的荧光强度,将检测线I与质控线I的荧光强度的比值以及检测线II与质控线II的荧光强度的比值对照实施例2得到的标准曲线,读取待测物溶液中的PA含量和CRP含量。
虽然,上文中已经用一般性说明、具体实施方式及试验,对本发明作了详尽的描述,但在本发明的基础上,可以对之作一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种st2定量检测方法及试剂盒的制作方法
- 一种定量药粉取用盒的制作方法
- 一种层粘连蛋白(ln)测试试剂盒及其测试方法
- 一种抗核糖体P蛋白抗体IgG的磁微粒化学发光定量测定试剂盒及制备和检测方法
- 一种阿胶胶液半成品或成品中驴、牛源性成分的定量检测方法、组合物及试剂盒的制作方法
- 一种抗PM-Scl抗体IgG的磁微粒化学发光定量测定试剂盒及制备和检测方法
- 一种抗LKM-1抗体IgG的磁微粒化学发光定量测定试剂盒及制备和检测方法
- 一种抗SLA/LP抗体IgG的磁微粒化学发光定量测定试剂盒及制备和检测方法
- 一种快速定量检测h-fabp的时间分辨荧光免疫层析试剂及制备方法
- 一种定量检测液体样品中汞离子的方法及试剂盒的制作方法
- 一种定量药粉取用盒的制作方法
- 一种层粘连蛋白(ln)测试试剂盒及其测试方法
- 一种抗核糖体P蛋白抗体IgG的磁微粒化学发光定量测定试剂盒及制备和检测方法
- 一种阿胶胶液半成品或成品中驴、牛源性成分的定量检测方法、组合物及试剂盒的制作方法
- 一种抗PM-Scl抗体IgG的磁微粒化学发光定量测定试剂盒及制备和检测方法
- 一种抗LKM-1抗体IgG的磁微粒化学发光定量测定试剂盒及制备和检测方法
- 一种抗SLA/LP抗体IgG的磁微粒化学发光定量测定试剂盒及制备和检测方法
- 一种快速定量检测h-fabp的时间分辨荧光免疫层析试剂及制备方法
- 一种定量检测液体样品中汞离子的方法及试剂盒的制作方法
- 一种轴抑制蛋白2基因突变检测试剂及应用