试样用夹持器的制作方法
本发明涉及在肿瘤部位识别装置中使用的试样用夹持器。
背景技术:
近年来的日本迎来了快速的老龄化社会,癌症患者数有增加的趋势。特别是淋巴结转移是重要的预后因素之一,因此,在决定患者的治疗方法的方面,准确地诊断淋巴结转移的有无是重要的。特别地,从原发灶离开的癌细胞最先到达的淋巴结被称为前哨淋巴结。到达前哨淋巴结的癌细胞的数量起初是有限的,因此,对前哨淋巴结进行调查,若癌细胞的转移极少,则可以认为基本没有从前哨淋巴结转移至末端的淋巴结。
作为术前的淋巴结转移诊断法,已知有ct(计算机断层摄影,computedtomography)、fdg-pet(氟脱氧葡萄糖正电子发射断层摄影,fluorodeoxyglucosepositronemissiontomography)等,但现状是在诊断精度的方面仍然不够充分。另外,术中、术后的淋巴结转移的诊断使用病理组织诊断,但通常仅根据从单一的切割面得到的标本来诊断转移的有无,因此有时会漏掉小的转移灶,其诊断精度不能说是充分的。此外,在术中的快速检查中,到诊断为止至少需要约30分钟,而且需要由病理医生做出判断,因此,也有可能因病理医生个人的技能差异而使诊断结果产生差异。此外,鉴于病理医生本身不足的目前的现状,需要不依靠病理医生的判断而能够以高精度进行淋巴结转移的诊断的新方法。
目前,在包括消化系统领域在内的广泛领域内,癌症的检测正在应用使用5-氨基乙酰丙酸(5-ala)的光线力学方法。5-ala是也存在于生物体内的氨基酸的一种,其为水溶性,能够经口、局部地给药。从体外给用5-ala时,在正常细胞中快速代谢为血红素,但在癌细胞中,由于代谢酶的活性的差异而选择性地蓄积作为代谢产物的原卟啉ix(ppix)。在此,血红素观察不到荧光,另一方面,ppix为荧光物质,因此,通过对该光进行检测,能够进行癌症的诊断(参考专利文献1、非专利文献1)。
现有技术文献
专利文献
专利文献1:国际公开第2013/002350号
非专利文献
非专利文献1:“使用5-氨基乙酰丙酸(5-ala)的消化系统癌症转移淋巴结的诊断”,京都府立医科大学杂志,122卷,no.4(2013)
技术实现要素:
发明所要解决的问题
上述内容在现阶段还处于实验室水平的研究阶段,设想在实际应用于人的诊断时会产生各种问题。本申请人目前正在进行通过对存在于试样的肿瘤部位的ppix所发出的荧光进行分光检测而进行肿瘤部位和非肿瘤部位的识别的装置的开发。在该开发过程中,本发明人发现,为了精度良好地进行肿瘤部位的识别,使收容试样的夹持器承担一定的要求,从而完成了本发明。
本发明的目的在于提供在肿瘤部位识别装置中使用的试样用夹持器,其是能够精度良好地进行肿瘤部位的识别的夹持器。
用于解决问题的方法
本发明为一种试样用夹持器,其为在通过对试样照射从光源部射出的激发光、对存在于上述试样的肿瘤部位的卟啉类所发出的荧光进行分光检测而进行上述肿瘤部位和非肿瘤部位的识别的肿瘤部位识别装置中使用的试样用夹持器,其特征在于,具备:
收容上述试样的收容部、
用于使从上述试样用夹持器的外侧射出的上述激发光透射而对收容在上述收容部内的上述试样照射该激发光的窗部、和
用于抑制收容在上述收容部内的上述试样的位移的试样固定部。
需要说明的是,本说明书中的“卟啉类”是指在卟啉环上带有取代基的化合物,例如除了ppix以外,还存在由ppix生成的光-原卟啉(ppp)等原卟啉类。
在使用肿瘤部位识别装置对试样中是否包含肿瘤部位进行检测时,首先,对作为受试者的患者给用5-ala。在正常细胞中,5-ala被吸收时,利用细胞内线粒体代谢为作为卟啉类之一的原卟啉ix(以下,适当记载为“ppix”),生物合成为血红素。但是,恶性肿瘤细胞与正常细胞相比,ppix生成过程中的酶(pbg脱氨酶)活性高,催化由ppix生物合成血红素的酶(亚铁螯合酶)活性低。因此,在恶性肿瘤细胞中,5-ala被吸收时,在该细胞中大量蓄积ppix。
ppix是荧光物质,而血红素不是荧光物质。因此,通过对试样照射规定的激发光并对从试样发出的荧光进行受光分析,能够进行肿瘤部位和非肿瘤部位的识别。
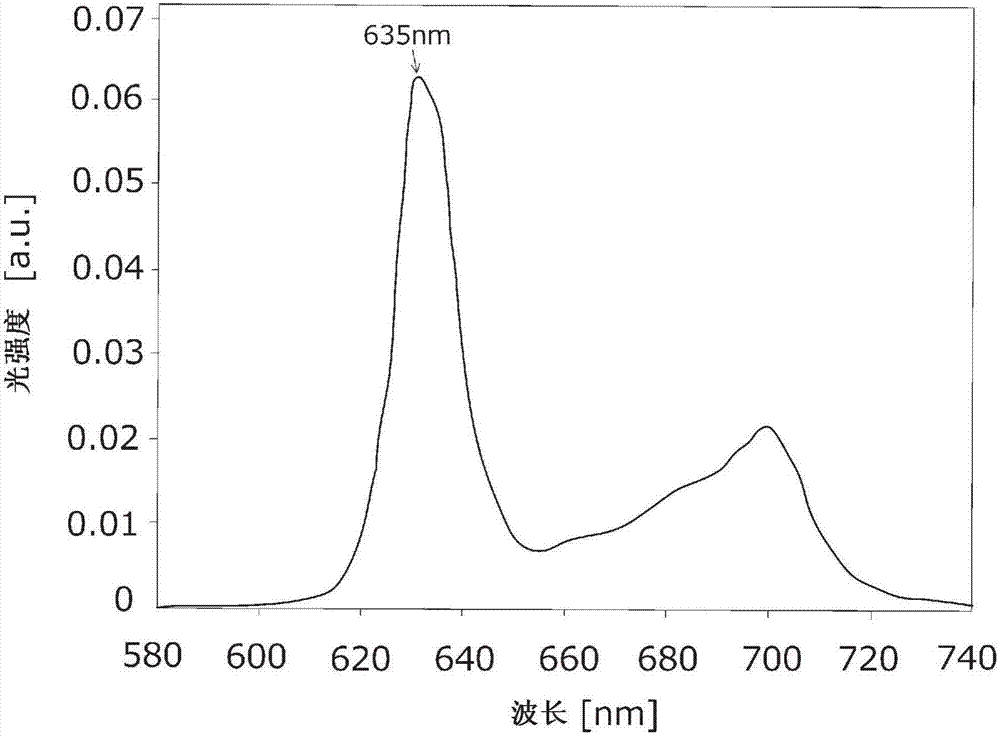
图1a是示出ppix的吸收光谱的图。另外,图1b是示出ppix的荧光光谱的图。ppix对规定波长的激发光显示出高吸光度。具体而言,如图1a所示,对波长370nm以上且450nm以下的光显示出高吸光度,特别是对波长385nm以上且425nm以下的光显示出极高的吸光度。而且,对ppix照射上述波长范围的光时,如图1b所示,从ppix放射出以635nm附近作为峰值、包含620nm以上且710nm以下的波长成分的荧光。
作为肿瘤部位识别装置,需要能够射出包含在上述波段内的波长的激发光的光源部、和接收从ppix放射出的荧光的受光部。另外,需要用于将试样设置到装置中的机构。
作为试样,假设淋巴结的切片等活检材料。在将这样的活检材料设置到装置中时,为了不产生污染装置等问题,本申请人想出了预先将试样收容到规定的夹持器内并将该夹持器设置到装置的规定位置的方法。
该夹持器具有收容部,在使用时将试样载置于该收容部内。另外,在夹持器设置有使从装置内的光源部射出的激发光透射的窗部。通过使激发光从窗部透射而照射到试样上,若试样中含有ppix,则该ppix被激发而发出荧光。通过对设置在装置侧的受光部中接收到的光进行分光分析,能够根据来自ppix的荧光的波长的光的强度对肿瘤部位和非肿瘤部位进行识别。
在此,根据本发明人的深入研究可知,在将收容有试样的夹持器设置到装置的规定位置后照射光、并在受光部接收荧光的期间,有时试样会发生收缩、或者相反地发生膨胀。
作为产生这种现象的理由之一,认为是由于假设了前哨淋巴结等活检材料作为试样。在使用如上所述的前哨淋巴结等活检材料作为试样的情况下,从人体切除后,在收容到夹持器之前利用生理盐水等进行清洗是一般做法。由此认为,在将含有大量水分的状态的活检材料作为试样的情况下,在将收容有试样的夹持器设置到装置的规定位置并照射光的期间,水分蒸发,试样发生了收缩。另外,活检材料因干燥而发生收缩,但有时也会由于此时产生的局部收缩所致的应力变形而局部地发生膨胀(向膨胀方向移动)。
在此,如上所述,利用根据来自ppix的荧光的波长的光的强度对肿瘤部位和非肿瘤部位进行识别的方法,首先,在设置于装置中的受光部,对各位置的光强度是否超过规定阈值进行判定。然后,在装置中,将光强度超过规定阈值的部位判断为肿瘤部位,将光强度为阈值以下的部位判断为非肿瘤部位。
在该方法的情况下,例如将经由窗部被照射到光的区域分割为各个规定的小区域,对该各个小区域进行光强度是否超过规定阈值的判定。由此,可以判定配置在收容部上的哪个区域的试样的位置为肿瘤部位。
但是,如上所述试样发生膨胀/收缩时,在受光部进行光量的判定的过程中试样会产生位置偏移。结果,根据试样的位置偏移而产生肿瘤部位的位置偏移,根据情况可能会误认肿瘤部位。
但是,根据如上所述的本发明的构成,在夹持器中具备用于抑制收容在收容部内的试样的位移(位置的变动)的试样固定部。因此,在将试样收容到夹持器内之后,利用试样固定部来抑制试样的位移。结果,即使试样发生膨胀/收缩,与以往相比也可抑制试样的位置的位移量,肿瘤部位被误认的可能性降低。
另外,专利文献1中还记载了对ppix照射规定波长的光而将其转变为光-原卟啉(ppp)、通过ppix的峰值波长附近的荧光强度与ppp的峰值波长附近的荧光强度的比率进行肿瘤部位的判定的方法。根据上述构成的试样用夹持器,在使用该方法进行肿瘤部位的判定的情况下也是有效的。以下,简单进行说明。
图2是示出对ppix照射波长436nm左右的光时的荧光光谱的变化方式的图。在照射波长436nm左右的光之前的状态下,荧光光谱的峰值波长为635nm附近。如参考图1b所说明的那样,这与ppix的荧光光谱一致。与此相对,在照射波长436nm左右的光之后的状态下,荧光光谱的峰值波长为675nm附近,与ppix的荧光光谱的峰值波长635nm不同。另外可知,在照射波长436nm左右的光之后的状态下,波长635nm附近的荧光强度降低。由此认为,通过对ppix照射波长436nm左右的光,使ppix转变为ppp。
通过利用该现象,例如,可以在照射波长436nm左右的光之前和之后,都测定波长675nm附近的荧光强度相对于波长635nm附近的荧光强度的比率,将该比率超过规定阈值的部位判断为肿瘤部位。
在利用该方法的情况下,也如上所述地将例如经由窗部被照射到光的区域分割为各个规定的小区域,对该各个小区域进行上述比率是否超过规定阈值的判定,由此判定配置在收容部上的哪个区域的试样的位置为肿瘤部位。由此,根据本发明的构成,即使试样发生膨胀/收缩,也可利用试样固定部抑制试样的位置的位移量,因此肿瘤部位被误认的可能性降低。
在此,上述试样固定部可以设定为特别是能够抑制收容在上述收容部内的上述试样的、与上述收容部的底面平行的方向、更详细地为水平方向的位移的构成。
更具体而言,可以如下构成试样用夹持器。
即,上述试样用夹持器可以在上述构成的基础上具备在一部分区域设置有上述收容部的基体部和用于覆盖上述收容部的上方的盖部,上述试样固定部由设置在上述基体部或上述盖部中的至少一者的凸部构成,以能够通过上述盖部的开合使上述凸部与上述试样接触的第一状态和上述凸部与上述试样分离的第二状态进行转变的方式构成。
根据该构成,通过在将试样收容到收容部内之后合上盖部,凸部与试样接触,因此,可抑制试样的水平方向的移动。需要说明的是,也可以是在合上盖部时凸部的前端与试样接触的构成。
更具体而言,上述试样固定部可以由离散地设置在上述盖部的多个上述凸部构成。作为该多个上述凸部的配置方式,可以为各种构成。作为一例,可以为各凸部具有方型形状且纵横地对齐配置的方式、以交错式(astaggeredarrangement)分散配置的方式。另外,作为各凸部的形状,也可以采用半球形状、圆锥形状、圆台形状、多棱锥形状、多棱台形状、波型形状、其他形状。
另外,上述试样用夹持器也可以如下构成:具备用于覆盖上述收容部的上方的盖部,上述试样固定部由设置在上述盖部的可伸缩的片状构件构成,在上述收容部内收容有上述试样的状态下合上上述盖部时,上述片状构件以接触的状态覆盖上述试样的外周。
设定为这样的构成时,在将试样收容到收容部内之后合上盖部时,设置在盖部的片状构件以与试样的外周接触的状态覆盖。结果,通过与试样的外表面密合的片状构件的存在,可抑制试样的水平方向的移动。
需要说明的是,上述盖部可以以相对于上述基体部可旋转的方式连接。
另外,可以为如下构成:在上述试样用夹持器中,在上述盖部或上述基体部中的至少一者设置有密封构件,合上上述盖部时,上述盖部与上述基体部经由上述密封构件接触而将上述收容部密闭。
通过设定为这样的构成,在合上盖部的状态下盖部与基体部完全密合,因此,可防止收容在收容部内的试样漏出到外部。
需要说明的是,作为上述试样,可以使用例如前哨淋巴结的切片、病理断端等活检材料。另外,上述的装置也可以用于印片细胞诊断。
发明效果
通过将试样收容到本发明的试样用夹持器中并安装到肿瘤部位识别装置中,能够精度良好地进行肿瘤部位的识别。
附图说明
图1a是示出ppix的吸收光谱的图。
图1b是示出ppix的荧光光谱的图。
图2是示出对ppix照射波长436nm左右的光时的荧光光谱的变化方式的图。
图3是示意性地示出肿瘤部位识别装置的外观的图。
图4是示意性地示出肿瘤部位识别装置的内部构成的框图。
图5a是试样用夹持器的第一实施例的立体图。
图5b是试样用夹持器的第一实施例中的基体部的俯视图。
图5c是试样用夹持器的第一实施例中的盖部的俯视图。
图6是示出第一实施例中的盖部的另一构成的图。
图7是示出第一实施例中的盖部的又一构成的图。
图8是示出第一实施例中的盖部的又一构成的图。
图9是示出第一实施例中的盖部的又一构成的图。
图10是示出第一实施例中的盖部的又一构成的图。
图11是示出第一实施例中的盖部的又一构成的图。
图12是示出第一实施例中的盖部的又一构成的图。
图13是示出第二实施例中的盖部的构成的图。
图14是示出第二实施例中的盖部的另一构成的图。
图15是试样用夹持器的另一实施方式的立体图。
具体实施方式
[装置概要]
在试样用夹持器的说明之前,先对利用该夹持器的肿瘤部位识别装置的构成进行说明。
图3是示意性地示出装置的外观的图。另外,图4是示意性地示出装置内部的构成的框图。需要说明的是,图3和图4是示出肿瘤部位识别装置的一例的图,利用本发明的夹持器的装置不拘泥于该图的内容。
如图3所示,肿瘤部位识别装置10(以下,有时适当称为“装置10”)具备夹持器安装口11和显示部12。夹持器安装口11是用于安装试样用夹持器1的机构。另外,显示部12对应于显示由肿瘤部位识别装置10判定的结果的监视器。需要说明的是,在此,示出了在肿瘤部位识别装置10的主体上设置有显示部12的构成,但也可以采用在装置10的主体上不设置显示部12而在其他监视器显示判定结果的构成。
如图4所示,装置10具备光源部21、滤光片22、分色镜23、物镜24、滤光片25、受光部26、运算处理部27。需要说明的是,在图4的示例中,假设了仿照图3使装置10具备显示部12的构成。
光源部21例如由汞灯、发光二极管元件、激光二极管元件等构成。滤光片22具有从由光源部21射出的光中选择性地使特定波长的光透射的功能,例如可以由电介质多层膜等构成。在此,以滤光片22具有选择性地使波长390nm的光透射的功能的情况进行说明,但只要具有选择性地使385nm以上且425nm以下的特定波段的光透射的功能即可。
分色镜23具有使规定波段的光反射、使其他规定波段的光透射的功能,例如可以由电介质多层膜等构成。在此,以分色镜23具有使波长390nm的光反射、使波长620nm以上的光透射的功能的情况进行说明。需要说明的是,该分色镜23只要具有使利用滤光片22选择出的波长的光反射、至少使从试样2发出的荧光的峰值波长附近的光透射的功能即可。
从光源部21射出、从滤光片22透射后的波长390nm的激发光31被分色镜23反射,导入到物镜24。然后,从物镜24通过后的光从夹持器1的规定区域(以下,适当记载为“窗部52”)透射,照射到收容在夹持器1中的试样2上。试样2中蓄积有ppix时,ppix被该波长390nm的激发光31激发,发出荧光32。荧光32从夹持器1的窗部52透射,与激发光反向行进,导入到物镜24。然后,从分色镜23透射,入射到滤光片25。
滤光片25具有从入射的光中选择性地使规定波长的光透射的功能。在此,以滤光片25具有选择性地使波长635nm的光透射的功能的情况进行说明,但只要具有选择性地使图1b所示的ppix的荧光光谱的峰值波长635nm附近的规定波长的光透射的功能即可。
从滤光片25透射后的波长635nm的荧光在受光部26被接收。受光部26例如可以由ccd相机等摄像装置构成。受光部26将接收的光的强度与试样2内的位置信息一起输出到运算处理部27。运算处理部27例如由微型计算机等构成,对各位置的光强度是否超过规定的阈值进行判定。然后,运算处理部27将光强度超过规定阈值的部位判断为肿瘤部位、将光强度为阈值以下的部位判断为非肿瘤部位。然后,将该判断结果输出到显示部12。
显示部12基于从运算处理部27输送的肿瘤部位的坐标信息,显示例如在试样2的图像上的规定位置实施表示其为肿瘤部位的标记或显色而得到的图像数据。另外,在不存在被运算处理部27判断为肿瘤部位的区域的情况下,可以将该内容的信息显示于显示部12。
检查员通过目视确认显示部12,由此能够获知在试样2中是否存在肿瘤部位,并且在存在肿瘤部位的情况下能够容易地获知其存在部位。另外,通过设定为例如在装置10上设置操作按钮、将收容有试样2的夹持器1安装到装置10中并按下该操作按钮时从光源部21射出激发光的结构,能够利用装置10自动地进行试样2的肿瘤部位识别判定,可消除由检查员的技术导致的判断结果的偏差,并且也不需要病理医生的判断。
需要说明的是,分色镜23是出于为了使装置10小型化而将激发光31和荧光32的光路部分共用的目的设置的,但在装置10中,分色镜23不是一定需要的构成。另外,滤光片22可以与光源部21一体化。滤光片25也可以与受光部26一体化。图4所示的装置10的构成只不过是一例,只要是实现相同功能的构成,则可以进行各种设计变更,这是不言而喻的。
[夹持器]
以下,对夹持器1的构成进行说明。
(第一实施例)
图5a是夹持器1的第一实施例的立体图。如图5a所示,夹持器1包含基体部42和盖部43而构成。图5b是本实施例中的基体部42的俯视图,图5c是本实施例中的盖部43的俯视图的一例。
基体部42和盖部43由铰链部51连接,盖部43以相对于基体部42可旋转的方式构成。在基体部42设置有用于将试样2收容到规定部位的收容部41。该收容部41的深度比其周围更深,即使在收容部41内收容有试样2的状态下将盖部43与基体部42重叠,试样2也不会被盖部43压碎。需要说明的是,图5b中示意性地示出了在收容部41内收容有试样2的状态。
进而,如图5a和图5c所示,在盖部43设置有多个凸部44。通过设定为该构成,在将试样2收容到收容部41内之后,合上盖部43而将基体部42与盖部43重叠,由此使凸部44的前端与试样2接触。由此,可抑制试样2的水平方向上的移动。在本实施例中,凸部44对应于“试样固定部”。在本实施例中,使凸部44的形状为圆锥形状或圆台形状。
如参考图4所说明的那样,在装置10中,激发光31从夹持器1透射,照射到试样2上。在此,在图5a中,从与盖部43相反的一侧对基体部42照射激发光31,从基体部42的规定部位透射,激发光被导入到收容在收容部41内的试样2中。在夹持器1的基体部42,激发光所透射的区域对应于“窗部52”(参考图4)。
如“用于解决问题的方法”的部分所述,将在收容部41内收容有试样2的夹持器1安装到装置10的夹持器安装口11内,对试样2照射从光源部21射出的激发光31、在受光部26接收荧光的期间,试样2有可能发生膨胀/收缩。假如在本实施例这样在夹持器1上不存在凸部44的情况下,在受光部26接收荧光的过程中,试样2在夹持器1内发生膨胀/收缩而在水平方向上移动。结果,有可能发生如下情况:在运算处理部27中判断为荧光强度超过规定阈值的部位实际上不是肿瘤部位;相反地,判断为荧光强度为规定阈值以下的部位实际上是肿瘤部位。
与此相对,在本实施例中,在夹持器1的盖部43存在有凸部44,因此,在将试样2收容到收容部41内之后,将盖部43合上,由此使凸部44的前端与试样2接触。结果,即使试样2发生膨胀/收缩,也可利用凸部44与试样2的接触所伴随的摩擦力来阻碍试样2的水平方向的移动,大大抑制在受光部26接收荧光的期间内试样2的位置发生变动的量。结果,能够利用装置10准确地判定试样2中的肿瘤部位。
需要说明的是,设置在盖部43的凸部44的形状可以进行各种变更。
图6是示出改变凸部44的形状而得到的盖部43的构成的图,(a)对应于立体图、(b)对应于俯视图、(c)对应于主视图。在该例中,采用了在盖部43的表面上纵横地对齐配置有棱柱形状的多个凸部44的构成。
图7是示出改变凸部44的形状而得到的盖部43的另一构成的图,(a)对应于立体图、(b)对应于俯视图、(c)对应于主视图。在该例中,采用了在盖部43的表面上以交错式配置(astaggeredarrangement)有棱柱形状的多个凸部44的构成。
图8是示出进一步改变凸部44的形状而得到的盖部43的构成的图,(a)对应于立体图、(b)对应于俯视图、(c)对应于主视图。在该例中,采用了在盖部43的表面上纵横地对齐配置有半球形状的多个凸部44的构成。
图9是示出进一步改变凸部44的形状而得到的盖部43的构成的图,(a)对应于立体图、(b)对应于俯视图、(c)对应于主视图。在该例中,采用了在盖部43的表面上以交错式配置有半球形状的多个凸部44的构成。
图10是示出进一步改变凸部44的形状而得到的盖部43的构成的图,(a)对应于立体图、(b)对应于俯视图、(c)对应于主视图。在该例中,采用了在盖部43的表面上对齐配置有波型形状的凸部44的构成。更详细而言,沿x方向延伸的波型形状的凸部44在y方向上分离地配置有多个。
图11是示出进一步改变凸部44的形状而得到的盖部43的构成的图,(a)对应于立体图、(b)对应于俯视图、(c)对应于主视图。在该例中,采用了在盖部43的表面上对齐配置有波型形状的凸部44的构成。更详细而言,如果与图10a、图10b和图10c所示的构成进行比较,则波型形状的凸部44在x方向上断开,结果形成了在x方向和y方向上分离地配置有多个凸部44的构成。
图12是示出进一步改变凸部44的形状而得到的盖部43的构成的图,(a)对应于立体图、(b)对应于俯视图、(c)对应于主视图。在该例中,采用了在盖部43的表面上以放射状配置有多个凸部44的构成。
如上所述,在第一实施例中说明的夹持器1均为在盖部43的表面上设置有多个凸部44的构成。但是,多个凸部44也可以设置在基体部42侧而非盖部43,更详细而言,也可以设置在收容部41的表面上。
需要说明的是,上述的凸部44的形状和配置方式只不过是一例,并不限定于该构成。另外,在上述的方式中,对设置有多个凸部44的构成进行了说明,但凸部44的个数也可以为一个。作为一例,在图10所示的凸部44的方式中,可以通过将沿x方向延伸的各凸部44在y方向上连接起来而构成为一个凸部44。
(第二实施例)
图13是示出第二实施例中的盖部43的构成的图,(a)对应于立体图、(b)对应于俯视图、(c)对应于主视图。在本实施例中,在盖部43设置有由刚性体构成的框状构件45和固定于框状构件45上的可伸缩的片状构件46。作为片状构件46,可以使用例如薄的硅膜或弹性体膜来构成。在本实施例中,该片状构件46对应于“试样固定部”。
在本实施例中,在夹持器1的盖部43设置有片状构件46。在该构成下,将试样2收容到收容部41内之后将盖部43合上时,首先,片状构件46的底面与试样2的上表面接触。然后,随着盖部43向收容部41侧靠近,片状构件46以将试样2的外周包在里面的方式改变形状,在最终利用盖部43将收容部41完全覆盖的时刻,以试样2的外周被片状构件46密合的状态覆盖。结果,即使试样2发生膨胀/收缩,也可利用片状构件46与试样2的接触所伴随的摩擦力来阻碍抑制试样2的水平方向的移动。
需要说明的是,在图13的示例中,将框状构件45设定为矩形形状,但也可以将框状构件45设定为圆形,还可以设定为其他形状。图14中示出了将框状构件45设定为圆形时的示例。在图14中,(a)对应于立体图、(b)对应于俯视图、(c)对应于主视图。
[其他实施方式]
以下,对其他实施方式进行说明。
<1>如“用于解决问题的方法”的部分所述,在装置10中,可以通过对试样2照射规定波长的光而将ppix转换为ppp,根据来自ppix的荧光强度与来自ppp的荧光强度的比率的值来进行肿瘤部位的判定。
ppp的荧光光谱的峰值波长为675nm附近,与ppix的荧光光谱的峰值波长635nm不同。在此,若将用于产生荧光而照射的光称为“第一激发光”、将用于使ppix转换为ppp而照射的光称为“第二激发光”,则可以根据在照射第二激发光之前照射第一激发光而得到的荧光的光谱和在照射第二激发光之后照射第一激发光而得到的荧光的光谱的变化的方式来确定ppix。更具体而言,可以将波长635nm附近的荧光强度与波长675nm附近的荧光强度的比率在第二激发光的照射前后变化至超过规定阈值的程度的部位判断为肿瘤部位。
在该构成的情况下,光源部21可以以能够射出第一激发光和第二激发光这两种光的方式构成。
需要说明的是,也可以将肿瘤部位识别装置10作为用于基于来自ppix和ppp以外的卟啉类的荧光强度进行肿瘤部位的判定的装置来利用。
<2>在图4所示的装置10中,可以设定为如下构成:对于从ppix发出的荧光32,利用受光部26接收多种不同波长的荧光32并进行分析。这种情况下,可以设定为例如如下构成:装置10具备滤光片更换机构,并且准备与各波长对应的多个滤光片25,在利用该滤光片更换机构更换滤光片25的同时在受光部26接收光。另外,也可以设定为如下构成:利用光学系统按照各波长将光路分支,可以在受光部26同时接收不同波长的荧光32。
另外,在图4所示的装置10中,可以利用多种不同波长的激发光31。特别是在使用其他实施方式<1>中记载的方法的情况下,假设利用第一激发光和第二激发光。这种情况下,可以在利用滤光片更换机构更换滤光片22的同时对夹持器1进行照射,也可以利用光学系统按照各波长将光路分支并对夹持器1进行照射。
<3>图15是试样用夹持器的立体图的另一例。如图15所示,夹持器1可以具备密封构件(密封部)61。由此,在将盖部43重叠到基体部42上时,能够利用密封构件61进行封印,能够将收容在收容部41内的试样2完全地密闭,从而防止污染。
<4>在上述的实施方式中,对夹持器1具备基体部42和盖部43的构成进行了说明。但是,夹持器1也可以为不具备盖部43的构成。这种情况下,为了使载置在基体部42上的试样2不会落下、或者使试样2中含有的生理盐水等液体不会流出,可以采用将基体部42的外缘用壁包围的构成。
这种情况下,可以在夹持器1的基体部42侧、更详细而言在收容部41的表面上设置有作为试样固定部的凸部44。于是,在将夹持器1安装到装置10内时,在装置10内从基体部42的上方安装用于从上方覆盖基体部42的构件,此时该构件靠近试样2,由此使试样2被凸部44挤压固定。
标号说明
1:试样用夹持器
2:试样
10:肿瘤部位识别装置
11:夹持器安装口
12:显示部
21:光源部
22:滤光片
23:分色镜
24:物镜
25:滤光片
26:受光部
27:运算处理部
31:激发光
32:荧光
41:收容部
42:基体部
43:盖部
44:凸部
45:框状构件
46:片状构件
51:铰链部
52:窗部
61:密封构件(密封部)
- 还没有人留言评论。精彩留言会获得点赞!