一种基于ABTS的水中六价铬浓度的测定方法与流程
本发明属于水污染控制水质检测技术领域。
背景技术:
铬是自然界中广泛存在的一种多价态过渡金属元素,主要分布在水、土壤、岩石中,动植物体内也含有微量的铬。铬主要以六价(Cr(VI))和三价(Cr(III))的形式存在,其毒性与价态密切相关。Cr(III)在人体内参与糖和脂肪代谢,是人体必需的微量元素之一,若人体铬缺乏,则可表现为不明原因的体重下降,外周神经炎,血浆对葡萄糖的消除率受损,呼吸率降低。而Cr(VI)的毒性高出Cr(III)数十倍甚至百倍,且更易为人体吸收且在体内蓄积,可通过皮肤、粘膜、消化道和呼吸道进入人体内,损伤人体器官,具有致癌、致畸、致突变的风险。鉴于Cr(VI)对环境的持久危险性,美国环保局(USEPA)将其认定为环境优先污染物。
铬及其化合物,在工业上的应用非常广泛。铬是重要的电镀材料,也可用于制造合金,与铁、镍组成各种性能的、抗腐蚀的不锈钢;在毛皮与制革行业中,铬的主要作用为靴制和媒染;在纺织和印染中,铬一般作为助染剂和媒染剂使用;鉴于铬在高温时可保证足够的强度及耐氧化能力,在低温时又有较强的韧性,机器工业中用途十分广泛。此外,铬也被大量应用于采矿冶炼、化工、颜料、制药、轻工纺织等行业。大量的Cr(VI)通过这些行业的工业废水排放或事故排放和泄露等方式进入到天然水体、土壤和地下水中,使得Cr(VI)成为最常见的环境污染物之一。基于Cr(VI)污染的广泛性及其危害性,含Cr(VI)废水的治理成为国内外重金属污染领域优先控制的项目之一,发展高效、经济的Cr(VI)废水处理工艺已成为研究的热点。各类水质标准均对总铬与Cr(VI)的最高允许排放浓度做出了规定,USEPA规定饮用水和地表水体中浓度最高限值分别为0.05mg·L-1和0.1mg·L-1。我国《污水综合排放标准》规定总铬与Cr(VI)的最高允许排放浓度分别为1.5mg/L和0.5mg/L;《生活饮用水水质卫生规范》规定Cr(VI)的最高限值为0.05mg/L。无论是考察各种方法对Cr(VI)的去除效果还是监测环境中的Cr(VI),都需要对Cr(VI)的浓度进行分析。
目前,测定地表水和工业废水中铬的方法主要有光谱法和电化学方法两大类。光谱法包括紫外-可见分光光度法、原子吸收分光光度法、电感耦合等离子体原子发射光谱法、X-射线荧光光谱法、化学发光法等。测定铬的电化学法目前发展较多,根据测定方式的差异可分为电导分析法、库仑分析法、电位法、伏安法、极谱分析法、电导滴定、电位滴定、电流滴定法和电解分析法等。其中,光谱法中的二苯碳酰二肼分光光度法因灵敏性高,选择性好,且需要的试剂少、仪器简单,目前被环境监测者广泛使用,是测定水中Cr(VI)的经典分析方法。该方法的原理如下:在酸性溶液中,水中呈现强氧化性的Cr(VI)将二苯碳酰二肼氧化为二苯缩二氨基脲,生成的二苯缩二氨基脲再与Cr(VI)还原产物三价铬形成紫红色络合物,在一定范围内,该紫红色络合物色度与Cr(VI)的含量成线性关系,吸光度与浓度的关系符合朗伯-比尔定律,即溶液对光的吸收程度与溶液的浓度及液层厚度的乘积成正比关系,在540nm处有最大吸收,由此定量关系实现Cr(VI)的测定。
但是二苯碳酰二肼分光光度法的显色剂二苯碳酰二肼需溶解在丙酮中,而丙酮试剂是易挥发液体,人体皮肤易吸收,长期接触该试剂对人体产生毒害;在酸性介质中许多能与二苯碳酰二肼反应生成化合物的金属离子,如Fe(III)、Mo(VI)、Cu(II)和Hg(II)可能对检测带来一定干扰;在540nm处具有光度吸收的物质如Co(II)等也会有一定影响。另外,当采用该方法分析亚硫酸钠还原Cr(VI)过程中Cr(VI)的浓度变化时,会受到亚硫酸根离子的影响,测量结果误差较大。因此急需开发可以取代二苯碳酰二肼分光光度法的抗干扰能力较强的新的检测水中Cr(VI)浓度的新方法。
技术实现要素:
为了提高Cr(VI)检测过程中的抗干扰能力、灵敏度和选择性,本发明提供了一种基于ABTS和Cr(VI)在强酸性条件下的显色反应来检测水中Cr(VI)浓度的方法,尤其是一种利用ABTS检测亚硫酸盐还原Cr(VI)过程中或者Cr(VI)与Co(II)共存时Cr(VI)浓度的方法。
本发明的目的是通过以下技术方案实现的:
本发明新检测方法技术方案概括为,通过ABTS和Cr(VI)在强酸性环境中的氧化还原反应,定量产生了绿色的ABTS自由基(ABTS·+),在ABTS·+浓度小于100μmol/L时,ABTS·+的吸光度与浓度的关系符合朗伯-比尔定律,在特征吸收峰处的吸光度与Cr(VI)的含量成线性关系,间接实现了对水中Cr(VI)的检测。
所选择的ABTS·+的特征吸收峰为415nm或649nm或732nm。
本发明技术方案的反应机理:
水溶液中的Cr(VI)主要以CrO42-、HCrO4-和Cr2O72-的形式存在,酸性溶液中Cr(VI)具有较高的氧化还原电位(E0(HCrO4-/Cr3+)=1.35VNHE),呈现较强的氧化性。而ABTS是一种还原剂,ABTS·+/ABTS的氧化还原电位为0.68V,ABTS容易发生电子转移,生成稳定的绿色自由基ABTS·+,ABTS·+在多个波长下有特征吸收峰。我们发现在酸性条件下,Cr(VI)与ABTS通过反应(1)发生氧化还原反应,定量生成ABTS·+,该自由基的吸光度在2小时内变化不超过1%。我们也通过多个试验证明了Cr(VI)与ABTS反应的化学计量关系为3:1,如图10所示(该图表示出不同Cr(VI)浓度时ABTS与其反应的化学计量比)。基于此原理,可通过检测加入Cr(VI)前后ABTS溶液在ABTS·+特征吸收峰处吸光度的变化来间接定量完成Cr(VI)的检测。
Cr(VI)+3ABTS→Cr(III)+3ABTS·+ (1)
基于上述方法技术方案,本发明ABTS的水中Cr(VI)含量的测定方法,通常可采用以下常规实施步骤操作:一、利用标准Cr(VI)溶液与ABTS反应所得到的ABTS·+在特征峰处的吸光度值制作标准曲线;二、测量加入待测水样前后ABTS·+在特征峰处的吸光度值;三、将步骤二测量值的差值代入到步骤一的标准曲线中,计算得出待测水样中Cr(VI)的含量。
具体详述如下:
步骤一:制作标准曲线:将一定量的ABTS母液和浓酸加入比色皿中,得混合液A,加入超纯水将混合液A稀释至一定体积,并测定稀释液中的ABTS·+在特征吸收峰处的吸光度值,记为a;向所得混合物A中加入相同体积不同浓度的Cr(VI)标准样,得混合物B,显色反应一定时间后,将混合物B稀释至一定体积,测定该稀释液中ABTS·+在特征峰处的吸光度值,记为b;以Cr(VI)标准样浓度为横坐标,以b与a的差值为纵坐标,建立标准曲线。其中,ABTS母液浓度为0.2-2.0mmol/L,Cr(VI)标准样浓度为0、0.025、0.05、0.10、0.15、0.20、0.25、0.50、1.00、1.5、2.00、2.50、3.60、4.80、6.40、8.00mg/L。ABTS母液、浓酸、超纯水与Cr(VI)标准样的体积比为1:(2.5-5.0):(0-12.0):(1.0-4.0)。
步骤二:将ABTS母液和浓酸加入比色皿中,得混合液C,加入超纯水将混合液C稀释至一定体积,并测定稀释液中的ABTS·+在特征吸收峰处的吸光度值,记为c;其中,ABTS母液、浓酸与超纯水的体积比为1:(2.5-5.0):(0-12.0)。
步骤三:向步骤二中所得的混合物C中加入待测的Cr(VI)水样进行显色反应,反应一定时间后,将混合物C稀释至一定体积,测定该稀释液中ABTS·+在特征峰处的吸光度值,记为d;其中,ABTS母液、浓酸、超纯水与Cr(VI)标准样的体积比为1:(2.5-5.0):(0-12.0):(1.0-4.0)。
步骤四:将步骤三和步骤二所得的d和c的差值带入到步骤一中所得的标准曲线公式中,计算得出待测水样中Cr(VI)的含量。
本发明方法简单易行,测定结果误差小,测定时间短,适用范围广,成本低。本发明适用于地表水、地下水以及工业废水中Cr(VI)浓度的检测。
本发明方法具有以下优越性:
(1)本发明使用的试剂为ABTS和浓酸溶液,试剂简单易得,安全无毒,且两种试剂均很稳定,ABTS母液在4℃环境中可稳定存在一个月,生成的ABTS·+也可以稳定存在数小时,可提供充足的Cr(VI)检测时间。
(2)本发明步骤简单,与传统的二苯碳酰二肼分光光度法相比,显色时间由5-10min缩短至2min内;适用范围广,可适用于各种pH值的地表水、地下水或工业废水中浓度为0.025-8.00mg/L的Cr(VI)测定。
(3)本发明具有较高的灵敏性,Cr(VI)测量的灵敏度高达104M-1cm-1以上。
(4)本发明具有良好的抗干扰能力,高浓度的Co(II)离子以及还原去除Cr(VI)所用的亚硫酸盐均不会对本发明中Cr(VI)的检测造成干扰。
附图说明
图1为实施例一中制得的标准曲线;
图2为实施例二中制得的标准曲线;
图3为实施例三中制得的标准曲线
图4为实施例四中制得的标准曲线;
图5为实施例五中制得的标准曲线;
图6为实施例六中制得的标准曲线;
图7为实施例七中制得的标准曲线;
图8为实施例八中制得的标准曲线;
图9为实施例九中制得的标准曲线;
图10表示不同Cr(VI)浓度时ABTS与其反应的化学计量比。
具体实施方式
本发明涉及一种基于ABTS(2,2’-联氮-双(3-乙基苯并噻唑啉-6-磺酸))和六价铬(Cr(VI))在强酸性环境中的显色反应来检测水中Cr(VI)浓度的方法,尤其涉及一种利用ABTS检测亚硫酸盐还原Cr(VI)过程中或者Cr(VI)与二价钴离子(Co(II))共存时Cr(VI)浓度的方法。本方法不仅可以用于地表水、地下水中Cr(VI)浓度的检测,也可以用于含铬矿石加工、电镀、制革、颜料制造等行业产生的高浓度工业废水中Cr(VI)浓度的检测。
以下结合实施例和附图,进一步介绍本发明。以下各个实施例中对吸光度值的确定,都是控制在2小时内完成的。
实施例一
本实施例是10mL比色管中,使用1cm比色皿完成的,具体步骤如下:
步骤一:制作标准曲线:将1.0mL浓度为0.2mmol/L的ABTS母液和5.0mL浓盐酸加入10mL比色管中,得混合液A,加入4.0mL超纯水将混合液A稀释至10mL,并使用1cm比色皿测定稀释液中的ABTS·+在415nm处的吸光度值,记为a;向所得混合物A中加入4.0mL Cr(VI)标准样,其浓度分别为0、0.025、0.05、0.10、0.15、0.20、0.25mg/L,得10mL混合物B,对混合物B进行显色反应2min后,使用1cm比色皿测定其中的ABTS·+在415nm处的吸光度值,记为b;以Cr(VI)标准样浓度为横坐标,以b与a的差值为纵坐标,建立标准曲线,标准曲线的方程为bi-ai=nCi,其中i为标准样品号,Ci是第i个标准样品的浓度,n是标准曲线的斜率。
步骤二:将1.0mL浓度为0.2mmol/L的ABTS母液和5.0mL浓盐酸加入10mL比色管中,得混合液C,加入4.0mL超纯水将混合液C稀释至10mL,并测定稀释液中的ABTS·+在415nm处的吸光度值,记为c。
步骤三:向步骤二中所得的混合物C中加入待测的Cr(VI)水样4.0mL对混合物C中的ABTS进行显色反应,反应2min后,使用1cm比色皿测定该混合液中ABTS·+在特征峰处的吸光度值,记为d。
步骤四:将步骤三和步骤二所得的d和c的差值带入到步骤一中所得的标准曲线公式中,计算得出待测水样中Cr(VI)的含量为(d-c)/n。
以上a,b,c,d的值均小于2。
标准曲线见图1。
实施例二
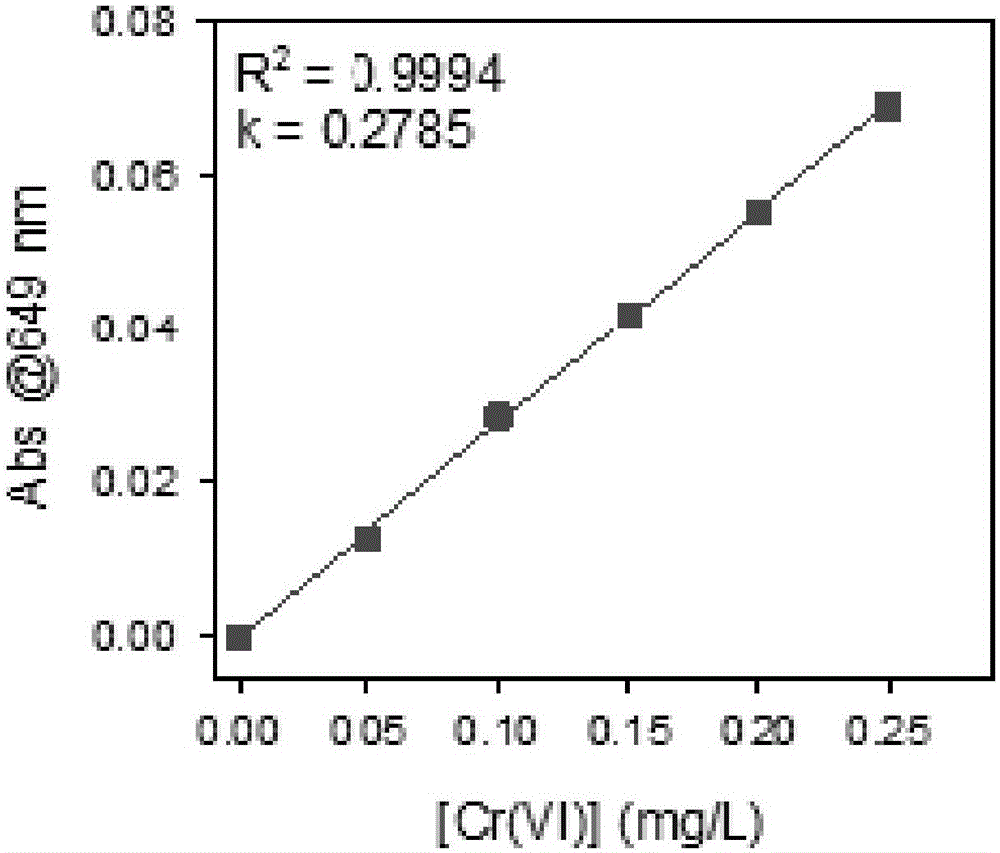
本实施例与实施例一不同的是吸光度的检测是在649nm处完成的。
标准曲线见图2。
实施例三
本实施例与实施例一不同的是吸光度的检测是在732nm处完成的。
标准曲线见图3。
实施例四
本实施例是10mL比色管中,使用1cm比色皿完成的,具体步骤如下:
步骤一:制作标准曲线:将1.0mL浓度为1.0mmol/L的ABTS母液和2.5mL浓硝酸加入10mL比色管中,得混合液A,加入6.5mL超纯水将混合液A稀释至10mL,并使用1cm比色皿测定稀释液中的ABTS·+在415nm处的吸光度值,记为a;向所得混合物A中加入1.0mL Cr(VI)标准样,其浓度分别为0.0、0.25、0.50、1.00、1.50、2.00、2.50mg/L,得混合物B,对混合物B进行显色反应2min后,加入5.5mL超纯水将其稀释至10mL,使用1cm比色皿测定该稀释液中ABTS·+在415nm处的吸光度值,记为b;以Cr(VI)标准样浓度为横坐标,以b与a的差值为纵坐标,建立标准曲线,标准曲线的方程为bi-ai=nCi,其中i为标准样品号,Ci是第i个标准样品的浓度,n是标准曲线的斜率。
步骤二:将1.0mL浓度为1.0mmol/L的ABTS母液和2.5mL浓硝酸加入10mL比色管中,得混合液C,加入6.5mL超纯水将混合液C稀释至10mL,并使用1cm比色皿测定稀释液中的ABTS·+在415nm处的吸光度值,记为c。
步骤三:向步骤二中所得的混合物C中加入待测的Cr(VI)水样1.0mL对混合物C中的ABTS进行显色反应,反应2min后,加入5.5mL超纯水将其稀释至10mL,使用1cm比色皿测定该混合液中ABTS·+在特征峰处的吸光度值,记为d。
步骤四:将步骤三和步骤二所得的d和c的差值带入到步骤一中所得的标准曲线公式中,计算得出待测水样中Cr(VI)的含量为(d-c)/n。
标准曲线见图4。
实施例五
本实施例与实施例四不同的是吸光度的检测是在649nm处完成的。
标准曲线见图5。
实施例六
本实施例与实施例四不同的是吸光度的检测是在732nm处完成的。
标准曲线见图6。
实施例五
本实施例是50mL比色管中,使用5cm比色皿完成的,具体步骤如下:
步骤一:制作标准曲线:将2.5mL浓度为2.0mmol/L的ABTS母液和12.5mL浓盐酸加入50mL比色管中,得混合液A,加入35.0mL超纯水将混合液A稀释至50mL,并使用5cm比色皿测定稀释液中的ABTS·+在415nm处的吸光度值,记为a;向所得混合物A中加入5.0mL Cr(VI)标准样,其浓度分别为0.0、1.20、2.40、3.60、4.80、6.40、8.00mg/L,得混合物B,对混合物B进行显色反应2min后,加入30.0mL超纯水将其稀释至50mL,使用5cm比色皿测定该稀释液中ABTS·+在415nm处的吸光度值,记为b;以Cr(VI)标准样浓度为横坐标,以b与a的差值为纵坐标,建立标准曲线,标准曲线的方程为bi-ai=nCi,其中i为标准样品号,Ci是第i个标准样品的浓度,n是标准曲线的斜率。
步骤二:将2.5mL浓度为2.0mmol/L的ABTS母液和12.5mL浓盐酸加入50mL比色管中,得混合液C,加入35.0mL超纯水将混合液C稀释至50mL,并使用5cm比色皿测定稀释液中的ABTS·+在415nm处的吸光度值,记为c。
步骤三:向步骤二中所得的混合物C中加入待测的Cr(VI)水样5.0mL对混合物C中的ABTS进行显色反应,反应2min后,用30.0mL超纯水将其稀释至50mL,使用5cm比色皿测定该稀释液中ABTS·+在特征峰处的吸光度值,记为d。
步骤四:将步骤三和步骤二所得的d和c的差值带入到步骤一中所得的标准曲线公式中,计算得出待测水样中Cr(VI)的含量为(d-c)/n。
标准曲线见图7。
实施例八
本实施例与实施例七不同的是吸光度的检测是在649nm处完成的。
标准曲线见图8。
实施例九
本实施例与实施例七不同的是吸光度的检测是在732nm处完成的。
标准曲线见图9。
综上各个实施例,本发明本质上公开的是一种在强酸性环境中Cr(VI)会氧化ABTS(2,2’-联氮-双(3-乙基苯并噻唑啉-6-磺酸))生成ABTS·+的显色反应来检测水中Cr(VI)浓度的方法,可以解决现有测定方法所使用得试剂挥发性强、毒性高、抗干扰能力差的问题。本发明可大大降低亚硫酸盐还原Cr(VI)过程中的亚硫酸盐对Cr(VI)浓度检测的干扰及共存二价钴离子(Co(II))对Cr(VI)浓度检测的干扰。
- 还没有人留言评论。精彩留言会获得点赞!