一种微流控纸芯片及化学发光免疫检测方法与流程
本发明涉及免疫检测领域,特别是涉及一种微流控纸芯片及化学发光免疫检测方法。
背景技术:
微流控纸芯片是近年来备受关注的一种快速检测、即时诊断分析器件,具有广阔的应用前景。微流控纸芯片是以纸作为制作材料,用一定的技术手段在纸上形成亲水和疏水相间的区域,并集成了进样、反应、检测等基本操作单元。由于它具有重量轻、成本低廉、生物相容性好、一次性便携式分析、操作简便、所需样品的体积小、分析速度快、可以进行多种物质同时检测等优点,己经被越来越多地应用于临床检测、环境监控、食品安全分析等领域。
微流控纸芯片的研究工作主要集中于芯片制作方法和芯片检测技术上。常见的微流控纸芯片制作方法包括光刻法、蜡印法、喷墨打印法、绘图法、等离子蚀刻法、柔印等。微流控纸芯片上生物大分子通常利用免疫反应进行检测,靠抗原与抗体特异性结合而建立的高选择性生物化学方法,而化学发光免疫分析技术最新发展起来的一项免疫测定技术,具有高灵敏性和高特异性的特点。将微流控纸芯片实验室与化学发光免疫分析方法结合后,具有成本低、操作简单、特异性强、灵敏度高、线性范围宽、检测快速等特点。
现有的微流控纸芯片用于免疫反应检测时,需要在每个测试点上分别进行多步洗涤分离操作,繁琐费时。
技术实现要素:
本发明的目的是提供一种微流控纸芯片,通过进样层和吸水层围绕各自转轴旋转,进而与检测层对齐形成亲水通道,化学发光免疫分析检测时,在进样层进样口上统一滴加缓冲溶液和显色液,通过不同的旋转及操作,可以完成纸芯片上免疫分析检测,减少滴加时的繁复操作,以解决现有微流控纸芯片免疫分析检测时每个测试点上分别进行多步洗涤分离操作,繁琐费时的问题。
为实现上述目的,本发明提供了如下方案:
一种微流控纸芯片,所述微流控纸芯片包括:进样层、检测层、吸水层、转轴和转轴孔;所述进样层包括进样口、通道和交换口;所述检测层包括第一进样观察孔和反应池;所述吸水层包括第二进样观察孔和吸水区;所述进样口、所述第一进样观察孔和所述第二进样观察孔直径相同;当所述进样口、所述第一进样观察孔和所述第二进样观察孔重合时,所述交换口、所述反应池和所述吸水区位置对应重合;所述进样层包括第一进样层和第二进样层;所述转轴包括第一转轴和第二转轴,所述进样层的转轴孔位于所述进样层的一端,所述检测层的转轴孔位于所述检测层的两端,所述吸水层的转轴孔位于所述吸水层的一端;所述第一转轴通过转轴孔从上至下依次连接所述第一进样层的一端、所述检测层的一端和所述第二进样层的一端;所述第二转轴通过转轴孔从上至下依次连接所述检测层的另一端和所述吸水层的一端,所述吸水层位于所述第二进样层的下方。
可选的,所述进样层包括疏水区和亲水区,所述疏水区由蜡打印后融化形成,所述亲水区由所述进样口、所述通道和所述交换口组成。
可选的,所述检测层包括疏水区和亲水区,所述疏水区由蜡打印后融化形成,所述亲水区由所述第一进样观察孔和所述反应池组成。
可选的,所述检测区的反应池个数大于1。
可选的,所述吸水层包括疏水区和亲水区,所述疏水区由蜡打印后融化形成,所述亲水区由所述第二进样观察孔和吸水区组成。
可选的,所述转轴采用鸡眼铆钉。
一种化学发光免疫检测方法,所述方法包括:
将微流控纸芯片的进样层和吸水层旋转至检测层两侧,使所述进样层和所述检测层不重叠、所述检测层和所述吸水层不重叠,所述微流控纸芯片包括:进样层、检测层、吸水层、转轴和转轴孔;所述进样层包括进样口、通道和交换口;所述检测层包括第一进样观察孔和反应池;所述吸水层包括第二进样观察孔和吸水区;所述进样口、所述第一进样观察孔和所述第二进样观察孔直径相同;当所述进样口、所述第一进样观察孔和所述第二进样观察孔重合时,所述交换口、所述反应池和所述吸水区位置对应重合;所述进样层包括第一进样层和第二进样层;所述转轴包括第一转轴和第二转轴,所述进样层的转轴孔位于所述进样层的一端,所述检测层的转轴孔位于所述检测层的两端,所述吸水层的转轴孔位于所述吸水层的一端;所述第一转轴通过转轴孔从上至下依次连接所述第一进样层的一端、所述检测层的一端和所述第二进样层的一端;所述第二转轴通过转轴孔从上至下依次连接所述检测层的另一端和所述吸水层的一端,所述吸水层位于所述第二进样层的下方;
向所述检测层的反应池滴加抗原;
将所述第一进样层旋转至与所述检测层重合,并将所述吸水层旋转至与所述检测层重合,使得所述第一进样层的进样口与所述检测层的第一进样观察孔和所述吸水层的第二进样观察孔重合;
向所述第一进样层的进样口滴加缓冲液进行冲洗;
将微流控纸芯片的进样层旋转至所述检测层一侧,使所述进样层和所述检测层不重叠;
向所述检测层的反应池滴加抗体;
将所述第一进样层旋转至与所述检测层重合,并将所述吸水层旋转至与所述检测层重合,使得所述第一进样层的进样口与所述检测层的第一进样观察孔和所述吸水层的第二进样观察孔重合;
向所述第一进样层的进样口滴加缓冲液进行冲洗;
将所述第一进样层旋转至所述检测层一侧,使得所述第一进样层的进样口与所述检测层的第一进样观察孔不重合;并将所述第二进样层旋转至与所述检测层重合,使得所述第二进样层的进样口与所述检测层的第一进样观察孔重合;
通过所述第一进样观察孔向所述第二进样层的进样口滴加显色液;
在暗室拍摄所述检测层图片并分析所述图片的灰度;
根据所述图片的灰度计算所述抗原的浓度。
可选的,所述向所述检测层的反应池滴加抗原具体包括:
向第一反应池分别滴加已知不同浓度的标准抗原,向第二反应池滴加待检测抗原,所述第一反应池个数大于1,所述第二反应池个数大于等于1。
可选的,所述根据所述图片的灰度计算所述抗原的浓度具体包括:
首先根据所述已知不同浓度的标准抗原浓度与相应灰度关系得到标准曲线;
然后根据待检测抗原的灰度利用所述标准曲线计算出待检测抗原浓度。
以上方法步骤不固定于一种执行顺序,可根据实验需要调换顺序。
根据本发明提供的具体实施例,本发明的有益效果为:
通过微流控纸芯片的结构设计,进样层和吸水层围绕各自转轴旋转,进而与检测层对齐形成亲水通道,化学发光免疫分析检测时,在进样层进样口上统一滴加缓冲溶液和显色液,通过不同的旋转及操作,可以完成纸芯片上免疫分析检测,减少了滴加时的繁复操作。在检测层上设置多个反应池,可以分别滴加抗原标品和检测样品,实现同时检测以便制作标准曲线,增加了检测的准确性。本发明应用于生物分子(如肿瘤、心梗、肝炎指标标志物等)的免疫反应检测中,能够更快速准确完成相关指标检测。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动性的前提下,还可以根据这些附图获得其他的附图。
图1为本发明微流控纸芯片结构图;
图2为本发明化学发光免疫检测实施例1得到的检测结果图;
图3为本发明化学发光免疫检测实施例2得到的检测结果图。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
为使本发明的上述目的、特征和优点能够更加明显易懂,下面结合附图和具体实施方式对本发明作进一步详细的说明。
图1为本发明微流控纸芯片结构图。图1(Ⅰ)为微流控纸芯片组装图,图1(Ⅱ)为微流控纸芯片分解图。微流控纸芯片由whatman 1号层析纸喷蜡打印后110℃烘干0.5min后形成疏水区和亲水区,进而组装而成。如图1所示,所述微流控纸芯片包括:进样层101和103,检测层102,吸水层104、105和106,转轴107。其中进样层101与进样层103完全相同,吸水层104、105、106完全相同。
由于进样层101与进样层103完全相同,以进样层103为例进行说明,进样层103包括疏水区、亲水区和转轴孔,疏水区由蜡打印后融化形成,其亲水区由进样口1031、通道1032和交换口1033组成,进样口直径10-15mm,通道宽度2-4mm,通道长度5-20mm,交换口直径5mm,可以在进样口1031上统一滴加缓冲溶液或显色液,减少滴加时的繁复操作,滴加后液体沿通道1032流动,并通过交换口1033到达检测层102的检测区,在进样层103的一侧有一个转轴孔,在微流控纸芯片中用转轴107,转轴107可以采用鸡眼铆钉。
检测层102包括疏水区、亲水区、进样观察孔1021和转轴孔,疏水区由蜡打印后融化形成,其亲水区由多个反应池1022组成,反应池1022数量不定,一般大于5个,可以按需要设计,反应池1022直径5mm,可以在其上滴加抗原和抗体,是化学发光免疫分析反应的区域,进样观察孔1021在进样层上按设计剪裁得到,进样观察孔1021直径10-15mm,与进样层进样孔1031直径一致,转轴孔在检测层102两侧各有一个,在微流控纸芯片中转轴通过一端转轴孔固定进样层101、103与检测层102,通过另一端转轴孔固定吸水层104、105、106与检测层102。
由于吸水层104、105、106完全相同,以吸水层106为例进行说明。吸水层106包括疏水区、亲水区和进样观察孔1061,疏水区由蜡打印后融化形成,疏水区的疏水坝可以阻挡来自不同检测层反应池的废液混合,避免干扰污染,其亲水区为吸水区1063,转轴孔1062在吸水层一侧,洗涤分离时吸水层与检测层102贴合对齐,吸水区1063吸收通过检测层反应池1022的废液,在微流控纸芯片中转轴固定吸水层104、105、106与检测层102。
微流控纸芯片组装时,转轴通过转轴孔从上至下依次组装进样层101、检测层102(通过检测层其中一侧转轴孔)、进样层103,检测层102在中间,进样层101、103可以围绕转轴旋转,另一转轴通过转轴孔依次从上至下依次组装检测层102(通过检测层另一侧转轴孔)和吸水层104、105、106,吸水层数量可以根据检测操作步骤灵活增减,吸水层在进样层103下方,并可以围绕转轴旋转。当进样层101、103的进样口、检测层102的进样观察孔1021和吸水层104、105、106的进样观察孔重合时,进样层101、103的交换口、检测层102的反应池1022和吸水层104、105、106的吸水区位置对应重合。其中转轴可以采用鸡眼铆钉。
本发明化学发光免疫检测方法,实施方式可以为:
当向检测层滴加抗原或抗体时,将微流控纸芯片的进样层和吸水层旋转至检测层两侧,使进样层和检测层不重叠、检测层和吸水层不重叠,进样层包括第一进样层和第二进样层,第一进样层位于所述检测层上方,第二进样层位于检测层下方,吸水层位于第二进样层下方;吸水层的数量根据实验需要可增减;然后向检测层的反应池根据使用要求滴加抗原或抗体,检测层的反应池有多个,一般大于5个,其中一部分用来添加不同浓度的标准抗原,另一部分用来添加待检测抗原,抗体可以采用辣根过氧化物酶(Horseradish Peroxidase,HRP)标记的抗体。
当洗涤分离时,将第一进样层(缓冲液进样层)旋转至与检测层重合,并将吸水层旋转至与检测层重合,使得第一进样层(缓冲液进样层)的进样口与检测层的进样观察孔和吸水层的进样观察孔重合;然后向缓冲液进样层的进样口滴加缓冲液进行冲洗,冲洗后撕掉用过的所述吸水层。
当发光反应测定时,将缓冲液进样层旋转至检测层一侧,使得缓冲液进样层的进样口与检测层的进样观察孔不重合;并将第二进样层(显色液进样层)旋转至与检测层重合,将另一吸水层旋转至与检测层重合,使得显色液进样层的进样口与检测层的进样观察孔和吸水层的进样观察孔重合;通过检测层的进样观察孔向显色液进样层的进样口滴加显色液。
然后在暗室拍摄检测层图片并分析图片的灰度,根据图片的灰度计算所述抗原的浓度。
本发明免疫检测实施例1:CRP间接法ELISA实验
(CRP:C反应蛋白(C-reactive protein,CRP);ELISA:酶联免疫吸附测定法(enzyme-linked immunosorbent assay,ELISA))
按图1(Ⅰ)微流控纸芯片结构图喷蜡打印whatman 1号层析纸后110℃烘干0.5min,剪裁后按图1(Ⅱ)所示组装微流控纸芯片。
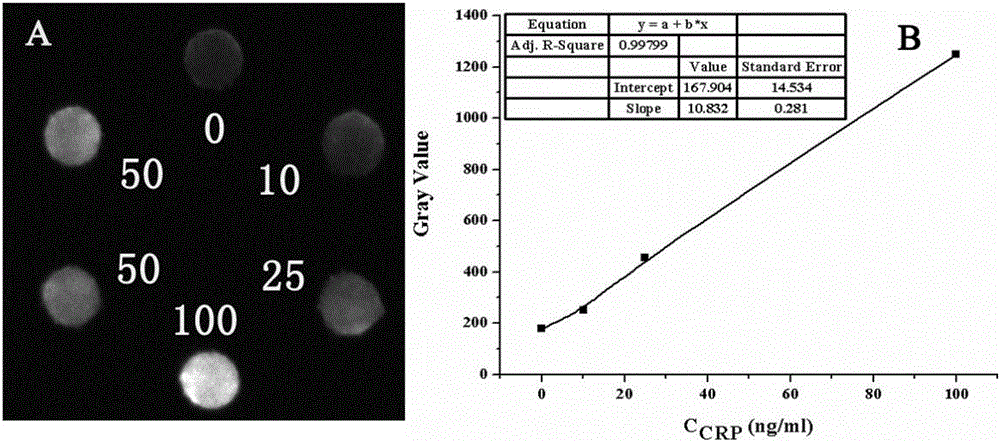
首先将进样层与吸水层全部旋转至检测层两侧,向预先包被捕获抗体和用封闭缓冲液封闭好的检测层6个反应池各滴加5μl CRP不同浓度的标准样品(100ng/ml、50ng/ml、50ng/ml、25ng/ml、10ng/ml、0ng/ml),其中100ng/ml、25ng/ml、10ng/ml、0ng/ml为CRP标线浓度,50ng/ml、50ng/ml为检测样品浓度,室温放置10min;
旋转检测层上面的进样层(称之为缓冲液进样层)与检测层对齐,旋转检测层下部的吸水层与检测层对齐,向进样层进样口每次滴加200μl缓冲液冲洗两次,冲洗后撕掉用过的吸水层,旋转缓冲液进样层至检测层一侧,;
向检测层各反应池滴加5μl生物素标记的检测抗体,室温放置5min;
旋转检测层上面的缓冲液进样层与检测层对齐,旋转另一个吸水层至与检测层下层对齐,向进样层进样口每次滴加200μl缓冲液冲洗两次,冲洗后撕掉用过的吸水层,旋转缓冲液进样层至检测层一侧;
向检测层各反应池滴加5μl HRP标记的亲和素,室温放置5min;
旋转检测层上面的缓冲液进样层与检测层对齐,旋转一个吸水层至于检测层下层对齐,向进样层进样口每次滴加200μl缓冲液冲洗两次,冲洗后撕掉用过的吸水层和缓冲液进样层;
最后检测层下方进样层(称之为发光液进样层)与检测层对齐,并通过检测层进样观察口向发光液进样层进样口滴加500μl显色液,1min后,在暗室用CCD拍摄图片并分析灰度,首先根据标准样品浓度与灰度关系得到标准曲线;然后根据检测样品的灰度利用所述标准曲线计算出检测样品浓度。
图2为本发明免疫检测实施例1得到的检测结果图。如图2所示,A图为免疫分析化学发光图片,B为免疫分析标准曲线。多张纸芯片检测计算结果如表1所示:
表1
本发明免疫检测实施例2:小鼠IgG间接法ELISA实验
(IgG:免疫球蛋白G(Immunoglobulin G,IgG))
按图1(Ⅰ)微流控纸芯片结构图喷蜡打印whatman 1号层析纸后110℃烘干0.5min,剪裁后按图1(Ⅱ)所示组装微流控纸芯片。
将进样层与吸水层旋转至检测层两侧,在检测层反应池分别滴加4μl不同浓度的(20μg/ml、10μg/ml、10μg/ml、5μg/ml、1μg/ml、0μg/ml)小鼠IgG,其中20μg/ml、5μg/ml、1μg/ml、0μg/ml为样品标线浓度,10μg/ml、10μg/ml为检测样品浓度,室温放置10min;
旋转检测层上面的缓冲液进样层与检测层对齐,旋转检测层下部的吸水层与检测层对齐,向进样层进样口每次滴加200μl缓冲液冲洗两次,冲洗后撕掉用过的吸水层,旋转缓冲液进样层至检测层一侧;
向检测层各反应池滴加10μl封闭缓冲液,室温放置10min;
旋转检测层上面的缓冲液进样层与检测层对齐,旋转另一个吸水层至与检测层下层对齐,向进样层进样口每次滴加200μl缓冲液冲洗两次,冲洗后撕掉用过的吸水层,旋转缓冲液进样层至检测层一侧;
向检测层各反应池滴加5μl anti-mousuIgG HRP抗体,室温放置10min;
旋转检测层上面的缓冲液进样层与检测层对齐,旋转一个吸水层至于检测层下层对齐,向进样层进样口每次滴加200μl缓冲液冲洗两次,冲洗后撕掉用过的吸水层和缓冲液进样层;
旋转检测层下部发光液进样层与检测层对齐,并通过检测层进样观察口向进样层进样口滴加500μl显色液,1min后,在暗室用CCD拍摄图片并分析灰度,首先根据标准样品浓度与灰度关系得到标准曲线;然后根据检测样品的灰度利用所述标准曲线计算出检测样品浓度。
图3为本发明免疫检测实施例2得到的检测结果图。如图3所示,A图为免疫分析化学发光图片,B为免疫分析标准曲线。多张纸芯片检测计算结果如表2所示:
表2
本说明书中各个实施例采用递进的方式描述,每个实施例重点说明的都是与其他实施例的不同之处,各个实施例之间相同相似部分互相参见即可。对于实施例公开的系统而言,由于其与实施例公开的方法相对应,所以描述的比较简单,相关之处参见方法部分说明即可。
本文中应用了具体个例对本发明的原理及实施方式进行了阐述,以上实施例的说明只是用于帮助理解本发明的方法及其核心思想;同时,对于本领域的一般技术人员,依据本发明的思想,在具体实施方式及应用范围上均会有改变之处。综上所述,本说明书内容不应理解为对本发明的限制。
- 还没有人留言评论。精彩留言会获得点赞!