一种检测福莫特罗的酶联免疫试剂盒及其制备方法与应用与流程
本发明涉及一种检测福莫特罗的酶联免疫试剂盒及其制备方法与应用,其特别适于动物组织中福莫特罗残留的检测,属于免疫学技术领域和兽药残留分析技术领域。
背景技术:
福莫特罗(Formoterol)是由日本山之内制药株式会社中央研究所开发的第三代β2-肾上腺素受体激动剂平喘药物,具有支气管扩张作用,还有抗过敏和抑制水肿的作用,可用于治疗慢性支气管哮喘、夜间哮喘、运动性哮喘、慢性阻塞性肺病以及儿童非哮喘性呼吸道疾病。近年来,随着我国对食品安全监管力度的加强,对违禁使用兽药的监管力度逐渐加大,滥用违禁兽药的现象有所控制,但是出现了使用生物活性相似的替代品代替重点监管兽药的新现象。新型“瘦肉精”福莫特罗与克伦特罗等三种常用“瘦肉精”物质具有同样的促进生长、增加瘦肉率的作用,2002年农业部1519号条例规定食品动物禁止使用β激动剂类药物作为饲料添加剂。福莫特罗检测手段滞后,尤其是快速检测产品缺乏,国家及各省市正在加紧建立新型“瘦肉精”物质的确证方法,同时也急需适合批量、快速筛选的检测产品,满足政府和企业的需要。
目前有关福莫特罗残留的检测技术主要有高效液相色谱法(HPLC)、液相色谱-质谱联用法(LC-MS)、液相色谱串联质谱法(LC-MS/MS)及免疫分析技术,前三种方法灵敏、准确,但操作繁琐,对实验设备和技术要求较高,不适合大批量样品的快速检测。免疫分析方法包括酶联免疫吸附法(ELISA)和胶体金免疫层析法(GICA),具有灵敏度高、特异性好、成本低、操作方便等特点,适于大批量样品筛选。开发福莫特罗免疫分析方法有助于福莫特罗残留快速、准确的检测,有效遏制其在水产品中的违规使用及残留超标问题,提高人民群众水产品餐桌质量安全水平。
技术实现要素:
本发明所要解决的技术问题是克服现有技术缺陷提供一种检测福莫特罗的酶联免疫试剂盒,该酶联免疫试剂盒具有灵敏度、精密度、准确度高,交叉反应率高,稳定性好储存时间长,操作简单,快速,适合大批量样品初筛的优点。此外,本发明进一步提供该检测福莫特罗的酶联免疫试剂盒的制备方法与应用。
本发明所述技术问题是由以下技术方案实现的。
一种检测福莫特罗的酶联免疫试剂盒,该酶联免疫试剂盒由包被有福莫特罗抗原的酶标板、抗福莫特罗单克隆抗体、酶标记物、福莫特罗标准品溶液、底物显色液、终止液、浓缩洗涤液、样本复溶液组成。
上述酶联免疫试剂盒,福莫特罗单克隆抗体为鼠源单克隆抗体,由CCTCC NO:C2016182的杂交瘤细胞株Formoterol-3E6产生,该杂交瘤细胞株被命名为杂交瘤细胞株Formoterol-3E6,于2016年10月26日送交中国典型培养物保藏中心(CCTCC)保藏,保藏号为CCTCC NO:C2016182。
上述酶联免疫试剂盒,所述福莫特罗单克隆抗体由福莫特罗抗原产生,该福莫特罗抗原为由福莫特罗与载体蛋白采用碳化二亚胺法合成的偶联物,包括免疫原与检测原;所述载体蛋白为牛血清白蛋白、鼠血清白蛋白、免疫血清蛋白、甲状腺蛋白、卵清蛋白、血蓝蛋白或人血清白蛋白,免疫原优选载体为牛血清白蛋白,检测原优选载体为卵清蛋白;所述酶标记物为酶标记抗原、酶标记抗体或酶标记抗抗体;所述酶标记物中的标记酶为辣根过氧化物酶或碱性磷酸酯酶;。
上述酶联免疫试剂盒,所述福莫特罗单克隆抗体为鼠源、马源、羊源、兔源或豚鼠源抗体,优选福莫特罗鼠源单克隆抗体;其由福莫特罗抗原免疫得到。
上述酶联免疫试剂盒,所述酶标记抗抗体为酶标记羊抗鼠抗抗体,其采用碘酸钠法将标记酶与山羊抗鼠抗抗体偶联得到。
为了方便现场监控和大量样本筛查,所述酶联免疫试剂盒还包括福莫特罗标准液、底物显色液、终止液、浓缩洗涤液、样本复溶液,且均以工作液形式提供。
上述酶联免疫试剂盒,所述福莫特罗标准品溶液的浓度分别为0μg/L、0.1μg/L、0.3μg/L、0.9μg/L、2.7μg/L、8.1μg/L;所述底物显色液由底物A和底物B组成,底物A为过氧化氢或过氧化脲,底物B为邻苯二胺或四甲基联苯胺,底物A和底物B按体积比1:1混混合均匀;所述终止液为1-2mol/L的硫酸溶液;所述浓缩洗液为含有1%吐温-20的0.2mol/L PH7.4的磷酸缓冲液;所述样本复溶液为含有0.1-5%脱脂奶粉的0.02mol/L PH7.4的磷酸缓冲液。
本发明所述的酶联免疫试剂盒制备方法,包括如下步骤:
(1)制备福莫特罗抗原工作液:
(a)活化对氨基苯甲酸的制备:称取6mg亚硝酸钠,溶在0.35mL蒸馏水中,然后称取10mg对氨基苯甲酸,溶入1.1mL 1mol/L的盐酸中,冰浴搅拌,将上述亚硝酸钠溶液逐滴加入到对氨基苯甲酸溶液中,避光反应1h,得到活化对氨基苯甲酸;
(b)带有羧基的福莫特罗活性中间体的制备:称取福莫特罗30mg溶在5mL、0.05mol/L冰冷的硼砂缓冲溶液中(pH=9,含0.15mol/L的氯化钠),冰浴搅拌,将此溶液逐滴加入到活化对氨基苯甲酸溶液中,4℃避光反应3h,得到带有羧基的福莫特罗活性中间体溶液;
(c)免疫原的合成:在上述带有羧基的福莫特罗活性中间体溶液中加入0.1mol/LNaOH调pH至7.4,将EDC 140mg、NHS 60mg溶解在2mL PBS中,少量多次加到溶液中室温搅拌3h。称取BSA 200mg溶解在1mL 0.01mol/L的PBS中,边搅拌边加入上述溶液中,反应过夜后,将偶联物溶液转移至透析袋,在PBS缓冲液中4℃透析72h,然后改用蒸馏水4℃透析48h,每天换液2次。透析后的溶液于6000rmp离心30min,取上清-20℃保存。标记为Formoterol-BSA;
(d)检测原的合成:在上述带有羧基的福莫特罗活性中间体溶液中加入0.1mol/LNaOH调pH至7.4,将EDC 140mg、NHS 60mg溶解在2mL PBS中,少量多次加到溶液中室温搅拌3h。称取OVA150mg溶解在1mL0.01mol/L的PBS中,边搅拌边加入上述溶液中,反应过夜后,将偶联物溶液转移至透析袋,在PBS缓冲液中4℃透析72h,然后改用蒸馏水4℃透析48h,每天换液2次。透析后的溶液于6000rmp离心30min,取上清-20℃保存。标记为Formoterol-OVA。
(2)制备包被有福莫特罗抗原的酶标板:
(a)用包被缓冲液将福莫特罗抗原溶液稀释成0.25mg/ml,100ul/孔加入到酶标板孔内;
(b)4℃过夜或37℃孵育2h,倾去孔中液体,洗涤液洗涤4-5次,拍干;
(c)加入含有10%小牛血清的封闭液缓冲液,200ul/孔,37℃孵育2h;
(d)倾去孔中液体,拍干,室温在真空干燥箱中抽干5h,用铝箔袋真空塑封,即得包被有福莫特罗抗原的酶标板;
其中,所述包被缓冲液为pH9.6的0.05mol/L的碳酸盐缓冲液,封闭缓冲液为10%的小牛血清溶液;
(3)制备福莫特罗单克隆抗体工作液:
(a)动物免疫:选择载体蛋白为牛血清白蛋白的免疫原,免疫6-8周龄的雌性Balb/c小鼠,间隔2周免疫1次,3次免疫后断尾取血测定效价和抑制率,选择结果最佳的小鼠准备融合;
(b)细胞融合:取步骤(a)选定的小鼠的脾细胞和小鼠骨髓瘤SP2/0细胞进行融合,间接ELISA法测定上清液选取阳性高的孔,通过有限稀释法对阳性孔进行亚克隆,直至建立产生单一抗福莫特罗的单克隆抗体的杂交瘤细胞株;
(c)单克隆抗体的大量制备:选取个体较大的雌性Balb/c小鼠,采用体内诱生腹水法,大量制备腹水,并通过辛酸-硫酸铵沉淀纯化腹水,分成小管,-20℃保存,得福莫特罗单克隆抗体;
(d)单克隆抗体特性鉴定:对抗体的效价、亲和力、亚型等特性进行鉴定。
(4)制备酶标记物浓缩工作液:
(a)羊抗鼠抗抗体的制备:以羊为免疫动物,以鼠源抗体为免疫原免疫无病原体羊,得到羊抗鼠抗抗体;
(b)酶标记羊抗鼠抗抗体的制备:将辣根过氧化物酶与羊抗鼠抗抗体采用碘酸钠法进行偶联;
(5)组建用于检测福莫特罗的酶联免疫试剂盒,包括下述各组分:
(a)包被有福莫特罗抗原的酶标板;
(b)福莫特罗单克隆抗体工作液;
(c)酶标记物:辣根过氧化物酶-羊抗鼠抗抗体;
(d)福莫特罗标准品溶液:采用梯度稀释法配制福莫特罗标准品溶液,1ml/瓶,浓度分别为0μg/L、0.1μg/L、0.3μg/L、0.9μg/L、2.7μg/L、8.1μg/L;
(e)底物显色液A液为过氧化脲溶液,底物显色液B液为四甲基联苯胺(TMB)溶液;
(f)终止液为1-2mol/L的硫酸溶液;
(g)浓缩洗涤液为含有1%吐温-20的0.2mol/L PH7.4的磷酸盐缓冲液;
(h)样本复溶液为含有0.1-5%脱脂奶粉的0.02mol/L PH7.4的磷酸缓冲液。
上述酶联免疫试剂盒在用于检测动物组织、尿液和饲料中福莫特罗的应用。
上述酶联免疫试剂盒在用于检测动物组织、尿液和饲料中福莫特罗的应用,包括如下步骤:
(1)样品前处理
(a)尿样:取尿样室温5000rpm离心5min,取上清100μL用样品稀释液稀释4倍,取上清进行检测;
(b)(肉类、肾脏、肝脏等)组织:称取肉样组织2.0g±0.05g,加入5mL乙酸乙酯,振荡1min,5000rpm离心10min;移取上层乙酸乙酯层溶液于另一离心管中,水相再用5mL乙酸乙酯重复萃取,合并有机相氮气吹干;加入1mL复溶工作液溶解,取50μL用于分析;
(c)饲料:称取饲料2.0g±0.05g,加入5mL乙酸乙酯,振荡1min,5000rpm离心10min;移取上层乙酸乙酯层溶液于另一离心管中,水相再用5mL乙酸乙酯重复萃取,合并有机相氮气吹干;加入1mL复溶工作液溶解,取50μL用于分析。
(2)使用试剂盒进行检测
取出所述检测福莫特罗残留的酶联免疫试剂盒,试剂恢复至室温(20-25℃),在室内放置30min以上;按需要取出板条,放置在酶标板上;按需要的量将福莫特罗单克隆抗体工作液和酶标记物工作液按5:1比例混合;向孔内依次加入标准品或待测样品50ul、福莫特罗单克隆抗体工作液和酶标记物工作液的混合液50ul,轻轻振荡混匀,25℃避光孵育30min;将孔内液体甩干,将洗涤工作液用去离子水将20×浓缩洗涤液20倍稀释后,250ul/孔,洗涤4次,拍干,;将显色液A和显色液B按体积比1:1比例混合,100ul/孔加入显色,25℃避光孵育15min;加终止液50ul终止反应,酶标仪450nm下采用双波长450nm/630nm测定,根据标准曲线进行定量或定性;
(3)分析检测结果
(a)定量分析:分别计算标准品和待测样本的平均吸光度值,标准品或待测样本的吸光度值(B)除以0μg/L标准品的吸光度值(B0)再乘以100%,即为百分吸光度值,百分吸光度值=(B/B0)×100%;以百分吸光度值为纵坐标,标准浓度的对数为横坐标,绘制标准曲线;将待测样本的百分吸光度值代入标准曲线,即可求出对应的浓度,再乘以稀释倍数即为样本的实际残留;
(b)定性分析:用待测样本的平均吸光度值和标准品的吸光度值相比较,即可得出待测样本的浓度范围,测试范围为0.1μg/mL-8.1μg/mL。
本发明所述的酶联免疫试剂盒检测原理为微孔条上包被有福莫特罗偶联抗原,当加入待测样本时,待测样本中福莫特罗与预包被的偶联抗原竞争福莫特罗特异性抗体,同时加入酶标物,显色后终止,吸光度值与待测样品中福莫特罗含量呈负相关。本发明所述的酶联免疫试剂盒的曲线范围在0.0975-6.25μg/L范围内;组织中福莫特罗回收率分别为94.66±6.04、83.92±6.65、78.62±6.70,批内变异系数均在9.48%以下,批间变异系数均在10.84%以下;尿液中福莫特罗回收率分别为96.43±6.43、85.51±6.24、82.10±6.41,批内变异系数均在10.26%以下,批间变异系数均在11.85%以下;饲料中福莫特罗回收率分别为78.48±6.46、81.06±5.44、84.85±6.69,批内变异系数均在7.81%以下,批间变异系数均在8.52%以下,符合《农业部文件》农医发[2005]17号文件中规定的试剂盒备案参考评判标准中的精密度和准确度规定。此外,通过测定福莫特罗类似物(苯乙醇胺A、沙丁胺醇、妥布特罗、盐酸克伦特罗、莱克多巴胺、西马特罗)及动物组织中常检的其他药物(氯霉素、四环素类、喹诺酮类、磺胺类)等几种药物的交叉反应率,福莫特罗的交叉反应率为100.00%,与其它几种相似物和常检药物无交叉反应;通过将酶联免疫试剂盒放置在2℃-8℃保存12个月,期间每隔1个月检测一次,测定试剂盒的IC50值、ODmax、回收率等各项参数,结果显示各参数均在正常范围内,同时将试剂盒放置在37℃和-20℃放置6天,每天检测一次,测定试剂盒的IC50%、ODmax、回收率等各项参数均在正常范围之内,因此,此试剂盒可以在2℃-8℃保存至少12个月。
附图说明
图1本发明所述福莫特罗单克隆抗体亲和力测定图
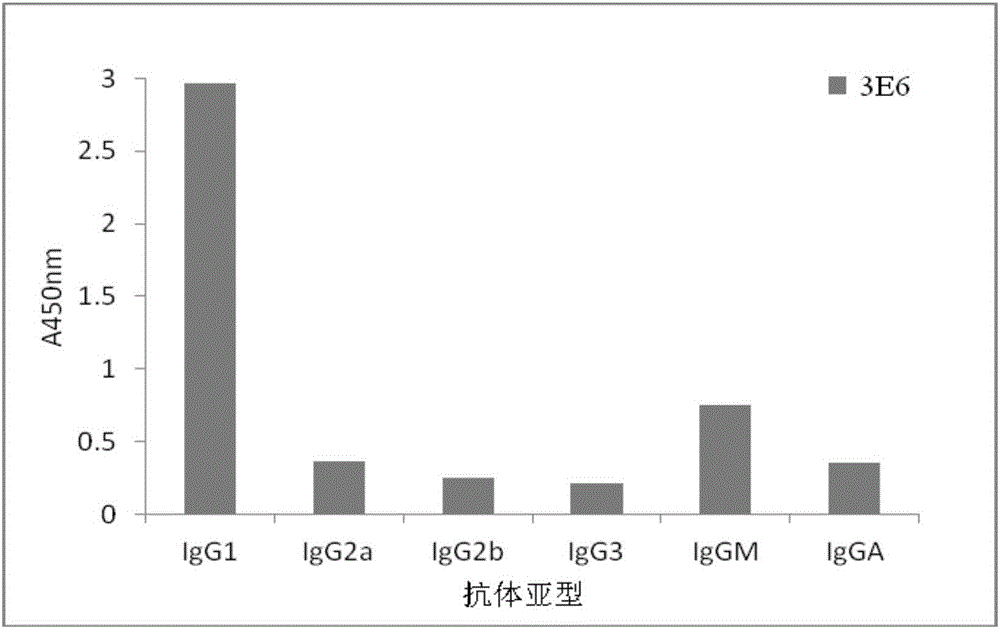
图2本发明所述福莫特罗单克隆抗体亚型测定图
图3本发明所述酶联免疫试剂盒的福莫特罗的标准曲线图
本发明所述的抗福莫特罗单克隆抗体的杂交瘤细胞株Formoterol-3E6,已于2016年10月26日送交中国典型培养物保藏中心(简称CCTCC,地址:武汉大学,中国典型培养物保藏中心,邮编:430072)保藏,保藏编号CCTCC NO:C2016182。
具体实施方式
下面结合具体的实例来进一步阐述本发明。应理解,这些实例仅用于说明本发明,而不用来限制本发明的范围。
下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
实施例一本发明所述福莫特罗抗原的制备
(1)活化对氨基苯甲酸的制备:称取6mg亚硝酸钠,溶在0.35mL蒸馏水中,然后称取10mg对氨基苯甲酸,溶入1.1mL 1mol/L的盐酸中,冰浴搅拌,将上述亚硝酸钠溶液逐滴加入到对氨基苯甲酸溶液中,避光反应1h,得到活化对氨基苯甲酸;
(2)带有羧基的福莫特罗活性中间体的制备:称取福莫特罗30mg溶在5mL、0.05mol/L冰冷的硼砂缓冲溶液中(pH=9,含0.15mol/L的氯化钠),冰浴搅拌,将此溶液逐滴加入到活化对氨基苯甲酸溶液中,4℃避光反应3h,得到带有羧基的福莫特罗活性中间体溶液;
(3)免疫原的合成:在上述带有羧基的福莫特罗活性中间体溶液中加入0.1mol/LNaOH调pH至7.4,将EDC 140mg、NHS 60mg溶解在2mL PBS中,少量多次加到溶液中室温搅拌3h。称取BSA 200mg溶解在1mL 0.01mol/L的PBS中,边搅拌边加入上述溶液中,反应过夜后,将偶联物溶液转移至透析袋,在PBS缓冲液中4℃透析72h,然后改用蒸馏水4℃透析48h,每天换液2次。透析后的溶液于6000rmp离心30min,取上清-20℃保存。标记为Formoterol-BSA;
(4)检测原的合成:在上述带有羧基的福莫特罗活性中间体溶液中加入0.1mol/LNaOH调pH至7.4,将EDC 140mg、NHS 60mg溶解在2mL PBS中,少量多次加到溶液中室温搅拌3h。称取OVA 150mg溶解在1mL 0.01mol/L的PBS中,边搅拌边加入上述溶液中,反应过夜后,将偶联物溶液转移至透析袋,在PBS缓冲液中4℃透析72h,然后改用蒸馏水4℃透析48h,每天换液2次。透析后的溶液于6000rmp离心30min,取上清-20℃保存。标记为Formoterol-OVA。
实施例二本发明所述包被有福莫特罗抗原的酶标板的制备
用PH9.6的碳酸盐缓冲液将福莫特罗抗原稀释成0.25mg/ml,100μL/孔加入到酶标板孔上,其中福莫特罗抗原包括免疫原、检测原,免疫原牛血清白蛋白为载体,检测原卵清蛋白为载体;4℃过夜或37℃孵育2h,洗涤4-5次,拍干;加入含有10%小牛血清的封闭缓冲液,200μL/孔,37℃孵育2h;室温在真空干燥箱中抽干5h,用铝箔袋真空塑封。
实施例三本发明所述福莫特罗单克隆抗体的制备
(1)动物免疫:载体蛋白为牛血清白蛋白的免疫原免疫6-8周龄的雌性Balb/c小鼠,间隔2周免疫1次,三免后断尾取血测定效价和抑制率,选择结果最佳的小鼠准备融合;
(2)细胞融合:取小鼠的脾细胞和小鼠骨髓瘤SP2/0细胞,进行融合,间接ELISA法测定上清选取阳性高的孔,通过有限稀释法对阳性孔进行亚克隆,直至建立产生单一抗福莫特罗的单克隆抗体的杂交瘤细胞株;
(3)单克隆抗体的大量制备:选取个体较大的雌性Balb/c小鼠,采用体内诱生腹水法,大量制备腹水,并通过辛酸-硫酸铵沉淀纯化腹水,分成小管,-20℃保存,得福莫特罗单克隆抗体。
实施例四本发明所述福莫特罗单克隆抗体特性鉴定
1、亲和力测定
采用非竞争酶联免疫法测定福莫特罗单克隆抗体的亲和常数,结果如图1所示,亲和常数Ka=7.24×108L/mol。
2、亚型测定
采用购自Sigma公司的鼠源单抗亚型鉴定试剂盒进行亚型测定,结果见图2所示,福莫特罗单克隆抗体亚型为IgG1。
3、效价测定
以1:40000稀释包被原包被检测板,将纯化后的单克隆抗体进行1:2000,1:4000,
1:8000,……1:1024000稀释,加入到酶标板孔内,反应后加入HRP标记的羊抗鼠二抗,最后用TMB显色,结果显示纯化后的福莫特罗单克隆抗体浓度为1mg/mL时的效价达1:512000。
实施例五本发明所述酶标记羊抗鼠抗抗体的制备
羊抗鼠抗抗体的制备:以羊为免疫动物,以鼠源抗体为免疫原免疫无病原体羊,得到羊抗鼠抗抗体;
酶标记羊抗鼠抗抗体(酶标记抗抗体)的制备:将辣根过氧化物酶与羊抗鼠抗抗体采用碘酸钠法进行偶联。
实施例五本发明所述用于检测福莫特罗的酶联免疫试剂盒的组建
组建福莫特罗酶联免疫检测试剂盒,包括下述各组分:
(1)包被有福莫特罗抗原的酶标板;
(2)福莫特罗单克隆抗体工作液;
(3)酶标记抗抗体:辣根过氧化物酶-羊抗鼠抗抗体;
(4)福莫特罗标准品溶液:采用梯度稀释法配制福莫特罗标准品溶液,1mL/瓶,浓度分别为0μg/L、0.1μg/L、0.3μg/L、0.9μg/L、2.7μg/L、8.1μg/L;
(5)底物显色液A液为过氧化脲溶液,底物显色液B液为四甲基联苯胺(TMB)溶液;
(6)终止液为1-2mol/L的硫酸溶液;
(7)浓缩洗涤液为含有1%吐温-20的0.2mol/L PH7.4的磷酸盐缓冲液;
(8)样本复溶液为含有0.1-5%脱脂奶粉的0.02mol/L PH7.4的磷酸缓冲液。
实施例六使用本发明所述的酶联免疫试剂盒检测样本中福莫特罗
1、样本的前处理
(a)尿样:取尿样室温5000rpm离心5min,取上清100μL用样品稀释液稀释4倍,取上清进行检测;
(b)(肉类、肾脏、肝脏等)组织:称取肉样组织2.0g±0.05g,加入5mL乙酸乙酯,振荡1min,5000rpm离心10min;移取上层乙酸乙酯层溶液于另一离心管中,水相再用5mL乙酸乙酯重复萃取,合并有机相氮气吹干;加入1mL复溶工作液溶解,取50μL用于分析;
(c)饲料:称取饲料2.0g±0.05g,加入5mL乙酸乙酯,振荡1min,5000rpm离心10min;移取上层乙酸乙酯层溶液于另一离心管中,水相再用5mL乙酸乙酯重复萃取,合并有机相氮气吹干;加入1mL复溶工作液溶解,取50μL用于分析。
2、检测方法
(1)取出酶联免疫试剂盒,试剂恢复至室温(20-25℃),至少在室内放置30min;
(2)按需要取出板条,放置在酶标板上;
(3)按需要的量将福莫特罗单克隆抗体工作液和酶标记物工作液按5:1比例混合;
(4)向孔内依次加入标准品(或待测样品)50μL、福莫特罗单克隆抗体工作液和酶标记物工作液的混合液50μL,轻轻振荡混匀,25℃避光孵育30min;
(5)将孔内液体甩干,用洗涤工作液(用去离子水将20×浓缩洗涤液20倍稀释)250μL/孔,洗涤4次,拍干;
(6)将显色液A和显色液B按1:1比例混合,100ul/孔加入显色,25℃避光孵育15min;
(7)加终止液50μL终止反应,酶标仪450nm下测定(建议采用双波长450/630测定),根据标准曲线进行定量或定性。
3、检测结果
((a)定量分析:分别计算标准品和待测样本的平均吸光度值,标准品或待测样本的吸光度值(B)除以0μg/L标准品的吸光度值(B0)再乘以100%,即为百分吸光度值,百分吸光度值=(B/B0)×100%;以百分吸光度值为纵坐标,标准浓度的对数为横坐标,绘制标准曲线;将待测样本的百分吸光度值代入标准曲线,即可求出对应的浓度,再乘以稀释倍数即为样本的实际残留;
(2)定性分析:用待测样本的平均吸光度值和标准品的吸光度值相比较,即可得出待测样本的浓度范围。
检测结果也可以用专业的计算机软件进行计算,测试范围为0.1μg/ml-8.1μg/ml。
实施例七本发明所述酶联免疫试剂盒灵敏度、特异性、精密度、准确度和保质期实验
1、试剂盒灵敏度测定
灵敏度以最低检测限(mg/kg或μg/kg)表示。分别测定20份猪肉组织、猪尿和饲料等空白样品,及20份福莫特罗标准品。求(B/B0)%值的平均值(X)和标准差(SD),从标准曲线上求出X-2SD值对应的标准品浓度,作为各样本的最低检测限。
试剂盒的曲线范围在0.0975-6.25μg/L范围内(见图3),组织中福莫特罗检测限为0.5μg/L,尿液中检测限为0.2ug/L,饲料中检测限为0.3ug/L。
2、试剂盒准确度及精确度测定
准确度是指测定值与真实值间的符合程度,常用回收率表示;精密度是反应测定方法对某一特定样本多次测定所得结果的重复程度,常用变异系数表示。从检测合格的试剂盒中选取同一批次和不同批次的酶标板,在组织(猪肉)、尿液和饲料中添加终浓度为0.9μg/L、2.7μg/L、8.1μg/L的福莫特罗标准品根据以上所述的处理方法提取,同一批次、不同批次分别重复5次,测定批内、批间变异系数及回收率。结果见表1、表2和表3。
表1组织(猪肉)样品批内、批间变异系数及回收率测定
表1为猪肉组织中福莫特罗添加回收率和变异系数。结果表明,在3个添加浓度下,对应的虾肉组织中福莫特罗回收率分别为94.66±6.04、83.92±6.65、78.62±6.70,批内变异系数均在9.48%以下,批间变异系数均在10.84%以下。
表2尿液样品批内、批间变异系数及回收率测定
表2为尿液中福莫特罗添加回收率和变异系数。结果表明,在3个添加浓度下,对应的尿液中福莫特罗回收率分别为96.43±6.43、85.51±6.24、82.10±6.41,批内变异系数均在10.26%以下,批间变异系数均在11.85%以下。
表3饲料样品批内、批间变异系数及回收率测定
表3为饲料中福莫特罗添加回收率和变异系数。结果表明,在3个添加浓度下,对应的牛奶中福莫特罗回收率分别为78.48±6.46、81.06±5.44、84.85±6.69,批内变异系数均在7.81%以下,批间变异系数均在8.52%以下。
综上所述,针对组织(猪肉)、尿液、饲料的添加回收率实验,回收率均在77%-86%之间,批内、批间变异系数均在15%以下,符合《农业部文件》农医发[2005]17号文件中规定的试剂盒备案参考评判标准中的精密度和准确度规定。
3、交叉反应率测定
选择如下所示苯乙醇胺A、沙丁胺醇、妥布特罗、盐酸克伦特罗、莱克多巴胺、西马特罗及动物组织中常检的其他药物(氯霉素、四环素类、喹诺酮类、磺胺类)等几种药物的交叉反应率,结果如表4所示。交叉反应率CR=(福莫特罗的IC50/各结构类似物的IC50)×100℅。
表4试剂盒的交叉反应性
4、试剂盒保存期实验
将试剂盒放置在2℃-8℃保存12个月,期间每隔1个月检测一次,测定试剂盒的IC50值、ODmax、回收率等各项参数均在正常范围内。同时将试剂盒放置在37℃和-20℃放置6天,每天检测一次,测定试剂盒的IC50%、ODmax、回收率等各项参数均在正常范围之内。
从以上结果看出,三种条件保存试验,本试剂盒的各项指标均符合质量要求,因此,此试剂盒可以在2℃-8℃保存至少12个月。
上述实施例只为说明本发明的技术构思和优点,本发明也可以具有其它的形式变化,如本领域技术人员所熟知,上述实施例仅仅起到对上述发明保护范围内的示范作用,对本领域普通技术人员来说,在本发明所限定的保护范围内还有很多常规变形和其它实施例,这些变形和实施例都将在本发明待批的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!