磁共振成像方法及装置与流程
本发明属于磁共振技术领域,尤其涉及一种磁共振成像方法及装置。
背景技术:
MRI(Magnetic ResonanceImaging,磁共振成像)具有极好的软组织对比度,能够多参数、多平面任意角度成像,对流动组织的敏感性高,更为重要的是具有无创、无X线辐射损害等众多优势,使其被广泛应用于临床诊断和医学研究中。MRI是以人体组织内丰富存在的H质子为成像基础,通过外加一个与H质子自旋相同频率的射频脉冲来产生共振信号。由于磁兼容的金属介入装置是不存在H质子,从而在传统的MR成像图像上其本身的位置区域表现出信号缺失,而且很难识别介入装置周围组织特征,从而无法帮助医生对介入装置进行精准定位并无法诊断评估周围组织以及介入物官腔情况。
基于上述问题,提出一种可实现磁共振兼容金属介入装置的磁共振正对比成像方法,以磁化率强度为图像对比度,巧妙地回避传统磁共振成像中以H质子信号强度为基础的物理机制。但该方法是以自旋回波序列进行数据采集,虽然其信噪比较高,但是扫描速度非常慢(大于25分钟),致使该理论技术还不能在临床中得到应用。
技术实现要素:
有鉴于此,本发明实施例提供了一种磁共振成像方法及装置,以解决现有技术中扫描时间较长的问题。
本发明实施例的第一方面,提供了一种磁共振成像方法,包括:
建立多通道线圈并行采集的快速自旋回波正对比的磁共振成像序列采集模型;
根据磁化率图和结构图像建立联合估计模型;
根据所述联合估计模型,并结合根据所述磁共振成像序列采集模型采集磁共振数据,对磁共振图像进行重建。
优选的,所述建立多通道线圈并行采集的快速自旋回波正对比磁共振成像序列采集模型包括:
通过多通道的相控阵线圈阵列,并结合预设被数的欠采集相位编码线,建立所述磁共振成像序列采集模型;
其中,所述相位编码线的中间采集密度大于边缘采集密度。
优选,所述磁共振成像序列采集模型的有效回波时间为0.2毫秒至0.7毫秒。
优选,所述对磁共振图像进行重建具体包括:
通过定量磁敏感成像方法对磁共振图像进行重建,得到包含金属介入装置正对比度图像的图像。
优选,所述通过定量磁敏感成像方法对磁共振图像进行重建包括:
通过定量磁敏感成像方法对磁共振图像进行重建,得出重建模型为:
其中,ρ1和ρ2分别为梯度偏移预设时间之前和偏移所述预设时间之后的重建图像,P为欠采样矩阵,F为傅里叶变化算子,λ1和λ2为重建参数;
根据所述重建模型对磁共振图像进行重建。
本发明实施例的第二方面,提供了一种磁共振成像装置,包括:
第一模型建立模块,用于建立多通道线圈并行采集的快速自旋回波正对比磁共振成像序列采集模型;
第二模型建立模块,用于根据磁化率图和结构图像建立联合估计模型;
重建模块,用于根据所述联合估计模型,并结合根据所述磁共振成像序列采集模型采集磁共振数据,对磁共振图像进行重建。
可选的,所述第一模型建立模块具体用于:通过多通道的相控阵线圈阵列,并结合预设被数的欠采集相位编码线,建立所述磁共振成像序列采集模型;
其中,所述相位编码线的中间采集密度大于边缘采集密度。
可选的,所述磁共振成像序列采集模型的有效回波时间为0.2毫秒至0.7毫秒。
可选的,所述重建模块具体用于:通过定量磁敏感成像方法对磁共振图像进行重建,得到包含金属介入装置正对比度图像的图像。
可选的,所述重建模块包括:
重建模型单元,用于通过定量磁敏感成像方法对磁共振图像进行重建,得出重建模型为:
其中,ρ1和ρ2分别为梯度偏移预设时间之前和偏移所述预设时间之后的重建图像,P为欠采样矩阵,F为傅里叶变化算子,λ1和λ2为重建参数;
处理单元,用于根据所述重建模型对磁共振图像进行重建。
本发明实施例相对于现有技术所具有的有益效果:本发明实施例通过多通道线圈并行采集的快速自旋回波正对比的磁共振成像序列,结合根据磁化率图和结构图像建立的联合估计模型,对磁共振图像进行重建,可对磁兼容金属介入装置进行正对比成像的磁共振技术及相应的成像脉冲序列和图像重建,实现磁兼容金属介入装置准确定位和可视化,能够获得快速鲁棒的定量磁化率图像,获得稳定的金属介入装置正对比度图像,准确的正对比的显示出金属装置位置,并能清晰的识别介入装置与周围组织的位置关系,评估支架装置官腔情况,而不是亮的显示介入装置周围。而且上述磁共振成像方法,成像分辨率较高,加入的并行采集和FSE高空间分辨采集,在提高成像速度的时候,不损失图像空间分辨率,信噪比较高。
附图说明
为了更清楚地说明本发明实施例中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动性的前提下,还可以根据这些附图获得其他的附图。
图1是本发明实施例提供的磁共振成像方法的流程图;
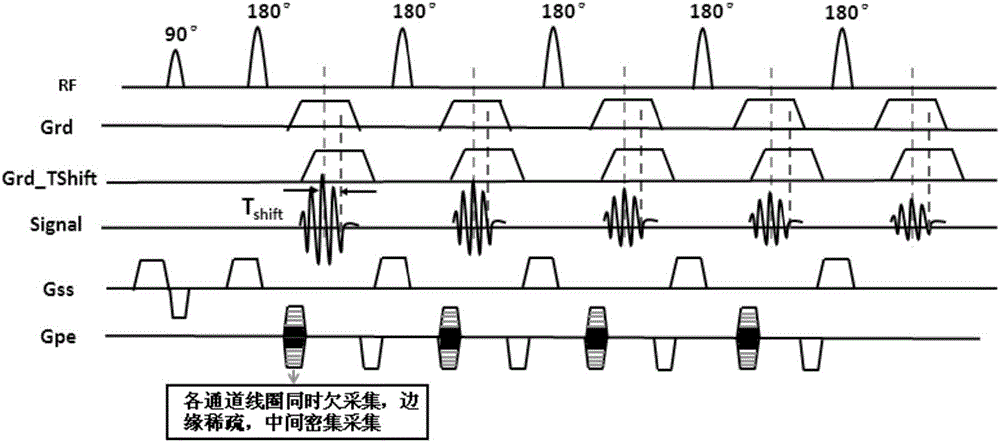
图2是本发明实施例提供的多通道线圈并行采集的快速自旋回波正对比成像序列;
图3是本发明实施例提供的磁共振成像方法在未加速下的气管支架图像;
图4是SUMO方法在未加速下的气管支架图像;
图5是GRASP方法在未加速下的气管支架图像;
图6是采用本发明实施例提供的磁共振成像方法的支架正对比图叠加在幅值图上的图像;
图7是采用SUMO方法的支架正对比图叠加在幅值图上的图像;
图8是采用GRASP方法的支架正对比图叠加在幅值图上的图像;
图9是本发明实施例提供的磁共振成像装置的结构框图。
具体实施方式
以下描述中,为了说明而不是为了限定,提出了诸如特定系统结构、技术之类的具体细节,以便透彻理解本发明实施例。然而,本领域的技术人员应当清楚,在没有这些具体细节的其它实施例中也可以实现本发明。在其它情况中,省略对众所周知的系统、装置、电路以及方法的详细说明,以免不必要的细节妨碍本发明的描述。
为了说明本发明所述的技术方案,下面通过具体实施例来进行说明。
实施例一
图1示出了本发明实施例一提供的磁共振成像方法的实现流程,详述如下:
步骤S101,建立多通道线圈并行采集的快速自旋回波正对比的磁共振成像序列采集模型。
可以理解的,由于磁兼容的金属介入装置是不存在H质子,从而在传统的MR成像图像上其本身的位置区域表现出信号缺失,而且这些金属介入装置在MR外磁场中会被磁化,产生局部磁场,从而会对周围组织区域产生干扰,也即磁化率伪影,因此在介入装置周围区域表现出一个较大的黑洞(该区域远远的大于其装置本身的大小),也即负对比图像,图像的负对比使得区分金属介入装置和磁化率伪影以及因其它空隙造成的负对比变得十分困难,而且很难识别介入装置周围组织特征,从而无法帮助医生对介入装置进行精准定位并无法诊断评估周围组织以及介入物官腔情况。
本实施例中,可以通过多通道的相控阵线圈阵列,并结合预设被数的欠采集相位编码线,建立所述磁共振成像序列采集模型。其中,所述相位编码线的中间采集密度大于边缘采集密度。
其中,FSE(Fast spin echo,快速自旋回波)序列是在SE(Spin echo,自旋回波)序列的基础上发展起来的。与SE序列相比,FSE序列在90°射频脉冲激发后利用多个(2个以上)180°回聚脉冲产生多自旋回波,并对每个回波进行相位编码,实现一次激发多条相位线的采集,因此具有数据采集速度快、信噪比高等优点。
本步骤中的多通道线圈并行采集的快速自旋回波(Parallel-FSE-based)正对比磁共振成像序列,通过多通道的相控阵线圈阵列,并结合预设被数的欠采集相位编码线,能够实现进一步的数据加速采集,以便更实用的应用到临床。
但FSE序列的180°回聚脉冲使得所有因主磁场不均匀性造成的失相位信号进行回聚,不能用于正对比磁共振成像。为此,可以在Parallel-FSE-based序列基础上读出梯度Grd偏移预设时间(参见图2),使得梯度的有效回波时间很短(为所述预设时间),在避免信号严重缺失的同时得到因组织本身磁化率的差异造成的相位变化,实现植入放射性粒子正对比磁共振成像的数据采集。图2中,RF表示射频脉冲,Grd表示读出梯度,Grd_Tshift表示偏移Tshift时间的读出梯度,Signal表示采集信号,Gss表示层选择梯度,Gpe表示相位编码梯度。
本实施例中,所述预设时间为0.2毫秒至0.7毫秒,即所述磁共振成像序列采集模型的有效回波时间为0.2毫秒至0.7毫秒,但并不以此为限。在其他实施例中,还可以根据需要将所述预设时间设置的更短或更长。
所述磁共振成像序列采集模型,不仅能够保留FSE序列数据采集速度快、信噪比高的优点,而且能够有效避免因180°回聚脉冲而导致失相位信号完全回聚的问题;同时与QSM(Quantitative Susceptibility Mapping,定量磁敏感成像)理论中常用的梯度回波序列相比,其有效回波时间很短(只有0.2~0.7ms),从而克服因有效回波时间太长而采集不到有用信号的缺陷,而且加入的多通道并行采集更进一步的加速采集,实现金属介入装置正对比磁共振成像的临床快速采集需求。
步骤S102,根据磁化率图和结构图像建立联合估计模型。
随着CS被引入到磁共振成像中,很多先验信息,如图像的稀疏性,线圈灵敏度矩阵的平滑性等都可以作为先验约束在图像重建中。由于对线圈灵敏度和图像进行联合估计的非线性迭代方法能重建出高质量的图像,且在采用较大的欠采因子的情况下,磁化率图是高度稀疏的,因此可以把磁化率图和图像这些先验约束一起去联合估计来改进重建图像质量,也即JSMAI(Joint estimation of susceptibility map and image by nonlinear iterative methods)模型。
步骤S103,根据所述联合估计模型,并结合根据所述磁共振成像序列采集模型采集磁共振数据,对磁共振图像进行重建
本实施例中,可以将不同所述预设时间下的图像稀疏性来作为先验约束,同时对磁化率图进行稀疏约束来实现准确的图像重建,这样能够在保证快速采集的同时获得高质量的正对比图。另外,可以通过QSM方法对磁共振图像进行重建,得到包含金属介入装置正对比度图像的图像。
参见图2,步骤S103具体可以通过以下过程实现:
步骤S201,通过定量磁敏感成像方法对磁共振图像进行重建,得出重建模型为:
其中,ρ1和ρ2分别为梯度偏移预设时间之前和偏移所述预设时间之后的重建图像,P为欠采样矩阵,F为傅里叶变化算子,λ1和λ2为重建参数。
令:f3(X)=||MGχ||1,X=(ρ1,ρ2,χ),K=γ·Tshift·B0,求解公式(1),可以转化为如下方程
则
其中,conj(x)代表x的共轭,μ=[10-15,10-6],XH代表X的共轭转置。
需要说明的是,求解方程(1)有很多种非线性迭代方法,比如最速下降法,共轭梯度法,高斯牛顿法等。在一个迭代搜索方法中,最关键的是在每一步迭代中找到搜索方向,共轭梯度法是一种线性搜索方法,是目前求解线性方程中最重要的一个方法,它可以很快的线性收敛到局部最优解。因此在求解非线性最优化问题公式(1)时,采用共轭梯度法来求解。
步骤S202,根据所述重建模型对磁共振图像进行重建。
传统的磁化率计算方法需要去除复杂的背景场干扰,而本实施例中的图像重建算法不需要去除背景场干扰,计算更为简单;而且引入贝叶斯正则化约束和JSMAI联合估计图像和磁化率矩阵模型,可准确重建出磁化率图像,提供更丰富的局部细节信息并高对比地显示介入装置位置和大小形状等。
本发明实施例中,成像的空间分辨率不低于1.0mm×1.0mm,层厚不低于3.0mm,成像扫描时间在5分钟以内。
以下通过仿真实验进行说明:图3为上述磁共振成像方法在未加速下的气管支架正对比图;图4为采用SUMO(Susceptibility gradient mapping using the original resolution,保持原始成像分辨率的磁化率梯度成像)方法的正对比图;图5为采用GRASP(Gradient echo acquisition for super-paramagnetic particles with positive contrast,梯度回波获取的超顺磁性标记物的正对比成像)方法的支架正对比图;图6为采用上述磁共振成像方法的支架正对比图叠加在幅值图上的图像;图7为采用SUMO方法的支架正对比图叠加在幅值图上的图像;图8为采用GRASP方法的支架正对比图叠加在幅值图上的图像。结合图3至图8,从重建结果来看,上述磁共振成像方法能够有效的抑制金属伪影,在实现高时空分辨率的前提下,获得清晰的正对比图像,准确的定位出支架位置,并能有效的评估支架与周围组织关系。
上述磁共振成像方法,通过多通道线圈并行采集的快速自旋回波正对比的磁共振成像序列,结合根据磁化率图和结构图像建立的联合估计模型,对磁共振图像进行重建,可对磁兼容金属介入装置进行正对比成像的磁共振技术及相应的成像脉冲序列和图像重建,实现磁兼容金属介入装置准确定位和可视化,能够获得快速鲁棒的定量磁化率图像,获得稳定的金属介入装置正对比度图像,准确的正对比的显示出金属装置位置,并能清晰的识别介入装置与周围组织的位置关系,评估支架装置官腔情况,而不是亮的显示介入装置周围。而且上述磁共振成像方法,成像分辨率较高,加入的并行采集和FSE高空间分辨采集,在提高成像速度的时候,不损失图像空间分辨率,信噪比较高。
应理解,上述实施例中各步骤的序号的大小并不意味着执行顺序的先后,各过程的执行顺序应以其功能和内在逻辑确定,而不应对本发明实施例的实施过程构成任何限定。
实施例二
对应于上文实施例一所述的磁共振成像方法,图9示出了本发明实施例二提供的磁共振成像装置的结构框图。为了便于说明,仅示出了与本实施例相关的部分。
参照图9,该装置包括第一模型建立模块101、第二模型建立模块102和重建模块103。其中,第一模型建立模块101,用于建立多通道线圈并行采集的快速自旋回波正对比磁共振成像序列采集模型。第二模型建立模块102,用于根据磁化率图和结构图像建立联合估计模型。重建模块103,用于根据所述联合估计模型,并结合根据所述磁共振成像序列采集模型采集磁共振数据,对磁共振图像进行重建。
可选的,所述第一模型建立模块101具体用于:通过多通道的相控阵线圈阵列,并结合预设被数的欠采集相位编码线,建立所述磁共振成像序列采集模型;其中,所述相位编码线的中间采集密度大于边缘采集密度。
优选的,所述磁共振成像序列采集模型的有效回波时间为0.2毫秒至0.7毫秒。
作为一种可实施方式,所述重建模块103具体用于:通过定量磁敏感成像方法对磁共振图像进行重建,得到包含金属介入装置正对比度图像的图像。
一个实施例中,所述重建模块103包括重建模型单元201和处理单元202。其中,重建模型单元201,用于通过定量磁敏感成像方法对磁共振图像进行重建,得出重建模型为:
其中,ρ1和ρ2分别为梯度偏移预设时间之前和偏移所述预设时间之后的重建图像,P为欠采样矩阵,F为傅里叶变化算子,λ1和λ2为重建参数。
处理单元202,用于根据所述重建模型对磁共振图像进行重建。
上述磁共振成像装置,通过多通道线圈并行采集的快速自旋回波正对比的磁共振成像序列,结合根据磁化率图和结构图像建立的联合估计模型,对磁共振图像进行重建,可对磁兼容金属介入装置进行正对比成像的磁共振技术及相应的成像脉冲序列和图像重建,实现磁兼容金属介入装置准确定位和可视化,能够获得快速鲁棒的定量磁化率图像,获得稳定的金属介入装置正对比度图像,准确的正对比的显示出金属装置位置,并能清晰的识别介入装置与周围组织的位置关系,评估支架装置官腔情况,而不是亮的显示介入装置周围。而且上述磁共振成像方法,成像分辨率较高,加入的并行采集和FSE高空间分辨采集,在提高成像速度的时候,不损失图像空间分辨率,信噪比较高。
所属领域的技术人员可以清楚地了解到,为了描述的方便和简洁,仅以上述各功能单元、模块的划分进行举例说明,实际应用中,可以根据需要而将上述功能分配由不同的功能单元、模块完成,即将所述装置的内部结构划分成不同的功能单元或模块,以完成以上描述的全部或者部分功能。实施例中的各功能单元、模块可以集成在一个处理单元中,也可以是各个单元单独物理存在,也可以两个或两个以上单元集成在一个单元中,上述集成的单元既可以采用硬件的形式实现,也可以采用软件功能单元的形式实现。另外,各功能单元、模块的具体名称也只是为了便于相互区分,并不用于限制本申请的保护范围。上述系统中单元、模块的具体工作过程,可以参考前述方法实施例中的对应过程,在此不再赘述。
本领域普通技术人员可以意识到,结合本文中所公开的实施例描述的各示例的单元及算法步骤,能够以电子硬件、或者计算机软件和电子硬件的结合来实现。这些功能究竟以硬件还是软件方式来执行,取决于技术方案的特定应用和设计约束条件。专业技术人员可以对每个特定的应用来使用不同方法来实现所描述的功能,但是这种实现不应认为超出本发明的范围。
在本发明所提供的实施例中,应该理解到,所揭露的装置和方法,可以通过其它的方式实现。例如,以上所描述的系统实施例仅仅是示意性的,例如,所述模块或单元的划分,仅仅为一种逻辑功能划分,实际实现时可以有另外的划分方式,例如多个单元或组件可以结合或者可以集成到另一个系统,或一些特征可以忽略,或不执行。另一点,所显示或讨论的相互之间的耦合或直接耦合或通讯连接可以是通过一些接口,装置或单元的间接耦合或通讯连接,可以是电性,机械或其它的形式。
所述作为分离部件说明的单元可以是或者也可以不是物理上分开的,作为单元显示的部件可以是或者也可以不是物理单元,即可以位于一个地方,或者也可以分布到多个网络单元上。可以根据实际的需要选择其中的部分或者全部单元来实现本实施例方案的目的。
另外,在本发明各个实施例中的各功能单元可以集成在一个处理单元中,也可以是各个单元单独物理存在,也可以两个或两个以上单元集成在一个单元中。上述集成的单元既可以采用硬件的形式实现,也可以采用软件功能单元的形式实现。
所述集成的单元如果以软件功能单元的形式实现并作为独立的产品销售或使用时,可以存储在一个计算机可读取存储介质中。基于这样的理解,本发明实施例的技术方案本质上或者说对现有技术做出贡献的部分或者该技术方案的全部或部分可以以软件产品的形式体现出来,该计算机软件产品存储在一个存储介质中,包括若干指令用以使得一台计算机设备(可以是个人计算机,服务器,或者网络设备等)或处理器(processor)执行本发明实施例各个实施例所述方法的全部或部分步骤。而前述的存储介质包括:U盘、移动硬盘、只读存储器(ROM,Read-Only Memory)、随机存取存储器(RAM,Random Access Memory)、磁碟或者光盘等各种可以存储程序代码的介质。
以上所述实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的精神和范围,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!