一种Au/DABT纳米探针及其制备方法和应用与流程
本发明属于纳米材料分析检测技术,涉及一种纳米材料‐有机分子探针的设计与合成,特别涉及一种Au/DABT纳米探针及其制备方法和应用。
背景技术:
一氧化氮是一种重要的生物体内信使和效应分子,在神经传递、免疫应答和心血管调节方面发挥着多样且至关重要的作用。19世纪80年代发现一氧化氮产生于内皮细胞,作为内皮舒张因子可引起血管平滑肌的舒张,进一步起到调节血压的作用。一氧化氮在体内主要来源于三种一氧化氮合酶(NOS),分别是诱生型一氧化氮合酶(iNOS)、内皮型一氧化氮合酶(eNOS)和神经元型一氧化氮合酶(nNOS)。体内过量或者不正常的NO浓度可能会是一系列病症的诱发原因,包括:癌症,内皮功能紊乱,或者神经退行性疾病如阿尔兹海默症和帕金森综合症。
由于一氧化氮在生物体内的重要作用,目前有很多研究一氧化氮的方法,如电化学检测法、化学发光法、分光光度法、荧光法、顺磁共振法等。这些方法易受到其他杂质的干扰,或存在较复杂的制样过程,较难实现对生物体内一氧化氮的检测。荧光法虽然可以实现对细胞内的检测,但是很容易受光漂白的影响。
应用表面增强拉曼光谱技术具有高灵敏性与高选择性及对生物样本无损伤等优点,日益受到人们的关注。传统的表面增强拉曼技术大多关注于平面增强基底的构建,应用于对物质的定性检测当中,而无法实现对细胞内的物质进行实时检测。基于纳米颗粒的表面增强拉曼光谱技术可以实现在液体中的定量检测和细胞中的定量检测,但是由于生物样品的环境复杂性,所以对探针的稳定性、灵敏性、选择性等有很高的要求。
技术实现要素:
针对现有技术的上述缺陷,本发明提出了一种Au/DABT纳米探针及其制备方法,以纳米颗粒为基底,通过化学键将特异性响应分子DABT与纳米颗粒链接,制备得到Au/DABT纳米探针,本发明的方法操作简单方便、成本低,制备得到的Au/DABT纳米探针毒性小,对一氧化氮进行检测具有高稳定性、高选择性、高准确性和高灵敏度的优点。
本发明提供了一种Au/DABT纳米探针的制备方法,包括以下步骤:
(1)金纳米颗粒(AuHT纳米颗粒)的合成
十六烷基三甲基氯化铵、氯金酸和抗坏血酸在溶剂中进行还原反应,得到金纳米颗粒。
(2)DABT探针分子的合成
(2.1)4-氨基-3硝基苯硫酚的合成:在溶剂中,KOH和4-硫氰基-2-硝基苯胺进行水解反应,然后加入硫酸乙醇溶液,得到4-氨基-3硝基苯硫酚。
(2.2)3,4-二氨基苯硫酚的合成:在溶剂中,4-氨基-3硝基苯硫酚和连二亚硫酸钠进行还原反应,得到3,4-二氨基苯硫酚。
(3)Au/DABT纳米探针的合成
在溶剂中,步骤(2)制备的DABT和步骤(1)制备的AuHT纳米颗粒进行金硫键自组装,得到所述Au/DABT纳米探针。
步骤(1)中,所述还原反应的温度为0~30℃;优选地,所述还原反应在室温(25℃)下进行。
步骤(1)中,所述还原反应的时间为2~12小时;优选地,为4~6小时。
步骤(1)中,所述十六烷基三甲基氯化铵、氯金酸、抗坏血酸的摩尔比为50:3:10~20;优选地,为50:3:20。
步骤(1)中,所述溶剂选自水、乙醇、丙酮;优选地,为水。
步骤(1)中,溶液由无色透明变为浅紫色,反应结束有橘色沉淀生成;可选地,可以将反应溶液离心,沉淀经多次洗涤后再次溶于水溶液中,用于下一步反应。
步骤(1)中,优选地,将十六烷基三甲基氯化铵溶液和氯金酸混合后,快速加入新配置的抗坏血酸溶液,然后轻轻摇晃。
步骤(2.1)中,所述水解反应的温度为0-30℃;优选地,为10℃。
步骤(2.1)中,所述水解反应的时间为5~30min;优选地,为30min。
步骤(2.1)中,优选地,KOH溶于溶剂中,于10℃将4-硫氰基-2-硝基苯胺缓慢加入上述溶液中,然后在室温下进行水解反应。
步骤(2.1)中,所述KOH、4-硫氰基-2-硝基苯胺的摩尔比为35~70:9;优选地,为53:9。硫酸乙醇在该反应中的作用是中和作用。
步骤(2.1)中,所述溶剂选自水、乙醇、甲醇;优选地,为乙醇。
步骤(2.1)中,配置的所述硫酸乙醇的质量百分比为10%。
步骤(2.1)中,所述硫酸乙醇溶液的作用为调整溶液pH,发生复分解反应,合成4-氨基-3硝基苯硫酚。
步骤(2.2)中,所述还原反应的温度为90~130℃;优选地,为120℃。
步骤(2.2)中,所述还原反应的时间为0.5~3h;优选地,为1h。
步骤(2.2)中,所述4-氨基-3硝基苯硫酚、连二亚硫酸钠的摩尔比为1:1~1:6;优选地,为1:4。
步骤(2.2)中,所述溶剂选自乙醇、水、50%乙醇水溶液;优选地,为50%乙醇水溶液。
步骤(3)中,所述金硫键自组装反应的温度为10~30℃;优选地,为25℃。
步骤(3)中,所述金硫键自组装反应的时间为0.5~4h;优选地,为1-2h。
步骤(3)中,所述DABT、AuHT纳米颗粒用量比为2μmol:1mL~1μmol:2mL;优选地,为1μmol:1mL。
步骤(3)中,所述溶剂选自水、乙醇、PBS;优选地,为水。
步骤(3)中,优选地,反应结束后还包括离心去除未连接的DABT,将Au/DABT纳米探针重新分散在20mM的磷酸缓冲溶液中(pH=7.4)中的步骤。
步骤(3)中,金纳米颗粒与有机分子DABT通过Au-S化学键相连,形成Au/DABT纳米探针,并进一步利用该纳米探针实现SERS对NO的检测。
在一个具体的实施方式中,所述Au/DABT纳米探针的制备方法,包括以下步骤:
(1)金纳米颗粒(AuHT纳米颗粒)的合成
室温下,将30mL的十六烷基三甲基氯化铵溶液(0.01M)加入30mL氯金酸溶液(0.6mM)中,之后快速加入1.2mL新配置的抗坏血酸溶液(0.1M),轻轻摇晃。溶液由无色透明变为浅紫色,最后有橘色沉淀生成。将上述溶液离心,并多次洗涤。最后再次溶于水溶液中,以备待用。
(2)DABT探针分子的合成
合成4-氨基-3硝基苯硫酚:6g KOH溶于100mL乙醇中,于10℃将3.51g的4-硫氰基-2-硝基苯胺缓慢加入上述溶液中。混合物在室温搅拌30min。之后10%的硫酸乙醇溶液慢慢加入直至溶液由深紫色变为橙黄色。之后混合物倒入400mL水中,用乙酸乙酯萃取。有机相用饱和食盐水洗涤,之后用无水硫酸镁干燥。旋蒸之后得到红色固体。
合成3,4-二氨基苯硫酚:3.4g 4-氨基-3硝基苯硫酚溶于50%乙醇中,之后加入13.93g连二亚硫酸钠(80mmol)。反应回流1h之后冷却至室温。氯仿萃取,之后水层旋蒸。得到的固体再用甲醇溶解后旋蒸,粗产物用柱层析的方法提取分离,最后得到黄褐色固体。
(3)Au/DABT纳米探针的合成
0.2mL DABT加入4mLAuHT纳米颗粒的水溶液中,搅拌1-2h之后,离心去除未连接的DABT。之后纳米颗粒重新分散在20mM的磷酸缓冲溶液中(pH=7.4)。
本发明还提供了由上述方法制备得到的Au/DABT纳米探针,该纳米探针利用金硫键的自组装将Au纳米颗粒与有机探针分子连接起来,从而大大提高了探针对NO检测的稳定性。化学键的稳定连接也使该纳米探针具有更好的准确性。另外,该纳米探针具有高的灵敏度和高选择性,对细胞存活率影响小的特点,有利于实现对生物体内NO的检测成像。
本发明还提供了所述Au/DABT纳米探针在体内和/或体外检测NO中的应用。
本发明还提供了一种体外检测NO的SERS方法,所述方法包括以下步骤:
利用DABT可以特异性与NO反应的特点,将上述方法制备得到的Au/DABT纳米探针与NO发生重氮化反应,通过SERS光谱的变化,即利用Au/DABT纳米探针比率型拉曼特征峰的值(I698/I974)来定量检测NO浓度。
其中,所述重氮化反应的温度为0~30℃;优选地,为25℃。
其中,所述重氮化反应的时间为3~10min;优选地,为5min。
其中,所述重氮化反应的溶剂为水、PBS;优选地,为PBS。
其中,所述重氮化反应的适宜的pH为5.0-8.0;优选地,为7.4。
其中,体外检测NO的SERS方法的线性范围为54~918nM,最低检测限为0.1nM。
其中,所述Au/DABT纳米探针储存24h内(0-24h)内,拉曼谱图基本没有差异。
其中,所述激光波长为780nm。
其中,所述体外检测NO的SERS方法不受ROS、RNS以及金属离子的影响;其中,所述ROS包括H2O2,·OH,ClO-,O2-,1O2,;所述RNS包括ONNO-,HNO,NO2-,NO3;所述金属离子包括K+,Na+,Ca2+,Mg2+,Co2+,Fe3+,Cu2+,Ni2+,Mn2+,Cd2+,Pb2+,Ba2+。优选地,所述ROS的加入量为10μM,或所述RNS的加入量为10μM,或所述金属离子的加入量为1mM时,体外检测NO的SERS方法不受ROS、RNS以及金属离子的影响。
本发明的一个具体实施方式中,所述体外检测NO的SERS方法,包括:
(1)标准曲线制作
利用激光拉曼光谱,选用780nm的激光波长,测量制备好的Au/DABT纳米探针的拉曼光谱。随后向其中逐步加入NO溶液(0,54,162,270,378,486,594,702,810,918nM),并且测量每次加入后的拉曼光谱。利用比率型拉曼特征峰的值(I698/I974)与NO浓度的关系做出标准曲线,I=6.608C-2.871(I=I698/I974,C=C(NO))。
(2)样品中NO的检测
在PBS溶液中,所述Au/DABT纳米探针与样品中的NO在室温条件下发生重氮化反应5min,利用Au/DABT纳米探针比率型拉曼特征峰的值(I698/I974),根据标准曲线来定量检测样品中NO的浓度。
本发明还提出了一种细胞内NO的SERS检测和成像方法,所述方法包括以下步骤:
将Au/DABT纳米探针和细胞共培养,使探针进入细胞,然后加入LPS,利用LPS可以刺激细胞产生NO的特点,利用Au/DABT纳米探针比率型拉曼特征峰的值I698/I974来定量检测NO浓度,通过SERS光谱随LPS刺激细胞时间的变化实现对细胞内NO含量的拉曼细胞mapping成像。
其中,所述细胞为PC 12细胞、神经瘤母细胞、Hela细胞;优选地,为PC 12细胞。
其中,所述Au/DABT纳米探针、PC 12细胞、LPS的用量关系为300μL:5mL:20μL。
其中,所述共培养的时间为4~6h;优选地,为4h。
其中,所述LPS刺激细胞产生NO的时间为0.5h-12h;优选地,为1h。
其中,细胞内检测NO的SERS方法的线性范围为54~918nM,最低检测限为0.1nM。
其中,所述Au/DABT纳米探针对细胞没有毒性。
本发明一个具体的实施方式中,所述细胞内NO的SERS检测和成像方法,包括:
(1)标准曲线制作
利用激光拉曼光谱,选用780nm的激光波长,测量制备好的Au/DABT纳米探针的拉曼光谱。随后向其中逐步加入NO溶液(0,54,162,270,378,486,594,702,810,918nM),并且测量每次加入后的拉曼光谱。利用比率型拉曼特征峰的值(I698/I974)与NO浓度的关系做出标准曲线,I=6.608C-2.871(I=I698/I974,C=C(NO))。
(2)细胞内NO的检测
先将Au/DABT纳米探针和PC 12细胞共培养4h使探针进入细胞,之后移去培养液,用PBS洗三遍。再加入LPS,利用LPS可以刺激细胞产生NO的特点,通过SERS光谱随LPS刺激细胞时间的变化实现对细胞内NO含量做出拉曼细胞mapping成像。
本发明的反应机理为,以纳米颗粒为基底,通过化学键将对一氧化氮有特异性响应的DABT探针分子与纳米颗粒链接,制备得到Au/DABT纳米探针。利用Au/DABT纳米探针与一氧化氮反应后生成Au/BTAH,其拉曼光谱会发生变化,从而实现对一氧化氮的定量检测(如图11所示)。
本发明的有益效果在于,本发明金纳米颗粒与有机DABT探针分子通过Au-S化学键相连,制备所述Au/DABT纳米探针。并进一步利用纳米溶胶增强基底(纳米颗粒),利用SERS对NO进行检测。本发明制备得到的Au/DABT纳米探针具有优良的稳定性、高选择性、高准确性和高灵敏度,可以用于体内和/或体外检测NO,线性范围为54~918nM,最低检测限为0.1nM,可以选择性的检测无机体系和生物体有机体系中的一氧化氮(见图6),也可以原位检测细胞中产生的NO并进行拉曼细胞mapping成像。
附图说明
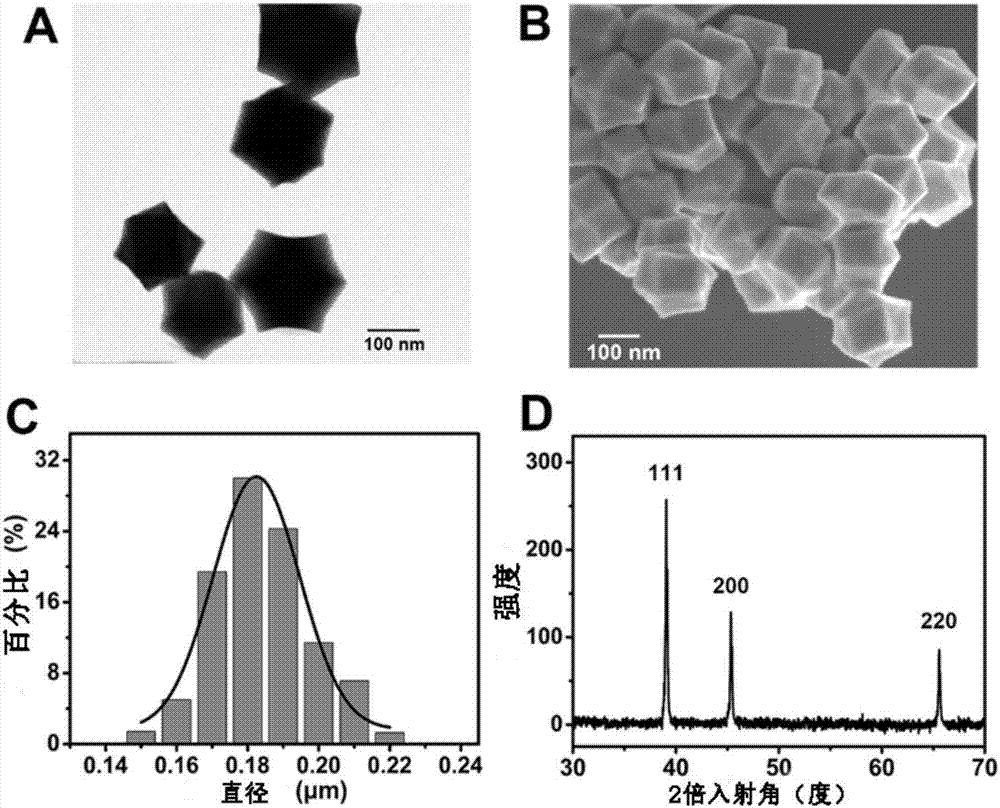
图1为金纳米颗粒的TEM(A),SEM(B),粒径分布图(C)以及XRD(D)。
图2为DABT探针分子的核磁共振氢谱。
图3为DABT探针分子的核磁共振碳谱。
图4为DABT探针分子的高分辨质谱。
图5为体外检测NO浓度(a~j:0,54,162,270,378,486,594,702,810,918nM)时,SERS变化图(A)以及利用Au/DABT纳米探针比率型拉曼特征峰的值(I698/I974)得到线性关系图(B)。
图6为干扰物质ROS、RNS以及金属离子加入时,I698/I974的变化与只加入NO变化的比值情况;其中,A为ROS和RNS加入时,I698/I974的变化与只加入NO变化的比值情况,B为金属离子加入时,I698/I974的变化与只加入NO变化的比值情况;黑色柱状图为单独干扰物质存在时情况,白色柱状图为干扰物质与NO共存时的情况。
图7为Au/DABT纳米探针在pH(5.0‐8.0)时的拉曼谱图(A)以及在储存时间(0‐24h)的拉曼谱图。
图8为Au/DABT纳米探针与NO反应时间关系。
图9为Au/DABT纳米探针浓度与细胞存活率关系图。
图10为利用Au/DABT纳米探针对细胞内NO进行SERS Mapping成像。A、B是PC12细胞和Au/DABT纳米探针共培养4h后在拉曼显微镜下的明场、暗场照片;C是以Au/DABT纳米探针拉曼特征峰比值I698/I974为标准,PC12细胞的SERS Mapping;D是在LPS作用之后,以Au/DABT纳米探针拉曼特征峰比值I698/I974为标准,PC12细胞的SERS Mapping。
图11为本发明的反应机理图。
具体实施方式
结合以下具体实施例和附图,对本发明作进一步的详细说明。实施本发明的过程、条件、实验方法等,除以下专门提及的内容之外,均为本领域的普遍知识和公知常识,本发明没有特别限制内容。
实施例1:利用Au/DABT纳米探针的制备
(1)金纳米颗粒(AuHT纳米颗粒)的合成
室温下,将30mL的十六烷基三甲基氯化铵溶液(0.01M)加入30mL氯金酸溶液(0.6mM)中,之后快速加入1.2mL新配置的抗坏血酸溶液(0.1M),轻轻摇晃。溶液由无色透明变为浅紫色,最后有橘色沉淀生成。将上述溶液离心,并多次洗涤。最后再次溶于水溶液中,以备待用。图1为金纳米颗粒的TEM(A),SEM(B),粒径分布图(C)以及XRD(D);从图A和B中可以看出,合成的Au纳米颗粒具有很好的三八面体形貌。从图C中可以看出合成的该纳米颗粒具有较为均一的粒径,且直径在180±20nm。从D图中可以看出在39.0°,45.2°,65.5°的三个XRD峰,分别对应于金的(111),(200),(220)面,从而也证明了该纳米颗粒为面心立方结构的金的晶体。
(2)DABT探针分子的合成
合成4-氨基-3硝基苯硫酚:6g KOH溶于100mL乙醇中,于10℃将3.51g的4-硫氰基-2-硝基苯胺缓慢加入上述溶液中。混合物在室温搅拌30min。之后10%的硫酸乙醇溶液慢慢加入直至溶液由深紫色变为橙黄色。之后混合物倒入400mL水中,用乙酸乙酯萃取。有机相用饱和食盐水洗涤,之后用无水硫酸镁干燥。旋蒸之后得到红色固体。
合成3,4‐二氨基苯硫酚:3.4g 4‐氨基‐3硝基苯硫酚溶于50%乙醇中,之后加入13.93g连二亚硫酸钠(80mmol)。反应回流1h之后冷却至室温。氯仿萃取,之后水层旋蒸。得到的固体再用甲醇溶解后旋蒸,粗产物用柱层析的方法提取分离,最后得到黄褐色固体。图2为DABT探针分子的核磁共振氢谱。图3为DABT探针分子的核磁共振碳谱。图4为DABT探针分子的高分辨质谱。从图2~4可知,采用本发明方法合成了纯度很高的3,4‐二氨基苯硫酚。
(3)Au/DABT纳米探针的合成
0.2mL DABT加入4mLAuHT纳米颗粒的水溶液中,搅拌1-2h之后,离心去除未连接的DABT。之后纳米颗粒重新分散在20mM的磷酸缓冲溶液中(pH=7.4)。
实施例2:利用Au/DABT纳米探针实现体外对NO的比率型拉曼检测
(1)SERS体外检测NO线性
利用DABT可以特异性与NO反应的特点,将Au/DABT纳米探针与不同浓度的NO在室温条件下于PBS溶液中发生重氮化反应5min,SERS变化图(图5A)(a~j:0,54,162,270,378,486,594,702,810,918nM)以及利用Au/DABT纳米探针比率型拉曼特征峰的值(I698/I974)得到线性关系图(图5B),通过SERS光谱的变化来定量检测NO浓度。结果表明所述Au/DABT纳米探针的线性范围为54~918nM,最低检测线为0.1nM。
(2)Au/DABT纳米探针对检测NO的选择性实验
由于在生物体复杂的环境中可能存在的干扰,对Au/DABT纳米探针与常见活性氧(ROS)和活性氮(RNS)和一些金属离子的反应情况进行实验(图6)。实验结果分为潜在干扰物单独与Au/DABT纳米探针反应情况(黑色柱状图),以及存在潜在干扰物时加入NO的反应情况(白色柱状图)两部分。用ΔI/ΔINO来表示结果,ΔI=(I698-I’698)/I974,表明在加入潜在干扰物时比率型拉曼峰I698/I974的强度。ΔINO指加入NO之后比率型拉曼峰值的变化。由图6A、B可以看出,ROS、RNS以及金属离子对NO的检测基本无干扰,从而表明该纳米探针具有很好的选择性,适合运用于生物体系的检测。
(3)Au/DABT纳米探针对NO检测的pH和时间稳定性
将Au/DABT纳米探针置于不同pH(5.0‐8.0)的磷酸缓冲溶液中,测量其拉曼谱图,如图7A所示,可以看出拉曼谱图在pH(5.0‐8.0)之间基本没有差异,表明该纳米探针具有很好的pH稳定性,能够在一定pH范围内实现对NO准确的检测,适合运用于生物体系中。
测量Au/DABT纳米探针在储存24h内(0‐24h)的拉曼谱图。结果见图7B所示,可以看出拉曼谱图在储存24h内(0‐24h)内基本没有差异,说明该纳米探针具有很好的稳定性。这得益于Au纳米颗粒与DABT分子之间通过稳定的化学键相连。也说明该探针能够运用于较长时间的生物样品检测中。
(4)Au/DABT纳米探针对NO检测的响应时间
Au/DABT纳米探针溶液中加入NO,之后在一定时间测量拉曼谱图,并用比率型拉曼峰I698/I974的强度表示反应时间(图8)。结果可以看出,反应在5分钟内结束,说明该探针与NO作用时间较快,在对NO的体外与体内检测实验中,有很强的适用性和准确性。并且能够实现对NO较为实时快速的检测。
实施例3:Au/DABT纳米探针对PC 12细胞中的NO进行检测成像
(1)Au/DABT纳米探针的细胞毒性实验
将处于增殖期的PC 12细胞培养在96孔板中12小时后,向内加入Au/DABT纳米探针共培养48小时后,移除细胞培养基。加入20μL的MTT溶液(5mg/mL),再培养4小时。之后再次移除MTT溶液,加入180μLDMSO。用酶标仪测定490nm的吸光度。细胞活性用以下公式计算:细胞活性(%)=实验组吸收峰值/对照组吸收峰值×100%。结果如图9,表明Au/DABT纳米探针对细胞活性影响很小,能够在保留细胞活性的条件下,实现对细胞中NO含量的检测成像。
(2)Au/DABT纳米探针对PC 12细胞中NO的检测以及成像
将处于增殖期的PC 12细胞培养在玻璃底培养皿中,继续培养12小时后,向内加入Au/DABT纳米探针共培养4小时后,进行Mapping成像。然后加入LPS培养,诱导PC 12细胞产生NO,进行Mapping成像(图10)。结果可以看出在加入LPS刺激之后,以比率型拉曼峰I698/I974的强度作图,可以看到明显的细胞形状,与之前的细胞明暗场图片一致。明暗场图说明该Au/DABT纳米探针能够很容易的进入细胞中,并且主要分布于细胞质中。用比率型拉曼峰I698/I974的强度作图得到的mapping图说明该探针能够准确运用于NO的细胞内检测和成像。
本发明的保护内容不局限于以上实施例。在不背离发明构思的精神和范围下,本领域技术人员能够想到的变化和优点都被包括在本发明中,并且以所附的权利要求书为保护范围。
- 还没有人留言评论。精彩留言会获得点赞!