一种儿童口服液在线检测方法与流程
本发明属于中草药口服液质量控制技术领域,具体涉及一种儿童口服液在线检测方法,尤其是用近红外光谱法结合化学计量学测定儿童口服液的多种成分含量的方法。
背景技术:
儿童口服液是根据传统中医理论,运用现代研究成果及实践经验,从金针菇、枸杞子、山楂、红枣、茯苓、芡实等多种补益类及药食两用的天然植物中提取活性多糖精制而成。儿童口服液可以有效调节、增强人体免疫力,提高机体抵抗力、防止疾病的侵袭,增强并改善体质。
多糖含量是儿童口服液的功效指标,多糖含量测定方法目前没有统一的国家标准,测定方法较多,对同一个产品,不同地区、不同文献采用的方法不同,得出的结果就不同,因而制定的质量标准和控制的指标值不一样。目前多糖含量检测常采用的方法有高锰酸钾滴定法、硫酸苯酚法、硫酸蒽酮法,各方法主要的差距来自于前处理方法的不同,其显色方法对同一样品测定的结果差距并不是很大。硫酸苯酚法主要用来测定所有单糖和各类多糖,在进行多糖测定时要先沉淀多糖,去除单糖的干扰。硫酸蒽酮法主要用于测定己糖和含己糖的多糖,如果呈蓝色,则为己糖,呈绿色,则为其他糖。直接滴定法测定结果偏高,淀粉等多糖对其有干扰作用。复合多糖的多糖值范围分布宽,儿童口服液的多糖值分布范围从300到800mg/100ml,使得含多糖原料与产品的质量控制很难掌握,目前国内只能进行粗多糖的控制。
目前无论哪种化学测定法,均需要对样品进行预处理,需要消耗大量化学试剂,对环境也造成一定污染。而由于预处理操作步骤多,时间长,人为误差对最终的检测结果影响较大,导致最终产品的多糖含量测定结果波动较大,检测周期长(1-2天),不利于儿童口服液产品检测及生产过程快速质量监控。
技术实现要素:
有鉴于此,本发明的目的在于为提供一种快速的儿童口服液的在线检测方法,准确、实时在线检测儿童口服液多糖含量、可溶性固形物含量及以及溶液的ph值,从而在线监控儿童口服液的质量,为儿童口服液生产过程质量监控提供了有力的支持。
为实现本发明的目的,本发明提供了如下技术方案:
一种儿童口服液的在线检测方法,采用近红外光谱结合偏最小二乘法建立儿童口服液样品质量指标成分的最佳定量分析模型,根据质量指标成分的最佳定量分析模型对样品质量指标进行预测。
本发明所述儿童口服液的在线检测方法可以在线检测儿童口服液的多糖含量、可溶性固形物含量以及ph值。
其中,建立最佳定量分析模型的具体方法包括以下步骤:
(1)近红外仪器采集儿童口服液样品的近红外光谱数据,同时收集样品;
(2)测定儿童口服液样品的质量指标成分的化学值;
(3)将步骤(1)收集到的光谱数据使用spxy训练集样本的选取方法对收集的样品进行训练集和验证集的分组;
(4)对训练集的近红外光谱数据进行预处理和波段的选择;
(5)运用偏最小二乘法将步骤(2)所测得的质量指标成分的化学值与步骤(4)所得的训练集的近红外光谱数据进行关联,建立质量指标成分的定量分析模型;
(6)用验证集光谱数据对定量分析模型进行验证,确定质量指标成分的最佳定量分析模型。
近红外光谱(near-infraredspectroscopy,nir),波长范围为780~2526nm(12820~3959cm-1)。nir吸收带是由-ch、-nh、-oh等官能团伸缩振动的倍频和合频吸收形成的。近红外光谱法具有快速、低消耗、无破坏性、几乎无需样品预处理等优点。nir可以代替传统的化学分析方法离线或在线取样测量。本发明所述方法利用在线近红外仪器在线测量探头,实时检测产品质量数据,及时进行操作工况的调控。
其中本发明具体生产儿童口服液的过程中,将近红外探头深入样品中对样品进行实时扫描检测,在采集光谱的同时收集样品,用于后续质量指标的测定。本发明采集各季节不同批次的儿童口服液的近红外光谱数据,收集数据时间长达一年,包含了不同月份、不同批次的儿童口服液,收集的样品代表性强。
其中,优选的,使用赛默飞世尔科技近红外光谱仪nicoletantarisii采集光谱。所述近红外光谱采集条件优选为:透反射模式采集光谱,以空气为参比,采集波长为1000-2500nm,扫描次数为32,分辨率为8cm-1,吸光度数据格式为spa,每个样品重复扫描三次,计算三次平均光谱作为样品近红外光谱数据。
本发明所述建立校正模型的步骤(2)采用化学方法对儿童口服液样品中的各质量指标进行测定。优选的,各质量指标的测定方法分别为:
采用硫酸蒽酮法测量儿童口服液样品的多糖含量;
采用折光计法测量儿童口服液样品的可溶性固形物含量;
采用酸度计测量儿童口服液样品的ph值。
具体的,采用硫酸蒽酮法测定多糖的含量原理是糖类与浓硫酸脱水生成糖醛或其衍生物,可与蒽酮试剂缩合产生有色物质,反应后溶液呈蓝色,于620nm处有最大吸收,显色与多糖含量呈线性关系,通过测定其吸光度,可以确定多糖的含量,并设置平行样。
具体的,采用折光计法测定可溶性固形物的含量的原理是在20℃用折光计测量待测样液的折光率,并查表或从折光计上直接读出可溶性固形物的含量。
具体的,使用以玻璃电极为指示电极,饱和甘汞电极为参比电极的酸度计进行ph值的测定。测定时将适量包装容器中的样品放入烧杯中或将小包装去盖后直接将电极插入其中即可。
本发明所述建立校正模型的步骤(3)采用samplesetpartitioningbasedonjointx-ydistance训练集样本的选取方法(spxy方法)将步骤(1)收集到的光谱数据进行分组。spxy方法综合考虑了光谱数据和化学值之间的差异,将收集到的样品自动分为用于建立模型的训练数据和用于模型外部验证的验证数据。
本发明所述建立校正模型的步骤(4)对训练集的近红外光谱数据进行预处理和波段的选择。对于每个指标成分,均对光谱进行不同的预处理,从中找出最优的预处理方法,再使用遗传算法对建模波段进行优化选择,建立每个指标成分的定量分析模型。所用建模软件为matlab工具箱pls_toolbox。
其中本发明采用多种光谱预处理方法消除光谱的噪音,重叠峰,基线漂移等。
优选的,步骤(4)所述预处理方法为一阶求导、二阶求导、一阶微分、二阶微分、detrend、baseline、msc、snv中的至少一种。
优选的,本发明所述波段选择方法为间隔偏最小二乘法(ipls)、随机蛙跳(randomfrog),竞争性自适应重加权算法(cars)、蒙特卡洛无信息变量消除法(mcuve)、遗传算法(ga)中的至少一种。
对不同的指标成分,最佳预处理方法和建模的有效波段不同。
在一些实施方案中,所述多糖模型所用预处理方法为detrend(linear),窗口宽度为6,有效波段为波数219-1532间的336个波数;可溶性固形物模型预处理方法为detrend(linear),窗口宽度为3,有效波段为192-1538间的336个波数;ph模型预处理方法为一阶求导,窗口宽度为7,有效波段为168-1543间的346个波数。
进一步,运用偏最小二乘法将步骤(2)所测得的质量指标成分的化学值与步骤(4)所得的训练集的近红外光谱数据进行关联,建立质量指标成分的定量分析模型,然后用验证集光谱数据对定量分析模型进行验证,确定质量指标成分的最佳定量分析模型。
首先最佳定量分析模型与模型参数有关。模型参数包括相关系数(r2)、校正误差均方根(rmsec)、交叉验证误差均方根(rmsecv)、验证误差均方根(rmsep)。r2越接近1,rmsec与rmsep越接近,说明各指标成分的化学值与模型预测值越接近,即二者相关性越好;rmsec、rmsecv、rmsep越小,则模型越准确,即预测精度越高。选择模型参数r2越接近1,rmsec与rmsep越接近,rmsec、rmsecv、rmsep越小的定量分析模型为初步确定最佳模型。
进一步通过验证集的近红外光谱数据,运用所述初步确定最佳模型对质量指标进行预测,将预测值与化学值进行误差计算,逐步对模型进行修正,直至所得模型满足各项误差要求。
优选的,各质量指标的验证集的预测值与化学值的误差应均小于10%。
进一步的,儿童口服液多糖含量预测的相对误差应小于10%,儿童口服液可溶性固形物含量预测的相对误差应小于5%,儿童口服液ph预测的相对误差应小于3%。
在一些实施方案中,将建立的最佳定量分析模型集成到一个在线检测软件中,在线近红外光谱仪在线采集儿童口服液的近红外光谱图,并将光谱数据实时传输到集成有最佳定量分析模型的软件里面,并由最佳定量分析模型实时预测出该批儿童口服液样品的质量参数,在线监控儿童口服液的质量。
由上述技术方可知,本发明提供了一种儿童口服液的在线检测方法,该方法为采用近红外光谱结合偏最小二乘法建立儿童口服液样品质量指标成分的最佳定量分析模型,根据质量指标成分的最佳定量分析模型对样品质量指标进行预测。本发明所述在线检测方法操作简单,快速,准确性高,可实时检测产品质量,实现儿童口服液关键质量控制指标的实时在线快速测定,在检测步骤上不需对样品进行预处理,直接对样品进行检测,经济环保;在检测时间上将化学法检测的1-2天时间缩短为15-30秒;在检测费用上由于检测过程中无耗材,每年可节省耗材费用5万元,为儿童口服液生产过程质量监控提供了有力的支持,是中草药口服液多糖控制技术上的一大突破。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍。
图1为儿童口服液多糖模型有效建模波段图;
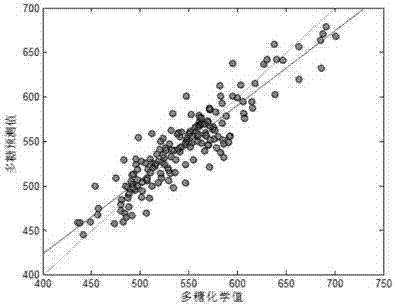
图2为儿童口服液多糖模型训练集实测值与近红外预测值的相关图;
图3为儿童口服液多糖模型训练集、验证集、新数据(盲样)实测值与近红外预测值相对误差图;其中calibrationdata为训练集数据,validationdata为验证集数据;unknowndata为新数据(盲样)数据;
图4为儿童口服液可溶性固形物模型有效建模波段图;
图5为儿童口服液可溶性固形物模型训练集实测值与近红外预测值的相关图;
图6为儿童口服液可溶性固形物模型训练集、验证集、新数据(盲样)实测值与近红外预测值相对误差图;其中calibrationdata为训练集数据,validationdata为验证集数据;unknowndata为新数据(盲样)数据;
图7为儿童口服液ph值模型有效建模波段图;
图8为儿童口服液ph模型训练集实测值与近红外预测值的相关图;
图9为儿童口服液ph模型训练集、验证集、新数据(盲样)实测值与近红外预测值相对误差图;其中calibrationdata为训练集数据,validationdata为验证集数据;unknowndata为新数据(盲样)数据。
具体实施方式
本发明公开了一种儿童口服液的在线检测方法。本领域技术人员可以借鉴本文内容,适当改进工艺参数实现。特别需要指出的是,所有类似的替换和改动对本领域技术人员来说是显而易见的,它们都被视为包括在本发明。本发明的方法及产品已经通过较佳实施例进行了描述,相关人员明显能在不脱离本发明内容、精神和范围内对本文所述的方法进行改动或适当变更与组合,来实现和应用本发明技术。
其中(a)多糖含量测定参考《食品中还原糖的测定》-gb/t5009.7-2008第二法硫酸-蒽酮法;
检测原理:糖类与浓硫酸脱水生成糖醛或其衍生物,可与蒽酮试剂缩合产生有色物质,反应后溶液呈蓝色,于620nm处有最大吸收,显色与多糖含量呈线性关系,通过测定其吸光度,可以确定多糖的含量。
试剂:无水乙醇(分析纯)、丙酮(分析纯)、乙醚(分析纯)、蒽酮试剂(分析纯)称取25mg蒽酮,用50ml浓硫酸溶解,临用新配。葡聚糖标准溶液(分析纯,分子量为40000):称取葡聚糖标准适量,加水制成0.1mg/ml的溶液。
测定:多糖的提取:称量:精密称取口服类样品2g,加入8ml无水乙醇至醇量达80%。转入离心管中,离心,倾去上清液,沉淀分别用10ml无水乙醇洗涤、摇荡、离心(3000r/min,10min)一次,再各用10ml丙酮和乙醚洗涤、摇荡、离心(3000r/min,10min)一次,在通风橱内将有机溶剂挥发掉,干燥得多糖提取物。
供试液的制备:将上述提取的多糖提取物,用蒸馏水定容于100ml容量瓶中,摇匀,即为供试液。
测定样品中多糖含量:(标准曲线法)
精密量取葡聚糖标准液0.0、0.2、0.4、0.6、0.8、1ml,置于具塞试管中,并用蒸馏水补充至1.0ml,将试管放入冷水浴中,分别加入蒽酮试剂4.0ml,摇匀。置沸水浴中加热15min,取出置冷水中冷却至室温。40min后,以空白作对照,用1cm比色杯,在分光光度计上,620nm波长处测定吸光度。以吸光度为横坐标,浓度为纵坐标,绘制标准曲线。
精密量取样品供试液1ml,置具塞试管中,照标准曲线的绘制项下操作,测定吸光度,要求误差≤5%。
计算:
式中:c:样品管葡聚糖的浓度(mg/ml);n:供试液稀释倍数;v:取供试液的毫升数(ml)w:样品数量(g)平行两次测定,取其平均值报告。相对误差小于等于5%。
(b)可溶性固形物含量的测定:折光计法
原理:在20℃用折光计测量待测样液的折光率,并查表或从折光计上直接读出可溶性固形物的含量。
仪器:数字折光仪:测量范围0%~80%,精确度±0.1%。
试剂的制备:将待测样品捣碎,用四层纱布挤出滤液并弃去最初几滴,收集滤液供测试用。
测定步骤:测定前按说明书校正折光仪;分开折光仪两面棱镜,用脱脂棉蘸乙醚或乙醇擦净;用末端熔圆的玻璃棒蘸取试液2~3滴,滴于折光计棱镜面中央(注意勿使玻璃棒触及镜面);迅速闭合棱镜,静置1min,使试液均匀无气泡,并充满视野;对准光源,通过目镜观察物镜。调节指示规,使视野分成明暗两部,再旋转微调螺旋,使明暗界限清晰,并使其分界线恰好在接物镜的十字交叉点上。读取目镜视野中的报分数或折光率,并记录棱镜温度;如目镜读数标尺刻度为百分数,即为可溶性固形物含量(%);同一样品两次测定值之差,不应大于0.5%。取两次测定的算术平均值作为结果,精确到小数点后一位。
(c)ph值的测定:使用以玻璃电极为指示电极,饱和甘汞电极为参比电极的酸度计进行测定。测定时将适量包装容器中的样品放入烧杯中或将小包装去盖后直接将电极插入其中即可。
为了进一步理解本发明,下面将结合本发明实施例,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
如无特殊说明,本发明实施例中所涉及的试剂及仪器均为市售产品,均可以通过商业渠道购买获得。
实施例1、儿童口服液多糖含量快速测定
(1)儿童口服液近红外光谱数据的采集。
采用赛默飞世尔科技近红外光谱仪nicoletantarisii在生产线中于2015年11月-2016年11月采集不同批次的儿童口服液的近红外光谱数据共224批。使用samplesetpartitioningbasedonjointx-ydistance(spxy)方法对224批近红外光谱数据进行训练集和验证集的分组,将数据分组为训练集180批,验证集44批,又于2017年1月在同一生产线同一浓缩暂存罐中采集口服液样品20批用于模型的进一步检验,称之为盲样。
(2)测定儿童口服液多糖含量
对224批儿童口服液样品用实验室常规检测方法检测多糖含量,作为参考数据。多糖含量范围为:435.65-701.09(mg/100ml)。
(3)有效建模波段的选择
使用pls_toolbox自带的遗传算法选波段功能,选用detrend(linear)预处理方法,窗口宽度从1-50进行有效波段的选择,处理对象为180批训练集,所选最佳建模波段为窗口宽度为6时波数219-1532间的336个波数。儿童口服液多糖模型有效建模波段图见附图1。
(4)偏最小二乘法对近红外光谱和多糖值进行关联
采用偏最小二乘法(pls)对训练集的光谱数据在建模波段上进行detrend(linear)预处理,通过化学计量学的方法将所采集的光谱数据的有效建模波段和对应参考数据进行关联,建立多糖的定量模型。儿童口服液多糖模型训练集实测值与近红外预测值的相关图及多糖模型训练集、验证集、盲样实测值与近红外预测值相对误差图见附图2、3。
(5)模型对验证集的预测
将44批验证集样品及20批盲样的近红外光谱数据输入已建好的近红外多糖模型中,得到验证集和盲样的多糖预测值,预测结果见表1,前44号为验证集,后20号为盲样。
表1儿童口服液44批验证集样品及20批盲样多糖预测结果
由表1可知,该模型对于验证集及未知样品的预测结果中,64组数据中仅有2组数据误差大于10%,且有一组为10.742%,在同行业中对复合多糖的预测精度已实现首次突破,该模型可用于多糖的预测,可为生产中复合多糖的含量控制提供极大的技术支持。
实施例2儿童口服液可溶性固形物含量快速测定
(1)儿童口服液近红外光谱数据的采集
采用赛默飞世尔科技近红外光谱仪nicoletantarisii在生产线中于2015年11月-2016年11月采集不同批次的儿童口服液的近红外光谱数据共235批。使用samplesetpartitioningbasedonjointx-ydistance(spxy)方法对先采集的243批近红外光谱数据进行训练集和验证集的分组,分组后训练集200批,验证集35批,又于2017年1月在同一生产线同一浓缩暂存罐中采集口服液样品20批,用于模型的进一步检验,称之为盲样。
(2)测定儿童口服液可溶性固形物含量
对235批儿童口服样品用实验室常规检测方法检测可溶性固形物含量,作为参考数据。可溶性固形物含量范围为:14.8-17.3(%)
(3)有效建模波段的选择
使用pls_toolbox自带的遗传算法选波段功能,选用detrend(linear)预处理方法,窗口宽度从1-50进行有效波段的选择,处理对象为200批训练集,所选最佳建模波段为窗口宽度为3时波数192-1538间的336个波数。儿童口服液可溶性固形物模型有效建模波段见附图4。
(4)偏最小二乘法对近红外光谱和可溶性固形物含量进行关联
采用偏最小二乘法(pls)对训练集的光谱数据在建模波段上进行detrend(linear)的预处理,通过化学计量学的方法将所采集的光谱数据的有效建模波段和对应参考数据进行关联,建立可溶性固形物的定量模型。儿童口服液可溶性固形物模型训练集实测值与近红外预测值的相关图及模型训练集、验证集、盲样实测值与近红外预测值相对误差见附图5、6。
(5)模型对验证集的预测
将35批验证集样品及20批盲样的近红外光谱数据输入已建好的近红外可溶性固形物模型中,得到验证集及盲样的可溶性固形物含量预测值,预测结果见表2,前35号为验证集样品,后20号为盲样。
表2儿童口服液35批验证集样品及20批盲样固形物预测结果
注:e-03为×10-3。
由表2可知,该模型对于可溶性固形物验证集及未知样品的预测结果中,所有数据的误差均不超过5%,说明该模型可准确的对可溶性固形物进行预测,可为生产中可溶性固形物的含量控制提供极大的技术支持。
实施例3儿童口服液ph值快速测定
(1)儿童口服液近红外光谱数据的采集
采用赛默飞世尔科技近红外光谱仪nicoletantarisii在生产线中于2015年11月-2016年11月采集不同批次的儿童口服液的近红外光谱数据共185批。使用samplesetpartitioningbasedonjointx-ydistance(spxy)方法对先采集的185批近红外光谱数据进行训练集和验证集的分组,分组后训练集160批,验证集25批,又于2017年1月在同一生产线同一浓缩暂存罐中采集口服液样品20批,用于模型的进一步检验,称之为盲样。
(2)测定儿童口服液ph值
对185批儿童口服样品用实验室常规检测方法检测ph值,作为参考数据。ph值范围为:4.26-4.65。
(3)有效建模波段的选择
使用pls_toolbox自带的遗传算法选波段功能,选用一阶求导窗口宽度为7的预处理方法,窗口宽度从1-50进行有效波段的选择,处理对象为160批训练集,所选最佳建模波段为窗口宽度为2时波数在168-1543间的346个波数。有效建模波段图见附图7。
(4)偏最小二乘法对近红外光谱和可溶性固形物含量进行关联
采用偏最小二乘法(pls)对训练集的光谱数据在建模波段上进行一阶求导窗口宽度为7的预处理,通过化学计量学的方法将所采集的光谱数据的有效建模波段和对应参考数据进行关联,建立ph值的定量模型。ph模型训练集实测值与近红外预测值的相关图及ph模型训练集、验证集、盲样实测值与近红外预测值相对误差见附图8、9。
(5)模型对验证集的预测
将25批验证集样品及20批盲样的近红外光谱数据输入已建好的近红外ph值模型中,得到验证集和盲样的ph值预测值,预测结果见表3,前25号为验证集样品,后20号为盲样。
表3儿童口服液25批验证集样品及20批盲样ph值预测结果
由表3可知,该模型对于ph验证集及未知样品的预测结果中,所有数据的误差均不超过4%,说明该模型可准确的对口服液的ph进行预测,可为生产中口服液的ph值控制提供极大的技术支持。
- 还没有人留言评论。精彩留言会获得点赞!