一种以纳米金棒为探针检测化妆品中鞣花酸含量的方法与流程
本发明涉及化妆品中鞣花酸含量的检测,具体涉及一种以纳米金棒为探针检测化妆品中鞣花酸含量的方法。
背景技术:
鞣花酸(c14h6o8)是没食子酸的二聚衍生物,是一种多酚二内酯。天然的鞣花酸存在于多种植物的果实中,呈反式没食子酸单宁结构,生物毒性低,具有优异的抗癌变、抗突变功效,特别对结肠癌、食管癌、肝癌等有很好的预防作用。鞣花酸有抑制酪氨酸酶过剩的作用,从而使皮肤雀斑、黄褐斑形成的黑色素难以形成,达到美白皮肤的效果。目前,市面上有多个品牌的化妆品推出了含鞣花酸系列产品,并大力宣传其美白等功效。由于化妆品质量良莠不齐,虚假标准有效成分的情况时有发生,因而对化妆品中鞣花酸含量进行准确测定具有重要的意义。尽管目前已报道了多种检测鞣花酸的方法,如纸色谱分析法、滴定法、分光光度法等,但因化妆品中鞣花酸的含量相对偏低,且存在多种无机和有机杂质的干扰,而上述常规检测方法的灵敏度低,所以其实用性较差。有文献报道采用高效液相色谱法来检测化妆品中鞣花酸的含量,其优点是检测结果精确可靠,但也存在设备投资大、运行成本高、对化验人员要求高、检测耗时等缺点。因此,开发操作简便、快速、灵敏度高、实用性强的鞣花酸检测新方法具有十分重要的意义。
技术实现要素:
为了解决现有技术中的问题,本发明的目的在于提供一种化妆品中鞣花酸含量的检测方法,该方法操作简便、检测时间短、灵敏度高、实用性强。
本发明的目的是这样实现的:
一种化妆品中鞣花酸含量的检测方法,以纳米金棒作为检测探针,利用鞣花酸在纳米金棒表面还原agno3并形成一种棒状的银包金纳米结构,从而导致其局域表面等离子体共振吸收峰发生蓝移,同时做空白试验;根据其峰位移程度与鞣花酸含量所作标准曲线计算化妆品样品中鞣花酸的含量。
本发明化妆品中鞣花酸含量的检测方法,其特征在于:将纳米金棒、agno3溶液与化妆品样品在br缓冲液中反应,反应结束后在紫外-可见光分光光度计上扫描450-900nm的吸收光谱,同时做空白试验;根据吸收峰的位移程度与鞣花酸的含量所作标准曲线,即可算出所述化妆品样品中鞣花酸的含量。
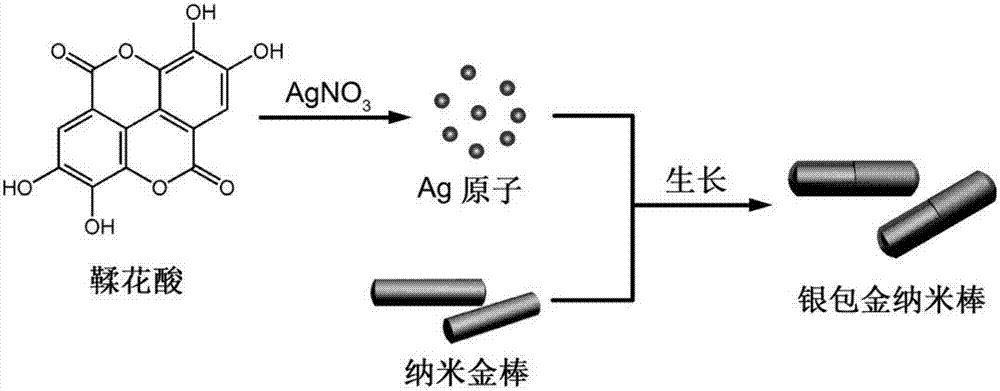
本发明化妆品中鞣花酸的检测原理如图1所示,鞣花酸与agno3进行氧化还原反应(其中鞣花酸为还原剂,agno3为氧化剂),生成的产物(即ag原子)在纳米金棒表面发生异相成核和外延生长,形成一种棒状的银包金纳米结构,从而导致纳米金棒的局域表面等离子体共振吸收峰发生蓝移。
作为优化,上述化妆品中鞣花酸含量的检测方法,其特征在于,采用如下步骤:将纳米金棒、agno3溶液与化妆品样品在br缓冲液中反应,反应时间为17.5~24min;所述br缓冲溶液的ph为8.69~11.92;所述agno3溶液的浓度为1.0×10-5~2.0×10-4mol/l;反应结束后在紫外-可见光分光光度计上扫描450-900nm的吸收光谱,同时做空白试验;根据吸收峰的位移程度与鞣花酸的含量所作标准曲线,即可算出所述化妆品样品中鞣花酸的含量。
作为进一步优化,上述化妆品中鞣花酸含量的检测方法,其特征在于:所述br缓冲溶液的ph为11.4~11.92;所述agno3溶液的浓度为7.5×10-5~1.5×10-4mol/l;所述反应时间为20~24min。
作为更进一步优化,上述化妆品中鞣花酸含量的检测方法,其特征在于,采用如下步骤:将纳米金棒、agno3溶液与化妆品样品在br缓冲液中反应,反应时间为20min;所述br缓冲溶液的ph为11.4;所述agno3溶液的浓度为1.0×10-4mol/l;反应结束后在紫外-可见光分光光度计上扫描450-900nm的吸收光谱,同时做空白试验;所述化妆品样品中鞣花酸含量的按下式计算:
δλ=7.05c+1.62(标准曲线方程)
式中:
δλ为试剂空白与样品的最大吸收波长差值(λ0–λ,单位:nm);
c为样品中鞣花酸的摩尔浓度(单位:μmol/l)。
作为最优化,上述化妆品中鞣花酸含量的检测方法,包括空白试验、样品检测和计算结果步骤,其特征在于:
(1)空白试验:
在1.5ml的离心管中依次加入适量纳米金棒,100μlph为11.40的br缓冲液,100μl5.0×10-4mol/l的agno3溶液,加入二次蒸馏水补充体积至500μl,用可调式混匀仪混匀后室温反应20min,然后在紫外-可见分光光度计上扫描450-900nm的吸收光谱,测得最大吸收波长λ0;
(2)样品检测:
在1.5ml的离心管中依次加入适量纳米金棒,100μlph为11.40的br缓冲液,100μl5.0×10-4mol/l的agno3溶液和100μl化妆品样品,最后加入二次蒸馏水补充体积至500μl,用可调式混匀仪混匀后室温反应20min,然后在紫外-可见分光光度计上扫描450-900nm的吸收光谱,测得最大吸收波长λ;
(3)计算结果:
所述化妆品样品中鞣花酸的含量按下式计算:
δλ=7.05c+1.62(标准曲线方程)
式中:
δλ为试剂空白与样品的最大吸收波长差值(λ0–λ,单位:nm);
c为样品中鞣花酸的摩尔浓度(单位:μmol/l)。
本发明所述br缓冲液即伯瑞坦-罗宾森(britton-robinson)缓冲液,为本领域所熟知的缓冲液。本发明所述化妆品是指以涂抹、喷洒或者其他类似方法,散布于人体表面的任何部位(如皮肤),以达到清洁、保养、美容,保持良好状态为目的的化学工业品或精细化工产品,为本领域所熟知的护肤品。纳米金棒是一种尺度从几纳米到上百纳米的棒状金纳米颗粒,为本领域所熟知的概念,本发明中纳米金棒的用量由本领域普通技术人员根据实际情况确定。
有益效果:
本发明基于纳米金棒独特的结构和局域表面等离子体共振吸收性质,并结合晶种诱导外延生长的基本原理,利用鞣花酸在纳米金棒表面还原agno3并形成一种棒状的银包金纳米结构,通过改变鞣花酸的含量来控制银在纳米金棒表面的外延生长,从而调控其局域表面等离子体共振吸收峰的位移程度,然后根据峰位移程度与鞣花酸含量之间的关系,发明了一种以纳米金棒为探针检测化妆品中鞣花酸含量的方法。本发明方法用于化妆品中鞣花酸含量的检测,化妆品中常见无机、有机物质如氯化钠、醋酸钠、磷酸钠、葡萄糖、氯化钾、草酸钠、乙醇、乙二醇、乙酸、精氨酸、柠檬酸等,对检测结果影响小,方法实用性较强;尤其是化妆品中鞣花酸的浓度在0.2~20μmol/l范围内时,鞣花酸与棒状银包金纳米结构的吸收峰位移程度呈良好的线性关系,标准曲线方程为δλ=7.05c+1.62,相关系数为0.9970,加标回收率为97.4~105.8%,平均加标回收率为103.1%。本发明方法用于化妆品中鞣花酸含量的检测,操作简便,对技术人员要求相对较低;同时检测时间短,准确度好,灵敏度高,实用性强,适合大规模推广。
附图说明
图1为本发明化妆品中鞣花酸含量检测的原理图;
图2为纳米金棒与鞣花酸反应前后的局域表面等离子体共振吸收光谱图;
图3为纳米金棒在加入鞣花酸前后的透射电子显微成像图:(a)加入鞣花酸前,(b)加入鞣花酸后;
图4为本发明中溶液ph对检测信号的影响;
图5为本发明中agno3浓度对检测信号的影响;
图6为本发明中的化学反应动力学考察及检测时间优化;
图7为纳米金棒的吸收光谱随鞣花酸含量变化的位移图;
图8为本发明检测方法的标准曲线图;
图9为本发明检测方法抗干扰能力实验结果图。
具体实施方式
下面通过具体实施例对本发明进行具体描述,在此指出以下实施例只用于对本发明进行进一步说明,不能理解为对本发明保护范围的限制,本领域的技术熟练人员可以根据上述发明内容对本发明作出一些非本质的改进和调整。本发明所有原料及试剂均为市售产品。
仪器与试剂
uv-2500紫外-可见分光光度计(日本岛津公司),mx-s可调式混匀仪(北京大龙兴创实验仪器有限公司),tgl-16m高速离心机(湖南湘仪实验室仪器开发有限公司)。复合鞣花酸精华原液(品牌:艾丽素),纳米金棒(参照文献acsnano2012,6,2804-2817自制),ph8.69~11.92的br缓冲液,硝酸银(国药集团化学试剂有限公司),二甲亚砜(重庆川东化工集团有限公司),甲醇(重庆川东化工集团有限公司),鞣花酸标准品(上海阿拉丁生化科技股份有限公司)。所有试剂均为分析纯,所有水均为二次蒸馏水。
实施例1标准溶液和样品溶液的配制及检测方法
精密称取鞣花酸对照品15.1mg,加入5ml二甲亚砜,并用可调式混匀仪使鞣花酸充分溶解,然后转移到50ml容量瓶中,用甲醇稀释至刻度,摇匀,得到浓度为1.0×10-3mol/l的鞣花酸标准溶液,该标准溶液现配现用。
本发明所使用样品为复合鞣花酸精华液,溶于水,直接用二次蒸馏水稀释至合适的浓度进行检测。
检测方法:在1.5ml的离心管中依次加入100μl纳米金棒(制备得到的原液稀释5倍),100μlph为11.40的br缓冲液,100μl5.0×10-4mol/l的agno3溶液,100μl鞣花酸标准溶液或样品溶液,最后加入二次蒸馏水补充体积至500μl,用可调式混匀仪混匀后室温反应20min,最后在紫外-可见分光光度计上扫描450-900nm的吸收光谱。
参照实施例1标准溶液和样品溶液的配制及检测方法,运行实施例2-7。
实施例2光谱特征考察与检测机理验证
发明人研究了纳米金棒单独存在、与鞣花酸共存、与硝酸银共存、与鞣花酸和硝酸银共存时的局域表面等离子体共振吸收光谱特征,结果显示,与纳米金棒自身的吸收光谱相比,当其与鞣花酸共存、与硝酸银共存均未观察到光谱的变化,仅在纳米金棒、硝酸银和鞣花酸三者共同存在时,光谱才会发生明显的蓝移现象。纳米金棒自身的吸收光谱与纳米金棒、硝酸银和鞣花酸三者共同存在时的吸收光谱见图2。透射电子显微成像结果(图3)进一步证明,三者共存时agno3被鞣花酸还原为ag原子并在纳米金棒表面均匀沉积,形成了一种新型棒状银包金纳米结构,从而改变了其局域表面等离子体共振吸收性质。
实施例3影响因素考察
发明人研究了体系的ph、agno3浓度及检测时间对检测结果的影响,具体如下。
在1.0×10-4mol/l的agno3中加入鞣花酸和不加鞣花酸的条件下,体系在ph8.69~11.92的br缓冲溶液中的最大吸收峰波长变化情况如图4所示。实验结果表明,在ph11.40以下,其吸收峰波长位移差值随ph的增大逐渐增大,ph11.40时其波长位移差值达到最大,超过ph11.40时其位移差趋于稳定,确定该体系最佳ph条件为11.40。
当鞣花酸浓度为5.0×10-5mol/l和不加入鞣花酸时,1.0×10-5~2.0×10-4mol/l浓度范围的agno3对其最大吸收峰位移的影响如图5所示。结果显示,当agno3的浓度为1.0×10-4mol/l时,体系的最大吸收峰波长位移差值最大。
固定agno3浓度为1.0×10-4mol/l和溶液ph11.40,考察了在加入鞣花酸和不加鞣花酸条件下,时间在0~24min内其最大吸收峰波长的变化,结果如图6所示。结果显示,随着反应时间的延长,其吸收峰逐渐蓝移,当反应时间为20min及以后,其吸收峰波长位移基本保持不变,故选择该体系的最佳反应时间为20min。
实施例4标准曲线的绘制
发明人以纳米金棒作为检测探针,利用鞣花酸在纳米金棒表面还原agno3并形成一种棒状的银包金纳米结构,从而导致其局域表面等离子体共振吸收峰发生蓝移,同时做空白试验;根据其峰位移程度与鞣花酸含量所作标准曲线计算化妆品样品中鞣花酸的含量。实验结果如图7所示,空白试验中(即不加鞣花酸),纳米金棒的最大吸收峰波长位于778nm(0号曲线);随着鞣花酸含量的增加(浓度依次为0.2,2.0,5.0,10.0,15.0,20.0μmol/l),其还原agno3的能力大大提高,被还原且均匀沉积在纳米金棒表面的银原子的数量增多(即银壳层增厚),从而使得纳米金棒的局域表面等离子体共振吸收峰逐渐蓝移(对应1-6号曲线)。
体系在最佳实验条件(即br缓冲溶液的ph为11.4,agno3溶液的浓度为1.0×10-4mol/l,反应时间为20min)下,以棒状银包金纳米颗粒的局域表面等离子体共振吸收峰波长位移程度(δλ,nm)对鞣花酸浓度(c,μmol/l)作图,得到标准曲线,如图8所示。其线性回归方程为:δλ=7.05c+1.62,相关系数r=0.9970。鞣花酸的浓度在0.2~20μmol/l范围内与棒状银包金纳米颗粒的局域表面等离子体共振吸收峰波长位移程度呈良好的线性关系。
实施例5化妆品中鞣花酸的检测
试剂空白:在1.5ml的离心管中依次加入100μl纳米金棒(制备得到的原液稀释5倍),100μlph为11.40的br缓冲液,100μl5.0×10-4mol/l的agno3溶液,加入二次蒸馏水补充体积至500μl,用可调式混匀仪混匀后室温反应20min,然后在紫外-可见分光光度计上扫描450-900nm的吸收光谱,测得最大吸收波长位于778nm,即λ0。
样品溶液:在1.5ml的离心管中依次加入100μl纳米金棒(制备得到的原液稀释5倍),100μlph为11.40的br缓冲液,100μl5.0×10-4mol/l的agno3溶液和100μl已稀释20倍后的复合鞣花酸精华液(稀释倍数根据原样品浓度而定,目的是将样品中的鞣花酸浓度稀释至检测线性浓度范围内),最后加二次蒸馏水补充体积至500μl,用可调式混匀仪混匀后室温反应20min,然后在紫外-可见分光光度计上扫描450-900nm的吸收光谱,测得最大吸收波长位于726nm,即λ。
将上述测量结果带入公式δλ=7.05c+1.62,即778–726=7.05c+1.62,可计算出c=7.146μmol/l,即测试的样品溶液中鞣花酸的浓度为7.146μmol/l。由于测试样品溶液为样品原液稀释20倍所得,故原样品中鞣花酸的浓度为7.146×20=142.9μmol/l。
实施例6干扰实验
发明人还考察了化妆品中其他可能共存的物质对本发明检测方法的干扰情况,如图9所示,主要考察了只存在鞣花酸(1号)、鞣花酸与氯化钠共存(2号)、鞣花酸与醋酸钠共存(3号)、鞣花酸与磷酸钠共存(4号)、鞣花酸与葡萄糖共存(5号)、鞣花酸与氯化钾共存(6号)、鞣花酸与硝酸镁共存(7号)、鞣花酸与草酸钠共存(8号)、鞣花酸与乙醇共存(9号)、鞣花酸与乙二醇共存(10号)、鞣花酸与乙酸共存(11号)、鞣花酸与l-精氨酸共存(12号)、鞣花酸与柠檬酸共存(13号)所获得信号的差值,用于说明样品中可能存在的常见干扰物质对该方法的影响。实验结果表明:当鞣花酸的浓度固定为2.0×10-5mol/l时,体系中分别存在100倍或50倍于鞣花酸浓度的以上所述干扰物质,均不干扰测定,可见本发明所建立的检测化妆品中鞣花酸的方法具有较好的抗干扰能力。
实施例7加标回收实验
为了考察该检测方法的准确性和实用性,发明人购买了商品化的复合鞣花酸精华液(品牌:艾丽素)并采用逐级稀释法将其稀释至测定的线性范围内,按照实施例5的实验方法对其中的鞣花酸含量进行测定,样品平行测定3次,且同时进行加标回收实验,结果见表1。
表1鞣花酸样品分析及回收率实验结果
从表1可看出,本发明方法准确度高、实用性强,可用于美白化妆品中鞣花酸含量的定量检测,加标回收率为97.4~105.8%,rsd为0.97~2.00。
- 还没有人留言评论。精彩留言会获得点赞!