一种食用油中游离脂肪酸的测定方法与流程
本发明涉及食用油质量控制技术领域,特别是涉及一种食用油中游离脂肪酸的测定方法。
背景技术:
食用油中的游离脂肪酸(ffa)主要产生于其加工与储存过程中。游离脂肪酸发生变质就会产生对人体有害的h2o2。因此,食用油中游离脂肪酸的含量(总含量)通常作为评估食用油质量和经济价值的一项很重要的参数。目前检测的标准方法主要有美国油品化学学会(aocs)、欧共体(ec)以及我国的国家标准方法(gb/t5530-2005),这些方法大同小异,都推荐将样品溶解在乙醇中,使用强碱作为滴定剂,酚酞为指示剂对游离脂肪酸含量进行测定。滴定方法不仅存在耗时、耗溶剂等缺点,而且当待测油样品颜色较深时通过滴定方法很难判断其滴定终点。有鉴于此,如何能够更快速的检测食用油中的游离脂肪酸成为本领域技术人员亟待解决的问题。
技术实现要素:
纳米金(aunps)是指直径在1~100nm的金的微小颗粒,研究发现,当纳米金粒径在10-50nm的范围内时,纳米金溶液呈红色。而当纳米金发生聚集后,其表面等离子体共振吸收带发生红移,相应地,纳米金溶液颜色经历由红色变为蓝色,这种变化用肉眼就可以观察。更重要的是,它们的摩尔消光系数很高,比常规有机染色剂高三个数量级,因此检测灵敏度高。
阳离子聚合物的表面一般或在一定条件下会带有正电荷,这个特性可以引起分散态的纳米金发生聚集,形成聚集态的纳米金,从而改变纳米金溶液的颜色,使纳米金溶液颜色由红色(分散态)变为蓝色(聚集态)。
本发明研究发现微摩尔浓度(um)级别的阳离子聚合物,尤其是整代的树枝状聚酰胺胺很容易让纳米金发生聚集现象;纳米金(分散态)溶液颜色为红色,中心吸收波长在520nm;当向其中加入一定浓度的阳离子聚合物,例如1代的树枝状聚酰胺胺(pamamg1.0)大分子后,大分子使纳米金颗粒发生了聚集现象,造成了纳米金溶液颜色在短时间内,例如3-5秒钟变为蓝色,此时中心最大吸收波长转移到650nm。当向纳米金(分散态)溶液中加入浓度相同但链长不同的脂肪酸,再加入上述的阳离子聚合物时,发现丁酸和己酸对聚集几乎没有抑制作用,加入pamam后溶液立即变蓝;但是,随着碳链长度的增加,加入的脂肪酸对聚集的抑制作用也增大,表现为溶液的颜色没有完全变蓝,还保持一定程度的红色,即可以不同程度地抑制这种聚集的发生。本发明研究进一步发现,碳链长度为c16-c18的脂肪酸对纳米金的聚集抑制能力接近;同时,食用油中的脂肪酸主要为棕榈酸(c16-0)、硬脂酸(c18-0)、油酸(c18-1)和亚油酸(c18-2)(gb19111-2003;journalofagriculturalandfoodchemistry,2011,59,10775-10780),有鉴于此,本发明实施例提供了一种食用油中游离脂肪酸的测定方法,以实现能够更快速的检测食用油中的游离脂肪酸。具体技术方案如下:
本发明第一方面提供了一种食用油中游离脂肪酸的测定方法,其包括:
(1)用萃取剂萃取食用油中的游离脂肪酸,得到含有游离脂肪酸的待测萃取相,其中,所述萃取剂的体积与食用油的体积相同;
(2)取指定体积的所述待测萃取相,将其与纳米金溶液和阳离子聚合物溶液混合,至颜色不再变化,得到待测比色体系;
(3)将所述待测比色体系的颜色与标准比色体系的颜色进行对比,确定食用油中游离脂肪酸的含量范围;
其中,所述标准比色体系通过以下方法确定:
用所述萃取剂与脂肪酸标准品配制不同脂肪酸含量的标准溶液,所述标准溶液中的脂肪酸含量已知,所述脂肪酸标准品选自c16-c18的脂肪酸;
分别取所述指定体积的所述标准溶液,将其与纳米金溶液和阳离子聚合物溶液混合,至颜色不再变化,得到标准比色体系;所述标准比色体系及所述待测比色体系的体积相同;且所述标准比色体系中纳米金和阳离子聚合物的浓度分别与所述待测比色体系中纳米金和阳离子聚合物的浓度相同。
在本发明第一方面的一种具体实施方式中,在步骤(3)中,确定食用油中游离脂肪酸的含量范围,具体为:当所述待测比色体系的颜色介于两个相邻脂肪酸含量的标准溶液所对应的标准比色体系的颜色之间时,确定食用油中游离脂肪酸的含量在所述两个相邻脂肪酸含量之间。
在实际应用中,可以根据国家标准规定的食用油酸度值上限配制不同脂肪酸含量的标准溶液,比如,国家标准gb19111-2003规定一级、二级、三级及四级压榨成品食用玉米油的酸度值(以koh计,mg/g)应不超过0.2,0.3,1.0,3.0;对应的标准溶液中的脂肪酸含量以脂肪酸摩尔浓度表示,分别为4.46mm,6.70mm,22.3mm以及67.0mm。在此情况下,在步骤(3)中,可以将待测比色体系的颜色与例如一级、二级、三级及四级标准所对应的标准比色体系的颜色进行比较;当待测比色体系的颜色在相邻两个级别所对应的颜色之间时,就可以确定食用油中的游离脂肪酸的含量在该相邻两个级别之间,可以实现半定量的含量测定。在本发明中,所说的所述待测比色体系的颜色介于两个相邻脂肪酸含量的标准溶液所对应的标准比色体系的颜色之间,可以理解为所述待测比色体系所呈现的红色相(蓝色相)介于两个相邻脂肪酸含量的标准溶液所对应的标准比色体系所呈现的红色相(蓝色相)之间。
在本发明第一方面的一种具体实施方式中,脂肪酸标准品选自棕榈酸、硬脂酸、油酸和亚油酸中的至少一种。
在本发明的一种具体实施方式中,在配制出标准比色体系后,可以将其颜色通过任选的方式记录于载体上,例如可以记录在卡片或板材上,制作为具有标准比色体系颜色的标准比色卡或标准比色板;这样可以长时间保存住标准比色体系的颜色,当需要检测待测比色体系的颜色范围时,只要将其与标准比色卡或标准比色板的颜色对比即可。需要说明的是,所说的载体除了可以是卡片或板材外,还可以其它任何适于呈现标准比色体系颜色的材质的载体。
在本发明的一种具体实施方式中,所述待测比色体系的颜色与标准比色体系的颜色具体可以用待测比色体系与标准比色体系各自的紫外-可见吸收光谱的吸光度峰值来表示。具体地,可以通过520nm处吸光度值a520来表示,或通过通过650nm处吸光度值a650来表示。在此实施方式中,当所述待测比色体系的a520介于两个相邻脂肪酸含量的标准溶液所对应的标准比色体系的a520之间时,确定食用油中游离脂肪酸的含量在所述两个相邻脂肪酸含量之间。或当所述待测比色体系的a650介于两个相邻脂肪酸含量的标准溶液所对应的标准比色体系的a650之间时,确定食用油中游离脂肪酸的含量在所述两个相邻脂肪酸含量之间。
为了进一步缩短食用油中脂肪酸的测定时间,可以预先将标准比色体系的吸光度峰值,例如a520或a650记录下来,当检测时,可以在确定待测比色体系的吸光度峰值,例如a520或a650后,直接与已记录的标准比色体系的吸光度峰值进行比较即可;方便、快速。
在本发明的技术方案中,萃取剂应选择能够充分地、将游离脂肪酸从食用油中萃取出来,即使游离脂肪酸从食用油中转移至萃取剂中,形成含有脂肪酸的萃取相,以便于检测。基于此,在本发明第一方面的一种具体实施方式中,萃取剂为甲醇与水的混合溶剂,优选地,所述萃取剂中甲醇与水的体积比为2:1,即所述萃取剂由体积比为2:1的甲醇与水的混合而成。
在本发明第一方面的一种具体实施方式中,所述纳米金溶液中所含的纳米金的粒径范围为10-50nm;优选为10-20nm,更优选为13nm。在本发明中,对纳米金的来源不进行限定,例如,可以采用还原法制备纳米金溶液;在还原法制备纳米金的过程中,氯金酸在原还剂的作用下,聚成一定大小的纳米金颗粒,形成带负电的纳米金疏水胶溶液,该纳米金疏水胶溶液即可作为纳米金溶液使用。常见的还原法有白磷还原法、抗坏血酸还原法、柠檬酸钠还原法及鞣酸-柠檬酸钠还原法等。本领域技术人员可以根据实际需,例如纳米金的粒径来确定具体的还原法,本发明在此不进行确定。
本发明的阳离子聚合物溶液可以通过将阳离子聚合物溶解于溶剂中而获得,所用的溶剂可以选择水或有机溶剂,所述有机溶剂可以非限定地选自甲醇、乙醇或乙腈等。
在本发明第一方面的一种具体实施方式中,阳离子聚合物选自但不限于树枝状聚酰胺胺(pamam)、超支化聚丙烯亚胺(poly(propyleneimine),ppi),超支化聚乙烯亚胺(pei),多熔素(polylysine)以及壳聚糖(chitosan)中的至少一种;在本发明第一方面的另一种具体实施方式中,阳离子聚合物选自树枝状聚酰胺胺;在本发明第一方面的再一种具体实施方式中,阳离子聚合物选自1代、2代、3代和/或4代的树枝状聚酰胺胺。对于树枝状聚酰胺胺的制备方法,本发明在此不进行限定。
在本发明第一方面的一种具体实施方式中,在所述待测比色体系和所述标准比色体系中,纳米金的浓度为4.6×10-10m至1.04×10-9m,优选为6.0×10-10m至1.0×10-9m;阳离子聚合物的浓度为0.05-0.3um,优选为0.1-0.2um。
在步骤(2)中,当将指定体积的待测萃取相与纳米金溶液和阳离子聚合物溶液混合后,纳米金在阳离子聚合物以及待测萃取相中的脂肪酸的作用下会改变颜色;一般地,在将纳米金溶液和阳离子聚合物溶液与待测萃取相混合后,振荡混合大约3-5分钟,颜色基本稳定不再变化。在本发明的一种具体实施方式中,将待测萃取相与纳米金溶液和阳离子聚合物溶液混合,具体优选为:先将待测萃取相与纳米金溶液混合,混匀后,再加入阳离子聚合物溶液;
将标准溶液与纳米金溶液和阳离子聚合物溶液混合,具体优选为:先将标准溶液与纳米金溶液混合,混匀后,再加入阳离子聚合物溶液。
在本发明第一方面的一种具体实施方式中,尤其是以pamam作为阳离子聚合物时,所述待测比色体系和所述标准比色体系中的ph值为4-10,优选在ph值为4.6-7.2,在此范围内,体系对脂肪酸的含量都有响应,更优选为ph值为5.2,此时的灵敏度最高。在此ph值内,更适于进行脂肪酸的检测。
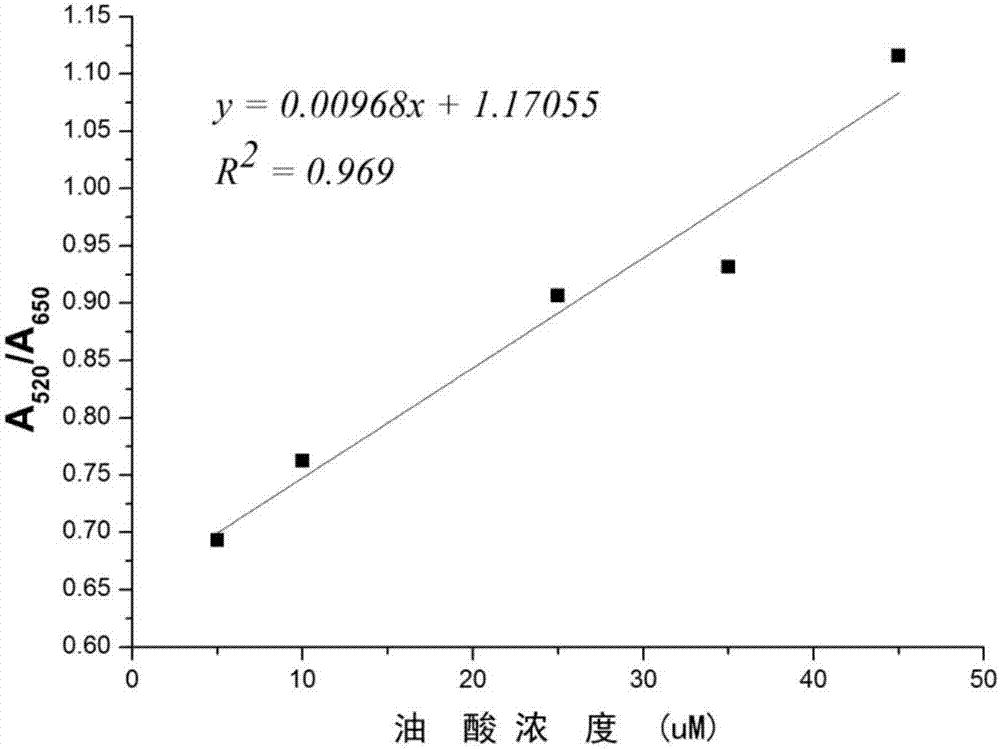
发明人在前述的研究基础上进一步研究发现,当将纳米金溶液和阳离子聚合物溶液混合,组成纳米金-阳离子聚合物体系后,向其中加入脂肪酸,脂肪酸的浓度影响pamam对aunps抑制能力,浓度越大,抑制能力越大,表现为随着脂肪酸浓度的增加,聚集态aunps在650nm处的吸收值降低,同时,分散态aunps处于520nm的吸收值增加,如图1所示。将抑制能力以分散态的aunps的最大吸光度a520与聚集态的最大吸光度a650的比值a520/a650来衡量,并将其与所加入的脂肪酸(以油酸为例)的浓度作图,发现在一定的浓度范围内呈线性关系,如图2所示。说明基于这种原理可以对脂肪酸的含量进行定量检测。紫外光谱的研究进一步证明,如果利用比色法检测,以520nm处和650nm处吸光度的比值a520/a650(y)对脂肪酸的浓度(x,μm)作线型回归(5个浓度水平),校正曲线的斜率相近,如表1所示,亦即这四种脂肪酸的灵敏度相近。
表1碳链长度为c16-c18的检测线性范围及校正曲线
基于上述的研究,本发明第二方面提供了一种食用油中游离脂肪酸的定量测定方法,其包括:
(a)向n份萃取剂中的n-1份分别加入不同已知量的脂肪酸标准品,获得n份脂肪酸标准品含量不同的标准溶液;n份标准溶液的体积相同,n≥3;所述脂肪酸标准品选自c16-c18的脂肪酸;
(b)用n份标准溶液分别萃取n份食用油中的游离脂肪酸,得到n份待测样品萃取相,其中,食用油的体积与标准溶液的体积相同;
(c)从n份待测样品萃取相中,分别获取体积为v1的测试溶液;将n份测试溶液中分别与纳米金溶液和阳离子聚合物溶液混合,至颜色不再变化,得到n份体积为v0的待测样品溶液;在所有的待测样品溶液中,纳米金的浓度相同,且阳离子聚合物的浓度相同;
(d)将体积为v1的的萃取剂和纳米金溶液和阳离子聚合物溶液混合,至颜色不再变化,得到体积为v0的空白样品溶液;所述空白样品溶液中的纳米金的浓度及阳离子聚合物的浓度分别与待测样品溶液相同;
(e)分别对n份待测样品溶液及空白样品溶液进行紫外-可见吸收光谱测试;确定每份待测样品溶液在520nm处和650nm处吸光度的比值a520/a650;
(f)以a520/a650为纵坐标,以待测样品溶液中加入的脂肪酸标准品的含量为横坐标,绘制标测样品溶液的标准加入曲线,所述横坐标与纵坐标的交点处的纵坐标的值为空白样品溶液的a520/a650;并根据公式
需要说明的是,阳离子聚合物虽然使纳米金溶液的颜色变蓝,但是并没有使所有纳米金颗粒产生团聚,还有部分处于分散态的纳米金颗粒;因此,即使测试体系只包含萃取剂、纳米金溶液及阳离子聚合物溶液,其吸光度的比值a520/a650也不为0。基于此,在本发明的技术方案中,将空白样品溶液的a520/a650作为横坐标与纵坐标的交点处的纵坐标的值,交点处的横坐标的值仍然为0。
需要说明的是,本文中,所说的食用油中的游离脂肪酸的含量指的是食用油中的游离脂肪酸的总含量,也称酸度值。
在本发明第二方面的一种具体实施方式中,脂肪酸标准品选自棕榈酸、硬脂酸、油酸和亚油酸中的至少一种。
在本发明第二方面的一种具体实施方式中,所述萃取剂为甲醇与水的混合溶剂,优选地,所述萃取剂中甲醇与水的体积比为2:1。
在本发明第二方面的一种具体实施方式中,所述纳米金溶液中所含的纳米金的粒径范围为10-50nm;优选为10-20nm,更优选为13nm。
在本发明第二方面的一种具体实施方式中,阳离子聚合物选自树枝状聚酰胺胺、超支化聚丙烯亚胺、超支化聚乙烯亚胺、多熔素及壳聚糖中的至少一种;优选地,阳离子聚合物选自树枝状聚酰胺胺;更优选地,阳离子聚合物选自1代、2代、3代和/或4代的树枝状聚酰胺胺。
在本发明第二方面的一种具体实施方式中,在所述待测样品溶液中,纳米金的浓度为4.6×10-10m至1.04×10-9m,优选为6.0×10-10m至1.0×10-9m;阳离子聚合物的浓度为0.05-0.3um,优选为0.1-0.2um。
在本发明第二方面的一种具体实施方式中,将测试溶液与纳米金溶液和阳离子聚合物溶液混合,具体为:先将测试溶液与纳米金溶液混合,混匀后,再加入阳离子聚合物溶液。发明人发现,按此顺序进行混合时,紫外光谱分析的线性关系更好。
在本发明第二方面的一种具体实施方式中,所述待测比色体系、所述标准比色体系和所述待测样品溶液中的ph值为4-10,优选在ph值为4.6-7.2,在此范围内,体系对脂肪酸的含量都有响应,更优选为ph值为5.2,此时的灵敏度最高。在此ph值内,更适于进行脂肪酸的检测。
在本发明第二方面的一种具体实施方式中,待测样品溶液中脂肪酸标准品的含量≤10μm。
需要说明的是,本发明第二方面与第一方面相关的内容可以参照第一方面的记载,本发明在此不再进行赘述。
进一步需要说明的是,本文中所说的“含量”是指特定物质中所包含的某种成分的量,例如,食用油中包含游离脂肪酸的量,或待测样品溶液中包含脂肪酸标准品的量等。在本文中,有时可能也称含量为浓度,尤其是在同一计算公式或与其类似的场景中同时出现含量及浓度时,应当将浓度与含量作为同一概念,浓度与含量具有相同的单位。
本发明实施例提供的食用油中游离脂肪酸的测定方法,可以实现半定量或定量的测定食用油中游离脂肪酸的含量。并具有以下优点:
(1)本发明分析时间短,可以在几分钟内完成半定量分析,与滴定方法相比,检测更快速。
(2)本发明使用有机溶剂的量少,绿色环保。
(3)由于aunp有极高的摩尔消光系数,本发明定量分析的灵敏度非常高。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
图1为油酸浓度对纳米金-阳离子聚合物体系可见光谱的影响,其中,曲线1-6对应的体系中,纳米金的浓度为6.5×10-10m,pamamg1.0的浓度为0.13um;曲线1-6对应的体系中,油酸的浓度分别为:0、5um、10um、20um、35um、45um;曲线7为浓度6.5×10-10m的纳米金溶液;
图2为不同浓度的油酸对应的纳米金-阳离子聚合物体系的a520/a650的校正曲线图,其中,纳米金-阳离子聚合物体系中的纳米金的浓度均为6.5×10-10m,pamamg1.0的浓度均为0.13um;
图3为实施例2制备的pamamg1.0核磁谱图(400mhz,cdcl3,ppm),
峰归属:δ2.35(m,8h,nch2ch2conh),2.40(s,1,4h,nch2ch2n),2.65(m,8h,conhch2ch2nh2),2.81(m,8h,nch2ch2conh),3.27(m,8h;conhch2)。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
需要说明的是,以下实施例虽然是以pamamg1.0为例作为阳离子聚合物进行说明本发明的技术方案,但是,对于其它整代数的pamam,尤其是2-4代的pamam,以及超支化聚丙烯亚胺、超支化聚乙烯亚胺、多熔素及壳聚糖等阳离子聚合物,也同样可以实现本发明的技术方案。
实施例1纳米金溶液的制备
将1ml1%haucl4加入到250ml的圆底烧瓶中,加入99ml的三次蒸馏水。在磁力搅拌下加热,待沸腾后向其中快速加入1.5ml的1%柠檬酸钠溶液作为还原剂,待颜色由浅黄色经蓝色再变至酒红色(溶液回流25min)后停止搅拌至溶液冷却。将此纳米金溶液转移至100ml容量瓶中,用三次水稀释至刻度线后避光储存在4℃冰箱中。此纳米金溶液浓度用光谱法测定为8.5×10-10m。
实施例2pamam的制备
以乙二胺为核,甲醇为反应溶剂,采用发散法向外扩增。室温下乙二胺首先与过量的丙烯酸甲酯进行迈克尔加成反应24小时,产物在50℃减压除杂。第一步得到的酯再与过量的乙二胺在室温下进行氨基化反应72小时,产物在72℃减压除杂,得到0代树枝状大分子。交替重复迈克尔加成反应和氨基化反应可以得到1.0代树枝状大分子。产品经除杂、干燥后冷冻保存。通过核磁共振波谱(abrukeradvanceⅲ-400mhznmrspectrometer,rheinstettengermany)进行表征。结果如图3所示。将所制备的pamamg1.0制备成浓度为0.53um的水溶液。
实施例3食用玉米油中游离脂肪酸的半定量检测
萃取剂为甲醇与水的混合溶液,体积比为2:1.将等体积(都为1ml)的萃取剂与食用玉米油混合,振荡3分钟,待分层后将待检测萃取相与食用玉米油分离。
在5ml的具塞玻璃瓶中加入1.5ml实施例1制备的纳米金溶液,在搅拌条件下加入10μl待检测萃取相,待充分混合后,加入490μl浓度为0.53um的pamamg1.0树枝状大分子(实施例2制备),充分混合待颜色稳定后,得到待测比色体系(待测比色体系中pamamg1.0最终浓度为0.13um,纳米金的浓度为6.5×10-10m)。
根据国家标准规定的食用油酸度值上限配制游离脂肪酸的标准溶液,国家标准gb19111-2003规定一级、二级、三级及四级压榨成品食用玉米油的酸度值(以koh计,mg/g)应不超过0.2,0.3,1.0,3.0;对应的脂肪酸摩尔浓度分别为4.46mm,6.70mm,22.3mm以及67.0mm。以油酸作为脂肪酸标准品,将油酸溶解于萃取剂,制得上述浓度的4份标准溶液。在5ml的具塞玻璃瓶中分别加入1.5ml实施例1制备的纳米金溶液,在搅拌条件下加入10μl标准溶液,待充分混合后,加入490μl浓度为0.53um的pamamg1.0树枝状大分子(实施例2制备),充分混合待颜色稳定后,得到4份标准比色体系(待测比色体系中pamamg1.0最终浓度为0.13um,纳米金的浓度为6.5×10-10m)。
将待测比色体系与4份标准比色体系的颜色对比可知,待测比色体系的颜色比一级玉米油所对应的标准比色体系的颜色更蓝,因此确定所测量的食用玉米油中脂肪酸含量没有超过一级压榨成品使用玉米油的脂肪酸含量(酸度值)。
实施例4食用玉米油中游离脂肪酸的定量检测
萃取剂为甲醇与水的混合溶液,体积比为2:1。向5个2ml具塞玻璃瓶中分别加入0.5ml油酸的萃取剂溶液,其中油酸的浓度分别为0,400,800,1200,1600μm。再分别向上述瓶中加入0.5ml食用玉米油,混合后振荡3分钟,待分层后将萃取相与食用玉米油分离,得到5份待测样品萃取相。在5ml的具塞玻璃瓶中分别加入1.5ml实施例1制备的纳米金溶液,在搅拌条件下加入10μl上述待测样品萃取相(测试溶液),待充分混合后,加入490μl浓度为0.53um的pamamg1.0树枝状大分子(实施例2制备),充分混合待颜色稳定后,得到5份待测样品溶液;
在5ml的具塞玻璃瓶中先后加入1.5ml实施例1制备的纳米金溶液,10μl萃取剂及490μl浓度为0.53um的pamamg1.0树枝状大分子(实施例2制备),充分混合待颜色稳定后,得到空白样品溶液;
用紫外可见分光光度计(uv-2450,岛津,日本)对各待测样品溶液及空白样品溶液进行吸光度测定,紫外光谱扫描范围为400-900nm,并以520nm处和650nm处吸光度的比值a520/a650(y)对待测样品溶液中的油酸含量(浓度)(x,μm)作图,绘制标测样品溶液的标准加入曲线,所述横坐标与纵坐标的交点处的纵坐标的值为空白样品溶液的a520/a650,其值为0.58;横坐标的值为0μm;确定标准加入曲线与横坐标的交点处的含量值c=…15.25μm;v1=10μl;v0=2000μl;并根据公式
对比例1标准滴定法测定食用玉米油中游离脂肪酸含量
脂肪酸总含量的测量参照国家标准gb/t5530-2005进行检测:
(1)精确称取一定量食用玉米油(实施例4中检测所用的油)置于锥形瓶中,加入50ml95%乙醇。
(2)加入2ml1%的酚酞指示剂,酚酞指示剂用95%的乙醇配制,之后让食用植物油和乙醇充分混合。
(3)用0.01m氢氧化钾标准溶液进行滴定,一边滴一边摇匀,直到溶液变成粉红色保持30s不变。
测量三次,得结果如下表:
表2食用玉米油中脂肪酸的滴定法测量
从实施例4及对比文件1的检测结果来看,本发明提供的定量检测方法与传统滴定法的测量结果接近,因此,可以代替传统的滴定法用于对食用油中的游离脂肪酸的含量进行检测。
以上对本发明所提供的一种食用油中游离脂肪酸的测定方法进行了详细介绍。本文中应用了具体实施例对本发明的原理及实施方式进行了阐述,以上实施例的说明只是用于帮助理解本发明的方法及其中心思想。应当指出,对于本领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也落入本发明权利要求的保护。
- 还没有人留言评论。精彩留言会获得点赞!