电化学发光分析装置和使用其分析样品的方法与流程
本发明涉及电化学发光分析装置和使用其分析样品的方法,具体而言涉及利用电化学发光现象的分析方法和装置。本发明特别适合于定量床边快速诊断。
背景技术:
目前,对于快速、灵敏和定量诊断技术有大量需求。这类技术适合于广泛的市场领域,包括公共卫生、研究、种植、环保、兽医和某些工业制造领域。改善的灵敏度、速度、稳健性、稳定性和降低的每次分析的费用是考虑因素,在诊断技术中实现这些因素之后,可以在非常新的领域中找到用途。
极高灵敏度可以用某些诊断仪器获得,但其太昂贵。另一方面,某些方法可能足够便宜(由免疫色谱法所示例),但其不适用于市场的某些需求。满足一组此类需求的任何技术都将在未来诊断中具有重要位置和巨大市场潜力。
在诊断实用中有许多不同的分析原理:例如,基于放射活性的测定、酶联免疫吸附测定(elisa)、比色测定和基于荧光和化学发光(包括阳极以及热电子诱导(阴极)电化学发光(ecl))的测定。热电子诱导ecl详细记载于kulmalas.等人的美国专利6,251,690号。这些技术各自对于灵敏度、稳健性、稳定性、速度和价格的整合具有其作用。技术之间的差异反映了物理限制的作用或方法的优点。例如,从安全性和环境二者角度来看,基于放射活性化合物的应用的缺陷在于标记在一段时间内衰减和放射活性废弃物的额外费用。诊断上最灵敏测定的应用受到测试和仪器复杂性的限制,只有专家才能进行该测定。测定的复杂性通常与仪器和/或测试的价格成正比。在复杂仪器的情况中,可以举出现在变得越来越流行的阳极电化学发光技术:仪器是复杂的实验室机器人,其操纵需要专业人员,并且其中测量过程涉及重复的洗涤和制备步骤。它们是增加分析费用以及增加废弃物量的因素,因此会使该方法无法满足小实验室、医务室等的需求(床边或护理分析点)。
商业上有利的方法基于通过所谓的标记物质在混合物中鉴定和测量待分析物质的原理。在基于生物分子的独特性质的测量中,如在免疫化学测定中,待测量分析物(x)可以选择性地从分子混合物吸附到固相结合抗体,然后使用选择性结合到(x)的另一标记抗体测量结合的分子。标记物质可以为共价地连接到抗体的放射活性同位素、酶、吸光、荧光或磷光分子、特定金属螯合物等。作为另选,可以标记纯化的(x),并通过竞争反应可以测量未知的未标记样品(x)的量。dna和rna的测定也可以基于选择性结合(生物亲和性)。通过相同原理也可以进行许多其他化学和生化分析。为了减少费用和/或提高测量准确度,目前有在样品中同时测量多个不同参数的趋势。一种可能性是使用在不同波长发荧光或磷光(发光)或者拥有不同荧光寿命的标记。可以用于免疫诊断的不同测量原理和策略记载于书籍theimmunoassayhandbook,editedbydavidwild,stocktonpressltd.,newyork,1994,onpages1-618。
现有技术中已知有机物质和金属螯合物可有利地作为标记物质,并且其可以通过光或通过电化学激发而产生对标记具有特异性的发光。这些方法特别灵敏并且很合适。不过,因为测量浓度极低,也有案例依赖性的难题;荧光的使用可能受到干扰,特别是通过丁达尔、瑞利和拉曼散射。当测量生物物质时,几乎毫无例外地,在激发脉冲后,有快速释放高背景荧光。主要仅使用镧系离子和专门合成的有机分子之间的螯合物,可以利用溶液相中的磷光。使用光致发光标记的激发技术的缺陷在于仪器的复杂性和灵敏光学部件的高价格。
通常,ecl的优点在于电激发部件的低价格和更简单的光学元件。与光致发光相比,可以避免多种缺陷。使用惰性金属电极的传统阳极电化学发光可以使用有机发光体通过相对简单的仪器在非水性溶剂中进行。不过,在聚集了最大的商业期望的生物亲和性测定中,采用水溶液。生物样品几乎总是在非有机溶液中采集,因此测量体系应工作在水性溶液中或至少在胶束水溶液中。仅仅非常有限数量的传统金属螯合物可作为在阳极ecl中的ecl标记在水或胶束溶液中工作。
至今阳极ecl的商业上最重要的分析化学应用是使用ru(bpy)32+螯合物的衍生物的方法,其中,标记的检测阶段发生在胶束相中。由教科书可知,由于胶束平衡的不受控制的复杂性,胶束混合物总是易于受到不同干扰影响。因此不依赖于胶束的热电子诱导ecl相对于阳极ecl具有许多关键优点。其可以应用于免疫杂交和dna杂交方法(参见blackburn,g.,etal.,1991,clin.chem.37:1534-1539;kenten,j.,etal.1992,clin.chem.33:873-879)。rochediagnosticsltd.的免疫测定和dna或rna探针应用利用了磁性颗粒,由此标记物质被带到金工作电极上(massey;richardj.,etal.u.s.pat.no.5,746,974;leland;jonathank.,etal.u.s.pat.no.5,705,402)。不过磁性胶乳颗粒的可再现操纵在许多方面都很困难,因此该方法仅用于昂贵的具有复杂和精密的液体操纵系统的实验室机器人(例如elecsys1010和2010)。此外,永久性大块金工作电极在每次分析之间需要长时间的清洁和预处理(elecsysservicemanual,p.70)。
尽管在很多方面良好,然而热电子诱导ecl在生物亲和性测定中的缺陷是为了使反应分子达到平衡而需要长时间温育。根据本发明,如权利要求1-10所述,利用将薄多孔膜置于工作电极上(后文称为cipf装置),可以获得性能的显著改善。
技术实现要素:
本发明提供一种电化学发光分析装置,其包含:
一种材料的工作电极;
位于所述工作电极上或者适合于能够移动到所述工作电极上的固体多孔膜;和
支架,
其中:
所述工作电极的材料为由电绝缘体层覆盖的导体或强掺杂半导体,
所述装置的工作电极被支撑到所述支架,经由所述支架,所述工作电极能够连接到发光测量仪器的激发电子设备,
所述工作电极充当所述装置的阴极,
所述固体多孔膜由附着至保持其形状的框架的pe聚酯材料制成,其具有液体渗透性,厚度小于100μm,并且孔径为1μm,其中,所述固体多孔膜位于所述工作电极附近,但不与所述工作电极直接接触,
在所述工作电极与所述多孔膜之间存在小于100μm的游离液体结,
所述装置适合于使被带到所述多孔膜和/或阴极上的样品和其他试剂能够相互反应。
优选的是,所述阴极工作电极由硅或铝制成,并且所述硅或铝的表面含有氧化物层。
优选的是,所述工作电极上的多孔膜的厚度为1-20μm,并且在生物亲和性反应期间和在电致发光测量期间所述多孔膜和工作电极经由溶剂连接而接触。
优选的是,所述工作电极的表面或所述工作电极上的多孔膜,或它们的组合体,涂覆有适合于与期望的待分析分子结合的生物亲和性分子。
优选的是,在测量过程之前,所述装置上的特异性反应分子以固体或无定形状态储存在所述装置的表面上。
优选的是,所述装置为测试条装置,所述工作电极形成所述测试条装置的结构基础,所述工作电极和/或多孔膜涂覆有生物吸附剂,含有干燥的带标记生物分子的多孔膜适合于与所述工作电极接触。
优选的是,所述工作电极涂覆有能够机械移动的多孔膜。
优选的是,所述工作电极的表面或所述工作电极上的多孔膜,或它们的组合体,涂覆有适合于与期望的待分析分子结合的生物亲和性分子。
优选的是,所述装置为测试条装置,所述工作电极形成所述测试条装置的结构基础,所述工作电极和/或多孔膜涂覆有生物吸附剂,含有干燥的带标记生物分子的多孔膜适合于与所述工作电极接触。
优选的是,所述电绝缘体层的厚度为1-10nm。
本发明还提供一种使用电化学发光分析装置分析样品的方法,所述装置包含:
一种材料的工作电极;
位于所述工作电极上或者适合于能够移动到所述工作电极上的多孔膜;和
支架,
在所述装置中,所述工作电极的材料为由电绝缘体层覆盖的导体或强掺杂的半导体,所述装置的工作电极被支撑到所述支架,经由所述支架,所述工作电极可以连接到发光测量仪器的激发电子设备,所述工作电极充当所述装置的阴极,所述多孔膜由附着至保持其形状的框架的pe聚酯材料制成,其具有液体渗透性,厚度小于100μm,并且孔径为1μm,其中,所述固体多孔膜位于所述工作电极附近,但不与所述工作电极直接接触,所述电激发发生在离所述导体至少3nm处,
所述方法包括:
将待分析样品带到所述多孔膜上,并使所述样品与带到所述多孔膜和/或所述阴极上的其他试剂反应,
向经反应的样品施加激发脉冲,其中,所述经反应的样品产生发光信号;和
对于所关注的分析物的量,分析所述发光信号。
在所述方法中,优选的是,所述工作电极上的多孔膜的厚度为1-20μm,并且在反应期间和在发光分析测量期间所述膜和所述电极经由溶剂连接而接触。
在所述方法中,优选的是,,所述方法包括在进行所述发光分析测量之前除去所述多孔膜。
在所述方法中,优选的是,所述装置为测试条装置;所述工作电极形成所述测试条装置的结构基础;所述工作电极和/或所述多孔膜涂覆有生物吸附剂;并且所述多孔膜含有干燥的带标记生物分子,
在所述方法中,优选的是,所述方法包括:使含有所述干燥的带标记生物分子的所述多孔膜与所述工作电极接触;将样品和/或缓冲液带到所述多孔膜上以引发生物亲和性反应;使所述生物亲和性反应继续;停止所述生物亲和性反应;从所述工作电极除去所述多孔膜;和使用电致发光仪器进行测量。
在所述方法中,优选的是,用于移动所述多孔膜的主要机械力由弹性材料获得。
在所述方法中,优选的是,用于移动所述多孔膜的主要机械力由弹性材料获得。
在所述方法中,优选的是,所述电绝缘体层的厚度为1-10nm。
附图说明
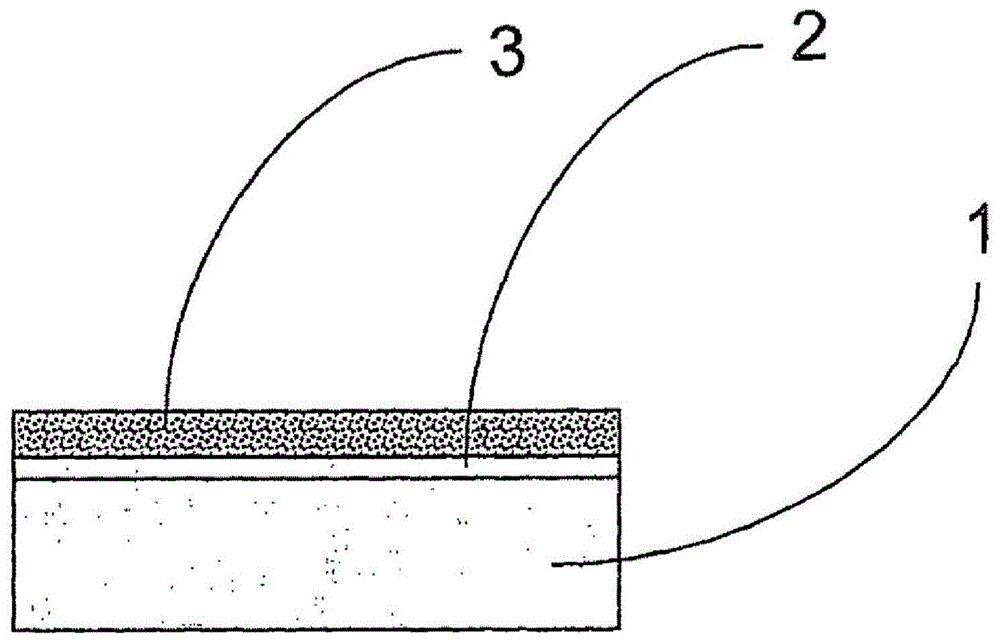
图1.本发明的导体/绝缘体/多孔膜装置(cipf)的示意图。电极结构可以含有导体(1)、绝缘体(2)和多孔膜(3)。该结构称为cipf。
图2a-图2e.根据cipf原理构建用于阳极ecl读取器的测试条的一种实施方式。热电子注射穿过覆盖有绝缘膜的硅(si)芯片。该图还显示了附着到滑动雪橇上的多孔膜。滑盖和测试条的结构被构造为在低位处多孔膜附着到si芯片的表面。当盖向上滑动时,多孔膜升出阴极表面,并在上位相对于臂部再次进行。测试条结构的实例(图2)。测试条含有移动盖(1),其在沿壁(3)移动时将升起(9),并将臂的最后端锁定在其位置。经开口(2)加入待分析样品。多孔膜(5)位于开口之下,并且膜倚靠si电极(6)与钉状物(8)平放。在硅之下,有金属导体(7),由此存在到外部电流源的连接(4)。
图3a-图3b.发光读取器的测量池结构。图3a:池(1)中的测试条(4)位于测量位置。振动发动机(3)连接到池的上部,池还包含用于电激发的测试条中的接触(5)。经连接器(2)布置洗涤。图3b:测量池(8)具有一次性构造。经连接器(2)布置洗涤。洗涤/测量溶液经还充当阳极的辅助钢管(conducivesteelpipe)(6)被带到测量池中。溶液的吸出由另一管(7)执行。测试条(4)的电接触位于条的上部。
图4.测量池的洗涤系统的组装。蠕动泵(1)将洗涤液(5)经管道(2)输送到池(4)中。同一蠕动泵从池上部经另一管道(3)吸出,管道(3)具有比其他管道(2)更高的抽吸效率。阀门(9)选择池从底部或顶部吸出。当较细管道的阀门(10)关闭时,池可以从池底部排放。在需要时,池可以通过调节阀门(8)来洗涤(6)。
图5a-图5b.安装到测试条的一次性测量池。图5a:硅电极安装到具有电绝缘物质(2)的导电框(3)。图5b:显示了如何由电极的整个区域得到发光(4)。
图6a-图6b.测试条。在图6a中,从顶部观察测试条,在图6b中从底部观察。硅电极(1)安装到具有电绝缘物质(2)的测试条。还存在从测试条的背侧到阴极(1)和阳极(3)的直接电接触。
图7a-图7c.测试条,其中所有需要的试剂以干式就绪,并且控制分析反应的开始和停止。在图7a中,测试条即刻可用。在框(1)的底部,薄多孔膜(2)含有干式的所有需要的试剂。多孔膜平放在硅表面上,但不接触电极。弹性材料(3)的构造插入框之下,并且其表现为弹簧。当样品添加到多孔膜(2)上时,样品溶解干试剂。通过将框压下,当多孔膜沉降在硅上并且样品在其表面上铺展时,硅电极表面上的反应开始。在希望的时间之后,框(1)可以由下位释放,反应停止。在图7b中,在固定反应时间之后,框(1,3)被压到测试条中。硅电极(4)附着到具有电绝缘材料(6)的测试条,阳极(5)同时充当下部容器的屏障。在图7c中,测试条位于洗涤步骤。在ecl测量之前,如果需要,利用洗涤臂(7),洗涤硅电极。
图8.多参数测试条。可以向测试条加入多个反应区。它们中的部分可以充当阴性和阳性对照。
图9.使用cipf-装置和发光读取器通过异源hcrp免疫测定测量的一年中si芯片的稳定性。crp浓度为(a)0,(b)10,(c)30,(d)100ng/ml。
图10.si芯片的氧化层的厚度对于阴极ecl的影响,(a)10-7m与2,6-二[n,n-二(羧甲基)氨基甲基]-4-苯甲酰基苯酚螯合的tb(iii)(b)对照溶液(测量缓冲液)。
图11.使用ecl读取器和测试条(cipf)测量的纯铽2,6-二[n,n-二(羧甲基)氨基甲基]-4-苯甲酰基苯酚螯合物的标记发光体的校准曲线。测量池填充有测量缓冲液和标记发光体。
图12.适合于标记抗体的不同发光体的结构和ecl谱(ans4-氨基-1-萘磺酸盐,fmoc-oh=水解的9-芴基甲基氯甲酸酯,tb(iii)-l1=2,6-二[n,n-二(羧甲基)氨基甲基]-4-苯甲酰基苯酚螯合的tb(iii),ru(bpy)32+=钌(ii)三(2,2′-联吡啶)螯合物,yb(iii)-l1=2,6-二[n,n-二(羧甲基)氨基甲基]-4-苯甲酰基苯酚螯合的yb(iii))。可以得到结论,整个uv-vis-nir光谱区域是可工作的。测量使用cipf装置和发光读取器完成。
图13.异源hcrp免疫测定的校准曲线(参见实施例2)。
图14.使用血清样品的异源hcrp免疫测定(参见实施例3)。
图15.使用标准样品溶液的同源hcrp免疫测定(参见实施例4)。
图16.通过标准样品测量的异源htsh免疫测定的校准曲线(参见实施例5)。
图17.使用血清样品测量的异源htsh免疫测定的校准曲线。htsh标准样在血清中制备(参见实施例6)。
图18.使用全血样品的异源htsh免疫测定的校准曲线。htsh标准样在肝素化全血样品中制备(参见实施例7)。测量使用cipf-装置和发光读取器完成(图9,实施例2)。
图19a-图19b.图19a描述了cipf装置的流通池应用,其中基于亲和性的反应可以在多孔膜上或硅阴极上完成。在图19b中剥离侧面(7)使构造可视化。多孔膜(4)充当的液体的运输者。而且,不同试剂可以在其上干燥(例如标记的抗体)。ecl测量可以经多孔膜(4)直接进行。样品直接添加到多孔膜(4)上使免疫反应能够开始。将液体充分添加到池(6)中,形成阳极(5)和硅电极(3)之间的电解接触。洗涤经入口(1)和出口(2)进行,并且液体沿多孔膜移动。具有用于添加样品的孔的盖可以在腔室(6)之上。
图20.使用图15中所示的装置测量的异源hcrp免疫测定的典型校准曲线(参见实施例8)。
图21.通过物理吸附具有抗体的si芯片的涂层的afm质量控制图像。
图22.使用afm测量获得的聚苯乙烯的表面图像。表面的粗糙度阻止了afm在涂层控制中的有效使用(参见实施例10)。
图23示出了现有的血液渗透到常规聚碳酸酯(pc)材料的多孔膜(a)和本发明的聚酯(pe)材料的多孔膜(b)之后的状态。
图24示出了pe材料的多孔膜(10)附着到保持其形状的框架(11)上。
图25示出了pe材料的多孔膜(porousfilm)的示例性层结构。
具体实施方式
根据本发明,使用简单、便宜的装置可以与使用之前记载的复杂化装置一样地进行不同分析,只要实际免疫测定或dna杂交使用在工作电极表面上的多孔膜(cipf装置)进行即可。于是测量装置和测量池对于床边分析的需求而言足够便宜。
血液由白细胞、红细胞和血清等成分组成。其中,相对较大的血细胞会干扰基于ecl的分析,这可能导致诸如假阳性(falsepositive)或假阴性(falsenegative)等错误分析。然而,为了从血液中分离血细胞和血清,必须使用离心分离等方法,而现有方法存在对血液分离花费很长时间的缺点。在本发明中,使用多孔膜(porousfilm)可以容易地将血清成分从血液中分离。
多孔膜在本发明中指的是厚度小于100μm的多孔液体渗透性膜,其设置在ecl阴极上。阴极ecl电极,与阳极ecl电极不同,发挥与传统电化学完全不同的作用,因为阴极在其表面上带有如美国专利6,645,776b号(kulmala等人)所述的薄绝缘膜。多孔膜平放在所述阴极的绝缘膜上。本发明的电极因此含有至少两个膜,即一个不导电的绝缘膜和其上的厚度小于100μm的多孔膜。与所述绝缘膜不同,多孔膜是导电的。多孔膜因此与美国专利6,645,776b号中记载的电极材料完全不同。在阳极ecl应用(美国专利4,280,815a号,technicon;美国专利5,324,457a号,univtexasinstruments;美国专利6,090,545a号,mesoscaletechnologies)之前应用不同多孔材料作为电极本身或作为电极的涂层。不过,多孔材料在所述发明中的目的与本发明不相似。因为阴极ecl以与阳极ecl不同的电化学原理发挥作用(特别是激发区离电极的距离不同),本发明中的多孔膜本身从不作为电极工作。通过将多孔膜设置在电极上,将发现与现有技术相比新颖的令人惊讶的性质。而且,通过阴极上的多孔膜,可以快速铺展均匀的样品层。
本发明公开了特别是在阴极ecl的情况下的导体/绝缘体/多孔膜装置(cipf)。如图8所例示的,可以用其激发极其不同种类的标记。cipf-装置的原理描述于图1。通过添加用于实现多孔膜上的液体接触的液体样品或缓冲液,由此样品或缓冲液在整个工作电极上铺展,从而装置投入工作状态。发现装置工作为令人惊讶的快速免疫测定系统。令人惊讶的是,还发现标记可以在多孔膜中低于100μm的距离内激发。根据本发明,可以制造便宜的含有一次性工作电极的cipf装置、传感器或探针,于是ecl的传统工作电极可以由一次性工作电极替代。同时,例如可以避免需要复杂的用于微粒操纵的机器人的清洁和平衡操作。
通过使制造便宜的定量快速测试成为可能,本发明相对于目标是poc市场的装置和方法的现有技术构成显著的改善。这通过将ecl机构和使用各种薄多孔膜的测量原理组合而实现。
现有技术中已知可以将不同多孔材料用于基于免疫色谱法的测定中的液体输送和过滤(hybritechinc.,参见clinicalchemistry31(1985)1427)。不过,这些方法不是定量的,并且它们不用于阴极ecl的情况,阴极ecl的原理完全不同于传统电化学。
在微流体系统中或在使用微升体积尺寸的方法中,常常有气泡的问题、热扩散的有害影响、层流引起的问题(即液体与流动的不混合)和毛细现象引起的表面力。在本发明中,证明了采用薄多孔膜的新方式,不仅用于过滤,而且作为液流的同源均衡器和铺展器。这可以特别容易地用电子诱导ecl的平滑硅电极实现。而且,cipf装置极大了简化了在由ecl检测方法和仪器完成的测定中的全血采样和操纵过程。通过在这些微流体方法中使用多孔膜,可以完全消除或显著降低现有技术的多个缺点。
本发明包含一种装置,通过该装置,以使得工作电极组件可以用作基于免疫测定和dna探针法的快速测试装置的方式在ecl工作电极上铺展分析物和其他试剂、然后进行电激发。
本发明的目的通过使用在生物亲和性测定的基于ecl的检测方法中使用具有厚度小于100μm的薄多孔膜作为液流的同源均衡器和作为微流通池或微层池的液体的铺展器的cipf装置而达到,其中,装置的特征如权利要求1-10所述。本发明特别关注可以在实践中进行阴极ecl的方法和装置。另外,本发明特别的特征在于,阴极激发发生在电极附近(邻近测定原理)。可以紧接电极放置辅助多孔膜,这在其他检测方法中是不可能的。作为另选,多孔膜可以被带到电极,从而开始生物亲和性反应,之后在ecl测量前取下。不过,测量也可以直接经某些多孔膜进行。标记物质可以干燥到置于电极的多孔膜上或工作电极的表面上。多孔膜与工作电极之间的液体结最优地为小于100μm。多孔膜可以经由现有技术中但不是在ecl中的应用的情况中已知的方法共价地或通过直接吸附于表面而结合(例如在schleicher&schuellltd.的产品中)。
本发明的主要实施方式是ecl工作电极。根据美国专利6,251,690号(kulmala等),热电子诱导ecl中的电极材料是由薄绝缘膜覆盖的导体,其材料可以是al或si。最优选地,其为氧化至由厚度为1-10nm的绝缘膜、最优选厚度为3-4nm的绝缘膜覆盖的平坦硅。不过,硅基板可以为有通道的,或者可以修饰表面形貌从而改善液流或其电气性质。硅芯片的尺寸可以随目的用途和是否要在同一时间测量一种或多种分析物而变。通常,硅芯片的尺寸为4×9mm,厚度小于1mm。硅芯片附着到支持结构,其可以具有取决于所用测量仪器的尺寸和材料要求的各种形状。通常,支持结构由环境友好并且易于处置的塑料制成。取决于膜性质,多孔膜以湿或干态铺展在置于支持结构表面的硅芯片上。
本发明的置于电极表面的多孔膜的特征在于,其为微孔的,并且厚度小于100μm。本发明的材料可从多个商业来源获取,如millipore、msi、sartorius、pall、sigma和dupont。多孔膜可以是各向同性的或各向异性的。制造技术可变化,其可以涉及压缩或拉伸,孔可以通过化学或物理手段完成,或在各向异性多孔膜的情况中通过相转移完成。还可以使用微粒烧结。可以选择多孔膜的合适材料,但不限于ptfe、聚偏氟乙烯、聚碳酸酯、聚砜、尼龙和纤维素酯。这些膜和其他的膜可以以不同孔径和厚度以及不同物理化学性质从商业来源获取。在有用的纤维材料中,可以提及玻璃纤维、滤纸和滤布。
多孔膜在分离血液的同时,还具有吸附结合标记(label)物质的2次抗体的作用。因此,多孔膜优选为亲水性且通过血清易于从多孔膜脱落的材料。
在现有的基于电化学发光(ecl)的分析方法中,使用pc(聚碳酸酯)材料的多孔膜。另一方面,在本发明中,使用pe(聚酯)材料的多孔膜。与以往使用的pc或ca材料的多孔膜相比,pe材料的多孔膜具有约25%以上的信号发射量和高精度。
多孔膜的材料、厚度以及孔隙的大小影响用于分析所注入的血液量和分析时间的确定。pc材料的多孔膜由于血清成分的渗透度低,因此不适于血液的分析,并且由于血液的扩散程度低,因此需要较长的分析时间。然而,若使用pe材料的多孔膜,则可以快速分离血液中的血清成分并缩短分析时间。
图23示出了现有的血液渗透到常规聚碳酸酯(pc)材料的多孔膜(a)和本发明的聚酯(pe)材料的多孔膜(b)之后的状态。(b)的情况可以明确看出优异的血液的渗透性。
多孔膜在cipf装置中的使用相对于生物亲和性测定的现有技术提供了显著的优点。使用多孔膜,样品可以相等地铺展在涂覆有抗体的工作电极上。多孔膜出乎意料地作为液流的同源均衡器工作,防止在微流体系统中形成气泡(ecl的特殊问题)、热扩散、不需要的表面力和层流的影响,于是消除了微流体微流通池中或微层池中的问题。
在基于ecl的生物亲和性测定中多孔膜足够薄、小于100μm的情况下,反应化合物也可以被带到置于电极上的多孔膜,从而多孔膜与电极表面液体接触。与理论考虑(参见美国专利6,251,690号,kulmalas.等和其他出版物)不同,根据本发明,来自电极的激发脉冲可以在离电极比至今预期显著更长的距离内、即在厚度小于100μm的多孔膜中激发多孔膜中的标记分子。
电极的表面可以通过已知手段涂覆有抗体或dna和使用电脉冲激发的结合标记分子。在这种情况下,用于铺展样品和试剂的多孔膜在测量前在需要时可以被除去。
患者样品(血浆、血清、全血、脑脊液、尿液等)也可以被带到多孔膜、干燥并储存于其上。这可以是本发明的特别优点,例如,从而使样品的输送更容易。含有样品的多孔膜可以插入以作为cipf装置的正常工作部分,分析物的浓度如本发明的上下文中其他部分所述测量。
电极或倚靠放置的多孔膜的表面可以通过之前已知的在表面上实现高密度的活性抗原或抗体的方法用抗体或抗原涂覆。根据本发明,电极或倚靠电极放置的多孔膜的表面可以涂覆有实施例中所述的langmuir-blodgett膜。
出于生产原因有利的是干燥存放cipf装置。然后仅通过向多孔膜表面添加液体样品或缓冲液在多孔膜和电极之间的生物亲和性反应实现合适的条件,将装置带到工作条件。
本发明中所述的cipf装置除了支持结构以外还可以包含多孔膜和电极(cipf),包括在使用中使装置更实用的其他部分和屏蔽。如果从全血测量分析物,血细胞的除去也可以通过实施例中所示的特定多孔膜完成。本发明的装置还含有从工作电极到激发和发光测量操作的电连接。对于cipf装置典型的是,通过自动化生产线可以大量生产。cipf装置的各种不同部件的生产方法和将其组装得到装置基本上是现有技术中已知的。
在本发明中,使用pe(聚酯)材料的多孔膜,同时,可以解决以往由于膜不固定而导致的分析结果的可靠性降低的问题。另外,通过应用保持形状的框架(frame)来防止多孔膜的变形。
如上所述,在现有的基于电化学发光(ecl)的分析方法中,使用pc(聚碳酸酯)材料的多孔膜,并且存在以下不便:在分析期间需手动去除膜。另外,由于膜的形状不固定,因此存在分析结果的可靠性降低的问题。
为了克服这个问题,在本发明中,通过将pe膜附着到能够保持膜的形状的框架上来防止膜的变形。通过应用框架,可以通过适当的机构装置(mechanism)自动去除多孔膜。
特别地,使用1μm孔径的pe多孔膜来有效地分离血清,并且结合能够维持间隔的框架以在多孔膜和工作电极之间保持100μm的游离液体结空间。因此,即使3.5μl的少量血液,也可以将血清均匀地分布在工作电极的表面上。
图24示出了pe材料的多孔膜(10)附着到保持其形状的框架(11)上。框架可以由弹性材料或聚氨酯制成,但不限于此。
图25示出了pe材料的多孔膜的示例性层结构。'11'是框架,'12'是由poron4790-92-30012-04sp制成的0.3mm的层,'13'是由作为胶粘剂的be-24-005-ba制成的0.05mm的层,'14'由相同的be-24-005-ba材料形成0.05mm,‘15’作为胶粘剂层仍由be-24-005-ba以0.05mm形成,‘16’由孔径为1.0μm的pe膜形成。
平滑表面优选用作本发明的电极材料。电极由生物亲和性材料涂覆的质量对于cipf装置的工作是关键的。因此,质量控制可以直接基于极其准确的穿隧和/或原子力显微镜。这可以通过直接观察例如活性涂覆抗体而实现,这在实践中使用其他类型的诊断方法是不可能的,因此质量控制的可能性是本发明的核心力量之一,以此方式诊断方法的最核心质量标准将得到满足。常用的由抗体涂覆聚苯乙烯并不具有这种控制可能性,因为注射成型后的聚苯乙烯的表面对于鉴定材料表面上的分子而言太粗糙。
定量快速测试和之前的确定步骤,例如全血样品所需要的预处理,可以使用本发明中所示的方法和装置相当地简化。例如,防止全血样品凝血的肝素处理在本方法中不是必需的。铺展分析物的多孔膜还排除了血细胞与电极接触,并且带有血细胞的多孔膜可以容易除去,露出生物亲和性涂覆的电极。当然,肝素处理的全血样品也可以使用此装置和方法测量。
所关注的工作电极(在阴极ecl中为al、si等)或工作电极上的薄多孔膜可以用抗体涂覆。如果多孔膜涂覆有抗体/抗原/rna/dna,测量将在不除去多孔膜的情况下完成,不过如果工作电极涂覆有识别分析物的生物分子,多孔膜也可以在ecl测量步骤前除去。本发明的ecl测量优选使用热电子诱导电化学发光(美国专利6,251,690号)进行。
取决于目的应用,本发明的cipf装置有多种替代方式。根据本发明,有典型的单独测试条(向其添加分析物)。样品通过多孔膜铺展到硅电极的抗体涂覆片的表面。样品溶解在多孔膜上干燥的标记生物亲和性分子。在样品的移液步骤中和在温育时间然后在洗涤和测量步骤之前滑走的过程中,多孔膜可以使用胶带贴附到在工作电极上的滑盖部。在胶带上具有工作电极尺寸的开口,以使多孔膜仅从边缘与胶带相粘。在样品添加到样品孔之后,多孔膜上干燥的标记抗体溶解,免疫反应在抗体涂覆工作电极表面上开始。多孔膜工作为液体的同源铺展器。其还防止了气泡引起的问题,也消除了微流体系统中的其他上述问题。将测试条转移到测量装置中,在此使用摇晃或不使用摇晃实现生物亲和性反应。摇晃通过连接到仪器测量池池身的振动电机实现,或通过仪器中的其他手段实现湍流。当工作电极露出以供洗涤和测量时,在平衡达到想要的程度之后,将测试条转移到测量池,同时工作电极上的薄多孔膜上滑。在ecl系统中,对电极可以为测量池的集成部分。测量池的体积可以为50-500μl。异源生物亲和性/免疫测定包括测试条的洗涤步骤,但在同源测定中仅包括ecl测量。洗涤和测量溶液的组成可以相同。洗涤可以通过填充和吸出测量池来进行。溶液的运输可以在测量仪器中由泵实施。在测量后,应将池清洗。仪器中的阀门控制是否有洗涤/测量缓冲液或蒸馏水流入池中。更简单的便携式快速测试ecl仪器不涉及通过仪器处置液体,而在一次性测试条本身中包括溶液容器。
生物亲和性测定的ecl测量(其中,薄多孔膜(例如硝基纤维素)涂覆/浸渍有抗体)也可以使用cipf装置原理进行,但与上述模型(膜反应装置)相比然后需要修改的测量池和测试条。因为反应明确地发生在多孔膜中,因此测试条被构造为有开盖以供更大尺寸多孔膜和测量池的洗涤布置(其中可以插入测试条)。
cipf装置的上述膜反应构造也可以应用于更复杂的实验室设备。工作电极可以附着到池,如微流通池,并且阳极可以为涂覆有一面导电材料的材料,如zno玻璃或ito膜,或阳极结构可以为网状,例如钢网或仅仅薄钢线。多孔膜以游离或固定方式位于电极之间。因为多孔膜和其上紧密附着的对电极超过工作电极的长度,池中的流通将通过将流动管道或微升尺寸移液容器连接到穿孔的对电极实现。作为另选,整个cipf装置或传感器可以成型在配备有到样品和洗涤注入的连接器的塑料的液流通道内部。装置构造还可以包括在阴极工作电极周围的阳极对电极。于是最有利的铺展(样品、标记和洗液)溶液的方式在异源测定的情况下也为电极间的多孔膜。异源测定也可以使用类似的方法和装置进行,因为洗涤不是必需的。这是基于阴极ecl仅激发通过生物亲和性反应浓缩到电极表面的标记的事实(所谓的邻近效应)。
标记试剂可以干燥到多孔膜上。对于干燥生物亲和性标记,多孔膜材料可以为厚度小于100μm的任何多孔膜,例如聚碳酸酯或硝基纤维素。对于工作电极的涂层的质量控制,有利的是使用原子力显微镜(afm)。工作电极可以通过物理吸附或通过共价结合以及通过抗体-表面增强langmuir-blodget(lb)膜和langmuir-shaefer方法的程度而用抗体涂覆。
接下来将通过附图和非限制性实例及相关附图来进一步阐述本发明。
实施例1
通过热氧化、切割和用抗体涂覆从si晶片制备涂覆有绝缘膜的电极
si晶片的氧化。晶片(si晶片:电阻率0.01-0.023ωcm,p++硼掺杂,取向<100>,厚度525+/-25μm,生产商okmeticoyj)用工业上常用的rca洗涤进行洗涤,并放入700℃的烘箱中,其中气氛含有95%氮气和5%氧气。将温度升至850℃,增加氧分压:90%氮气、10%氧气,并温育期望的时间。将晶片用纯氮气流清洗30min。在纯氮中将温度降回至700℃,并将晶片从烘箱中取出。
使用不同氧化时间得到以下结果:
厚度由椭圆偏振仪通过激光速的偏振变化测量。在使用薄膜的方法中,折射率固定,对氧化物使用1.465的典型值。将表面保护胶带固定到si晶片的未抛光侧。将待切割的晶片贴附到切割基台,并通过计算机控制金刚石刀锯切割成si传感器预制件的需要尺寸。
抗体涂覆可以进行至例如使经切割当仍然结合有保护带的si晶片将被放置为抛光面向下漂浮在塑料碗中的涂布液(涂布液:50mmtrizma基质,0.05%nan3,0.9%nacl,用hcl调至ph7.8,含有抗crp抗体7.0μg/ml;medixbiochemicaoyabanti-hcrpclone6405,1.0mg/ml)上。涂覆体积为50ml/晶片或4.5μg抗体/cm2。使涂覆在潮湿空间中过夜进行,然后将晶片转移到装有新饱和溶液(50mmtrizma基质,0.05%nan3,0.9%nacl,0.1%bsa,6%d-山梨醇,1mmcacl2*h2o,用hcl调至ph7.8)的碗,使饱和过夜进行。为了存储,将经切割和涂覆的制好的含si传感器的板在30℃干燥2.5h,然后与干燥物质一起气密地放到冰箱中。当测试条组装好后,将si切片从存储中取出,除去贴附于测试条的保护胶带(图2)。图9显示了涂覆有抗体的cipf装置的存储稳定性。氧化层厚度对ecl信号的影响呈现在图10中。图11显示了在溶液相中游离测量的铽-2,6-二[n,n-二(羧甲基)氨基甲基]-4-苯甲酰基苯酚螯合物标记的浓度相关性。图12显示了各种可用的标记发光体的光谱,证明全部光谱区域(uv-vis-nir)可以与阴极ecl装置和方法一起使用。
实施例2
使用标准溶液和按照图1和2的测试条和测量池例示的异源crp免疫测定
使用根据实施例1制备的si芯片进行crp免疫测定。测试条的构造如图1和图2所示。使用图3a所示的池和装置测量含有滑动多孔膜的测试条。免疫测定基于多孔膜与ecl检测的组合使用。作为另选,通过轻微地修改测试条,可以使用图3b所述的一次性测量池进行测量。
附着于测试条的滑盖部分的多孔膜含有干燥标记。将外形尺寸为7.00×12.0mm的聚碳酸酯多孔膜(厚度6-11μm,1×105-6×108孔/cm2,whatman)插入具有si芯片尺寸为4.00×9.00mm的开口的相同尺寸的带框(3m465,两面丙烯酸胶带,无背衬材料)。多孔膜上的标记的干燥如下。将含有经标记抗体(medixbiochemicaoyabanti-hcrpclone6404,2.22mg/ml)的溶液(50mmtrizma基质,0.05%nan3,0.9%nacl,0.5%bsa,0.05%牛γ球蛋白,0.01%tween20,1mmcacl2*h2o,用hcl调至ph7.7,含有tb-2,6-二[n,n-二(羧甲基)氨基甲基]4-苯甲酰基苯酚螯合物标记的抗体0.074mg/ml)移液(0.5μl),并作为直径为2mm的液滴在多孔膜(12.0×7.00mm)中心干燥。使干燥在室温过夜进行。
通过用稀释溶液(50mmtrizma基质,0.05%nan3,0.9%nacl,0.5%bsa,1mmcacl2*h2o,用hcl调至ph7.7)稀释crp标准溶液(scripps,目录号c0124,2.37mg/mlcrp),而在试管中制备免疫测定标准样品(crp浓度0.3、1.0、3.0、10.0、30.0、100.0、300.0、1000.0、3000.0ng/ml)。将3.5μl的样品水平移液到测试条盖上的多孔膜上(图1),在此样品溶解干燥标记。将带转移到测量仪器中竖直位置,通过用测量池盖部中安置的振动发动机摇晃,使样品与经涂覆的si在多孔膜下一起温育5min。在温育后,将多孔膜连同其框架从si上滑走,同时测试条移动到洗涤/测量池中。将池用组合洗涤/测量液(50mmna2b4o7,0.1%nan3,0.003%tween20,用h2so4调至ph7.9)填充4次并吸出3次。在最后填充后,使用美国专利6,251,690号中记载的发光仪器测量ecl(f=10hz,q=20μas,脉冲时间250μs,60脉冲,u=25v)。在测量后,将池抽出并取出si片。在下一个si片之前将池用排放填充物洗涤3次。最后填充用蒸馏水完成。池的洗涤布置示于图4。crp免疫测定的标准曲线示于图13。
实施例3
在包含阳极围绕硅阴极的测量池中测量tb螯合物
在图5a的实验布置中,用胶带将硅电极贴附到孔的底部,并用uv聚合胶粘剂(loctite322或epo-tekog142)填充至表面。在聚合后,除去胶带。将池用实验2中提到的洗涤/测量液填充,其中tb螯合物溶液的浓度为10-3mol/l。测量ecl(f=20hz,i=316mm,脉冲时间500μs,u=67v),用数码相机拍摄照片。收集10次脉冲以得到照片。图5b显示发光来自整个电极区域。
实施例4
图3的电极单元可以附着到有利于与两个电极之间的容易的电连接的塑料基底。测试条示于图6a和6b。其也可以基于与实施例2的测试条相同的原理建造,如图7所示。因此,通过向条加入单个电极单元,可以建造由此可以同时进行许多测定的测试条。测定的部分可以充当阴性或阳性对照。这样的测试条示于图8。
实施例5
使用血清样品的异源crp免疫测定
在稀释后通过ecl免疫测定测量crp浓度为133000、37000、13000、7000、234ng/ml的已知血清样品(在认可实验室中浊度计测量)。将样品用稀释溶液(50mmtrizma基质、0.05%nan3、0.9%nacl、0.5%bsa、1mmcacl2*h2o、用hcl调至ph7.7)稀释100倍并如实施例2所示测量。所得血清样品曲线示于图14。
实施例6
使用标准溶液的同源crp免疫测定
如实施例2那样使用标准溶液通过基于ecl检测的cipf装置进行同源crp免疫测定,修改在于,在温育之后和在将测试条下压到测量池中之后,不进行洗涤但通过泵用测量溶液填充测量池并直接进行测量。同源免疫测定的结果示于图15。
实施例7使用标准样品的异源tsh免疫测定
几乎按照与实施例2所示相同的方式使用crp进行异源htsh免疫测定。使用si芯片的测试条如实施例1制备。si芯片的抗体涂覆溶液的组成为0.1mmes、0.03mh3bo3、0.5mm柠檬酸钾、0.025%葡萄糖醛、0.05%牛γ球蛋白,含有6.87mg/ml的抗体(mit0406moabantihtshmedixbiotechinc.usa),饱和溶液的组成为50mmtrizma基质、0.1%bsa、0.1%nan3、0.1%tween20、使用h2so4调至ph7.5。另外,使用tb-2,6-二[n,n-二(羧甲基)氨基甲基]-4-苯甲酰基苯酚螯合物标记的标记抗体(单克隆抗htsh,clone5404,5.5mg/ml,medixbiochemicaoyab)如上所述干燥到测试条的多孔膜部分上。
通过用稀释溶液(50mmtrizma基质、0.05%nan3、0.9%nacl、0.5%bsa、1mmcacl2*h2o、使用hcl调至ph7.7)稀释tsh标准溶液(wallac,delfiahtshkit,324miu/mltsh)而在试管中制备标准样品(tsh浓度0.1、1.0、3.0、10.0、30.0和100.0miu/l)。洗涤和测量如实施例2所示进行,不同之处在于温育时间为连续摇晃15min。异源htsh免疫测定的标准曲线示于图16。
实施例8
使用血清样品的tsh的异源免疫测定
几乎按照与实施例2中的crp测定相同的方式进行异源htsh免疫测定。si芯片如实施例1制备。si芯片的抗体涂覆溶液的组成为0.1mmes、0.03mh3bo3、0.5mm柠檬酸钾、0.025%葡萄糖醛、0.05%牛γ球蛋白,含有6.87mg/ml抗体(anti-htshmedixbiotechinc.usa),饱和溶液的组成为50mmtrizma基质、0.1%bsa、0.1%nan3、0.1%tween20、使用h2so4调至ph7.5。另外,使用tb-2,6-二[n,n-二(羧甲基)氨基甲基]-4-苯甲酰基苯酚螯合物标记的标记抗体(anti-htsh,medixbiochemicaoyab)如上所示干燥到cipf装置的多孔膜。
通过用血清稀释tsh标准溶液(scrippslaboratories,inc.,sandiego,usa)制备血清标准样(tsh浓度1.0、3.0、10.0、30.0和100.0miu/l)。血清tsh浓度为0.45mu/l。洗涤和测量如实施例2所示完成,不同之处在于温育时间为连续摇晃15min。htsh免疫测定的标准曲线示于图17。
实施例9
使用全血样品的异源tsh
几乎按照与实施例7相同的方式进行异源htsh免疫测定。通过用肝素化全血稀释tsh标准溶液(scrippslaboratories,inc.,sandiego,usa)制备全血标准样(tsh浓度1.0、3.0、10.0和30.0miu/l)。全血的tsh浓度为0.5mu/l。洗涤和测量如实施例5进行。全血htsh免疫测定的标准曲线呈现于图18。
实施例10
使用si阴极对抗体涂覆的硝基纤维素多孔膜的crp免疫测定
通过在室温在缓冲液(50mmtris-hcl,ph7.8,0.05%nan3,0.9%nacl)中温育过夜而用抗crp抗体(101g/ml)涂覆硝基纤维素多孔膜(7×4mm,schleicher&schuell,12μm)。然后,将硝基纤维素用饱和溶液(50mmtris-hcl,ph7.8,0.05%nan3,0.9%nacl,0.1%bsa,6%d-山梨醇,1mmcacl2)洗涤,最后将多孔膜在室温在此饱和溶液中保存过夜。饱和后,将多孔膜在滤纸上干燥。
将抗体涂覆的硝基纤维素多孔膜附着到变至装置的流通池(图19),在其上加入crp标准样50μl。在温育(5min)后,将多孔膜在池中用1ml的洗涤/测量液(50mm硼酸盐缓冲液,ph7.9,0.1%nan3,0.003%tween20)洗涤,在其上添加tb螯合物标记的抗体50μl。在温育(5min)后,将多孔膜用1ml的洗涤/测量液洗涤。在洗涤后,在500μl的洗涤/测量缓冲液(f=5hz,q=20μas,脉冲时间250μs,500脉冲,u=34.8v)中测量ecl。典型的标准曲线示于图20。
实施例11
使用langmuir-blodget(lb)膜的电极涂覆和表面的分子检查
使用普通langmuir槽进行实验。通过wilhelmy板法以0.2mn/m的精度测量表面张力。蛋白膜的制备按照nagagawat.(1991)thinsolidfilms,202,151和owaku,k.,(1989)thinsolidfilms180,61进行。通过langmuir-shaefer法将制得的蛋白膜转移到电极板。此涂层中使用的蛋白为针对b型肝炎表面抗原的小鼠单克隆抗体。使用tris-hcl缓冲液(10mm,ph8.2)和烷基化聚乙烯亚胺(aldrich,germany)将lb膜形成为水/空气边界。
使用nanoscopeiifm仪器(digitalinstruments)创建lb涂覆表面的原子力穿隧图像。仪器使用恒流(穿隧)或恒定偏压(原子力)工作。通过滤波并通过2d傅里叶变换记录稳定至少30min的图片。观察尺寸为25×15nm的圆形图案,其被鉴定为抗体。表面密度经估算为1×1015分子/m-2。对比结果示于图21和22。
- 还没有人留言评论。精彩留言会获得点赞!