一种试剂盒以及检测系统的制作方法
本发明实施例涉及化学分析
技术领域:
,特别是涉及一种试剂盒以及检测系统。
背景技术:
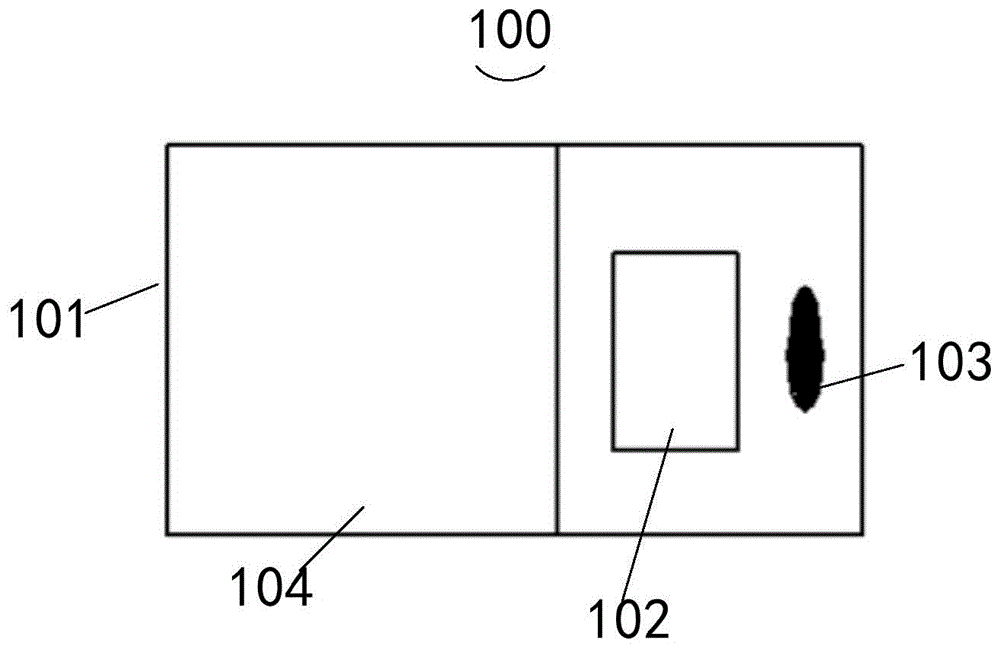
:血清淀粉样蛋白a(serumamyloida,saa)是组织淀粉样蛋白a的前体物质,是一种多基因编码的多形态蛋白质,属于急性时相反应蛋白[1]。根据表达情况,saa可分成两类:组成型saa(constitutivesaa,c-saa)以及急性期saa(acutesaa,a-saa)。正常情况下,人体中saa主要来源于肝细胞中的c-saa,占saa总量的90%以上。在机体受到刺激时,如炎症、感染、肿瘤等,机体大量释放促炎因子(如白介素、肿瘤坏死因子-α等),使a-saa大量合成,成为此时体内主要的saa,并且其在5-6小时内迅速上升100-1000倍,并且在疾病的恢复期迅速下降。基于此,检测血清淀粉样蛋白a的含量具有重要的临床参考价值。目前,常采用酶联免疫吸附法检测血清淀粉样蛋白a。酶联免疫吸附法采用辣根过氧化物酶或碱性磷酸酶标记抗体,并催化底物产生颜色变化,具有特异性较强,试剂稳定期长的特点。但是,本发明的发明人在实现本发明实施例的过程中,发现:酶联免疫吸附试验法的检测灵敏度较低,且操作步骤复杂,每次检测时均需同时做标准曲线,耗时且耗力。技术实现要素:鉴于上述问题,本发明实施例提供了一种试剂盒以及检测系统,克服了上述问题或者至少部分地解决了上述问题。根据本发明实施例的一个方面,提供了一种试剂盒,包括壳体、试剂、磁卡以及搅拌子;所述壳体设置有收容空间,所述试剂收容于所述收容空间内,所述磁卡以及搅拌子均设置于所述壳体,所述磁卡存储有所述试剂盒的标准曲线信息;所述试剂包括:抗血清、缓冲液和质控品;其中,所述抗血清包括第一磷酸盐缓冲液以及与羊抗人血清淀粉样蛋白a多克隆抗体偶联的乳胶颗粒,所述缓冲液包括第二磷酸盐缓冲液、氯化钠和叠氮钠,所述质控品包括含血清淀粉样蛋白a的溶液,所述第一磷酸盐缓冲液和所述与羊抗人血清淀粉样蛋白a多克隆抗体偶联的乳胶颗粒的质量比为(3-10):1,所述第二磷酸盐缓冲液与氯化钠的质量比为1:(1-2),所述第二磷酸盐缓冲液与叠氮钠的质量比为(9-12):1,所述质控品中的所述血清淀粉样蛋白a的浓度为5-300mg/l。在一种可选的方式中,所述第一磷酸盐缓冲液和所述与羊抗人血清淀粉样蛋白a多克隆抗体偶联的乳胶颗粒的质量比优选为5.14:1。在一种可选的方式中,所述与羊抗人血清淀粉样蛋白a多克隆抗体偶联的乳胶颗粒的浓度为2g/l。在一种可选的方式中,所述第二磷酸盐缓冲液与氯化钠的质量比优选为1:1.54。在一种可选的方式中,所述第二磷酸盐缓冲液与叠氮钠的质量比优选为10.82:1。在一种可选的方式中,所述氯化钠的浓度为15.8g/l。在一种可选的方式中,所述叠氮钠的浓度为0.95g/l。在一种可选的方式中,所述第一磷酸盐缓冲液和第二磷酸盐缓冲液的浓度均为20mmol/l。在一种可选的方式中,所述质控品中血清淀粉样蛋白a溶液浓度为55mg/l。根据本发明实施例的一个方面,提供了一种检测系统,包括检测设备以及上述的试剂盒。本发明实施例的有益效果是:区别于现有的试剂盒,本发明实施例提供的试剂盒包括:壳体、试剂、磁卡以及搅拌子;所述壳体设置有收容空间,所述试剂收容于所述收容空间内,所述磁卡以及搅拌子均设置于所述壳体,所述磁卡存储有所述试剂盒的标准曲线信息;所述试剂包括:抗血清、缓冲液和质控品;其中,所述抗血清包括第一磷酸盐缓冲液以及与羊抗人血清淀粉样蛋白a多克隆抗体偶联的乳胶颗粒,所述缓冲液包括第二磷酸盐缓冲液、氯化钠和叠氮钠,所述质控品包括含血清淀粉样蛋白a的溶液,所述第一磷酸盐缓冲液和所述与羊抗人血清淀粉样蛋白a多克隆抗体偶联的乳胶颗粒的质量比为(3-10):1,所述第二磷酸盐缓冲液与氯化钠的质量比为1:(1-2),所述第二磷酸盐缓冲液与叠氮钠的质量比为(9-12):1,所述质控品中的所述血清淀粉样蛋白a的浓度为5-300mg/l。使用所述试剂盒检测血清淀粉样蛋白a的含量,不需要现场配置所需要的试剂并做标准曲线测试,其检测时间短,操作过程简单。附图说明一个或多个实施例通过与之对应的附图中的图片进行示例性说明,这些示例性说明并不构成对实施例的限定,附图中具有相同参考数字标号的元件表示为类似的元件,除非有特别申明,附图中的图不构成比例限制。图1是本发明实施例提供的试剂盒的示意图。具体实施方式为了使本发明的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅用以解释本发明,并不用于限定本发明。本发明实施例提供了一种试剂盒,所述试剂盒适用于检测血液样本中的血清淀粉样蛋白a的含量。请参阅图1,试剂盒100包括壳体101、试剂(图未示)、磁卡102以及搅拌子103。所述壳体101设置有收容空间104,所述试剂收容于所述收容空间104内,所述磁卡102以及搅拌子103均设置于所述壳体101,所述磁卡102存储有试剂盒100的标准曲线信息。对于上述磁卡102,磁卡102内已经储存所述试剂盒100标准曲线信息,在使用所述试剂盒100所述测试前,通过将所述磁卡102与所述检测设备上的磁卡感应区的接触,刷卡成功后,磁卡感应区会识别储存于磁卡102内的标准曲线信息,不用在测试前再通过反复实验确定标准曲线,节省了大量的检测时间。对于上述搅拌子103,搅拌子100为不锈钢制品,所述搅拌子103设置于所述壳体101内,用于搅拌待测血液样本,使所述血液样本与所述试剂充分混合,增加测试结果的准确性。在一些实施例中,所述搅拌子103为不锈钢制品。所述试剂包括:抗血清、缓冲液和质控品。对于上述抗血清,抗血清包括第一磷酸盐缓冲液以及与羊抗人血清淀粉样蛋白a多克隆抗体偶联的乳胶颗粒,所述第一磷酸盐缓冲液和所述与羊抗人血清淀粉样蛋白a多克隆抗体偶联的乳胶颗粒的质量比为(3-10):1,优选的,所述第一磷酸盐缓冲液和所述与羊抗人血清淀粉样蛋白a多克隆抗体偶联的乳胶颗粒的质量比为5.14:1。所述第一磷酸盐缓冲液的浓度为20mmol/l。所述与羊抗人血清淀粉样蛋白a多克隆抗体偶联的乳胶颗粒的浓度为2g/l。所述第一磷酸盐缓冲液,由磷酸二氢钠和磷酸氢二钠组成,其中,磷酸二氢钠酸性较强,如果血液中的ph值过高时,多余的碱就会与磷酸二氢钠结合生成磷酸氢二钠,反之,ph值过低的时,多余的酸会与磷酸氢二钠反应产生磷酸二氢钠,从而调节人体血液的ph值。所述与羊抗人血清淀粉样蛋白a多克隆抗体偶联的乳胶颗粒用于与样本发生抗原抗体反应产生凝集。对于上述缓冲液,缓冲液包括第二磷酸盐缓冲液、氯化钠和叠氮钠。其中,所述第二磷酸盐缓冲液的浓度与所述第一磷酸盐缓冲液的浓度相同,为20mmol/l,所述第二磷酸盐缓冲液与氯化钠的质量比为1:(1-2),优选的,所述第二磷酸盐缓冲液与氯化钠的质量比为1:1.54。所述第二磷酸盐缓冲液与叠氮钠的质量比为(9-12):1,优选的,所述第二磷酸盐缓冲液与叠氮钠的质量比为10.82:1。所述氯化钠用于调节溶液的离子强度,避免引起细胞渗透压的改变,所述氯化钠的浓度为15.8g/l。所述叠氮钠作为防腐剂,所述叠氮钠的浓度为0.95g/l。对于上述质控品,质控品包括含血清淀粉样蛋白a的溶液,所述血清淀粉样蛋白a溶液的浓度为5-300mg/l,优选的,所述血清淀粉样蛋白a溶液的浓度为50-60mg/l。所述质控品的靶值已知,所述质控品用于鉴定所述检测设备的测量结果是否准确。需要说明的是,将羊抗人血清淀粉样蛋白a多克隆抗体偶联到乳胶颗粒上,与所述血液样本中的血清淀粉样蛋白a发生特异性的结合形成乳胶颗粒-抗体-血清淀粉样蛋白a抗原的免疫复合物。由于所述免疫复合物的生成量和所述血液样本中的血清淀粉样蛋白a浓度正相关,所述免疫复合物被所述检测设备检测,通过比对所述磁卡内储存的标准曲线数据,即可获得所述血液样本中的血清淀粉样蛋白a的含量,使用所述试剂盒100能够检测血液样本中的所述血清淀粉样蛋白a的含量。对所述试剂盒100检测血清淀粉样蛋白a的含量使用检测设备1、检测设备2、检测设备3以及检测设备4进行性能评价,如下:(1)阳性参考范围准备自觉健康,无消化系统疾病(肝硬化、肝炎、脂肪性肝病、胆结石、胆囊炎和慢性腹泻等),无急慢性感染(急性呼吸道感染、肺炎和肺结核),无肾脏疾病(慢性肾脏疾病、急性肾损伤等),无代谢和营养疾病(糖尿病、代谢综合征、血脂异常等),无风湿性疾病(类风湿性关节炎、系统性红斑狼疮等),无甲状腺疾病(甲状腺亢进症、甲状腺功能减退症),无血液系统疾病(贫血,白血病等),无肥胖、高血压、烧伤和肌肉创伤;近期未曾献血、输血、大量失血、手术或者服用药物,女性未处于怀孕或者哺乳期的正常人。所述正常人无性别差异,无年龄段要求。选择20岁-79岁的标本,要求每10岁作为一个年龄段,每个年龄段3-4人,男女均分,共20人。采集所述正常人的血液,剔除脂血、溶血和黄疸等不合格样本,得到血液样本1-20。使用所述检测设备1、检测设备2以及检测设备3分别检测所述血液样本1-20,数据记录在表1。需要说明的是,在检测的数据中,如果有疑似离群的数据,应将疑似离群值的检测结果和其相邻值的差d和数据全距r相除,若d/r≥1/3,考虑为离群值。剔除离群值后不满20例需补足。将20个测得值与需验证的参考范围比较,若落在参考限外的测定值不超过2个,则该参考范围可直接使用。如果3个或3个以上测得值超出参考限,则重新筛选20人进行验证,若不超过2个测定值超出该参考范围的则可以使用,若仍然有3个或3个以上测定值超出参考限,则应重新检查所用分析系统,考虑是否有人群差异,考虑是否需要自己建立参考范围。表1阳性参考范围验证数据统计表由表1可知,采用所述试剂盒100测试所述血液样本中的血清淀粉样蛋白a的百分比含量,其阳性参考范围为4.2%-6.2%,符合测试标准。(2)空白限的确定以生理盐水为空白样本重复测试20次,分别按公式(1)和公式(2)计算测试结果的平均值和标准差(s),则检测低限(lowerlimitofdetection,应小于空白限5mg/l,测试结果记录在表2。式中:xi—第i次测试浓度值;n—测试次数。表2空白限测试结果由表2可知,采用所述试剂盒100测试血清淀粉样蛋白a的空白限,测试结果均小于5mg/l,符合测试空白限的测试标准,因此,采用所述试剂盒100测试血清淀粉样蛋白a的空白限满足测试要求。(3)线性范围用接近线性区间上限的高浓度(活性)血液样本,按表3所示的稀释比例混合成6个稀释浓度(xi)分别检测所述试剂盒,每个稀释浓度测试3次,分别求出检测结果的均值(yi)。以稀释浓度(xi)为自变量,以检测结果均值(yi)为因变量求出线性回归方程。按公式(3)计算线性回归的相关系数(r),测试结果在2%~15%范围内应符合r≥0.990,测试结果记录在表4。表3稀释比例示例表序号012345高浓度(活性)血液样本0份1份2份3份4份5份血液样本稀释液5份4份3份2份1份0份式中:xi—第i次测试浓度值;—试剂测试结果平均值;yi—第i次的估算值;—试剂估算结果的平均值;i—1,2,3,……,n。表4血清淀粉样蛋白a线性测试结果%由表4可知,按公式(3)计算线性回归的相关系数(r),测得第i次的估算值以及试剂估算结果的平均值均在5mg/l~300mg/l范围内且测得线性回归的相关系数r为0.9988大于0.990,因此,采用所述试剂盒100测试血清淀粉样蛋白a,其线性回归系数满足线性范围的规定。(4)准确度(相对偏差≤±15%)分别测试可用于评价常规方法的有证参考物质(crm)或其他公认(ifcc)的参考物质,或由参考方法定值的高、中、低三个浓度的人源样品,每个浓度样品重复检测3次,分别取测试结果均值,根据公式(4)计算的相对偏差(b),若相对偏差(b)≤±15%,即判为合格,测试结果如表5所示。式中:m—测试均值;t—有证参考物质标示值(靶值),或各浓度人源样品定值。表5血清淀粉样蛋白a准确度测试结果由表5可知,将表5中的测试均值和靶值分别带入公式(4)计算,得出相对偏差b均位于±15%以内,因此,该试剂盒的准确性高,符合测试要求。(5)批内重复性(cv≤8%)用所述试剂盒100分别测试一个医学决定水平正常浓度控制物质和一个异常浓度控制物质,各重复测试10次,分别按公式(5)和公式(6)计算测量值的平均值和标准差(s),按公式(7)计算变异系数(cv),应符合cv≤8%,测试结果参见表6。式中:cv—变异系数;xi—第i次测试浓度值;n—测试次数。表6血清淀粉样蛋白a重复性测试结果由表6可知,采用所述试剂盒100测试血清淀粉样蛋白a批内重复性质控测试实验,实验结果表明,采用四个不同的检测设备测试同一个所述试剂盒100内的所述质控品测试10次后,其测试结果的变异系数均小于8%,同一批所述试剂盒100内测试血清淀粉样蛋白a重复性好。(6)批间差(r≤10%)用3个不同批号的所述试剂盒100(试剂盒1、试剂盒2和试剂盒3)测试相同控制物质,每个批号测试3次,按公式(5)计算每个批号3次重复测定的均值按公式(8)计算所有次测定结果的均值并按公式(9)求出三个批号试剂测定的相对极差(r),所得结果应≤10%,测试结果参见表7。式中:—中的最大值;—中的最小值;—总均值。表7血清淀粉样蛋白a批间差测试结果由表7可知,分别检测设备1、检测设备2、检测设备3以及检测设备4通过3个不同批号的所述试剂盒100测试同一浓度的控制物质,测试结果表明,三个批号试剂盒测定的相对极差(r)分别为4.17%,4.11%,4.81%和4.60%,测试结果均小于10%,说明所述试剂盒100的批间差相对较小,符合测试要求。(7)特异性(bias≤±10%)本实验方法参照clsiep07-a2临床化学检验的干扰评价文件制定,评估待检试剂盒的常规抗干扰能力。取一已知浓度的质控品或者校准品作为样本,将样本分装于6支离心管中,标号为0-5号,将0号样本重复测试5次,按公式(5)求取测定结果均值(tv)作为样本标示值,再将约30mg/dl胆红素加入1号样本,将750mg/dl血红蛋白加入2号样本,将400mg/dl甘油三酯加入3号样本,将30mg/dl抗坏血酸加入4号样本,将10mg/dl类风湿因子加入5号样本中进行测定,重复测定3次,根据公式(5)求取加入干扰物质后的测定结果均值根据公式(4)计算结果,结果应符合“加入干扰物质”后,测试结果与参考物质或者校准品靶值的相对偏差应符合≤±10%”的要求。表8血清淀粉样蛋白a特异性测试结果由表8可知,取所述试剂盒100内已知浓度的所述质控品,分别加入不同的干扰因子进行测试,结果表明,得到测试结果与参考物质的相对偏差均位于±10%内,所述试剂盒100的特异性好,符合测试要求。在本发明实施例中,试剂盒包括壳体、试剂、磁卡以及搅拌子;所述壳体设置有收容空间,所述试剂收容于所述收容空间内,所述磁卡以及搅拌子均设置于所述壳体,所述磁卡存储有所述试剂盒的标准曲线信息;所述试剂包括:抗血清、缓冲液和质控品;其中,所述抗血清包括第一磷酸盐缓冲液以及与羊抗人血清淀粉样蛋白a多克隆抗体偶联的乳胶颗粒,所述缓冲液包括第二磷酸盐缓冲液、氯化钠和叠氮钠,所述质控品包括含血清淀粉样蛋白a的溶液,所述第一磷酸盐缓冲液和所述与羊抗人血清淀粉样蛋白a多克隆抗体偶联的乳胶颗粒的质量比为(3-10):1,所述第二磷酸盐缓冲液与氯化钠的质量比为1:(1-2),所述第二磷酸盐缓冲液与叠氮钠的质量比为(9-12):1,所述质控品中的所述血清淀粉样蛋白a的浓度为5-300mg/l。使用所述试剂盒检测血清淀粉样蛋白a的含量,不需要现场配置所需要的试剂并做标准曲线测试,其检测时间短,操作过程简单。本发明实施例还提供了一种检测系统,检测系统包括检测设备以及所述试剂盒100。所述检测设备适用于使用所述试剂盒100检测所述血清淀粉样蛋白a的含量。所述检测设备使用所述试剂盒100检测所述血清淀粉样蛋白a的含量的检测方法为:开机显示主测试界面,在项目栏选择需要测试项目和样本类型;在批号栏点击“批号”,进入刷卡界面,将所述磁卡与所述检测设备的磁卡感应区接触,听到“滴”一声,说明刷卡成功,其中,同一批所述试剂盒,只需刷卡一次;在所述检测设备的提示下,取出测试杯,在测试杯中加入所述搅拌子,并准确加入400μl的所述缓冲液;然后加入2μl的所述血液样本;将所述测试杯放入测量通道,仪器自动搅拌一次;仪器界面提示“请放入测量杯”;取出测试杯,在测试杯中加入一粒搅拌子,并准确加入400μl的缓冲液;然后加入2μl的样品;将测试杯放入测量通道,仪器自动搅拌一次;在所述检测设备的提示下加入抗血清,然后用移液器准确加入100μl的所述抗血清;立即按下相应通道的触发按键,所述检测设备自动搅拌,测试完成后,所述检测设备将显示测量结果并自动打印所述测试结果。在一些实施例中,所述检测设备为全自动检测设备,所述全自动检测设备使用所述试剂盒100检测所述血清淀粉样蛋白a的含量的检测方法为:开机显示主测试界面,在项目栏选择需要测试项目和样本类型;在批号栏点击“批号”,进入刷卡界面,将相应项目的磁卡与所述全自动检测设备的所述磁卡感应区上方接触,其中,同一批所述试剂盒,只需刷卡一次;将所述血液样本放到试剂位,所述全自动检测设备自动吸样,并自动完成测量过程。测试完成后,仪器将显示测量结果并自动打印测试结果。所述检测设备使用所述试剂盒100在进行血清淀粉样蛋白a时,不需要现场配置测试所用的试剂并做标准曲线测试,不仅节省测试时间,提高检测效率,也简化了测试步骤。最后应说明的是:以上实施例仅用以说明本发明的技术方案,而非对其限制;在本发明的思路下,以上实施例或者不同实施例中的技术特征之间也可以进行组合,步骤可以以任意顺序实现,并存在如上所述的本发明的不同方面的许多其它变化,为了简明,它们没有在细节中提供;尽管参照前述实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1