以共价有机框架为共反应剂的电化学发光方法及亚砷酸根检测应用与流程
本发明涉及一种以共价有机框架为共反应剂的电化学发光方法及亚砷酸根检测应用,属于电致化学发光传感技术领域。
背景技术:
砷元素在自然界分布广泛,其中无机砷是一类致癌剧毒物质,可导致肺癌和皮肤癌。砷中毒主要来源于被污染的饮用水,因此开发复杂环境水样中砷的检测方法具有重要意义。近年来,亚砷酸根as(iii)的检测手段多种多样,包括电感耦合等离子质谱法、荧光法、拉曼散射法、电化学法、比色法以及电致化学发光法(ecl)等,其中,ecl具有高灵敏度、宽的线性范围、低的背景信号和成本低等特点,在分析检测应用上具有突出优势。双波长比率ecl利用ecl发射体具有可区分的发射波长可进一步降低背景信号,并提高检测的选择性和灵敏度。然而,ecl传感方法检测砷的研究很少。所以,发展双波长比率ecl传感器的as(iii)检测方法对环境水样中as(iii)的污染检测具有重要意义。
三联吡啶钌(ru(bpy)32+)和三联苯基吡啶铱(ir(ppy)3)是常用的ecl发光试剂,它们常用的共反应剂主要有三丙胺、三乙胺、三乙醇胺等,但这些胺类共反应剂易挥发、毒性大、对人体健康有危害。ru(bpy)32+作为阴极电致化学发光发光试剂时,还原生成的ru(bpy)3+在水溶液中不稳定,且ru(bpy)32+/+的还原电势与析氢反应的电势相当,使得ru(bpy)32+的阴极ecl研究受到限制,因此,研究ru(bpy)32+的新型共反应剂用于阴极ecl应用具有重要意义。xing等发展了以氮化硼量子点为ru(bpy)32+阳极共反应剂的ecl法用于检测多巴胺(xing,h.;zhai,q.;zhang,x.;li,j.;wange.boronnitridequantumdotsasefficientcoreactantforenhancedelectrochemiluminescenceofruthenium(ii)tris(2,2’-bipyridyl),anal.chem.,2018,90,2141-2147)。raju等研究了以谷胱甘肽为ru(bpy)32+阴极共反应剂的ecl法检测谷胱甘肽(raju,c.v.;kumar,s.s.highlysensitivenovelcathodicelectrochemiluminescenceoftris(2,2’-bipyridine)ruthenium(ii)usingglutathioneasaco-reactant,chem.commun.,2017,53,6593-6596)。目前,尚未见ir(ppy)3的阴极ecl共反应剂的研究报道。
共价有机骨架(cof)是一类结晶聚合材料,在储能金属离子的分离和回收、催化、气体吸附等方面具有优异的应用前景。与金属有机骨架(mof)以及其他聚合材料相比,cof材料具有显着的优势,例如规则的孔结构、灵活的拓扑连接性、出色的可调节功能性等。最近,cof的荧光性能已用于检测小分子和离子。然而,尚未见cof作为ecl共反应剂的研究报道。
技术实现要素:
本发明的目的在于提供一种以共价有机框架为共反应剂的电化学发光方法及亚砷酸根检测应用,它具有检测灵敏度高、检测限低、选择性好的优点。
本发明通过如下技术方案实现:
以共价有机框架为共反应剂的电化学发光方法,其特征在于,先将三醛基间苯三酚与5,5’-二氨基-2,2’-联吡啶通过席夫碱反应合成含吡啶的共价有机框架(tp-bpycof),将tp-bpycof和壳聚糖的混合溶液涂覆于玻碳电极表面,通过酰胺反应将(ac)29单链dna组装到电极表面,再通过dna互补杂交将(gt)29单链dna连接到电极上制得(gt)29/(ac)29/tp-bpycof修饰玻碳电极,以(gt)29/(ac)29/tp-bpycof修饰玻碳电极为工作电极,将工作电极、参比电极和对电极一起置于ir(ppy)3的乙腈溶液中,构成以tp-bpycof为ir(ppy)3的阴极电化学发光共反应剂的tp-bpycof-ir(ppy)3体系,采用mpi-b型电化学发光测试系统测试tp-bpycof修饰玻碳电极在-2.5~+0.2v电位范围内的ecl信号;(gt)29/(ac)29/tp-bpycof修饰电极在ir(bpy)3的乙腈溶液中有强的阴极电化学发光信号;当将(gt)29/(ac)29/tp-bpycof修饰电极置于ru(bpy)32+的磷酸盐缓冲溶液反应后,ru(bpy)32+通过静电作用嵌入到(gt)29/(ac)29双链中,构成以tp-bpycof为ru(bpy)32+的阴极电化学发光共反应剂的tp-bpycof-ru(bpy)32+体系,产生强的ru(bpy)32+的阴极电化学发光信号;此外,ir(ppy)3的电化学发光发射光谱与ru(bpy)32+的紫外吸收光谱重叠,ir(ppy)3为能量供体,ru(bpy)32+为能量受体,ru(bpy)32+与ir(ppy)3之间发生电化学发光共振能量转移,使得ru(bpy)32+的电化学发光信号增强而ir(bpy)3的电化学发光信号减弱。
(gt)29/(ac)29/tp-bpycof修饰玻碳电极的制备,步骤如下:
s1、制备tp-bpycof:先将三醛基间苯三酚与5,5’-二氨基-2,2’-联吡啶加入玻璃管中,再加入1,4-二恶烷、1.0ml均三甲苯和6m乙酸溶液,混合溶液在液氮浴中快速冷冻,同时将玻璃管内抽真空并进行火焰密封,将密封好的玻璃管放置在120℃的烘箱中反应3天,将产物用无水四氢呋喃洗涤,将得到的棕红色产物在100℃下干燥24h,制成含吡啶的共价有机框架tp-bpycof;
s2、玻碳电极预处理:将玻碳电极依次用1.0、0.3和0.05μm的氧化铝悬浊液打磨,再依次在0.1m的硝酸、无水乙醇和超纯水中超声清洗1分钟,用氮气吹干电极表面;
s3、(gt)29/(ac)29/tp-bpycof修饰玻碳电极的制备:将步骤s1制备的tp-bpycof和壳聚糖的混合溶液滴涂在经步骤s2处理干净的玻碳电极表面,在室温下晾干后,通过酰胺反应将羧基修饰的(ac)29单链dna修饰到玻碳电极表面,再通过dna互补杂交反应将(gt)29单链dna连接到电极上,制得(gt)29/(ac)29/tp-bpycof修饰玻碳电极。
作为优选,三醛基间苯三酚与5,5’-二氨基-2,2’-联吡啶的物质的量分别为0.3mmol和0.2mmol,二者的物质的量的比值为3:2;磷酸盐缓冲溶液的浓度为20mm,ph为7.4;滴涂在玻碳电极表面的tp-bpycof的浓度为0.5mgml-1,壳聚糖的质量百分浓度为0.002%;ir(ppy)3的浓度为5μm;(ac)29和(gt)29的浓度为100nm;(ac)29单链修饰到电极表面的反应条件为室温下反应12h,(gt)29与(ac)29在37℃条件下反应30min杂交形成双链;ru(bpy)32+的浓度为50mm,电极与ru(bpy)32+溶液的反应时间为30min;ir(ppy)3的电化学发光位于505nm处,ru(bpy)32+的电化学发光位于620nm处。
以共价有机框架为共反应剂的电化学发光方法应用于亚砷酸根检测,先将(gt)29/(ac)29/tp-bpycof修饰玻碳电极浸泡在含有不同浓度as(iii)的磷酸盐缓冲溶液中12h,用超纯水清洗电极表面,将电极置于50μl50mmru(bpy)32+的磷酸盐缓冲溶液中30min,用超纯水清洗电极表面,以该电极为工作电极,将工作电极、参比电极和对电极一起置于5μmir(ppy)3的乙腈溶液中,采用mpi-b型电化学发光测试系统测试电极在-2.5~+0.2v电位范围内以及505nm和620nm滤波片条件下的电化学发光信号,根据505nm处ir(ppy)3的电化学发光信号和620nm处ru(bpy)32+的的电化学发光信号的比值(ecl505/ecl620)与as(iii)浓度之间的关系,实现对as(iii)的检测,对as(iii)检测的线性范围为0.1ppt-20ppb,检测限低至0.05ppt。
本发明相较于现有技术,其有益效果是:
(1)本发明以tp-bpycof作为ru(bpy)32+和ir(ppy)3的阴极ecl共反应剂,建立了tp-bpycof-ir(ppy)3和tp-bpycof-ru(bpy)32+的ecl新体系。
(2)本发明构建了基于ir(ppy)3与tp-bpycof之间ecl-ret效应的双波长比率ecl方法,揭示了方法的机理,并用于灵敏检测as(iii)。
(3)以tp-bpycof为ru(bpy)32+和ir(ppy)3的阴极ecl共反应剂,替代传统毒害性大的胺类共反应剂,有利于生态环境的可持续发展。
(4)实现了实际水样中as(iii)的灵敏性和选择性检测,具有良好的应用前景。
附图说明
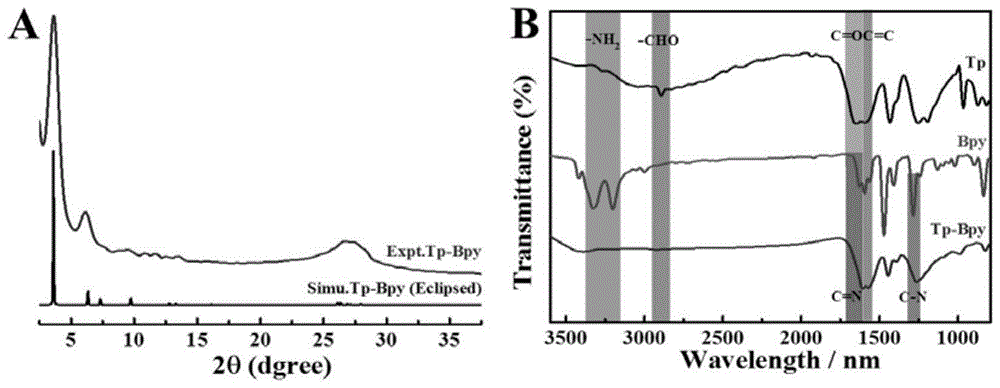
图1是(a)tp-bpycof的pxrd图;(b)tp、bpy和tp-bpycof的红外光谱图。
图2是双波长比率ecl方法构建过程以及对as(iii)检测的示意图。
图3是电极组装过程的cv和eis表征:gce(a);tp-bpycof/gce(b);(ac)29/tp-bpycof/gce(c);(gt)29/(ac)29/tp-bpycof/gce(d);ru(bpy)32+/(gt)29/(ac)29/tp-bpycof/gce(e);ru(bpy)32+/as(iii)/(gt)29/(ac)29/tp-bpycof/gce(f),as(iii)的浓度为10ppb。
图4是ecl-电位曲线。(a)gce(a),tp-bpycof/gce(b),tp/gce(c)和bpy/gce(d)在ir(ppy)3溶液中;(b)gce(a),tp-bpycof/gce(b),tp/gce(c)和bpy/gce(d)在ru(bpy)32+溶液中。
图5是不同电极在505nm和620nm处的ecl-时间曲线。tp-bpycof/gce(a),(ac)29/tp-bpycof/gce(b),(gt)29/(ac)29/tp-bpycof/gce(c),ru(bpy)32+/(gt)29/(ac)29/tp-bpycof/gce(d),ru(bpy)32+/as(iii)/(gt)29/(ac)29/tp-bpycof/gce(e)。as(iii)的浓度为10ppb;内插图为620nm处ru(bpy)32+的ecl信号放大图。
图6是(a)双波长ecl传感器505nm和620nm处的ecl信号对不同浓度as(iii)的响应;(b)lg(ecl505/ecl620)-lncas(iii)曲线。
图7是(a)不同干扰物质分别对阴极和阳极的ecl强度的影响;(b)干扰物质对ecl505/ecl620的影响。as(iii)的浓度为10ppb,干扰物质的浓度为100ppb。
具体实施方式
下面结合附图和具体实施例对本发明作进一步阐述,本发明并不限于此;
实施例1
tp-bpycof的制备及表征
制备tp-bpycof:先将三醛基间苯三酚(tp)与5,5’-二氨基-2,2’-联吡啶(bpy)加入玻璃管中,再加入1,4-二恶烷、1.0ml均三甲苯和6m乙酸溶液,混合溶液在液氮浴中快速冷冻,同时将玻璃管内抽真空并进行火焰密封,将密封好的玻璃管放置在120℃的烘箱中反应3天,将产物用无水四氢呋喃洗涤,将得到的棕红色产物在100℃下干燥24h,制成含吡啶的共价有机框架tp-bpycof。
图1a为tp-bpycof的粉末x射线衍射图(pxrd),tp-bpycof在3.6°有很强的衍射峰,这归因于(100)晶面的反射,在7.2°和26.9°处的衍射峰分别归因于tp-bpycof的(200)和(002)晶面,表明tp-bpycof具有高度结晶度。此外,实验测得的pxrd图谱与模拟的pxrd谱图(图1a内插图)基本一致。通过77k下的n2吸附和解吸等温线测得tp-bpycof的比表面积为755m2g-1。图1b为tp、bpy和tp-bpycof的红外光谱图,tp-bpycof的红外光谱图中,tp在2895cm-1处的-cho的伸缩振动峰和bpy在3280cm-1处的-nh2的特征伸缩振动峰消失,在1287cm-1处出现一个新的伸缩振动峰,这归因于-c-n的伸缩振动。以上结果表明,本发明方法成功制备了高结晶度的tp-bpycof。热重实验结果可知,tp-bpycof在高达340℃的温度下仍保持稳定,表明具有良好的热稳定性。
实施例2
tp-bpycof的共反应剂效应
将玻碳电极依次用1.0、0.3和0.05μm的氧化铝悬浊液打磨,再依次在0.1m的硝酸、无水乙醇和超纯水中超声清洗1分钟,用氮气吹干电极表面。10μl0.5mgml-1tp-bpycof和0.002%的壳聚糖(cs)的混合溶液涂覆在处理干净的gce表面,在室温下晾干后,将电极置于含有100nm羧基修饰的(ac)29的单链dna的pbs(20mmph7.4)缓冲溶液中反应12h,将(ac)29通过酰胺反应修饰到电极表面,在用超纯水清洗电极之后,再将制得的电极浸泡在含有100nm(gt)29的单链dna的pbs(20mmph7.4)缓冲溶液中,在37℃反应30min,(gt)29通过dna互补杂交反应连接到电极上,制得(gt)29/(ac)29/tp-bpycof/gce,电极修饰过程以及对as(iii)检测示意图如图2所示。
由图3a可见,在ir(ppy)3的乙腈溶液中,gce只有弱的阴极ecl(曲线a),tp-bpycof/gce在-2.4v处显示出强的ecl信号(曲线b),tp/gce(曲线c)和bpy/gce(曲线d)的阴极信号稍有增强,但ecl信号明显差于tp-bpycof/gce,因此,tp-bpycof/gce可作为ir(ppy)3的阴极ecl共反应剂增强ir(ppy)3的阴极ecl信号。在ru(bpy)32+的磷酸盐缓冲溶液中,tp-bpycof/gce也呈现出阴极ecl的增强作用(图3b)。因此,tp-bpycof既可以作为ir(ppy)3的阴极ecl共反应剂也可以作为ru(bpy)32+的阴极ecl共反应剂。
tp-bpycof的共反应剂效应机理解释如下:以tp-bpycof-ru(bpy)32+体系为例,ru(bpy)32+在阴极电位下失去电子被还原成ru(bpy)3+,同时tp-bpycof上的吡啶n也失去电子并发生质子化反应,电子转移后生成更加稳定的tp-bpycof·自由基;tp-bpycof·与ru(bpy)32+反应生成ru(bpy)33+和tp-bpycof;反应生成的ru(bpy)33+进一步与ru(bpy)3+反应生成激发态的ru(bpy)32+*;同时tp-bpycof·也可以与ru(bpy)3+发生氧化还原反应生成ru(bpy)32+*;所得的ru(bpy)32+*释放能量返回到基态,产生强的阴极ecl信号。对于tp-bpycof-ir(ppy)3体系,其反应机理与tp-bpycof/gce-ru(bpy)32+体系相同。
实施例3
ecl传感器的构建及表征
采用循环伏安法(cv)和交流阻抗法(eis)对ecl传感器的构建过程进行表征。由图4a可见,在[fe(cn)6]3-/4-溶液中,gce有一个明显的氧化还原峰(曲线a);tp-bpycof/gce上的峰电流明显减弱(曲线b);由于(ac)29单链dna具有带负电的磷酸骨架,(ac)29/tp-bpycof/gce上的电流进一步减小(曲线c);当(gt)29通过dna杂交连接到电极表面时,峰电流进一步减小(曲线d);(gt)29/(ac)29/tp-bpycof/gce在ru(bpy)32+溶液中反应30min后,因为ru(bpy)32+带正电,电极的峰电流略有增加(曲线e);当存在10ppbas(iii)时,电极的峰电流明显增强(曲线f),这是由于as(iii)与(gt)29特异性结合,使得(gt)29不能通过dna杂交连接到电极上所致。图4b为电极组装过程的eis谱图,阻抗大小与循环伏安法的结果相对应,以上结果表明成功构建了ecl传感器。
图5是不同电极在505nm和620nm处的ecl-时间曲线。在ir(ppy)3的乙腈溶液中,tp-bpycof/gce在505nm处有强的阴极ecl信号(曲线a),这是由于tp-bpycof作为ir(ppy)3的共反应剂能增强ir(ppy)3的阴极ecl信号。当(ac)29通过酰胺反应连接到电极上(曲线b),(gt)29通过dna杂交连接到电极表面(曲线c),ecl信号逐步减弱,这是由于dna单链以及双链的磷酸骨架带负电阻碍了电子的传递。(gt)29/(ac)29/tp-bpycof/gce在ru(bpy)32+溶液中反应30min后,ru(bpy)32+嵌入到dna双链中,在620nm处产生强的ru(bpy)32+的阴极ecl信号;此外,由于ir(ppy)3和ru(bpy)32+之间的能量共振转移效应以及ru(bpy)32+引入电极表面后与ir(ppy)3竞争tp-bpycof的共反应剂增强作用,505nm处ir(ppy)3的ecl信号由于上述双重猝灭效应而明显减弱,620nm处ru(bpy)32+的ecl信号则由于双重放大效应而明显增强(曲线d)。当as(iii)存在时,as(iii)与(gt)29特异性结合,导致(gt)29不能通过dna互补杂交连接到电极表面,ru(bpy)32+也不能通过静电作用嵌入到到电极表面,从而505nm处的ir(ppy)3的ecl信号恢复,而620nm处ru(bpy)32+的ecl减弱(曲线e)。以上结果表明该传感器可以用于检测as(iii)。
实施例4
双波长比率ecl传感器对as(iii)的检测
先将(gt)29/(ac)29/tp-bpycof/gce浸泡在含有不同浓度as(iii)的磷酸盐缓冲溶液中12h,用超纯水清洗电极表面,将电极置于50μl50mmru(bpy)32+的磷酸盐缓冲溶液中30min,用超纯水清洗电极表面,以该电极为工作电极,将工作电极、参比电极和对电极一起置于5μmir(ppy)3的乙腈溶液中,采用mpi-b型电化学发光测试系统测试电极在-2.5~+0.2v电位范围内以及505nm和620nm滤波片条件下的电化学发光信号,根据505nm处ir(ppy)3的电化学发光信号和620nm处ru(bpy)32+的的电化学发光信号的比值(ecl505/ecl620)与as(iii)浓度之间的关系,实现对as(iii)的检测,
图6a是双波长ecl传感器505nm和620nm处的ecl信号对不同浓度as(iii)的响应。随着as(iii)浓度的增加,as(iii)与(gt)29结合的越多,更多的(gt)29不能通过dna杂交修饰到电极上,导致ru(bpy)32+不能修饰到电极表面,所以505nm处ir(ppy)3的ecl信号逐渐恢复,而620nm处ru(bpy)32+的ecl信号逐渐减小。图6b是lg(ecl505/ecl620)-lncas(iii)曲线,对as(iii)检测的线性范围为0.1ppt-20ppb,检测限为0.05ppt(s/n=3),远低于环境保护署规定的饮用水中as(iii)浓度的最高限值(10ppb)。本发明方法对as(iii)的检测限比wang等人基于砷与小分子化合物的结合构建的荧光传感器检测砷的1.32ppb(tian,x.;chen,l.;li,y.;yang,c.;nie,y.;zhou,c.;wang,y.,designandsynthesisofamoleculewithaggregation-inducedemissioneffectsanditsapplicationinthedetectionofarseniteingroundwater.j.mater.chem.c2017,5,3669-3672)和kam等人通过双金属纳米粒子阳极溶出伏安法检测砷的1.2ppb(moghimi,n.;mohapatra,m.;leung,k.t.,bimetallicnanoparticlesforarsenicdetection.anal.chem.2015,87,5546-5552)更低。
为了评估本发明方法构建的ecl传感器的选择性,考察了ecl传感器对含100ppb其它离子的ecl响应,结果如图7a所示,505nm处ir(ppy)3的ecl信号和620nm处ru(bpy)32+的ecl信号在hg2+和ag+存在时分别稍有变化,这是由于hg2+和ag+分别会与t碱基和c碱基结合而影响(gt)29和(ac)29的dna杂交,从而影响ru(bpy)32+嵌入到双链中的效率。但是,比率型ecl传感器对as(iii)有良好的响应,而对浓度是as(iii)十倍的其它离子几乎没有响应(图7b),表明本发明构建的双波长比率型ecl方法对as(iii)检测具有良好的选择性。
为了验证本发明方法在环境样品分析中的实用性,对自来水、湖水以及赣江水进行了加标回收实验,分别向实际水样中加入不同浓度的as(iii),本发明方法对as(iii)的加标回收率为96.2%-110%,表明本发明方法对as(iii)检测具有良好的可靠性。
- 还没有人留言评论。精彩留言会获得点赞!