一种药物对破骨细胞抑制程度的标曲定量方法
1.本发明属于生物技术方法领域,具体涉及一种药物对破骨细胞抑制程度的标曲定量方法。
背景技术:
2.破骨细胞是人体中维持骨代谢平衡的重要细胞,但是在特定情况下破骨的异常活化导致了骨量丢失甚至骨质疏松的出现。因此,研究破骨细胞抑制的药物成为一个热门方向。其中重要的一项评估,是药物对于破骨细胞trap染色阳性细胞的抑制效果。
3.目前对于trap染色,通常采用组间的trap阳性破骨细胞面积、破骨细胞数量比较来进行药物对破骨细胞的抑制程度,这种方式在半定量指标上具有显著优势。
4.但同时,trap染色评估药物对破骨细胞抑制程度的研究也主要限于组间比较,未有能以标准数值衡量的方法。申请号为cn201910074013.6的专利公布了一种白细胞介素2抑制破骨细胞生成和功能的新用途,其中评估方式为比较trap染色阳性细胞数,这一指标易随培养条件而改变,不具有稳定性。申请号为cn201811074899.6的专利公开了奇任醇在制备抑制破骨细胞形成和/或破骨细胞活性药物中的应用,其中评估方式为比较trap染色阳性面积及细胞数,同理具有不稳定性。诸如此类的专利对破骨细胞抑制程度的评价限于不稳定性指标。因此需要一种药物对破骨细胞抑制程度的标曲定量方法,使药物的破骨细胞抑制得到定量化统计,从而更好地实现对药物效果的评估。
技术实现要素:
5.有鉴于此,本发明的目的在于提供一种药物对破骨细胞抑制程度的标曲定量方法及其应用。将药物对破骨细胞抑制程度指标定量化,更准确地实现对药物效果的评估。
6.为实现上述目的,本发明提供以下技术方案:设置梯度rankl浓度诱导破骨细胞组,并设置梯度rankl浓度加药物诱导破骨细胞组,根据两组的破骨trap指标及rankl浓度标曲,根据横轴差得出药物的rankl拮抗当量。
7.进一步,所述梯度rankl浓度范围为0
‑
100ng/ml,优选地,采用0、12.5、25、50、75、100ng/ml rankl浓度作为标准梯度。
8.进一步,所述药物包括含rank抗体、rankl拮抗剂的药物。
9.进一步,所述破骨trap指标包括破骨细胞面积及破骨细胞面积,优选地,采用破骨细胞面积作为指标。
10.相比现有评估药物对破骨细胞抑制功能的方法,本发明显著的进步在于:
11.1)通过rankl当量指标定量化药物抑制作用。
12.2)具有高度可重复性及可复制性。
13.因此,药物对破骨细胞抑制程度的标曲定量方法可更加精确地实现对药物破骨细胞抑制程度地评估。
附图说明
14.为了使本发明的目的、技术方案和有益效果更加清楚,本发明提供以下附图进行说明:
15.图1确认药物的破骨抑制作用。
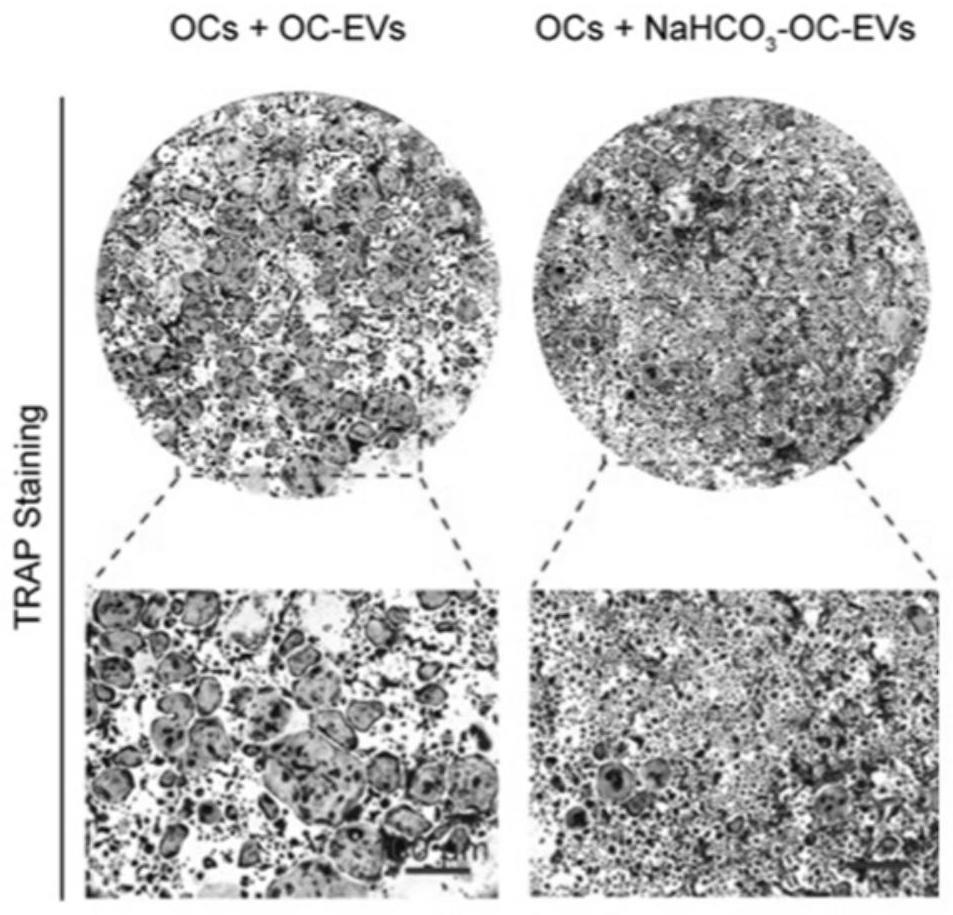
16.图2梯度rankl浓度下的破骨细胞trap染色。
17.图3梯度rankl浓度下的破骨细胞指标统计。
具体实施方式
18.下面结合实施例对本发明提供的一种药物对破骨细胞抑制程度的标曲定量方法及其应用进行详细的说明,但是不能把它们理解为对本发明保护范围的限定。
19.本发明中的优选案例为采用0、12.5、25、50、75、100ng/ml rankl浓度作为标准梯度,采用破骨细胞面积为指标,进行含rankl药物的破骨细胞抑制的定量评估。
20.本发明还可以使用其他浓度梯度、其他的评价指标、其他上述药物,均可获得相同的技术效果。
21.实施例1、对含rankl药物的0、12.5、25、50、75、100ng/ml rankl浓度的破骨细胞面积指标评估。
22.1、培养bmdm细胞,加入20ng/ml m
‑
csf诱导。
23.2、5天后,按10000每孔进行96孔板铺板。
24.3、各孔加入20ng/ml m
‑
csf和梯度浓度rankl,并设置含rankl药物组和对照组。
25.4、5天后,将两组细胞进行trap染色,计算破骨细胞面积。
26.5、将破骨细胞面积进行定量统计,并绘制标准曲线进行比较。
27.6、计算横轴差,即为药物抑制破骨细胞的rankl当量。
28.实施例2、对含rankl药物的0、20、40、60、80、100ng/ml rankl浓度的破骨细胞数量指标评估。
29.1、培养bmdm细胞,加入20ng/ml m
‑
csf诱导。
30.2、5天后,按10000每孔进行96孔板铺板。
31.3、各孔加入20ng/ml m
‑
csf和梯度浓度rankl,并设置含rankl药物和对照组。
32.4、5天后,将两组细胞进行trap染色,计算破骨细胞数量。
33.5、将破骨细胞数量进行定量统计,并绘制标准曲线进行比较。
34.6、计算横轴差,即为药物抑制破骨细胞的rankl当量。
35.实施例3、对含rank抗体药物的0、12.5、25、50、75、100ng/ml rankl浓度的破骨细胞数量指标评估。
36.1、培养bmdm细胞,加入20ng/ml m
‑
csf诱导。
37.2、5天后,按10000每孔进行96孔板铺板。
38.3、各孔加入20ng/ml m
‑
csf和梯度浓度rankl,并设置含rank抗体药物组和对照组。
39.4、5天后,将两组细胞进行trap染色,计算破骨细胞数量。
40.5、将破骨细胞数量进行定量统计,并绘制标准曲线进行比较。
41.6、计算横轴差,即为药物抑制破骨细胞的rankl当量。
42.实施例1中确认药物的破骨抑制作用。
43.1、将正常培养破骨细胞与药物抑制破骨细胞进行培养,并进行trap染色。
44.2、统计比较两组trap阳性细胞面积比和数量,如图1。
45.实施例1中梯度rankl浓度下的破骨细胞trap染色。
46.1、将对照组和药物组细胞分别以0、12.5、25、50、75、100ng/ml rankl浓度诱导。
47.2、统计比较两组trap阳性细胞面积比和数量,发现各组组内呈现与rankl浓度相关的破骨细胞诱导效果,如图2。
48.实施例1中梯度rankl浓度下的破骨细胞指标统计。
49.1、对两组trap阳性细胞面积比进行统计,并绘制柱状图和标曲。
50.2、计算两条标准曲线的横轴差,即为药物破骨抑制的rankl当量。
51.对实施例2、3所得的药物对破骨细胞抑制程度的标曲定量方法分别进行确认药物的破骨抑制作用、梯度rankl浓度下的破骨细胞trap染色、梯度rankl浓度下的破骨细胞指标统计,与实施例1中间药物对破骨细胞抑制程度的标曲定量方法结果相似,这表明可通过其他浓度梯度、其他的评价指标、其他上述药物,实现效果类似的药物对破骨细胞抑制程度的标曲定量方法。
52.由上述实施例可知,本发明提供的药物对破骨细胞抑制程度的标曲定量方法及其应用,将药物对破骨细胞抑制程度指标定量化,更准确地实现对药物效果的评估。
53.以上所述仅是本发明的优选实施方式,应当指出,尽管通过上述优选实施例已经对本发明进行了详细的描述,但本技术领域的技术人员来应当理解,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围,不偏离本发明权利要求书所限定的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1