一种硝酸盐和亚硝酸盐的分光光度法检测方法
1.本发明涉及检测技术领域,尤其是涉及一种硝酸盐和亚硝酸盐的分光光度法检测方法。
背景技术:
2.硝酸盐和亚硝酸盐作为环境污染物而广泛存在于大自然中,在地表水、地下水以及动植物和食品中都有发现。随着工业化的不断推进,硝酸盐和亚硝酸盐的污染来源也日益增多。人工化肥、生活污水以及一些化石燃料燃烧后的含氨废气在自然条件下经降雨分解形成硝酸及亚硝酸盐渗入地下,从而造成水质的污染,不仅会影响人类,而且会涉及整个生物圈。这是硝酸盐和亚硝酸盐不利的影响,因此需要检测和定量。另外,硝酸盐和亚硝酸盐也有其有利的一面,比如刚刚兴起的等离子体活化水。用放电等离子体辐照水可将等离子体中的活性成分转移到水中,若在空气中放电,则可在水中形成硝酸根离子、亚硝酸根离子及双氧水等重要的活性成分,可应用于灭菌、消毒等领域,因此对等离子体活化水中硝酸根离子、亚硝酸根离子的定量也十分重要。当前存在许多硝酸盐和亚硝酸盐的探测方法,包括分光光度法、荧光法、化学发光法和液相色谱法等。采用griess试剂的分光光度法检测是目前最常用的技术。但上述技术要么工艺复杂、要么需要有毒的化学试剂,目前仍缺乏能同时检测硝酸盐和亚硝酸盐的简单、快速方法,因此开发一种简单、快速、无需有毒试剂的技术来检测硝酸盐和亚硝酸盐是十分必要的。
技术实现要素:
3.本发明的目的在于提供一种简单、快速、不需要有毒试剂且可同时检测硝酸盐和亚硝酸盐的分光光度法检测方法。由于能够同时测定硝酸盐和亚硝酸盐,可大大提高检测效率。
4.本发明包括以下步骤;
5.1)试样预处理:将待测溶液的ph值调节至6~10之间待用;
6.2)配制标准浓度溶液:用去离子水配制硝酸钠和亚硝酸钠母液,通过逐级稀释得到各种浓度的溶液待用(各溶液ph值在6~10之间);
7.3)绘制标准浓度曲线:以去离子水为基底,采用紫外
‑
可见分光光度计测量步骤2)所制备标准浓度溶液的吸收光谱,通过逐级求导得到其二阶和三阶导数吸收光谱;分别得到硝酸钠和亚硝酸钠纯组分溶液在其二阶和三阶导数吸收光谱上的拐点,并依据比尔
‑
朗伯吸收定律得出相应的计算公式(具体原理及公式见具体实施方式的工作曲线绘制部分);
8.4)待测溶液测定:将步骤1)的所述待测溶液置于光谱仪上测定其吸收光谱,通过逐级求导得到二阶及三阶导数吸收光谱,再通过步骤3)所得公式,利用导数光谱拐点处的数据即可计算得出硝酸盐和亚硝酸盐在待测溶液中的浓度。
9.在步骤1)中,所述试样预处理的具体步骤可为:取待测溶液检测其ph值,若待测溶液ph值满足6<ph<10,则不进行处理,待用;若待测溶液ph<6或ph>10,则用ph=7的磷酸
缓冲液调节至ph值到6~10之间待用,并记下稀释比例,待测定后换算;
10.在步骤3)中,所述绘制标准浓度曲线具体方法可为:以去离子水为基底,测量所制备已知浓度纯组分标准浓度溶液的吸收光谱,通过逐级求导得到二阶和三阶导数吸收光谱,从导数光谱分别得到硝酸钠和亚硝酸钠溶液在其二阶和三阶导数吸收光谱上的拐点,并依据比尔
‑
朗伯吸收定律得出相应硝酸盐和亚硝酸盐的水溶液n阶导数吸收光谱的计算公式:
[0011][0012]
其中,a
λ
表示在波长λ处的吸光度,l表示样品光程长度,n为2或3;和分别表示在波长λ处硝酸盐和亚硝酸盐的消光系数,c
no3
‑
和c
no2
‑
分别表示在溶液中硝酸盐和亚硝酸盐的浓度;和分别表示纯组分硝酸盐和亚硝酸盐溶液n阶吸收光谱强度的干扰项。
[0013]
在步骤4)中,所述利用导数光谱拐点处的数据即可计算得出硝酸盐和亚硝酸盐在待测溶液中的浓度的具体方法为:在纯组分的导数吸收光谱中存在拐点波长,在该波长处,纯组分溶液的导数吸收光谱强度为零;若在硝酸根的拐点波长λ
a
处,d
n
α
no3
‑
λ
/dλ
n
=0,则对硝酸盐和亚硝酸盐的混合溶液,在波长λ
a
处的n阶吸收光谱强度为:
[0014][0015]
亚硝酸盐在待测溶液中的浓度为:
[0016][0017]
同理,硝酸盐在待测溶液中的浓度可从亚硝酸根的拐点波长λ
b
处得到:
[0018][0019]
本发明的优点:本发明原理是纯组分硝酸盐或亚硝酸盐溶液的二阶和三阶导数的吸收光谱中存在拐点。对纯组分硝酸盐(亚硝酸盐)溶液,在其吸收光谱的拐点处,导数吸收光谱强度为零且与硝酸盐(亚硝酸盐)浓度无关。因此对硝酸盐和亚硝酸盐的混合溶液,可通过硝酸盐拐点处的吸收强度来测量溶液中亚硝酸盐的浓度,同理,硝酸盐的浓度也可以从亚硝酸盐的拐点处获得。本发明采用紫外
‑
可见分光光度计直接对样品进行吸收光谱检测,通过对吸收光谱进行求导,可有效将不同成分重叠的光谱带分离开来,同时可减少散射、背地、基质或其他吸收物的干扰。本发明方法快速、简单、可操作性强且不需要任何化学试剂,可应用于饮用水、等离子体活化水等中的硝酸盐和亚硝酸盐快速探测。本发明采用二阶及三阶导数吸收光谱中的拐点来进行计算,但若所用光谱仪精度高,也可扩展到更高阶导数中的拐点。
附图说明
[0020]
图1为所测已知浓度纯组分硝酸钠和纯亚硝酸钠的零阶、二阶及三阶导数吸收光谱。
[0021]
图2为所测几组已知浓度硝酸钠和亚硝酸钠混合溶液的零阶、二阶及三阶导数吸收光谱。
具体实施方式
[0022]
为了更好地理解本发明,下面实施例将结合附图进一步阐明本发明的内容,但本发明不仅仅局限于下面的实施例。
[0023]
以下实施例中用到的试剂、仪器及工作曲线如下:
[0024]
1、试剂:分析纯硝酸钠、亚硝酸钠试剂。
[0025]
2、仪器:岛津uv
‑
1780紫外分光光度计。
[0026]
3、工作曲线绘制:
[0027]
(1)硝酸钠及亚硝酸钠标准液配制(1000mg/l):准确称取0.1g的硝酸钠或硝酸钠,分别溶解于含有100ml去离子水的两个容量瓶中,得到1000mg/l标准溶液,通过逐级稀释配制得到浓度分别为500mg/l、250mg/l、100mg/l、50mg/l、25mg/l、10mg/l、8mg/l、6mg/l、4mg/l、2mg/l的硝酸钠及亚硝酸钠溶液,待用。
[0028]
(2)采用10mm光程的石英比色皿,以去离子水作为背底,测量以上所配各种溶液的在190~500nm的吸收光谱,结果如图1所示。
[0029]
(3)找出纯组分溶液导数吸收光谱中的拐点波长。在二阶导数吸收光谱中,224.5nm(≤25mg/l)和294.5(≥100mg/l)是亚硝酸根的吸收光谱拐点,用于硝酸根测量;217.0nm(≤25mg/l)、390nm(≥100mg/l)是硝酸根的吸收光谱拐点,用于亚硝酸根测量;在三阶导数吸收光谱中,236.5nm(≤25mg/l)和284.5(≥100mg/l)是亚硝酸根的吸收光谱拐点,用于硝酸根测量;228.5nm(≤25mg/l)、402.0nm(≥100mg/l)是硝酸根的吸收光谱拐点,用于亚硝酸根测量。由实验可知,硝酸根和亚硝酸根浓度若在25mg/l~100mg/l之间,其吸收谱在短波长拐点处,不满足比尔吸收定律,而在长波长拐点处,吸收强度过低,因而都不能用于计算其浓度。因此,对硝酸根和亚硝酸根浓度在25mg/l~100mg/l之间的溶液,可先稀释,再用短波长拐点处强度进行计算。
[0030]
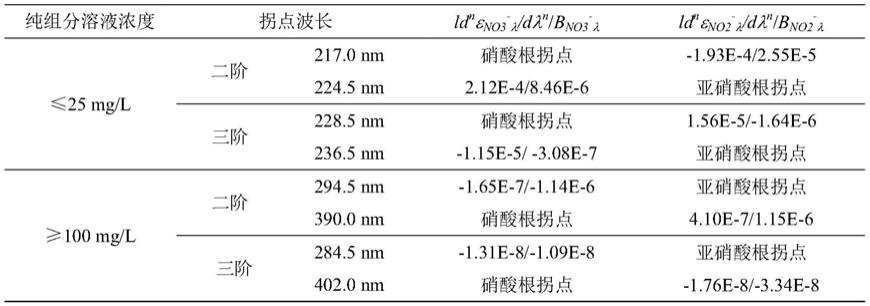
根据图1中所得数据,通过线形拟合得到在二阶及三阶吸收光谱中的硝酸根及亚硝酸根拐点处强度和浓度的线性关系式,见表1,可供计算混合溶液中硝酸盐和亚硝酸盐的浓度。
[0031]
表1.利用图1中标准吸收曲线,在各拐点处得到的各线性关系中的斜率及截距
[0032][0033]
本发明实施例包括试样预处理、标准浓度曲线绘制、各样品测定;具体步骤如下:
[0034]
1)试样预处理:取待测溶液检测其ph值,若溶液ph值满足6<ph<10,则不进行处理,待用,若ph<6或ph>10,则用ph=7的磷酸缓冲液调节至6
‑
10之间待用,并记下稀释比例待测定后换算。溶液ph值要求:因为硝酸根和亚硝酸根的吸收光谱和溶液ph值有关,故测量需要溶液ph值满足6<ph<10(tachibana k and nakamura t 2020japanese journal of applied physics 59 056004)。
[0035]
2)标准浓度曲线绘制:用去离子水配制一定浓度的硝酸钠和亚硝酸钠母液,通过逐级稀释得到各种浓度的溶液待用,各溶液ph值在6~10之间。
[0036]
3)仪器工作条件设定:按照仪器操作规程将光谱仪调至最佳状态;
[0037]
4)标准浓度曲线的绘制:以去离子水为基底,测试步骤2)所制备已知浓度纯组分标准品的吸收光谱,通过逐级求导得到二阶和三阶导数吸收光谱,分别得到硝酸钠和亚硝酸钠溶液在其二阶和三阶导数吸收光谱上的拐点,并依据比尔
‑
朗伯吸收定律得出相应的计算公式(具体原理见步骤7)。
[0038]
5)拐点波长的位置:在二阶导数吸收光谱中,224.5nm(≤25mg/l)和294.5(≥100mg/l)是亚硝酸根的吸收光谱拐点,用于硝酸根测量;217.0nm(≤25mg/l)、390.0nm(≥100mg/l)是硝酸根的吸收光谱拐点,用于亚硝酸根测量;在三阶导数吸收光谱中,236.5nm(≤25mg/l)和284.5(≥100mg/l)是亚硝酸根的吸收光谱拐点,用于硝酸根测量;228.5nm(≤25mg/l)、402.0nm(≥100mg/l)是硝酸根的吸收光谱拐点,用于亚硝酸根测量。
[0039]
6)待测溶液测定:将步骤1)的所述待测溶液置于光谱仪上测定其吸收光谱,通过逐级求导得到二阶及三阶导数吸收光谱。通过步骤4)所得出的计算公式,利用导数光谱拐点处的数据即可计算得出硝酸钠和亚硝酸钠在待测溶液中的浓度。
[0040]
7)测量所依据的原理及公式:依据各组分吸收强度的可叠加性,在波长λ处,含有硝酸盐和亚硝酸盐的水溶液的吸收光谱强度为:
[0041][0042]
其中,a
λ
表示在波长λ处的吸光度,l表示样品光程长度,和分别表示在波长λ处硝酸盐和亚硝酸盐的消光系数,c
no3
‑
和c
no2
‑
分别表示在溶液中硝酸盐和亚硝酸盐的浓度。则含有硝酸盐和亚硝酸盐的水溶液的n阶导数吸收光谱为:
[0043][0044]
和可通过线性拟合纯硝酸盐或纯亚硝酸盐溶液的n阶吸收
光谱强度得到(公式3和公式4)。因实际拟合中通常会存在一些干扰因素,从而在式(3)和(4)需要引入截距和而硝酸盐和亚硝酸盐的水溶液的n阶导数吸收光谱式(2)变为式(5);
[0045][0046][0047][0048]
实验发现,在纯组分的导数吸收光谱中,存在拐点波长,在该波长处,纯组分溶液的导数吸收光谱强度为零;在硝酸根的拐点波长λ
a
处,则对硝酸盐和亚硝酸盐的混合溶液,在波长λ
a
处的n阶吸收光谱强度为:
[0049][0050]
因此,亚硝酸盐浓度可从公式(6)得到:
[0051][0052]
同理,硝酸盐浓度可从亚硝酸根的拐点波长λ
b
处得到:
[0053][0054]
本发明先配制各种浓度比例硝酸钠及亚硝酸钠混合溶液,测量混合溶液ph值,各值均在6~10的范围内,符合检测所要求ph值范围,再用紫外
‑
可见分光光度计测量所配制混合溶液的吸收光谱,通过逐级求导计算其二阶及三阶导数吸收光谱,图2给出几组已知浓度硝酸钠和亚硝酸钠混合溶液的零阶、二阶及三阶导数吸收光谱。根据本发明公式及表1中线形关系,计算溶液中硝酸钠及亚硝酸钠的浓度,结果如表2,可见测量结果与实际情况符合较好。
[0055]
表2.硝酸钠和亚硝酸钠混合溶液中相应成分浓度的实际值与测量值
[0056][0057]
*
在二阶导数吸收光谱中,224.5nm(≤25mg/l)和294.5(≥100mg/l)是no2‑
的吸收光谱拐点,用于no3‑
测量;217.0nm(≤25mg/l)、390.0nm(≥100mg/l)是no3‑
的吸收光谱拐点,用于no2‑
测量;在三阶导数吸收光谱中236.5nm(≤25mg/l)和284.5(≥100mg/l)是no2‑
的吸收光谱拐点,用于no3‑
测量;228.5nm(≤25mg/l)、402.0nm(≥100mg/l)是no3‑
的吸收光谱拐点,用于no2‑
测量。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1