干血片样本采集质量的监控方法与流程
1.本发明属于血液(尤指指尖血)样本采集中干血片样本采集质量控制技术领域,具体涉及一种利用甘氨鹅脱氧胆酸(glycochenodeoxycholic acid)和/或甘油三酯tag 56:4作为判断干血片样本采集质量的质检指示物的应用,还涉及通过利用甘氨鹅脱氧胆酸和/或甘油三酯tag 56:4在干血片样本中的相对含量为指标进行判断的干血片样本采集质量的监控方法以及干血片样本代谢组学检测结果的评价方法。
背景技术:
2.血液是研究、诊断、健康和药物监测中最常用的生物样本,也是代谢组学研究的常用样本,检测其中的代谢物已成为诊断疾病和评估健康水平等的有效手段。随着精准医疗、个性化治疗和健康管理等多种代谢组学应用场景的扩展,已提出多种血液样本采集方式的应用需求,主要包括末梢采血、静脉采血、动脉采血等血液检验的常见样本采集方式,其中静脉采血最为常用,末梢采血操作最为简单。指尖血干血片采样作为末梢采血的一种方式,与静脉采血相比,具有很多优势:1.微创,成本低;2.样本需求量少;3.在常规环境下稳定,方便运输和储存;4.操作简单,简单培训即可操作,为居家检测提供了可能性;5.适合医疗条件不足或偏远地区的采样和多个中心的大队列研究。
3.尽管指尖血干血片采样操作简单,但相对于其他采血方式更容易受到环境、个体差异(出血量)、饮食和组织液及细胞内液混入等情况的影响。因此,指尖血干血片样本的采集需标准化,并把握质控关键点,以保证样本的质量和稳定性。然而,目前尚未有针对血液代谢组学研究的指尖血干血片样本采集中质量监控的方法,尤其缺少基于干血片样本采集质量对样本中代谢组学检测结果是否可用的评价方法和判定标准。
技术实现要素:
4.针对现有技术中存在的问题的一个或多个,本发明的一个方面提供一种干血片样本采集质量的监控方法,其包括对采集后的干血片样本中的甘氨鹅脱氧胆酸或/和甘油三酯tag 56:4及外加的各自的标定物质的信号强度(以液相色谱质谱(lc
‑
ms)和气相色谱质谱(gc
‑
ms)之一检测的峰面积或峰高表示)进行检测,以甘氨鹅脱氧胆酸及其标定物质赤霉酸的信号强度比值表示的甘氨鹅脱氧胆酸在干血片样本中的相对含量(m),或/和甘油三酯tag 56:4及其标定物质磷脂酰乙醇胺pe(17:0/17:0)的信号强度比值表示的甘油三酯tag 56:4在干血片样本中的相对含量(n)作为监控指标,当m或/和n满足某数值时,判定干血片样本的采集质量符合要求。
5.上述监控方法中,其中当所述甘氨鹅脱氧胆酸在干血片样本中的相对含量m小于由以下式(i)表示的x1,优选不大于由下式(ii)表示的x2,进一步优选处于由以下式(iii)表示的x3的范围内时,所述干血片样本的采集质量符合要求(例如:用于采集所述干血片样本的受试者处于空腹状态,优选至少禁食12小时):
[0006][0007][0008][0009]
式(i)中,k1=0.413;式(ii)中,k2=0.168;式(iii)中,k3=0.051~0.168;
[0010]
式(i)、(ii)和(iii)中,ra为0.84μg/ml,r1表示实际上机检测时样品中赤霉酸的上机终浓度(检测浓度),其单位为μg/ml;
[0011]
优选地,其中当采用液相色谱质谱联用仪(lc
‑
ms)测定甘氨鹅脱氧胆酸在干血片样本中的相对含量时,具体包括以下步骤:
[0012]
t1)将干血片样本置于冷(甲基叔丁基醚:甲醇,体积比3:1)溶液(在该溶液中预先加入甘氨鹅脱氧胆酸的标定物质赤霉酸)中,涡旋混匀提取血液样品,获得第一样品提取液;
[0013]
t2)向第一样品提取液中加入(甲醇:水,体积比3:1)溶液,涡旋并离心分层;
[0014]
t3)样品分层后,取下层水相的澄清部分至离心管中,并向其中加入冰甲醇沉淀蛋白质,蛋白质沉淀后离心,取上清液转移至新的离心管中,并干燥过夜;
[0015]
t4)向步骤t3)干燥后的离心管中加入水,并孵化;
[0016]
t5)孵化后,将离心管涡旋混匀,并在超声处理后离心;
[0017]
t6)取步骤t5)离心后的上清液作为水相,上机检测获得甘氨鹅脱氧胆酸及其标定物质赤霉酸的质谱数据;
[0018]
t7)由步骤t6)上机检测获得的质谱数据中的峰面积或峰高作为检测信号强度,计算出干血片样本中甘氨鹅脱氧胆酸的相对含量。
[0019]
上述监控方法中,其中当所述甘油三酯tag 56:4在干血片样本中的相对含量n小于由以下式(iv)表示的y1,优选不大于由以下式(v)表示的y2,进一步优选处于由以下式(vi)表示的y3的范围内时,所述干血片样本的采集质量符合要求(例如:用于采集所述干血片样本的受试者处于空腹状态,优选至少禁食12小时):
[0020][0021][0022][0023]
式(iv)中,l1=0.0295;式(v)中,l2=0.0253;式(vi)中,l3=0.0129~0.0253;
[0024]
式(iv)、(v)和(vi)中,rb为2.33μg/ml,r2表示实际上机检测时样品中磷脂酰乙醇胺pe(17:0/17:0)的上机终浓度(检测浓度),其单位为μg/ml;
[0025]
优选地,其中当采用液相色谱质谱联用仪(lc
‑
ms)测定甘油三酯tag 56:4在干血片样本中的相对含量时,具体包括以下步骤:
[0026]
s1)将干血片样本置于冷(甲基叔丁基醚:甲醇,体积比3:1)溶液(在该溶液中预先加入甘油三酯tag 56:4的标定物质磷脂酰乙醇胺pe(17:0/17:0))中,涡旋混匀提取血液样
品,获得第二样品提取液;
[0027]
s2)向第二样品提取液中加入(甲醇:水,体积比3:1)溶液,涡旋并离心分层;
[0028]
s3)样品分层后,取上层有机相至离心管中;
[0029]
s4)有机相干燥后,加入(乙腈:异丙醇,体积比3:1)溶液,孵化后涡旋混匀,并在超声处理后离心;
[0030]
s5)取步骤s4)离心后的上清液作为有机相,上机检测获得甘油三酯tag 56:4及其标定物质磷脂酰乙醇胺pe(17:0/17:0)的质谱数据;
[0031]
s6)由步骤s5)上机检测获得的质谱数据中的峰面积或峰高作为检测信号强度,计算出干血片样本中甘油三酯tag 56:4的相对含量。
[0032]
上述监控方法中,其中当所述甘氨鹅脱氧胆酸在干血片样本中的相对含量m小于由式(i)表示的x1,优选不大于式(ii)表示的x2,进一步优选处于式(iii)表示的x3的范围内,且
[0033]
所述甘油三酯tag 56:4在干血片样本中的相对含量n小于由式(iv)表示的y1,优选不大于式(v)表示的y2,进一步优选处于式(vi)表示的y3的范围内时,所述干血片样本的采集质量符合要求(例如:用于采集所述干血片样本的受试者处于空腹状态,优选至少禁食12小时);
[0034]
优选地,其中当采用液相色谱质谱联用仪(lc
‑
ms)测定甘氨鹅脱氧胆酸和甘油三酯tag 56:4在干血片样本中的相对含量时,具体包括以下步骤:
[0035]
1)将干血片样本置于冷(甲基叔丁基醚:甲醇,体积比3:1)溶液(在该溶液中预先加入甘氨鹅脱氧胆酸的标定物质赤霉酸和甘油三酯tag 56:4的标定物质磷脂酰乙醇胺pe(17:0/17:0))中,涡旋混匀提取血液样品,获得第三样品提取液;
[0036]
2)向第三样品提取液中加入(甲醇:水,体积比3:1)溶液,涡旋并离心分层;
[0037]
3)分别按照上述步骤t3)至t7)获得干血片样本中甘氨鹅脱氧胆酸的相对含量m,以及按照上述步骤s3)至s6)获得干血片样本中甘油三酯tag 56:4的相对含量n。
[0038]
本发明另一方面提供一种甘氨鹅脱氧胆酸或/和甘油三酯tag 56:4作为判断干血片样本采集质量的质检指示物的应用,通过上述甘氨鹅脱氧胆酸或/和甘油三酯tag 56:4在干血片样本中的相对含量为监控指标来判断干血片样本的采集质量。
[0039]
本发明再一方面提供一种赤霉酸或/和磷脂酰乙醇胺pe(17:0/17:0)作为判断干血片样本采集质量的标定物质的应用,其中所述赤霉酸作为甘氨鹅脱氧胆酸的标定物质,所述磷脂酰乙醇胺pe(17:0/17:0)作为甘油三酯tag 56:4的标定物质,通过上述甘氨鹅脱氧胆酸相对赤霉酸在干血片样本中的相对含量m,或/和甘油三酯tag 56:4相对磷脂酰乙醇胺pe(17:0/17:0)在干血片样本中的相对含量n为监控指标来判断干血片样本的采集质量。
[0040]
在本发明又一方面提供一种干血片样本代谢组学检测结果的评价方法,其包括:
[0041]
对干血片样本中的多种代谢化合物进行检测得到干血片样本代谢组学检测结果,以及外加的作为代谢化合物中的甘氨鹅脱氧胆酸的标定物质的赤霉酸的检测结果,或/和作为代谢化合物中的甘油三酯tag 56:4的标定物质的磷脂酰乙醇胺pe(17:0/17:0)的检测结果;
[0042]
从所得检测结果中计算甘氨鹅脱氧胆酸的检测信号强度与赤霉酸的检测信号强度的比值a,或/和甘油三酯tag 56:4的检测信号强度与磷脂酰乙醇胺pe(17:0/17:0)的检
测信号强度的比值b;
[0043]
以该比值a或/和比值b是否满足某数值来评价干血片样本代谢组学检测结果是否可用。
[0044]
上述评价方法中,其中根据比值a的评价标准为:
[0045]
当所述比值a不小于由式(i)表示的x1时,该干血片样本代谢组学检测结果不可用;
[0046]
当所述比值a小于由式(i)表示的x1,且大于式(ii)表示的x2时,该干血片样本代谢组学检测结果存疑;
[0047]
当所述比值a不大于式(ii)表示的x2,进一步优选处于式(iii)表示的x3的范围内时,该干血片样本代谢组学检测结果可用;
[0048]
优选地,其中当采用液相色谱质谱联用仪(lc
‑
ms)对干血片样本中的多种代谢化合物和赤霉酸进行检测时,具体包括以下步骤:
[0049]
使用上述的第一样品提取液分别按照上述步骤t2)至t7)获得所述干血片样本中的水相中的各代谢化合物和外加的赤霉酸的lc
‑
ms检测数据,以及按照上述步骤s2)至s6)获得所述干血片样本中的有机相中的各代谢化合物的lc
‑
ms检测数据。
[0050]
上述评价方法中,其中根据比值b的评价标准为:
[0051]
当所述比值b不小于由式(iv)表示的y1时,该干血片样本代谢组学检测结果不可用;
[0052]
当所述比值b小于由式(iv)表示的y1,且大于式(v)表示的y2时,该干血片样本代谢组学检测结果存疑;
[0053]
当所述比值b不大于式(v)表示的y2,进一步优选处于式(vi)表示的y3的范围内时,该干血片样本代谢组学检测结果可用;
[0054]
优选地,其中当采用液相色谱质谱联用仪(lc
‑
ms)对干血片样本中的多种代谢化合物和磷脂酰乙醇胺pe(17:0/17:0)进行检测时,具体包括以下步骤:
[0055]
使用上述第二样品提取液分别按照上述步骤t2)至t7)获得所述干血片样本中的水相中的各代谢化合物的lc
‑
ms检测数据,以及按照上述步骤s2)至s6)获得所述干血片样本中的有机相中的各代谢化合物和外加的磷脂酰乙醇胺pe(17:0/17:0)的lc
‑
ms检测数据。
[0056]
上述评价方法中,其中根据比值a和比值b的评价标准为:
[0057]
当所述比值a不小于由式(i)表示的x1,和/或所述比值b不小于由式(iv)表示的y1时,该干血片样本代谢组学检测结果不可用;
[0058]
当所述比值a小于由式(i)表示的x1,且大于式(ii)表示的x2,和/或所述比值b小于由式(iv)表示的y1,且大于式(v)表示的y2时,该干血片样本代谢组学检测结果存疑;
[0059]
当所述比值a不大于式(ii)表示的x2,进一步优选处于式(iii)表示的x3的范围内,且所述比值b不大于式(v)表示的y2,进一步优选处于式(vi)表示的y3的范围内时,该干血片样本代谢组学检测结果可用;
[0060]
优选地,其中当采用液相色谱质谱联用仪(lc
‑
ms)对干血片样本中的多种代谢化合物,以及赤霉酸和磷脂酰乙醇胺pe(17:0/17:0)进行检测时,具体包括以下步骤:
[0061]
使用上述第三样品提取液分别按照上述步骤t2)至t7)获得所述干血片样本中的水相中的各代谢化合物和赤霉酸的lc
‑
ms检测数据,以及按照上述步骤s2)至s6)获得所述
干血片样本中的有机相中的各代谢化合物和磷脂酰乙醇胺pe(17:0/17:0)的lc
‑
ms检测数据。
[0062]
基于以上技术方案,本发明以甘氨鹅脱氧胆酸或/和甘油三酯tag 56:4(其中56:4表示甘油三酯的具体结构,即在甘油三酯中3条脂肪酸链共包含56个碳(c)原子,其中4个碳键是不饱和键)在干血片样本中的相对含量(其中甘氨鹅脱氧胆酸的相对含量为相对于同一样本中的赤霉酸,而甘油三酯tag 56:4的相对含量为相对于同一样本中的磷脂酰乙醇胺pe(17:0/17:0)(其中17:0/17:0表示该物质的结构,即pe(17:0/17:0)所含的2条脂肪酸碳链各含有17个碳(c)原子且均为饱和碳键))m或/和n作为质检指标,来判断干血片样本的采集质量是否符合要求(例如,用于采集干血片样本的受试者是否处于空腹状态)。本发明研究结果表明,当干血片样本中甘氨鹅脱氧胆酸的相对含量m小于式(i)表示的x1,优选不大于式(ii)表示的x2,进一步优选处于式(iii)表示的x3的范围内,和/或干血片样本中甘油三酯tag 56:4的相对含量n小于式(iv)表示的y1,优选不大于式(v)表示的y2,进一步优选处于式(vi)表示的y3的范围内时,该干血片样本的采集质量符合要求,即用于采集干血片样本的受试者在进行指尖血干血片采样时处于空腹状态(例如至少禁食12小时)。
[0063]
利用该应用,本发明提供了基于甘氨鹅脱氧胆酸和/或甘油三酯tag 56:4在代谢组学干血片样本中的检测信号强度分别与各自的标定物质在相同代谢组学干血片样本中的检测信号强度的比值的代谢组学干血片样本采集质量的监控方法和干血片样本代谢组学检测结果的评价方法,通过对采集后的干血片样本中的甘氨鹅脱氧胆酸和/或甘油三酯tag 56:4的相对含量进行检测,可以快速、准确地对代谢组学干血片样本的采集质量进行判断和监控,对代谢组学检测结果进行评价,保证干血片样本代谢组学检测结果的准确性和可靠性。
[0064]
本发明使用m或n作为质检指标,其值的变化与受试者是否处于空腹状态有直接关联,且通过实验数据表明,在是否空腹的情况下,其值范围有明显的差异,使其作为质检指标有足够的代表性和灵敏性。本发明可以单独使用m或n作为质检指标,即在干血片样本检测中根据实验室情况可以仅添加赤霉酸或仅添加磷脂酰乙醇胺pe(17:0/17:0)),依据m或n的数值来判断干血片样本是否符合采集质量要求,如此能以最简方式实现对干血片样本采集质量的监控,快速筛检出不合格样本,从而避免了对不合格样本进一步做大量生物代谢物检测的无谓劳动。当本发明的m和n结合使用时,可以充分考虑检测中甘氨鹅脱氧胆酸及其标定物质赤霉酸、甘油三酯tag 56:4及其标定物质磷脂酰乙醇胺pe(17:0/17:0))在干血片样本检测中各自的分布(前一组分布在水相,后一组分布在有机相)以及检测峰的位置和形状,两个指标均符合使得对干血片样本采集质量的监控更稳妥;而两个指标出现不一致时,将其应用到代谢组学检测结果的评价中,能更准确地分辨出结果是否值得怀疑,后续使用时应着重关注该类数据,为数据异常剔除、数据后期分析的提供支持。
附图说明
[0065]
图1为甘氨鹅脱氧胆酸在禁食组和非禁食组干血片样本中的提取离子流色谱图;
[0066]
图2为甘油三酯tag 56:4在禁食组和非禁食组干血片样本中的提取离子流色谱图;
[0067]
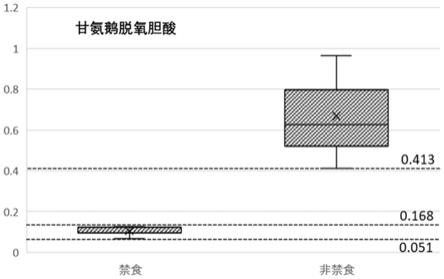
图3为甘氨鹅脱氧胆酸在禁食组和非禁食组干血片样本中的相对含量差异对比
图;
[0068]
图4为甘油三酯tag 56:4在禁食组和非禁食组干血片样本中的相对含量差异对比图。
具体实施方式
[0069]
本发明首先提供甘氨鹅脱氧胆酸和/或甘油三酯tag 56:4作为判断干血片样本采集质量的质检指示物的应用。具体的,可以液相色谱质谱仪(lc
‑
ms)和/或气相色谱质谱联用仪(gc
‑
ms)为检测手段,对采集的干血片样本中的甘氨鹅脱氧胆酸和/或甘油三酯的相对含量(即甘氨鹅脱氧胆酸和/或甘油三酯的检测信号强度分别与各自的标定物质(其中甘氨鹅脱氧胆酸对应的标定物质为赤霉酸(gibberellic acid,ga3),甘油三酯对应的标定物质为磷脂酰乙醇胺pe(17:0/17:0))的检测信号强度的比值)进行测定,根据其数值判断干血片样本的采集质量是否合格,还用于评价代谢组学检测结果是否可用。
[0070]
本发明另一方面基于干血片样本中的甘氨鹅脱氧胆酸和/或甘油三酯的相对含量,还提供一种干血片样本的采集质量的监控方法,为干血片样本的正确采集提供准确参考标准和判断依据。
[0071]
本发明另一方面还基于干血片样本中的甘氨鹅脱氧胆酸和/或甘油三酯的相对含量,提供一种干血片样本代谢组学检测结果的评价方法,可进行异常干血片样本(例如干血片样本采集前受试者饮食)的初步筛查,为数据异常剔除、数据后期分析的提供支持。
[0072]
以下结合具体实施方式和附图详细说明本发明的内容。
[0073]
在下文中,仅简单地描述了某些示例性实施例。正如本领域技术人员可认识到的那样,在不脱离本发明的精神或范围的情况下,可通过各种不同方式修改所描述的实施例。因此,附图和描述被认为本质上是示例性的而非限制性的。
[0074]
下述实施例中所用方法如无特别说明均为常规方法。
[0075]
实施例中描述到的各种生物材料的取得途径仅是提供一种试验获取的途径以达到具体公开的目的,不应成为对本发明生物材料来源的限制。事实上,所用到的生物材料的来源是广泛的,任何不违反法律和道德伦理能够获取的生物材料都可以按照实施例中的提示替换使用。
[0076]
实施例1:确定判断干血片样本采集质量的质检指示物
[0077]
1)利用3名人受试者(年龄范围为30
‑
33岁,已签署知情同意书)的指尖血制备干血片样本:分别在早晨空腹状态(禁食不短于12小时,即禁食组)和进食后2小时(即非禁食组)两种状态下采集指尖血制备干血片样本,每个受试者各采集2个样本(分别作为禁食组样本和非禁食组样本),共6个干血片样本;
[0078]
2)从每个干血片样本中取4个直径为3毫米的血片,作为4个重复,分别置于预冷(甲基叔丁基醚:甲醇,体积比3:1)溶液700μl(在该溶液中已预先加入浓度为0.45μg/ml的赤霉酸(标准品,以赤霉酸的水溶液形式加入)和浓度为1.0μg/ml的pe(17:0/17:0)(标准品,以pe(17:0/17:0)的二氯甲烷溶液形式加入))中,涡旋混匀提取各自的血液样品,获得各自的样品提取液;
[0079]
3)向样品提取液中加入(甲醇:水,体积比3:1)溶液350μl,超声、静置,涡旋并离心分层;
[0080]
4)样品分层后,取上层350μl至离心管中,为有机相;
[0081]
5)有机相干燥后,加入(乙腈:异丙醇,体积比3:1)200μl,并在室温下孵化15分钟;
[0082]
6)孵化后,将离心管涡旋混匀,超声辅助处理5分钟,再将离心管在室温下离心5分钟(12000rpm);
[0083]
7)经步骤6)的离心后,从离心管中取180μl上清液至2ml玻璃进样小瓶中,为有机相物质,上机(lc
‑
ms)检测(上机检测前检测pe(17:0/17:0)在该有机相物质中的终浓度为2.33μg/ml),在步骤13)中详述;
[0084]
8)取步骤3)中离心分层后的400μl下层水相至离心管中,并向其中加入冰甲醇1100μl,沉淀蛋白质;
[0085]
9)离心管中蛋白质沉淀后,将离心管离心,取上清液1000μl转移至新离心管中,并干燥过夜;
[0086]
10)向干燥后的离心管中加入200μl水,并在室温下孵化15分钟;
[0087]
11)孵化后,将离心管涡旋混匀,超声辅助处理5分钟,再将离心管在室温下离心5分钟(12000rpm);
[0088]
12)经步骤11)的离心后,从离心管中取180μl上清液至2ml玻璃进样小瓶中,为水相物质,上机(lc
‑
ms)检测(上机检测前检测赤霉酸在该水相物质中的终浓度为0.84μg/ml),在步骤13)中详述;
[0089]
13)样品上机检测:使用液相色谱
‑
质谱仪(lc
‑
ms,acquity uplc i
‑
class液相色谱系统(沃特世)和q
‑
exactive质谱系统(赛默飞世尔科技))采集数据信息,获得各组检测样品(有机相和水相)中各化合物的lc
‑
ms检测数据(包括质谱数据和液相色谱数据),其中质谱仪由电喷雾电离源(esi)和静电场轨道阱(orbitrap)质量分析仪组成。
[0090]
具体为:取步骤12)获得的水相物质3μl溶液注入经acquity uplc hss t3(2.1
×
100mm,1.8μm)色谱柱分离,取步骤7)获得的有机相物质2μl溶液注入经acquity uplc hss beh c8(2.1
×
100mm,1.7μm)色谱柱分离。下表1和表2列出了液相色谱的洗脱梯度。
[0091]
表1:hss t3色谱柱洗脱梯度
[0092] 时间(min)流速(ml/min)%a%bcurve1initial0.4991initial210.499163110.4604064130.4307065150.419966180.419967190.499168210.49916
[0093]
注:表1中流动相a为含0.1%甲酸水溶液,流动相b为含0.1%甲酸的乙腈溶液,均为色谱纯
[0094]
表2:hss beh c8色谱柱洗脱梯度
[0095] 时间(min)流速(ml/min)%a%bcurve1initial0.44555initial
210.445556340.4257564120.4118965150.401006619.50.445556719.510.4455568240.445556
[0096]
注:表2中流动相a为含0.1%乙酸水溶液,流动相b为含0.1%乙酸和1%乙酸铵的乙腈
‑
正己烷(体积比7:3)溶液,均为色谱纯
[0097]
14)数据处理:将步骤13)获得的各组检测样品的lc
‑
ms数据转化为h5格式后使用rstudio软件(商用软件)进行分析,按照说明书操作完成,其中数据经多次筛选,包括去除同位素峰、源内碎裂的离子和同一物质的不同加合方式以及重复的化合物等。最终导出csv格式数据,再由代谢组学分析网站metaboanalyst 5.0(商用网站)分析,注解并计算出各测得的化合物(代谢物)的检测信号强度。
[0098]
15)经处理后的数据用t
‑
test方法分析独立样本间的重复性
[0099]
该实施例中经r studio软件和代谢组学数据库metaboanalyst 5.0注解并计算出了各化合物(代谢物)的检测信号强度(检测信号强度以对应化合物的提取离子流色谱图的峰面积/峰高数值表示)。对各化合物在禁食组和非禁食组样本中的检测信号强度进行比对,在非禁食组样本中的检测信号强度高于禁食组样本中的检测信号强度的化合物(异常代谢物)中,筛选出两种代谢物甘氨鹅脱氧胆酸和甘油三酯tag 56:4,其在非禁食组样本中的检测信号强度显著高于禁食组样本中的检测信号强度,如图1和图2(纵坐标表示色谱峰相对强度,横坐标表示色谱峰保留时间范围,实线和虚线分别用于标注非禁食组和禁食组色谱峰高度)所示,分别示出了甘氨鹅脱氧胆酸和甘油三酯tag 56:4在两组样本(禁食组和非禁食组)中的提取离子流色谱图。经t
‑
test分析具有统计学意义(p分别为0.043和0.0053),而检测的其他异常代谢物经t
‑
test分析,在检测信号强度变化上均无统计学意义,因此本发明确定干血片样本中的代谢物甘氨鹅脱氧胆酸和甘油三酯tag 56:4可以作为判断干血片样本的采集质量是否符合要求的质检指示物。
[0100]
为了量化干血片样本的采集质量判断标准,本发明人以干血片样本中的甘氨鹅脱氧胆酸和/或甘油三酯tag 56:4的检测信号强度分别与各自的标定物质的检测信号强度的比值作为质检指标。具体地,在前述步骤2)中外加赤霉酸或/和磷脂酰乙醇胺pe(17:0/17:0),以水相物质中甘氨鹅脱氧胆酸的检测信号强度与赤霉酸的检测信号强度的比值a,和/或有机相物质中甘油三酯tag 56:4的检测信号强度与磷脂酰乙醇胺pe(17:0/17:0)的检测信号强度的比值b作为质检指标,优选两者同时作为质检指标。
[0101]
具体到本实施例,用作甘氨鹅脱氧胆酸的标定物质的赤霉酸在上机检测的水相物质中的上机终浓度(即上机检测时的浓度)为0.84μg/ml,用作甘油三酯tag 56:4的标定物质的磷脂酰乙醇胺pe(17:0/17:0)在上机检测的有机相物质中的终浓度为2.33μg/ml。如图3和图4所示,分别示出了甘氨鹅脱氧胆酸和甘油三酯tag 56:4在禁食组和非禁食组干血片样本中的相对含量差异对比,可见相对于禁食组样本,甘氨鹅脱氧胆酸和甘油三酯tag 56:4在非禁食组样本的相对含量更高。依据图3所示,甘氨鹅脱氧胆酸的相对含量在非禁食组
样本中不小于0.413,而在禁食组样本中,甘氨鹅脱氧胆酸的相对含量小于0.413,更准确为未超过0.168,位于0.051
‑
0.168之间;依据图4所示,甘油三酯tag56:4的相对含量在非禁食组样本中不小于0.0295,而在禁食组样本中小于0.0295,更准确为不大于0.0253,位于0.0129
‑
0.0253之间。因此确定质检指标的评判标准为:当测定的干血片样本中甘氨鹅脱氧胆酸的相对含量m小于0.413,优选不大于0.168,进一步优选为0.051
‑
0.168时,或者测定的干血片样本中甘油三酯tag56:4的相对含量n小于0.0295,优选不大于0.0253,进一步优选为0.0129
‑
0.0253时,或者测定的干血片样本中甘氨鹅脱氧胆酸和甘油三酯tag56:4的相对含量m和n均满足上述要求时,干血片样本的采集质量符合要求,本实施例中的采集质量要求即为用于采集干血片样本的受试者处于空腹状态(例如至少禁食12小时)。
[0102]
在实际检测中,外加至血液样品提取溶液中作为甘氨鹅脱氧胆酸的标定物质的赤霉酸在上机检测时的浓度以及作为甘油三酯tag56:4的标定物质的磷脂酰乙醇胺pe(17:0/17:0)在上机检测时的浓度可不局限于前述使用的检测浓度,相应地,检测到的赤霉酸的信号强度和磷脂酰乙醇胺pe(17:0/17:0)的信号强度也会随之发生变化,进而会导致计算的甘氨鹅脱氧胆酸的相对含量和甘油三酯tag56:4的相对含量也发生变化。由于赤霉酸和磷脂酰乙醇胺pe(17:0/17:0)的检测信号强度实际上表示的也是检测样品中两者的浓度,因此检测信号强度的变化可以直接表明检测浓度的变化,并且呈线性相关关系,例如,假设甘氨鹅脱氧胆酸的检测信号强度表示为p,赤霉酸的原始检测浓度表示为ra(单位是μg/ml),检测的信号强度表示为p0,变化后赤霉酸的检测浓度表示为r1(单位是μg/ml),相应检测的信号强度表示为p1,则存在以下关系:r1/ra=p1/p0,则赤霉酸的检测浓度变化后计算的甘氨鹅脱氧胆酸的相对含量m=p/p1=(p/p0)
·
(ra/r1)。这种关系也同样适用于甘油三酯tag56:4和磷脂酰乙醇胺pe(17:0/17:0)。因此:
[0103]
对于赤霉酸,当其原始检测浓度ra为本实施例的0.84μg/ml时,设禁食组干血片样本中计算的p/p0的值为k’(依据前述数据,设定k’的最大值为k1=0.413,优选值为k2=0.168,进一步优选为k3=0.051~0.168),那么在禁食组干血片样本中的赤霉酸的检测浓度变为r1(即实际检测时的浓度)时,计算的甘氨鹅脱氧胆酸的相对含量m如以下式(i
‑
i)表示:
[0104]
m=p/p1=(p/p0)
·
(ra/r1)=k’·
(ra/r1)(i
‑
i)
[0105]
当式(i
‑
i)中k’分别为k1、k2和k3时,对应的甘氨鹅脱氧胆酸的相对含量m分别表示为:x1=k1
·
(0.84/r1),x2=k2
·
(0.84/r1),x3=k3
·
(0.84/r1),其中r1为实际上机检测时水相物质样品中的赤霉酸的检测浓度(单位为μg/ml),k1=0.413,k2=0.168,k3=0.051~0.168。
[0106]
同样地,对于磷脂酰乙醇胺pe(17:0/17:0),当磷脂酰乙醇胺pe(17:0/17:0)的检测浓度由原始检测浓度rb(2.33μg/ml)变化为r2(即实际检测时的浓度)时,计算的甘油三酯tag56:4的相对含量n如以下式(i
‑
ii)表示:
[0107]
n=l’·
(rb/r2)(i
‑
ii)
[0108]
式(i
‑
ii)中,l’表示本实施例中在磷脂酰乙醇胺pe(17:0/17:0)的检测浓度为2.33μg/ml时计算的禁食组上机检测时有机相物质样品中甘油三酯tag56:4的检测信号强度与磷脂酰乙醇胺pe(17:0/17:0)的检测信号强度的比值,其最大值l1=0.0295,优选值为l2=0.0253,进一步优选值为l3=0.0129~0.0253。当式(i
‑
ii)中l’分别为l1、l2和l3时,
对应的甘油三酯tag 56:4的相对含量n分别表示为:y1=l1
·
(2.33/r2),y2=l2
·
(2.33/r2),y3=l3
·
(2.33/r2),其中r2为实际上机检测时有机相物质样品中的磷脂酰乙醇胺pe(17:0/17:0)的检测浓度(单位为μg/ml)。
[0109]
综上,以甘氨鹅脱氧胆酸和/或甘油三酯tag 56:4在干血片样本中的相对含量作为质检指标判断干血片样本的采集质量是否符合要求,依据外加标定物质(赤霉酸和磷脂酰乙醇胺pe(17:0/17:0))的种类和数量,选用以下判断标准(1)至(3)中的任一种:
[0110]
(1)仅加入赤霉酸时,当干血片样本中的甘氨鹅脱氧胆酸的相对含量小于由x1表示的值,优选不大于由x2表示的值,进一步优选处于由x3表示的范围内时,该干血片样本的采集质量符合要求(本例中采集质量符合要求是指用于采集干血片样本的受试者处于空腹状态,例如至少禁食12小时。下同);
[0111]
(2)仅加入磷脂酰乙醇胺pe(17:0/17:0)时,当干血片样本中的甘油三酯tag 56:4的相对含量小于由y1表示的值,优选不大于由y2表示的值,进一步优选处于由y3表示的范围内时,该干血片样本的采集质量符合要求;
[0112]
(3)同时加入赤霉酸和磷脂酰乙醇胺pe(17:0/17:0)时,当干血片样本中的甘氨鹅脱氧胆酸的相对含量小于由x1表示的值(优选不大于由x2表示的值,进一步优选处于由x3表示的范围内),且干血片样本中的甘油三酯tag 56:4的相对含量小于由y1表示的值(优选不大于由y2表示的值,进一步优选处于由y3表示的范围内时),该干血片样本的采集质量符合要求。
[0113]
实施例2:甘氨鹅脱氧胆酸作为判断干血片样本采集质量的质控指示物的验证
[0114]
1)以1名受试者不同时间三次采样的指尖血干血片样本作为检测样本,共3个干血片样本,并记录三次干血片样本采集时的信息,列于下表3中;
[0115]
2)从每个干血片样本中取4个直径为3毫米的血片,作为4个重复,分别置于预冷(甲基叔丁基醚:甲醇,体积比3:1)溶液700μl(在该溶液中已经预先加入赤霉酸)中,涡旋混匀提取各自的血液样品,获得各自的样品提取液;
[0116]
3)向样品提取液中加入加入(甲醇:水,体积比3:1)溶液,去除上层有机相后,取400μl下层水相至离心管中,并向其中加入冰甲醇1100μl,沉淀蛋白质;
[0117]
4)蛋白质沉淀后,将离心管离心,取上清液转移至新离心管中,并干燥过夜;
[0118]
5)向干燥后的离心管中加入200μl水,并在室温下孵化15分钟;
[0119]
6)孵化后,将离心管涡旋混匀,超声辅助处理5分钟,再将离心管在室温下离心5分钟(12000rpm);
[0120]
7)经步骤6)的离心后,从离心管中取180μl上清液至2ml玻璃进样小瓶中,为水相物质,参照实施例1,上机(lc
‑
ms)检测,获得甘氨鹅脱氧胆酸及其标定物质赤霉酸的质谱数据;
[0121]
8)按照实施例1的数据处理方法从质谱数据中获得各干血片样本中甘氨鹅脱氧胆酸的检测信号强度信息(提取离子流色谱图的峰面积表示),及其标定物质赤霉酸的检测信号强度信息,并计算获得甘氨鹅脱氧胆酸的相对含量。
[0122]
检测结果如下表3所示,可见在不同时间点从同一受试者采集的1和3号干血片样本中甘氨鹅脱氧胆酸的相对含量均超过0.413,从甘氨鹅脱氧胆酸的相对含量可判断该受试者处于非空腹状态,即在采集样本前饮食,这与采集干血片样本时记录的受试者信息一
致。检测的2号干血片样本中甘氨鹅脱氧胆酸的相对含量小于0.413,从甘氨鹅脱氧胆酸的相对含量可判断该受试者处于空腹状态,即在采集样本前未饮食,这与采集干血片样本时记录的受试者信息一致。该结果验证了干血片样本中的代谢物甘氨鹅脱氧胆酸确实可以作为判断干血片样本的采集质量的质检指示物,并可以通过检测干血片样本中甘氨鹅脱氧胆酸的相对含量来监控干血片样本的采集质量。
[0123]
表3:不同干血片样本检测结果
[0124][0125]
实施例3:甘油三酯tag 56:4作为判断干血片样本采集质量的质控指示物的验证
[0126]
1)以1名受试者不同时间三次采样的指尖血干血片样本作为检测样本(该检测样本与实施例2中使用的检测样本一致),共3个干血片样本,并记录三次干血片样本采集时的信息,列于下表4中;
[0127]
2)从每个干血片样本中取4个直径为3毫米的血片,作为4个重复,分别置于预冷(甲基叔丁基醚:甲醇,体积比3:1)溶液700μl(在该溶液中已经预先加入pe(17:0/17:0))中,涡旋混匀提取各自的血液样品,获得各自的样品提取液;
[0128]
3)向样品提取液中加入(甲醇:水,体积比3:1)溶液350μl,超声、静置,涡旋并离心分层;
[0129]
4)样品分层后,取上层有机相200μl至离心管中,为有机相物质;
[0130]
5)有机相干燥后,加入(乙腈:异丙醇,体积比3:1)200μl,并在室温下孵化15分钟;
[0131]
6)孵化后,将离心管涡旋混匀,超声辅助处理5分钟,再将离心管在室温下离心5分钟(12000rpm);
[0132]
7)经步骤6)的离心后,从离心管中取180μl上清液至2ml玻璃进样小瓶中,为有机相物质,参照实施例1,上机(lc
‑
ms)检测,获得甘油三酯tag 56:4及其标定物质pe(17:0/17:0)的质谱数据;
[0133]
8)按照实施例1的数据处理方法从质谱数据中获得各干血片样本中甘油三酯tag 56:4的检测信号强度信息(提取离子流色谱图的峰面积表示),及其标定物质pe(17:0/17:0)的检测信号强度信息,并计算获得甘油三酯tag 56:4的相对含量。
[0134]
检测结果如下表4所示,可见在不同时间点从同一受试者采集的1和3号干血片样本中甘油三酯tag 56:4的相对含量均超过0.0295,从甘油三酯tag 56:4的相对含量可判断该受试者处于非空腹状态,即在采集样本前饮食,这与采集干血片样本时记录的受试者信息一致。检测的2号干血片样本中甘油三酯tag 56:4的相对含量小于0.0295,从甘油三酯tag 56:4的相对含量可判断该受试者处于空腹状态,即在采集样本前未饮食,这与采集干血片样本时记录的受试者信息一致。该结果验证了干血片样本中的代谢物甘油三酯tag 56:4确实可以作为判断干血片样本的采集质量的质检指示物,并可以通过检测干血片样本中甘油三酯tag 56:4的相对含量来监控干血片样本的采集质量。
[0135]
表4:不同干血片样本检测结果
[0136][0137]
实施例4:干血片样本代谢组学检测结果的评价
[0138]
该实施例利用的是实施例1的代谢物化合物的检测方法(即检测多种代谢物数据的方法步骤,得到代谢组学检测结果),使用采自某医院的一批干血片样本按实施例1的方法制备检测样品,检测结果中,以甘氨鹅脱氧胆酸在干血片样本中的相对含量m不大于0.168,和甘油三酯tag 56:4在干血片样本中的相对含量n不大于0.0253作为干血片样本的代谢组学检测结果是否可用的标准,进而将达标的干血片样本获得的化合物的检测数据判断为可用的代谢组学检测结果以做进一步数据分析,将不达标的干血片样本代谢组学检测结果判断为存疑(当0.168<m<0.413,和/或0.0253<n<0.0295时)或完全不可用(当m≥0.413,和/或n≥0.0295时),在做进一步数据分析时着重关注此类数据。
[0139]
下表5示出了干血片样本的代谢组学检测结果的评价结果,其中样本1、4、5中甘氨鹅脱氧胆酸和甘油三酯tag 56:4在干血片样本中的相对含量(m和n)均未超标,从其对应干血片样本得到的化合物检测数据可作为代谢组学检测结果数据使用;样本2的m和n数值均超标,且m>0.413,n>0.0295,从样本2得到的化合物检测数据不能作为代谢组学检测结果数据使用;样本3的m值超标,而n值未超标,且0.168<m<0.413,样本6的m值未超标,而n值超标,且0.0253<n<0.0295,从样本3和6得到的化合物检测数据是否可作为代谢组学检测结果数据使用存疑,但鉴于样本3和样本6已完成检测,可结合其他指标判断从其得到的代谢组学检测结果数据是否可用,或者对两者的样本重新进行检测。可见,可以通过检测甘氨鹅脱氧胆酸和/或甘油三酯tag 56:4在干血片样本中的相对含量来对异常干血片样本(例如用于干血片样本采集的受试者在采集前饮食)的初步筛查,为数据异常剔除、数据后期分析的提供支持。
[0140]
表5:干血片样本代谢组学检测结果评价
[0141][0142]
最后应说明的是:以上所述仅为本发明的优选实施例,并不用于限制本发明,尽管参照前述实施例对本发明进行了详细的说明,对于本领域的技术人员来说,其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1