一种快速测定食品添加剂中多糖及糖醇的方法与流程
1.本发明涉及食品添加剂中糖及糖醇的检测,具体为一种快速测定食品添加剂中多糖及糖醇的方法。
背景技术:
2.食品添加剂随着我国经济的飞速增长和人们生活水平的不断提高,我们对食品的质量也提出了更高的要求。食品安全问题频发使得食品安全一度成为人们关注的热点。对食品进行检验检测是保障食品安全的重要手段,也是提高食品质量的重要途经。其中糖类化合物是人们维持生命活动所需能量的主要来源。糖醇是糖类的醛基或酮基被还原成羟基而形成的物质,主要是由对应的糖反应生成的甜味剂,不会引起血糖升高,因此具有预防糖尿病和肥胖病的作用。醇类是分子中含有跟烃基或苯环侧链上的碳结合的烃基的化合物,许多醇类对人体健康有益,但有些醇类具有一定的毒性。糖类、糖醇类组分的检测是分析化学领域的难点,也是分析测试领域的研究热点,目前我国食品安全国家标准《预包装食品营养标签通则》中规定,必须在食品标签标注食品的糖含量。
3.甜味剂中糖及糖醇的含量直接影响甜味剂的品质。当前糖类及糖醇的主要检测方法有气相色谱法、液相色谱法、酶电极法、离子色谱法等。气相色谱法,具有快速、灵敏的优点,但前处理步骤复杂,定量不够准确。液相色谱法,具有准确、选择性好的特点,但灵敏度低。酶电极法,一般仅对一种糖类进行检测,专一性好,但是检测效率不高。离子色谱法具有简便、快速、灵敏、准确等优点,是一种新型多组分同时检测的理想方法。
4.目前,人们对于甜味剂中糖及糖醇同时检测的方法虽然有研究,但在目前资料库中所能检索到的仅仅是对某一类组分(如单纯的糖类或醇类)或者同时检测的组分数量较少,不能满足日益增长的检测需求,因此,研究并建立一种适用性强、选择性好、灵敏度高的多种糖及糖醇同时检测的方法,具有重要的现实意义和应用价值。
技术实现要素:
5.本发明提出了一种快速测定食品添加剂中多糖及糖醇的方法,采用积分脉冲安培
ꢀ‑
离子色谱法,优化前处理检测方法,通过对组分分离的影响因素的研究,建立了一次性同时检测甜味剂中7种糖类及糖醇的方法,该方法快速、简便、灵敏度高、稳定性好,实现了快速分析和绿色分析,解决了糖及糖醇多组分同时分析的技术问题,适合用于检测甜味剂中糖及糖醇的测定。
6.为达到上述目的,本发明采用以下技术方案为:
7.一种食品添加剂中多糖及糖醇的检测方法,所述食品添加剂为甜味剂,其检测步骤如下;
8.步骤一、混合标准溶液的配置:
9.将山梨糖醇、海藻糖、麦芽糖醇、葡萄糖、蔗糖、甘露糖醇、果糖的标准溶液按需要配置混合标准储备液;
10.步骤二、待测样品前处理:
11.取甜味剂待检样品0.1000g于100ml烧杯中,加入超纯水约50ml,混匀静置10min,采用0.10mol/l氢氧化钠溶液调节稀释液ph值至7.0~8.5,将其全部转移至500ml 容量瓶中,采用超纯水定容至刻度,摇匀、静置15min,取10.0ml溶液,先过0.22um 滤膜,收集后段清液,待检测。
12.步骤三、离子色谱条件及多级梯度淋洗条件:
13.分析柱:carbopacpa20(3
×
150mm);
14.保护柱:carbopacpa20(3
×
30mm);
15.工作电极:gold;
16.参比电极:agcl电极
17.流动相:a:200mmol/l naoh溶液,b:超纯水;
18.步骤四、校准曲线绘制:
19.将步骤一中配置的混合标准溶液按照步骤三给出的色谱分析条件与多级梯度淋洗条件使用离子色谱仪进行检测,以待测组分峰面积为纵坐标,来绘制校准曲线,外标法定量;
20.步骤五、样品溶液的检测:
21.将步骤二中所得清液按照步骤三给出的色谱分析条件与多级梯度淋洗条件使用离子色谱仪进行检测,并计算结果;
22.步骤六、结果计算:
23.通过步骤四混合标准溶液所测得的结果来校正步骤五所测得计算结果,从而计算所测所述食品添加剂为甜味剂,中各组分含量。
24.优选地,所述上述溶液均使用电阻率为18.2mω
·
cm的超纯水配制。
25.优选地,所述步骤二中,称取甜味剂0.1000g于100ml烧杯中,加入超纯水50ml,混匀静置10min得到稀释液,将其全部转移至500ml容量瓶中,采用超纯水定容至刻度,摇匀、静置15min,取10.0ml溶液,先过0.22um滤膜,收集清液,待检测。
26.进一步优选地,所述步骤二中,稀释液采用0.10mol/l氢氧化钠溶液调节稀释液ph值至7~8.5。
27.优选地,所述步骤三中,淋洗的为多级梯度淋洗,多级梯度淋洗程序为:(-40.0)
ꢀ‑
(-30.05)min时,淋洗液naoh浓度为200.0mmol/l,(-30.05)-(8.00)min 时,淋洗液naoh浓度为50.0mmol/l。
28.表1离子色谱淋洗条件
29.时间/mina:naoh溶液(200mmol/l)b:超纯水-40.00100%0-30.05100%0-30.0025%75%0.0025%75%8.0025%75%
30.优选地,所述步骤三中,流速:0.50ml/min。
31.优选地,所述步骤三中,柱温:30℃。
32.本发明具有以下有益效果:
33.1、在实际生产中,很多甜味剂中糖及糖醇化学分子式及性质相似,由于检测方法、检测内容有限,很多糖及糖醇难以快速准确的检测处理,本发明一次性同时快速测定甜味剂中7中糖及糖醇,解决了目前采用多种标准、多种仪器、多种前处理方法进行多种组分测定时效率低的技术难题,大幅提高了检测效率,降低了检测成本。
34.2、为了同时分离检测甜味剂种7种糖及糖醇组分,提高组分的整体分离度,通过实验分析对比,本发明选择在样品前处理时将样品溶解且将溶液ph调节至 7.0-8.5,前10min内采用高浓度淋洗的方法,用200mmol/l的氢氧化钠溶液进行色谱柱的强力冲洗,去除影响待测组分的干扰物,可以大幅度提高检测的准确度。再用50mmol/l的氢氧化钠溶液冲洗系统30min,以保证系统的稳定性。
35.3、本发明通过多因素多基质考察分析,先后研究分析了多级梯度淋洗条件、初始淋洗浓度、淋洗液流速、色谱柱温度,最大程度地提高了多种组分同时测定时方法的准确性和适用性。
36.4、本发明研究了色谱柱温度对检测的重要影响,色谱柱温度的细小变化,同样会导致组分重叠。在30℃柱温时,恰好能满足7组分的定性定量要求。
37.5、本发明检测方法操作简便快速、检测灵敏度高,经过简单前处理操作,即可上机检测。
38.6、在本发明检测方法中并没有使用或产生对人类健康、生态环境有害的溶剂、试剂、副产物,符合绿色分析的理念。
附图说明
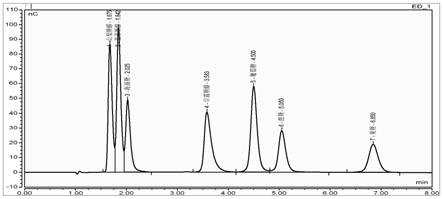
39.图1为7种糖、糖醇混合标准溶液的离子色谱图。
40.图2为不同初始淋洗液浓度下混合标准溶液的离子色谱图。
41.图3为不同柱温下混合标准溶液的离子色谱图。
42.图4为3种复配甜味剂的离子色谱图。
43.附图中各编号对应的物质:1.山梨糖醇;2.麦芽糖醇;3.海藻糖;4.甘露糖醇;5.葡萄糖;6.蔗糖;7.果糖。
44.图5为未预冲洗的7种糖、糖醇混合标准溶液的离子色谱图。
具体实施方式
45.下面结合实施例来进一步说明本发明,但本发明要求保护的范围并不局限于实施例表述的范围。
46.实施例1
47.一种甜味剂中7中糖及糖醇同时检测的方法,包括以下步骤:
48.1.仪器和试剂
49.ics6000+离子色谱系统配有电化学检测器和自动进样器(美国thermo scientific公司);milli-q超纯水仪(美国millipore公司);电子天平(梅特勒公司ml802/02);实验用水:超纯水(电阻率18.2mω
·
cm);糖类及糖醇类标准品或标准试剂(纯度>98%);氢氧化钠溶液(50%w/w,fisher chemical);盐酸(优级纯);
50.2.离子色谱条件
51.carbopacpa20(3
×
150mm)分析柱,carbopacpa20(3
×
30mm)保护柱;工作电极: gold(au);参比电极:agcl电极;流动相:naoh淋洗液(氮气保护);流速:0.50ml/min;柱温:30℃;进样量:25ul。初始淋洗液浓度:50mmol/l naoh溶液。
52.3.多级梯度淋洗条件:
53.多级梯度淋洗程序为:(-40.0)-(-30.05)min时,淋洗液naoh浓度为 200.0mmol/l,(-30.05)-(8.00)min时,淋洗液naoh浓度为50.0mmol/l;
54.4.混合标准溶液的配置:
55.将山梨糖醇、海藻糖、麦芽糖醇、葡萄糖、蔗糖、甘露糖醇、果糖的标准溶液或标准品按需要配置为一定浓度的混合标准溶液,在配置混合标准溶液的过程中,调节溶液酸碱性配成ph值至7.0的混合标准溶液。
56.5.待测样品前处理:
57.取复配甜味剂样品0.1000g于100ml烧杯中,加入超纯水约50ml,混匀静置 10min,采用0.10mol/l氢氧化钠溶液调节稀释液ph值至7.0,将其全部转移至500ml 容量瓶中,采用超纯水定容至刻度,摇匀、静置15min,取10.0ml溶液,先过0.22um 滤膜,收集后段清液,待检测。
58.按照上述实验分析的条件,对混合标准溶液的7种糖及糖醇进行检测,其检测结果如图1所示。
59.实施例2:流速对检测的影响
60.按照实施例1中的实验分析的条件,在其他条件不变的情况下先后测试淋洗液的流速为0.30ml/min、0.40ml/min、0.50ml/min、0.60ml/min流速条件下混合标准溶液的组分分离情况,其淋洗液流速与系统压力的关系如表2所示。
61.表2淋洗液流速与系统压力的关系
62.流速0.30ml/min0.40ml/min0.50ml/min0.60ml/min系统压力1678psi2248psi2739psi3125psi
63.从表2可以得出淋洗液流速在0.30ml/min时,系统压力为1678psi,因为流速较低,压力较小,峰宽增大,峰灵敏度下降,整体分离度不高。0.40ml/min流速时,系统压力达到2248psi,虽然组分灵敏度有所提高,但是个别组分间的分离度已不理想。0.60ml/min流速时,系统压力达到3125psi,系统压力较大,超过色谱柱推荐压力上限3000psi,组分的整体分析时间缩短,但是组分的整体分离度降低,而且压力较大会在一定程度上影响色谱柱的使用寿命。0.50ml/min流速时初始压力2739psi,压力大小适中,组分灵敏度和分离度均能满足检测要求。因此,从系统稳定性、分离度、灵敏度因素考虑,本发明选择在0.5ml/min流速下进行实验。
64.实施例3:多级梯度淋洗条件对检测的影响
65.按照实施例1中的实验分析的条件,在其他条件不变的情况下先后测试初始淋洗液浓度分别在10、20、50、100、200mmol/l的条件下混合标准溶液组分分离情况,由于初始浓度对组分1、2、3这三种组分的分离度影响很小,这里重点讨论初始浓度对后4种组分的影响,其混合标准溶液的组分分离情况如图2所示。
66.从图2种可以看出,初始淋洗浓度分别为100、200mmol/l时,组分2海藻糖与组分3
麦芽糖醇、组分4甘露糖醇与组分5葡萄糖均未实现分离;初始淋洗浓度越低,这7种组分的整体分离度和灵敏度均比较理想,但是考虑到峰型与时间成本。因此,本发明选择初始淋洗浓度50mmol/l进行实验检测。
67.实施例4:色谱柱温对检测的影响
68.按照实施例1中实验分析条件,在其它条件不变的情况下先后测试在25℃、 27.5℃、30℃、32.5℃、35℃色谱柱温条件下,7种糖类及糖醇的分离效果,其检测结果如图3所示。
69.从图3中可以看出,25℃和27.5℃温度条件下,色谱柱温较低,多数组分的分离效果良好,但整体出峰时间推迟,组分6蔗糖和组分7果糖还出现了轻微的拖尾情况,不利于定量的准确性计算。当色谱柱温为32.5℃和35℃时,离子交换速率提高,柱效得到提高,缩短了分析时间,但组分2麦芽糖醇和组分3海藻糖,出峰时间非常相近,分离效果不理想,无法确保定量准确性。在30℃柱温时,分析速率适中,分离度良好,7种组分的总体分离效果好,由此可见,温度对7种组分同时检测有显著的影响,从提高方法的分离度、灵敏度、选择性角度考虑,本发明选取在30℃柱温下进行实验分析。
70.实施例5:线性范围与检出限
71.配置不同浓度的混合标准溶液,使用实施例1中色谱条件进行校准曲线拟合。通过色谱峰信噪比来计算待测组分的检出限(s/n=3),在0.10mg/l~20.0mg/l浓度范围内,进行了8个浓度水平(0.10、0.20、0.50、1.0、2.0、5.0、10.0、20.0mg/l) 混合标准溶液的检测和线性拟合,其结果如表3所示。
72.表3检测组分的线性范围、线性方程、相关系数及检出限(s/n=3)
[0073][0074]
y:峰面积(nc
·
min),x:质量浓度(mg/l)
[0075]
从表3可以看出,7种组分线性相关系数均大于0.999,说明在该实验条件下,组分同时线性良好。7种组分检测限在0.0059~0.2059mg/l之间。
[0076]
实施例6:回收率与精密度
[0077]
分别选取3种混匀样品,依次向3个样品中添加浓度水平分别为0.50mg/l、 1.00mg/l、5.00mg/l的混合标准溶液,每个浓度水平进行6次平行测定实验,来验证不同甜味剂基质检测方法的回收率和精密度,根据基质浓度、添加浓度和添加后检测浓度计算回收率。表4列出三种浓度水平、六次检测的平均回收率和rsd数据。
[0078]
表4检测组分的回收率及精密度(rsd)(n=6)
[0079][0080]
从表4中可以看出,7种糖及糖醇回收率都在90%~110%之间,所有回收率数据均满足食品理化检验技术要求(检测含量小于0.10mg/l,回收率应在60%~120%),这充分说明7种糖及糖醇回收率良好。三浓度水平下,7种组分检测rsd在1.03%~ 4.85%范围内。从总体上来看,三种基质、六次平行检测的回收率数据结果,符合食品理化检测要求,说明该检测方法准确性高、精密度好。
[0081]
实施例7:实际样品的检测
[0082]
抽取3种复配甜味剂(配方a、配方b、配方c),按照实施例1种离子色谱条件和前处理步骤,进行了实际样品种7种糖类及糖醇含量的检测分析,表5是检测组分数据结果,图4是实际样品检测的离子色谱图。
[0083]
表5甜味剂中检测结果(mg/l)
[0084]
序号组分配方a配方b配方c1山梨糖醇8.90786.37874.94262海藻糖8.53217.33225.61533麦芽糖醇7.77068.20638.89484葡萄糖7.58879.76718.43725蔗糖0.38349.92469.22476甘露糖醇6.95267.27237.85597果糖8.04609.76197.2114
[0085]
从3种甜味剂谱图对比来看,7种甜味剂中共检测7种组分,甜味剂中含有的主要糖类是葡萄糖、海藻糖、蔗糖、果糖,糖醇主要是山梨糖醇、麦芽糖醇、甘露糖醇;配方a中含有大量磷酸盐和少量碳酸钠,溶液呈弱碱性;配方b中含有大量的氯化钠、碳酸氢钠和磷酸盐,溶液呈中性;配方c含有大量柠檬酸钠和磷酸盐,溶液呈酸性,但是对于测定结果的准确性并没有影响,说明该方法完全满足测定甜味剂这种复杂基体的中糖及糖醇的检测。
[0086]
实施例8:甜味剂待检样品预处理中预冲洗对检测的影响
[0087]
按照实施例1中实验分析条件,在其它条件不变的情况下多级梯度淋洗条件:
[0088]
多级梯度淋洗程序为:(-30.05)-(8.00)min时,淋洗液naoh浓度为50.0mmol/l;图谱见图5,组分4葡萄糖、组分5蔗糖、组分6甘露糖醇三种组分重叠在一起,分离效果较差。说明前10min内采用高浓度淋洗的方法,用200mmol/l的氢氧化钠溶液进行色谱柱的强力冲洗,去除影响待测组分的干扰物,可以大幅度提高检测的准确度。
[0089]
实施例9:甜味剂待检样品预处理中ph对检测的影响
[0090]
按照实施例1中实验分析条件,在其它条件不变的情况下,依次配制不同ph值 (3.0、5.5、7.0、8.5、10.0)的同一理论浓度的混合标准溶液进行检测,实验结果表明,组分1山梨糖醇、组分2麦芽糖醇、组分3海藻糖、组分5葡萄糖、组分6 蔗糖、组分7果糖这6种组分含量受溶液ph值的影响较大,甘露糖醇受ph值影响较小,不同ph值对各个组分的检测影响如表6所示。
[0091]
从表6种可以看出,葡萄糖测定含量在强酸和强碱性条件下,均出现一定程度的增大,其他糖及糖醇回收率均有所降低,这是因为大部分糖及糖醇在强酸和强碱条件下容易分解成葡萄糖,从而使得葡萄糖检测含量增加。山梨糖醇、麦芽糖醇、海藻糖、葡萄糖、果糖在ph大于8.5的碱性和ph小于7.0条件下,回收率大幅度降低,影响了定量分析。从表6中分析出,在ph值7.0~8.5的弱碱性条件下,7种组分测定含量变化很小,波动全部在2.36%以内,说明溶液在此时各组分含量稳定。
[0092]
表6溶液ph值对检测结果的影响
[0093][0094]
本发明通过对初始淋洗液浓度、流速、柱温等多种实验影响因素的深入研究,探索出了甜味剂中糖及糖醇同时检测的色谱条分离条件,建立了积分脉冲安培-离子色谱法同时检测7种糖及糖醇的分析方法。该方法简便、快速、灵敏、准确,完全适于甜味剂中糖及糖醇的快速分析。
[0095]
上述的实施例仅为本发明的优选技术方案,而不应视为对于本发明的限制,本技术中的实施例及实施例中的特征在不冲突的情况下,可以相互任意组合。本发明的保护范围应以权利要求记载的技术方案,包括权利要求记载的技术方案中技术特征的等同替换方案为保护范围。即在此范围内的等同替换改进,也在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1