一种用于快速检测甲状腺乳头状癌淋巴结转移的胶体金层析试纸条及其制备方法
1.本发明涉及生物医学技术领域,具体涉及一种用于快速检测甲状腺乳头状癌淋巴结转移的胶体金层析试纸条及其制备方法。
背景技术:
2.2020年全球新发586202例甲状腺癌病人,居全球癌症新发病例第9位,甲状腺癌是最常见的头颈部及内分泌系统恶性肿瘤。除与接触放射性物质有明确关联外,绝大部分甲状腺癌发病机理不清,最好的治疗办法就是早期发现、早期诊断与早期治疗,这是提高甲状腺癌临床诊疗水平的关键。其中,95%的甲状腺癌为甲状腺乳头状癌,60%-80%的甲状腺乳头状癌病人初次就诊时即伴随着颈部淋巴结肿大,多项研究表明甲状腺人太杂早期局部淋巴结转移率高达40%-60%。而淋巴结转移是导致甲状腺癌术后复发最重要的危险因素之一,部分患者会经历2次或者多次手术,给患者带来生理心理以及经济上的沉重负担。当前临床上检测淋巴结癌细胞转移方式为术中冰冻切片和术后组织病理学检查,由于术中冰冻切片假阴性率较高、检测样本数量受限及术后组织病理学耗时长等因素极大地影响了甲状腺癌手术效率,因此临床亟需一种术中客观检测甲状腺淋巴结癌细胞转移状态的方法。
3.肿瘤标志物是由肿瘤组织和细胞产生的异常表达的生物活性物质,根据其生化或免疫特性可以识别或诊断肿瘤。多数甲状腺癌患者组织中可发现分子标志物表达明显升高,正常淋巴结中不表达或低表达,且与疾病的相关性已得到认可,所以肿瘤标志物检查对甲状腺乳头状癌淋巴结转移方面具有重要的意义。
4.braf基因位于染色体7q34,参与rasraf-mapk、细胞外信号调节激酶
ꢀ‑
mapk途经的信号传导,常见于密码子600的突变,导致braf激酶持续激活,是mapk下游传导通路高表达,从而细胞过度增殖,恶化。braf v600e在检测甲状腺癌中有着极高的特异性,因braf突变常发生于ptc中,并且在良性结节中几乎并不存在,是ptc的特征性分子事件,并且该基因表达与肿瘤的进展、复发、甲状腺的外浸润、淋巴结转移和晚期肿瘤有着密切关系。多项国内外回顾性研究也表明,在braf突变阳性患者更容易发生中央区淋巴结转移。
5.细胞角蛋白来缘于单侧或者复层上皮基底细胞,是形成表皮细胞的构成细胞骨架一种中间丝状物,细胞角蛋白19(cytokeratin 19,ck19)是一种低分子量的细胞角蛋白,存在于各种上皮及正常上皮来源的肿瘤,在肌肉组织(平滑肌、心肌、骨骼肌等)、结缔组织(血液、骨、脂肪)和神经组织中均不表达。既往多项观察及回顾性研究表明,在dtc中,ck19呈高表达,在甲状腺的良性肿瘤中呈低表达甚至不表达。cyfra21-1是细胞角蛋白19片段抗原21-1 (cytokeratin 19fragment antigen 21-1)的英文缩写,1992年bodenmuler等釆用杂交瘤技术制备出bm19.21和ks19.1两株单克隆抗体,经配对组成免疫测定方法,可特异性的识别细胞角蛋白19的片段抗原。在正常情况下细胞角蛋白 19在外周血、骨髓、淋巴结中无表达或低表达,而在恶性上皮癌中,激活的蛋白酶加速了细胞的降解,使得大量可溶性的cyfra21-1被释放,造成血液中 cyfra21-1浓度升高。cyfra21-1作为一种新的上皮来源性
质的肿瘤标志物,近几年来在肿瘤临床的应用越来越广泛,在许多上皮性癌如肺癌、鼻咽癌等都有不同程度的检出率;最新的研究表明,血清cyfra21-1水平与甲状腺癌的远处转移和肿瘤进展相关。lee等测量了130枚淋巴结fna穿刺洗脱液中cyfra21-1含量,发现以cyfra21-1来判定淋巴结转移,良性和恶性淋巴结中之间几乎没有重叠,并其诊断临界值不受手术影响。因此通过检测淋巴结中cyfra21-1及braf v600e 含量,可以推测淋巴结中癌细胞转移情况。
技术实现要素:
6.针对上述技术背景中的问题,本发明目的是提供一种方便、快捷、准确度高的检测淋巴结中cyfra21-1/braf v600e含量的胶体金层析试纸条及其制备方法。
7.为了实现以上目的,本发明采用的技术方案为:
8.一种用于快速检测淋巴结中cyfra21-1/braf v600e含量的胶体金层析试纸条,该层析试纸条包括底板,在所述底板的一端自左至右顺次搭接有样品垫、结合垫、硝酸纤维素膜和吸收垫;所述结合垫为喷涂有cyfra21-1/braf v600e捕获抗体-胶体金复合物的聚酯膜,所述硝酸纤维膜上包被检测t线和质控c线,所述检测t线位于所述质控c线的左侧,所述检测t线内抗体为cyfra21-1/brafv600e单抗,所述质控c线为羊抗鼠igg。
9.进一步地,所述检测t线包被的cyfra21-1/braf v600单抗的浓度为 0.1-3mg/ml,包被参数为10-20μl/cm;所述质控线c线包被的蛋白的浓度为 0.5-2mg/ml,包被参数为15-20/cm;所述层析试纸条的检测t线与质控c线之间的距离为2-5mm。
10.更进一步地,所述检测t线包被的cyfra21-1/braf v600单抗的浓度为 2-3mg/ml,包被参数为15-20μl/cm;所述质控线c线包被的蛋白的浓度为 0.5-1mg/ml,包被参数为18-20μl/cm;所述层析试纸条的检测t线与质控c线之间的距离为2-3mm。
11.更进一步地,所述检测t线包被的cyfra21-1/braf v600e单抗的浓度为 2mg/ml,包被参数为15μl/cm;所述质控线c线包被的蛋白的浓度为1mg/ml,包被参数为18μlμl/cm;所述层析试纸条的检测t线与质控c线之间的距离为 2mm。
12.进一步地,所述层析试纸条还包括卡壳,所述层析试纸条置于所述卡壳内,所述卡壳上开有显色区和加样孔,加样孔对准所述样品垫所在区域,显色区对准所述检测t线和质控c线所在区域。
13.本发明的另一目的在于,提供一种上述用于快速检测淋巴结中cyfra21-1及 braf v600e含量的胶体金层析试纸条的制备方法,包括如下步骤:
14.(1)制备结合垫:
15.颗粒直径为20-40nm,取20ml胶体金溶液置于烧杯中,加入150μl 0.1m 的k2co3溶液调节溶液的ph至7.0,搅拌均匀,然后加入cyfra21-1/braf v600e 捕获抗体,搅拌30min左右,然后加入2ml 10%的bsa溶液,离心,(20min, 10000rpm),然后弃去上清液,再加入1%的bsa的溶液(ph 8.6的缓冲溶液溶解)继续离心,弃去上清液,使用恢复液对沉淀物进行恢复;之后喷涂在在200平方厘米大小的玻璃纤维膜上面,37度烘干2小时,作为结合垫,室温避光保存备用;
16.(2)在底板上一端顺次相互搭接地贴附样品垫、结合物垫、硝酸纤维素膜和吸收垫;
17.(3)通过三维平面划膜仪在硝酸纤维素膜上包被检测t线和质控c线,质控c线为羊抗鼠igg,浓度为0.5-5mg/ml,包被参数为18μl/cm;检测t线为cyfra21-1/braf v600e的检测,浓度为0.1-3mg/ml,包被参数为15μl/cm;
18.(4)将底板连同其上贴附的材料切成5mm宽度的试纸条;
19.(5)将步骤(4)中的试纸条装入卡壳内,卡壳上开有显色区和加样孔,加样区对准样品垫位置,显色区对准t线和c线所在区域;
20.(6)将试纸条装在铝箔袋中,内装一个干燥剂和滴管,进行密封室温保存。
21.进一步地,所述恢复液的成分为:150mm的nacl,1%的bsa,0.5%的蔗糖,0.5%的酪蛋白钠。
22.进一步地,采用柠檬酸钠还原氯金酸法制备胶体金:将所用的玻璃仪器用超纯水过夜浸泡,然后冲洗干净,将烧杯中加入1000ml三蒸水,然后加入10ml 的1%的柠檬酸钠溶液,加热至沸腾后,再加入10ml 1%的氯金酸溶液,煮沸 15min后停止加热,待冷却后置于4度冰箱保存。
23.更进一步地,所述胶体金可替换为修饰银、铜、铁、钳、絕、硒、碳、硼、镁、铝、钙、钛、钻、锭、钥、锌或镉、铭纳米材料中的任意一种或多种组合。
24.进一步地,所述质控c线为羊抗鼠igg,浓度为0.5-5mg/ml,包被参数为 18μl/cm;检测t线为cyfra21-1/braf v600e的检测,浓度为0.1-3mg/ml,包被参数为15μl/cm。
25.与现有技术相比,本发明具有以下优点:
26.本发明提供了一种用于甲状腺癌转移淋巴结裂解液中cyfra21-1/braf v600e 含量检测的胶体金层析试纸条及其制备方法,较之前的方法使用更加简便、快捷、灵敏度高、特异性好。能够用于术中检测,为临床医生提供后续手术方案的指导。术中冰冻切片通常每隔3mm对淋巴结样本进行一次切片检测,因此只有30-40%的淋巴结样本被检测,而试纸条检测的对象为整个淋巴结,通过研磨完整的淋巴结样本,可提高样本的组织利用率,减少了假阴性结果。同时,brafv600e突变检测为当前临床实践中确诊甲状腺癌的检测的方式,试纸条通过检测淋巴结中cyfra21-1及braf v600e蛋白确认癌细胞来源于上皮且起源于甲状腺,并且通过层析试纸条的方法加快了检测速度,最终达到降低漏诊率、减轻病人疾病负担、提高甲状腺外科手术工作效率的目的,具有重要的临床意义。
附图说明
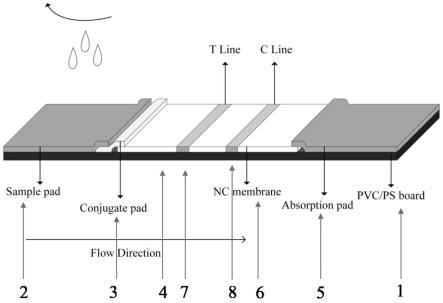
27.图1为用于检测淋巴结中cyfra21-1/braf v600e的胶体金试纸条示意图;
28.图2为胶体金试纸条的产品示意图。
29.图中:1-底板;2-样品垫;3-金标垫;4-层析垫;5-吸收垫;6-硝酸纤维素膜;7-检测线;8-质控线;
具体实施方式
30.以下结合附图对本发明的具体实施方式进行详细说明。应当理解的是,此处所描述的具体实施方式仅用于说明和解释本发明,并不用于限制本发明。
31.实施例1胶体金层析试纸条的制作
32.如图1所示,胶体金试纸条,包括底板1,在所述底板1的一端自左至右顺次搭接有
样品垫2、结合垫3、硝酸纤维素膜4和吸收垫5;所述结合垫3为喷涂有cyfra21-1/braf v600e捕获抗体-胶体金复合物的聚酯膜,所述硝酸纤维膜4 上包被检测t线6和质控c线7,所述检测t线6位于所述质控c线7的左侧,所述检测t线6内抗体为cyfra21-1/braf v600e单抗,所述质控c线7为羊抗鼠igg。
33.底板1的材料为pvc胶板;样品垫2的材料为玻璃纤维素膜;吸收垫5的材料为吸水纸。
34.1)胶体金制备(柠檬酸钠还原氯金酸法)
35.将所用的玻璃仪器用超纯水过夜浸泡,然后冲洗干净,将烧杯中加入1000 ml三蒸水,然后加入10ml的1%的柠檬酸钠溶液,加热至沸腾后,再加入10 ml 1%的氯金酸溶液,煮沸15min后停止加热,待冷却后置于4度冰箱保存。
36.2)结合垫的制备
37.取20ml胶体金溶液置于烧杯中,加入150μl 0.1m的k2co3溶液调节溶液的ph至7.0,搅拌均匀,然后加入cyfra21-1/braf v600e捕获抗体,搅拌30min 左右,然后加入2ml 10%的bsa溶液,离心,(20min,10000rpm),然后弃去上清液,再加入1%的bsa的溶液(ph 8.6的缓冲溶液溶解)继续离心,弃去上清液,将沉淀物进行恢复,恢复液的成分为:150mm的nacl,1%的bsa,0.5%的蔗糖,0.5%的酪蛋白钠;将其喷涂在在200平方厘米大小的玻璃纤维膜上面,37 度烘干2小时,作为结合垫,室温避光保存备用。
38.3)在聚氯乙烯(pvc)胶板上一端顺次相互搭接地贴附样品垫、结合物垫、硝酸纤维素膜和吸水垫;
39.4)通过三维平面划膜仪在硝酸纤维素膜上包被t线和c线,c线为羊抗鼠 igg,浓度为0.5-5mg/ml,包被参数为18μl/cm;t线为cyfra21-1/braf v600e的检测,浓度为0.1-3mg/ml,包被参数为15μl/cm;
40.5)将pvc胶板及贴附的材料切成5mm宽度的试纸条;
41.6)将步骤(4)中的试纸条装入卡壳内,卡壳上开有显色区和加样孔,加样区对准样品垫位置,显色区对准t线和c线所在区域。
42.上述胶体金层析试纸条检测甲状腺乳头状癌淋巴结中cyfra21-1/braf v600e 含量的方法如下:
43.①
临床样本收集及后处理:
44.自手术台上取下肿大淋巴结,生理盐水及pbs清洗,以无菌刀片将淋巴结均分左右两等份,一份放入装有福尔马林溶液的无菌标本袋中,送往病理科等待术后病理结果,一份立刻放置无菌标本袋中,于-80℃冰箱保存。
45.后处理:将样本自负八十度冰箱取出后,剪切成小块,尽量去除淋巴结周围的其他非目的组织,加入适量的预冷的1x pbs于4℃,700g(3000rpm)离心3min,弃掉上清,重复洗涤两次。称量后以5μl/mg洗涤后的组织中加入预冷的ripa组织裂解液,置匀浆器冰上均质直至淋巴结样本完全成匀质状液体无明显组织小块,再于4℃,12830g(12000rpm)离心3min以沉淀组织或细胞碎片,转移上清为组织活性总蛋白部分,分装并保存于-80℃,用于下游实验。
46.②
开始检测,打开铝箔袋,取出试纸条,平放在检测台面上,自加样孔将60μl淋巴结裂解上清液加入,由于吸附垫吸水纸具的虹吸作用,裂解后淋巴结上清液向吸水纸一端
移动,经过t线及c线时,淋巴结上清液内cyfra21-1/brafv600e蛋白与包被在此处的cyfra21-1/brafv600e捕获抗体及羊抗鼠igg结合形成纳米金-cyfra21-1/brafv600e捕获抗体复合物,胶体金聚集,肉眼可见红色条带形成;
47.③
结果判断:10-15分钟观察试纸条,如果t线和c线都变红,则样品被记录为阳性,此淋巴结发生癌细胞转移。如果c线变红,而t线没有变红,则将样品记录为阴性。无论何种情况下,如果c线不显色,则认为试纸条无效。
③
层析读数仪读取15分钟时样品试纸条t线及c线的灰度积分并且转化为t/c比值。
48.通过以上方法可以方便快速地检测甲状腺乳头状癌淋巴结裂解液上清中是否存在cyfra21-1及brafv600e蛋白,进而检测甲状腺乳头状癌淋巴结是否发生肿瘤转移,操作简便快速、灵敏性高、特异性好,可作为现有术中甲状腺淋巴结癌细胞转移快速检测方法的辅助方法,甚至是取代方法。
49.以上显示和描述了本发明的基本原理、主要特征和本发明的优点。本行业的技术人员应该了解,本发明不受上述实施例的限制,上述实施例和说明书中描述的只是本发明的原理,在不脱离本发明精神和范围的前提下本发明还会有各种变化和改进,这些变化和改进都落入要求保护的本发明的范围内。本发明要求的保护范围由所附的权利要求书及其等同物界定。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1