重建颅骨的方法与流程
本发明涉及一种使用具有避免翻转插值曲面的复杂3d模型的非刚性配准来重建的骨架例如颅骨的方法。尽管并不排除其他目的,但本发明特别地涉及一种为了颅颌面(cmf)手术规划、法医调查和身体人类学研究中的一个或多个目的而重建颅骨的方法。
背景技术:
重建人类颅骨的方法在颅颌面(cmf)手术规划、法医调查和身体人类学研究中是重要的。
在颅颌面手术中,外科医生的任务是在有缺损的(目标)颅骨上进行手术以恢复患者的正常外观。颅骨缺损可能由撞击损伤(例如交通或工作事故、暴力),先天性畸形(即婴儿颅骨的异常发育)或肿瘤生长引起。比如博医来(博医来)
在法医调查中使用重建受损或腐烂的颅骨来帮助根据受害者的遗体对他或她进行识别。一旦产生了无缺损的颅骨模型,法医调查员就可以通过在颅骨上铺设皮肤和肌肉“组织”来重建受害者的面部。可以手动或使用软件工具生成颅骨的重建模型。重建的颅骨越接近受害者受伤或死亡之前颅骨的正常形状,所重建的面部越将准确地识别受害者。
人类学家重建原始人类(有时是化石化的)颅骨,以便了解不同物种特征的颅骨形状的差异。由于暴力、疾病、先天性畸形或腐烂,这些颅骨可能有缺损。根据人类所属物种的识别,手动或使用软件工具重建有缺损的颅骨。换句话说,人类学家从该物种的已知正常颅骨形状的模型开始。
通常,有五种已知的生成一重建颅骨的方法:
手动操作方法:在监视器上显示颅骨的3d模型。这允许外科医生例如在3d模型中手动切割和重新定位骨骼以规划和生成一重建模型。然而,手动骨骼重新定位是缓慢、耗时和主观的,因为它是建立在外科医生的经验和判断的基础上的。
基于对称的方法:颅骨的无缺损或健康的部分反映在横向对称平面上,反射部分用作对缺损部分正常形状的估计。不需要参考模型,但必须有颅骨的无缺损部分才能工作。如果颅骨两侧都有缺损,则不能使用这些方法。
几何重建方法:3d模型配准涉及参考模型的空间变换,以使其与目标模型对齐。3d模型配准算法使用线性变换(例如缩放,旋转,平移)或非刚性(弹性)变换。在已知的颅骨重建方法中,参考模型非刚性地配准到颅骨缺损模型的健康或无缺损部分。配准的参考模型用于估计有缺损的颅骨部分的正常形状。这些方法不需要对称的健康部分,而是使用单个参考模型来生成重建模型。这些方法的准确性取决于参考模型和目标模型之间的相似性以及配准算法中使用的点数。现有方法倾向于仅使用稀疏分布的少量点,以最小化错误的对应关系。错误的对应关系将导致错误的配准,从而导致错误的重建。
统计重建方法:这些方法通过将统计参考模型与缺损模型的健康部分相匹配,并使用匹配的统计模型推断缺损模型的缺损部分的正常形状,改进了上述几何重建方法的局限性。然而,这些方法需要大量正常颅骨模型的训练样本以构建统计模型。重建精度取决于统计模型在正常颅骨中捕获形状变化的程度。如果没有充分捕获这种正常的形状变化,则重建将不准确。统计重建方法还依赖于健康部位和缺损部位之间的相关性。
骨骼重新定位方法:这些方法涉及将受损颅骨的断裂骨骼的碎片重新定位到其正确位置,例如wo2015142291a1中所述。如果碎片缺失或不完整,则无法应用这些方法。此外,他们需要从医学图像中获得单独断裂骨骼的碎片。手动获得骨骼碎片可能非常耗时。
由于所有已知的生成重建颅骨的方法都有缺点,因此希望提供一种自动、方便和准确的方法,用于从可能是由于断裂、损伤或先天性畸形造成的有缺损的颅骨重建颅骨。
如上所述,重建的几何和统计方法都涉及3d参考模型的非刚性配准方法。现有的非刚性配准方法可以分为两大类:近似和插值。
近似方法通过将参考曲面拟合到目标曲面来产生近似曲面。根据平滑度约束,使相应参考曲面和目标曲面之间的平均距离最小化。位置对应被认为是软约束,并且配准曲面与目标曲面具有非零距离或误差。
另一方面,插值方法通过拟合参考曲面产生插值曲面,使其精确地通过相应的目标点。位置对应被认为是硬约束,因此配准的曲面相对于相应的目标点具有零误差。因此,插值方法通常比用于形状复杂的3d对象配准的近似方法更准确。
使用插值曲面执行非刚性配准有三种方法:自由变形(ffd),拉普拉斯变形和薄板样条(tps)。
自由变形(ffd)使用在3d空间内包围形状(网格)的想法。3d空间上的变形点会使包围的网格扭曲或变形。3d空间被划分为平行六面体区域,其顶点是控制点。当控制点移动到新位置时,ffd根据伯恩斯坦多项式变换控制点。ffd主要用于动画并且往往不用于颅骨重建,因为控制点不在3d模型上,使得在自由变形之后难以确定控制点的所需位置。
拉普拉斯变形通过保留网格顶点的曲率和曲面法线来使参考模型变形以拟合目标点。它将曲面点与其所需位置完全对应地移动。与tps不同,拉普拉斯变形的线性方程组仅捕获网格顶点而没有对应关系。其数据矩阵的大小与没有对应关系的网格顶点数的平方成比例。因此,数据矩阵的大小以及时间和空间复杂度随着对应关系的增加而降低。拉普拉斯变形尚未用于颅骨重建。
相比之下,薄板样条(tps)是颅骨配准和重建的常用方法。tps翘曲的过程类似于薄金属板的弯曲。tps使用最小化弯曲能量的平滑映射函数转换网格的曲面点。映射函数由仿射变换和非线性扭曲组成,非线性扭曲定义为薄板样条函数的加权和。映射函数的参数通过产生唯一解的线性方程组求解。该线性组的数据矩阵的大小与关键点(landmark)数量的平方成比例。因此,随着相应关键点数量的增加,tps的时间和空间复杂度迅速增加。
当在点对应中存在被视为硬约束的冲突时,非刚性配准插值方法可以产生“翻转的曲面”。曲面翻转是指导致曲面自相交的曲面法线的局部反转。翻转的曲面会导致曲面形状严重变形,并且很难去除。用于颅骨的配准和重建的现有tps方法使用足够稀疏分布的一组对应点以避免曲面翻转。然而,这种稀疏分布降低了tps配准和重建结果的准确性。
因此,期望提供一种用于复杂3d对象的非刚性配准和重建的算法,其具有更高的准确度。
已经开发了计算机辅助系统用于规划cmf和整形外科手术。例如,已知的系统使外科医生能够手动重新定位颅骨的骨骼,然后预测面部外观。然而,手动重新定位骨骼是耗时且不准确的。其他已知的系统,例如博医来的爱普兰(iplan)
因此,希望提供一种计算机辅助系统,其方便且准确地从患者的缺损颅骨产生正常颅骨模型,用于cmf手术规划、法医调查和人类学研究。
技术实现要素:
根据本发明的第一方面,提供了一种获得一重建骨架的三维模型的方法,包括使用迭代曲面插值算法。该方法包括以下步骤:提供待重建的骨架的目标三维模型;提供骨架的参考三维模型;基于位置约束非刚性地将参考模型配准到目标模型,以便产生配准的参考模型;并将初始重建模型设置为配准参考模型。该方法还包括以下步骤:迭代地进行第一对应搜索以识别该重建和目标模型上的第一组对应点,并且在每次迭代期间,基于该对应点刚性地将重建的模型递增地配准到目标模型;进行第二对应搜索以识别该重建和目标模型上的第二组对应点;去除所识别的对应点中的交叉点,并基于剩余的对应点将所重建的模型非刚性地配准到目标模型,以便产生配准的完全重建的模型,该模型是该重建骨架的模型。
第一对应搜索可以包括确定所述第一组中的一对对应点之间的距离小于或等于第一预定参数,并且该对对应点的曲面法线相差不超过10度。第一预定参数可以是0.5mm。
第二对应搜索可以包括确定所述第二组中的一对对应点之间的距离小于或等于第二预定参数,并且目标模型上的点是该重建的模型上的对应点的最近曲面点。该第二预定参数可以是3mm。
迭代地进行第一对应搜索可以进一步包括通过应用无交叉条件来选择第一组的稀疏子集。稀疏子集可以包含目标模型上大约少于10%的顶点。
去除交叉可以包括获得一组密集的对应点。该一组密集的对应点可以包含目标模型上大约80%的顶点。
可以通过在参考模型和目标模型上手动标记重要的解剖学关键点来获得位置约束。关键点可以分开以确保没有交叉。
目标模型可以是缺损颅骨的模型,参考模型可以是无缺损颅骨的模型。
可以使用拉普拉斯变形来执行非刚性配准。
该方法还可以包括基于缺损颅骨的图像提供目标模型。可以修改图像的图像强度和/或关注体积。可以编辑目标模型以移除不相关的部分。该方法还可以包括标记目标模型的缺损部分。可以通过软件包的用户界面手动执行修改、编辑和标记中的至少一个。
该方法可以进一步包括基于目标模型和参考模型之间的相似性从多个参考模型中选择参考模型。
骨架可包括颅骨。该方法还可以包括在颅颌面手术期间利用重建的颅骨的模型。
可以使用可编程计算机的处理器来执行该算法。
根据本发明的第二方面,提供了一种计算机程序,包括计算机可读代码,当在计算机处理器上运行时,该计算机可读代码使处理器根据上述的第一个方面执行获得重建的骨架的三维模型的方法。
附图说明
图1是使用迭代曲面插值算法获得重建的骨架的三维模型的方法的流程图;
图2是计算机辅助cmf手术规划的方法的流程图;
图3示出了软件包中的颅骨分割工具的用户界面,用于使用包括三个标准解剖视图的输入的ct图像生成颅骨的3d模型;
图4示出了对图3的三个视图中的每一个的关注体积的确定;
图5说明了图3的三个视图的裁剪;
图6示出了图3的三个视图的图像强度阈值的修改,使得强度不大于阈值的体素被滤除;
图7示出了基于图6的修改的三个视图生成网格模型;
图8示出了用于生成颅骨的3d模型的软件包中的颅骨重建工具的用户界面,包括图7的网格模型;
图9示出去除了图7的模型的不相关部分,其中切割平面将脊柱与主颅骨分开;
图10示出了图7的网格模型的颅骨,其中去除了不相关的部分;
图11a和11b示出了在图7的网格模型上的关键点的放置,每个关键点对应于参考模型上的关键点;
图12示出了包含图7的网格模型的缺损部分的体积的标记;
图13示出了图7的网格模型的缺损部分的标记;
图14说明放置在参考模型上的关键点;
图15a示出了标记有缺损部分的目标模型;以及
图15b示出了目标模型的非缺损部分的叠加和使用本发明的算法的重建。
具体实施方式
这里参考图1至图15描述的是使用迭代曲面插值算法获得一重建骨架的三维模型的方法。在示出的例子中的骨架是颅骨。在以下描述中,使用cmf手术规划作为示例。然而,应当理解,该方法可以应用于颅骨和面部重建,以用于法医调查、人类学研究等。该方法还可以应用于其他大骨重建。
使用本文描述的方法获得的三维模型可以在手术期间使用,例如,以提高重建的人体骨架的准确性。
产生重建颅骨的3d模型的方法包括使用具有避免翻转插值曲面(fais)的非刚性配准算法。该算法非刚性地将3d参考模型配准到受试者(即患者)的目标模型。非刚性配准的3d参考模型,即通过配准产生的模型,可以被视为受试者目标模型的重建的正常无缺损的模型。受试者的目标模型可能是正常的或有缺损的。如果有缺损,受试者的目标模型可能包含断裂部分,畸形部分或缺失部分。受试者的目标模型也可能包含异常值,例如x射线金属伪影。
算法的输入包括正常无缺损的3d参考模型f,可能有缺损的受试者的目标模型t,以及它们的对应关系c*。对应关系c*是一组对应点(p,p'),其中p是参考模型f上的关键点,p'是目标模型t上的对应关键点。c*是从重要解剖关键点((lt))的手动标记获得的,放置在参考模型f和目标模型t上。关键点被充分分开以确保没有交叉。算法的输出是目标模型t的重建的正常模型r。
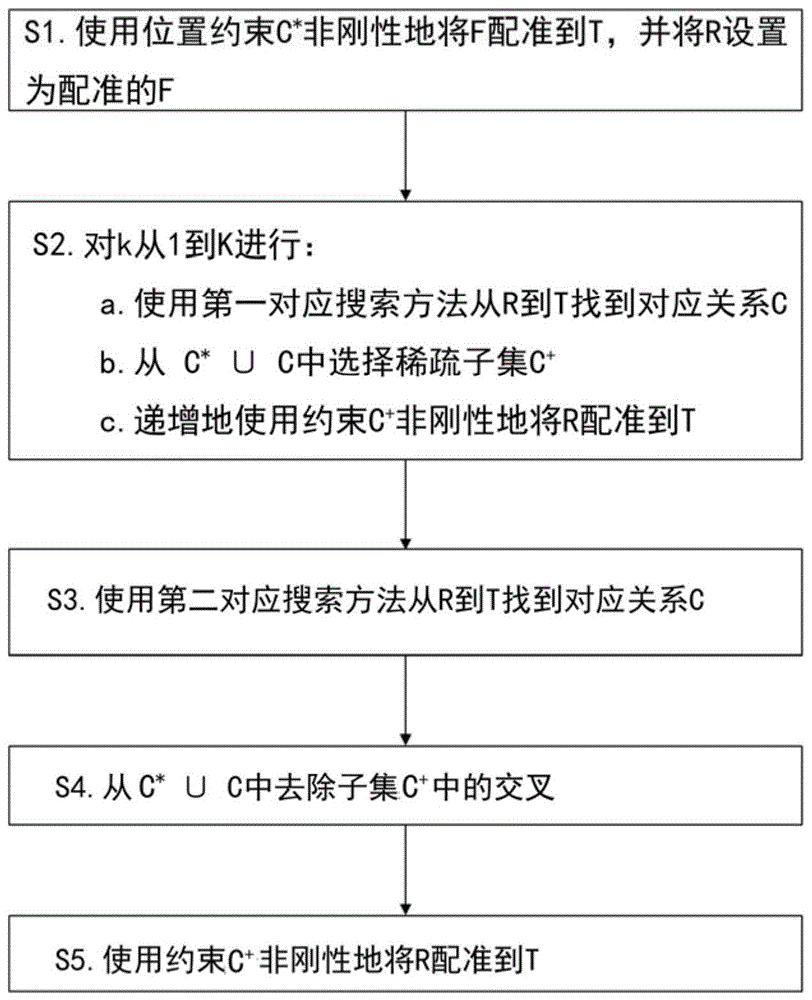
如图1所示,非刚性配准算法fais是一种迭代算法,包括以下步骤:
s1.使用位置约束c*非刚性地将f配准到t,并将r设置为配准的f.
s2.对k从1到k进行:
a.使用第一对应搜索方法(如下所述)从r(即配准的f)到t找到对应关系c。
b.从c*∪c(如下所述)中选择稀疏子集c+。
c.递增地使用约束c+非刚性地将r配准到t。
s3.使用第二对应搜索方法(如下所述)从r到t找到对应关系c。
s4.从c*∪c中去除子集c+中的交叉(方法5)。
s5.使用约束c+非刚性地将r配准到t。
与使用薄板样条的已知重建方法相比,上面概述的步骤1、2c和5使用拉普拉斯变形执行非刚性配准。因此,本发明方法随着对应点数量的增加执行得更快,而现有方法随着对应点数量的增加执行得更慢。
现在将更详细地描述上面概述的非刚性配准,迭代算法fais的步骤2a,步骤2b,步骤3和步骤4。
s2a.使用第一对应搜索方法从r到t找到对应关系c
在早期迭代中应用的第一对应搜索方法针对满足以下条件的配准参考模型f(即r)上的每个网格顶点p在目标模型t上搜索对应的网格顶点p':
·p'足够接近p:||p-p’||≤d1,其中d1是搜索范围的常数参数,以及
·p'和p具有相似的曲面法线,相差不超过10°。
例如,d1可以设定为0.5mm。曲面法线是在给定点垂直于曲面的矢量。步骤2a的输出是(p,p')形式的一组对应矢量。
s2b.从c*∪c中选择稀疏子集c+
该步骤包括基于简单的无交叉条件选择对应关系集c*∪c的稀疏子集c+(其中c*是f和t的对应关系,c是r和t的对应关系):如果符合以下情况,则所有对不存在交叉:
c+中的(p,p’)和(q,q’),||p–q||>2d
其中d是在c*∪c中||p’–p||的上限,且其中p和q是参考模型曲面上的点,p'和q'是目标模型曲面上的点。
稀疏子集c+包含在3d网格模型(目标模型)上小于10%的顶点的区域中。
该选择包括以下子步骤:
s2b.1将上限d设置为c*∪c中最大的||p’–p||。
s2b.2初始化c+=c*。
s2b.3对于每个(p,p’)∈c,如果c中没有(q,q'),那么||p–q||≤2d,然后将(q,q’)加到c+。
对应矢量的交叉可以导致曲面法线的局部反转(曲面翻转)。
s3.使用第二对应搜索方法从r到t找到对应关系c。
在迭代的最后步骤中使用的第二对应搜索方法针对参考f上的每个网格顶点p在目标t上搜索对应点p',使得:
·p'是t上p的最近曲面点,即p处的曲面法线与t的最近交点,以及
·||p-p’||≤d2,其中d2是常数参数
例如,d2可以设定为3mm。输出是一组(p,p')形式的对应矢量。
s4.从c*∪c中去除子集c+中的交叉点
该步骤基于一般无交叉条件选择对应关系集c*∪c的密集子集c+:如果符合以下情况,则不存在交叉:
对于每个(p,p’)∈c,cosθ(p;q)<||p–q||/(2d),
其中d是c*∪c中||p’–p||的上限。
尽管稀疏子集包含3d网格模型上少于10%的顶点,但是密集子集c+包含3d网格模型(目标模型)上大约80%的顶点。
该选择包括以下子步骤:
s4.1将上限d设置为c*∪c中最大的||p’–p||。
s4.2初始化c+=c*。
s4.3对于每个(p,p’)∈c,如果所有q∈n(p)={q|||p-q||≤2d},
使得(q,q’)∈c满足cosθ(p;q)<||p–q||/(2d),然后将(p,p')添加到c+。
由于是非常密集的对应关系集,因此该算法相对于目标颅骨的无缺损部分可以实现几乎零误差。因此,颅骨的无缺损部分的重建形状几乎与所使用的参考模型无关。现有的重建方法使用稀疏的一组对应点来隐含地避免曲面翻转。现有方法中使用的对应点的数量比本发明方法的数量小两个数量级,因此本发明方法比使用非刚性配准的现有方法精确得多。
另外,可以通过检测和排除冲突的硬约束来避免曲面翻转,而不是尽力去除曲面翻转。由于选择了非常密集的对应关系集,因此排除冲突的硬约束是可以承受的。同样,任何异常值都可以忽略。
如上所述,在早期迭代中,算法以小增量将参考模型配准到目标模型,以减少错误对应的风险。因此,参考模型(即初始重建的模型或配准的参考模型)仅在早期迭代中非常轻微地变形以拟合目标模型。由于参考模型配准在后续迭代中更接近于目标模型,减少了错误对应的风险,因此允许参考模型变形更多。在最后的迭代中,算法将参考模型精确地配准到目标模型,以产生目标颅骨的完全重建模型。因此,利用上述步骤1至5中描述的算法的本发明的重建方法比现有方法更稳健。
例如,上述生成一重建颅骨的3d模型的方法可以用于cmf手术的规划过程。在手术之前对要重建颅骨的个体进行规划。在计算机的处理器(例如,服务器、个人计算机、笔记本电脑、平板电脑或其他一个或多个处理设备)上运行的颅骨重建工具使用非刚性配准算法中包括的具有如上所述避免翻转插值曲面(fais)的步骤来执行该方法。
现在将参考图2至图15描述计算机辅助的cmf手术规划程序。图3至图13示出了为此目的而开发的软件包的用户界面,其结合了颅骨分割工具和使用fais算法的颅骨重建工具。用户界面被配置为接收用户输入,例如来自外科医生的输入,并且向用户显示颅骨或其他大骨结构的图像和/或一个或多个模型。软件包由计算机处理器操作。
手术规划程序有四个主要阶段,如图2所示:
阶段1:外科医生(或其他用户)指示颅骨分割工具以5个步骤从ct图像中分割并构建患者颅骨在其当前状态下的3d目标模型(下面更详细地描述)。
阶段2:外科医生使用颅骨重建工具以7个步骤准备目标颅骨以进行重建(下面更详细地描述)。
阶段3:外科医生指示颅骨重建工具执行具有避免翻转插值曲面(fais)的非刚性配准算法,以从患者的缺损颅骨模型生成他的正常颅骨模型的重建。将在步骤2中捕获的用户输入传递给算法。
阶段4:外科医生指示颅骨重建工具以stl(stereolithography)(立体光刻)格式输出重建的颅骨。可以将stl文件导入规划软件,例如爱普兰(iplan)
下面将更详细地描述这四个阶段。
第一阶段:3d颅骨模型的分割与构建
cmf手术规划程序的这一阶段从一组ct图像生成颅骨的3d网格模型(目标模型),其通常以dicom(医学数字成像和通信)格式存储。换句话说,患者颅骨在其当前(可能是受损的)状态下的3d模型是从对患者颅骨的扫描中获得的。阶段1包括5个步骤:
s1.1:导入ct图像
颅骨分割工具的导入功能用于导入ct图像。如图3所示,导入的ct图像显示在外科医生熟知的三个标准解剖视图中。这三个视图是横断面(轴向)视图(如图3中左上方所示),冠状面(正面)视图(如图3中左下方所示)和矢状面(内侧)视图(如图3中右下方所示))。
s1.2:确定关注的体积(voi)
如图4所示,外科医生调整三个视图中的每一个中的voi线以定义voi。尽可能小地形成包括颅骨的体积,但不包括颈部和脊柱。然后,如图5所示,应用voi裁剪工具以使用软件工具去除voi外部的体积。
s1.3:调整强度阈值
通过滤除强度值不大于给定阈值的体素(3d空间中的规则网格上的值)来实现颅骨分割。该方法简单,有效,并且可以在短时间内执行颅骨分割。颅骨分割工具的阈值功能用于调整强度阈值,使大多数软组织在三个视图中消失,如图6所示。强度阈值不应太低,否则要构建的颅骨模型将包含过多的软组织,这可能会影响重建的精确度。此外,强度阈值不应该太高,否则要构建的颅骨模型会不完整。
s1.4:生成网格模型
该工具的网格生成功能用于从强度值大于阈值的体积元素(体素)生成网格模型,如图7所示。然后,如果需要,网格被简化和平滑。网格模型表示患者颅骨在其当前状态下的3d目标模型。
s1.5:保存网格模型
该工具的导出功能用于以ply(多边形文件格式)或stl(立体光刻)格式保存生成的网格。以ply格式存储的网格模型的文件大小通常小于stl格式。stl格式用于计算机辅助手术规划系统,如爱普兰(iplan)
因此,在上述步骤中使用颅骨分割工具产生患者颅骨在其当前身体条件下的3d目标模型。该模型最初是根据扫描图像生成的,并且经过修改以为下一阶段的规划程序作准备。应当理解,第一阶段中的一些步骤可以以替代顺序执行,例如,可以在裁剪之前调整强度体积。
阶段2:颅骨模型的准备
在cmf手术规划程序的这个阶段,外科医生使用颅骨重建工具来准备目标(有缺损的)颅骨模型以进行重建。该准备包括去除不相关的部分和标记颅骨的缺损部分。目标模型还标有一组关键点,这些关键点对应于参考(无缺损)模型上的点。关键点指示颅骨曲面的特征点。
规划程序的阶段2包括7个步骤:
2.1:导入网格模型
如图8所示,颅骨重建工具的导入功能用于将网格模型导入到颅骨重建工具中,该工具形成软件包的一部分。导入的网格模型包括在阶段1中生成的目标(缺损)模型t,其被渲染在重建工具的中心区域中。当然,只要文件格式为ply或stl,该工具也可以接受由此处未描述的其他工具生成的目标模型。
2.2:去除不相关的部分
网格模型t可以包含脊柱,管柱和与颅骨重建无关的其他部分,并且如果包括的话可能降低重建的准确性。如图9和10所示,颅骨重建工具的切割功能用于去除这些不相关的部分。通过拟合将无关部分与主颅骨分开的切割平面来实现切割。此步骤与阶段1中执行的裁剪不同;阶段2.2执行从裁剪和阈值化的3d体积图像构建的3d模型的切割。
2.3:放置关键点
颅骨重建工具的关键点功能用于将关键点lt放置在目标模型t上,如图11a和11b所示。使用一小组的关键点来确保参考模型到目标模型的配准在解剖学上是正确的。每个目标模型关键点lt对应于参考模型f上的关键点lf。目标模型关键点lt不应放置在目标模型t的缺损部分上。因此,目标模型关键点集lt是参考关键点集lf的子集,因为在参考模型f的区域上通常会有关键点,由于损坏,它们不能放置在目标模型t的对应区域上。然而,颅骨重建工具不需要在目标模型上存在特定的关键点。例如,如果需要,该工具可以在没有正中矢状平面(msp)或法兰克福平面(fp)关键点的情况下操作。
目标关键点lt由用户放置得彼此足够远以避免可能的冲突。根据软件工具提供的参考图像放置关键点,这确保了关键点彼此足够远。这些手动放置的关键点形成本发明算法中的集合c*。
2.4:标记缺损部分
如图12和13所示,颅骨重建工具的绘画功能用于标记目标模型t的缺损部分,即患者颅骨需要重建的部分。通过定位包围缺损部分的voi来执行缺损部分的标记,如图13所示。
2.5:选择参考模型
颅骨重建工具的参考选择功能用于选择参考模型f。如下所述准备多个参考模型,并且具有避免翻转插值曲面(fais)的非刚性配准算法应使用与目标颅骨模型t最相似的模型。每个参考模型都是从不同人的ct扫描中产生的。这些参考模型存储在软件包中。对与目标颅骨模型最相似的参考模型的选择,可以由人类专家手动执行或者可以通过人工智能等自动执行。外科医生(或其他人类专家)对合适的参考模型的视觉选择倾向于在实践中实现最精确的重建。
参考模型的准备包括:
1.如上文阶段1中所述,从ct图像分割和构建3d颅骨模型。
2.提取3d颅骨模型的外曲面作为参考模型。
3.使用人类专家指示参考模型上的解剖关键点集。参考关键点集lf由48个或更多个关键点组成,如图14所示。其中8个定义了正中矢状平面(msp),其中4个定义了法兰克福平面(fp)。
在此处未示出的替代实施例中,颅骨重建工具可以被配置为自动识别与所输入目标颅骨模型最相似的参考模型。
2.6:目标颅骨外曲面的提取
颅骨重建工具用于自动提取目标颅骨模型t的外曲面。
2.7:参考颅骨与目标颅骨的刚性对齐
颅骨重建工具用于将参考模型f自动对齐到目标模型t。通过应用从参考关键点lf到目标关键点lt的最佳相似性变换来实现对齐。
一旦cmf手术规划程序的阶段1和阶段2完成,就可以完成阶段3。阶段3要求使用阶段2中产生的输入(即参考模型f和参考模型关键点lf,目标模型t和目标模型关键点lt)执行如上所述的具有避免翻转插值曲面(fais)的非刚性配准算法。如图15a和15b所示,使用fais的颅骨重建非常紧密地拟合目标模型的非缺损部分,这由图15b的叠加上的交替颜色图案表示。
通常,这里描述的方法比已知的重建方法更直观和更容易使用,因为它需要的用户输入更少。这减少了生成精确重建模型所需的时间。阶段3输出的是目标模型t重建的正常模型r。算法的执行由计算机系统的处理器进行。
cmf手术规划程序的阶段4包括使用颅骨重建工具来输出重建的模型r,通常以stl格式。可以将stl文件导入已知的规划软件包,例如爱普兰(iplan)
因此,本文描述的本发明方法提供了一种计算机辅助程序,其使用自动算法从受试者的缺损颅骨生成3d颅骨的重建。该方法可用于颅颌面外科规划、法医调查和人类学研究。可以设想该方法的其他用途,例如cmf外科医生的训练和cmf手术的植入物建模。该方法可以结合到3d建模软件和/或3d分割工具中,例如用于体积图像的3d分割。该方法适用于大骨结构或框架,例如颅骨或骨盆,其中所有手术决定都是根据骨的形状做出的。
该方法利用一种算法,该算法应用迭代曲面插值方法将参考模型配准到目标模型。它采用避免翻转技术来检测和去除对应矢量的可能交叉,从而避免在配准后网格曲面翻转。利用这种避免翻转技术,算法fais可以使用一组非常密集的对应点来执行配准。算法的对应关系集比现有方法高两个数量级。因此,它比非刚性配准中的现有方法准确得多。此外,它对于比如x射线金属伪像的异常值也是稳健的,因为第一对应搜索方法使用距离和曲面法线来寻找对应点。与颅骨曲面的曲面法线相比,金属伪影具有非常不同的曲面法线。有利的是,该算法在目标模型的重建模型和非缺损部分即未损坏或无缺损的颅骨部分之间产生精确匹配。
此外,该方法可以精确地生成正常的重建模型,不仅来自断裂的颅骨,而且来自不完整和变形的颅骨。因此,它适用于比许多已知重建方法更广泛的应用。
另外,由于几何重建的性质,该方法可以处理双侧有缺损的颅骨。这克服了仅适用于一侧有缺损的颅骨的基于对称性的方法的局限性。因此,该方法可以生成完整的重建模型而不是部分模型。
该软件包由各种操作系统支持,例如windows,linux和osx。
本领域技术人员将理解,在不脱离本发明的范围的情况下,可以对上述实施例进行各种修改。
例如,该方法可以利用上述算法而无需任何用户特定的关键点。可选地或进而,该方法可以包括处理目标颅骨模型的断裂或变形部分,就好像它们是缺失部分一样。可选地或进而,该方法可以包括将横向对称性作为算法中的附加约束。可以使用薄板样条(tps)代替拉普拉斯变形。
在使用拉普拉斯变形的情况下,这可以包括基于参考模型的形状(即,配准的参考模型或重建的模型)对目标模型的左右对称性的约束。
该方法还可用于从受试者的断裂框道重建正常框道。如本文所提及的,术语“颅骨”可包括眼睛的眼眶骨。
上述算法fais的步骤s2b和步骤4可以以各种方式实现。一种替代方法是将c+初始化为c*∪c并去除c+中与条件冲突的(p,p')。
在此处未描述的另外的实施例中,本文描述的算法的步骤1之前可以有初始化步骤,其可以包括刚性配准。
该方法还可以用于将参考模型配准到一组训练3d模型中的每一个。配准参考模型具有训练模型的形状和相同的网格连通性,可以直接用作构建活动形状模型的训练模型。
可选地或进而,分数icp(ficp)或平面拟合配准可用于颅骨重建工具中的初始刚性配准。
另一种修改是使用该方法将参考面部模型配准到颅骨模型上方的面部关键点,以便从颅骨重建面部。这对cmf手术、法医调查和人类学研究很有用。
如本文所述,“正常”颅骨是指“无缺损”颅骨。在发生伤害、事故或疾病之前,无缺损的颅骨可能对应于或接近个体颅骨的实际构造或结构。可选地或进而,如果个体未经历异常发育(例如,先天性畸形),则无缺损的颅骨可以对应于或接近个体颅骨会具有的构造或结构。因此,“重建的”颅骨是指例如在手术后实现的无缺损的颅骨构造或结构。
如本文所述,“目标”颅骨是指要重建的实际人体颅骨,即受试者的有缺损或受损的颅骨。因此,目标模型是要重建的人体颅骨的模型。
- 还没有人留言评论。精彩留言会获得点赞!