活性物质、非水电解质电池、电池包及车辆的制作方法
实施方式涉及活性物质、非水电解质电池、电池包及车辆。
背景技术:
近年来,作为高能量密度电池,锂离子二次电池等非水电解质电池的研究开发如火如荼。非水电解质电池作为混合动力汽车或电动汽车等车辆、移动基站的不间断电源用等电源备受期待。另外,非水电解质电池作为昼夜耗电量的均衡化或智能电网等用途的固定型电源用电池也备受关注。因此,非水电解质电池除了要求高能量密度之外,还要求快速充放电性能、长期可靠性等其他特性也优异。例如,能够快速充放电的非水电解质电池具有充电时间非常短的优点。另外,这种非水电解质电池在混合动力汽车中还可以提高动力性能。进而,这种非水电解质电池还可以有效地将动力的再生能量回收。
为了能够进行快速充放电,需要电子和锂离子能够在正极与负极之间迅速地移动。但是,使用了碳系负极的电池在反复进行快速充放电时,有金属锂的树枝状结晶析出在电极上的情况。树枝状结晶有导致内部短路、结果引起发热和/或着火的危险。
因此,开发了代替碳质物而使用金属复合氧化物作为负极活性物质的电池。特别是,使用了钛氧化物作为负极活性物质的电池具有可进行稳定的快速充放电、寿命也比碳系负极长的特性。
但是,钛氧化物与碳质物相比,相对于金属锂的电位更高,即更贵。而且,钛氧化物的每单位重量的容量低。因此,负极使用了钛氧化物的电池具有能量密度低的问题。特别是,作为负极材料使用相对于金属锂的电位高的材料时,与使用了碳质物的电池相比,电压减小。因而,当将这种材料应用于电动汽车等车辆或大规模蓄电系统等需要高电压的系统中时,具有电池的串联数增大的问题。
例如,钛氧化物的电极电位以金属锂基准计为约1.5V,比碳系负极的电位更高(贵)。钛氧化物的电位是因电化学地对锂进行嵌入和脱嵌时的Ti3+与Ti4+之间的氧化还原反应所致,因而受到电化学方面的制约。因而,为了提高能量密度而降低电极电位实际上是困难的。
技术实现要素:
本发明的目的在于提供能够实现具有高能量密度、并兼具高的快速充放电性能和优异的寿命性能的非水电解质电池的活性物质、使用了该活性物质的非水电解质电池、具备该非水电解质电池的电池包及搭载有该电池包的车辆。
根据第1实施方式,提供含有复合氧化物的活性物质。该复合氧化物以通式LixM14-yTi10-zM22+zO27+δ表示。这里,M1含有选自Na、K、Cs中的至少1种。M2含有选自Zr、Sn、V、Nb、Ta、Mo、W、Fe、Co、Mn、Ni、Al中的至少1种。x满足0≤x<18。y满足0<y<4。z满足0<z<4。δ满足-0.3≤δ≤0.3。
根据第2实施方式,提供非水电解质电池。该非水电解质电池包含含有第1实施方式的活性物质的负极、正极、和非水电解质。
根据第3实施方式,提供电池包。该电池包具备第2实施方式的非水电解质电池。另外,根据实施方式,提供搭载有该电池包的车辆。
根据上述构成的活性物质,能够实现具有高能量密度、且兼具高的快速充放电性能和优异的寿命性能的非水电解质电池、电池包及车辆。
附图说明
图1是表示Li2Na2Ti6O14及Na3Ti9Nb3O27的充放电曲线的曲线图。
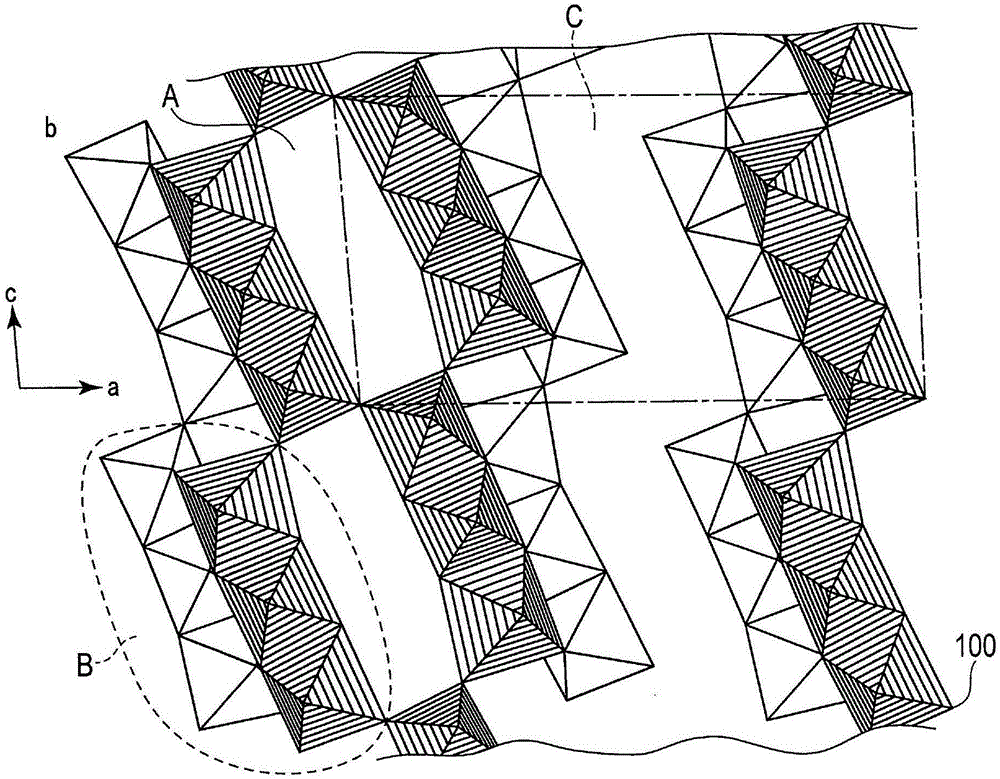
图2是表示Na3Ti9Nb3O27的结晶结构的示意图。
图3是第2实施方式的扁平型非水电解质电池的截面图。
图4是图3的A部的放大截面图。
图5是示意地表示第2实施方式的另一个扁平型非水电解质电池的部分缺失立体图。
图6是图5的B部的放大截面图。
图7是第3实施方式的电池包的分解立体图。
图8是表示图7的电池包的电路的模块图。
图9是表示搭载了实施方式的电池包的车辆的示意图。
具体实施方式
以下参照附图说明实施方式。其中,实施方式中共同的构成带有相同的符号且省略重复的说明。另外,各图是用于促进实施方式的说明及其理解的示意图,其形状或尺寸、比例等与实际的装置有不同的方面,但这些也可参照以下的说明和公知的技术适当地进行设计变更。
(第1实施方式)
根据第1实施方式,提供含有具有单斜晶型结晶结构的复合氧化物的电池用活性物质。该复合氧化物以通式LixM14-yTi10-zM22+zO27+δ表示。这里,M1是选自Na、K、Cs中的至少1种元素。M2是选自Zr、Sn、V、Nb、Ta、Mo、W、Fe、Co、Mn、Ni、Al中的至少1种元素。x处于0≤x<18的范围内。y处于0<y<4的范围内。z处于0<z<4的范围内。δ处于-0.3≤δ≤0.3的范围内。
第1实施方式的电池用活性物质所含的复合氧化物可对应于在以通式LixM14Ti10M22O27+δ表示的具有单斜晶型结晶结构的复合氧化物中、在M1位点的一部分中导入空孔位点、并用M2元素将Ti位点的至少一部分置换了的置换氧化物。通过改变结晶结构中的M1元素的种类或量,可以改变相对于金属锂的氧化还原电位的电位。另外,通过在M1位点上制作空孔,易于使Li离子嵌入脱嵌,可以进一步提高充放电容量。进而,通过改变结晶结构中的M2元素的种类或置换Ti位点的M2元素的置换量,可以改变Li离子的充放电容量。
第1实施方式的电池用活性物质可以相对于金属锂的氧化还原电位具有0.5V~1.45V(vs.Li/Li+,相对于Li/Li+)的范围内的锂嵌入的平均电位。由此,负极含有第1实施方式的电池用活性物质的非水电解质电池相比较于负极含有例如锂嵌入电位为1.55V(vs.Li/Li+)的钛复合氧化物的非水电解质电池,可以显示更高的电池电压。
另外,第1实施方式的电池用活性物质在1.0V~1.45V(vs.Li/Li+)的电位范围内可以对许多的Li离子进行嵌入及脱嵌。以下一边参照图1一边对第1实施方式的电池用活性物质在低于1.55V的电位下能够显示高容量的理由进行说明。
图1示出了对电极使用金属锂而制成半电池时的复合氧化物Li2Na2Ti6O14的充放电曲线(虚线)及复合氧化物Na3Ti9Nb3O27的充放电曲线(实线)。实线的充放电曲线(放电/Li脱嵌曲线50及充电/Li嵌入曲线51)表示具有单斜晶型结晶结构的复合氧化物Na3Ti9Nb3O27的电位变化,该复合氧化物是第1实施方式的电池用活性物质能够含有的复合氧化物。另一方面,虚线的充放电曲线(放电/Li脱嵌曲线40及充电/Li嵌入曲线41)表示复合氧化物Li2Na2Ti6O14的电位变化,该复合氧化物是以通式Li2+wNa2Ti6O14+δ所示的具有单斜晶型结晶结构的复合氧化物。另外,复合氧化物Na3Ti9Nb3O27是在复合氧化物Na4Ti10Nb2O27的结晶结构中将Na位点的一部分制成空孔、并用Nb将Ti位点的一部分置换所获得的复合氧化物。
如图1所示,任一种复合氧化物在平均电压为1.25V~1.45V(vs.Li/Li+)的范围内均可将Li离子嵌入脱嵌。但是,复合氧化物Li2Na2Ti6O14的充放电容量低达95mAh/g左右。另一方面,如图1所示,复合氧化物Na3Ti9Nb3O27的电池容量可以显示高达150mAh/g的值。
第1实施方式的电池用活性物质能够含有的复合氧化物在1.55V(vs.Li/Li+)以下的工作电位下能够对许多的Li离子嵌入脱嵌的原因在于,结晶结构中具有大的隧道结构。接着,对该复合氧化物在结晶结构中具有大的隧道结构的理由进行说明。
第1实施方式的电池用活性物质能够含有的复合氧化物以通式LixM14-yTi10-zM22+zO27+δ表示。这里,M1为选自Na、K、Cs中的至少1种。M2为选自Zr、Sn、V、Nb、Ta、Mo、W、Fe、Co、Mn、Ni、Al中的至少1种。其中,x处于0≤x<18的范围内、y处于0<y<4的范围内、z处于0<z<4的范围内、δ处于-0.3≤δ≤0.3的范围内。
这里,M2的总价数是,在占有M2位点的M2元素含有3价元素为z3摩尔、4价元素为z4摩尔、5价元素为z5摩尔及6价元素为z6摩尔时,成为和:(z3×3)+(z4×4)+(z5×5)+(z6×6)(这里,z3+z4+z5+z6=2+z)。另外,这里所说的M2元素的价数是指锂离子未电化学地嵌入复合氧化物中的状态下的价数。例如,在利用后述方法使电池完全放电的状态下,可以变成锂离子未电化学地嵌入复合氧化物的状态。这些M2元素的总价数若大于5价,则能够将空孔导入到M1位点中,因此优选。特别是当在M1位点上导入空孔时,可成为Li嵌入位点的位点的电荷排斥减少。如此,复合氧化物能够对更多的锂离子进行嵌入脱嵌,可以显示高的能量密度及高的电池电压,进而可以实现快速充放电性能和寿命性能这两者优异的非水电解质电池。
接着,对第1实施方式的电池用活性物质能够含有的复合氧化物可以兼具高的快速充放电性能(速率性能)及优异的寿命性能的理由进行说明。
复合氧化物Li2Na2Ti6O14中,相对于含有成为结晶结构骨架的Ti的位点数为6、氧化物离子的数量为14。即,该复合氧化物中,相对于每1个该位点的氧化物离子的数量为14/6,即约2.33。另一方面,第1实施方式的电池用活性物质能够含有的复合氧化物以通式LixM14-yTi10-zM22+zO27+δ表示。该复合氧化物中,相对于含有成为结晶骨架的Ti及M2的总位点数为12、氧化物离子的数量为27(δ=0时),相对于每1个该位点的氧化物离子的数量为27/12,即2.25个。另一方面,在为《Electrochemistry communications、8(2006)、673-677》所记载的Na2Ti6O13时,相对于含有成为结晶骨架的Ti的总位点数为6、氧化物离子的数量为13,相对于每1个该位点的氧化物离子的数量为13/6、即约2.17。
如此,在类似的结晶结构中,氧化物离子相对于含有构建结晶骨架的Ti的位点的数量是不同的。一般来说,Li离子在结构中移动时,氧化物离子数量少者的情况下,带有正电荷的Li离子与带有负电荷的氧化物离子的相关性减少。因此,当结构中的氧化物离子数量减少时,则Li离子的移动变得容易、速率性能提高。另一方面,构成骨架的Ti离子由于也带有正电荷,因此与Li离子同样,氧化物离子的数量少的情况下,Ti离子与氧化物离子的相关性减少。因此,当结构中的氧化物离子的数量减少时,则Ti-O的键合强度降低、结晶骨架的稳定性受损。结果,有寿命性能降低的倾向。因而,虽然Li离子的移动变得容易、但为了保持结晶骨架的稳定性,氧化物离子的数量过多或过少均不优选。实施方式的复合氧化物LixM14-yTi10-zM22+zO27+δ由于氧化物离子数的平衡优异,因此能够使Li离子的移动变得顺畅、同时可以稳定地维持晶格。
另一方面,关于复合氧化物的通式LixM14-yTi10-zM22+zO27+δ中的下角标x,可根据复合氧化物的充电状态在0≤x<18之间发生变化。例如,利用后述的制造方法时,可以制造上述通式中下角标x为0的复合氧化物。通过在非水电解质电池中作为负极活性物质含有下角标x为0的复合氧化物、并对该非水电解质电池进行充电,成为x的值上升到大于0且小于18的范围内的值的状态。或者,利用例如后述的方法,在进行初次充电之前也按照式中的Li量x的值达到大于0且小于18的范围内的方式对原料组成比进行控制,也可合成复合氧化物。含有在进行初次充电之前Li量x的值也处于大于0且小于18的范围内的状态的复合氧化物的电池用活性物质可以抑制在初次充放电时锂离子被捕获在该结构中。结果,可以提高初次充放电效率。
另外,根据上述通式,可以通过改变下角标y的值来改变结晶结构中的M1的量。作为一例,当M1含有Na时,可以根据结晶结构中的Na量,在相对于金属锂的氧化还原电位为1.2V~1.5V(vs.Li/Li+)的范围内对电极的平均工作电位进行调节。即,通过控制下角标y的值,电池的工作电位设计可以容易地进行。
通式LixM14-yTi10-zM22+zO27+δ所示的复合氧化物具有属于空间群C2、Cm、C2/m中的至少1种的单斜晶型结晶结构,a轴、b轴、c轴的晶格常数优选分别满足可以是单斜晶型结晶的结晶结构包含上述空间群中的一种,或者也可以是单斜晶型结晶的结晶结构包含上述空间群中的2种以上。
图2是表示具有空间群C2/m的对称性的复合氧化物之一例的Na3Ti9Nb3O27的结晶结构图。
图2所示的结晶结构中,多面体的顶点位置100表示氧化物离子的位置。
另外,图2所示的结晶结构中,区域A表示在结晶结构中具有锂离子能够3维地移动的通道的隧道状空隙位点。该区域A可以对锂离子进行嵌入和脱嵌。区域B具有以成为结晶结构的骨架的Ti或Nb为中心的氧化物的多面体结构。另一方面,区域C是能够进行嵌入和脱嵌的锂离子所存在的层状空隙位点。该例的化合物的a轴、b轴、c轴的晶格常数分别为的范围内。
这种复合氧化物由于可获得足以对锂离子进行嵌入和脱嵌的空间,因此优选。含有该例的复合氧化物的电池用活性物质在充放电时的锂离子的可逆性提高。由此,活性物质的实际容量增加、速率性能高、还可以提高非水电解质电池的寿命性能,因此优选。
第1实施方式的电池用活性物质也可以含有具有除了带有空间群C2、Cm、C2/m的对称性的结晶相之外、还带有其他对称性的结晶相混合存在的结晶结构的复合氧化物,或者还可以含有具有类似于空间群C2、Cm、C2/m的对称性的结晶结构的复合氧化物。即便是含有这种复合氧化物的电池用活性物质,也可以获得与含有具有空间群C2、Cm、C2/m的对称性的复合氧化物的形态的电池用活性物质相同的的效果。作为类似于C2/m对称性的对称性的具体例子,可举出Cmca、F222、Pmcm、Pmma及Cmma等。可以含有一种这样的具有类似于C2/m的对称性的复合氧化物。或者,可以含有分别具有类似于C2/m的彼此相同或不同的对称性的2种以上的复合氧化物。
通式LixM14-yTi10-zM22+zO27+δ中的下角标x可根据复合氧化物的充电状态、在0≤x<18之间发生变化。另外,下角标y表示从通式LixM14Ti10M22O27+δ所示的复合氧化物的结晶结构中的M1位点中除去了M1元素的量。y处于0<y<4的范围内。y优选处于1.0<y≤3.0的范围内、更优选处于0.1≤y≤2.0的范围内。下角标z表示从Ti位点上除去了Ti的量以及在M2位点上追加了M2元素的量。z处于0<z<4的范围内。z更优选处于0.1≤z≤2.0的范围内。δ处于-0.3≤δ≤0.3的范围内。下角标δ可以根据以该通式表示的复合氧化物的氧缺损或在电池用活性物质的制造工艺中不可避免地混入的氧的量、在-0.3≤δ≤0.3的范围内发生变化。
作为一例,在M1元素为Na的通式LixNa4-yTi10-zM22+zO27+δ所示的复合氧化物的单斜晶型结晶结构中,可以减少占有Na的位点的Na的一部分、在该位点上构成成为Li离子的嵌入位点的空孔位点。由此,可以在保持锂离子的嵌入及脱嵌容易的晶格体积的状态下,增加每单位重量或单位容积的能量密度。另外,通过改变Na量,可以改变电极的平均工作电位。由此,电池的电位设计变得容易。
进而,该方式中更为优选的方式是M2元素为Nb。即,该更优选的方式中,第1实施方式的电池用活性物质所含的复合氧化物以通式LixNa4-yTi10-zNb2+zO27+δ表示。Ti可以从4价1价还原成3价,而Nb可以从5价2价还原成3价。因此,通过将Ti的至少一部分置换成Nb,可以增加复合氧化物的锂嵌入量。通过在Na位点产生空孔位点、同时将Ti的一部分置换为Nb,从而可以进一步增加复合氧化物的锂嵌入量。进而,Nb的相对于嵌入Li时的金属锂的氧化还原电位在1.5V~1.0V的宽范围内平稳地变化。因此,通过将Ti的至少一部分置换为Nb,不仅充放电容量增加,而且如一边参照图1一边前述说明的那样,电位平坦部变得更为平稳。因此,在将Ti的一部分置换成Nb的复合氧化物中,易于获得充放电电位与充电状态的相关性、电池的充电状态管理等变得容易。
第1实施方式的电池用活性物质所含的复合氧化物例如可以取粒子的形态。第1实施方式的电池用活性物质所含的复合氧化物的平均粒径并无特别限定,可以根据所希望的电池特性使其变化。
另外,第1实施方式的电池用活性物质优选含有上述复合氧化物的粒子和被覆在其表面上的碳等导电性物质。这种优选方式的电池用活性物质可以显示经提高的快速充放电性能。上述复合氧化物中,由于利用均匀固相反应而产生锂的嵌入及脱嵌,因此具有随着锂嵌入量增加、电子导电性增大的性质。这种复合氧化物中,在锂嵌入量少的区域中,电子导电性相对地降低。因此,通过预先在复合氧化物粒子的表面上被覆碳等导电性物质,可以与锂嵌入量无关地获得高的快速充放电性能。
或者,代替碳等导电性物质、在复合氧化物粒子的表面被覆伴随锂嵌入而电子导电性得以表现的钛酸锂,也可获得相同的效果。进而,在电池的内部短路时,由于锂从被覆在复合氧化物粒子表面上的钛酸锂中被脱嵌,因此该钛酸锂发生绝缘化。因而,可以发挥优异的安全性。
<BET比表面积>
第1实施方式的电池用活性物质含有的复合氧化物的BET比表面积并无特别限定,优选为5m2/g以上且小于200m2/g。更优选为5m2/g以上且30m2/g以下。
BET比表面积为5m2/g以上时,则可以确保与电解液的接触面积、易于获得良好的放电速率性能、而且可以缩短充电时间。另一方面,当BET比表面积小于200m2/g时,与电解液的反应性不会变得过高、可以提高寿命性能。另外,当使BET比表面积为30m2/g以下时,由于可以抑制与电解液的副反应性,因此可以期待更长寿命化。另外,此时可以使后述的制造电极中所用的含有活性物质的浆料的涂饰性变得良好。
这里,比表面积的测定利用以下方法:在液氮温度下使吸附占有面积已知的分子吸附在粉体粒子表面上,由其量求得试样的比表面积。最常利用的方法是利用不活泼性气体的低温低湿物理吸附的BET法。BET法的基础理论是将单分子层吸附理论Langmuir理论扩张到多分子层吸附的作为比表面积计算方法最为有名的理论。将由此求得的比表面积称作BET比表面积。
<制造方法>
第1实施方式的电池用活性物质优选如以下说明地那样进行合成。具体地说,利用固相反应法合成起始化合物,对该起始化合物进行质子交换而生成前体。之后,对前体实施热处理、脱水,从而可以合成。
首先,以适当的化学计量比混合原料的氧化物或化合物盐等,获得混合物。此时,按照起始化合物的组成比达到M13-0.5yTi5-0.5zM21+0.5zO14的方式调节原料的混合比。上述的盐优选是碳酸盐及硝酸盐等在较低温下发生分解而产生氧化物的盐。接着,将所得混合物粉碎,尽量达到均匀地进行混合。
接着,对进行粉碎和混合所获得的混合物进行预烧成。预烧成在大气中、在600~850℃的温度范围内共计进行1~3小时。接着,提高烧成温度,在大气中、在900~1500℃的范围内进行主烧成。在主烧成之前,优选对进行了预烧成的混合物进行再混合。通过如此预先进行预烧成、对原料中的碳酸盐等进行分解后再混合,从而在主烧成中原料粒子之间可以密合。结果,可以获得均匀且具有高结晶性的粒子。
另外,作为轻元素的锂在900℃以上的温度下进行烧成时有时会发生蒸散。此时,预先研究烧成条件下的锂的蒸散量,使锂原料以该量过量地含有在原料的混合物中,补充蒸散部分,获得准确组成的试样。
进而,更优选防止因氧缺损等所导致的晶格缺陷。例如,在主烧成前对原料粉进行加压成型而加工成料粒状或棒条状,从而可以在减少与大气接触的面积且增加粒子之间的接触面积的情况下来进行烧成。这样,可以抑制晶格缺陷的生成。在工业上批量生产时,优选在烧成原料粉时在氧气氛下等氧分压高的条件下进行烧成,或者在通常的大气中烧成后在400~1000℃的温度范围下进行热处理(退火)以对氧缺损进行修复。如果不这样抑制晶格缺陷的生成,则有结晶性降低的可能性。
接着,将通过上述固相反应获得的钛酸碱化合物(起始化合物)分散在盐酸、硝酸、硫酸等酸性水溶液中并进行搅拌。调整与酸性水溶液的处理时间,获得用质子将起始化合物中的M1的一部分置换了的前体HM12-0.5yTi5-0.5zM21+0.5zO14·H2O。在900℃~1100℃之间加热该前体,使结晶水完全地脱水,从而获得目标的LixM14-yTi10-zM22+zO27+δ(此时为x=0)。这里,为了合成x>0的复合氧化物、即预先嵌入有锂的状态的复合氧化物,可以将所得M14-yTi10-zM22+zO27+δ浸渍在氢氧化锂水溶液(1M)中进行离子交换,从而获得LixM14-yTi10-zM22+zO27+δ。
在上述合成方法中,复合氧化物的结晶结构具有基于空间群C2、Cm、C2/m任一者的对称性,按照a轴、b轴、c轴的晶格常数分别为的范围内,期待依次调整M1及M2的元素的种类、调整对M1位点进行空孔位点化的量或M2元素的置换量。
如上进行合成时,如之前说明的那样,例如可以制造在上述通式中下角标x为0的复合氧化物。将下角标x为0的复合氧化物作为负极活性物质组装在非水电解质电池中,通过对该非水电解质电池进行充电,成为式中的Li量x的值上升为大于0且小于18的范围内的值的状态。或者,还可以作为原料使用碳酸锂等锂源,以最终x的值为大于0且小于18的范围内的原料组成比合成复合氧化物。如此,可以合成x值为大于0且小于18的范围内的状态的复合氧化物。或者,如上地合成复合氧化物之后,即便是将该复合氧化物浸渍于氢氧化锂水溶液等中,也可获得x的值为大于0且小于18的范围内的状态的复合氧化物。
接着,对利用粉末X射线衍射法的复合氧化物的X射线衍射图的获取方法及复合氧化物组成的确认方法进行说明。
当在非水电解质电池的电极材料中含有成为测定对象的活性物质时,如下进行前处理。
首先,形成接近于锂离子自活性物质的结晶完全脱嵌的状态的状态。当负极中含有成为测定对象的活性物质时,使电池处于完全放电状态。使电池完全地放电的状态是指通过在相对于金属锂电位为+3.0V的电位下将含有该活性物质的电极保持1小时以上、从而使该活性物质中的可动Li离子脱嵌了的状态。
具体地说,为了制作完全地放电的状态,在干燥氩气气氛下对上述电池进行分解之后,将含有该活性物质的电极取出。使用该电极,构成以金属锂作为对电极及参比电极的3极式半电池。此时,该电极相对于金属锂负极作为正极进行工作。使用充放电装置,在充电方向(Li从该电极脱嵌的方向)上流入电流直至半电池的单电池电位达到3.0V。达到3.0V之后,再保持于该电位1小时以上,由此进行Li离子从含有该活性物质的电极上的脱嵌,从而可以成为完全放电的状态。但是,有时即便是放电状态下也会稍存在残留的锂离子,但对于以下说明的粉末X射线衍射测定结果不会造成大的影响。
接着,在填充有氩的手套箱中对电池(半电池)进行分解,取出电极。利用适当的溶剂对取出的电极进行洗涤,实施减压干燥。溶剂例如可以使用碳酸甲乙酯等。洗涤干燥后,确认表面上没有锂盐等白色的析出物。
供至粉末X射线衍射测定时,将如后述那样进行了洗涤的电极剪切成与粉末X射线衍射装置的托架面积基本相同的面积,作为测定试样。
供至组成分析时,如后述那样从洗涤后的电极中将活性物质取出,对取出的活性物质进行分析。
<利用粉末X射线衍射法的复合氧化物的X射线衍射图的获取方法>
活性物质的粉末X射线衍射测定如下进行。
首先,将对象试样粉碎至平均粒径达到5μm左右。即便是原本平均粒径小于5μm时,为了将凝集块粉碎,也优选利用研钵等进行粉碎处理。平均粒径可以利用激光衍射法求得。将经过粉碎的试样填充在形成于玻璃试样板上的深度为0.5mm的托架部分中。玻璃试样板例如使用Rigaku公司制的玻璃试样板。此时,留意将试样充分地填充在托架部分中。另外,注意不要因为试样的填充不足而引起裂纹及空隙等。接着,自外部使用另外的玻璃板充分地按压试样以进行平滑化。此时,注意不要因填充量的过于不足而使得自托架的基准面产生凹凸。接着,将填充有试样的玻璃板设置在粉末X射线衍射装置中,使用Cu-Kα射线获得衍射图案(XRD(X-ray diffraction)图案)。
另外,根据粒子的形状,有由Rietveld解析的结果可见填充试样时结晶面在特定方向上排列的所谓取向性的情况。此时,根据试样的填充方法,有峰的位置偏离、峰强度比发生变化的可能性。这种取向性高的试样优选使用毛细管(圆柱状的玻璃细管)进行测定。具体地说,将试样插入到毛细管中,将该毛细管载置于旋转式试样台上,一边旋转一边进行测定。利用这种测定方法,可以获得缓和了取向性的结果。
作为粉末X射线衍射测定的装置,例如使用Rigaku公司制SmartLab。测定条件如下:测定法:平行电子束法(θ/2θ连动扫描);Cu靶;45kV 200mA;滤波器:Kβ滤波器或单色仪;梭拉狭缝:入射及受光均为5°;步宽:0.02deg;扫描速度:20deg/分钟(使用单色仪时为5deg/分钟);半导体检测器:D/teX Ultra 250;试样板托架:平板玻璃试样板托架(厚度为0.5mm);测定范围:5°≤2θ≤90°的范围。使用其他装置时,按照获得与上述同等测定结果的方式,进行使用了粉末X射线衍射用标准Si粉末的测定,在峰强度及峰顶位置与上述装置一致的条件下进行。另外,当试样的取向性强、根据平板玻璃托架中的填充密度而峰强度发生变化时,使用玻璃毛细管及旋转试样台进行测定。
如此获得的X射线衍射(XRD)图案优选可以应用于Rietveld解析。为了收集Rietveld用数据,按照步宽达到衍射峰的最小半峰宽的1/3~1/5、最强反射的峰位置处的强度达到5000cps以上的方式来适当地调整测定时间或X射线强度。
利用Rietveld法对如上获得的XRD图案进行解析。Rietveld法中,由预先推测的结晶结构模型计算衍射图案。通过使该计算值与实测值全部地拟合,可以精密地分析与结晶结构有关的参数(晶格常数、原子坐标、占有率等)。由此,可以研究所合成的氧化物的结晶结构的特征。另外,可以研究构成元素在各位点中的占有率。作为用于估算Rietveld解析中的观测强度和计算强度的一致程度的尺度,使用拟合参数S。需要按照该S小于1.8的方式来进行解析。另外,在决定各位点的占有率时,必须要考虑标准偏差σj。对于这里所定义的拟合参数S及标准偏差σj,利用《粉末X線解析の実際日本分析化学会X線分析研究懇談会編(粉末X射线解析的实际日本分析化学会X射线分析研究座谈会编)中井泉、泉富士夫编著(朝仓书店)》所记载的数学式进行推测。
利用以上的方法,可以获得与测定对象的活性物质的结晶结构有关的信息。例如,如上所述测定第1实施方式的电池用活性物质时,可知测定对象的电池用活性物质含有具有单斜晶结构的复合氧化物。另外,通过如上所述地进行测定,例如可以研究空间群C2/m等测定对象的结晶结构的对称性。
当成为测定对象的活性物质含有在非水电解质电池的电极材料中时,首先利用之前说明过的步骤,将电极从非水电解质电池中取出并进行洗涤。将取出并进行了洗涤的电极剪切成与粉末X射线衍射装置的托架面积基本相同的面积,制成测定试样。
将所得测定试样直接粘贴在玻璃托架上进行测定。此时,预先测定来自金属箔等电极基板的峰的位置。另外,还预先测定导电剂或粘结剂等其他成分的峰。当基板的峰与活性物质的峰重叠时,优选将含有活性物质的层(例如后述的活性物质层)从基板上剥离后供至测定。这是为了在定量地测定峰强度时将重叠的峰分离。例如,通过在溶剂中对电极基板照射超声波,可以将活性物质层剥离。将活性物质层封入在毛细管中,载置于旋转试样台上进行测定。通过这种方法,可以在减小了取向性的影响的基础上获得活性物质的XRD图案。
<复合氧化物组成的确认方法>
电池用活性物质的组成例如可以使用电感耦合等离子体(Inductively Coupled Plasma;ICP)发光分光法进行分析。此时,各元素的存在比依赖于所使用的分析装置的灵敏度。因此,例如使用ICP发光分光法对第1实施方式的一例电池用活性物质的组成进行分析时,有时数值自之前说明的元素比以测定装置的误差量有所偏离。但是,即便是测定结果如上所述以分析装置的误差范围发生了偏离,第1实施方式的一例电池用活性物质也可充分地发挥之前说明过的效果。
利用ICP发光分光法测定组装在电池中的电池用活性物质的组成时,具体地通过以下步骤进行。首先,通过之前说明的步骤,将含有成为测定对象的活性物质的电极从非水电解质电池中取出,进行洗涤。将经过洗涤的电极体放在适当的溶剂中,照射超声波。例如,在装于玻璃烧杯中的碳酸甲乙酯中放入电极体,在超声波洗涤机中使其振动,从而可以将含有电极活性物质的电极层从集电体基底上剥离。接着,进行减压干燥,对所剥离的电极层进行干燥。利用研钵等对所得电极层进行粉碎,从而成为含有对象的电池用活性物质、导电助剂、粘合剂等的粉末。利用酸将该粉末溶解,从而可以制作含有电池用活性物质的液体样品。此时,作为酸可以使用盐酸、硝酸、硫酸、氟化氢等。将该液体样品供至ICP发光分光分析,从而可以了解电池用活性物质的组成。
根据第1实施方式,提供含有具有单斜晶型结晶结构的复合氧化物的电池用活性物质。该复合氧化物以通式LixM14-yTi10-zM22+zO27+δ表示。该复合氧化物在1.0V~1.45V(vs.Li/Li+)的电位范围内可以显示平稳的电位变化,其平均工作电位可以通过改变Na量来进行调整。进而,结晶结构具有锂离子易于嵌入脱嵌的结晶结构、可以增加充放电容量。结果,第1实施方式的电池用活性物质可以实现具有高能量密度、电池电压可容易地设计、快速充放电性能和寿命性能优异且充放电状态的管理容易的非水电解质电池。
(第2实施方式)
根据第2实施方式,提供非水电解质电池。该非水电解质电池包含含有第1实施方式的电池用活性物质的负极、正极和非水电解质。
第2实施方式的非水电解质电池还可以进一步具备配置于正极与负极之间的隔膜。正极、负极及隔膜可以构成电极组。非水电解质可以保持在电极组中。
另外,第2实施方式的非水电解质电池可以进一步具备收容电极组及非水电解质的外包装构件。
进而,第2实施方式的非水电解质电池可以进一步具备电连接于正极的正极端子及电连接于负极的负极端子。正极端子的至少一部分和负极端子的至少一部分可以伸出至外包装构件的外侧。
以下,对负极、正极、非水电解质、隔膜、外包装构件、正极端子及负极端子详细地进行说明。
1)负极
负极可以含有集电体和负极层(即负极活性物质含有层)。负极层可形成在集电体的单面或两面上。负极层可以含有负极活性物质和任意的导电剂及粘结剂。
负极层作为负极活性物质可以含有第1实施方式的电池用活性物质。使用了第1实施方式的电池用活性物质的负极具有电位在1.4V(vs.Li/Li+)~1.0V(vs.Li/Li+)的范围内平稳地变化的低电极电位,可以调整其平均工作电位。进而,通过具有锂离子易于嵌入脱嵌的结晶结构,可以提高充放电容量。因此,具备这种负极的第2实施方式的非水电解质电池的充放电状态管理容易、显示优异的寿命性能、高的能量密度及容易的平均工作电压调整且高的电池电压。
作为负极活性物质,可以单独使用第1实施方式的电池用活性物质,也可以使用混合了第1实施方式的电池用活性物质和其他活性物质的混合物。其他的活性物质的例子可举出具有斜方锰矿结构的钛酸锂(例如Li2Ti3O7)、具有尖晶石结构的钛酸锂(例如Li4Ti5O12)、单斜晶型二氧化钛(TiO2)、锐钛矿型二氧化钛、金红石型二氧化钛、锰钡矿型钛复合氧化物、单斜晶型铌钛复合氧化物(例如Nb2TiO7)、钛酸钠锂(Na2Li2Ti6O14)、钛酸锶锂(Li2SrTi6O14)等。可以将这些其他活性物质中的一种与第1实施方式的活性物质组合使用。或者也可以将这些其他活性物质中的2种以上与第1实施方式的活性物质组合使用。
导电剂是为了提高集电性能且抑制负极活性物质与集电体的接触电阻而配合的。导电剂的例子包含气相生长碳纤维(Vapor Grown Carbon Fiber;VGCF)、乙炔黑、炭黑及石墨等碳质物。可以将它们中的1种作为导电剂使用,或者也可以组合2种以上作为导电剂使用。
粘结剂是为了填埋所分散的负极活性物质的空隙、且使负极活性物质和集电体粘结而配合的。粘结剂的例子包含聚四氟乙烯(polytetrafluoro ethylene;PTFE)、聚偏氟乙烯(polyvinylidene fluoride;PVdF)、氟系橡胶及苯乙烯丁二烯橡胶、聚丙烯酸化合物及酰亚胺化合物。可以将它们中的1种作为粘结剂使用,或者也可以组合2种以上作为粘结剂使用。
负极层中的活性物质、导电剂及粘结剂优选以分别为68质量%以上且96质量%以下、2质量%以上且30质量%以下及2质量%以上且30质量%以下的比例配合。通过使导电剂的量为2质量%以上,可以提高负极层的集电性能。另外,通过使粘结剂的量为2质量%以上,负极层与集电体的粘结性变得充分、可以期待优异的循环性能。另一方面,从谋求高容量化的方面出发,优选导电剂及粘结剂分别为28质量%以下。
集电体使用在负极活性物质的锂的嵌入及脱嵌电位下电化学稳定的材料。集电体优选由铜、镍、不锈钢或铝、或者含有选自Mg、Ti、Zn、Mn、Fe、Cu及Si中的1种以上元素的铝合金制作。集电体的厚度优选为5μm~20μm。具有这种厚度的集电体可以获得负极的强度和轻量化的平衡。
通过使用第1实施方式的电池用活性物质,可以使负极层的密度(不含集电体)为1.8g/cm3~2.8g/cm3的范围。负极层的密度为该范围内的负极可以显示优异的能量密度、且可以显示电解液的优异保持性。更优选负极层的密度为2.1g/cm3~2.6g/cm3。
负极例如如下制作。首先,将负极活性物质、粘结剂和导电剂混悬在常用的溶剂中,制备浆料。接着,将该浆料涂布在集电体上并进行干燥,形成负极层。之后,对形成于集电体上的负极层实施压制,从而制作负极。负极还可通过将负极活性物质、粘结剂及导电剂形成为料粒状而制成负极层、将其配置在集电体上来制作。
2)正极
正极可以含有集电体和正极层(正极活性物质含有层)。正极层可形成在集电体的单面或两面上。正极层可以含有正极活性物质和任意的导电剂及粘结剂。
作为正极活性物质,例如可以使用氧化物或硫化物。氧化物及硫化物的例子包含可以对锂进行嵌入及脱嵌的化合物、即二氧化锰(MnO2)、氧化铁、氧化铜、氧化镍、锂锰复合氧化物(例如LixMn2O4或LixMnO2)、锂镍复合氧化物(例如LixNiO2)、锂钴复合氧化物(例如LixCoO2)、锂镍钴复合氧化物(例如LiNi1-yCoyO2)、锂锰钴复合氧化物(例如LixMnyCo1-yO2)、具有尖晶石结构的锂锰镍复合氧化物(例如LixMn2-yNiyO4)、具有橄榄石结构的锂磷氧化物(例如LixFePO4、LixFe1-yMnyPO4、LixCoPO4)、硫酸铁[Fe2(SO4)3]、钒氧化物(例如V2O5)及锂镍钴锰复合氧化物。上述式中,0<x≤1、0<y≤1。作为活性物质,可以单独使用这些化合物或者组合使用多个化合物。
更优选的正极活性物质的例子包含正极电压高的锂锰复合氧化物(例如LixMn2O4)、锂镍复合氧化物(例如LixNiO2)、锂钴复合氧化物(例如LixCoO2)、锂镍钴复合氧化物(例如LiNi1-yCoyO2)、具有尖晶石结构的锂锰镍复合氧化物(例如LixMn2-yNiyO4)、锂锰钴复合氧化物(例如LixMnyCo1-yO2)、锂磷酸铁(例如LixFePO4)及锂镍钴锰复合氧化物。上述式中,0<x≤1、0<y≤1。
作为电池的非水电解质使用常温熔融盐时,优选的正极活性物质的例子包含锂磷酸铁、LixVPO4F(0≤x≤1)、锂锰复合氧化物、锂镍复合氧化物及锂镍钴复合氧化物。这些化合物由于与常温熔融盐的反应性低,因此可以提高循环寿命。
正极活性物质的一次粒径优选为100nm以上且1μm以下。一次粒径为100nm以上的正极活性物质在工业生产上的处理容易。一次粒径为1μm以下的正极活性物质可以使锂离子的固体内扩散顺畅地进行。
正极活性物质的比表面积优选为0.1m2/g以上且10m2/g以下。具有0.1m2/g以上的比表面积的正极活性物质可以充分地确保锂离子的嵌入、脱嵌位点。具有10m2/g以下的比表面积的正极活性物质在工业生产上易于处理且可以确保良好的充放电循环性能。
粘结剂是为了将正极活性物质和集电体粘结而配合的。粘结剂的例子包含聚四氟乙烯(polytetrafuloro ethylene;PTFE)、聚偏氟乙烯(polyvinylidene fluoride;PVdF)、氟系橡胶、聚丙烯酸化合物、酰亚胺化合物。可以将它们中的1种作为粘结剂使用,或者也可以组合2种以上作为粘结剂使用。
导电剂是为了提高集电性能且抑制正极活性物质与集电体的接触电阻而根据需要配合的。导电剂的例子包含乙炔黑、炭黑及石墨等碳质物。可以将它们中的1种作为导电剂使用,或者也可以组合2种以上作为导电剂使用。
正极层中,优选正极活性物质及粘结剂以分别为80质量%以上且98质量%以下、及2质量%以上且20质量%以下的比例进行配合。
粘结剂通过达到2质量%以上的量,可获得充分的电极强度。另外,通过达到20质量%以下,可以减少电极的绝缘体的配合量、减小内部电阻。
添加导电剂时,优选正极活性物质、粘结剂及导电剂以分别为77质量%以上且95质量%以下、2质量%以上且20质量%以下及3质量%以上且15质量%以下的比例进行配合。导电剂通过达到3质量%以上的量,可以发挥上述效果。另外,通过达到15质量%以下,可以减少高温保存下的正极导电剂表面上的非水电解质的分解。
集电体优选是铝箔或含有选自Mg、Ti、Zn、Ni、Cr、Mn、Fe、Cu及Si中的一种以上元素的铝合金箔。
铝箔或铝合金箔的厚度优选为5μm以上且20μm以下、更优选为15μm以下。铝箔的纯度优选为99质量%以上。铝箔或铝合金箔所含的铁、铜、镍及铬等过渡金属的含量优选为1质量%以下。
正极例如如下制作。首先,将正极活性物质、粘结剂及根据需要配合的导电剂混悬在适当的溶剂中,制备浆料。接着,将该浆料涂布在正极集电体上并进行干燥,形成正极层。之后,对形成于正极集电体上的正极层实施压制,从而制作正极。正极还可以通过将活性物质、粘结剂及根据需要配合的导电剂形成为料粒状而制成正极层、将其配置在集电体上来制作。
3)非水电解质
非水电解质例如可以是通过将电解质溶解在有机溶剂中而制备的液状非水电解质、或将液状电解质和高分子材料复合化而成的凝胶状非水电解质。
液状非水电解质优选是以0.5摩尔/L以上且2.5摩尔/L以下的浓度将电解质溶解在有机溶剂中而成的。
电解质的例子包含高氯酸锂(LiClO4)、六氟化磷酸锂(LiPF6)、四氟化硼酸锂(LiBF4)、六氟化砷锂(LiAsF6)、三氟甲磺酸锂(LiCF3SO3)及双三氟甲烷磺酰亚胺锂(LiN(CF3SO2)2)等锂盐及它们的混合物。电解质优选是即便在高电位下也难以氧化的物质,最优选LiPF6。
有机溶剂的例子包含碳酸亚丙酯(propylene carbonate;PC)、碳酸亚乙酯(ethylene carbonate;EC)、碳酸亚乙烯酯(vinylene carbonate;VC)等环状碳酸酯;碳酸二乙酯(diethyl carbonate;DEC)、碳酸二甲酯(dimethyl carbonate;DMC)、碳酸甲乙酯(methyl ethyl carbonate;MEC)等链状碳酸酯;四氢呋喃(tetrahydrofuran;THF)、2-甲基四氢呋喃(2-methyltetrahydrofuran;2-MeTHF)、二氧杂戊环(dioxolane;DOX)等环状醚;二甲氧基乙烷(dimethoxyethane;DME)、二乙氧基乙烷(diethoxyethane;DEE)等链状醚;γ-丁内酯(gamma-butyrolactone;GBL)、乙腈(acetonitrile;AN)及环丁砜(sulfolane;SL)。这些有机溶剂可单独使用或者作为混合溶剂使用。
高分子材料的例子包含聚偏氟乙烯(polyvinylidene fluoride;PVdF)、聚丙烯腈(polyacrylonitrile;PAN)、及聚环氧乙烷(polyetheylene oxide;PEO)。
或者作为非水电解质,还可以使用含有锂离子的常温熔融盐(离子性融体)、高分子固体电解质、无机固体电解质等。
常温熔融盐(离子性融体)是指由有机物阳离子和阴离子的组合构成的有机盐中在常温(15~25℃)下可作为液体存在的化合物。常温熔融盐包含单独地作为液体存在的常温熔融盐、通过与电解质混合而变成液体的常温熔融盐、通过溶解在有机溶剂中而变成液体的常温熔融盐。一般来说,非水电解质电池中使用的常温熔融盐的熔点为25℃以下。另外,有机物阳离子一般具有季铵骨架。
高分子固体电解质通过将电解质溶解在高分子材料中并进行固体化来制备。
无机固体电解质是具有锂离子传导性的固体物质。
4)隔膜
隔膜例如可以由含有聚乙烯、聚丙烯、纤维素或聚偏氟乙烯(polyvinylidene fluoride;PVdF)的多孔质膜或者合成树脂制无纺布形成。其中,由聚乙烯或聚丙烯形成的多孔质膜由于可以在一定温度下熔融、能够阻断电流,因而可以提高安全性。
5)外包装构件
作为外包装构件,可以使用例如厚度为0.5mm以下的层压膜或厚度1mm以下的金属制容器。层压膜的厚度更优选为0.2mm以下。金属制容器更优选厚度为0.5mm以下、进一步优选厚度为0.2mm以下。
外包装构件的形状并无特别限定,例如可以是扁平型(薄型)、方型、圆筒型、硬币型、纽扣型等。外包装构件还可以是对应电池尺寸、例如装载在便携电子设备等中的小型电池用外包装构件、装载在二轮~四轮的汽车等车辆中的大型电池用外包装构件。
作为层压膜,使用含有树脂层和介于这些树脂层之间的金属层的多层膜。金属层为了轻量化优选是铝箔或铝合金箔。树脂层例如可以使用聚丙烯(polypropylene;PP)、聚乙烯(polyethylene;PE)、尼龙、及聚对苯二甲酸乙二醇酯(polyethylene terephthalate;PET)等高分子材料。层压膜可以通过热熔融粘合进行密封而成形为外包装构件的形状。
金属制容器例如由铝或铝合金等制作。铝合金优选含有镁、锌、硅等元素中的一种以上的合金。合金中含有铁、铜、镍、铬等过渡金属时,其含量优选为1质量%以下。
6)正极端子及负极端子
正极端子例如可以由具有相对于锂的氧化还原电位的电位为3V以上且5V以下(vs.Li/Li+)范围内的电稳定性和导电性的材料形成。具体地说,正极端子由铝或含有Mg、Ti、Zn、Mn、Fe、Cu、Si等元素中的一种以上的铝合金形成。正极端子为了减小与正极集电体的接触电阻,优选由与正极集电体相同的材料形成。
负极端子可以由在上述负极活性物质的Li嵌入脱嵌电位下电化学稳定、且具有导电性的材料形成。具体地说,负极端子的材料可举出铜、镍、不锈钢或铝。负极端子为了减小与负极集电体的接触电阻,优选由与负极集电体相同的材料形成。
接着,参照附图具体地说明第2实施方式的非水电解质电池。
首先,参照图3及图4说明第2实施方式的一例非水电解质电池。
图3是第2实施方式的一例非水电解质电池的截面图。图4为图3的A部的放大截面图。
图3及图4所示的非水电解质电池10具备图3所示的袋状外包装构件2、图3及图4所示的电极组1、以及未图示出的非水电解质。将电极组1及非水电解质收纳在外包装构件2内。非水电解质保持在电极组1中。
袋状外包装构件2由含有2张树脂层和介于它们之间的金属层的层压膜构成。
如图3所示,电极组1是扁平状的卷绕电极组。扁平状的卷绕电极组1如图4所示,通过将自外侧开始依次层叠负极3、隔膜4、正极5、隔膜4而成的层叠物卷绕成漩涡状、并进行压制成型而形成。
负极3含有负极集电体3a和负极层3b。负极层3b中含有第1实施方式的电池用活性物质。最外壳的负极3如图4所示,具有仅在负极集电体3a的内表面侧的单面上形成有负极层3b的构成。其他的负极3在负极集电体3a的两面上形成有负极层3b。
正极5含有正极集电体5a和形成于其两面上的正极层5b。
如图3所示,在卷绕电极组1的外周端附近,将负极端子6连接在最外壳的负极3的负极集电体3a上,将正极端子7连接于内侧的正极5的正极集电体5a。这些负极端子6和正极端子7从袋状外包装构件2的开口部向外部延伸。
图3和图4所示的非水电解质电池10例如可以按照以下步骤制作。首先,制作电极组1。接着,将电极组1封入在袋状外包装构件2内。此时,负极端子6和正极端子7的各自的一端向外包装构件2的外侧伸出。接着,将外包装构件2的周边部分残留地进行热封。接着,从未热封的部分将例如液状非水电解质从袋状外包装构件2的开口部注入。最后,通过将开口部热封,将卷绕电极组1和液状非水电解质密封。
第2实施方式的非水电解质电池并非限于前述图3和图4所示例的非水电解质电池,还可以是例如图5和图6所示构成的电池。
图5是示意地表示第2实施方式的另一例的非水电解质二次电池的部分缺失立体图,图6是图5的B部的放大截面图。
图5及图6所示的非水电解质电池10具备图5及图6所示的电极组11、图5所示的外包装构件12和未图示出的非水电解质。将电极组11及非水电解质收纳在外包装构件12内。非水电解质保持在电极组11中。
外包装构件12由含有2张树脂层和介于它们之间的金属层的层压膜构成。
电极组11如图6所示那样为层叠型的电极组。层叠型电极组11如图6所示,具有将正极13和负极14在其间存在有隔膜15的情况下交替地层叠而成的结构。
电极组11含有多个正极13。多个正极13分别具有正极集电体13a和担载于正极集电体13a的两面上的正极层13b。另外,电极组11含有多个负极14。多个负极14分别具备负极集电体14a和担载于负极集电体14a的两面上的负极层14b。各负极14的负极集电体14a的一边自负极14突出。突出的负极集电体14a电连接于带状的负极端子16。带状的负极端子16的前端从外包装构件12向外部伸出。另外,虽未图示,但正极1的正极集电体13a的位于与负极集电体14a的突出边成相反侧的边自正极13突出。自正极13突出的正极集电体13a电连接于带状的正极端子17。带状的正极端子17的前端位于与负极端子16相反的一侧,且从外包装构件12的边向外部伸出。
第2实施方式的非水电解质电池含有第1实施方式的电池用活性物质。因此,第2实施方式的非水电解质电池可以显示高的能量密度,显示优异的快速充放电性能和长寿命性能,且可以容易地进行电压管理。
(第3实施方式)
根据第3实施方式,提供电池包。该电池包具备第2实施方式的非水电解质电池。
第3实施方式的电池包可以具有1个或多个之前说明的第2实施方式的非水电解质电池(单电池)。含有多个单电池时,将各单电池电串联或电并联地连接、配置。或者,第3实施方式的电池包可以含有的多个非水电解质电池还可以相互间电串联或电并联地连接而构成组电池。第3实施方式的电池包还可以含有多个组电池。
第3实施方式的电池包可以进一步具备保护电路。保护电路对非水电解质电池的充放电进行控制。或者,还可以将作为电源使用电池包的装置(例如电子设备、汽车等)中所含的电路作为电池包的保护电路进行使用。
另外,第3实施方式的电池包还可以进一步具备通电用的外部端子。通电用的外部端子是用于将来自非水电解质电池的电流输出至外部和/或用于将电流输入至非水电解质电池中的构件。换而言之,作为电源使用电池包时,电流通过通电用的外部端子供给至外部。另外,对电池包进行充电时,充电电流(包含汽车等的动力的再生能量)通过通电用的外部端子供给至电池包。
接着,一边参照附图一边说明第3实施方式的一例电池包。
图7是第3实施方式的一例电池包的分解立体图。图8是表示图7的电池包的电路的模块图。
图7及图8所示的电池包20具备多个单电池21。多个单电池21是一边参照图3及图4一边说明过的扁平型非水电解质电池10。
将多个单电池21按照延伸至外部的负极端子6及正极端子7统一为相同方向的方式进行层叠,利用胶带22进行捆扎,从而构成组电池23。这些单电池21如图8所示,电串联地连接。
印刷布线基板24面向负极端子6及正极端子7伸出的组电池23的侧面进行配置。印刷布线基板24上如图8所示,搭载有热敏电阻25、保护电路26及作为通电用外部端子的向外部设备的通电用端子27。此外,在印刷布线基板24面向组电池23的面上,为了避免与组电池23的布线不需要的连接,安装有绝缘板(未图示)。
正极侧引线28连接于位于组电池23最下层的正极端子7,其前端插入在印刷布线基板24的正极侧插孔29中进行电连接。负极侧引线30连接于位于组电池23最上层的负极端子6,其前端插入在印刷布线基板24的负极侧插孔31中进行电连接。这些插孔29和31通过形成于印刷布线基板24的布线32和33,连接于保护电路26。
热敏电阻25对单电池21的温度进行检测,将其检测信号发送至保护电路26。保护电路26可以在规定条件下阻断保护电路26与作为通电用外部端子的向外部设备的通电用端子27之间的正极侧布线34a及负极侧布线34b。规定条件是指例如热敏电阻25检测出的检测温度达到规定温度以上的时刻。另外,规定条件的另一例是指检测到单电池21的过充电、过放电及过电流等的时刻。该过充电等的检测对各个单电池21或组电池23整体进行。检测各个单电池21时,可以检测电池电压,也可检测正极电位或负极电位。为后者时,在各个单电池21中插入作为参比电极使用的锂电极。为图7及图8所示的电池包20时,将用于检测电压的布线35连接于各个单电池21,通过这些布线35,将检测信号发送至保护电路26。
在除了正极端子7和负极端子6突出的侧面之外的组电池23的三个侧面上,分别配置有由橡胶或树脂构成的保护片材36。
将组电池23与各保护片材36及印刷布线基板24一起收纳在收纳容器37内。即,在收纳容器37的长边方向的两个内侧面和短边方向的内侧面上分别配置保护片材36,在短边方向的相反侧的内侧面上配置印刷布线基板24。组电池23位于被保护片材36和印刷布线基板24所包围的空间内。将盖38安装在收纳容器37的上面。
另外,组电池23的固定中还可代替胶带22而使用热收缩带。此时,在组电池的两侧面配置保护片材,缠绕热收缩带之后,使热收缩带发生热收缩,从而捆扎组电池。
图7及图8中示出了串联连接单电池21的形态,但为了增大电池容量也可并联地连接。或者,还可以将串联连接和并联连接组合。还可以将组装好的电池包进一步串联连接或并联连接。
另外,图7及图8所示的电池包具备多个单电池21,但第3实施方式的电池包也可具备1个单电池21。
另外,第3实施方式的电池包的样式根据用途可适当变更。第3实施方式的电池包优选用于要求在取出大电流时循环性能优异的用途中。具体地说,作为数码相机的电源、或例如二轮~四轮的混合电动汽车、二轮~四轮的电动汽车及电动助力自行车等车辆的车载用电池使用。特别优选作为搭载于车辆的车载用电池进行使用。
搭载有第3实施方式的电池包的汽车等车辆中,电池包例如对车辆的动力的再生能量进行回收。作为车辆的例子,例如可举出二轮~四轮的混合电动汽车、二轮~四轮的电动汽车及电动助力自行车及电车。
图9表示具备第3实施方式的一例电池包的一例汽车。
图9所示的汽车41在车体前方的机舱内搭载有第3实施方式的一例电池包42。汽车中的电池包的搭载位置并非限定于机舱。例如,电池包还可以搭载于汽车的车体后方或座席下面。
第3实施方式的电池包具备第2实施方式的非水电解质电池。因此,第3实施方式的电池包可以显示高能量密度、显示优异的快速充放电性能和长寿命性能、且可以容易地进行电压管理。
[实施例]
以下基于实施例更为详细地说明上述实施方式。此外,所合成的单斜晶型复合氧化物的结晶相的鉴定及结晶结构的推测通过使用了Cu-Kα射线的粉末X射线衍射法来进行。另外,利用ICP法对产物的组成进行分析,确认到获得了目标物。
(合成)
<实施例1~12>
实施例1~12中,按照第1实施方式的制造方法的步骤合成实施例1~12的产物。
具体地说,如下合成。首先,利用固相反应法合成起始化合物。接着,在酸性溶液中对起始化合物所含的碱金属的一部分进行质子交换,获得前体。通过对所得前体进行脱水热处理,合成具有最终目标组成的化合物。将实施例1~12的各自的最终目标组成、起始化合物的目标组成示于以下表1中。
首先,通过固相反应合成表1所记载的起始化合物。作为起始原料,准备以下表1所示的市售氧化物或碳酸盐试剂(M1源、Ti源、M2源),使得它们满足该表1所示的摩尔比且总重量达到50g。接着,对如上准备的起始原料进行混合,将该混合物投入到球磨机用玛瑙制容器(容积为300ml)中。在该容器中以1:1的数量投入直径分别为10mm及5mm的玛瑙制小球使其达到容器容积的1/3。之后,在该容器中投入乙醇50ml,以120rpm湿式混合60分钟,获得混合物。通过这种湿式混合,原料被均匀地混合,因此可以获得目标结晶相的单相。
接着,将如此获得的混合物放入到电炉中,按照以下的步骤供至加热处理。
首先,在650℃的温度下用6小时的时间在大气气氛中进行预烧成。接着,将进行预烧成所获得的粉末从炉中取出,进行再粉碎,进一步进行混合。
对如此获得的混合物,继续在950℃的温度下花6个小时的时间进行第1次的烧成。烧成之后,将烧成粉从炉中取出,对烧成粉进行再混合。
接着,将进行了再混合的烧成粉放在炉内,在大气气氛中、950℃的温度下供至花费6小时的第2次的烧成。将第2次烧成后、即950℃的温度下共计烧成12小时所获得的粉末粉碎,作为实施例1~12的起始化合物。
接着,按照每1L溶液的投入量达到1g的方式,将所得起始化合物粉末投入1M盐酸水溶液中。如此,每1小时对试样进行采集,利用ICP法对产物的组成进行分析,与此同时进行质子交换,从而获得具有目标组成HM12-0.5yTi5-0.5zM21+0.5zO14·H2O的前体。
在900℃~1100℃之间对该前体进行加热,将结晶水完全地脱水,从而获得实施例1~10及12的最终目标组成的产物。
另一方面,在合成实施例11的产物时,将与实施例1同样获得的产物投入到1M氢氧化锂水溶液中,使得投入量达到每1L溶剂为1g,在60℃下搅拌1小时,对锂离子进行化学嵌入,从而制成实施例11的最终目标组成的产物。
<比较例1、2>
比较例1及2中,为了获得目标化合物,作为起始原料准备表1所示的市售氧化物或碳酸盐试剂(Li源、M1源、Ti源),使得它们满足该表1所示的摩尔比且总重量达到50g。接着,对如上准备的起始原料进行混合,将该混合物投入到球磨机用玛瑙制容器(容积为300ml)中。在该容器中以1:1的数量投入直径分别为10mm及5mm的玛瑙制小球,使其达到容器容积的1/3。之后,在该容器中投入乙醇50ml,以120rpm湿式混合60分钟,获得混合物。通过这种湿式混合,原料被均匀地混合,因此可以获得目标结晶相的单相。
接着,将如此获得的混合物放入到电炉中,按照以下的步骤供至加热处理。比较例1及2中,通过一般的固相反应法(1次烧成)来进行合成。在900℃的温度下连续12小时在大气气氛中进行烧成。将如此获得的混合物取出,进行粉碎,由此合成了比较例1及2的产物。
(产物组成的确认)
利用之前说明的ICP法分析实施例1~12的产物及比较例1和2的组成。将其结果示于以下的表2中。
表2
由此结果可知,获得了目标元素比的化合物。
(粉末X射线衍射测定)
对于实施例1~12的产物及比较例1和2的产物,按照之前说明的步骤进行粉末X射线衍射测定。使产物的粒度分布统一,利用Rietveld法解析上述粉末X射线衍射法的结果,结果可知,实施例1~12中获得的产物是具有图2所示空间群C2/m或Cm的对称性的单斜晶型化合物。另外,为了研究各个结晶中是否含有结构水(结晶水),在室温~600℃的范围内进行示差热重量测定。结果是,由于未产生因脱水导致的重量变化,因此确认了是不含结晶水的。将各个产物的空间群、晶格常数、单位晶格体积等解析结果一并记载于以下的表3中。
表3
(电化学测定)
对上述实施例及比较例中获得的各产物,按照以下的步骤进行电化学测定。另外,以下对使用了实施例1的产物的例子进行说明,但对于其他的实施例及比较例的各产物,也与实施例1的产物同样地进行电化学测定。
首先,对实施例1的产物粒子进行粉碎,使其平均粒径达到5μm以下,获得粉碎物。接着,以相对于该活性物质为10质量份的比例混合作为导电剂的乙炔黑,获得混合物。接着,将该混合物分散在NMP(N-甲基-2-吡咯烷酮)中,获得分散液。在该分散液中,以相对于实施例1的产物为10质量份的比例混合作为粘结剂的聚偏氟乙烯(PVdF),制作电极浆料。使用刮板将该浆料涂布在由铝箔构成的集电体上。对其在真空下、130℃下干燥12小时之后,按照电极层(除了集电体以外)的密度达到2.2g/cm3的方式进行压制,获得电极。
使用该电极、作为对电极的金属锂箔和非水电解质,制作实施例1的电化学测定单电池。作为非水电解质,使用以1M的浓度将六氟化磷酸锂(LiPF6)溶解在碳酸亚乙酯及碳酸二乙酯的混合溶剂(体积比1:1)中而成的溶液。
对于实施例1的电化学测定单电池,在室温下进行充放电试验。充放电试验是在以金属锂电极基准计为1.0V~3.0V的电位范围内、使充放电电流值为0.2C(时间放电率)来进行。将该试验中的最初的Li嵌入量作为初次充电容量、将Li脱嵌量作为初次放电容量。此时,将初次放电容量除以初次充电容量再乘以100所得的值(初次放电容量/初次充电容量×100)作为初次充放电效率。
接着,为了确认实施例1的产物能够稳定地进行充放电,对实施例1的电化学测定单电池反复进行200个循环的充放电。1个循环是1次的充电及1次的放电。充放电是在以金属锂电极基准计为1.0V~3.0V的电位范围内、使电流值为1C(时间放电率)、在室温下进行。
为了确认200个循环后的放电容量维持率,使实施例1的电化学测定单电池再次在0.2C(时间放电率)下进行充放电,将初次放电容量设为100%,计算容量维持率。
另外,对于实施例1的电化学测定单电池,分别测定0.2C放电容量和20.0C放电容量。将通过测定获得的20.0C放电容量除以同样通过测定获得的0.2C容量,从而计算作为速率性能指标的放电速率。将它们的结果示于表4。另外,表4中示出电化学测定单电池处于SOC50%的状态时的负极电位。
表4
由这些结果可知,实施例1~12的电极容量较比较例1及2的更高。因此,实施例1~12的产物可以提供电极容量高的电池。
另外,实施例1~12的速率性能较比较例1的更高。另一方面,200个循环后的容量维持率也较比较例2的高。如此,在各个比较例中产生了速率性能高则循环性能低,循环性能高则速率性能低的所谓二律背反。而与此相对,实施例1~12的速率性能和循环性能这两者均优异。因此可知,就实施方式的组成而言,兼顾了锂离子的快速移动和稳定的骨架结构。
如这些结果所示可知,通过使用实施方式的化合物,可以提供兼顾了高的充放电容量和速率性能及寿命性能的电池。
根据以上的实施方式及实施例,可提供含有复合氧化物的活性物质。该复合氧化物以通式LixM14-yTi10-zM22+zO27+δ表示。这里,M1含有选自Na、K、Cs中的至少1种。M2含有选自Zr、Sn、V、Nb、Ta、Mo、W、Fe、Co、Mn、Ni、Al中的至少1种。x满足0≤x<18。y满足0<y<4。z满足0<z<4。δ满足-0.3≤δ≤0.3。通过使用该活性物质,可以实现具有高能量密度、电池电压的设计容易、快速充放电性能和寿命性能均优异的非水电解质电池。
说明了本发明的数个实施方式,但这些实施方式只是作为例子示出的,并非是为了限定发明的范围。这些新的实施方式可以以其他各种方式进行实施,在不偏离发明主旨的范围内,可以进行各种省略、替换、变更。这些实施方式及其变形包含于发明的范围或主旨之内,同时包含在权利要求书所记载的发明及其均等的范围内。
- 还没有人留言评论。精彩留言会获得点赞!