本发明涉及有机光电技术领域,具体涉及一种包含芴衍生物的有机电致发光器件。
背景技术:
数字通讯时代不断进步,需要性能更好的新一代平面显示器来满足生活需求。平面显示的未来趋势是能够在轻巧的载体上传输更多的信息和更清晰的图像。其中有机发光二极管(organiclightemittingdiode,oled作为新一代的平面显示器,引起了国内外的广泛关注,原因是oled显示器具有自发光、视角广、反应时间短、发光效率高、色域广、工作电压低、面板薄、尺寸设计灵活、形状设计灵活及制备方法简单等特性。
一般的有机发光器件是由阴极、阳极及阴极和阳极之间的有机功能层构成的。器件最早的结构就是在阴极和阳极之间加入一个有机层,随着科学的不断进步,器件结构不断优化,目前有机发光器件的组成包括透明ito阳极、空穴注入层(hil)、空穴传输层(htl)、发光层(el)、空穴阻挡层(hbl)、电子传输层(etl)、电子注入层(eil)、阴极等。通过引入空穴注入层和电子注入层后,使得空穴传输层和电子传输层与阳极和阴极之间有良好的附着性,使阳极和阴极的载流子更容易地注入有机功能层,从而提高了器件效率。
有机电致发光器件主要应用在面板和照明领域,这些都要求器件满足发光效率高、驱动电压低、使用寿命长等特点。所以oled研究的主要内容为提高器件的效率、降低驱动电压、延长使用寿命等,一方面优化器件的制作工艺,通过增加多种功能辅助层、多采用掺杂的方式提高器件的效率;另一方面寻找性能优良的有机电致发光材料,材料性能的好坏直接影响器件的效率、寿命及稳定性。
现阶段来说,应用于有机发光器件中的材料种类较为局限,导致有机发光器件仍旧存在许多亟待解决的问题,目前常用于空穴传输层的材料为三芳胺、联苯胺化合物,其中,npb、tapc为最常使用的空穴传输层材料,tapc的空穴迁移率可达到1.0×10-2cm2v-1s-1,且具有较高的三线态能级,但其玻璃转化温度仅为89℃,在使用过程中易结晶,严重影响器件的稳定性;npb的空穴迁移率为8.8×10-4cm2v-1s-1,玻璃转化温度提升到99℃,但其三线态能级仅为2.29ev,不能有效的避免激子向空穴传输层的逸散,导致器件效率低以及器件稳定性的下降等问题。
随着市场需要日益提高,工业技术不断进步,对于有机发光器件的要求也会越来越高,相应的,对于有机发光器件材料的选择也会更加严苛,目前研究较高空穴迁移率、高的玻璃转化温度、高的三线态能级的空穴传输材料,成为亟待解决的问题。
技术实现要素:
技术问题
为了解决现阶段由于空穴传输材料玻璃转化温度低、三线态能级较低导致的器件稳定性较差、寿命短等问题,本发明提供一种有机电致发光器件,该器件空穴传输层包含的本发明化合物具有较好的空穴传输能力、高玻璃转化温度以及较高的三线态能级,其作为空穴传输材料时,能有效改善结晶问题、同时能够有效阻挡激子向阳极侧逸散,从而能够提高器件的稳定性、提高器件的发光效率,延长器件的使用寿命。
技术解决方案
本发明提供了一种有机电致发光器件,该有机电致发光器件包括:基板;阳极,该阳极位于所述基板之上;有机层,该有机层位于所述阳极之上;阴极,该阴极位于所述有机层之上;
其中,所述有机层包括空穴传输层,所述空穴传输层包含式ⅰ化合物:
其中,r1在每种情况下相同或不同的选自氢、氘、卤素原子、氰基、取代或未取代的c1~c12的烷基、取代或未取代的c6~c30的芳基、取代或未取代的c3~c30的杂芳基中的任意一种;
e存在或不存在,出现时独立的选自取代或未取代的苯基;
a选自0、1、2、3、4或5,m、n独立的选自0或1,且m+n=1;
k选自0或1,k为0时,x不存在;k为1时,x选自单键;
a选自式ⅱ或式ⅲ所示基团中的任意一种:
l1选自单键、取代或未取代的c6~c30的亚芳基、取代或未取代的c3~c30的亚杂芳基中的任意一种;
ar1选自氢、氘、卤素原子、氰基、取代或未取代的c1~c12的烷基、取代或未取代的c6~c30的芳基、取代或未取代的c3~c30的杂芳基中的任意一种;
在式ⅱ中,ar2选自取代或未取代的c6~c30的芳基、取代或未取代的c3~c30的杂芳基中的任意一种;
在式ⅲ中,m选自式ⅲ-1所示基团:
“*”表示与咔唑环的键合位点;
r2、r3独立的选自氢、取代或未取代的c1~c12的烷基、取代或未取代的c6~c30的芳基、取代或未取代的c3~c30杂芳基中的任意一种;
ar3选自氢、氘、取代或未取代的c1~c12的烷基、取代或未取代的c6~c30的芳基中的任意一种。
有益效果
本发明化合物在结构中引入了咔唑或茚并咔唑及其衍生基团,由于咔唑或茚并咔唑类基团本身具有较大的刚性,能有效提高玻璃转化温度;本发明化合物本身具有不对称性,与此同时,在结构中引入烷基等结构,破坏了分子的结晶,有效避免了分子间的聚集作用,从而改变了分子的成膜性以及薄膜的热稳定性,将其用作有机电致发光器件的空穴传输层时,能够明显提高器件的稳定性,延长器件的使用寿命。
另一方面,本发明化合物具有较大的共轭体系,使得电荷更加分散,能有效提高材料的稳定性;在芴衍生物结构上引入烷基等取代基团以及9,9’-螺二芴衍生物具有非平面结构,能够有效提高激子利用率,降低器件的驱动电压,从而提高器件的寿命。
同时,本发明化合物具有合适的homo值,并且具有较高的三线态能级,将其应用于有机电致发光器件的第二空穴传输层中时,可有效抑制激子向阳极侧逸散,提高激子在发光层中的复合效率,进而提高器件的发光效率。本发明所述的包含本发明化合物的有机电致发光器件,具有良好的应用效果,具备良好的产业化前景。
附图说明
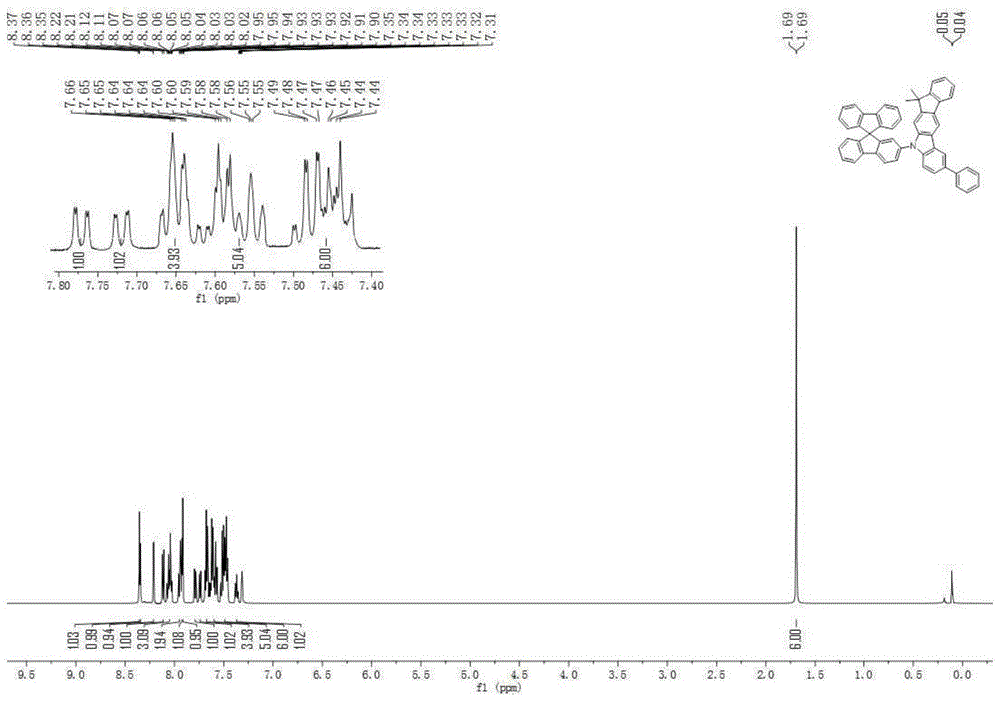
图1为本发明化合物1的1hnmr图;
图2为本发明化合物45的1hnmr图;
图3为本发明化合物112的1hnmr图;
图4为本发明化合物126的1hnmr图;
图5为本发明化合物141的1hnmr图;
图6为本发明化合物146的1hnmr图;
图7为本发明化合物234的1hnmr图。
具体实施方式
为了进一步理解本发明,下面结合实施例对本发明优选实施方案进行描述。然而,这些实施例为示例性且不限制本发明。
定义
在本说明书中,“*”意指与另一取代基连接的部分。
本发明所述的卤素原子,实例可包括氟、氯、溴和碘。
本发明所述的烷基是指烷烃分子中去掉一个氢原子而成的烃基,其可以为直链烷基、支链烷基、环烷基,优选具有1至12个碳原子,更优选1至8个碳原子,特别优选1至6个碳原子,实例可包括甲基、乙基、正丙基、异丙基、正丁基、异丁基、叔丁基、仲丁基、正戊基、异戊基、新戊基、叔戊基、环戊基、正己基、环己基等,但不限于此。
本发明所述的芳基是指芳烃分子的芳核碳上去掉一个氢原子后,剩下一价基团的总称,其可以为单环芳基、多环芳基或稠环芳基,优选具有6至30个碳原子,更优选6至18个碳原子,特别优选6至14个碳原子,最优选6至12个碳原子,实例可包括苯基、联苯基、三联苯基、萘基、蒽基、菲基、三亚苯基、芘基、芴基、螺芴基、
本发明所述的杂芳基是指由碳和杂原子构成的芳杂环的核碳上去掉一个氢原子,剩下一价基团的总称,所述杂原子包括但不限于氧、硫、氮原子,其可以为单环杂芳基、多环杂芳基或稠环杂芳基,优选具有2至30个碳原子,更优选2至20个碳原子,特别优选3至12个碳原子,最优选3至8个碳原子,实例可包括噻吩基、吡咯基、呋喃基、咪唑基、噻唑基、噁唑基、噁二唑基、噻二唑基、三唑基、吡啶基、吡嗪基、哒嗪基、嘧啶基、三嗪基、喹啉基、异喹啉基、喹喔啉基、喹唑啉基、吩噻嗪基、吩噁嗪基、吲哚基、苯并噻吩基、苯并呋喃基、苯并咪唑基、异苯并噻吩基、异苯并呋喃基、二苯并呋喃基、二苯并噻吩基、咔唑基等,但不限于此。
本发明所述的亚芳基是指芳烃分子的芳核碳上去掉两个氢原子后,剩下二价基团的总称,其可以为单环亚芳基、多环亚芳基或稠环亚芳基,优选具有6至30个碳原子,更优选6至18个碳原子,特别优选6至14个碳原子,最优选6至12个碳原子,实例可包括亚苯基、亚联苯基、亚三联苯基、亚萘基、亚蒽基、亚菲基、亚三亚苯基、亚芘基、亚芴基、亚螺芴基、亚
本发明所述的亚杂芳基是由碳和杂原子构成的芳杂环的核碳上去掉两个氢原子,剩下二价基团的总称,所述杂原子包括但不限于氧、硫、氮原子,其可以为单环亚杂芳基、多环亚杂芳基或稠环亚杂芳基,优选具有2至30个碳原子,更优选2至20个碳原子,特别优选3至12个碳原子,最优选3至8个碳原子,实施例可包括亚噻吩基、亚吡咯基、亚呋喃基、亚咪唑基、亚噻唑基、亚噁唑基、亚噁二唑基、亚噻二唑基、亚三唑基、亚吡啶基、亚吡嗪基、亚哒嗪基、亚嘧啶基、亚喹啉基、亚异喹啉基、亚喹喔啉基、亚喹唑啉基、亚吩噻嗪基、亚吩噁嗪基、亚吲哚基、亚苯并噻吩基、亚苯并呋喃基、亚苯并咪唑基、亚异苯并噻吩基、亚异苯并呋喃基、亚二苯并呋喃基、亚二苯并噻吩基、亚咔唑基等,但不限于此。
本发明所述的“取代或未取代”意指未取代的或被一个或多个以下基团取代的:氘、卤素原子、氨基、氰基、硝基或c1~c30的烷基、c2~c30的烯基、c1~c30的烷氧基、c3~c20的环烷基、c3~c20的杂环烷基、c6~c30的芳基及c2~c30的杂芳基,优选氘、卤素原子、氰基、硝基、c1~c12的烷基、c6~c30的芳基、c2~c30的杂芳基。具体实例可包括氘、氟、氯、溴、碘、氰基、硝基、甲基、乙基、异丙基、叔丁基、苯基、萘基、蒽基、菲基、苯并菲基、芘基、
本发明提供了一种有机电致发光器件,该有机电致发光器件包括:基板;阳极,该阳极位于所述基板之上;有机层,该有机层位于所述阳极之上,阴极,该阴极位于所述有机层之上;
其中,所述有机层包括空穴传输层,所述空穴传输层包含式ⅰ化合物:
其中,r1在每种情况下相同或不同的选自氢、氘、卤素原子、氰基、取代或未取代的c1~c12的烷基、取代或未取代的c6~c30的芳基、取代或未取代的c3~c30的杂芳基中的任意一种;
e存在或不存在,出现时独立的选自取代或未取代的苯基;a选自0、1、2、3、4或5,m、n独立的选自0或1,且m+n=1;k选自0或1,k为0时,x不存在;k为1时,x选自单键;
a选自式ⅱ或式ⅲ所示基团中的任意一种:
l1选自单键、取代或未取代的c6~c30的亚芳基、取代或未取代的c3~c30的亚杂芳基中的任意一种;
ar1选自氢、氘、卤素原子、氰基、取代或未取代的c1~c12的烷基、取代或未取代的c6~c30的芳基、取代或未取代的c3~c30的杂芳基中的任意一种;
在式ⅱ中,ar2选自取代或未取代的c6~c30的芳基、取代或未取代的c3~c30的杂芳基中的任意一种;
在式ⅲ中,m选自式ⅲ-1所示基团:
“*”表示与咔唑环的键合位点;r2、r3独立的选自氢、氘、取代或未取代的c1~c12的烷基、取代或未取代的c6~c30的芳基、取代或未取代的c3~c30杂芳基中的任意一种;ar3选自氢、氘、取代或未取代的c1~c12的烷基、取代或未取代的c6~c30的芳基中的任意一种。
优选的,所述式ⅰ化合物选自式ⅰ-1~式ⅰ-13中的任意一种:
再优选的,所述式ⅰ化合物选自如下基团中的任意一种:
更优选的,所述式ⅰ化合物选自如下基团中的任意一种:
优选的,所述r1在每种情况下相同或不同的选自氢、氘、氰基、甲基、乙基、异丙基、叔丁基中的任意一种。
优选的,所述a选自式a-1~式a-7所示基团中的任意一种:
优选的,所述ar1选自取代或未取代的苯基、取代或未取代的萘基、取代或未取代的联苯基、取代或未取代的9,9-二甲基芴基、取代或未取代的9,9-二苯基芴基、取代或未取代的9,9’-螺二芴基中的任意一种,其中所述“取代”的基团选自氘原子、氰基、甲基、乙基、正丙基、异丙基、叔丁基中的任意一种。
再优选的,所述a选自下列基团中的任意一种:
ar1、ar2、ar3、l1定义与上述限定相同。
优选的,所述ar1选自下列基团中的任意一种:
优选的,所述ar2选自取代或未取代的苯基、取代或未取代的萘基、取代或未取代的联苯基、取代或未取代的蒽基、取代或未取代的菲基、取代或未取代的二苯并呋喃基、取代或未取代的二苯并噻吩基、取代或未取代的9,9-二甲基芴基、取代或未取代的9,9-二苯基芴基、取代或未取代的9,9’-螺二芴基中的任意一种。
再优选的,所述ar2选自下列基团中的任意一种:
优选的,所述l1选自单键或下列基团中的任意一种:
优选的,所述r2、r3独立的选自氢、甲基、取代或未取代的苯基中的任意一种。
最优选的,所述式ⅰ化合物选自下列所示结构中的任意一种:
以上列举了本发明所述的有机化合物的一些具体结构形式,但本发明并不局限于所列这些化学结构,凡是以化学式ⅰ所示结构为基础,取代基为如上所限定的基团都应包含在内。
本发明所述有机化合物的制备方法可通过如下合成路线制备得到,但本发明不限于此:
1、本发明化合物的合成
2、中间体s5/s5’的合成
r1~r3、ar1~ar3、l1、e、a定义与上述限定相同;xa、xb、xc、xd分别为br、cl、i中的任意一种。
进一步的,所述的有机层还包含空穴注入层,所述空穴注入层包含式ⅳ表示的轴烯化合物,
其中,r2、r3、r4独立的选自取代的c6~c30的芳基、取代的c3~c30的杂芳基中的任意一种;
取代的基团选自氟、氯、溴、碘、氰基、三氟甲基或硝基中的任意一种。
优选的,所述式ⅳ表示的轴烯化合物选自下列所示结构中的任意一种:
本发明的有机电致发光器件的有机层可以由单层结构形成,也可以由层叠以上的有机层的多层结构形成。例如,本说明书的有机电致发光器件可以具有包含发光层、空穴注入层、空穴传输层、空穴阻挡层、电子阻挡层、电子传输层、电子注入层作为有机层的结构,同时,所述的各个有机层还可包含一层或多层结构,例如,所述空穴传输层包含第一空穴传输层以及第二空穴传输层。但是,有机电致发光器件的结构并不仅限于此,可以包含更少的有机层。
例如,根据本发明,优选如下器件层叠结构,但不限于此:
(1)阳极/空穴注入层/空穴传输层/发光层/阴极
(2)阳极/空穴注入层/空穴传输层/发光层/电子传输层/阴极
(3)阳极/空穴注入层/空穴传输层/发光层/电子传输层/电子注入层/阴极
(4)阳极/空穴注入层/空穴传输层/电子阻挡层/发光层/电子传输层/电子注入层/阴极
(5)阳极/空穴注入层/空穴传输层/发光层/空穴阻挡层/电子传输层/电子注入层/阴极
(6)阳极/空穴注入层/空穴传输层/电子阻挡层/发光层/空穴阻挡层/电子传输层/电子注入层/阴极
(7)阳极/空穴注入层/第一空穴传输层/第二空穴传输层/发光层/电子传输层/电子注入层/阴极
(8)阳极/空穴注入层/第一空穴传输层/第二空穴传输层/发光层/空穴阻挡层/电子传输层/电子注入层/阴极
根据本说明书的一实施方式,所述的有机层包含空穴传输层,所述空穴传输层为一层结构,包含式ⅰ化合物;
根据本说明书的一实施方式,所述有机层包含空穴传输层,所述空穴传输层为两层结构,包含第一空穴传输层及第二空穴传输层,第二空穴传输层包含式ⅰ化合物。关于本发明所述的有机电致发光器件,除了所述空穴传输层包含式ⅰ化合物外,其它层均可以使用现有技术中用于所述层的任何材料。
作为本发明的基板材料,可选用典型的有机发光装置中使用的任何基板。可以是玻璃或透明塑料基板,也可以是不透明材料如硅或不锈钢的基板,还可以是柔性pi膜。不同基板具有不同的机械强度、热稳定性、透明性、表面光滑度、防水性,根据基板的性质不同,使用方向不同。
作为本发明的阳极材料,优选具有高功函数的材料,以便容易地将空穴注入有机层。可用于本发明的阳极材料包括:金属,例如钒、铬、铜、锌或金,或者它们的合金;金属氧化物,例如氧化锌、氧化铟、氧化铟锡(ito)或氧化铟锌(izo);金属/氧化物组合物,例如zno:al或sno2:sb;以及导电聚合物,例如聚吡咯、聚3,4-乙烯二氧噻吩(pedot)、聚苯胺等,但不限于此。
作为本发明的空穴注入材料,优选具备如下能力的物质:良好的传输空穴的能力,具有来自阳极的空穴注入效果,可防止发光层中所产生的激子向电子注入层或电子注入材料迁移,而且薄膜形成能力优异,homo介于阳极物质的功函数与周围有机层的homo之间。可用于本发明的空穴传输材料除了本发明提供的式ⅳ化合物外,还可包括:咔唑衍生物、三芳胺衍生物、联苯二胺衍生物、芴衍生物、酞菁类化合物、六腈六氮杂苯并菲类化合物、喹吖啶酮类化合物、苝衍生物、蒽醌类化合物、f4-tcnq、聚苯胺、聚噻吩、聚乙烯咔唑等,但不限于此。
作为本发明的空穴传输材料,优选具备良好空穴迁移率的物质,同时,需具备合适的能级,可保证空穴有效地注入。可用于本发明的空穴传输材料除了本发明提供的式ⅰ化合物外,还可包括:咔唑衍生物、三芳胺衍生物、联苯二胺衍生物、芴衍生物、酞菁类化合物、六腈六氮杂苯并菲类化合物、喹吖啶酮类化合物、苝衍生物、蒽醌类化合物、f4-tcnq、聚苯胺、聚噻吩、聚乙烯咔唑等,但不限于此。
作为本发明的电子阻挡材料,优选三线态(t1)能级高于发光层中主体材料的t1能级的物质,起到阻挡发光层材料能量损失的作用;还需具备良好的空穴迁移率,利于空穴传输;同时,需要该材料具备合适的homo能级,能够有效阻挡电子。可作为本发明的电子阻挡材料包括三芳胺衍生物、芴衍生物、呋喃衍生物、咔唑衍生物等,但不限于此。
作为本发明的发光层材料,可以包含主体材料(也称基质材料)和掺杂材料(也称客体材料),发光层材料可包含多个主体材料和多个掺杂材料。发光层可为单一的发光层,也可为横向或纵向叠加在一起的复合发光层。对于掺杂材料的种类选择,可以为荧光材料,也可以为磷光材料,与荧光掺杂材料组合的主体材料称为荧光主体材料,与磷光掺杂材料组合的主体材料称为磷光主体材料。应予以说明,荧光主体材料和磷光主体材料不仅仅由分子结构进行区分,所谓荧光主体材料是指形成含有荧光掺杂材料的荧光发光层的材料,但不并意味着不能将其应用于磷光发光层中,磷光主体材料同理。对于掺杂材料的用量选择,优选0.1质量%~70%质量,更优选为0.1~30质量%、进一步优选为1~30质量%、更进一步优选为1~20质量%、特别优选为1~10质量%。
可用于本发明的荧光掺杂材料可包括:稠合多环芳族衍生物、苯乙烯基胺衍生物、稠环胺衍生物、含硼化合物、吡咯衍生物、吲哚衍生物、咔唑衍生物等,但不限于此。作为蓝色系荧光掺杂材料,可举出例如芘衍生物、苯乙烯基胺衍生物、
可用于本发明的磷光掺杂材料可包括:重金属配合物、磷光发光性的稀土类金属配合物等,但不限于此。重金属配合物可举出例如铱配合物、铂配合物、锇配合物等;稀土类金属配合物可举出例如铽络合物、铕络合物等,但不限于此。
可用于本发明的主体材料可包括:金属配合物、二苯乙烯基亚芳基衍生物、均二苯乙烯衍生物、三芳基胺衍生物、咔唑衍生物、蒽衍生物、菲衍生物、芘衍生物、
作为本发明的空穴阻挡材料,优选三线态(t1)能级高于发光层中主体材料的t1能级的物质,起到阻挡发光层材料能量损失的作用;还需具备良好的电子迁移率,利于电子传输;同时,需要该材料具备合适的homo能级,能够有效阻挡空穴。可作为本发明的空穴阻挡材料包括噁二唑衍生物、三唑衍生物、喹啉衍生物、二氮杂菲类化合物、蒽醌类化合物、蒽酮类化合物、氮杂苯衍生物、咪唑衍生物等、但不限于此。
作为本发明的电子传输材料,优选具备良好电子迁移率的物质,同时具备合适的homo和lumo能级。可作为本发明的电子传输材料包括金属螯合物、氧杂噁唑衍生物、噻唑衍生物、二氮唑衍生物、氮杂苯衍生物、二氮蒽衍生物、含硅杂环类化合物、含硼杂环类化合物、氰基类化合物、喹啉衍生物、菲罗啉衍生物、苯并咪唑衍生物等,但不限于此。
作为本发明的电子注入材料,优选具有传输电子能力的物质,同时具有从阴极注入电子的效应,具有优异的薄膜形成能力。可作为本发明的电子注入材料包括:碱金属化合物,例如氧化锂、氟化锂、8-羟基喹啉锂、氧化锂硼、碳酸铯、8-羟基喹啉铯、硅酸钾、氟化钙、氧化钙、氟化镁、氧化镁;芴酮;含氮五元环衍生物;金属配合物;蒽酮类化合物等,但不限于此,这些化合物可以单独使用,也可与其他材料混合使用。
作为本发明的阴极材料,优选具有低功函数的材料,以便容易地将电子注入有机层。可用于本发明的阴极材料具体实例包括:金属,例如镁、钙、钠、钾、钛、铟、钇、锂、铝、银、锡、铅,或者它们的合金;以及多层材料,例如lif/al或lio2/al,但不限于此。
本发明所述的有机电致发光器件可以通过依次层叠上述的结构而制造。制造方法可使用干式成膜法、湿式成膜法等公知方法。作为干式成膜法的具体例,可举出真空蒸镀法、溅射法、等离子体法、离子电镀法等。作为湿式成膜法的具体例,可举出旋涂法、浸渍法、流延法、喷墨法等各种涂布法,但不限于此。
本发明所述有机发光器件可广泛应用于面板显示、照明光源、柔性oled、电子纸、有机太阳能电池、有机感光体或有机薄膜晶体管、指示牌、信号灯等领域。
上述有机电致发光器件的制造在以下实施例中具体地进行说明。但是,下述实施例只是用于例示本说明书,而本说明书的范围并不限定于该实施例。
化合物的制备及表征
原料、试剂以及表征设备的说明:
本发明对以下实施例中所采用的原料来源没有特别的限制,可以为市售产品或采用本领域技术人员所熟知的制备方法制备得到。
质谱使用岛津集团英国kratosanalytical公司的axima-cfrplus基质辅助激光解吸电离飞行质谱仪,氯仿为溶剂;
元素分析使用德国elementar公司的varioelcube型有机元素分析仪,样品质量为5~10mg;
核磁共振(1hnmr谱)使用bruker-510型核磁共振谱仪(德国bruker公司),600mhz,cdcl3为溶剂,tms为内标。
[实施例1]化合物1的合成
中间体s3-1的合成
将中间体s2-1(6.0g,21mmol)溶解在500ml的n,n-二甲基甲酰胺(dmf)中,在避光、室温条件下,在30min内向混合物中添加n-溴代琥珀酰亚胺(nbs)(3.7g,21mmol),将得到的混合物搅拌8小时,反应完成后,将反应物倒入na2co3溶液(3m,1l)中,然后将得到的产物用二氯甲烷洗涤,分离有机相并用旋转蒸发器除去溶剂。随后对于固体进行重结晶,得到中间体s3-1(7.0g,92%),hplc检测固体纯度≥99.8%。
质谱m/z:361.0645(理论值:361.0466)。理论元素含量(%)c21h16brn:c,69.63;h,4.45;br,22.06;n,3.87。实测元素含量(%):c,69.60;h,4.47;br,22.03;n,3.90。上述结果证实获得的产物为目标产品。
中间体s4-1的合成
向反应瓶中加入中间体s3-1(6.5g,18mmol)、苯基硼酸(2.4g,20mmol)、甲苯溶剂(75ml)、乙醇溶剂(37ml),然后再向混合物中加入k2co3(2m,37ml),四三苯基膦钯[pd(pph3)4](1.4mg,0.0012mmol),抽真空置换氮气三次后,加热至120℃并搅拌4小时,反应停止后,将体系温度降至室温,将得到的产物用二氯甲烷洗涤,分离有机相并用旋转蒸发器除去溶剂。向所得固体中加入甲苯溶剂进行重结晶,最终得到中间体s4-1(4.5g,69%),hplc检测固体纯度≥99.9%。
质谱m/z:359.1487(理论值:359.1674)。理论元素含量(%)c27h21n:c,90.21;h,5.89;n,3.90。实测元素含量(%):c,90.17;h,5.90;n,3.93。上述结果证实获得的产物为目标产品。
化合物1的合成
在氮气保护下,加入中间体s5-1(4.0g,10mmol),中间体s4-1(4.3g,12mmol),150ml甲苯溶剂搅拌混合,加入叔丁醇钠(2.88g,30mmol),然后向反应物中加入pd2(dba)3(45.78mg,0.05mmol),三叔丁基膦(10.12mg,0.05mmol),加热至105℃,回流反应24h,反应完成后,将反应物冷却至室温,用二氯甲烷萃取反应物,合并有机相,将有机相水洗后用无水硫酸镁干燥,经硅藻土过滤得到滤液,滤液进行减压旋蒸,然后向固体中加入乙醇重结晶,得到化合物1(5.0g,74%),hplc检测固体纯度≥99.7%。
质谱m/z:673.2900(理论值:673.2770)。理论元素含量(%)c52h35n:c,92.69;h,5.24;n,2.08。实测元素含量(%):c,92.68;h,5.21;n,2.11。1hnmr(600mhz,cdcl3)(δ,ppm):8.37(s,1h),8.36(d,1h),8.21(d,1h),8.11(d,1h),8.08–8.02(m,3h),7.95–7.92(m,2h),7.91(d,1h),7.90(s,1h),7.77(dd,1h),7.72(dd,1h),7.67–7.63(m,4h),7.61–7.53(m,5h),7.49–7.42(m,6h),7.35–7.31(m,1h),1.69(d,6h)。1hnmr具体如附图1所示。上述结果证实获得的产物为目标产品。
[实施例2]化合物7的合成
中间体s4-2的合成
将实施例1中的苯基硼酸替换为等摩尔量的苯基-d5-硼酸,按照实施例1的合成方法制备得到中间体s4-2(4.4g,68%),hplc检测固体纯度≥99.1%。
质谱m/z:364.2133(理论值:364.1988)。理论元素含量(%)c27h16d5n:c,88.97;h,7.19;n,3.84。实测元素含量(%):c,88.94;h,7.20;n,3.86。上述结果证实获得的产物为目标产品。
化合物7的合成
将实施例1中的中间体s4-1替换为等摩尔量的中间体s4-2,按照实施例1的合成方法制备得到化合物7(5.1g,75%),hplc检测固体纯度≥99.4%。
质谱m/z:678.3235(理论值:678.3083)。理论元素含量(%)c52h30d5n:c,92.00;h,5.94;n,2.06。实测元素含量(%):c,92.04;h,5.91;n,2.05。上述结果证实获得的产物为目标产品。
[实施例3]化合物45的合成
将实施例1中的中间体s5-1替换为等摩尔量的中间体s5-2,按照实施例1的合成方法制备得到化合物45(5.2g,76%),hplc检测固体纯度≥99.9%。
质谱m/z:675.3104(理论值:675.2926)。理论元素含量(%)c52h37n:c,92.41;h,5.52;n,2.07。实测元素含量(%):c,92.44;h,5.51;n,2.05。1hnmr(500mhz,cdcl3)(δ,ppm):8.20(dd,1h),7.98(d,1h),7.89(d,1h),7.88(s,1h),7.86(dd,1h),7.83(d,1h),7.75–7.70(m,3h),7.67(d,1h),7.61–7.57(m,2h),7.54(t,2h),7.51(t,1h),7.49(d,2h),7.46–7.43(m,2h),7.40–7.37(m,1h),7.34–7.31(m,1h),7.28–7.21(m,6h),7.12–7.08(m,4h),1.72(s,6h)。1hnmr具体如附图2所示。上述结果证实获得的产物为目标产品。
[实施例4]化合物111的合成
中间体s5-3的合成
将2-溴联苯(4.7g,20mmol)和9-氯-7h苯并芴酮(5.3g,20mmol)溶解在thf中后,将反应物的温度降至-78℃后,缓慢滴加正丁基锂(2.5m己烷溶液),并将反应混合物在室温搅拌4小时。反应完成后,向反应物中加入h2o以终止反应,减压下过滤,并将有机溶剂浓缩。使用柱色谱法分离产物,然后向产物中添加hcl和乙酸,并在80℃搅拌1小时。反应结束后过滤,浓缩有机溶剂,使用柱色谱法分离得到中间体s5-3(6.5g,81%)hplc检测固体纯度≥99.4%。
质谱m/z:400.1327(理论值:400.1019)。理论元素含量(%)c29h17cl:c,86.88;h,4.27;cl,8.84。实测元素含量(%):c,86.85;h,4.28;cl,8.87。上述结果证实获得的产物为目标产品。
化合物111的合成
将实施例1中的中间体s5-1替换为等摩尔量的中间体s5-3,按照实施例1的合成方法制备得到化合物111(5.4g,76%),hplc检测固体纯度≥99.7%。
质谱m/z:723.2718(理论值:723.2926)。理论元素含量(%)c56h37n:c,92.91;h,5.15;n,1.93。实测元素含量(%):c,92.93;h,5.14;n,1.93。上述结果证实获得的产物为目标产品。
[实施例5]化合物112的合成
中间体s4-3的合成
将实施例1中的苯基硼酸替换为等摩尔量的4-叔丁基苯硼酸,按照实施例1的合成方法制备得到中间体s4-3(5.0g,67%),hplc检测固体纯度≥99.2%。
质谱m/z:415.2640(理论值:415.2300)。理论元素含量(%)c31h29n:c,89.60;h,7.03;n,3.37。实测元素含量(%):c,89.63;h,7.01;n,3.34。上述结果证实获得的产物为目标产品。
化合物112的合成
将实施例1中的中间体s4-1替换为等摩尔量的中间体s4-3,中间体s5-1替换为等摩尔量的中间体s5-3,按照实施例1的合成方法制备得到化合物112(6.1g,78%),hplc检测固体纯度≥99.4%。
质谱m/z:779.3726(理论值:779.3552)。理论元素含量(%)c60h45n:c,92.39;h,5.82;n,1.80。实测元素含量(%):c,92.35;h,5.84;n,1.81。1hnmr(500mhz,cdcl3)(δ,ppm):8.86(dd,1h),8.42(dd,1h),8.35(d,2h),8.20(d,1h),8.13(d,1h),8.05–8.01(m,3h),8.00–7.98(m,1h),7.96(dd,1h),7.90(dd,1h),7.86(s,1h),7.82(dd,1h),7.79(d,1h),7.77(dd,1h),7.75–7.73(m,2h),7.70(dd,1h),7.67–7.62(m,3h),7.61–7.57(m,3h),7.57–7.54(m,1h),7.51(dd,1h),7.49–7.45(m,2h),7.29(dd,1h),1.64(s,3h),1.42(s,3h),1.28(s,9h)。1hnmr具体如附图3所示。上述结果证实获得的产物为目标产品。
[实施例6]化合物123的合成
将实施例1中的中间体s5-1替换为等摩尔量的中间体s5-4,按照实施例1的合成方法制备得到化合物123(5.6g,77%),hplc检测固体纯度≥99.7%。
质谱m/z:723.3159(理论值:723.2926)。理论元素含量(%)c56h37n:c,92.91;h,5.15;n,1.93。实测元素含量(%):c,92.88;h,5.19;n,1.91。上述结果证实获得的产物为目标产品。
[实施例7]化合物126的合成
将实施例1中的中间体s5-1替换为等摩尔量的中间体s5-5,按照实施例1的合成方法制备得到化合物126(6.2g,79%),hplc检测固体纯度≥99.9%。
质谱m/z:785.4117(理论值:785.4022)。理论元素含量(%)c60h51n:c,91.68;h,6.54;n,1.78,实测元素含量(%):c,91.86;h,6.32;n,1.82。1hnmr(600mhz,cdcl3)(δ,ppm):8.38(s,1h),8.34(s,1h),8.17(s,1h),8.09–8.00(m,4h),7.98–7.90(m,2h),7.82(dd,2h),7.73(d,1h),7.69–7.63(m,5h),7.62–7.56(m,3h),7.52–7.42(m,6h),7.33(t,1h),1.76(s,6h),1.27(s,18h)。1hnmr具体如附图4所示。上述结果证实获得产物为目标产品。
[实施例8]化合物141的合成
将实施例1中的中间体s5-1替换为等摩尔量的中间体s5-6,按照实施例1的合成方法制备得到化合物141(6.4g,76%),hplc检测固体纯度≥99.9%。
质谱m/z:841.4731(理论值:841.4648)。理论元素含量(%)c64h59n:c,91.28;h,7.06;n,1.66。实测元素含量(%):c,91.45;h,7.01;n,1.1.54。1hnmr(500mhz,cdcl3)(δ,ppm):8.38–8.34(m,2h),8.14(d,1h),8.09(d,1h),8.05–8.01(m,3h),7.89–7.84(m,3h),7.81(d,1h),7.78–7.75(m,2h),7.71(dd,1h),7.68(d,1h),7.65–7.62(m,1h),7.61(d,1h),7.59(dd,2h),7.56(dd,1h),7.50–7.47(m,3h),7.44(t,2h),7.35–7.31(m,1h),1.74(s,3h),1.68(s,3h),1.27(s,27h)。1hnmr具体如附图5所示。上述结果证实获得的产物为目标产品。
[实施例9]化合物146的合成
中间体s5-7的合成
将实施例4中的2-溴联苯替换为等摩尔量的2,2'-二溴-4,4'-二叔丁基联苯,按照实施例4的合成方法制备得到中间体s5-7(8.2g,80%),hplc检测固体纯度≥99.4%。
质谱m/z:512.2485(理论值:512.2271)。理论元素含量(%)c37h33cl:c,86.61;h,6.48;cl,6.91。实测元素含量(%):c,86.64;h,6.46;cl,6.89。上述结果证实获得的产物为目标产品。
化合物146的合成
将实施例4中的中间体s5-3替换为等摩尔量的中间体s5-7,按照实施例4的合成方法制备得到化合物146(6.4g,76%),hplc检测固体纯度≥99.4%。
质谱m/z:835.4407(理论值:835.4178)。理论元素含量(%)c64h53n:c,91.94;h,6.39;n,1.68。实测元素含量(%):c,91.94;h,6.39;n,1.68。1hnmr(500mhz,cdcl3)(δ,ppm):8.69(dd,1h),8.55(d,1h),8.39–8.34(m,2h),8.26(d,1h),8.16(dd,1h),8.10(d,1h),8.04(dd,1h),7.94–7.91(m,2h),7.86(d,1h),7.84–7.81(m,2h),7.79(d,1h),7.77(dd,1h),7.73–7.70(m,3h),7.65–7.62(m,1h),7.59(dd,3h),7.57(d,1h),7.51–7.48(m,2h),7.44(t,2h),7.35–7.30(m,1h),7.30–7.26(m,1h),1.74(s,3h),1.69(s,3h),1.27(s,18h)。1hnmr具体如附图6所示。上述结果证实获得的产物为目标产品。
[实施例10]化合物149的合成
将实施例5中的中间体s5-3替换为等摩尔量的中间体s5-7,按照实施例5的合成方法制备得到化合物149(5.8g,65%),hplc检测固体纯度≥99.5%。
质谱m/z:891.4500(理论值:891.4804)。理论元素含量(%)c68h61n:c,91.54;h,6.89;n,1.57。实测元素含量(%):c,91.51;h,6.90;n,1.59。上述结果证实获得的产物为目标产品。
[实施例11]化合物186的合成
中间体s4-4的合成
将实施例1中的中间体s2-1替换为等摩尔量的中间体s2-2,按照实施例1的合成方法制备得到中间体s4-4(4.4g,68%),hplc检测固体纯度≥99.6%。
质谱m/z:359.1955(理论值:359.1674)。理论元素含量(%)c27h21n:c,90.21;h,5.89;n,3.90。实测元素含量(%):c,90.25;h,5.86;n,3.88。上述结果证实获得的产物为目标产品。
化合物186的合成
将实施例1中的中间体s4-1替换为等摩尔量的中间体s4-4,中间体s5-1替换为等摩尔量的中间体s5-7,按照实施例1的合成方法制备得到化合物186(6.2g,75%),hplc检测固体纯度≥99.5%。
质谱m/z:835.6205(理论值:835.4178)。理论元素含量(%)c64h53n:c,91.94;h,6.39;n,1.68。实测元素含量(%):c,91.96;h,6.36;n,1.68。上述结果证实获得的产物为目标产品。
[实施例12]化合物214的合成
将实施例1中的中间体s5-1替换为等摩尔量的中间体s5-8,按照实施例1的合成方法制备得到化合物214(5.3g,76%),hplc检测固体纯度≥99.8%。
质谱m/z:701.3675(理论值:701.3083)。理论元素含量(%)c54h39n:c,92.40;h,5.60;n,2.00。实测元素含量(%):c,92.40;h,5.60;n,2.00。上述结果证实获得的产物为目标产品。
[实施例13]化合物234的合成
中间体s6-1的合成
在氮气保护下,向三口瓶中加入原料a-2-1(5.6g,20mmol)、9,9-二甲基芴-2-硼酸(5.2g,22mmol)、100ml甲苯溶剂,搅拌溶解,然后再向混合物中加入k2co3(2m,37ml),然后再加入四三苯基膦钯[pd(pph3)4](1.4mg,0.0012mmol)、50ml乙醇和水1:1混合液,搅拌加热至120℃,回流反应24h,反应完成后,自然冷却至室温,过滤,滤液分层,取有机相减压旋蒸溶剂,然后过中性硅胶柱,得到中间体s6-1(5.4g,69%)hplc检测固体纯度≥99.8%。
质谱m/z:393.1650(理论值:393.1284)。理论元素含量(%)c27h20cln:c,82.33;h,5.12;cl,9.00;n,3.56。实测元素含量(%):c,82.37;h,5.11;cl,9.02;n,3.60。上述结果证实获得的产物为目标产品。
中间体s7-1的合成
在氮气保护下,向三口瓶中加入中间体s6-1(7.9g,20mmol)、苯基硼酸(2.7g,22mmol)、100ml甲苯溶剂,搅拌溶解,然后再向混合物中加入k2co3(2m,37ml),然后再加入四三苯基膦钯[pd(pph3)4](1.4mg,0.0012mmol)、50ml乙醇和水1:1混合液,搅拌加热至120℃,回流反应24h,反应完成后,自然冷却至室温,过滤,滤液分层,取有机相减压旋蒸溶剂,然后过中性硅胶柱,得到中间体s7-1(5.9g,68%)hplc检测固体纯度≥99.6%。
质谱m/z:435.2309(理论值:435.1987)。理论元素含量(%)c33h25n:c,91.00;h,5.79;n,3.22。实测元素含量(%):c,91.04;h,5.77;n,3.19。上述结果证实获得的产物为目标产品。
化合物234的合成
在氮气保护下,加入中间体s5-1(4.0g,10mmol),中间体s7-1(5.2g,12mmol),150ml甲苯溶剂搅拌混合,加入叔丁醇钠(2.88g,30mmol),然后向反应物中加入pd2(dba)3(45.78mg,0.05mmol),三叔丁基膦(10.12mg,0.05mmol),加热至105℃,回流反应24h,反应完成后,将反应物冷却至室温,用二氯甲烷萃取反应物,合并有机相,将有机相水洗后用无水硫酸镁干燥,经硅藻土过滤得到滤液,滤液进行减压旋蒸,加入乙醇重结晶,得到化合物234(5.7g,76%),hplc检测固体纯度≥99.4%。
质谱m/z:749.3621(理论值:749.3083)。理论元素含量(%)c58h39n:c,92.89;h,5.24;n,1.87。实测元素含量(%):c,92.86;h,5.26;n,1.88。1hnmr(500mhz,cdcl3)(δ,ppm):8.36(d,1h),8.34(d,1h),8.15(d,1h),8.04–8.00(m,3h),8.00–7.97(m,2h),7.95–7.90(m,4h),7.87–7.83(m,2h),7.72–7.68(m,3h),7.65(dd,1h),7.63–7.58(m,6h),7.56–7.52(m,2h),7.49–7.42(m,6h),7.35–7.31(m,1h),1.73(d,6h)。1hnmr具体如附图7所示。上述结果证实获得的产物为目标产品。
[实施例14]化合物194的合成
将实施例13中的中间体s5-1替换为等摩尔量的中间体s5-7,按照实施例13的合成方法制备得到化合物194(6.7g,74%),hplc检测固体纯度≥99.7%。
质谱m/z:911.4900(理论值:911.4491)。理论元素含量(%)c70h57n:c,92.17;h,6.30;n,1.54。实测元素含量(%):c,92.19;h,6.27;n,1.54。上述结果证实获得的产物为目标产品。
[实施例15]化合物257的合成
将实施例13中的中间体s5-1替换为等摩尔量的中间体s5-6,按照实施例13的合成方法制备得到化合物257(7.1g,77%),hplc检测固体纯度≥99.7%。
质谱m/z:917.5311(理论值:917.4961)。理论元素含量(%)c70h63n:c,91.56;h,6.92;n,1.53。实测元素含量(%):c,91.58;h,6.90;n,1.52。上述结果证实获得的产物为目标产品。
[器件实施例1]
首先,将厚度为
然后在已经清洗好的ito基板上蒸镀2-tnata作为空穴注入层,蒸镀厚度为
上述过程中,有机物的蒸镀速率维持在
[器件实施例2~30]
分别用化合物4、化合物7、化合物22、化合物37、化合物45、化合物52、化合物62、化合物78、化合物87、化合物105、化合物111、化合物112、化合物116、化合物124、化合物126、化合物127、化合物132、化合物141、化合物146、化合物149、化合物152、化合物186、化合物194、化合物213、化合物234、化合物245、化合物261、化合物279、化合物281替代器件实施例1中的化合物1作为空穴传输层,除此之外,通过与器件实施例1相同的制备方法,得到有机电致发光器件。
[器件实施例31]
以器件实施例1中相同方式清洗基板,然后在已经清洗好的ito基板上蒸镀2-tnata作为空穴注入层,蒸镀厚度为
[器件实施例32~38]
分别用化合物123、化合物146、化合物149、化合物186、化合物194、化合物214、化合物257替代器件实施例31中的化合物111作为第二空穴传输层,除此之外,通过与器件实施例31相同的制备方法,得到有机电致发光器件。
[器件实施例39]
以器件实施例1中相同的方式清洗基板,然后在基板上以95:5的重量比蒸镀npb以及本发明化合物ⅳ-2形成空穴注入层,蒸镀厚度为
[器件实施例40~41]
分别用化合物ⅳ-4、ⅳ-9替代器件实施例39中的化合物ⅳ-2,除此之外,通过与器件实施例39相同的制备方法,得到有机电致发光器件。
[对比实施例1]
用ht-1替代器件实施例1中的化合物1,作为空穴传输层,除此之外,通过与器件实施例1相同的制备方法,得到有机电致发光器件。
[对比实施例2]
用ht-2替代实施例1中的化合物1,作为空穴传输层,除此之外,通过与实施例1相同的制备方法,得到有机电致发光器件。
[对比实施例3]
用ht-3替代实施例1中的化合物1,作为空穴传输层,除此之外,通过与实施例1相同的制备方法,得到有机电致发光器件。
[对比实施例4]
用ht-4替代实施例替代实施例31中的化合物111作为第二空穴传输层,除此之外,通过与器件实施例31相同的制备方法,得到有机电致发光器件。
[对比实施例5]
用hi-1替代器件实施例39中的化合物ⅳ-2,除此之外,通过与器件实施例39相同的制备方法,得到有机电致发光器件。
将测试软件、计算机、美国keithley公司生产的k2400数字源表和美国photoresearch公司的pr788光谱扫描亮度计组成一个联合ivl测试系统来测试有机发光器件的发光效率、cie色坐标。寿命的测试采用mcscience公司的m6000oled寿命测试系统。测试的环境为大气环境,温度为室温。本发明器件实施例中器件1~41、对比实施例1~5所得有机发光器件的发光特性测试结果见表1所示。
[表1]
表1结果表明,本发明提供的芴衍生物应用于有机电致发光器件的空穴传输层时,可有效提高器件的稳定性、有效阻挡激子向阳极侧逸散,从而延长器件的使用寿命,同时,本发明提供的芴衍生物自身具有较好的空穴传输能力,应用于有机电致发光器件的空穴传输层时,能有效提高器件的发光效率。
应当指出,本发明用个别实施方案进行了特别描述,但在不脱离本发明原理的前提下,本领域普通技术人可对本发明进行各种形式或细节上的改进,这些改进也落入本发明的保护范围内。
- 该技术已申请专利。仅供学习研究,如用于商业用途,请联系技术所有人。
- 技术研发人员:杜明珠;朱鸫达;王英雪
- 技术所有人:长春海谱润斯科技有限公司
- 我是此专利的发明人
- 上一篇:一种高效防滑的螺母的制作方法
- 上一篇:一种立式板销接头的制作方法
- 该领域下的技术专家
- 如您需求助技术专家,请点此查看客服电话进行咨询。
- 1、贺老师:氮化物陶瓷、光功能晶体材料及燃烧合成制备科学及工程应用
- 2、杨老师:工程电磁场与磁技术,无线电能传输技术
- 3、许老师:1.气动光学成像用于精确制导 2.人工智能方法用于数据处理、预测 3.故障诊断和健康管理
- 4、王老师:智能控制理论及应用;机器人控制技术
- 5、李老师:1.自旋电子学 2.铁磁共振、电磁场理论
- 如您是高校老师,可以点此联系我们加入专家库。
- 还没有人留言评论。精彩留言会获得点赞!