1.本发明属于锂硫电池技术领域,涉及一种超分子冠醚多酸/硫复合正极材料及其制备方法和应用。
背景技术:2.随着便携式电子设备和电动汽车的蓬勃发展,以及当前锂离子电池的快速发展,高能量密度和长寿命电池越来越受到人们的关注,然而锂离子电池因其能量密度低制约了进一步发展。锂硫(li-s)电池体系的能量密度远高于目前已商业化的锂离子电池体系,被认为是最有发展潜力的下一代高能量密度二次电池体系。然而对于锂硫电池而言,单质硫的绝缘性导致了硫利用率低。“穿梭效应”是限制li-s电池实际应用的最关键问题,因为多硫化物的“穿梭效应”造成了活性物质不断流失和锂负极的表面钝化,继而出现电池容量衰减、库仑效率下降、循环稳定性差等严重问题,同时也增加电解液的过度消耗。
3.多金属氧酸盐(pom)是一种具有双功能催化性能的硫宿主材料,既有金属氧化物的特性,通过化学氧化还原来限制多硫化物溶解,又能在电池充放电过程中以分子催化剂的形式参与到整个充放电循环中,可逆储存和转移多个电子,并且可以双向催化多硫化锂的放电还原过程和硫化锂的充电氧化过程,促进电池中硫物种的固-液-固相转化,有望从本质上缓解多硫化物的“穿梭效应”问题。但是现有将多酸用于锂硫电池中的研究,电池的容量提升不高且循环稳定性仍较差,整体性能提升有限(w.yao,l.liu,x.wu,q.chao,h.xie,z su,acs appl.mater.interfaces,2018,10,35911-35918.)。
4.冠醚作为第一代超分子大环主体,在超分子化学领域的发展迅速。超分子冠醚具有与锂离子协调的能力,能够增加离子电导率,可以显著提高电池性能,因此超分子冠醚可应用于锂金属电池中(h.wang,j.he,j.liu,etal,adv.funct.mater.2020,31,2002578.)。
技术实现要素:5.本发明的目的在于提供一种超分子冠醚多酸/硫复合正极材料及其制备方法和在锂硫电池中的应用。本发明通过将超分子冠醚多酸复合材料作为锂硫电池正极的宿主材料,可以促进锂硫电池中多硫化物相互转化并改善反应动力学,增加电池的离子电导率和对多硫化物的吸附能力,显著提高电池性能。
6.实现本发明目的的技术解决方案如下:
7.超分子冠醚多酸/硫复合正极材料的制备方法,包括以下步骤:
8.(1)将keggin型多金属氧酸盐h3[pw
12o40
]或h3[pmo
12o40
]溶解在乙腈中,然后加入licl,加热至60~80℃,再加入18-冠醚-6,搅拌反应,反应结束后过滤,溶剂挥发,抽滤,洗涤,干燥得到超分子冠醚多酸晶体;
[0009]
(2)将超分子冠醚多酸晶体与升华硫球磨混合均匀,得到超分子冠醚多酸/硫复合正极材料。
[0010]
优选地,步骤(1)中,h3[pw
12o40
]或h3[pmo
12o40
]在乙腈中的浓度为1.67
×
10-3
mol/
l。
[0011]
优选地,步骤(1)中,搅拌反应时间为30~40分钟。
[0012]
优选地,步骤(1)中,h3[pw
12o40
]或h3[pmo
12o40
]、licl和18-冠醚-6的摩尔比为1:5:5。
[0013]
优选地,步骤(1)中,溶剂挥发的时间为7~10天,温度为室温。
[0014]
优选地,步骤(1)中,干燥温度为60℃,干燥时间为24h。
[0015]
优选地,步骤(2)中,升华硫与超分子冠醚多酸晶体的质量比为7:3。
[0016]
优选地,步骤(2)中,球磨混合时间为4小时。
[0017]
本发明还提供上述制备方法制得的超分子冠醚多酸/硫复合正极材料。
[0018]
进一步地,本发明提供上述超分子冠醚多酸/硫复合正极材料在锂硫电池中的应用。
[0019]
与现有技术相比,本发明的优点是:
[0020]
(1)本发明以超分子第一代大环冠醚18-冠醚-6为主体,keggin型多金属氧酸盐[pw
12o40
]
3-或[pmo
12o40
]
3-为客体,在乙腈中通过分子间作用力,自组装形成了超分子晶体材料,合成方法简单,产率较高。
[0021]
(2)本发明通过自组装得到超分子晶体,通过控制反应时间、各原料摩尔比和搅拌时间、温度等条件,制得晶体结构稳定的超分子晶体材料。
[0022]
(3)本发明制备的超分子冠醚多酸/硫复合材料解决了锂硫电池中的“穿梭效应”问题,可以促进锂硫电池中多硫化物相互转化并改善反应动力学,增加电池的离子电导率和对多硫化物的吸附能力,以其为正极材料的锂硫电池具有较好循环可逆性和稳定性。
附图说明
[0023]
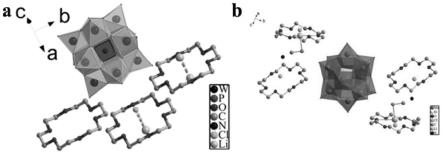
图1为(a)超分子冠醚磷钨酸晶体和(b)超分子冠醚磷钼酸晶体的多面体图。
[0024]
图2为(a)超分子冠醚磷钨酸晶体和(b)超分子冠醚磷钼酸晶体的堆积图。
[0025]
图3为(a)超分子冠醚磷钨酸晶体和(b)超分子冠醚磷钼酸晶体的扫描电镜图。
[0026]
图4为(a)超分子冠醚磷钨酸晶体和(b)超分子冠醚磷钼酸晶体的x-射线粉末衍射理论值与实验值对照图。
[0027]
图5为(a)超分子冠醚磷钨酸晶体和(b)超分子冠醚磷钼酸晶体以及其合成单体的傅里叶变换红外光谱分析对照图。
[0028]
图6为(a)超分子冠醚磷钨酸晶体和(b)超分子冠醚磷钼酸晶体以及他其合成单体的热重失重分析图。
[0029]
图7为(a)超分子冠醚磷钨酸/硫复合材料和(b)超分子冠醚磷钼酸/硫复合材料作为锂硫电池正极材料的电池倍率曲线图。
[0030]
图8为(a)超分子冠醚磷钨酸/硫复合材料和(b)超分子冠醚磷钼酸/硫复合材料作为锂硫电池正极材料的电池长循环曲线图。
具体实施方式
[0031]
为了使本发明的目的、技术方案及优点更加清楚明白,下面结合实施例和附图对本发明作进一步地详细说明。
[0032]
实施例1
[0033]
超分子冠醚磷钨酸/硫复合材料的制备,具体步骤如下:
[0034]
(1)超分子冠醚磷钨酸晶体的制备:将720mg(0.25mmol)的keggin型杂多酸h3[pw
12o40
]溶解在150ml的ch3cn中,并将体系的温度通过水浴加热至70℃,待h3[pw
12o40
]完全溶解后,依次加入53mg(1.25mmol)的licl和330mg(1.25mmol)的18-冠醚-6。将混合溶液搅拌反应30分钟后趁热过滤,在室温下,随溶液缓慢挥发得到黄绿色块状晶体。抽滤,用大量乙腈充分洗涤,得到超分子冠醚磷钨酸晶体li3pw
12o40
(ch3cn)2(c
12
o6h
24
)3hcl 0.833g,产率为88.0%(基于w)。
[0035]
超分子冠醚磷钨酸晶体的晶体学参数如表1所示。
[0036]
表1超分子冠醚磷钨酸晶体的晶体学参数
[0037][0038][0039]
(2)超分子冠醚磷钨酸/硫复合材料:将超分子冠醚磷钨酸晶体与升华硫球磨4小时混合均匀,得到超分子冠醚磷钨酸/硫复合材料。
[0040]
实施例2
[0041]
超分子冠醚磷钼酸/硫复合材料的制备方法,具体步骤如下:
[0042]
(1)超分子冠醚磷钼酸晶体的制备:将456mg(0.25mmol)的keggin型杂多酸h3[pmo
12o40
]溶解在150ml的ch3cn中,并将体系的温度通过水浴加热至70℃,待h3[pmo
12o40
]完
全溶解后,依次加入11mg(2.5mmol)的licl和660mg(2.5mmol)的18-冠醚-6。将混合液体搅拌30分钟后趁热过滤,在室温下,随溶液缓慢挥发得到黄绿色块状晶体。抽滤,用大量乙腈充分洗涤,得到超分子冠醚磷钼酸晶体h3pmo
12o40
(ch3cn)2(c
12
o6h
24
)3(h2o)4hcl 0.623g,产率为88.9%(基于mo)。
[0043]
超分子冠醚磷钼酸晶体的晶体学参数如表2所示。
[0044]
表2超分子冠醚磷钼酸晶体的晶体学参数
[0045][0046][0047]
(2)超分子冠醚磷钼酸/硫复合材料的制备:将超分子冠醚磷钼酸晶体与升华硫球磨4小时混合均匀,得到超分子冠醚磷钼酸/硫复合材料。
[0048]
对比例1
[0049]
本对比例与实施例1基本相同,唯一不同的是keggin型杂多酸h3[pw
12o40
]、licl和18-冠醚-6的摩尔比分别为1:10:10、1:4:4。该比例下均无法合成晶体,皆生成固体沉淀。
[0050]
对比例2
[0051]
本对比例与实施例1基本相同,唯一不同的是使用的多金属氧酸盐为硅钨酸。该条件下无法合成晶体,只能生成固体沉淀。
[0052]
对比例3
[0053]
本对比例与实施例1基本相同,唯一不同的是使用的锂盐为硝酸锂。该条件下无法
合成晶体,只能生成固体沉淀。
[0054]
对比例4
[0055]
本对比例与实施例1基本相同,唯一不同的是步骤(1)中的反应温度分别为55℃、85℃。该条件下均无法合成晶体,只能生成固体沉淀。
[0056]
对比例5
[0057]
本对比例与实施例1基本相同,唯一不同的是步骤(1)中的晶体和硫的质量比分别为3:1、3:2。该比例下制得的复合正极材料制备的电池效果不佳。
[0058]
图1为本发明制备的超分子冠醚磷钨酸晶体和超分子冠醚磷钼酸晶体的多面体图。可见,每个磷钨酸或磷钼酸分子通过分子间氢键与超分子冠醚结合形成超分子冠醚多酸晶体。
[0059]
图2为本发明制备的超分子冠醚磷钨酸晶体和超分子冠醚磷钼酸晶体的堆积图。可见,磷钨酸或磷钼酸和冠醚相互交错,通过分子间氢键紧密堆叠,形成有序的堆叠结构。
[0060]
图3为本发明制备的超分子冠醚磷钨酸晶体和超分子冠醚磷钼酸晶体的扫描电镜图,可以看出,晶体直径在400纳米左右,呈现方形结构。
[0061]
图4为本发明制备的超分子冠醚磷钨酸晶体和超分子冠醚磷钼酸晶体的x-射线粉末衍射理论值与实验值对照图,从图中可以明显看出晶体材料的x-射线粉末衍射实验值与理论模拟值出峰位置十分吻合,峰强度与峰形也保持一致,图谱几乎完全相同,且实验数据信噪较小,说明晶体解析完全正确,制备晶体材料纯度较高。
[0062]
图5为本发明制备的超分子冠醚磷钨酸晶体和超分子冠醚磷钼酸晶体以及其合成单体的傅里叶变换红外光谱分析图,可以看出存在磷钨酸或磷钼酸和冠醚的所有特征峰,说明超分子配合物晶体中确实含有这两个基本构件。
[0063]
图6为本发明制备的超分子冠醚磷钨酸晶体和超分子冠醚磷钼酸晶体以及其合成单体的热重失重分析图,较好的验证晶体解析中各组分的摩尔比,也再次证实了晶体结构解析的正确性。
[0064]
图7为采用本发明制备的超分子冠醚磷钨酸/硫复合材料和超分子冠醚磷钼酸/硫复合材料作为锂硫电池正极材料的电池倍率曲线图。超分子冠醚磷钨酸/硫正极复合材料的放电比容量约为1437mah g-1
,接近理论容量的86%(1675mah g-1
)。当在0.2、0.3、0.5、1.0、2.0、3.0和5.0c电流密度下循环时,超分子冠醚磷钨酸/硫正极可提供的放电容量分别为1249、1210、1184、1120、1019、913和622mah g-1
。当电流密度回到0.1c时,超分子冠醚磷钨酸/硫正极的放电容量恢复到1249mah g-1
,表现出了良好的电池容量和优异的可逆性。超分子冠醚磷钼酸/硫正极复合材料的放电比容量约为1341mah g-1
,接近理论容量的80%(1675mah g-1
)。当在0.2、0.3、0.5、1.0、2.0、3.0和5.0c电流密度下循环时,超分子冠醚磷钼酸/硫正极可提供的放电容量分别为1205、1149、1086、1068、893、783和566mah g-1
。当电流密度回到0.1c时,超分子冠醚磷钼酸/硫正极的放电容量恢复到1127mah g-1
,表现出了良好的电池容量和优异的可逆性。
[0065]
图8为采用本发明制备的超分子冠醚磷钨酸/硫复合材料作为锂硫电池正极材料的电池长循环曲线图。经过300次循环后,超分子冠醚磷钨酸/硫正极仍可在1.0c的电流速率下实现良好的循环稳定性(起始容量1112mah g-1
,1000次循环后为348mah g-1
),并且每个周期的容量衰减率仅为0.068%,库伦效率在95%以上。经过300次循环后,超分子冠醚磷
钼酸/硫正极仍可在1.0c的电流速率下实现良好的循环稳定性(起始容量923mah g-1
,300次循环后为713mah g-1
),并且每个周期的容量衰减率仅为0.076%,库伦效率在95%以上。
