一种奶牛生产性能测定标准物质及其制备方法和用途与流程
本发明属于奶牛生产性能测定领域,具体涉及一种奶牛生产性能测定标准物质及其制备方法和用途。
背景技术:
奶牛生产性能测定(dairyherdimprovement,dhi)又称奶牛群改良,旨在对奶牛泌乳性能及乳成分进行测定并建立完整的记录体系,也是奶牛数字化育种技术的核心和基础。dhi测定技术于1906年诞生并应用,经过100多年的发展,已成为“培育优良品种、实施科学饲养和提高生乳质量”的重要手段。dhi是世界奶业发达国家普遍用来管理和提高奶牛生产水平的一项综合技术,被业内人士公认为“牛群改良唯一有效的方法”。
乳成分分析仪(milkanalyzer)是采用中红外(midinfrared,mir)扫描来测定牛奶中各种营养成分的分析仪器,是一种快速而低成本的检测方法,目前作为一种经过认可的官方方法(aoac,2000)而广泛用于牛奶定价体系和dhi测定系统。中红外乳成分分析仪的精确度受仪器因素、分析因素以及牛奶样品的成分因素影响检测的精确度。因此,中红外乳成分分析仪必须定期用经过经典化学方法定值的dhi标准物质进行校准。
dhi标准物质是指用于校准乳成分快速分析仪的标准牛奶样品,英文名称是milkcalibrationsamples或milkcalibrationstandards。校准样品的特性如样品的个数,成分浓度的范围以及在此范围内的分布,脂肪和蛋白质浓度的天然相关性,以及不同套之间样品特性的变化都会影响校准的效果。一般情况下,增加一套标样中样品的个数可以降低95%置信区间的宽度,12-16个样品可以使置信区间的宽度降到最小;样品成分在浓度范围内的均匀分布可以使单个样品的影响降到最小;成分之间变化的相关性(如脂肪和蛋白质)可能引起斜率和截距的误差。aoac规定一套大于8个的牛奶样品可以用于红外乳成分分析仪的校准(aoac,2000;method972.16;33.2.31;idf,2000)。
传统的牛奶标准样品(producercalibrationsamples,牛场校准样品)是选用当地天然的不同成分含量的生牛奶稍加调整加工而成。一般低脂肪、高蛋白浓度样品通过脱脂方法得到,高脂肪浓度样品通过添加稀奶油调制而成。这种标准物质的特点是成分浓度范围较窄,杠杆值比较高,脂肪和蛋白质浓度之间具有正相关性,这些因素都会影响标准物质的精确度,通常表现为校准线性回归曲线的置信区间增大,而且其在4℃条件下的保质期较短,为15天。
技术实现要素:
因此,本发明要解决的技术问题在于提供一种奶牛生产性能测定标准物质及其制备方法,所述奶牛生产性能测定标准物质均一、稳定,达到了dhi测定工作的要求,成分浓度范围较宽,杠杆值比较低,脂肪和蛋白质浓度之间没有正相关性,使用所述dhi标准物质校准仪器后,仪器的精确度提高,测定水平提高且保持稳定,实验室间一致性增加。
为此,本发明提供了如下的技术方案:
一种奶牛生产性能测定标准物质,包括按照下述质量百分数范围的成分及相应水平梯度经正交设计得到:
脂肪的质量百分数范围为0.20%-6.00%,设计12个水平梯度;蛋白质的质量百分数范围为2.00%-4.50%,设计6个水平梯度;乳糖的质量百分数范围为4.00%-5.00%,设计4个水平梯度。
在所述的奶牛生产性能测定标准物质中,所述的奶牛生产性能测定标准物质包括标准品1-12,如表1所示。
本发明提供了一种制备所述的奶牛生产性能测定标准物质的方法,包括如下步骤:
s1、取原料奶进行热处理;
s2、将热处理后的原料奶进行乳脂分离,分离得到脱脂奶和乳脂肪,备用;
s3、取分离的脱脂奶进行微滤除菌,收集的滤液作为第一滤过液,备用;
s4、取部分收集的第一滤过液进行超滤浓缩,收集滤液和截留液,收集的滤液作为第二滤过液,备用;
s5、取剩余的第一滤过液与所述乳脂肪混合得到稀奶油、第二滤过液、截留液和乳糖进行调配。
在所述的制备方法中,所述原料奶的热处理温度为48-52℃,热处理时间为15-20s;优选的,为50℃。
在所述的制备方法中,在所述微滤除菌步骤中,选择1.4μm级的陶瓷膜进行微滤除菌。
在所述的制备方法中,在所述微滤除菌步骤中,将所述陶瓷膜安装至过滤系统,以不大于8℃/min的升温速度升温,在升温过程中清洗所述陶瓷膜至少3次,升温至50-55℃后加入所述脱脂奶,保持过膜压力2.8-3.0bar,结束后,用50-60℃的水进行连续清洗,然后降温。
在所述的制备方法中,选择20nm级的陶瓷膜进行超滤浓缩。
在所述的制备方法中,在所述超滤浓缩步骤中,所述陶瓷膜浓缩蛋白时的过膜压力为2.25-2.45mpa,浓缩时间为2.5-3h。
在所述的制备方法中,在所述超滤浓缩步骤中,所述陶瓷膜超滤浓缩结束后,还包括采用截留液对所述陶瓷膜进行反冲洗的步骤,反冲洗的时间为10-15min;优选的,还包括,将反冲洗后的陶瓷膜,先用水清洗,然后用质量百分比1.5-2%氢氧化钠溶液清洗30分钟,再以质量百分比0.15-0.2%次氯酸钠清洗30分钟,然后水洗15分钟;再用质量百分比0.2%的硝酸溶液清洗30分钟,最后再用水洗15分钟。
本发明提供的所述的奶牛生产性能测定标准物质或所述的方法制备得到的奶牛生产性能测定标准物质用于校准乳成分快速分析仪中的用途。
本发明技术方案,具有如下优点:
1.本发明提供的一种奶牛生产性能测定标准物质,包括按照下述质量百分数范围的成分及相应水平梯度经正交设计得到:脂肪的质量百分数范围为0.20%-6.00%,设计12个水平梯度;蛋白质的质量百分数范围为2.00%-4.50%,设计6个水平梯度;乳糖的质量百分数范围为4.00%-5.00%,设计4个水平梯度;上述奶牛生产性能测定标准物质,均一、稳定,达到了dhi测定工作的要求,成分浓度范围较宽,杠杆值比较低,减少了天然奶样中脂肪和蛋白含量的相关性对dhi标准物质校准精确度的影响,使用所述dhi标准物质校准仪器后,仪器的精确度提高,测定水平提高且保持稳定,实验室间一致性增加。
2.本发明提供的一种奶牛生产性能测定标准物质,所述的奶牛生产性能测定(dhi)标准物质包括标准品1-12,如表1所示,所述dhi标准物质具有如下优点:
产品的灌装均匀度均达到国标要求,脂肪和蛋白的瓶间标准偏差都为0.04%,乳糖的瓶间标准偏差为0.06%,完全能达到标准物质供应要求;对产品稳定性的研究表明:在4℃条件下贮存15天,产品的各项成分几乎不发生变化,通过回归分析计算出各配方的脂肪、蛋白和乳糖的斜率都接近于0,截距和各成分含量吻合性好,除#12配方的脂肪含量变化有点明显外,其它各配方、各成分均无可检测的不稳定性;
各标准品产品的细菌总数都在100cfu/ml以下,另外由于添加了防腐剂,在4℃贮存到22天时菌落数下降到0-10cfu/ml之间,说明微生物对产品稳定性的影响较小;
运用方差分析方法对使用改良校准奶样和传统校准奶样校准乳成分分析仪后的成分检测数据与化学方法检测数值进行分析,两者均没有显著性差异,但以sdd值可以看出使用改良校准奶样校准后的检测结果更接近化学值。通过对全国各dhi实验室2012年6月-2013年6月的脂肪、蛋白测定数据分析发现,多数实验室蛋白、脂肪的md%、sdd%和rmd%值符合美国标准,仅有一少部分超出美国标准规定范围,说明改良校准物质的生产和供应提高了各实验室的测定水平,其脂肪、蛋白测定值更接近于化学参考值。一年内改良校准奶样的使用,各实验室测定水平趋于平稳,测定准确性增加,一致性有很大提高;
综上,所述的dhi标准物质均一、稳定,达到了dhi测定工作的要求,各实验室使用本实验室研制的dhi标准物质校准仪器后,测定水平提高且保持稳定,实验室间一致性增加,该标准物质的正式生产和供应发挥了其应有的作用。
3.本发明提供的一种制备所述的奶牛生产性能测定标准物质的方法,包括如下步骤:s1、取原料奶进行热处理;s2、将热处理后的原料奶进行乳脂分离,分离得到脱脂奶和乳脂肪,备用;s3、取分离的脱脂奶进行微滤除菌,收集第一滤过液,备用;s4、取部分收集的第一滤过液进行超滤浓缩,收集第二滤过液和截留液,备用;s5、取剩余的第一滤过液与所述乳脂肪混合得到稀奶油、第二滤过液、截留液和乳糖进行调配;在上述方法中,首先对原料奶进行热处理,以便于后续的乳脂分离和陶瓷膜过滤操作,然后进行乳脂分离,将分离的脱脂奶微滤除菌,将获得的第一滤过液进行超滤浓缩,收集第二滤过液和截留液,取剩余的第一滤过液与所述乳脂肪混合得到稀奶油、第二滤过液、截留液和乳糖进行调配可以得到本发明所述的dhi标准物质。
4.本发明提供的一种制备所述的奶牛生产性能测定标准物质的方法,所述原料奶的热处理温度为48-52℃,热处理时间为15-20s;优选的,为50℃,经研究发现,50℃的热处理温度对原料奶成分影响最小,其成分以及随时间的变化最接近原料奶,同时能够达到最佳的乳脂分离效果。
5.本发明提供的一种制备所述的奶牛生产性能测定标准物质的方法,在所述微滤除菌步骤中,选择1.4μm级的陶瓷膜进行微滤除菌,除菌率可达到99.5%以上,完全可以满足生产需要。
6.本发明提供的一种制备所述的奶牛生产性能测定标准物质的方法,选择20nm级的陶瓷膜进行超滤浓缩,所述陶瓷膜浓缩蛋白时的过膜压力为2.3mpa,浓缩时间为2.5-3h,研究发现,在上述条件下,浓缩时间与截留液中蛋白质浓度成线性关系,浓缩2.5-3h可保证得到调配需要的蛋白质浓度6.0%以上,以保证可以调配出本发明所述的dhi标准物质。
附图说明
为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
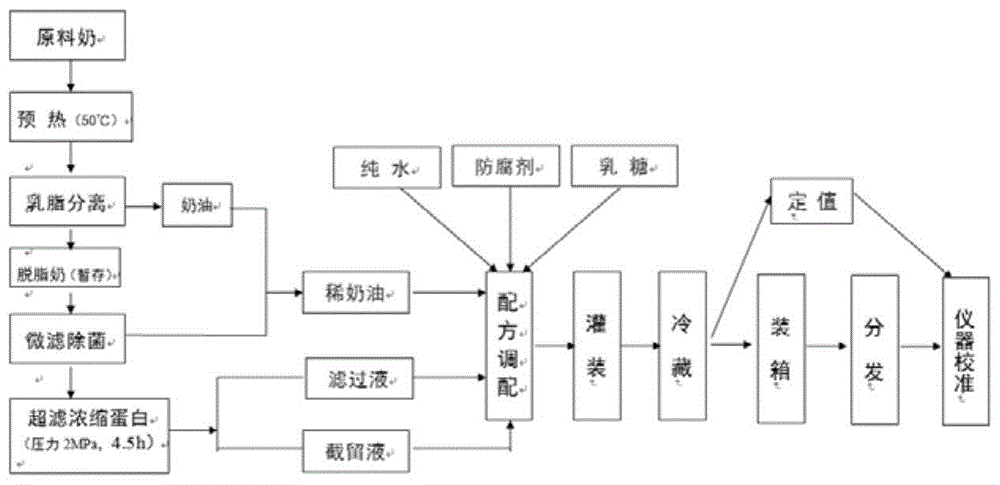
图1是本发明实施例3中的工艺流程图;
图2是本发明实验例1中不同热处理奶样的脂肪含量随存放时间的变化图;
图3是本发明实验例1中不同热处理奶样的蛋白含量随存放时间的变化图;
图4是本发明实验例1中不同热处理奶样的乳糖含量随存放时间的变化;
图5是本发明实验例5中dhi标准物质贮存过程中细菌总数的变化图;
图6是本发明实验例7中各实验室使用实施例3中的dhi标准物质对中红外乳成分分析仪校准后脂肪md%值变化图;
图7是本发明实验例7中各实验室使用实施例3中的dhi标准物质对中红外乳成分分析仪校准后蛋白md%值变化图;
图8是本发明实验例7中各实验室使用实施例3中的dhi标准物质对中红外乳成分分析仪校准后脂肪sdd%值变化图;
图9是本发明实验例7中各实验室使用实施例3中的dhi标准物质对中红外乳成分分析仪校准后蛋白sdd%值变化图。
具体实施方式
下述实施例中,将牛场提供原料奶的当天早晨5点左右挤出的新鲜牛奶作为dhi标准物质的原料奶。
对原料奶的验收按以下要求进行:
首先进行感官检测包括:正常新鲜牛奶色泽呈乳白色或微黄色;具有乳固有的香味,无异味;呈均匀一致液体,无凝块、无沉淀、无正常视力可见异物。感官检测由经过培训的接奶员完成。
采样员按照牛奶采样程序采集鲜奶样品,编号送至检测室,由检测员负责进行奶样检测。利用酸度计测定原料奶的ph值,利用foss乳成分分析仪对鲜奶中乳脂、乳蛋白、乳糖及体细胞数进行检测。若通过检测证实原料奶品质合格(按照国家相关标准),则接奶员执行鲜奶接收步骤,并认真填写《牛奶接收单》,完成接奶工作;若原料奶品质不合格则拒绝接收当批原料,并反馈至供奶商,重新供应鲜奶。鲜奶接收后,置于制冷式储存罐中,低温4℃暂存备用。
下述实施例中使用的20nm级的陶瓷膜,根据生产厂家说明,在使用前须保证膜水通量至少为70l/h,料液温度保持为48-52℃(减少对成分的破坏),初始过膜压力应为1.0mpa,然后逐渐增加过膜压力至适当压力,最高不能超过3.0mpa。膜滤完成后,采用截留液对膜进行反冲洗,以使粘附在膜表面的蛋白回到浓缩料液中,得到浓度高且均匀的截留液。陶瓷膜清洗程序为:膜滤后,先用清水将陶瓷膜冲洗至清澈为止,然后用碱液清洗,当膜滤次数超过5次时碱洗后须再进行酸洗,当然,每次碱洗后再用酸洗也可以。20nm陶瓷膜超滤截留蛋白的基础参数如表10所示。
表1020nm陶瓷膜超滤截留蛋白基础操作参数
备注:过膜压力(p4)计算公式:(p1+p2)/2-p3;
额定水洗通量:过膜压力(p4)为1bar、温度为65-75℃间的通量。
实施例1dhi标准物质的设计
本实施例提供了一种奶牛生产性能测定(dhi)标准物质,包括:
脂肪的质量百分数范围为0.20%-6.00%,设计12个水平梯度;蛋白质的质量百分数范围为2.00%-4.50%,设计6个水平梯度;乳糖的质量百分数范围为4.00%-5.00%,设计4个水平梯度,按照上述质量百分数范围的成分及相应水平梯度经正交设计得到dhi标准物质,所述dhi标准物质包括标准品1-12,如下表1所示:
表1dhi标准物质
实施例2dhi标准物质的调配
一、调配方法
通过预实验将得到的标准品1-12的原料(稀奶油、脱脂乳、膜截留液和膜滤过液)利用foss乳成分分析仪及化学测定法分别测定其脂肪、蛋白和乳糖的含量,另外加上纯水和分析纯乳糖作为原料,输入excel表格;利用其规划求解功能计算出各标准品原料的用量,然后进行配方调配;通过化学测定法测定产品的化学成分,考察其与标准品的符合程度。下表2是标准品1的调配示例。
表2标准品1调配表
二、调配的dhi标准物质的检验
将按照上述步骤一中调配的产品送到3个经过认证的分析实验室,利用经典化学方法检测其脂肪、蛋白和乳糖含量,剔除异常值后进行平均,然后和标准品设计值进行比较,验证调配方法的可行性。表2的标准品1-10的调配的产品的验证结果如下表3-5:
表3产品脂肪含量与标准品设计含量的比较
由表3可以看出:产品的脂肪含量都大于标准品设计含量,且差值的范围在0.16%~0.25%之间,平均值为0.21%,超过许可范围,但其差值的标准差很小(0.03%),可能是由于foss乳成分分析仪测定的原料脂肪含量与化学法有偏差,可以通过校准来解决。
表4产品蛋白含量与配方设计含量的比较
由上表4可以看出:产品的蛋白含量都小于标准品设计含量,平均差值为-0.08%,稍大于允许范围,其差值的标准差为0.04%,在许可范围之内,说明产品的蛋白质含量和标准品的符合程度较好。
表5产品乳糖含量与配方设计含量的比较
由表5可以看出:产品的乳糖含量和标准品设计含量的差值呈现不规律分布,平均差值为-0.04%,在允许范围内,其差值的标准差为0.06%,说明产品的乳糖含量和标准品的符合程度较好。
由以上结果显示,本发明的dhi标准物质及其调配方法是可行的,只要对foss乳成分分析仪进行定期校准,可以使调配出的产品与设计配方有良好的符合度。
实施例3dhi标准物质的制备
本实施例提供了一种制备dhi标准物质的制备方法,包括如下步骤:
(1)用95℃以上热水对管式杀菌机进行消毒处理,随后取原料奶加入至管式杀菌机进行热处理,热处理温度为50℃,处理时间为18s;
(2)将热处理后的原料奶直接加入乳脂分离机进行脱脂处理,得到的脱脂奶和乳脂肪分别进入不同储存罐中,备用;
(3)对脱脂奶进行微滤除菌,过滤设备采用pall陶瓷膜过滤设备,滤膜选择1.4微米级的陶瓷膜柱,将所述陶瓷膜柱安装至pall陶瓷膜过滤设备,以不大于8℃/min的速度升温,在升温过程中清洗所述陶瓷膜柱3次,升温至50-55℃之间后将脱脂奶泵入物料罐内,开启p1,5秒后开启p2,保持过膜压力3.0bar进行膜滤除菌,收集的滤液作为第一滤过液,除菌奶量达到生产要求后,用50-60℃热水连续清洗,降温后更换陶瓷膜柱(注意降温速度不大于8℃/min)。整个操作过程中注意物料与陶瓷膜柱温差不能超过10℃;
(4)取部分的第一滤过液进行超滤浓缩,过滤设备采用pall陶瓷膜过滤设备,滤膜选择20nm级的陶瓷膜,在使用前须保证膜水通量至少为70l/h,料液温度保持为48-52℃(减少对成分的破坏),初始过膜压力应为1.0mpa,然后逐渐增加过膜压力至2.3mpa,浓缩2.5-3h,收集滤液和截留液,收集的滤液作为第二滤过液,膜滤完成后,采用截留液对膜进行反冲洗10-15min,以使粘附在膜表面的蛋白回到截留液中,得到浓度高且均匀的截留液;
进一步的,为提高重复使用的陶瓷膜的膜通量和降低膜通量下降速度,经反冲洗后的陶瓷膜进行清洗的程序,包括:将反冲洗后的陶瓷膜,先用清水冲洗,然后用质量百分比1.5-2%氢氧化钠溶液清洗30分钟,再以质量百分比0.15-0.2%次氯酸钠清洗30分钟,然后水洗15分钟;再用质量百分比0.2%的硝酸溶液清洗30分钟,最后再用水洗15分钟;
(5)取剩余的第一滤过液与所述乳脂肪混合得到稀奶油、第二滤过液、截留液进行乳成分快速检测。根据配料成分,利用配方计算软件确定标准品1-12的配方调配;调配原料主要包括:第一滤过液,主要成分为蛋白质、水、乳糖;稀奶油,为由乳脂分离之后的乳脂肪和第一滤过液按一定的比例混合,使得乳脂肪含量在12%-17%之间;第二滤过液,主要成分为水和无机盐;截留液,乳蛋白含量必须保证达到6.0%以上;纯水,由二级反渗透系统处理后的纯净水,电导率指标在2μs/cm以下;乳糖,为分析纯;防腐剂,重铬酸钾,防腐剂添加量为使得最终调配好的dhi标准物质中的各标准品中重铬酸钾质量百分比为0.06%;
(6)灌装,将调配好的奶样泵入自动灌装机进行灌装,操作员严格按照灌装机操作规范进行标准物质灌装处理,并贴上标签,装入周转箱;将周转箱放入4℃恒温冰箱中暂存;将2套标准物质装入标准物质运输箱,在样品顶部及底部等位置放置一定数量的冰袋以保持低温;分发,包装好的标准物质,采用特快专递分发到全国各地奶牛生产性能测定实验室;定值,在定值步骤中,将该批次生产的标准物质送至2家平行检测实验室,利用经典化学方法检测样品化学值,并使用foss乳成分分析仪检测仪器值。经典化学方法检测采用国标法检测:蛋白质测定采用凯氏定氮法(gb5009.5-2010)、脂肪测定采用重量法(gb5413.3-2010)、乳糖测定采用液相色谱法(gb5413.5-2010)。同时检测微生物指标(gb4789.18-2010、gb4789.2-2010)。对平行检测结果进行分析处理,剔除异常值,计算平均值及不确定度,和仪器值进行分析比较,确定标准品1-12的标准值,并发送到各dhi测定实验室用于仪器校准。
实施例4
本实施例提供了一种制备dhi标准物质的制备方法,包括如下步骤:
(1)用95℃以上热水对管式杀菌机进行消毒处理,随后取原料奶加入至管式杀菌机进行热处理,热处理温度为48℃,处理时间为20s;
(2)将热处理后的原料奶直接加入乳脂分离机进行脱脂处理,得到的脱脂奶和乳脂肪分别进入不同储存罐中,备用;
(3)对脱脂奶进行微滤除菌,过滤设备采用pall陶瓷膜过滤设备,滤膜选择1.4微米级的陶瓷膜柱,将所述陶瓷膜柱安装至pall陶瓷膜过滤设备,以不大于8℃/min的速度升温,在升温过程中清洗所述陶瓷膜柱3次,升温至50-53℃之间后将脱脂奶泵入物料罐内,开启p1,6秒后开启p2,保持过膜压力2.8bar进行膜滤除菌,收集第一滤过液,除菌奶量达到生产要求后,用50-60℃热水连续清洗,降温后更换陶瓷膜柱(注意降温速度不大于8℃/min)。整个操作过程中注意物料与陶瓷膜柱温差不能超过10℃;
(4)取部分的第一滤过液进行超滤浓缩,过滤设备采用pall陶瓷膜过滤设备,滤膜选择20nm级的陶瓷膜,在使用前须保证膜水通量至少为70l/h,料液温度保持为48-52℃(减少对成分的破坏),初始过膜压力应为1.0mpa,然后逐渐增加过膜压力至2.25mpa,浓缩2.5h,收集第二滤过液和截留液,膜滤完成后,采用截留液对膜进行反冲洗10min,以使粘附在膜表面的蛋白回到截留液中,得到浓度高且均匀的截留液;
(5)取剩余的第一滤过液与所述乳脂肪混合得到稀奶油、第二滤过液、截留液进行乳成分快速检测。根据配料成分,利用配方计算软件确定标准品1-12的配方调配;调配原料主要包括:第一滤过液,主要成分为蛋白质、水、乳糖;稀奶油,为由乳脂分离之后的乳脂肪和第一滤过液按一定的比例混合,使得乳脂肪含量在12%-17%之间;第二滤过液,主要成分为水和无机盐;截留液,乳蛋白含量必须保证达到6.0%以上;纯水,由二级反渗透系统处理后的纯净水,电导率指标在2μs/cm以下;乳糖,为分析纯;
(6)灌装、4℃恒温冰箱中冷藏、装箱、分发和定值。
实施例5
本实施例提供了一种制备dhi标准物质的制备方法,包括如下步骤:
(1)用95℃以上热水对管式杀菌机进行消毒处理,随后取原料奶加入至管式杀菌机进行热处理,热处理温度为52℃,处理时间为15s;
(2)将热处理后的原料奶直接加入乳脂分离机进行脱脂处理,得到的脱脂奶和乳脂肪分别进入不同储存罐中,备用;
(3)对脱脂奶进行微滤除菌,过滤设备采用pall陶瓷膜过滤设备,滤膜选择1.4微米级的陶瓷膜柱,将所述陶瓷膜柱安装至pall陶瓷膜过滤设备,以不大于8℃/min的速度升温,在升温过程中清洗所述陶瓷膜柱3次,升温至52-55℃之间后将脱脂奶泵入物料罐内,开启p1,4秒后开启p2,保持过膜压力3.0bar进行膜滤除菌,收集第一滤过液,除菌奶量达到生产要求后,用50-60℃热水连续清洗,降温后更换陶瓷膜柱(注意降温速度不大于8℃/min)。整个操作过程中注意物料与陶瓷膜柱温差不能超过10℃;
(4)取部分的第一滤过液进行超滤浓缩,过滤设备采用pall陶瓷膜过滤设备,滤膜选择20nm级的陶瓷膜,在使用前须保证膜水通量至少为70l/h,料液温度保持为48-52℃(减少对成分的破坏),初始过膜压力应为1.0mpa,然后逐渐增加过膜压力至2.45mpa,浓缩3h,收集第二滤过液和截留液,膜滤完成后,采用截留液对膜进行反冲洗15min,以使粘附在膜表面的蛋白回到截留液中,得到浓度高且均匀的截留液;
(5)取剩余的第一滤过液与所述乳脂肪混合得到稀奶油、第二滤过液、截留液进行乳成分快速检测。根据配料成分,利用配方计算软件确定标准品1-12的配方调配;调配原料主要包括:第一滤过液,主要成分为蛋白质、水、乳糖;稀奶油,为由乳脂分离之后的乳脂肪和第一滤过液按一定的比例混合,使得乳脂肪含量在12%-17%之间;第二滤过液,主要成分为水和无机盐;截留液,乳蛋白含量必须保证达到6.0%以上;纯水,由二级反渗透系统处理后的纯净水,电导率指标在2μs/cm以下;乳糖,为分析纯;
(6)灌装、4℃恒温冰箱中冷藏、装箱、分发和定值。
实验例1原料奶的热处理温度的考察
一、实验方法
对原料奶进行热处理,目的是为了便于后续的乳脂分离和陶瓷膜过滤操作,要求选择对原料奶成分影响最小的温度处理。以管式热杀菌机对原料奶进行加热处理,分别选取处理温度40℃、50℃、60℃、73℃,以foss乳成分分析仪检测样品的脂肪、蛋白和乳糖含量,考察热处理温度对原料奶化学成分中红外测定值的影响;将样品储存在4℃,每天测定其乳成分,考察热处理奶样随时间的变化情况。
二、实验结果和分析
1、不同处理温度对原料奶脂肪、蛋白和乳糖的影响如下表6-表8所示。
表6热处理温度对原料奶脂肪含量的影响
表7热处理温度对原料奶蛋白质含量的影响
表8热处理温度对原料奶乳糖含量的影响
由表6可以看出:50℃和60℃加热处理对原料奶脂肪含量的影响较小;由表7可以看出:50℃加热处理对原料奶蛋白质含量的影响较小。由表8可以看出:40℃和50℃加热处理对原料奶蛋白质含量的影响较小。
2、热处理后的奶样随储存时间的变化情况如图2-图4所示。
由图2可以看出:50℃热处理后的原料奶与未处理的原料奶(图中原奶)最接近,其次是60℃热处理奶;图3显示:50℃热处理后的原料奶与未处理的原料奶(图中原奶)最接近,且其变化趋势与原料奶更加接近,其次是73℃热处理奶;由图4可以看出:50℃热处理后的原料奶与未处理的原料奶(图中原奶)最接近,其随时间的的变化趋势与原料奶更加接近。
3、结论
综合以上实验结果,50℃热处理其成分以及随时间的变化最接近原料奶,同时为了达到最佳的乳脂分离效果,生产上选取50℃的热处理方式。
实验例2陶瓷膜微滤除菌和超滤浓缩的考察
一、陶瓷膜微滤除菌的效果
按照实施例3操作,分别检测收集的第一滤过液(膜滤除菌奶)和未经处理的原始原料奶的菌落总数,计算除菌率,结果如下表9。
表9陶瓷膜微滤除菌效果
由表9可见,本发明的微滤除菌步骤原料奶的除菌率可达到99.5%以上,完全可以满足生产需要。
二、超滤时间对截留液蛋白含量的影响
以20nm陶瓷膜对除菌后的原料奶进行浓缩处理,可得到高浓度的蛋白截留液,用于调配高蛋白浓度配方。利用excel规划求解功能,通过对配方模拟计算发现,要将蛋白浓度达到4.2%的标准品调配出来,需要得到蛋白质含量(质量百分比)为6.0%以上的截留液。因此,按照实施例3操作,超滤时间分别选择0h、0.5h、1h、1.5h、2h、2.5h、3h,检测不同超滤时间下获得的截留液中的蛋白浓度,检测结果见下表11。
表1120nm陶瓷膜超滤时间对截留液中蛋白质含量的影响
由表11可以看出:当超滤时间为2.5-3h时,基本可保证得到截留液中的蛋白质浓度6.0%以上的截留液。
实验例3产品均匀性的考察
产品均匀性是dhi标准物质的一项重要考察指标。为了解每批次生产的dhi标准物质成分的均匀性,设计了灌装均匀度试验。
一、灌装均匀度实验标准品的样品乳成分检测
将实施例3中获得的标准品1-12号各调配6公斤料液,以半自动灌装机进行灌装,按照灌装顺序,每隔5瓶抽取1瓶样品瓶进行编号,共抽取20瓶产品,用foss乳成分快速分析仪依次对样品进行成分检测,每瓶检测3次,检测结果如下表所示,表格中“#1样品”代表标准品1的样品,“#2样品”……“#12样品”,以此类推。
表12灌装均匀度实验标准品1的样品乳成分检测值
表13灌装均匀度实验标准品2的样品乳成分检测值
表14灌装均匀度实验标准品3的样品乳成分检测值
表15灌装均匀度实验标准品4的样品乳成分检测值
表16灌装均匀度实验标准品5的样品乳成分检测值
表17灌装均匀度实验标准品6的样品乳成分检测值
表18灌装均匀度实验标准品7的样品乳成分检测值
表19灌装均匀度实验标准品8的样品乳成分检测值
表20灌装均匀度实验标准品9的样品乳成分检测值
表21灌装均匀度实验标准品10的样品乳成分检测值
表22灌装均匀度实验标准品11的样品乳成分检测值
表23灌装均匀度实验标准品12的样品乳成分检测值
二、分析方法
标准物质的均匀性检验数理统计方法有很多,有方差分析法、平均值一致性检验法、极差法、t检验法、“三分之一”检验法。这里采用的是能充分利用测试数据信息的方差分析法。
为检验样品均匀性,设抽取了m个样品,用精密度高的实验方法,在相同条件下得m组等精度测量数据如下:
(1)x11,x12,……
(2)x21,x22,……
……
(m)xm1,xm2,
设
则组间差方和:
组内差方和:
记v1=m-1(组间自由度),v2=n-m(组内自由度)
作统计量f:
因此可认为,该统计量是自由度(ν1,ν2)的f分布变量。
根据自由度(ν1,ν2)以及给定的显著性水平α,根据f表可查得临界的fα值。若f<fα,即统计检验结果不存在显著性差异时,就可判断所测定的样品是均匀的,若f≥fα,即统计检验结果存在显著性差异时,若记这个差异的标准偏差为sh,则有
如果每个ni均相同且都为n时,则上式变为:
经过均匀性检验,可能得出三种结果:
(1)sh<<s2,即同方法测量的标准偏差相比,物质的不均匀所引起的标准偏差可忽略不计,此时可认为样品均匀性好。
(2)sh>>s2,即不均匀性所带来的标准偏差远远大于方法测量的标准偏差,且在总的不确定度中是主要因素,在这种情况下,标准物质需要重新混匀或该物质的定值必须逐个样品进行。
(3)不均匀性所产生的标准偏差与方法测量的标准偏差大小相近,这时作为总的不确定度必须把均匀性因素考虑进去。
1、根据以上分析方法,由方差分析法计算步骤一中的每一瓶的瓶内方差,每个样品20瓶的瓶间方差和统计量f,所得数据见表24。
表24dhi标准物质中脂肪、蛋白、乳糖含量的瓶内方差、瓶间方差和统计量f
由f表查得临界的f0.05(19,40)=1.84,比较f与f0.05(19,40)样品的脂肪存在差异,蛋白有一部分存在差异,乳糖有一个存在差异。
2、用高精度的方法进行均匀性测量或某方法在合适含量范围内具有较高的测量精密度时,会发生应该通过均匀性测量的不被通过。这是由于组间存在微小的不均匀性q1,但组内差的平方和q2更小,分子数字不大,但当分母趋于0时,分数趋近∞。当均匀性检验数据的标准偏差s小到一定程度,表示其测量值都落在规定的不确定度范围内,无论统计量是否超过临界值,可以认为样品是均匀的。根据fossft+仪器的技术参数,乳脂肪的精密度小于1%,乳蛋白和乳糖精密度小于0.9%,由于仪器精密度较高,瓶内均匀性非常好,造成测定瓶间的重复性相对稍差,所以计算sh值,与s2进行比较,数据见表25。
表25灌装抽样产品脂肪、蛋白、和乳糖含量的瓶内标准差和瓶间标准差
由表25可知:所有样品三种成分的sh<<s2,可以判定制作出的标准物质是均匀的。
实验例4产品贮藏过程中成分稳定性研究
为了解实施例3中制备的dhi标准物质的贮藏稳定性,每2天用foss乳成分分析仪分别测定其脂肪、蛋白和乳糖含量,共进行8次(15天)测定;每次测定每个标准品选取3瓶样品,每瓶测定3次。
按照gb/t15000.3-2008分析计算各配方在贮存期间乳成分的变化,计算其平均值、标准差(sd)、斜率和截距,并依据直线拟合法判断标准样品稳定性。
dhi标准物质贮存过程中乳成分的变化如表26所示。
表26dhi标准物质贮存过程中成分含量变化
计算各配方在贮存期间乳成分的平均值(md)、标准差(sd),如表27所示。
表27dhi标准物质贮存过程中各成分平均值(md)及标准差(sd)
由表27可以看出:在4℃贮存条件下,所有标准品的乳成分在15天内基本没有变化,其标准差都在0-0.02%之间,远远低于国标检测方法的精确度要求,说明这种微小的变化,对经典化学方法检测的结果完全没有影响。如果以美国采用的sd%≤0.04%的标准判断,15天之内产品各成分的变化都在许可的范围。
对dhi标准物质各成分在15天的贮存过程中的变化,采用回归法进行直线拟合,所得拟合直线的斜率和截距如表28所示。
表28dhi标准物质贮存过程中各成分变化曲线的斜率和截距
通过对标准品各成分与贮存时间回归曲线的斜率和截距的计算可知:在贮存期间所有标准品、所有成分的斜率都接近0,说明产品在贮存过程中各成分都非常稳定;截距和平均值的吻合程度非常好,说明回归曲线与各检测点的差距非常小,直线性好。
根据gb/t15000.3-2008,对所得的数据进行进一步统计分析,计算其t*s(b1)值,并与其斜率进行比较,如果斜率的绝对值大于其t*s(b1)值,说明其斜率是显著的,观测到不稳定性;如果斜率的绝对值小于其t*s(b1)值,说明其斜率是不显著的,未观测到不稳定性。结果见下表,
表29dhi标准物质贮存过程中各成分变化曲线的斜率显著性分析
由表29可以看出:所有标准品产品的斜率绝对值都小于其斜率相关的不确定度s(b1)与t0.95,n-2的乘积,故斜率是不显著的,说明各标准品的脂肪、蛋白、乳糖含量在15天的贮藏过程中均未观测到不稳定性。
实验例5产品贮存过程中微生物稳定性研究
选取实施例3中制备的标准品5-9样品(#5-#9),每隔7天检测一次产品的细菌总数,直到22天,其菌落变化情况如图5所示。
由图5可以看出,dhi标准物质的初始细菌总数就很低,在30-90cfu/ml之间,在22天内所有标准品样品的菌落总数都呈现逐渐下降趋势,除#8号标准品的菌落数在20cfu//ml左右外,#5、#6、#7、#9的细菌总数都降到了10cfu/ml以下,甚至达到完全无菌的状态(检测出的菌落数为0cfu/ml),这是因为产品的初始菌数很低,再加上添加了0.06%的防腐剂重铬酸钾,对微生物起到了很大的抑制作用。
实验例6产品运输过程中成分稳定性研究
将实施例3中制备的dhi标准物质按规定包装后,放在运输车上,在常温条件下每天行驶6-8小时,取出3箱(每个标准品合计6瓶)样品进行成分含量检测,共进行3天,依据直线拟合法比较斜率显著性进而判断标准样品稳定性。结果如表30、31、32所示。
表30dhi标准物质运输过程中脂肪变化曲线的斜率显著性分析
表30续
表31dhi标准物质运输过程中蛋白变化曲线的斜率显著性分析
表31续
表32dhi标准物质运输过程中乳糖变化曲线的斜率显著性分析
表32续
由表30可以看出运输过程乳脂肪数据的斜率b1的绝对值均小于斜率相关的不确定度s(b1)与t0.95,n-2的乘积。故斜率是不显著的,因而在运输过程中,未观测到脂肪含量的不稳定性。
由表31可以看出运输过程乳蛋白数据的斜率b1的绝对值均小于斜率相关的不确定度s(b1)与t0.95,n-2的乘积。故斜率是不显著的,因而在运输过程中,未观测到蛋白含量的不稳定性。
由表32可以看出运输过程乳糖数据的斜率b1的绝对值均小于斜率相关的不确定度s(b1)与t0.95,n-2的乘积。故斜率是不显著的,因而在运输过程中,未观测到乳糖含量的不稳定性。
实验例7dhi标准物质的校准效果研究
校准样品的特性如样品数量、组分浓度和范围分布(高杠杆值样品存在)、脂肪和蛋白浓度相关性及连续批次样品间特性的变化等都影响校准效果(kaylegianetal.,2006)。本发明的dhi标准物质通过正交设计去除了高杠杆值样品,脂肪和蛋白浓度没有相关性,且每套标准样品之间化学成分含量、斜率和截距稳定。
本实验通过将实施例3中制备的dhi标准物质的mir测定值同参考化学值比较,计算各实验室每台仪器测定实施例3中制备的dhi标准物质的脂肪、蛋白的均差(md)和标准差(sdd),绘制校准奶样脂肪和蛋白的sdd和md的折线图评价校准性能。
根据美国标准,要求md%值在±0.05%以内,sdd%在±0.06%以内。
各实验室使用实施例3中的dhi标准物质对中红外乳成分分析仪校准后脂肪md%值变化图如图6所示,2012年6月-2013年6月,除内蒙实验室2012年7月、陕西实验室2012年8月和南京卫岗2013年1月脂肪md%值在±0.2%范围外,其余各实验室脂肪md%值均在±0.2%以内,2012年7月和8月两个月,各实验室的脂肪md%波动较大,可能由于夏季温度较高,实施例3的dhi标准物质在运输过程中脂肪发生变化,影响测定结果。各实验室使用实施例3的dhi标准物质校准仪器后的脂肪md%呈逐渐减小的趋势,仪器测定值与样品化学参考值更加接近,各实验室测定水平趋于一致。总体看来多数实验室脂肪md%值集中分布在±0.05%以内。
各实验室使用实施例3中的dhi标准物质对中红外乳成分分析仪校准后蛋白md%值变化图如图7所示,2012年6月-9月,各实验室蛋白md%相对较高,波动较大,最高的陕西实验室2012年6月测定蛋白md%值达0.359%。随后除山西实验室2012年12月、沈阳辉山实验室2013年1月和黑龙江完达山实验室2013年5月蛋白md%值较高外,其它实验室各月份的md%均分布在-0.15%和0.10%间,且曲线波动逐渐趋于平缓,大部分实验室蛋白md%集中分布在±0.05%以内。
各实验室使用实施例3中的dhi标准物质对中红外乳成分分析仪校准后脂肪sdd%值变化图如图8所示,2012年6月-2013年6月,各实验室脂肪sdd%均在0-0.2%内,且多数实验室sdd%值小于0.06%,沈阳辉山实验室全年看来脂肪sdd%值普遍较高,均大于0.06%,说明该实验室仍需提高其仪器操作能力。
各实验室使用实施例3中的dhi标准物质对中红外乳成分分析仪校准后蛋白sdd%值变化图如图9所示,2012年6月-2012年12月间,各实验室蛋白的sdd%值波动较大,南京卫岗实验室2012年10月蛋白sdd%值甚至达到0.176%,远高于美国标准规定值0.06%;2013年1月-6月,除新疆实验室2月和3月份的蛋白sdd值较高,其余各实验室蛋白sdd%值分布更加集中,均在0-0.06%内。
综上可知,全国各dhi实验室蛋白、脂肪的md%和sdd%值多数符合美国标准,仅有一少部分超出美国标准规定范围,说明实施例3制备的dhi标准物质的生产和供应提高了各实验室的测定水平,使其各成分测定值更接近于化学参考值,通过一年的使用校准,各实验室测定水平趋于平稳;少数超出部分通过走访和电话回访等方式发现,仪器校准效果不太理想的原因主要分为3个方面:(1)仪器近期经过维修或更换零部件(2)另有一些实验室则是由于仪器操作人员的更换,操作人员业务不熟练,从而导致部分实验室个别月份仪器测定不稳定(3)标准物质在运输过程中由于夏季温度较高,部分校准奶样在运输过程中发生化学腐败(如蛋白水解或脂肪水解),从而造成校准出现异常,校准效果较差。
显然,上述实施例仅仅是为清楚地说明所作的举例,而并非对实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。而由此所引伸出的显而易见的变化或变动仍处于本发明创造的保护范围之中。
- 还没有人留言评论。精彩留言会获得点赞!