包含可生物降解聚酯的医疗器械和材料的制作方法
包含可生物降解聚酯的医疗器械和材料
1.本发明涉及抗微生物制剂,特别是包含与小肽或类似肽的分子配混的聚合物的制剂。这些制剂特别用于医疗器械。
2.诸如导管、骨科器械和其他植入物以及外科紧固件如缝合线等医疗器械的使用已日益增加。尽管器械设计和外科手术有所改善,但与此类医疗器械相关的感染仍是主要问题。常规抗生素治疗通常由于实际感染部位和感染部位周围区域的抗生素水平低而失败。引入的生物材料/器械上存在的生物膜会损害抗生素治疗的功效,而耐药菌株的存在也会损害抗生素治疗的功效。
3.抗生素释放涂层已知用于医疗器械,诸如缝合线和导管。然而,患者可能感染抗性细菌,并且由于局部释放的模式,存在抗生素的浓度梯度,这增加了抗性细菌的竞争性选择的风险。特别地,用三氯生浸渍的缝合线在市场上销售,认识到该抗生素已过度使用并导致耐药性细菌菌株的发展,此外,已知其有助于对其他抗生素的交叉耐药性。因此,卫生当局面临限制其使用的压力。尽管研究表明三氯生涂敷缝合线可减少手术部位感染发生,但使用其他活性剂(诸如氯己定)涂层的缝合线数据有限(onesti等人,2018欧洲医学和药理学科学综述22:第5729-5739页(onesti et al.2018european review for medical and pharmacological sciences 22:pages 5729-5739))。
4.术后伤口感染是美国第三大常见的医院获得性感染。手术部位感染导致患者严重不适,是潜在的危及生命的事件,并延长住院时间。微生物粘附到缝合线和其他外科紧固件的表面已经被认为是产生切口感染的原因之一。
5.因此,显然需要替代的缝合线和其他医疗器械,其可起到提供抗微生物剂的受控释放以及限制器械本身定殖的作用。
6.本发明人已经发现,他们能够将某些小的抗微生物肽与可生物降解聚酯组合以提供本身可使用的材料(例如,通过3d打印制成的器械)或作为另一种医疗器械的涂层。
7.抗微生物肽是作为新抗微生物剂的前景斐然的候选物,因为他们对广谱浮游细菌和生物膜(包括抗生素抗性菌株)具有活性。此外,由于细菌的作用模式(包括脂膜的破坏,而非作用于蛋白质靶),细菌不太可能对这些快速作用的肽产生抗性。然而,将肽配制到可提供受控释放的基质中并不简单,与其他类型的药物相比,肽通常溶解性差,并且通常在将肽混合或配混到基质中所需要的温度下降解。
8.本发明人已经制备了可用于提供活性抗微生物剂的受控释放的材料,即,抗微生物剂是可浸出的并且可抑制周围环境中的细菌生长。抗微生物剂还用于控制材料内和/或涂覆有聚合物和抗微生物剂的共混物的器械上的微生物生长。
9.因此,在一个方面,本发明提供了一种包含可生物降解聚酯的制剂,所述可生物降解聚酯配混有式(i)的化合物
10.aa-aa-aa-x-y
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ(i)11.其中,以任意顺序,所述aa(氨基酸)部分中的2个是阳离子氨基酸,优选赖氨酸或精氨酸,但可以是组氨酸或在ph 7.0携带正电荷的任何非遗传编码或修饰的氨基酸,并且所述aa中的1个是具有大亲脂性r基团的氨基酸,所述r基团具有14至27个非氢原子并且优
选含有2个或更多个、例如2或3个可稠合或连接的环状基团,这些环状基团通常包含5或6个非氢原子,优选6个非氢原子(在稠合环的情况下,非氢原子当然可以共享);
12.x是n原子,其可以被支链或非支链的c
1-c
10
烷基或芳基(例如甲基、乙基或苯基)取代,但优选不被支链或非支链的c
1-c
10
烷基或芳基(例如甲基、乙基或苯基)取代,并且该基团可以包含至多2个选自n、o和s的杂原子;以及
13.y选自r
1-r
2-r3、
14.r
1-r
2-r
2-r3、r
2-r
2-r
1-r3、r
1-r3和r415.其中:
16.r1是c、o、s或n,优选c;
17.r2是c;
18.r1和r2各自可以被c
1-c4烷基取代或未被取代,优选y是-r
1-r
2-r3(其中r1优选是c)并且优选该基团不被取代,但y是-r
1-r
2-r
2-r3或r
2-r
2-r
1-r3时,则优选r1和r2中的一个或更多个被取代;
19.r3是包含1至3个环状基团的基团,所述环状基团各自具有5或6个非氢原子(优选全部为c原子,但可选地还含有n、o或s),所述环状基团中的2个或更多个可为稠合的;环中的一个或更多个可被取代并且这些取代可包括(但通常不会包括)极性基团、合适的取代基,包括卤素,优选溴或氟以及c
1-c4烷基;r3包含最多15个非氢原子,优选5至12个,最优选为苯基;以及
20.r4是具有2至20个非氢原子的脂族部分,优选这些非氢原子是碳原子,但可以并入氧、氮或硫原子,优选r4包含3至10个、最优选3至6个非氢原子,并且该部分可以是直链、支链或环状的。如果r4基团包含环状基团,则其优选直接连接至x的氮原子。
21.优选的化合物并入直链或支链的r4基团,特别是直链或支链的烷基,包括乙基、丙基、异丙基、丁基、异丁基、仲丁基、叔丁基、戊基及其异构体、己基及其异构体等;特别优选丙基、异丙基、丁基和异丁基。
22.在一些实施方案中,r4是具有6至16个非氢原子的脂族部分(优选烷基),优选这些是碳原子,但可以并入氧、氮或硫原子,并且所述部分可以是直链、支链或环状的。
23.一些优选的实施方案中,r4是异丙基。
24.在包含环状基团的r4基团中,优选其中r4是环己基或环戊基的分子。
25.可提供阳离子氨基酸的合适的非遗传编码氨基酸和修饰氨基酸包括赖氨酸、精氨酸和组氨酸的类似物,诸如高赖氨酸、鸟氨酸、二氨基丁酸、二氨基庚二酸、二氨基丙酸和高精氨酸以及三甲基赖氨酸和三甲基鸟氨酸、4-氨基哌啶-4-羧酸、4-氨基-1-甲脒哌啶-4-羧酸和4-胍基苯丙氨酸。
26.aa的大亲脂性r基团可含有杂原子,诸如o、n或s,通常存在不超过一个杂原子,优选其为氮。该r基团优选具有不超过2个极性基团,更优选没有极性基团或具有一个极性基团,最优选没有极性基团。
27.优选为肽的化合物优选具有式(ii)
28.aa
1-aa
2-aa
1-x-y
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(ii)
29.其中:
30.aa1是阳离子氨基酸,优选赖氨酸或精氨酸,但可以是组氨酸或在ph 7.0带有正电
荷的任何非遗传编码或修饰的氨基酸;
31.aa2是具有大亲脂性r基团的氨基酸,所述r基团具有14至27个非氢原子并且优选含有2个或更多个、例如2或3个可稠合或连接的环状基团,这些环状基团将通常包含5或6个非氢原子,优选6个非氢原子;以及
32.x和y如上所定义。
33.进一步优选的化合物包括式(iii)和(iv)的化合物:
34.aa
2-aa
1-aa
1-x-y
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(iii)
35.aa
1-aa
1-aa
2-x-y
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(iv)
36.其中aa1、aa2、x和y如上所定义。更优选式(ii)的分子。
37.在上述化合物中,某些化合物是特别优选的。特别地,其中以下化合物是最优选的:具有大亲脂性r基团的氨基酸(本文方便地称为aa2)是三丁基色氨酸(tbt)或联苯基丙氨酸衍生物,诸如phe(4-(2-萘基))[本文也称为bip(4-(2-萘基)]、phe(4-(1-萘基))[本文也称为bip(4-(1-萘基)]、bip(4-n-bu)、bip(4-ph)或bip(4-t-bu);phe(4-(2-萘基))和tbt。在一些优选的实施方案中,具有大亲脂性r基团的氨基酸是三丁基色氨酸(tbt)。
[0038]
另一组优选的化合物是其中如上定义y为-r
1-r
2-r3的那些,优选其中r1和r2是未取代的,最优选其中r1和r2都是碳原子。
[0039]
进一步优选的一组化合物是其中-x-y一起为基团-nhch2ch2ph的那些。
[0040]
所述化合物包括所有对映体形式,包括d和l氨基酸以及由氨基酸r基团和c-末端封端基团
“‑
x-y”内的手性中心产生的对映体。β和γ氨基酸以及α氨基酸包括在术语“氨基酸”内,n-取代的甘氨酸也包括在术语“氨基酸”内,n-取代的甘氨酸可以全部被认为是aa单元。本发明的分子包括β肽和缩肽。
[0041]
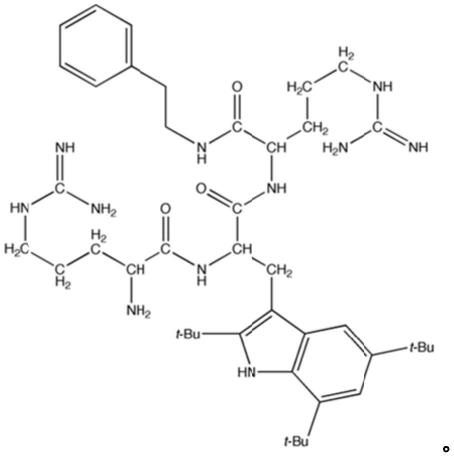
最优选的化合物如下:
[0042][0043]
t-bu表示叔丁基。并入氨基酸2,5,7-三-叔丁基-l-色氨酸的第二种化合物是本发明中最优选使用的化合物(本文也称为amc-109)。并入其他阳离子残基代替精氨酸(特别是赖氨酸)的该化合物的类似物也是高度优选的。还高度优选并入如上所定义的替代c端封端基团的类似物。
[0044]
进一步优选的一组化合物是以下的那些:其中-x-y一起选自-nhch(ch3)2、-nh(ch2)5ch3、-nh(ch2)3ch3、-nh(ch2)2ch3、-nhch2ch(ch3)2、-nh环己基和-nh环戊基的那些,特别优选的是其中-x-y为基团-nhch(ch3)2或-nh(ch2)5ch3的化合物。特别优选的一组化合物是其中-x-y一起为nhch(ch3)2的那些。
[0045]
优选的化合物是其中aa1为精氨酸、aa2为三丁基色氨酸且-x-y一起为nhch(ch3)2的化合物。
[0046]
用于本发明的化合物优选为肽。
[0047]
式(i)至(iv)的化合物可以是肽模拟物,并且本文描述和定义的肽的肽模拟物也代表根据本发明使用的化合物。肽模拟物的特征通常在于保留了其肽等价物的极性、三维大小和功能性(生物活性),但是其中肽键通常被更稳定的键连取代。“稳定的”是指对水解酶的酶促降解更具抗性。通常,取代酰胺键的键(酰胺键替代物)保留酰胺键的许多性质,例如构象、空间体积、静电特性、氢键的可能性等,“药物设计和开发(drug design and development)”第14章(krogsgaard,larsen,liljefors和madsen(编著)1996,horwood学术出版社)提供了肽模拟物的设计和合成技术的一般讨论。在分子与膜反应而非与酶的特定活性位点反应的当前情况下,所描述的精确模拟亲和力和功效或底物功能的一些问题并不相关,并且可以基于给定的肽结构或所需官能团的基序容易地制备肽模拟物。合适的酰胺键替代物包括以下基团:n-烷基化(schmidt,r.等人,int.j.peptide protein res.,1995,46,47)、逆反酰胺(chorev,m和goodman,m.,acc.chem.res,1993,26,266)、硫代酰胺(sherman d.b.和spatola,a.f.j.am.chem.soc.,1990,112,433)、硫酯、膦酸酯、酮亚甲基(hoffman,r.v.和kim,h.o.j.org.chem.,1995,60,5107)、羟基亚甲基、氟乙烯基(allmendinger,t.等人,tetrahydron lett.,1990,31,7297)、乙烯基、亚甲基氨基(sasaki,y和abe,j.chem.pharm.bull.1997 45,13)、亚甲基硫醇(spatola,a.f.,methods neurosci,1993,13,19)、烷烃(lavielle,s.等人,int.j.peptide protein res.,1993,42,270)和磺酰氨基(luisi,g.等人.tetrahedron lett.1993,34,2391)。
[0048]
本发明的肽模拟物化合物通常具有3个可鉴别的亚单位,其大小和功能与氨基酸(aa单元)近似相等。因此,术语“氨基酸”在本文中可方便地用于指肽模拟物化合物的等价亚单位。此外,肽模拟物可具有与氨基酸的r基团等同的基团,并且本文对合适的r基团以及n和c末端修饰基团的讨论比照适用于肽模拟物化合物。
[0049]
如上文引用的教科书中所讨论的,除了酰胺键的取代,肽模拟物可涉及用二肽或三肽模拟物结构取代较大的结构部分,并且在这种情况下,涉及肽键的模拟物部分,诸如吡咯衍生的模拟物可用作二肽取代。然而,优选肽模拟物,因此优选其中酰胺键已被如上所述取代的肽模拟物主链。
[0050]
合适的肽模拟物包括还原的肽,其中通过用还原剂(例如硼烷或氢化物试剂,诸如氢化铝锂)处理将酰胺键还原成亚甲基胺。此类还原具有增加分子整体阳离子性的额外优点。
[0051]
其他肽模拟物包括例如通过逐步合成酰胺官能化的聚甘氨酸而形成的类肽。一些肽模拟物主链将容易地由他们的肽前体获得,诸如已被过甲基化的肽,合适的方法由ostresh,j.m.等人在proc.natl.acad.sci.usa(1994)91,11138-11142中描述。强碱性条件将有利于n-甲基化而不是o-甲基化,并导致肽键和n-末端氮中的一些或全部氮原子的甲基化。
[0052]
优选的肽模拟物主链包括聚酯、聚胺及其衍生物以及取代的烷烃和烯烃。肽模拟物优选具有n和c末端,其可以如本文所述进行修饰。
[0053]
根据本发明使用的化合物(例如,肽)表现出抗微生物活性(通常是抗细菌活性),特别是它们通过直接的膜影响机制发挥细胞毒性作用并且可以被称为膜作用抗微生物剂。这些化合物裂解细胞膜、使细胞膜不稳定或甚至穿透细胞膜。这相对于作用于靶细胞的蛋白质组分(例如细胞表面受体)或与靶细胞的蛋白质组分相互作用的药剂提供了明显的治
疗优势。尽管突变可产生导致抗生素抗性的新形式的靶蛋白,但是,可能性更小的是,发生对脂膜的自由基改变以防止细胞毒性作用。裂解作用导致细胞极为快速死亡,因此具有在细菌有机会繁殖之前杀死细菌的优点。此外,分子可具有杀死或损害靶微生物的其他有用性质,例如抑制蛋白质合成的能力,因此他们可具有多靶活性。
[0054]
用于本发明的化合物可以以任何方便的方式合成。通常,存在的反应性基团(例如氨基、硫醇和/或羧基)将在整个合成期间得以保护。因此,合成中的最后步骤将是对本发明的受保护衍生物进行脱保护。
[0055]
在构建肽时,原则上可以在c-末端或n-末端开始,然而,优选c-末端开始的程序。
[0056]
肽合成的方法是本领域熟知的,但是对于本发明,在固相载体上进行合成可能特别方便,此类载体是本领域熟知的。
[0057]
氨基酸保护基的广泛选择是已知的,合适的胺保护基可包括苄酯基(也称为z)叔丁氧基羰基(也称为boc)、4-甲氧基-2,3,6-三甲基苯磺酰基(mtr)和9-芴基甲氧基-羰基(也称为fmoc)。应当理解,当从c-末端开始构建肽时,胺保护基将存在于每个添加的新残基的α-氨基上,并且在下一个偶联步骤之前需要被选择性地除去。
[0058]
例如,可以使用的羧基保护基包括容易裂解的酯基,诸如苄基(bzl)、对硝基苄基(onb)、五氯苯基(opclp)、五氟苯基(opfp)或叔丁基(otbu)以及固体载体上的偶联基团,例如与聚苯乙烯连接的甲基。
[0059]
硫醇保护基包括对甲氧基苄基(mob)、三苯甲基(trt)和乙酰胺基甲基(acm)。
[0060]
存在多种除去胺保护基和羧基保护基的程序。然而,这些必须与所采用的合成策略一致。侧链保护基必须对用于在下一偶联步骤之前除去临时α-氨基保护基的条件是稳定的。
[0061]
可以通过酸处理,例如用三氟乙酸,同时除去胺保护基(诸如boc)和羧基保护基(诸如tbu)。可以使用氧化剂(诸如碘)选择性地除去硫醇保护基团(诸如trt)。
[0062]
配混(compounding)(“配混的(compounded)”)是用于描述两种聚合物或聚合物与一种或更多种添加剂的混合和/或共混的术语。这可以方便地通过以熔融状态共混或通过在溶液中组合多种组分来实现。本文描述了这两种方法。所得混合物理想地是均匀的或接近均匀的。为了避免疑问,配混不涉及聚酯和式(i)化合物之间的共价连接,而是配混导致聚酯和式(i)化合物之间的非共价的、可释放的缔合。因此,可以认为该化合物与聚酯可释放地缔合。
[0063]
因此,式(i)的化合物能够从本发明的制剂中释放(或从本发明的制剂中浸出或扩散出)。这在本发明的上下文中是重要的,因为式(i)的化合物具有抗微生物活性,并且期望在使用中所述化合物能够从制剂释放至需要抗微生物活性的区域,例如以预防或治疗伤口、手术部位或医疗器械的植入部位的感染。
[0064]
优选地,在使用中,式(i)的化合物从制剂中受控(即,持续)释放。例如,可以释放治疗有效量的化合物至少6、8、12或14小时。治疗有效量将优选导致递送至局部环境的化合物浓度超过化合物对目标细菌的最小抑制浓度(mic)。可以通过在本发明的制剂的顶部(例如作为医疗器械上的外层)施加未与活性化合物配混的可生物降解聚酯的层来延长释放时间。
[0065]
可以通过任何合适的方法容易地确定活性化合物从本发明制剂中释放的能力,并
且技术人员熟悉这些方法。在本文的实施例中描述了合适的方法。例如,可以使用根据本发明的制剂涂覆的缝合线与接种了细菌(例如葡萄球菌属的细菌)的琼脂板接触,并且在适当的孵育时间后,可以检查所述板在缝合线周围是否存在“抑制区”(即,没有细菌生长或细菌生长减少的区)。“抑制区”的存在(例如,与对照缝合线(不含抗微生物化合物)的试验相比)指示化合物可从制剂中释放。
[0066]
本发明的制剂可被认为是体内释放式(i)化合物的受控释放制剂。式(i)的化合物可以被认为分散(可释放地分散)穿过(或至少部分分散穿过)聚酯。
[0067]
式(i)的化合物使聚酯抵抗微生物定殖和生物膜形成。因此,涂层和/或器械有效地保持自身清洁,这是非常有利的,因为留置或其他医疗器械通常是微生物附着和生长的部位。
[0068]
可以使用液体培养基试验来评价活性化合物的释放及其抗定殖作用。可以将用本发明的聚酯涂覆的器械浸入液体细菌肉汤中。通过计数肉汤中存活细菌的数目来确定泄漏功效(释放),通过计数暴露于细菌肉汤后粘附于器械的活细菌的数目来确定抗定殖功效。
[0069]
用于本发明的可生物降解的聚合物被分类为聚酯,因为他们含有重复的酯基,但也可以包含其他官能团。通常他们被酯基封端,但游离羧酸基团或烷基酯基团可用作端基。用酯封端的和烷基酯基团封端的聚合物通常显示出比游离羧酸基团更长的降解时间。
[0070]
特别合适的聚合物包括聚交酯(d或l形式)、聚乙交酯、聚二恶烷酮和聚己内酯。也可以使用掺入这些相同单体的共聚物(包括嵌段共聚物),例如d-丙交酯和l-丙交酯的共聚物(尽管优选l-丙交酯聚合物)、丙交酯和乙交酯的共聚物以及丙交酯和己内酯的共聚物。优选聚(d,l-丙交酯-共-乙交酯)的50:50对映异构体混合物。包括共聚物(其包含三亚甲基碳酸酯单体)的聚合物也可以是合适的。共聚物中的单体比例可以变化,但包括丙交酯的共聚物通常含有50%或更多、例如至少60%或70%的丙交酯单体。因此,制剂可包含单一聚合物类型、单一共聚物或者一种或更多种聚合物和/或共聚物的混合物。
[0071]
可生物降解聚合物通常是合成的。可生物降解聚合物的使用在生物医学领域中是众所周知的。在本发明中使用的可生物降解聚合物应该是无毒的并且不被患者认为是外来的。生物降解产物也应该是无细胞毒性的并且容易从体内清除。
[0072]
通过在使用中,即在动物体内(或与其接触)的降解速率,来判断可生物降解性。可生物降解聚酯也可被称为生物可吸收(即,分解并被身体吸收)。聚合物与聚合物之间的降解显著不同,但通常为1或2周至4年或更长。优选地,在原位,聚酯将在小于6个月内、例如在2-4个月内完全降解。尽管在其他优选的实施方案中,聚合物可保持长达4年或甚至更长。本领域技术人员知道所关注的不同聚合物的降解时间并且可以根据预期用途选择聚合物。例如,缝合线可能只需要持续一周或几周的时间,而一些植入物,例如骨科植入物或心脏植入物,可能在体内保留数年。与式(i)化合物的配混不显著影响聚合物的降解速率。
[0073]
聚合物的特性粘度(以dl/g测量)也将在聚合物之间变化,通常为0.1或0.2至6或8,优选0.5至2.5,更优选0.8至2.2,最优选0.8至1.2。
[0074]
分子量(重均)还将取决于所选的聚合物和所关注的具体医学应用。典型的分子量为3000-30000,例如5000-25000。尽管在一些情况下可以使用高达50000、80000、100000或更高的分子量。优选的分子量为3000-20000,例如3000-10000或15000。
[0075]
凝胶渗透色谱法可用于测量特性粘度和分子量。
[0076]
合适的医用级可生物降解聚酯的供应商包括evonik(其范围)。合适的聚合物容易商购获得并且可以通过许多反应方便地合成,包括醇和酸的直接缩合、开环聚合和金属催化的聚合反应。
[0077]
两种不同的方法可方便地用于制备本发明的制剂。
[0078]
首先,可以通过将两者熔融在一起来共混聚酯和式(i)的化合物。可以首先将聚合物熔融,然后加入式(i)的化合物,或可以在熔融之前加入化合物。化合物的加入对聚合物的熔点没有显著影响。非常令人惊讶的是,式(i)的化合物,特别是式(i)的肽,能够经受住将他们与可生物降解的聚酯配混所必需的加热。这些分子显示出乎意料的热稳定性。
[0079]
因此,在另一方面,本发明提供了制备包含与式(i)化合物配混的可生物降解聚酯的制剂的方法,所述方法包括将与式(i)化合物混合的可生物降解聚酯熔融。本文所述的本发明的其他方面的实施方案比照适用于本发明的该方面。这种通过熔融配混优选使用快速加热进行,例如加热至120-230摄氏度(取决于聚酯的熔点)。在5分钟内,例如在4分钟内,诸如约3分钟。以这种方式,聚合物在肽分解之前熔化。式(i)的化合物优选仅暴露于高温(例如,超过100度)达2或3分钟(允许热传递到混合物中)。一旦聚酯熔融并与式(i)的化合物混合,就将混合物从热源移除。在该实施方案中,优选熔点低于约230摄氏度的聚酯。
[0080]
可替代地,并且优选地,该聚合物和具有化学式(i)的化合物可以使用溶剂混配。在一个实施方案中,将可生物降解聚合物溶解于第一溶剂中,并将式(i)化合物溶解于可与第一溶剂混溶的第二溶剂中,然后将两种溶液混合。两种溶剂优选为有机溶剂,优选具有一定极性质量。
[0081]
两种溶剂必须选择为可混溶的并且能够分别溶解聚合物和式(i)化合物。当混合时,溶剂还必须保持其溶剂化其组分的能力,甚至当混合时,可混溶的溶剂可能导致一种组分沉淀。用于聚合物的合适溶剂包括氯仿、乙酸乙酯、丙酮和四氢呋喃(thf);极性非质子溶剂可以是优选的。式(i)化合物的合适溶剂更多变化,包括水、甲醇、乙醇、氯仿、thf和dmso。聚合物的优选溶剂是乙酸乙酯,式(i)化合物的优选溶剂是醇,例如乙醇。
[0082]
可替代地,式(i)的化合物和聚合物两者可在混合之前、混合之时或混合之后溶解于单一溶剂中。适用于该方法的溶剂包括thf和氯仿。可能需要将式(i)的化合物与溶剂(例如thf)长时间组合,例如至少4小时,优选至少12小时,可以是1天或更多天,可能至多7天或14天。非常令人惊讶的是,式(i)的化合物(诸如amc-109)可溶于thf和氯仿中。
[0083]
因此,在另一方面,本发明提供了一种制备包含配混有式(i)化合物的可生物降解聚酯的制剂的方法,所述方法包含:形成式(i)的化合物、可生物降解聚酯和一种或更多种溶剂的混合物,所述溶剂能够溶解所述化合物和所述聚酯,并任选地干燥所述混合物。
[0084]
在一个优选的实施方案中,本发明提供了一种制备包含配混有式(i)化合物的可生物降解聚酯的制剂的方法,所述方法包含:(i)提供包含式(i)化合物的第一溶液;(ii)提供包含可生物降解聚酯的第二溶液,其中所述第二溶液可与所述第一溶液混溶;以及(iii)混合所述第一溶液和所述第二溶液。本文描述的本发明的其他方面的实施方案加以必要的变更适用于本发明的这一方面。用于制备第一溶液和第二溶液的溶剂可以相同或不同。优选的溶剂如上所述。
[0085]
混合之后,可以干燥所得混合物,这可以是主动或被动过程,被动干燥过程可能需要几天,例如1-6天。
[0086]
将聚酯与式(i)化合物配混的另一种方法是静电纺丝。静电纺丝是由电流体动力现象控制的公知的电压驱动方法,其中纤维可由聚合物溶液制成。为了经由静电纺丝方法获得根据本发明的制剂,将包含聚酯和式(i)化合物的溶液(或“纺丝溶液”)静电纺丝成包含所述化合物的纤维。该溶液可以方便地包含如上所述的两种溶剂,他们是可混溶的并且各自能够溶解聚合物或式(i)的化合物。可替代地,可以使用单一溶剂,诸如thf。合适的静电纺丝方法如scaffaro等人,european polymer journal 96(2017),266-277中所述。
[0087]
以w/w计,配混的聚合物制剂中的式(i)的化合物的量可以低至2%或3%至最高达(up to)25%或30%,通常为4%至15%或20%。
[0088]
本发明的制剂优选作为涂层加入到医疗器械中,尽管一些医疗器械可以由本发明的制剂组成,或者医疗器械可以具有由该制剂制成的部分或组件,例如通过3d打印。因此,本发明的另一方面是用如本文所定义的本发明的制剂涂覆的医疗器械,其包括部分涂覆的医疗器械。优选地,器械的整个外表面涂覆有本发明的制剂。该涂层在器械的表面上(在与身体接触的任何表面上,包括与体液接触的表面上)带来制剂层。选择该层的厚度以提供所需的功能,特别是提供所需的原位受控释放曲线。
[0089]
在本发明的另一方面,提供了如本文所定义的本发明的制剂,其已经应用于医疗器械。
[0090]
器械包括缝合线、外科紧固件、导管、线等和植入物,包括骨科植入物(诸如髋和膝植入物)以及牙科植入物、针、支架、心律器械和脑深部刺激器械。尤其优选缝合线。
[0091]
可以将待涂覆的器械浸入本发明的熔融制剂或包含可生物降解聚酯、式(i)的化合物和一种或更多种溶剂的混合物中(可能若干次,例如3-10次),并进行干燥或使其干燥。合适的溶剂和可混溶的溶剂混合物如本文所讨论。浸渍方法特别适合于诸如缝合线的器械。可替代地,本发明的制剂可以通过涂刷到器械表面上,例如通过喷涂,而施加至医疗器械,例如植入物。包含本发明制剂的医疗器械也可通过3d打印生产。
[0092]
可应用本发明制剂的合适缝合线包括可吸收的、可选编织的缝合线。此类缝合线可由尼龙制成,包括ethicon、surgilon和nurolan缝合线。优选使用不含或具有除本发明制剂之外的任何涂层的缝合线。例如,可以首先处理缝合线以除去硅涂层。
[0093]
可吸收(可生物降解)缝合线是根据本发明的优选医疗器械,并且可以如下形成。他们方便地由选自以下的单体的聚酯制成:乳酸(单独或组合的两种对映体形式)、乙醇酸、己内酯和二氧杂环己酮。为了定制缝合线的性质,通常使这些单体中的两种(或更多种)共聚,或者可能使不同均聚物的较短的链嵌段聚合。可吸收缝合线中最常见的聚合物是l-乳酸和乙醇酸的共聚物plga,优选由约90%乙醇酸和约10%l-乳酸制成。polyglactin 910是一种这样的共聚物,具有高拉伸强度,并方便地用作可吸收缝合线中的细丝。涂层优选为以长丝质量的2-10%的量施用的65/35摩尔比的丙交酯-乙交酯共聚物(例如,polyglactin 370)。为了处理性能,可以加入等量的硬脂酸钙(即,与涂层聚合物相等)。式(i)的化合物优选配混在涂层中,或施加于其上的另外的涂层中,但也可配混在长丝中。
[0094]
本发明的缝合线可每米缝合线长度包含0.5-10mg式(i)化合物,优选1-5mg/m,例如1-3mg/m。
[0095]
在另一方面,本发明提供了一种生产本发明的医疗器械的方法,所述方法包含:(i)提供包含可生物降解聚酯的制剂,所述可生物降解聚酯配混有式(i)的化合物;以及
(ii)将所述制剂施加于医疗器械上(例如,通过将器械浸入所述制剂中,或将所述制剂涂刷(例如,喷涂)到器械上,或将所述制剂涂刷(例如,喷涂)到器械的芯(诸如缝合线的长丝部分)上)。在将制剂施加于医疗器械后,可将其主动干燥(例如,通过适度加热或施加空气流)或使其干燥。本文描述的本发明的其他方面的实施方案加以必要的变更适用于本发明的这一方面。如果施加含溶剂的制剂,则溶剂将在干燥期间蒸发并在所述医疗器械上留下包含本发明的制剂或由本发明的制剂组成的涂层(或层)。
[0096]
在类似的方法中,本发明提供了一种生产本发明的医疗器械的方法,所述方法包含:(i)提供可生物降解的聚酯的制剂,所述可生物降解聚酯配混有式(i)的化合物;以及(ii)将所述制剂施加于背衬片或其他载体上。以这种方式,可以制备由本发明的制剂组成或基本上由本发明的制剂组成的医疗器械,例如以形成薄膜、膜、片材或粘合剂。
[0097]
另一方面提供了通过本发明的方法制备的包含可生物降解聚酯的制剂,所述可生物降解聚酯配混有式(i)的化合物,或具有这种制剂施加于其上的医疗器械。本文描述的本发明的其他方面的实施方案加以必要的变更适用于本发明的这一方面。
[0098]
本发明的另一方面提供了本发明的制剂和器械用于疗法的用途。
[0099]“疗法(therapy)”包括治疗(treatment)和预防,即,其包括治疗和预防用途二者。
[0100]
在一些实施方案中,本发明提供了用于治疗或预防受试者感染的本发明的制剂或医疗器械。在一些优选的实施方案中,感染或潜在感染是手术部位感染或伤口感染,例如需要通过缝合线或其他手术紧固件闭合的伤口或其他部位。在其他优选的实施方案中,感染或潜在感染是与植入物(如上所述)相关的感染,包括在器械上或器械周围形成生物膜。
[0101]
优选地,感染是细菌感染,例如由革兰氏阳性细菌(例如葡萄球菌属或链球菌属的细菌)引起的感染。在一些实施方案中,感染是金黄色葡萄球菌感染。在一些实施方案中,感染是表皮葡萄球菌感染。
[0102]
本发明的制剂、器械、用途和方法优选对广谱细菌、特别是对革兰氏阳性和革兰氏阴性细菌有效(通过活性化合物的释放完全或部分抑制细菌在周围环境中的生长和/或完全或部分抗集群效应),例如,他们对金黄色葡萄球菌、铜绿假单胞菌、大肠杆菌和屎肠球菌都有效。
[0103]
本发明的另一方面提供了本发明的制剂或医疗器械用于抑制受试者中细菌生长的用途。本文描述的本发明的其他方面的实施方案加以必要的变更适用于本发明的这一方面。
[0104]
本发明的另一方面提供了本发明的制剂或医疗器械用于治疗的用途,优选用于治疗或预防受试者感染。在此描述的本发明的其他方面的实施方案加以必要的变更适用于本发明的这一方面。
[0105]
换一个角度来看,本发明提供了一种治疗或预防感染的方法,该方法包含向有需要的受试者施加(或施用)本发明的制剂或医疗器械。本文描述的本发明的其他方面的实施方案加以必要的变更适用于本发明这一方面。
[0106]
换一个角度来看,本发明提供了一种治疗或预防感染的方法,该方法包含向有需要的受试者施加(或施用)治疗有效量的本发明的制剂或医疗器械。本文描述的本发明的其他方面的实施方案加以必要的变更适用于本发明这一方面。
[0107]
对于选定的式(i)的化合物,将基于临床评估和抗目标细菌的mic值来确定治疗有
效量。
[0108]
本发明的另一个方面提供了式(i)化合物用于治疗的用途,优选用于治疗或预防受试者的感染的用途,其中所述化合物作为包含与所述化合物配混的可生物降解聚酯的制剂或以施加有此类制剂的医疗器械的形式施用于(或施加于)受试者。本文描述的本发明的其他方面的实施方案加以必要的变更适用于本发明这一方面。
[0109]
本文所用的术语“受试者”或“患者”包括任何哺乳动物,例如人和任何家畜、家养动物或实验室动物。具体实例包括小鼠、大鼠、猪、猫、狗、绵羊、兔、牛和猴。然而,优选地,受试者或患者是人类受试者。因此,根据本发明治疗的受试者或患者优选是人。
[0110]
在一些实施方案中,受试者或患者是患有感染的那些,或怀疑患有感染的那些,或处于患有(或染上)感染的风险中的那些。处于风险中的患者是优选的患者组,并且包括需要医疗植入物或必须进行手术或需要手术或其他伤口闭合的患者。对于这些患者,可选择掺入本发明制剂的本发明器械,例如缝合线、其他紧固件或假体植入物。此类器械释放抗微生物的式(i)化合物以促进形成器械周围患者体内无感染的局部环境,并且器械上/内的式(i)化合物的存在抑制了器械本身被细菌定殖。
[0111]
本发明还提供了试剂盒,该试剂盒包含一种或更多种本发明的医疗器械。优选地,所述试剂盒用于本文所述的治疗方法和用途。优选地,所述试剂盒包含试剂盒组分的使用说明书。优选地,所述试剂盒用于治疗或预防感染,例如如本文别处所述,并且可选地包含使用试剂盒组分治疗此类感染的说明书。
[0112]
如在整个申请中所使用的,术语“一(a)”和“一个(an)”以他们表示所引用的组分或步骤中的“至少一个”、“至少第一”、“一个或更多个”或“多个”的意义使用,除了其中之后本文专门陈述上限的情况。
[0113]
另外,当在本文中使用术语“包含(comprise)”、“包括(comprises)”、“具有(has)”或“含有(having)”或其他等效术语时,那么在一些更具体的实施方案中,这些术语包括术语“由
…
组成”或“基本上由
…
组成”或其他等效术语。
[0114]
现在将参考以下非限制性实施例和附图进一步描述本发明,其中:
[0115]
图1是显示在鼠科动物皮肤感染模型中使用化合物2针对金黄色葡萄球菌fda486的一天局部处理的效果的图。菌落形成单位(cfu)的数目显示在y轴上,并且施加于小鼠的局部处理的类型显示在x轴上。化合物2在本文中也称为amc-109。
[0116]
图2是显示在鼠科动物皮肤感染模型中使用化合物2针对酿脓链球菌的一天局部处理的效果的图。菌落形成单位(cfu)的数目显示在y轴上,并且施加于小鼠的局部处理的类型显示在x轴上。化合物2在本文中也称为amc-109。
[0117]
图3是显示在鼠科动物皮肤感染模型中针对金黄色葡萄球菌fda486的一天局部处理的效果的图。在上午9点、中午12点和下午3点处理每只小鼠。在下午6点采集皮肤活组织检查。显示了中值。
[0118]
图4是显示在鼠科动物皮肤感染模型中针对酿脓链球菌cs301的一天局部处理的效果的图。在上午7点、上午10点和下午1点处理每只小鼠。在下午4点采集皮肤活组织检查。显示了中值。
[0119]
图5是显示小鼠皮肤感染模型中针对金黄色葡萄球菌fda486的一天局部处理的效果的图。在上午9点、中午12点和下午3点处理每只小鼠。在下午6点采集皮肤活组织检查。显
示了中值。
[0120]
图6是显示通过提取涂层缝合线释放的amc-109的量的定量分析的图。第一个数据集来自试验-01批次,随后的三个数据集是试验-02批次中的三种不同缝合线。
[0121]
图7是显示首次使用时对金黄色葡萄球菌生长抑制试验结果的照片。
[0122]
图8是显示amc涂覆的缝合线对液体培养基中细菌生长的影响的图,通过暴露于缝合线后生长培养基中的cfu测量。
[0123]
图9是显示如实施例9中所述的抑制区的照片。
[0124]
图10是含有接种tsb的孔的照片,其中放置了各种缝合线。编号的孔如下:
[0125]
1:金黄色葡萄球菌ethibond涂覆有amc-109
[0126]
2:金黄色葡萄球菌ethibond未涂覆
[0127]
3:金黄色葡萄球菌生长对照
[0128]
4:表皮葡萄球菌ethibond涂覆有amc-109
[0129]
5:表皮葡萄球菌ethibond未涂覆
[0130]
6:表皮葡萄球菌生长对照
[0131]
图11是显示含有生物可吸收聚酯rg502和l206s的amc-109的泄漏(以总量的百分比计)随时间(分钟)而变化的图。
[0132]
实施例1
[0133]
肽合成
[0134]
化学试剂
[0135]
受保护的氨基酸boc-trp-oh、boc-arg-oh、boc-4-phenyl-phe和ac-arg-oh购自bachem公司,而boc-4-碘苯丙氨酸、boc-3,3-二苯丙氨酸和boc-(9-蒽基)丙氨酸购自aldrich。构成肽c-末端的苄胺、2-苯乙胺、3-苯丙胺、(r)-2-苯丙胺、(s)-2-苯基丙胺、n,n-甲基苄胺、n,n-乙基苄胺和n,n-二苄胺购自fluka,除了n-乙基苄胺购自acros。二异丙基乙胺(dipea)、1-羟基苯并三唑(1-hobt)、氯代三吡咯烷基六氟磷酸盐(pyclop)和o-(苯并三唑-1-基)-n,n,n’,n’四甲基脲六氟磷酸盐(hbtu)购自fluka。4-正丁基苯基硼酸、4-叔丁基苯基硼酸、4-联苯基硼酸、2-萘基硼酸、三邻甲苯基膦、苄基溴和乙酸钯购自aldrich。溶剂购自merck、riedel-de或aldrich。
[0136]
氨基酸的制备
[0137]
boc-2,5,7-三叔丁基色氨酸-oh的制备:将h2n-trp-oh(1.8g,8.8mmol)、t-buoh(4.7g,63.4mmol)在三氟乙酸(19ml)中的混合物于70℃搅拌3小时。将所得中棕色半透明溶液的体积在旋转蒸发器上于室温减少30分钟,然后通过逐滴添加60ml 7%(按重量计)nahco3来研磨。然后通过真空过滤回收得到的灰色/白色颗粒状固体,并在室温下真空干燥24小时。通过从40%乙醇在水中的接近沸腾的混合物中结晶分离产物。体积通常为每克粗产物约20ml。
[0138]
从粗产物中第一次结晶产生相对于样品中的所有其他物质纯度为80-83%(hplc)且相对于已知tbt类似物纯度为约94-95%的分离产物。该阶段的收率为60-65%。
[0139]
boc-4-碘苯丙氨酸的苄基化。将boc-4-碘苯丙氨酸(1当量)溶于90%甲醇的水溶液中,并通过加入碳酸铯中和直至弱碱性ph(通过石蕊试纸测定)。通过旋转蒸发除去溶剂,并通过与甲苯重复共沸蒸馏进一步减少boc-4-碘苯丙氨酸铯盐中剩余的水。将所得干燥盐
2h。将反应混合物用乙酸乙酯稀释并用柠檬酸、碳酸氢钠和盐水洗涤。真空除去溶剂,所得肽的boc保护基在暗处使用95%tfa或乙酰氯的无水甲醇溶液脱保护。
[0153]
使用pyclop形成溶液相酰胺。boc-arg-n(ch2ph)2的合成。boc-arg-oh(1当量)、nh(ch2ph)2(1.1当量)和pyclop(1当量)在无水dcm(通过氧化铝过滤)(2ml)和dmf(1ml)中的溶液。将溶液在冰上冷却并在搅拌下加入dipea(2当量)。将溶液在室温下搅拌1h。反应混合物被蒸发,再溶解于酸乙酯中,用柠檬酸、碳酸氢钠和盐水洗涤。真空除去溶剂,所得肽的boc保护基使用95%tfa在黑暗中脱保护。
[0154]
肽纯化和分析。使用反相hplc在delta-pak(waters)c
18
柱(15μm,25
×
100mm)上纯化肽,用水和乙腈的混合物(均含有0.1%tfa)作为洗脱剂。通过rp-hplc使用分析型delta-pak(waters)c
18
柱(15μm,3.9
×
150mm)和在vg quattro四极质谱仪(vginstruments公司,英国altringham)上的通过rp-hplc分析肽。
[0155]
实施例2
[0156]
本文定义的肽的体外活性
[0157]
材料和方法
[0158]
抗微生物剂
[0159]
预称重的化合物1和化合物2的小瓶由lytix biopharma公司提供。
[0160][0161]
细菌分离株
[0162]
本研究中使用的细菌分离株来自世界范围内的各种来源,储存于gr micro公司,并以最少传代培养保持,在-70℃下深度冷冻,作为未稀释马血清的高蛋白基质中的浓悬浮液。所用菌种及其特性列于表1中。这些菌种包括54种革兰氏阳性菌、33种革兰氏阴性菌和10种真菌。
[0163]
最低抑制浓度(mic)的测定
[0164]
使用由临床和实验室标准协会(clsi,以前称为nccls)公布的用于抗微生物敏感性试验的以下微量肉汤稀释方法来测定mic:
[0165]
m7-a6第23卷第2期,2003年1月,对有氧生长的细菌进行稀释抗微生物药敏试验的方法;批准的标准——第6版。m100-s15第25卷第1期,2005年1月,抗微生物药敏试验的性能标准;第十五次信息增补。m11-a6第24卷第2期,厌氧细菌的抗微生物药敏试验方法;批准的标准——第6版。m27-a2第22卷第15期,酵母肉汤稀释法抗真菌药敏试验参考方法;批准的标准——第二版。m38-a第22卷第16期,丝状真菌肉汤稀释抗真菌药敏试验参考方法;批准的标准。
[0166]
使用在gr micro公司制备的含有抗细菌剂或抗真菌剂的湿平板进行mic估算。
[0167]
将阳离子调节的mueller-hinton肉汤(oxoid公司(英国basingstoke)和trek diagnostic systems公司(英国east grinstead))(补充有5%的用于链球菌属、杰氏棒杆菌和单核细胞增生利斯特氏菌的裂解马血)用于需氧细菌,初始接种物为约105菌落形成单位(cfu)/ml。
[0168]
将嗜血杆菌试验培养基(含有0.5%酵母提取物的mueller-hinton肉汤和含有15mg/l血红蛋白和15mg/l nad的嗜血杆菌试验培养基补充物,均得自oxoid公司,英国basingstoke)用于流感嗜血杆菌并接种约105cfu/ml。
[0169]
补充的布氏肉汤(sbb)用于厌氧菌株,接种物为约106cfu/ml。sbb是由1%蛋白胨、0.5%“lab-lemco”、1%葡萄糖和0.5%氯化钠组成的肉汤,补充有5μg/l氯高铁血红素和1μg/l维生素k(均得自sigma aldrich公司)。
[0170]
酵母和丝状真菌mic在mops缓冲的rpmi 1640培养基(mops缓冲液得自sigma aldrich公司,rpmi 1640得自invitrogen公司(苏格兰paisley))中进行。酵母接种物为7.5
×
10
2-4
×
103cfu/ml,丝状真菌为约8
×
10
3-1
×
105cfu/ml。
[0171]
按照常规操作,预先制备含有mueller-hinton肉汤的所有平板,在制备当天于-70℃冷冻,并在使用当天解冻。真菌、嗜血杆菌和厌氧mic测定均在同一天制备的平板中进行。
[0172]
为了评价冷冻是否影响肽的活性,使用含有新鲜制备的mueller-hinton肉汤的平板重复一些mic测定。
[0173]
对照菌株
[0174]
试验菌株组中包括以下对照(参考)菌株
[0175]
大肠杆菌atcc 25922
[0176]
金黄色葡萄球菌atcc 29213
[0177]
粪肠球菌atcc 29212
[0178]
肺炎链球菌atcc 49619
[0179]
铜绿假单胞菌atcc 27853
[0180]
克鲁斯念珠菌atcc 6258
[0181]
以下对照菌株在试验菌株组之外,并在适当情况下纳入,以检查比较物是否在范围内。
[0182]
流感嗜血杆菌atcc 49247
[0183]
近平滑念珠菌atcc 22019
[0184]
脆弱拟杆菌atcc 25285
[0185]
迟缓埃格特菌atcc 43055
[0186]
结果
[0187]
结果作为单行列表示于表1中。重复对照菌株结果示于表2中。可以看出,对照菌株结果是高度可再现的,包括来自含有冷冻储存或新鲜使用的mueller hinton肉汤的平板的数据。冷冻平板对其他细菌菌株的mic也没有影响。
[0188]
获得的mic数据非常令人鼓舞,表明肽具有相当广谱的活性。
[0189]
表1:两种抗微生物肽和比较物抗一组革兰氏阳性菌、革兰氏阴性菌和真菌的体外活性的单行列表。
[0190]
[0191]
[0192][0193]
表2:两种抗微生物肽和比较物抗atcc对照菌株的体外活性
[0194]
(包括试验菌株组之外的atcc对照菌株)
[0195]
[0196][0197]
mhb,mueller hinton肉汤;htm,嗜血杆菌试验培养基;sbb,补充的布鲁氏肉汤。
[0198]
实施例3对胰蛋白酶降解和抗微生物活性的稳定性
[0199]
检测式aa
1-aa
2-aa
1-nhch2ch2ph化合物的胰蛋白酶抗性和抗微生物活性。
[0200]
肽半衰期的测量和计算
[0201]
将每种肽溶解在0.1m nh4hco3缓冲液(ph 6.5)中,得到1mg/ml的最终肽浓度。通过将1mg胰蛋白酶溶解在50ml 0.1m nh4hco3缓冲液(ph 8.2)中,来制备胰蛋白酶溶液。对于稳定性测定,将250μl新鲜制备的胰蛋白酶溶液和250μl肽溶液在摇床上于37℃在2ml 0.1m nh4hco3缓冲液(ph 8.6)中孵育。以不同的时间间隔取样0.5ml的等分试样,用0.5ml水:含有1%tfa的乙腈(60:40v/v)稀释:如上所述用rp-hplc分析。于37℃在0小时和20小时后采集的未添加胰蛋白酶的样品用作阴性对照。在测定的前5小时期间采集的样品在254nm的峰面积的积分用于产生τ
1/2
。在前24h期间显示无降解的肽被分类为稳定的。
[0202]
抗菌试验
[0203]
对金黄色葡萄球菌菌株atcc 25923、甲氧西林耐药金黄色葡萄球菌(mrsa)菌株atcc 33591和甲氧西林耐药表皮葡萄球菌(mrse)菌株atcc 27626的mic测定由toslab公司使用标准方法进行。amsterdam,d.(1996),在液体培养基中对抗微生物剂进行敏感性试验,《实验室药物中的抗生素(antibiotics in laboratory medicine)》第4版(lorian,v.编著)第75-78页,williams和wilkins公司,巴尔的摩。
[0204]
表3.aa
1-aa
2-aa
1-nhch2ch2ph肽对胰蛋白酶的稳定性(测量为半衰期(τ
1/2
))以及显示为mic的抗菌活性。
[0205][0206]a使用来自康奈尔大学的医用计算器(medical calculator)计算半衰期。
[0207]b最小抑制浓度
[0208]c金黄色葡萄球菌菌株atcc 25923
[0209]d甲氧西林耐药金黄色葡萄球菌atcc 33591
[0210]e甲氧西林耐药表皮葡萄球菌atcc 27626
[0211]f不在本发明的化合物定义之内
[0212]
实施例4化合物2的体内活性
[0213]
用金黄色葡萄球菌或酿脓链球菌感染小鼠皮肤,随后以3小时间隔给予总共3次处理。最后一次处理后3小时,收集皮肤活组织检查并测定皮肤样品中存在的集落形成单位(cfu)的数目。结果如图1和图2所示,表示为每只小鼠的集落形成单位数。
[0214]
在实验1(图1)中,将化合物2作为含有2%(w/w)化合物2的乳膏或凝胶的一部分施加于鼠科动物皮肤。不含化合物2的相同乳膏或凝胶用作阴性对照(安慰剂)。可以清楚看出,与阴性对照相比,当将含有化合物2的乳膏或凝胶施加于小鼠皮肤时,cfu的数量减少,表明化合物2对金黄色葡萄球菌发挥抗微生物作用。载体、乳膏或凝胶的性质没有显著影响。
[0215]
在实验2(图2)中,化合物2以两种不同浓度施加,作为1%或2%凝胶。安慰剂凝胶和已知的抗细菌剂“百多邦(bactroban)”用作对照。可以看出,含有化合物2的凝胶在减少cfu数方面比安慰剂凝胶或百多邦更有效。含有2%化合物2的凝胶比仅含有1%化合物2的凝胶更有效。
[0216]
实施例5
[0217]
本发明中使用的化合物的制备以及物理、抗微生物和溶血特性
[0218]
肽合成——相关信息也在实施例1中提供。
[0219]
化学品:
[0220]
保护的氨基酸boc-arg-oh和boc-4-苯基-phe购自bachem公司,而boc-4-碘苯丙氨酸购自aldrich。组成肽c-末端的异丙胺、丙胺、己胺、丁胺、十六烷基胺、异丁胺、环己胺和环戊胺购自fluka。二异丙基乙胺(dipea)、1-羟基苯并三唑(1-hobt)、氯代三吡咯烷基六氟磷酸盐(pyclop)和o-(苯并三唑-1-基)-n,n,n’,n’四甲基脲六氟磷酸盐(hbtu)购自fluka。4-正丁基苯基硼酸、4-叔丁基苯基硼酸、4-联苯基硼酸、2-萘基硼酸、三邻甲苯基膦、苄基溴和乙酸钯购自aldrich。溶剂购自merck、riedel-de或aldrich。
[0221]
boc-phe(4-4'-联苯基)-obn的制备:使用suzuki偶联的一般程序,由4-联苯基硼酸以61%收率制备标题化合物。通过从正庚烷重结晶粗产物分离boc-phe(4-4'-联苯基)-obn。
[0222]
boc-phe(4-(2'-萘基))-obn的制备:使用suzuki偶联的一般程序,由2-萘基硼酸以68%收率制备标题化合物。通过从正庚烷重结晶粗产物分离boc-phe(4-(2'-萘基))-obn。
[0223]
boc-phe(4-4'-联苯基)-oh的制备:使用用于脱酯化的一般程序,由boc-phe(4-4'-联苯基)-obn以61%收率制备标题化合物。
[0224]
boc-phe(4-(2'-萘基))-oh的制备:使用用于脱酯化的一般程序,由boc-phe(4-(2-萘基))-obn以68%收率制备标题化合物。
[0225]
使用hbtu的溶液相肽合成的一般程序描述于实施例1中。
[0226]
在实施例1中描述了使用pyclop形成溶液相酰胺。
[0227]
肽的纯化和分析如实施例1所述。
[0228]
表4
[0229]
化合物通式:arg-aa
2-arg-x-y
[0230][0231]
抗微生物试验
[0232]
对金黄色葡萄球菌菌株atcc 25923、甲氧西林耐药金黄色葡萄球菌(mrsa)菌株atcc 33591和甲氧西林耐药表皮葡萄球菌(mrse)菌株atcc 27626的mic测定由toslab公司使用标准方法进行。amsterdam,d.(1996),在液体培养基中对抗微生物剂进行敏感性试验,《实验室药物中的抗生素(antibiotics in laboratory medicine)》第4版(lorian,v.编著)第75-78页,williams和wilkins公司,巴尔的摩。
[0233]
表5
[0234]
本发明中使用的化合物的抗微生物和毒性特性
[0235][0236]
实施例6
[0237]
所选化合物的体外大实验组筛选
[0238]
材料和方法
[0239]
抗微生物剂
[0240]
预称重的化合物7和化合物8的小瓶由lytix biopharma公司提供。
[0241][0242]
细菌分离株
[0243]
本研究中使用的细菌分离株如实施例2所述。
[0244]
测定最低抑制浓度(mic)
[0245]
如实施例2所述测定mic。
[0246]
结果
[0247]
结果作为单行列表显示于表6中。
[0248]
获得的mic数据是非常令人鼓舞的,表明肽具有相当广谱的活性。
[0249]
表6:两种抗微生物肽对一组革兰氏阳性菌、革兰氏阴性菌和真菌的体外活性的单行列表。
[0250]
[0251]
[0252][0253]
实施例7化合物7和8的体内活性
[0254]
用金黄色葡萄球菌或酿脓链球菌感染小鼠皮肤,随后以3小时间隔给予总共3次处理。最后一次处理后3小时,采集皮肤活组织检查并测定皮肤样品中存在的集落形成单位(cfu)的数目。结果如图3、图4和图5所示,表示为每只小鼠的集落形成单位数。
[0255]
在实验1(图3)中,将化合物7作为含有2%(w/w)化合物7的乳膏或凝胶的一部分施加于鼠皮肤。不含化合物7的相同乳膏或凝胶用作阴性对照(安慰剂)。使用百多邦2%乳膏作为阳性对照。可以清楚地看出,与阴性对照相比,当将含有化合物7的乳膏或凝胶施用于小鼠皮肤时,cfu数减少,表明化合物7对金黄色葡萄球菌发挥抗微生物作用。标准临床治疗百多邦2%乳膏的疗效在治疗方案下无显著效果。载体、乳膏或凝胶的性质没有显著影响。
[0256]
在实验2(图4)中,化合物7以两种不同浓度施加,作为1%或2%凝胶。安慰剂凝胶和已知的抗细菌剂“百多邦(莫匹罗星)”用作对照。可以看出,含有化合物7的凝胶在减少来自酿脓链球菌cs 301感染的cfu数方面比安慰剂凝胶或百多邦更有效。含有2%化合物7的凝胶比仅含有1%化合物7的凝胶更有效。
[0257]
在实验3(图5)中,将化合物8以2%乳膏制剂施加于小鼠皮肤感染模型中的金黄色葡萄球菌fda 486感染。使用安慰剂乳膏和两种已知的抗细菌剂“夫西地酸(梭链孢酸)软膏2%”和“百多邦(莫匹罗星)乳膏2%”作为对照。可以看出,含有化合物8的乳膏在减少cfu数方面比安慰剂和夫西地酸或百多邦更有效。
[0258]
实施例8制备具有含amc-109的涂层的可吸收编织缝合线
[0259]
目的是研究含有amc-109的典型可生物降解聚(丙交酯-共-乙交酯)聚合物对编织缝合线的溶液涂层。工作分为四个方面:
[0260]
1.制备允许聚(丙交酯-共-乙交酯)聚合物和amc-109溶解的溶剂(或溶剂混合物)
[0261]
2.用以上第1项的溶液涂覆“裸”编织可吸收缝合线材料。
[0262]
3.研究涂覆的缝合线的amc-109泄漏
[0263]
4.研究涂覆的缝合线的微生物学有效性
[0264]
材料和方法:
[0265]
聚合物
[0266]
rg502,聚(d,l-丙交酯-共-乙交酯)sigma-aldrich编号719889是丙交酯:乙交酯50:50混合物,酯封端的,mw为7000-17000,可生物降解聚合物。其类似于通常用于涂覆商业可吸收缝合线的可生物降解聚合物。其化学结构如下式所示:
[0267][0268]
肽
[0269]
amc-109在本文中称为“化合物2”且具有式arg-tbt-arg-nhch2ch2ph。
[0270]
缝合线
[0271]
syneture surgilon 4-0号缝合线,具有硅涂层的尼龙编织缝合线,用于研究。
[0272]
涂覆的缝合线的制备程序
[0273]
在涂覆之前,用乙酸乙酯洗涤缝合线以除去大部分预先存在的涂层。
[0274]
将rg502溶于乙酸乙酯中,将amc-109溶于酒精中。在第一个试验(试验-01)中,将50mg rg502溶于300μl乙酸乙酯中,并与溶于50μl乙醇中的10mg amc-109混合。在第二个试验(试验-02)中,将50mg rg502溶于400μl乙酸乙酯中,并与溶于110μl乙醇中的10mg amc-109混合。所得溶剂混合物是均匀的。
[0275]
缝合线基材(乙酸乙酯洗涤后)通过反复浸入涂覆溶剂混合物中进行涂覆。
[0276]
微生物学
[0277]
·
细菌菌株:金黄色葡萄球菌
[0278]
·
用于(集落形成单位)cfu计数的缝合线:
[0279]
°
具有rg502聚合物的缝合线surgilon 4-0,对照
[0280]
°
具有rg502聚合物/amc-109的缝合线surgilon 4-0
[0281]
°
缝合线surgilon 4-0(原始),对照
[0282]
·
胰蛋白酶大豆肉汤(tsb)
[0283]
·
mueller hinton(mh)琼脂平板
[0284]
从血琼脂平板上挑取金黄色葡萄球菌的菌落,制成0.5mcfarland溶液(1
×
108cfu),该溶液用于:
[0285]
1.接种mh琼脂平板
[0286]
2.在tsb中进行稀释,以获得1
×
105cfu
[0287]
将缝合线置于琼脂平板上以观察抑制区,并接种于tsb中以检查涂覆的缝合线与未涂覆的缝合线的抗菌效果。
[0288]
将样品于37℃孵育16小时。
[0289]
将来自接种在tsb中的带有缝合线的试管的培养物通过系列稀释用于cfu测定。为了研究涂覆的缝合线的长期效应,冲洗缝合线并于37℃用tsb中的细菌再接种16小时。
[0290]
进行三个平行实验。
[0291]
菌落计数后测定cfu。
[0292]
结果
[0293]
涂层缝合线的制备
[0294]
通过用resomer rg-502和amc-109的溶液处理缝合线,可以容易地生产涂覆的缝合线。溶剂混合物的组成对于溶解resomer rg-502和amc-109并混合(并避免相分离或沉淀)的能力至为关键。
[0295]
amc-109释放量的定量分析
[0296]
用水提取涂覆的缝合线。将涂覆的缝合线置于0.4ml水中并静置30分钟。取出缝合线,干燥并第二次提取22小时。分析提取液的amc-109释放量。结果如图6所示。
[0297]
amc-109涂层缝合线的抗微生物功效测定
[0298]
通过琼脂生长抑制试验和液体肉汤试验评价resomer rg-502和amc-109涂覆的缝
合线的抗微生物功效。
[0299]
第1天:
[0300]
与未处理的对照缝合线以及涂覆有rg-502(未添加amc-109)的缝合线相比,在涂覆有amc-109的缝合线周围观察到抑制区(图7)。
[0301]
第一天,含有amc-109涂覆的缝合线的试管中的tsb培养基没有明显生长。制备cfu计数的稀释液,获得amc-109涂层缝合线0,500和3
×
103的cfu计数。在含有对照的试管中可见生长,得到cfu计数为5.8
×
108和4.7
×
108(数字是多个平行的平均值)(图8)。
[0302]
第2天:
[0303]
第2天,所有试管均可见生长,surgilon rg502/amc试管与对照品之间无可见差异。
[0304]
结论
[0305]
缝合线可以容易地用可生物降解聚合物和amc-109的溶液涂覆。得到的涂覆有amc的缝合线在16小时内具有抗菌效果。可以加入没有amc-109的最终resomer层以减少立即扩散,提供更持久的效果。
[0306]
实施例9-具有amc-109/聚合物涂层的缝合线
[0307]
材料和方法
[0308]
细菌菌株:金黄色葡萄球菌atcc29213和表皮葡萄球菌rp42a
[0309]
缝合线:用聚己内酯+5%amc-109涂层覆盖excel聚合物缝合线(johnson&johnson)。将聚合物(即,聚己内酯,平均分子量(mw)约14000)和肽通过在玻璃小瓶中快速加热(经过约3分钟)至120℃熔融,并且当聚己内酯熔融时进行混合。将缝合线浸泡在熔融混合物中以对其进行涂覆。
[0310]
对照:未涂覆的excel缝合线
[0311]
在一个实验中,将细菌菌落稀释至0.5mcfarland并铺展在mueller hinton琼脂平板上,在第二个实验中,将菌落稀释至0.5mcfarland并在胰蛋白酶大豆肉汤(tsb)中以1:100稀释。
[0312]
在第一个实验中,将amc涂覆的缝合线和未涂覆的对照物置于接种的平板上。将板在37℃下孵育16小时。在第二个实验中,将amc涂覆的缝合线和未涂覆的对照品置于接种培养基中,并在37℃下振荡培养16小时。
[0313]
结果
[0314]
与对照相比,表皮葡萄球菌和金黄色葡萄球菌均在amc-109涂层缝合线周围的琼脂板上观察到明显的抑制区(图9)。
[0315]
在孔1和4中观察到明显的细菌生长抑制(图10),其中已经加入了一部分涂覆有amc的ethibond缝合线。
[0316]
用syto 9和碘化丙啶进一步染色缝合线,并通过荧光显微镜进行研究。涂覆的缝合线和未涂覆的缝合线之间存在明显区别;在未涂覆的缝合线上观察到大量细菌生长。
[0317]
实施例10涂覆有amc-109的可吸收缝合线
[0318]
所描述的方法是可缩放的并且适合于工业开发。
[0319]
材料和方法:
[0320]
缝合线
[0321]
·
coviden(medtronic)聚山梨醇酯3-0
[0322]
·
ethicon vicryl plus 3-0(含三氯生,阳性对照)
[0323]
两种缝合线均由polyglactin 910内编织丝组成,覆盖在由聚(d,l-丙交酯-共-乙交酯)(丙交酯:乙交酯65:35)与硬脂酸钙混合的外部柔软的润滑层下。vicryl plus缝合线的外层还含有三氯生作为活性成分。
[0324]
聚合物
[0325]
resomer(evonik)rg-502,可降解的聚(d,l-丙交酯-共-乙交酯)(丙交酯:乙交酯50:50)m
w 7000-17000,降解时间《3个月。
[0326]
肽
[0327]
amc-109如前所述。
[0328]
缝合线剥离
[0329]
通过用乙酸乙酯洗涤缝合线10分钟,然后用水洗涤缝合线2分钟(部分)除去聚山梨醇酯缝合线的外层。在涂覆前对缝合线进行干燥。
[0330]
缝合线涂层混合物
[0331]
通过在一个小瓶中将rg-502溶于乙酸乙酯中,并在第二个小瓶中将amc-109溶于乙醇中,来制备涂层混合物。将两种溶液混合,产生轻微混浊的溶液,其在加入0.5ml乙酸乙酯后变得澄清。
[0332]
缝合线涂层
[0333]
将聚山梨醇酯缝合线(切成6cm的片)在涂层混合物中浸泡10分钟并干燥,然后在新制备的涂层混合物中第二次浸泡2分钟。
[0334]
制备两批缝合线,一批用于化学提取分析和抑制区测试(实验1),第二批用于在液体培养基中的功效试验(实验2)。
[0335]
表7.涂层中使用的质量和体积。
[0336][0337][0338]
提取
[0339]
选择缝合线样本进行水提取。
[0340]
第一次提取
[0341]
将缝合线置于小瓶中并加入水(1ml)。将样品放置1小时。通过hplc分析提取样品。
[0342]
第二次提取
[0343]
将来自第一次提取的缝合线样品置于新的小瓶中,加入水(1ml)并提取3.5h。通过hplc分析第二次提取样品。
[0344]
微生物学评价
[0345]
细菌菌株:
[0346]
·
金黄色葡萄球菌(8325)
[0347]
·
铜绿假单胞菌(pao1)
[0348]
·
大肠杆菌
[0349]
·
屎肠球菌
[0350]
使用不同细菌菌株的过夜菌落在0.5%nacl中制备0.5mcfarland(1
×
108cfu/ml)溶液,并在管中用2ml lb(lysogeny肉汤)进一步稀释至105cfu/ml。细菌溶液用于接种生长区抑制试验的琼脂平板,并用于直接接种lb培养基中的缝合线试验样品。将所有样品在37℃下孵育18小时。通过从i)接种试验样品的溶液(lb-培养基)或从ii)具有漂洗和涡旋(20s)样品的溶液(1ml氯化钠,0.5%)制备系列稀释液,来进行cfu计数。在1ml nacl中制备系列稀释液(10-1-10-6
)。从不同的稀释液中,将100μl涂布在血琼脂板上,并在37℃下进一步孵育18小时。
[0351]
结果:
[0352]
amc-109释放的定量
[0353]
表8.在含水缝合线提取液中发现的amc-109的量(μg/ml)。
[0354][0355]
*nq表示不可定量
[0356]
涂覆后得到的缝合线为0.4-0.5mg。水提取液中的amc-109浓度汇编在表8中,数据显示,在提取总共4.5小时后,高负载缝合线将25微克amc-109释放到水溶液中。在类似条件下,低负载缝合线释放5微克amc-109。
[0357]
amc-109的量表明包埋在高负载涂层中的amc-109的至少30%在4.5小时内释放到水中。低负载缝合线的释放似乎略低。
[0358]
微生物学评估
[0359]
在涂覆有15%amc-rg502的聚山梨醇酯周围总是观察到生长抑制区。相比之下,vicryl三氯生仅显示金黄色葡萄球菌和大肠杆菌的生长抑制,表9。
[0360]
表9:区域抑制试验抑制区
[0361][0362]
在细菌悬浮液中直接接种缝合线试验材料,导致所有菌株的15%amc-109涂层缝合线在lb培养基中的细菌生长减少。三氯生涂层缝合线仅抑制金黄色葡萄球菌生长,表10。
[0363]
表10.直接在lb培养基中接种缝合线实验样品的cfu。
[0364]
集落形成单位(cfu)
[0365][0366][0367]
结论
[0368]
amc-109可使用所述溶液涂覆技术掺入可吸收缝合线中。涂层溶液是混浊的,表明是过饱和溶液。这可以提高涂覆效率。
[0369]
amc涂覆的缝合线在4.5小时内将其amc-109含量的至少30%释放到含水环境中。amc-109的释放量取决于配混入缝合线的量。
[0370]
amc-109涂层缝合线提供了抗革兰氏阳性菌和革兰氏阴性菌(包括三氯生无效的重要病原体)的抗定殖功效。
[0371]
实施例11含有amc-109的生物可吸收薄膜的流延
[0372]
11.1生物可吸收聚合物
[0373]
·
resomerl206s(聚l-丙交酯酯封端的)(sigma aldrich 719854)溶于二氯甲烷(dcm)中,amc-109溶于氯仿中
[0374]
·
resomer rg502(聚-d,l-丙交酯-共-乙交酯)(sigma aldrich 719889)溶于四
氢呋喃(thf)中,amc-109也溶于thf中
[0375]
11.2生物可吸收薄膜的制备
[0376]
流延溶液
[0377]
将resomer rg502生物可再吸收聚合物材料和amc-109分别溶解在thf中,其方式使得amc-109与最终涂刷溶液中的生物可再吸收聚合物相比的量为5%。amc-109在thf中的溶解需要几个小时。
[0378]
将resomerl206s生物可吸收聚合物材料和amc-109分别单独溶解在二氯甲烷和氯仿中。amc-109和l206s之间的比例与上文相同。
[0379]
流延过程
[0380]
通过将8ml流延溶液置于具有浅压痕的铝箔上,或将涂料溶液倾倒在表面皿上,来制备薄膜样品。干燥(几天)后,以机械方式使薄膜流延膜从其表面脱离。
[0381]
11.3含有amc-109的生物可吸收薄膜的amc-109泄漏的测定
[0382]
提取
[0383]
从流延薄膜上切下样品并精确称重(100-150mg),计算样品中amc-109的量。将样品置于小瓶中,加入水(2ml)并摇动小瓶。进行了6次连续提取。每次提取时,用去离子水(2ml)替换旧提取液。以10s、5min、30min、3h、22h和48h的振荡周期进行提取。使用预制的标准曲线,通过在280nm的紫外分光光度测定法,测定各提取物中amc-109的量。结果示于图11中。
[0384]
11.4含有amc-109的可生物再吸收薄膜的微生物学评价
[0385]
细菌菌株:
[0386]
·
金黄色葡萄球菌8325
[0387]
改良aatcc-100法
[0388]
将金黄色葡萄球菌的过夜集落在0.9%nacl中稀释至0.5mcfarland,产生1
×
108个细菌的细菌浓度。将该溶液在tsb中进一步稀释成1
×
105个细菌。
[0389]
将l206s的薄膜材料切成约0.4
×
0.4cm的片。然后将材料浸没在dh2o中2分钟并在使用前风干。用50μl细菌溶液(1
×
105)接种样品。将样品置于载玻片上并在37℃的湿气室中孵育24小时。每种试验材料进行两个生物副本。
[0390]
孵育后,将薄膜材料彻底洗涤2分钟以除去amc-109,该amc-109容易提取或直接存在于表面上。然后将其置于1000μl nacl中并涡旋45秒,然后进行系列稀释(0-10-6
)并铺板100μl用于cfu计数。
[0391]
微生物学功效
[0392]
集落形成单位
[0393]
cfu数低于含amc材料的检出限。与对照材料相比,cfu数减少7log,见下表。
[0394]
表.含有amc-109的生物可吸收薄膜样品的cfu值。
[0395]
tpu/聚合物amc-109对照l206s08.7
×
107rg502**
[0396]
*rg502材料在24小时孵育期间崩解并牢固地粘附到载玻片表面。无法回收材料。
[0397]
11.5结论
[0398]
·
resomers可被一些溶剂溶解,thf和二氯甲烷在所测试的溶剂中具有最普遍的适用性。
[0399]
·
amc-109可被混合到溶解于thf或氯仿中的聚合物中。溶解amc-109的溶剂必须与用于溶解resomers的溶剂混溶。
[0400]
·
可将所得流延液施加在一些表面上或用于流延薄膜。
[0401]
·
流延薄膜首先快速泄漏amc-109,根据resomer的性质,在至少两天内维持较低浓度。
[0402]
·
resomer rg502薄膜显示出引入关注的泄漏行为。聚合物随时间崩解并且在延长的时间段内连续泄漏amc-109。
[0403]
·
resomer l206s薄膜不会像resomer rg502那样迅速崩解,并且可以具有更长时间段的活性。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1