一种高果糖诱发幼年SD大鼠膀胱过度活动症模型的建立方法与流程
本发明涉及生物,尤其涉及一种高果糖诱发幼年sd大鼠膀胱过度活动症模型的建立方法。
背景技术:
1、膀胱过度活动症(overactive bladder)是儿童期非常常见的功能性膀胱疾病,世界范围内其发病率高达12%。国际儿童控尿协会将其定义为“尿急,通常伴随着尿频和夜遗尿,有或没有合并日间尿失禁,无尿路感染或其他明显病理的神经症状”,是儿童最常见的排尿功能障碍。因为症状每天频繁发作,严重影响孩子的生活质量。目前,儿童oab研究较少,发生机制不明,且伦理上不允许临床外科医生对oab儿童进行膀胱组织活检,因此无法获取临床标本进行科学研究。但根据本发明团队的临床统计数据,近90%的儿童特发性oab的发生与近期高糖饮食相关,这样的临床发现催使我们提出一个假说:儿童期摄入食物中含有过多的糖分,可能导致的膀胱粘膜及平滑肌细胞的功能改变,这可能是诱发儿童oab的发生的重要原因之一。为了验证这一理论,我们需要高糖诱发幼年sd大鼠的动物模型。
2、目前,国内及国际常用的动物模型包括高代谢综合征、胰岛素抵抗诱发成年雌性鼠oab模型、脊髓神经损毁截瘫鼠神经性oab/低压力膀胱模型、膀胱出口梗阻诱发oab模型、转基因动物模型等,其本身诱导症状发生模拟的年龄无法模拟儿童,并且诱导症状发生的机制也不能反映儿童期摄糖后诱发oab发生的过程。因此,在幼年sd大鼠建立高糖作为诱发因素的动物模型,对于研究oab儿童膀胱逼尿肌及黏膜上皮细胞功能改变情况,从而进一步明确其发生机制,并寻找个体化治疗方案至关重要。
3、目前,与上述研究最有关联的是“高果糖诱发的成年sd大鼠高代谢综合征诱发的胰岛素抵抗引起的膀胱过度活动症”,lee wc等使用高果糖饲料喂养离笼sd大鼠13周达到胰岛素抵抗状态诱发oab模型。该模型验证的是“长期果糖应激后诱发的胰岛素抵抗状态下,所诱发的大鼠尿频模型”,本身用于模拟成年人女性的胰岛素抵抗状态诱发的尿频状态,所得结论是“高能量果糖的长期喂养导致胰岛素抵抗,对成年人女性的膀胱功能产生影响”,其同样无法模拟儿童期尿频的功能改变情况,也不能用于研究儿童期膀胱过度活动症的发病机制(儿童短期果糖摄入没有胰岛素抵抗)。
技术实现思路
1、本发明所要解决的技术问题在于提供一种高果糖诱发幼年sd大鼠膀胱过度活动症模型的建立方法,该方法可以模拟儿童期高糖饮食诱发尿频的发生过程,用于进一步研究儿童高糖诱发尿频机制。
2、本发明采用以下技术方案解决上述技术问题:
3、一种高果糖诱发幼年sd大鼠膀胱过度活动症模型的建立方法,包括如下步骤:
4、s1、准备spf级雌性3周龄sd大鼠;
5、s2、对大鼠进行环境适应性饲养4天;期间,给予大鼠纯化型维持饲料喂养,且保证食饮自由;
6、s3、进行体重、血压监测,同时留取血样查血脂、血糖和胰岛素水平;
7、s4、给予大鼠“60%高果糖饲料”喂养,饮用水和之前保持相同;饲养期为7天;
8、s5、复查大鼠体重、血压、血脂、血糖、胰岛素水平;
9、s6、进行旷场行为学检测或排尿印记实验,对验证为阳性的实验鼠进行尿流动力学测定;测定后,若诱发连续2个及以上不稳定收缩波,则判定为建模成功。
10、作为本发明的优选方式之一,所述步骤s1中,选择好相应的spf级雌性3周龄sd大鼠后,将其放入屏障环境检疫室,进行为期5天的检疫观察,无异常后进行后续步骤。
11、作为本发明的优选方式之一,所述步骤s2中,将大鼠饲养在屏障环境中,在24±0.5℃温度和12h/12h的明/暗循环下,进行环境适应性饲养4天。
12、作为本发明的优选方式之一,所述步骤s2中,食饮自由指“给予大鼠充足的纯化型维持饲料和饮用水,使所述大鼠进行自由进食和喝水”。
13、作为本发明的优选方式之一,所述步骤s2中,纯化型维持饲料选择江苏省协同医药生物工程有限责任公司生产的纯化型维持饲料xt704。
14、作为本发明的优选方式之一,所述步骤s4中,“60%高果糖饲料”择江苏省协同医药生物工程有限责任公司生产的60%高果糖饲料xt704。
15、作为本发明的优选方式之一,所述步骤s5中,复查大鼠体重、血压、血脂、血糖、胰岛素水平,用于证实未出现胰岛素抵抗及糖尿病。
16、作为本发明的优选方式之一,所述步骤s6中,旷场行为学检测步骤:在旷场行为学测定软件中设置好参数,记录好动物编号、日期、状态灯信息;将实验大鼠从饲养笼中取出,背向实验者,将实验大鼠放置于实验箱的中央区域;打开动物行为学分析软件,自动记录实验大鼠在箱体内的活动时间和范围,实验时间8min;其中,当实验大鼠相比对照组大鼠,活动范围增大、步数增多、活动力增大,认为是阳性结果。
17、作为本发明的优选方式之一,所述对照组大鼠在7天饲养期中,用纯化型维持饲料替代“60%高果糖饲料”。
18、作为本发明的优选方式之一,所述步骤s6中,排尿印记实验步骤:将实验大鼠置于代谢笼中,笼底铺入硫酸铜纸滤纸,连续监测5h,尿液滴至硫酸铜滤纸表面,呈现肉眼可见的蓝色斑点状印迹;拍摄照片,使用识图软件读取排尿印迹数量,计算排尿频率;其中,当实验大鼠的排尿印迹点数大于5个,认为结果阳性。
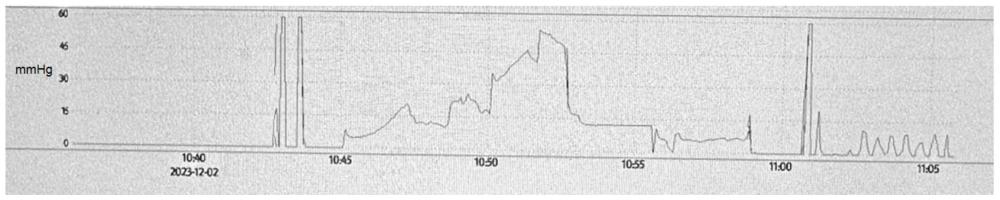
19、作为本发明的优选方式之一,所述步骤s6中,尿流动力学测定步骤:使用动物尿流动力学测定设备;通过软件体内置零膀胱内压力,0.9%生理盐水微量泵维持6ml/h速度持续向膀胱内灌注,灌注过程中观察大鼠尿道外口是否出现尿液溢出;当膀胱压力升高、并且出现尿液排出时,此时的膀胱收缩为正常收缩,记录此时的膀胱压力为排尿时膀胱最大压力,计算膀胱最大容量等于灌注时间乘以灌注速度;在灌注或者停止灌注过程中,膀胱压力异常升高又回落,但未观察到大鼠尿道外口尿液流出时,判定为膀胱不自主收缩;其中,每只鼠重复灌注4次,若膀胱充盈期逼尿肌不稳定收缩波存在、且连续2次及以上,则判定阳性,即do或oab;若不稳定收缩波只出现1次,则第二日再次行尿动力检查,仍在1次及以下判定阴性。
20、设计思路及原理:
21、由于对高果糖的短期影响认识不足,目前的研究者并没有发现“儿童短期高能量果糖饮食会大大提高膀胱过度活动症发生率”的临床现象,也没有尝试“短周期高能量果糖的建立模型”数据报道。对于“儿童高果糖饮食诱发膀胱过度活动症”这一现象,为本发明首先发现,除了临床研究证据外,需要相应的动物模型把这个现象进行复刻,以便对现象发生机制进行研究。之前,“高果糖诱发胰岛素抵抗导致的膀胱过度活动症”是成人糖尿病诱发这个疾病对应的动物模型,和“儿童期发生该疾病的病因和发病机制”完全不同(与之不同,儿童短期果糖摄入没有胰岛素抵抗)。因此,需要建立一个全新的“高果糖诱发幼年sd大鼠膀胱过度活动症模型”,以模拟儿童期高糖饮食诱发尿频的发生过程,便于进一步研究儿童高糖诱发尿频机制。
22、本发明相比现有技术的优点在于:
23、本发明使用3周龄幼年sd大鼠进行1周喂养,时间短,成本低,成模快,就可以诱发幼年sd大鼠的尿频和膀胱过度活动症的状态,该方法可以模拟儿童期高糖饮食诱发尿频的发生过程,并能够提供用于进一步研究儿童高糖诱发尿频机制的动物模型。其中,需注意的是,大鼠的性成熟和体成熟年龄在7周左右,因此从建立到症状诱发模型成型可供操作的时间只有高果糖喂养后2周(7周成年后的高果糖对于代谢的影响与幼年期完全不同,大鼠体内果糖喂养时间3~7天之后会出现果糖耐受,代谢会发生变化);我们的研究数据表明,“超过1周喂养高果糖饲料的膀胱过度活动症”诱发率大大降低,因此需要严格把握高果糖喂养7天的饲养时间。
- 还没有人留言评论。精彩留言会获得点赞!