利用益生菌制备发酵芝麻蛋白的方法及其用途与流程
本发明涉及蛋白加工领域,特别是一种利用益生菌制备发酵芝麻蛋白的方法及其用途。
背景技术:
民以食为天,食物安全性问题越来越受人们关注,其中食物过敏是一种重要的食品安全问题。它是指当人体摄入某种特定的食物后在体内发生特异性免疫反应,属机体对外源物质产生的一种变态反应,严重者可在几分钟内引起多种器官出现过敏反应,甚至导致个体休克或死亡。
随着食物品种越来越多样化,食物过敏原的种类和来源途径急剧增加,与之直接相关的过敏性疾病亦趋于复杂化、严重化。近年来,食物过敏患者日益增多,过敏症发病率也呈逐年上升趋势,据报道食物过敏影响近5%的成人和6%~8%的儿童【sicherersh.foodallergy:epidemiology,pathogenesis,diagnosis,andtreatment[j].jallergyclinimmunol,2014,133(2):291】,因此食物过敏已被视为一种严重的世界公共卫生问题。其中芝麻作为一种重要的食物过敏原,其过敏已引起世界各国的关注,欧盟,加拿大、澳大利亚和新西兰,均要求在含有芝麻成分的包装上必须标示含有芝麻过敏原,以防止有芝麻过敏体质的人群误食,中国台湾也要求在2020年7月强制标示此类标签。
芝麻作为一种药食两用食疗品,其食疗作用早已被公认,常食有益。《神农本草经》记载:“芝麻,补心脏,益气力,长肌肉,填髓脑,久服强身”。《本草经疏》中曰:“芝麻,气味和平,不寒不热,补肝肾之佳谷也”。《本草崇原》中言:“麻乃五谷之首,禀厥阴春生之气。夫五运始于木,而递相资生。主治伤中虚羸者,气味甘平,补中土也。补五内,益气力,所以治伤中也。长肌肉,填髓脑,所以治虚羸也”。《中国药典》2015版也收录黑芝麻功效为:补肝肾,益精血,润肠燥,用于精血亏虚,头晕眼花,耳鸣耳聋等;并且现代研究表明:芝麻中富含优质蛋白质(18%~20%),氨基酸组成与fao/who推荐的人类蛋白质标准具有很好的一致性【郑华丽,等.芝麻饼粕蛋白应用进展[j].粮食与油脂,2012(8):8】。此外,芝麻的良好风味,使其深受人们喜爱,作为一种食材,广泛添加于各种食品中,如零食、汤圆、酥糖、烧饼、饼干、麻花等。但近年来随着潜在过敏反应的发现,芝麻食物过敏的发病率呈上升趋势【appel,my,etal.evaluationofthebasophilactivationtestandskinpricktestingforthediagnosisofsesamefoodallergy[j].clinexpallergy.2018,48(8):1025】,芝麻作为重要的过敏原之一,其过敏及潜在过敏人群如果不小心误食可能会带来严重后果。所以,制备出低致敏性,高营养保健的芝麻制品迫在眉睫。
目前,减轻或降解食物过敏原的方法有物理法,包括加热、辐照、超高压等;化学法,包括糖基化修饰、强酸、强碱、水解等;生物法,包括酶解、发酵、基因改良等【黄婷,等.食物蛋白过敏原及其脱敏方法的研究进展[j].粮食与油脂,2015(8):4】。其中微生物发酵法作为一种新的脱敏技术,近年也取得了一定进展,包括发酵豆制品、发酵牛乳、发酵小麦、发酵花生制品、发酵鱼类等以降低致敏性【伍恒,等.发酵法对降低食品过敏原的作用[j].食品工业科技,2011,(8):453;中国发明专利cn106722382a“一种利用微生物降低鱼类过敏原活性的方法”】。发酵不仅可以改变过敏原中蛋白结构,将一些具有抗原活性的蛋白质分解或变性,降低其蛋白致敏性;而且蛋白经过微生物发酵后大分子蛋白抗原会被转化为小分子多肽和氨基酸,从而能更好的被人体吸收,营养价值提高【唐传核.食物蛋白质来源的水解物或多肽的现状及进展——(ⅰ)营养吸收特性、国内外现状以及生产工艺[a].中国食品添加剂协会成立十周年暨第七届中国国际食品添加剂展览会学术论文集[c].中国食品添加剂生产应用工业协会,2003:9;黄颖.微生物发酵法降解大豆致敏原的研究[d].江南大学,2012;】。
发酵使用的微生物包括乳酸杆菌、双歧杆菌、枯草芽孢杆菌、米曲霉、米根霉、酵母菌、及木糖葡萄球菌等【crossml,etal.anti-allergypropertiesoffermentedfoods:animportantimmunoregulatorymechanismoflacticacidbacteria[j].intimmunopharmacol,2001,1(5):891;伍恒,等.发酵法对降低食品过敏原的作用[j].食品工业科技,2011(8):453;中国发明专利cn1760360a“发酵乳酸杆菌gm-090及其在刺激inf-γ分泌及/或治疗过敏的用途”】。但乳酸杆菌的抗过敏作用具有菌株特异性,有的乳酸杆菌不仅不具有抗过敏作用,反而会增加过敏反应的程度【meijerinkm,etal.immunomodulatoryeffectsofpotentialprobioticsinamousepeanutsensitizationmodel[j].femsimmunolmedmicrobiol,2012,65(3):488】,因此发酵后致敏性是否降低,必须要进一步的研究。
罗伊氏乳杆菌,作为一种目前已报到几乎存在于所有哺乳动物肠道内的乳酸杆菌,具有改善过敏体质、预防过敏反应,缓解乳糖不耐症,增强人体免疫,降低胆固醇以及预防癌症和抑制肿瘤生长等益生保健作用,是一种益生菌【forsythep,etal.oraltreatmentwithlivelactobacillusreuteriinhibitstheallergicairwayresponseinmice.[j].amjrespircritcaremed.2007,175(6):561;李正华.罗伊氏乳杆菌生物学特性及功能性发酵乳的研究[d].江南大学,2008】。而且,在47株乳酸杆菌益生菌中,罗伊氏乳杆菌是唯一即具有很强的抑制病原微生物的能力,又不会对肠道中正常菌群造成抑制,还能在人体很好定植的乳酸杆菌【jacobsench,etal.screeningofprobioticactivitiesofforty-sevenstrainsoflactobacillusspp.byinvitrotechniquesandevaluationofthecolonizationabilityoffiveselectedstrainsinhumans[j].applenvironmicrobiol,1999,65(11):4949】。我国卫生部于2003年,批准了罗伊氏乳杆菌可作为人类保健品的微生物菌种。但是罗伊氏乳杆菌发酵芝麻蛋白,是否能降低芝麻过敏性,并将大分子蛋白转化为小分子多肽,尚无人研究。
综上,虽然上述专利或文献公开了近年来其他食品减敏的新方法,但如何制备出低敏性、高营养保健的芝麻产品,至今未见报道。
技术实现要素:
针对上述情况,为克服现有技术缺陷,本发明之目的就是提供一种利用益生菌发酵芝麻蛋白制备低敏产品的方法及其用途,可有效解决潜在芝麻过敏及芝麻过敏人群食用芝麻产品的安全性问题。
本发明解决的技术方案是,(1)芝麻蛋白溶液的制备:取芝麻筛净除杂后,加入芝麻重量6~12倍量的超纯水,用组织破碎法提取2次,每次提取均为粉碎30秒,间歇2秒,再粉碎60秒,间歇2秒,再粉碎30秒,提取液过滤,合并2次滤液,加入质量浓度5%的碳酸氢钠,调节ph6.5~7.5,即得芝麻蛋白溶液;(2)接种发酵:取罗伊氏乳杆菌,加入无菌生理盐水,调整至浓度为1×108cfu/ml~1×1010cfu/ml的菌液,接种于芝麻蛋白溶液中,接种量为10~15ml芝麻蛋白溶液使用1ml菌液,在30~43℃,50~100r/min的条件下,发酵2~12h;得液体状发酵芝麻蛋白溶液;或将得到的液体状发酵芝麻蛋白溶液浓缩至45℃下测定相对密度1.05~1.25,干燥,得粉状的发酵芝麻蛋白;所述的超纯水又称up水,是指电阻率达到18mω*cm(25℃)的水。
本发明的另一目的在于,提供上述发酵芝麻蛋白在制备低敏、高营养药物组合物、特殊食品或食品组合物中的应用,该发酵芝麻蛋白能有效降低芝麻的致敏性,不仅能够减轻芝麻过敏人群的过度免疫应答症状,而且其发酵所产生的芝麻肽分子量更小,45kda以上的大分子基本降解,能更好地被人体吸收,此外,还能巧妙利用罗伊氏乳杆菌的益生保健作用,从而具有低致敏性、高营养及保健的功能。
本发明还提供一种低敏、高营养药物组合物或特殊食品、食品组合物,均包含上述的发酵芝麻蛋白以及药学上或食品上可接受的载体。
所述的低敏、高营养药物组合物为口服制剂或注射剂。
所述的特殊食品或食品组合物为营养补充品、保健食品、特殊医学用途配方食品、普通食品或饮料。
本发明的优点在于:
(1)本发明使用罗伊氏杆菌益生菌发酵芝麻蛋白,充分利用其能很好在人体定植的优势,发挥罗伊氏杆菌的多种益生作用:改善过敏体质,预防过敏反应,抑制病原微生物,又不影响肠道中正常菌群。
(2)本发明制备的低致敏性发酵芝麻蛋白,既降低了芝麻蛋白的过敏性,又使大分子量蛋白降解,具有易被人体吸收的特点,营养价值提高。
附图说明
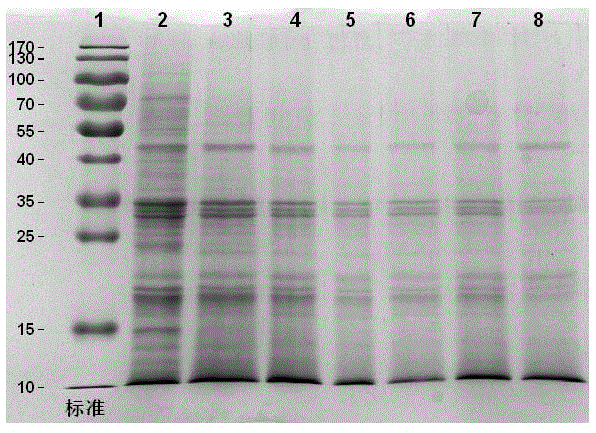
图1为本发明发酵芝麻蛋白随发酵时间变化的sds-page电泳图谱。
图2为本发明不同发酵时间得到的发酵芝麻蛋白与过敏小鼠血清结合能力的免疫印迹图谱。
图3为本发明中原生芝麻蛋白与发酵芝麻蛋白刺激的致敏小鼠血清免疫印迹图谱。
具体实施方式
以下结合实施例对本发明的技术方案作详细说明。
实施例1
取黑芝麻,筛净除杂后,加入黑芝麻重量12倍量的超纯水,用组织破碎法提取2次,每次提取均为粉碎30秒,间歇2秒,再粉碎60秒,间歇2秒,再粉碎30秒,提取液过滤,合并2次滤液,用质量浓度5%的碳酸氢钠调节ph为6.8,得芝麻蛋白溶液;取罗伊氏乳杆菌,加入无菌生理盐水,调整至浓度为1×108cfu/ml的菌液,接种于芝麻蛋白溶液中,接种量为10ml芝麻蛋白溶液使用1ml菌液,在37℃,70r/min的条件下,摇床发酵8h,将得到的液体状发酵芝麻蛋白溶液浓缩至45℃下测定相对密度1.2,冷冻干燥至粉状,即得粉状的发酵芝麻蛋白。
实施例2
取白芝麻,筛净除杂后,加入白芝麻重量10倍量的超纯水,用组织破碎法提取2次,每次提取均为粉碎30秒,间歇2秒,再粉碎60秒,间歇2秒,再粉碎30秒,提取液过滤,合并2次滤液,用质量浓度5%碳酸氢钠调节ph为7,得芝麻蛋白溶液;取罗伊氏乳杆菌,加入无菌生理盐水,调整至浓度为1×1010cfu/ml的菌液,接种于芝麻蛋白溶液中,接种量为15ml芝麻蛋白溶液使用1ml菌液,在35℃,100r/min的条件下,发酵罐发酵12h,将得到的液体状发酵芝麻蛋白溶液浓缩至45℃下测定相对密度1.05,真空减压干燥,至粉状,即得粉状的发酵芝麻蛋白。
实施例3
取黄芝麻,筛净除杂后,加入黄芝麻重量6倍量的超纯水,用组织破碎法提取2次,每次提取均为粉碎30秒,间歇2秒,再粉碎60秒,间歇2秒,再粉碎30秒,提取液过滤,合并2次滤液,用质量浓度5%碳酸氢钠调节ph为6.7,得芝麻蛋白溶液;取罗伊氏乳杆菌,加入无菌生理盐水,调整至浓度为3×108cfu/ml的菌液,接种于芝麻蛋白溶液中,接种量为13ml芝麻蛋白溶液使用1ml菌液,在40℃,50r/min的条件下,摇床发酵6h,将得到的液体状发酵芝麻蛋白溶液浓缩至45℃下测定相对密度1.1,喷雾干燥,即得粉状的发酵芝麻蛋白。
实施例4
取黑芝麻,筛净除杂后,加入黑芝麻重量8倍量的超纯水,用组织破碎法提取2次,每次提取均为粉碎30秒,间歇2秒,再粉碎60秒,间歇2秒,再粉碎30秒,提取液过滤,合并2次滤液,用质量浓度5%的碳酸氢钠调节ph为6.9,得芝麻蛋白溶液;取罗伊氏乳杆菌,加入无菌生理盐水,调整至浓度为1×108cfu/ml的菌液,接种于芝麻蛋白溶液中,接种量为14ml芝麻蛋白溶液使用1ml菌液,在30℃,80r/min的条件下,摇床发酵8h,即得液体状发酵芝麻蛋白溶液。
实施例5
取黄芝麻,筛净除杂后,加入黄芝麻重量11倍量的超纯水,用组织破碎法提取2次,每次提取均为粉碎30秒,间歇2秒,再粉碎60秒,间歇2秒,再粉碎30秒,提取液过滤,合并2次滤液,用质量浓度5%碳酸氢钠调节ph为7,得芝麻蛋白溶液;取罗伊氏乳杆菌,加入无菌生理盐水,调整至浓度为3×108cfu/ml的菌液,接种于芝麻蛋白溶液中,接种量为12ml芝麻蛋白溶液使用1ml菌液,在43℃,60r/min的条件下,发酵罐发酵4h,即得液体状发酵芝麻蛋白。
本发明制备的发酵芝麻蛋白,经试验验证,致敏性降低,可用于制备营养价值高的低致敏性芝麻蛋白食品或药品,有关试验的具体情况如下:
试验例1
芝麻蛋白组分分析:采用十二烷基磺酸钠-聚丙烯酰胺凝胶电泳(sds-page),检测芝麻蛋白发酵后成分变化的情况。按常规sds-page方法进行恒压电泳,浓缩胶浓度为5%,分离胶浓度为12%,蛋白样品上样量10µl,在浓缩胶中电泳电压为80v,进入分离胶后调至120v,至溴酚蓝到达底部时停止跑胶,电泳结束后用考马斯亮蓝r-250染色2~3h,再加入脱色液脱色过夜,以bio-rad凝胶成像系统观察蛋白质图谱,结果如图1:1~8蛋白泳道分别为蛋白marker、未发酵原生芝麻蛋白、按照本发明的方法用罗伊氏乳杆菌发酵2、4、6、8、10、12h的发酵芝麻蛋白,由图1可知,未发酵原生芝麻蛋白条带较多,除了55kda以上的大分量蛋白外,还有55kda以下11~14kda、15~20kda、30~35kda、45~50kda的蛋白。发酵后,既使只发酵2h以上,55kda以上的大分子量蛋白几乎就完全降解,说明发酵可降解大分子量蛋白;而且随着发酵时间的延长,55kda以下的蛋白条带强度也可见明显减弱,其中11~14kda、15kda、及55kda左右的条带几乎被完全降解消耗,芝麻过敏蛋白包括9~14kda的白蛋白,15kda的油质蛋白、及52.2kda和56.6kda的两种球蛋白,因此,发酵可降解芝麻过敏蛋白。由此可见,使用本发明方法可降解大分子量芝麻蛋白,并大大减少过敏蛋白的含量。
试验例2
过敏小鼠血清的免疫印迹分析:本试验使用过敏小鼠血清,作为一抗,与原生芝麻蛋白、及不同发酵时间芝麻蛋白(即本发明),孵育,以western-blot免疫印迹法,考察发酵后芝麻蛋白过敏原的减少。步骤如下:1)过敏小鼠模型制备:6只balb/c雌性小鼠,适应性饲养3天后,在第1天,腹腔注射0.2ml、1mg/ml(0.1ml完全弗氏佐剂+0.1ml的2.0mg/ml芝麻蛋白液)的生理盐水蛋白液,在第8、21天,腹腔注射0.2ml、1mg/ml(0.1ml不完全弗氏佐剂+0.1ml的2.0mg/ml芝麻蛋白液)的生理盐水蛋白液加强致敏,在第24天,灌胃芝麻蛋白液0.2ml激发,半小时后取血,血清放置-80℃冰箱保存。2)western-blot分析:取原生芝麻蛋白和不同时间发酵的芝麻蛋白(不同时间发酵的芝麻蛋白为按照本发明的方法用罗伊氏乳杆菌发酵2、4、6、8、10、12h的发酵芝麻蛋白),进行sds-page电泳,浓缩胶浓度为5%,分离胶浓度为12%,蛋白上样量15µl,浓缩胶中电泳电压为80v,进入分离胶后调至120v,电泳1h,然后,180ma16min湿法转膜,将胶中蛋白条带转移至pvdf膜;丽春红染色判断蛋白转移成功后,将膜浸入含有5%脱脂奶粉的pbst溶液(含有0.05%tween-20的pbs缓冲液)中,37℃封闭1h,接着以0.05%pbst溶液清洗pvdf膜4次,每次5min,再加入1:100稀释的过敏模型组小鼠血清进行一抗孵育,4℃过夜后,加入hrp标记的山羊抗小鼠igg(1:5000)作为二抗,37℃孵育1h后,用pbst洗涤3次,将pvdf膜放入成像仪中,滴加ecl发光液显色、曝光。结果如图2:m:marker,原生:原生芝麻蛋白,1~6:分别代表发酵2、4、6、8、10、12h的发酵芝麻蛋白;与一抗1:100稀释的过敏小鼠血清孵育,二抗为hrp标记的山羊抗小鼠igg。
由western-blotting结果可知,原生芝麻蛋白含有大量过敏原,主要包括分子量为35kda以下的3个条带(10kda以下、14kda左右、26kd左右)及45~55kda的2个条带。芝麻主要过敏蛋白主要包括缺少硫元素的2s白蛋白(sesi1,9~14kda),富含硫元素的2s白蛋白(sesi2,7kda),7s球蛋白(sesi3,45kda)【schöringhumerk,etal.developmentofareal-timepcrmethodtodetectpotentiallyallergenicsesame(sesamumindicum)infood,jagricfoodchem,2007,55(26):10540;马秀丽,等.芝麻过敏原分子特征与检测方法研究进展.食品科学,2018,1-15】,2种油质蛋白(sesi4,17kda;sesi5,15kda)以及两种11s球蛋白(sesi6,52.2kda;sesi7,56.6kda)等【张文举,等.芝麻过敏原pcr检测方法[j].食品与机械,2012,28(2):52-55;maruyaman,etal.measurementofspecificigeantibodiestosesi1improvesthediagnosisofsesameallergy.clinexpallergy,2016,46(1):163】。原生芝麻蛋白电泳结果跟文献中所述的过敏蛋白基本一致;其中45~55kda左右的2个条带(可能包括45kda、52.2kda及56.6kda的3个蛋白),与芝麻过敏小鼠的阳性血清免疫强烈结合,发生免疫原性反应,说明这两个蛋白是最严重的过敏原。过敏原与过敏小鼠血清,发生抗原抗体免疫结合反应的现象,在罗伊氏乳杆菌发酵芝麻蛋白中,明显减弱,随着发酵时间的延长,过敏蛋白条带都逐渐被降解消耗,尤其是11~14kda和45~50kda左右蛋白,在发酵2h时就开始被降解,在发酵8h时几乎消失,而且随时间延长,15~30kda左右的蛋白也开始降解,说明使用本发明方法可有效降解芝麻过敏原蛋白。
试验例3
过敏症状评分:本实验考察致敏小鼠,灌胃给予原生芝麻蛋白、不同发酵时间芝麻蛋白激发后,与过敏相关的行为学变化情况。在体内试验说明芝麻蛋白经发酵降解后,过敏性是否降低。步骤如下,芝麻蛋白小鼠过敏模型的制备:balb/c雌性小鼠共18只,适应性喂养3天后,随机分组(每组各6只),分为模型组,罗伊氏乳杆菌发酵蛋白组(按照本发明方法用罗伊氏乳杆菌发酵8h的发酵芝麻蛋白为代表,简称发酵蛋白组,以下同)和空白组。在第1、8、21天,模型组和发酵蛋白组同试验例2,腹腔注射,致敏小鼠,空白组在同样时间点,腹腔注射等量生理盐水,在第24天,模型组灌胃芝麻蛋白液0.2ml激发过敏,发酵蛋白组灌胃本发明的方法用罗伊氏乳杆菌发酵8h的芝麻蛋白液0.2ml激发,空白组灌胃等量生理盐水,观察小鼠动物学行为,半小时后处死,摘除眼球取血,血清放置-80℃冰箱保存。
致敏小鼠动物学行为评分结果如表1。由表1可知,空白组未出现1~5号的过敏症状,模型组跟发酵蛋白组小鼠均有不同程度的过敏学行为反应出现,但模型组的过敏学行为更加严重,已有2只出现第四等级的严重过敏行为,而发酵蛋白组小鼠整体向过敏学行为更低的等级移动,不再出现第四等级的过敏行为,而向更弱的第二或第一等级偏移,说明发酵蛋白刺激的小鼠过敏反应行为减少,程度减轻,即发酵蛋白的致敏性降低。
表1过敏小鼠动物学评分
试验例4
发酵蛋白小鼠血清的免疫印迹分析:本实验考察灌胃给予原生芝麻蛋白、发酵芝麻蛋白(按照本发明方法用罗伊氏乳杆菌发酵8h的发酵芝麻蛋白为代表,简称发酵蛋白组,以下同)及空白生理盐水的各组小鼠血清,与原生芝麻蛋白发生免疫反应的情况,从另一方面说明发酵后芝麻蛋白免疫原性降低。步骤为:同试验例3制备空白组、模型组及发酵蛋白组小鼠血清。然后,取原生芝麻蛋白,进行电泳、转膜、封闭后,分别加入1:100稀释的空白组、模型组及发酵蛋白组小鼠血清进行一抗孵育,4℃过夜,加入hrp标记的山羊抗小鼠igg(1:5000)作为二抗,37℃,1h,用pbst洗涤3次,滴加ecl发光液显色、曝光、成像,结果如图3(m:marker、1:空白组血清、2:模型组血清、3:发酵蛋白组血清)。由结果可知,原生芝麻蛋白(即未发酵芝麻蛋白)与各组小鼠血清孵育后,空白组血清不含与原生芝麻蛋白发生免疫应答反应的蛋白,故无条带;模型组灌胃原生芝麻蛋白激发后,小鼠血清中产生了大量的免疫原性物质,与原生芝麻蛋白进行免疫应答变态反应,蛋白条带多而深;而灌胃罗伊氏乳杆菌发酵蛋白刺激后,小鼠血清对原生芝麻蛋白的抗原抗体免疫反应明显降低,远低于模型组血清,由此再次验证,发酵后芝麻过敏蛋白被降解消耗。
试验例5
鼠李糖乳杆菌,亦是一种益生乳酸杆菌,与罗伊氏乳杆菌类似,也具有改善过敏体质、预防过敏、增强免疫能力、抑菌、平衡和改善胃肠道功能,预防腹泻等多种益生作用【方拴锋,等.鼠李糖乳杆菌改善卵清蛋白诱导的食物过敏小鼠症状及其机制[j].细胞与分子免疫学杂志,2017,33(05):597;魏华,等.鼠李糖乳杆菌的生物学特性及发酵性能研究[j].食品与发酵工业,2001,27(09):11;刘冬梅,等.鼠李糖乳杆菌产生抗菌物质的抑菌作用和特性研究[j].中国乳品工业,2006,34(01):13;王桂英.鼠李糖乳杆菌片对小鼠肠道菌群失调性腹泻的治疗作用[j].药学进展,2009,33(05):218】。按本方法用鼠李糖乳杆菌发酵芝麻蛋白得到的鼠李糖乳酸杆菌发酵芝麻蛋白,对芝麻过敏性的影响也进行了试验,具体如下:
同试验例2、3及4,使用鼠李糖乳酸杆菌发酵芝麻蛋白,进行过敏小鼠血清的免疫印迹分析、过敏症状评分及发酵蛋白小鼠血清的免疫印迹分析,结果发现,使用鼠李糖乳酸杆菌发酵芝麻蛋白,芝麻过敏原蛋白没有被降解,也没有改善过敏行为学,而且灌胃鼠李糖乳酸杆菌发酵芝麻蛋白的小鼠血清,对原生芝麻蛋白的抗原抗体免疫,基本与模型组一样,没有差别。因此,鼠李糖乳酸杆菌发酵芝麻蛋白不能降低芝麻蛋白的致敏性。
综上,具有改善过敏症状的乳酸杆菌,经发酵后不一定能降低所发酵物的过敏性,如鼠李糖乳酸杆菌;而本发明所保护的罗伊氏乳杆菌益生菌发酵芝麻蛋白制备的产品,不仅降解芝麻大分子蛋白,又能使芝麻致敏性降低,达到了即降低芝麻致敏性,又易吸收,且保留益生菌保健作用的目的,为进一步优化具有高营养保健作用的低敏芝麻产品提供了依据。
以上仅是对本发明实施方式的具体举例,不能被理解为在不付出创造性劳动的前提下,还可以根据这些技术方案获得其他的技术方案,凡是在本发明的基础上所做出的等同或等效的替换,均属于本发明保护的范围。
- 还没有人留言评论。精彩留言会获得点赞!