植物性多聚糖作为制备肠型相关的高尿酸血症药物的应用的制作方法
本申请涉及肠型相关的高尿酸血症治疗或预防药物领域,特别是涉及植物性多聚糖作为制备肠型相关的高尿酸血症药物的应用。
背景技术:
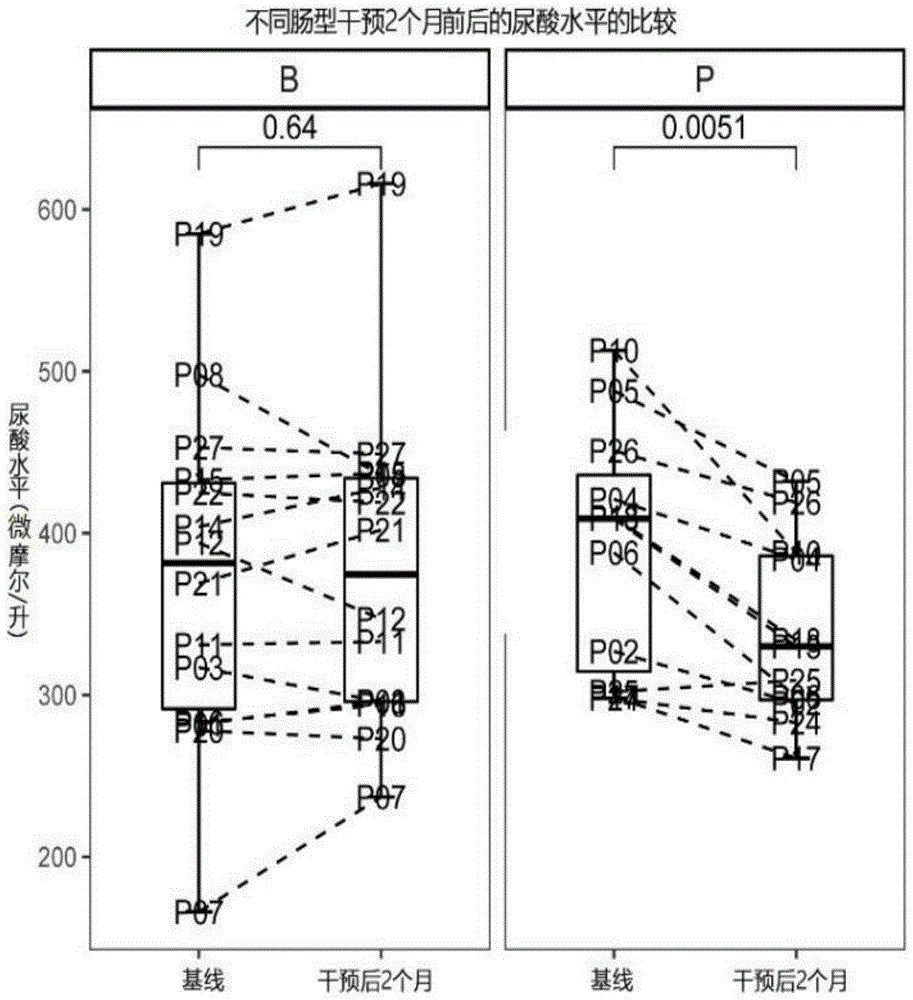
:高尿酸血症(hua)是指在正常嘌呤饮食状态下,非同日两次空腹血尿酸水平男性高于420μmol/l,女性高于360μmol/l,即称为高尿酸血症,属于代谢性疾病。2011年,肠型(enterotypes)的概念首次在《nature》杂志上由arumugam等人提出(arumugam,manimozhiyan,etal."enterotypesofthehumangutmicrobiome."nature473.7346(2011):174-180),该研究发现可以将人类肠道微生物组分为稳定的3种类型,其不受年龄、性别、体重及其地域显示,且稳定性高,与血型类似,因此将其称为“肠型”。由于肠型是连续而非离散的分布,其后的研究也有2种或者4种肠型的报道,造成差异的原因是由于不同方法抽取不同维度进行观测,观测的其实都是复杂肠道菌群大数据整体的某个子集的不同切面,然而不论如何观测,包括更多数据积累发现新类型,都无法否认目前人群中常见的几种肠型,如拟杆菌(bacteroides)型、普氏菌(prevotella)型等的客观存在性。肠型是肠道微生物组在高维数据空间中呈现的客观存在的聚集效应,目前主流的计算方法有2种,一种是基于样品间的jensen-shannon距离(jensen-shannondistance,jsd),利用围绕中心点划分算法(partitioningaroundmedoids,pam),最佳分类数据通过calinski-harabasz(ch)指数确定;另一种则是基于物种丰度,利用狄利克雷多项混合模型(dirichletmultinomialmixturemodel,dmm)进行肠型分类。高尿酸血症肠型的划分对于临床应用具有重要意义,比如作为人体特定状态的风险或易感指标等。此外,由于不同肠型可影响异质性的物质代谢,比如拟杆菌属肠型倾向于分解碳水化合物,而普氏菌属则倾向于降解肠道黏蛋白等,因此肠型在疾病的精准治疗方面也显示出巨大的潜在应用前景。一项对有关2型糖尿病的精准用药研究(naturecommunications2017;8(1):1785)中发现,基线为拟杆菌属肠型的患者在接受阿卡波糖治疗后其获益包括降糖效果、胰岛素抵抗、腰臀比明显优于普氏菌属肠型。其作用机制主要是由于服用阿卡波糖可增加肠道中的双歧杆菌和乳杆菌,降低拟杆菌的丰度,因此改变了参与血浆代谢产物胆汁酸代谢相关菌群的丰度,这对2型糖尿病病人的精准用药提供了重大依据。植物性多聚糖,又称植物多糖或植物多聚糖,是指植物来源的天然聚糖,例如淀粉、果胶、菊粉、圆苞车前子壳等。植物性多聚糖的种类繁多,不同的植物性多聚糖在不同领域都有不同应用,例如用于免疫功能调节、延缓衰老、抗疲劳、降血糖等。菊粉又名菊糖、旋复花粉,土香粉,由德国科学家于1804年从土木香中提取。菊粉是一类天然果聚糖组成的混合物,由β-d-呋喃果糖残基通过β-2,1糖苷键连接而成的链状多糖,末端含有一个葡萄糖残基。通常一个糖苷键叫一个聚合度,不同的植物来源、收获季节、作物的成熟度、土壤以及生产加工技术将对菊粉聚合度和平均分子质量产生重要影响。商品化的菊粉聚合度介于2~60,平均分子量在3500~6000之间,聚合度介于2~9间的菊粉又叫低聚果糖。2009年,菊粉被中国卫生部批准为“新资源食品”。2015年,欧盟发布法规(eu)2015/2314,批准菊苣菊粉(chicoryinulin)有助维持正常肠道功能的健康声称。目前已经有将具有直链结构果聚糖的菊粉用于治疗或预防高尿酸血症及其并发血脂、血糖等多种代谢紊乱疾病的研究和报道。但是,临床数据显示,菊粉在治疗高尿酸血症的过程中,患者尿酸值的响应性差异很大;也就是说,菊粉对不同个体的高尿酸血症治疗效果各不相同;这极大的影响了菊粉真正作为治疗高尿酸血症临床药物的推广和广泛应用。因此,临床上提出了个体化诊疗的概念。然而,目前尚未有实际实施个体化诊疗的具体指导策略。圆苞车前子壳,又称洋车前子纤维,是车前科车前属圆苞车前子(拉丁学名:plantagoovata)种子的外壳。圆苞车前子壳呈椭圆形、不规则长圆形或三角状长圆形;其纤维占80%以上,远高于其他富含纤维谷物,如燕麦和小麦;吸水可膨胀30-50倍,形成果冻状的黏稠物质;其他成分主要包括葡萄糖甙、蛋白质、多糖、维生素b1和胆碱。圆苞车前子壳富含胶质,由树胶醛糖、木糖和少量珊瑚木苷等组成。其中树胶醛糖也称l-阿拉伯糖,是一种戊醛糖,广泛存在于水果和粗粮皮壳中,已有几千年的人类食用历史;然而,直至最近几年树胶醛糖才被发现具有改善血糖、血脂的重要功能。目前,圆苞车前子壳已经于2014年第10号文件批准为新食品原料。目前的研究显示,圆苞车前子壳中的有效成分之一多糖分子——阿拉伯木聚糖,能在小肠中吸水形成糊状物质,可改善粪便和肠壁的润滑作用,促进排空速度;因此,圆苞车前子壳自古以来都被用于润肠排便。近年的研究发现,圆苞车前子壳还可以被肠道内的微生物作用,分解为短链脂肪酸,从而阻止胆固醇的合成,因此具有降低胆固醇的功效。此外,人群干预试验显示,圆苞车前子壳有助于糖尿病患者的血糖控制。美国食品药品管理局(fda)在1998年的声明公告,圆苞车前子壳可溶性纤维能降低心血管疾病风险。但目前未见圆苞车前子壳对高尿酸血症相关的报道。技术实现要素:本申请的目的是提供一种植物性多聚糖的新用途,即植物性多聚糖作为制备防治肠型相关的高尿酸血症药物的应用。本申请采用了以下技术方案:本申请的一方面公开了植物性多聚糖作为制备肠型相关的高尿酸血症药物、食品、保健品或食品添加剂的应用;其中,植物性多聚糖为菊粉和/或圆苞车前子壳,肠型相关的高尿酸血症为普氏菌属肠型高尿酸血症和/或拟杆菌属肠型高尿酸血症。需要说明的是,本申请的关键在于,研究发现植物性多聚糖菊粉对普氏菌属肠型高尿酸血症有极好的治疗效果,而圆苞车前子壳对拟杆菌属肠型高尿酸血症有极好的治疗效果。可以理解,菊粉和圆苞车前子壳可以一起使用,用于治疗复杂的肠型相关的高尿酸血症;两者一起使用时,能够同时对普氏菌属肠型高尿酸血症和拟杆菌属肠型高尿酸血症都有良好的治疗效果。当然,也可以根据实际情况,只使用菊粉或圆苞车前子壳,用于治疗相应的普氏菌属肠型高尿酸血症或拟杆菌属肠型高尿酸血症。具体如何使用,或者两者一起使用时具体的配方可以根据实际情况而定,在此不作具体限定。本申请的一方面公开了菊粉作为制备防治普氏菌属肠型高尿酸血症的药物、食品、保健品或食品添加剂的应用。需要说明的是,本申请创造性的发现并证实菊粉对于普氏菌属肠型高尿酸血症有极好的治疗效果,这对于个体化诊疗的实施具有很好的指导作用。优选的,本申请的菊粉的结构为果糖单元间以经β-2,1糖苷键脱水聚合物组成,在果糖残基末端连有一个葡萄糖残基的直链结构多糖,其果聚糖聚合度值为2~60。优选的,菊粉的果聚糖聚合度值为2~9的低聚合物和果聚糖聚合度值为10~60的高聚合物,两者的比值为1:1。需要说明的是,菊粉本身是一种不同聚合度的多糖的混合物,其中,低聚合物和高聚合物两者的比值为1:1,该比例只是一个大概的比值;可以理解,其要表达的意思是低聚合物和高聚合物两者的含量大约是各占一半。因此,在实际情况中,例如,以菊苣根为原料提取的菊粉中,低聚合物和高聚合物两者的比例并非准确的1:1,只要两者大概各占总量的一半即可,在此不作具体限定。优选的,菊粉为以菊苣根为原料,去除蛋白质和矿物质后获得的固体物质,其中,果聚糖聚合度值为2~60的菊粉直链结构的果聚糖的含量在90%以上,其它单糖和双糖含量小于10%。本申请的另一方面公开了菊粉作为制备针对普氏菌属肠型高尿酸血症的降尿酸药物、食品、保健品或食品添加剂的应用。可以理解,本申请创造性的发现并证实菊粉对于普氏菌属肠型高尿酸血症有极好的治疗效果,当然可以将菊粉制成相应的针对普氏菌属肠型高尿酸血症的降尿酸药物、食品、保健品或食品添加剂。本申请的再一方面公开了一种用于防治普氏菌属肠型高尿酸血症的组合物,组合物中含有菊粉作为有效活性成分,其中,菊粉的结构为果糖单元间以经β-2,1糖苷键脱水聚合物组成,在果糖残基末端连有一个葡萄糖残基的直链结构多糖,其果聚糖聚合度值为2~60,并且,菊粉有效成分中,果聚糖聚合度值为2~9的低聚合物和果聚糖聚合度值为10~60的高聚合物,两者的比值为1:1。需要说明的是,本申请创造性的发现并证实菊粉对于普氏菌属肠型高尿酸血症有极好的治疗效果,基于该研究和认识,本申请创造性的提出了一种特别针对普氏菌属肠型高尿酸血症的组合物,该组合物中含有菊粉,尤其适用于治疗或预防普氏菌属肠型高尿酸血症。优选的,本申请含有菊粉的组合物为药物、食品、保健品或食品添加剂。可以理解,本申请的组合物根据其中菊粉的含量或者其它有效活性成份的含量,可以将组合物制成药物、食品、保健品或食品添加剂。将其作为食品、保健品或食品添加剂时,可以起到针对普氏菌属肠型高尿酸血症的预防、保健作用。优选的,本申请含有菊粉的组合物中还含有药学上或食品上可接受的载体或辅料。优选的,药学上或食品上可接受的载体或辅料选自葡萄糖、乳糖、蔗糖、淀粉、甘露醇、糊精、脂肪酸甘油酯、聚乙二醇、羟乙基淀粉、乙二醇、聚氧乙烯山梨糖醇酐脂肪酸酯、氨基酸、明胶、白蛋白、水和生理食盐水中的至少一种。需要说明的是,本申请的组合物可以是任意剂型,而根据不同剂型也可以添加不同的药学上或食品上可接受的载体或辅料,在此不做具体限定。本申请的再一面公开了菊粉作为制备防治普氏菌属肠型高尿酸血症引起的相关疾病的药物、食品、保健品或食品添加剂的应用。需要说明的是,本申请创造性的发现并证实菊粉对于普氏菌属肠型高尿酸血症有极好的治疗效果;可以理解,在普氏菌属肠型高尿酸血症得以治疗的情况下,由其引起的相关疾病同样可以得到相应的治疗或预防;因此,本申请的菊粉或菊粉组合物同样可以用于制备防治普氏菌属肠型高尿酸血症引起的相关疾病的药物、食品、保健品或食品添加剂。需要说明的是,本申请的菊粉或含菊粉的组合物中的菊粉有效成分,其结构均为果糖单元间以经β-2,1糖苷键脱水聚合物组成,在果糖残基末端连有一个葡萄糖残基的直链结构多糖,其果聚糖聚合度值为2~60,并且,果聚糖聚合度值为2~9的低聚合物和果聚糖聚合度值为10~60的高聚合物,两者的比值约为1:1。本申请的菊粉或菊粉组合物中的菊粉有效成分,都可以是提取自菊苣根的菊粉材料,并且,所提取的菊粉材料中果聚糖聚合度值为2~60的菊粉直链结构的果聚糖的含量在90%以上,其它单糖和双糖含量小于10%。本申请的一方面公开了圆苞车前子壳作为制备防治拟杆菌属肠型高尿酸血症的药物、食品、保健品或食品添加剂的应用。需要说明的是,本申请创造性的发现并证实圆苞车前子壳对于拟杆菌属肠型高尿酸血症有极好的治疗效果,这对于个体化诊疗的实施具有很好的指导作用。本申请的再一方面公开了圆苞车前子壳作为制备针对拟杆菌属肠型高尿酸血症的降尿酸药物、食品、保健品或食品添加剂的应用。可以理解,本申请创造性的发现并证实圆苞车前子壳对于拟杆菌属肠型高尿酸血症有极好的治疗效果,当然可以将圆苞车前子壳制成相应的针对拟杆菌属肠型高尿酸血症的降尿酸药物、食品、保健品或食品添加剂。本申请的再一面公开了一种用于防治拟杆菌属肠型高尿酸血症的圆苞车前子壳组合物,组合物中含有圆苞车前子壳作为有效活性成分。需要说明的是,本申请创造性的发现并证实圆苞车前子壳对于拟杆菌属肠型高尿酸血症有极好的治疗效果,基于该研究和认识,本申请创造性的提出了一种特别针对拟杆菌属肠型高尿酸血症的组合物,该组合物中含有圆苞车前子壳,尤其适用于治疗或预防拟杆菌属肠型高尿酸血症。优选的,本申请的圆苞车前子壳组合物为药物、食品、保健品或食品添加剂。可以理解,本申请的圆苞车前子壳组合物根据其中圆苞车前子壳的含量或者其它有效活性成份的含量,可以将组合物制成药物、食品、保健品或食品添加剂。将其作为食品、保健品或食品添加剂时,可以起到针对拟杆菌属肠型高尿酸血症的预防、保健作用。优选的,本申请的圆苞车前子壳组合物中还含有药学上或食品上可接受的载体或辅料。优选的,本申请的圆苞车前子壳组合物中,药学上或食品上可接受的载体或辅料选自葡萄糖、乳糖、蔗糖、淀粉、甘露醇、糊精、脂肪酸甘油酯、聚乙二醇、羟乙基淀粉、乙二醇、聚氧乙烯山梨糖醇酐脂肪酸酯、氨基酸、明胶、白蛋白、水和生理食盐水中的至少一种。需要说明的是,本申请的圆苞车前子壳组合物可以是任意剂型,而根据不同剂型也可以添加不同的药学上或食品上可接受的载体或辅料,在此不做具体限定。本申请的再一面公开了圆苞车前子壳作为制备防治拟杆菌属肠型高尿酸血症引起的相关疾病的药物、食品、保健品或食品添加剂的应用。需要说明的是,本申请创造性的发现并证实圆苞车前子壳对于拟杆菌属肠型高尿酸血症有极好的治疗效果;可以理解,在拟杆菌属肠型高尿酸血症得以治疗的情况下,由其引起的相关疾病同样可以得到相应的治疗或预防;因此,本申请的圆苞车前子壳或圆苞车前子壳组合物同样可以用于制备防治拟杆菌属肠型高尿酸血症引起的相关疾病的药物、食品、保健品或食品添加剂。本申请的有益效果在于:本申请为菊粉和圆苞车前子壳两种植物性多聚糖提供了一种新的用途,即用于治疗或预防肠型相关的高尿酸血症,尤其是普氏菌属肠型高尿酸血症和拟杆菌属肠型高尿酸血症,该新用途的发现不仅对个体化诊疗的实施具有很好的指导作用,而且对于植物性多聚糖的临床应用和深入研究具有重要意义。本申请创造性的发现并证实了菊粉能够针对普氏菌属肠型高尿酸血症具有特异性的治疗或预防效果,该新用途的发现不仅对个体化诊疗的实施具有很好的指导作用,而且对于菊粉的临床应用和深入研究具有重要意义。本申请创造性的发现并证实了圆苞车前子壳能够针对拟杆菌属肠型高尿酸血症具有特异性的治疗或预防效果,该新用途的发现不仅对个体化诊疗的实施具有很好的指导作用,而且对于圆苞车前子壳的临床应用和深入研究具有重要意义。附图说明图1是本申请实施例一中采用菊粉对不同肠型的高尿酸血症进行干预两个月的血尿酸变化的对比图;图2是本申请实施例一中采用菊粉对不同肠型的高尿酸血症进行干预五个月的血尿酸变化的对比图;图3是本申请实施例二中采用菊粉对不同肠型的高尿酸血症进行干预五周的血尿酸变化的对比图;图4是本申请实施例三中采用圆苞车前子壳对不同肠型的高尿酸血症进行干预五周的血尿酸变化的对比图。具体实施方式植物性多聚糖是一大类物质,其在高尿酸血症方面的研究相对较少;目前,用于治疗或预防高尿酸血症的植物性多聚糖主要是菊粉,圆苞车前子壳未见相关研究和报道。现有技术中虽然已经有将菊粉用于治疗或预防高尿酸血症的研究和报道,但是,实际临床应用发现,菊粉对不同的高尿酸血症患者时而有效、时而无效或者效果不佳,这对于菊粉的临床应用具有很大的影响。本申请在对菊粉治疗高尿酸血症进行深入的研究时,创造性的发现,菊粉能够特异性的对普氏菌属肠型高尿酸血症具有很好的治疗或预防效果,而对其他肠型的高尿酸血症则不敏感,基于该研究发现,本申请提出了菊粉的一种新用途,即菊粉作为制备防治普氏菌属肠型高尿酸血症的药物、食品、保健品或食品添加剂的应用。与此同时,本申请创造性的发现,圆苞车前子壳能够特异性的对拟杆菌属肠型高尿酸血症具有很好的治疗或预防效果,而对其他肠型的高尿酸血症则不敏感,基于该研究发现,本申请提出了圆苞车前子壳的一种新用途,即圆苞车前子壳作为制备防治拟杆菌属肠型高尿酸血症的药物、食品、保健品或食品添加剂的应用。基于以上研究和认识,本申请进一步的提出了菊粉和圆苞车前子壳两种植物性多聚糖作为制备肠型相关的高尿酸血症药物、食品、保健品或食品添加剂的应用;其中,菊粉和圆苞车前子壳可以一起使用,也可以单独使用。下面通过具体实施例对本申请作进一步详细说明。以下实施例仅对本申请进行进一步说明,不应理解为对本申请的限制。实施例一本例研究了菊粉对不同肠型人群的干预效果,详细如下:1.样本收集本试验开展了为期5个月的菊粉干预计划,共入组中国人25例,其中男性14例、女性11例,本试验的受试者多数为高尿酸血症患者,高尿酸血症患者的判断标准为,高尿酸血症患者空腹血尿酸值:男性>420μmol/l,女性>360μmol/l。本试验所有受试者都为未发生痛风者,同时,需要剔除以下几类受试者:1)孕妇、乳母;2)近3个月内服用/注射过抗生素、类固醇激素、降尿酸药物、益生菌、益生元等;3)患有严重胃肠道疾病,包括结直肠癌、ibs、ibd、慢性或急性腹泻、长期便秘患者等;4)一年内接收胃肠道手术及腹部手术治疗患者,如胆囊切除术等;5)严重心脏肝脏及肾脏功能异常患者、精神类疾病患者,传染类疾病患者,肿瘤患者,严重贫血患者、严重自免疫型疾病合并患者,如类风湿性关节炎、红斑狼疮等;6)3个月内已参与其他相关干预活动;7)其他研究者评估不适宜参与项目者。所有受试者均按2次/天、每次10g(即1袋)服用统一的菊粉,共服用5个月。将受试者分成若干小组,管理员与参与者密切联系,并监督和激励受试者完成。本试验所有受试者都严格按照要求进行菊粉干预。本试验的菊粉购自维乐夫集团:丰宁平安高科实业有限公司;产品批号:26041801402。样本采集方式:在干预开始前(即基线或0月)、2个月干预时(即中期干预)、干预结束后(即5个月)分别采取空腹血进行尿酸和其他肝肾功能的检测,并同时发放粪便采样套装,要求其1周内自采样粪便并交回。使用粪便采样套装取样,在室温下可保证微生物的稳定性长达7天。粪便样本被送往实验室,在取样7天内-80度冷冻保存。2.微生物dna提取和测序取粪便样本解冻,选用试剂盒qiaampdnaminikit(qiagen),并参照生产厂商提供的说明书进行dna提取。本试验的dna提取和测序参考qin,j.etal.ametagenome-wideassociationstudyofgutmicrobiotaintype2diabetes.nature490,55–60(2012).。采用试剂盒提取dna后,取500ng提取好的dna用于建库,方法如下:首先用covarise220超声将dna打断成300-700bp左右的片段。没有剪断的dna用axygentmaxypreptmmagpcrclean-upkit试剂盒进行纯化处理。然后往每份样品中加入等量的磁珠,并用45微升的te缓冲液进行洗脱。dna的末端修饰和a尾加工则使用2:2:1混合的t4dna聚合酶(enzymaticstmp708-1500)、t4多核酸激酶(enzymaticstmy904-1500)和rtaqdna聚合酶(takaratmr500z)。取20ng纯化后的dna75℃下将酶灭活,并于23℃使用t4dna连接酶(enzymaticstml603-hc-1500)将barcode条码ad1532b与dna片段相连,然后进行pcr扩增。取55ng纯化后的pcr扩增产物在95℃下变性,并在37℃使用t4dna连接酶(enzymaticstml603-hc-1500)产生单链环状dna文库。每8个等量的barcode条码制成dna纳米球(缩写dnb),每个dnb加载到一个泳道准备测序。然后根据制造商提供的说明书,在测序平台bgiseq-500按pe150模式进行高通量测序。以上dna测序过程参考fangc,zhongh,liny,etal.assessmentofthecpas-basedbgiseq-500platformformetagenomicsequencing[j].gigascience,2017,7(3):gix133.。结果显示,本试验平均每个样本获得3.58gb的原始数据,平均每个样本71,633,404reads,基于累计准确率(overallaccuracy,oa)的方法,以oafragment≥0.8为阈值,过滤去除接头序列污染序列、去低质量序列和去人基因组污染序列后获得高质量宏基因组测序数据用于后续分析。具体试验过程参考qin,junjie,etal."ametagenome-wideassociationstudyofgutmicrobiotaintype2diabetes."nature490.7418(2012):55.。3.物种分类鉴别将过滤后高质量测序序列通过soap2.22软件进行比对分析。基于相似度(identity)≥0.9的阈值与hg19比对以删除人源序列,将所得到的干净序列以相似度≥0.95的阈值再比对到人肠道微生物完整基因集(icg)上。比对结果显示,比对到包含9,879,896个基因的人肠道微生物完整基因集(icg)。将比对的上述基因集的基因及其物种注释信息,构建本试验宏基因组样本的基因、物种相对丰度谱。soap2软件比对分析参考li,ruiqiang,etal."soap2:animprovedultrafasttoolforshortreadalignment."bioinformatics25.15(2009):1966-1967.。4.肠型和趋势分析为了得到肠型分类,对人群基于菌群结构分层,本试验参考arumugam,manimozhiyan,etal."enterotypesofthehumangutmicrobiome."nature473.7346(2011):174.。本试验选取了2303例健康人的宏基因组数据作为数据集,基于“3.物种分类鉴别”的物种分类结果和物种的属水平的相对丰度信息,采用jensen-shannondistance(jsd)和partitioningaroundmedoids(pam)进行聚类分析,并使用calinskiharabasz(ch)评估最佳的聚类数,构建出分类模型。该模型在二分类时达到最佳分类效果,因此将肠道分为两类:一类是以拟杆菌(bacteroides)为优势物种,另一类则是以普氏菌(prevotella)为优势物种。然后基于该模型对本试验的所有样本进行肠道微生物肠型分类,并研究不同肠型人群对菊粉干预的响应程度,及在不同肠型分组下菊粉干预对尿酸的调节作用。本试验的受试者按肠型结果分成bacteroides,prevotella两组,即拟杆菌属(bacteroides)肠型(以下简称b肠型)和普氏菌属(prevotella)肠型(以下简称p肠型),如表1所示。采用配对的秩和检验,对比基线和干预2个月,以及基线和干预5个月后的血尿酸的变化趋势,结果如表2、表3以及图1和图2所示。表1不同肠型基本信息的组间对比b肠型组p肠型组秩和检验(平均值±标准差)(平均值±标准差)p值样本数(n)1411-性别(%男)53.8%60%0.78256年龄(y)30.14±5.7129.09±2.950.95603身高(cm)166.32±8.97164.54±8.530.58378体重(kg)71.94±20.2768.53±8.30.59812表2基线分别和干预2个月、5个月后的血尿酸变化的对比b肠型组p肠型组中位数(25%,75%)中位数(25%,75%)基线(干预0个月)尿酸(μmol/l)381.5(291.5,431)409.0(314.5,436.0)干预2个月的尿酸(μmol/l)296.0(374.5,434.0)330.0(297.0,386.0)干预5个月的尿酸(μmol/l)333.0(304.5,419.5)346.0(324.0,408.0)p值(基线vs2个月)0.640.0051p值(基线vs5个月)0.820.038表3菊粉干预前后,即基线、干预2个月、干预5个月的尿酸水平表1至表3中,b表示bacteroides,p表示prevotella。表3中的编号为样本编号,尿酸单位为μmol/l。图1是采用菊粉对受试者干预两个月后相当于基线(即干预0个月)的血尿酸变化对比图,图2是采用菊粉对受试者干预五个月后相当于基线(即干预0个月)的血尿酸变化对比图。图1和图2中,基线是采用菊粉干预前即干预0个月的血尿酸,b表示拟杆菌(bacteroides)肠型高尿酸血症,p表示普氏菌属(prevotella)肠型高尿酸血症。从表2、表3、图1和图2的结果可以看出,两种肠型的人群在年龄、性别、身高和体重间无统计学差异。分别干预2个月和5个月,p肠型人群的血尿酸水平均显著性下降,p=0.0051和p=0.038;而b肠型的人群血尿酸的水平干预前后均无统计学差异,p=0.64和p=0.82;以上结果说明,服用菊粉对p肠型人群存在明显的降尿酸效果,而对b肠型人群的尿酸干预并不明显。实施例二为了进一步验证实施例一的结果,本试验扩大样本量,重新招募另一批高尿酸血症的患者60例,开展为期35天的菊粉干预试验,以确定不同肠型的干预效果。受试者的纳入标准为:高尿酸血症人群,空腹血尿酸值:男性>420μmol/l,女性>360μmol/l。同样的,排除以下几种情况的受试者:1)孕妇、乳母;2)近3个月内服用/注射过抗生素、类固醇激素、降尿酸药物、益生菌、益生元等;3)患有严重胃肠道疾病,包括结直肠癌、ibs、ibd、慢性或急性腹泻、长期便秘患者等;4)一年内接收胃肠道手术及腹部手术治疗患者,如胆囊切除术等;5)严重心脏肝脏及肾脏功能异常患者、精神类疾病患者,传染类疾病患者,肿瘤患者,严重贫血患者、严重自免疫型疾病合并患者(如类风湿性关节炎、红斑狼疮等)等;6)3个月内已参与其他相关干预活动;7)其他研究者评估不适宜参与项目者。干预物:菊粉,本试验采用的菊粉与实施例一相同。干预方式和时长:温水冲服,2次/天,每次10g/1袋,餐前服用,持续服用35天。干预流程和志愿者管理:1)所有纳入人员均在干预开始前签署知情同意书;2)分别在干预开始前(即0天)和结束时(即35天)由有资质的护士采集全血样本10ml;3)分别在干预开始前(0天)和结束时(35天)进行人体测量学检测;4)分别在干预开始前(0天)、三周(21天)和结束时(35天)向志愿者发放粪便采样套装,由志愿者在一周内完成自采样粪便样本各1份并交回;5)干预期间,志愿者保持正常生活习惯;6)干预期间不服用其他的药物或保健品,如确实因健康原因需要服用,应及时告知项目组;7)如志愿者的日常生活方式因故必须进行改变,如长期出差、长期加班、患病治疗等,应及时告知项目组。检测指标:1)人体测量学指标:身高、体重、血压;2)血液检测:血常规、血生化,包括空腹血糖、血脂四项、肝功两项、肾功三项;3)肠道微生物检测。参照实施例一的研究方法,对样本进行微生物dna提取和测序、物种分类鉴别、肠型和趋势分析。结果如图3所示,图中,纵坐标为尿酸水平,单位为微摩尔/升;横坐标为菊粉干预时间,单位为周数;上部分“bacteroides”表示拟杆菌属肠型高尿酸血症的结果,下部分“prevotella”表示普氏菌属肠型高尿酸血症的结果;图3展示了菊粉干预0周和5周(即35天)两种肠型高尿酸血症的结果。图3的结果显示,经过为期35天的菊粉干预,高尿酸血症人群中的p肠型人群的血尿酸水平显著性下降,b肠型的人群血尿酸的水平干预前后无统计学差异(p=0.93)。该结果说明,服用菊粉对p肠型的高尿酸血症人群存在明显的降尿酸效果(p=0.033),而对b肠型的高尿酸血症人群的尿酸干预并不明显。实施例三本例研究了圆苞车前子壳对不同肠型人群的干预效果,详细如下:1.样本收集本试验招募一批高尿酸血症的患者28例,开展为期35天的圆苞车前子壳干预试验,以确定圆苞车前子壳对不同肠型的干预效果。本试验的受试者均为高尿酸血症患者,高尿酸血症患者的判断标准为,高尿酸血症患者空腹血尿酸值:男性>420μmol/l,女性>360μmol/l。本试验所有受试者都为未发生痛风者,同时,需要剔除以下几类受试者:1)孕妇、乳母;2)近3个月内服用/注射过抗生素、类固醇激素、降尿酸药物、益生菌、益生元等;3)患有严重胃肠道疾病,包括结直肠癌、ibs、ibd、慢性或急性腹泻、长期便秘患者等;4)一年内接收胃肠道手术及腹部手术治疗患者,如胆囊切除术等;5)严重心脏肝脏及肾脏功能异常患者、精神类疾病患者,传染类疾病患者,肿瘤患者,严重贫血患者、严重自免疫型疾病合并患者,如类风湿性关节炎、红斑狼疮等;6)3个月内已参与其他相关干预活动;7)其他研究者评估不适宜参与项目者。干预物:圆苞车前子壳粉末。干预方式和时长:温水冲服,2次/天,每次4g/1袋,餐前服用,持续服用35天。将受试者分成若干小组,管理员与参与者密切联系,并监督和激励受试者完成。本试验所有受试者都严格按照要求进行圆苞车前子壳干预。干预流程和志愿者管理:1)所有纳入人员均在干预开始前签署知情同意书;2)分别在干预开始前(即0天)和结束时(即35天)由有资质的护士采集全血样本10ml;3)分别在干预开始前(0天)和结束时(35天)进行人体测量学检测;4)分别在干预开始前(0天)、三周(21天)和结束时(35天)向志愿者发放粪便采样套装,由志愿者在一周内完成自采样粪便样本各1份并交回;5)干预期间,志愿者保持正常生活习惯;6)干预期间不服用其他的药物或保健品,如确实因健康原因需要服用,应及时告知项目组;7)如志愿者的日常生活方式因故必须进行改变,如长期出差、长期加班、患病治疗等,应及时告知项目组。检测指标:1)人体测量学指标:身高、体重、血压;2)血液检测:血常规、血生化,包括空腹血糖、血脂四项、肝功两项、肾功三项;3)肠道微生物检测。样本采集方式:在干预开始前(即基线或0天)、干预结束后(即35天)分别采取空腹血进行尿酸和其他肝肾功能的检测,并同时发放粪便采样套装,要求其1周内自采样粪便并交回。使用粪便采样套装取样,在室温下可保证微生物的稳定性长达7天。粪便样本被送往实验室,在取样7天内-80度冷冻保存。2.微生物dna提取和测序取粪便样本解冻,选用试剂盒qiaampdnaminikit(qiagen),并参照生产厂商提供的说明书进行dna提取。本试验的dna提取和测序参考qin,j.etal.ametagenome-wideassociationstudyofgutmicrobiotaintype2diabetes.nature490,55–60(2012).。采用试剂盒提取dna后,取500ng提取好的dna用于建库,方法如下:首先用covarise220超声将dna打断成300-700bp左右的片段。没有剪断的dna用axygentmaxypreptmmagpcrclean-upkit试剂盒进行纯化处理。然后往每份样品中加入等量的磁珠,并用45微升的te缓冲液进行洗脱。dna的末端修饰和a尾加工则使用2:2:1混合的t4dna聚合酶(enzymaticstmp708-1500)、t4多核酸激酶(enzymaticstmy904-1500)和rtaqdna聚合酶(takaratmr500z)。取20ng纯化后的dna75℃下将酶灭活,并于23℃使用t4dna连接酶(enzymaticstml603-hc-1500)将barcode条码ad1532b与dna片段相连,然后进行pcr扩增。取55ng纯化后的pcr扩增产物在95℃下变性,并在37℃使用t4dna连接酶(enzymaticstml603-hc-1500)产生单链环状dna文库。每8个等量的barcode条码制成dna纳米球(缩写dnb),每个dnb加载到一个泳道准备测序。然后根据制造商提供的说明书,在测序平台bgiseq-500按pe150模式进行高通量测序。以上dna测序过程参考fangc,zhongh,liny,etal.assessmentofthecpas-basedbgiseq-500platformformetagenomicsequencing[j].gigascience,2017,7(3):gix133.。结果显示,本试验平均每个样本获得3.49gb的原始数据,平均每个样本71,713,006reads,基于累计准确率(overallaccuracy,oa)的方法,以oafragment≥0.8为阈值,过滤去除接头序列污染序列、去低质量序列和去人基因组污染序列后获得高质量宏基因组测序数据用于后续分析。具体试验过程参考qin,junjie,etal."ametagenome-wideassociationstudyofgutmicrobiotaintype2diabetes."nature490.7418(2012):55.。3.物种分类鉴别将过滤后高质量测序序列通过soap2.22软件进行比对分析。基于相似度(identity)≥0.9的阈值与hg19比对以删除人源序列,将所得到的干净序列以相似度≥0.95的阈值再比对到人肠道微生物完整基因集(icg)上。比对结果显示,比对到包含9,907,153个基因的人肠道微生物完整基因集(icg)。将比对的上述基因集的基因及其物种注释信息,构建本试验宏基因组样本的基因、物种相对丰度谱。soap2软件比对分析参考li,ruiqiang,etal."soap2:animprovedultrafasttoolforshortreadalignment."bioinformatics25.15(2009):1966-1967.。4.肠型和趋势分析为了得到肠型分类,对人群基于菌群结构分层,本试验参考arumugam,manimozhiyan,etal."enterotypesofthehumangutmicrobiome."nature473.7346(2011):174.。本试验选取了2303例健康人的宏基因组数据作为数据集,基于“3.物种分类鉴别”的物种分类结果和物种的属水平的相对丰度信息,采用jensen-shannondistance(jsd)和partitioningaroundmedoids(pam)进行聚类分析,并使用calinskiharabasz(ch)评估最佳的聚类数,构建出分类模型。该模型在二分类时达到最佳分类效果,因此将肠道分为两类:一类是以拟杆菌(bacteroides)为优势物种,另一类则是以普氏菌(prevotella)为优势物种。然后基于该模型对本试验的所有样本进行肠道微生物肠型分类,并研究不同肠型人群对菊粉干预的响应程度,及在不同肠型分组下菊粉干预对尿酸的调节作用。本试验的受试者按肠型结果分成bacteroides,prevotella两组,即拟杆菌属(bacteroides)肠型(以下简称b肠型)和普氏菌属(prevotella)肠型(以下简称p肠型);分型结果显示,本试验的28例高尿酸血症患者中,拟杆菌属肠型高尿酸血症占18例,普氏菌属肠型高尿酸血症10例。采用配对的秩和检验,对比基线和干预35天后的血尿酸的变化趋势,结果如图4所示。图4的纵坐标为尿酸水平,单位为微摩尔/升;横坐标为圆苞车前子壳干预时间,单位为周;左部分“b”表示拟杆菌属肠型高尿酸血症的结果,右部分“p”表示普氏菌属肠型高尿酸血症的结果;图4展示了圆苞车前子壳干预0周和5周(即35天)两种肠型高尿酸血症的结果。图4的结果显示,经过为期35天的圆苞车前子壳干预,高尿酸血症人群中的b(拟杆菌属,bacteroides)肠型人群的血尿酸水平显著性下降(p=0.0079),p(普氏菌属,prevotella)肠型的人群血尿酸的水平干预前后无统计学差异(p=0.61)。该结果说明,服用圆苞车前子壳对b肠型的高尿酸血症人群存在明显的降尿酸效果,而对p肠型的高尿酸血症人群的尿酸干预并不明显。以上内容是结合具体的实施方式对本申请所作的进一步详细说明,不能认定本申请的具体实施只局限于这些说明。对于本申请所属
技术领域:
的普通技术人员来说,在不脱离本申请构思的前提下,还可以做出若干简单推演或替换。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1