可强肾健体的海参肠提取物益生菌饮品的制作方法
1.本发明属于发酵型功能饮料加工领域,尤其是一种可强肾健体的海参肠提取物益生菌饮品。
背景技术:
2.随着现代生活节奏的加快及生活环境的影响,患有慢性疲劳综合征等亚健康疾病人群不断扩大,预防和对症机体健康的调整已经成为解决亚健康问题的共识。中医认为肾主藏经,关系人的生长、发育、生殖等多种生理活动,肾气的盛衰决定人的健康状态。为此,强肾是改善人们亚健康状态的一种有效手段。海参是一种有益于身体健康的食品,在中药中占有重要地位。《本草纲目拾遗》中记载:“海参性温补,足敌人参,故名海参”,“补肾经、益精髓、消痿涎,摄小便,壮阳,生百脉”。研究表明,海参肠比海参体壁含有更多的活性物质,如刺参皂苷、锌、硒、钒等成分。但是,迄今为止并没有充分利用海参肠中的有效成分,辅以其他药食同源的植物进行配伍,制备显著提高强肾健体效果的海参肠提取物益生菌饮品的相关报道。
技术实现要素:
3.本发明是为了解决现有技术所存在的上述技术问题,提供一种可强肾健体的海参肠提取物益生菌饮品。
4.本发明的技术解决方案是:一种可强肾健体的海参肠提取物益生菌饮品,其特征在于按照如下方法制备:a. 将新鲜的海参肠匀浆,加入海参肠质量10~15倍的磷酸盐缓冲液,4℃下静置过夜,得海参肠自溶酶解液,所述磷酸盐缓冲液的浓度为0.1mol/l, ph6.3;b. 在海参肠自溶酶解液中接种酿酒酵母、干酪乳杆菌在在30~37℃密封静置发酵24~72h,所述酿酒酵母、干酪乳杆菌、海参肠自溶酶解液的质量比为0.5:0.5:100,所述酿酒酵母≥1
×
106cfu/g,干酪乳杆菌≥1
×
106cfu/g,固液分离得第一次海参肠发酵原汁,将第一次海参肠发酵原汁冷冻干燥得海参肠提取物冻干粉a;c. 在海参肽冻干粉a中加入纯水,制成质量浓度为40%的底物,接种酿酒酵母、干酪乳杆菌在30~37℃密封静置发酵24~72h,所述酿酒酵母、干酪乳杆菌、底物的质量比为0.5:0.5:100,酿酒酵母≥1
×
106cfu/g,干酪乳杆菌≥1
×
106cfu/g,固液分离得第二次海参肠发酵原汁,将第二次海参肠发酵原汁冷冻干燥得海参肠提取物冻干粉b;d. 将海参海参肠提取物冻干粉b、蓝莓干粉、覆盆子干粉及桑葚干粉加水制成混合培养液,各组分的质量百分比为海参肠提取物冻干粉b 0.1~5%、蓝莓干粉0.1~10%、覆盆子干粉0.1~10%、桑葚干粉0.1~10%,再加入混合培养液质量2~6%的益生菌粉在30~37℃密封静置发酵24~72h,所述益生菌粉是由保加利亚乳酸菌、青春双歧杆菌、干酪乳杆菌、嗜酸乳杆菌等质量组成,所述保加利亚乳酸菌≥1
×
106cfu/g、青春双歧杆菌≥1
×
106cfu/g、干酪乳杆菌≥1
×
106cfu/g、嗜酸乳杆菌≥1
×
106cfu/g;
e. 将发酵液转移到后储罐中进行发酵后熟,发酵至ph为3.10~4.00,总酸达到5~7g/l,得海参肠提取物益生菌饮品。
5.本发明是以海参肠为原料,首先制备成海参肠自溶酶解液,再通过二次发酵方法制备成富含海参肽、皂苷、锌、硒、钒的海参肠提取物,与蓝莓干粉、覆盆子干粉、桑葚干粉及益生菌发酵制备成饮品,各组分相互作用,可显著增强强肾健体效果,从而有效改善人们的亚健康状态。
具体实施方式
6.实施例1本发明的一种可强肾健体的海参肠提取物益生菌饮品,按照如下方法制备:a. 将新鲜的海参肠匀浆,加入海参肠质量12倍的磷酸盐缓冲液,4℃下静置过夜,得海参肠自溶酶解液,所述磷酸盐缓冲液的浓度为0.1mol/l,ph6.3;b. 在海参肠自溶酶解液中接种酿酒酵母、干酪乳杆菌在35℃密封静置发酵50h,所述酿酒酵母、干酪乳杆菌、海参肠自溶酶解液的质量比为0.5:0.5:100,所述酿酒酵母≥1
×
106cfu/g,干酪乳杆菌≥1
×
106cfu/g,固液分离得第一次海参肠发酵原汁,将第一次海参肠发酵原汁冷冻干燥得海参肠提取物冻干粉a;c. 在海参肽冻干粉a中加入纯水,制成质量浓度为40%的底物,接种酿酒酵母、干酪乳杆菌在35℃密封静置发酵50h,酿酒酵母、干酪乳杆菌、海参肠自溶酶解液的质量比为0.5:0.5:100,酿酒酵母≥1
×
106cfu/g,干酪乳杆菌≥1
×
106cfu/g,固液分离得第二次海参肠发酵原汁,将第二次海参肠发酵原汁冷冻干燥得海参肠提取物冻干粉b;d. 将海参海参肠提取物冻干粉b、蓝莓干粉、覆盆子干粉及桑葚干粉加水制成混合培养液,各组分的质量百分比为海参肠提取物冻干粉b 3%、蓝莓干粉5%、覆盆子干粉5%、桑葚干粉5%,再加入混合培养液质量4%的益生菌粉在32℃密封静置发酵50h,所述益生菌粉是由保加利亚乳酸菌、青春双歧杆菌、干酪乳杆菌、嗜酸乳杆菌等质量组成,所述保加利亚乳酸菌≥1
×
106cfu/g、青春双歧杆菌≥1
×
106cfu/g、干酪乳杆菌≥1
×
106cfu/g、嗜酸乳杆菌≥1
×
106cfu/g;e. 将发酵液转移到后储罐中进行发酵后熟,发酵至ph为3.6,总酸达到6g/l,得海参肠提取物益生菌饮品。
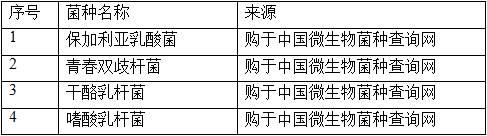
7.所用原料均为外购商品,其中酿酒酵母购于安琪公司,益生菌粉来源如表1所示。
8.表1实施例2:本发明的可强肾健体的海参肠提取物益生菌饮品,按照如下方法制备:a. 将新鲜的海参肠匀浆,加入海参肠质量10倍的磷酸盐缓冲液,4℃下静置过夜,
得海参肠自溶酶解液,所述磷酸盐缓冲液的浓度为0.1mol/l,ph6.3;b. 在海参肠自溶酶解液中接种酿酒酵母、干酪乳杆菌在30℃密封静置发酵72h,所述酿酒酵母、干酪乳杆菌、海参肠自溶酶解液的质量比为0.5:0.5:100,所述酿酒酵母≥1
×
106cfu/g,干酪乳杆菌≥1
×
106cfu/g,固液分离得第一次海参肠发酵原汁,将第一次海参肠发酵原汁冷冻干燥得海参肠提取物冻干粉a;c. 在海参肽冻干粉a中加入纯水,制成质量浓度为40%的底物,接种酿酒酵母、干酪乳杆菌在30℃密封静置发酵72h,所述酿酒酵母、干酪乳杆菌、海参肠自溶酶解液的质量比为0.5:0.5:100,酿酒酵母≥1
×
106cfu/g,干酪乳杆菌≥1
×
106cfu/g,固液分离得第二次海参肠发酵原汁,将第二次海参肠发酵原汁冷冻干燥得海参肠提取物冻干粉b;d. 将海参海参肠提取物冻干粉b、蓝莓干粉、覆盆子干粉及桑葚干粉加水制成混合培养液,各组分的质量百分比为海参肠提取物冻干粉b 0.1%、蓝莓干粉0.1%、覆盆子干粉0.1%、桑葚干粉0.1%,再加入混合培养液质量2%的益生菌粉在30℃密封静置发酵72h,所述益生菌粉是由保加利亚乳酸菌、青春双歧杆菌、干酪乳杆菌、嗜酸乳杆菌等质量组成,所述保加利亚乳酸菌≥1
×
106cfu/g、青春双歧杆菌≥1
×
106cfu/g、干酪乳杆菌≥1
×
106cfu/g、嗜酸乳杆菌≥1
×
106cfu/g;e. 将发酵液转移到后储罐中进行发酵后熟,发酵至ph为3.10,总酸达到7g/l,得海参肠提取物益生菌饮品。
9.原料来源同实施例1。
10.实施例3:本发明的可强肾健体的海参肠提取物益生菌饮品,按照如下方法制备:a. 将新鲜的海参肠匀浆,加入海参肠质量15倍的磷酸盐缓冲液,4℃下静置过夜,得海参肠自溶酶解液,所述磷酸盐缓冲液的浓度为0.1mol/l, ph6.3;b. 在海参肠自溶酶解液中接种酿酒酵母、干酪乳杆菌在37℃密封静置发酵24h,酿酒酵母、干酪乳杆菌、海参肠自溶酶解液的质量比为0.5:0.5:100,所述酿酒酵母≥1
×
106cfu/g,干酪乳杆菌≥1
×
106cfu/g,固液分离得第一次海参肠发酵原汁,将第一次海参肠发酵原汁冷冻干燥得海参肠提取物冻干粉a;c. 在海参肽冻干粉a中加入纯水,制成质量浓度为40%的底物,接种酿酒酵母、干酪乳杆菌在37℃密封静置发酵24h,酿酒酵母、干酪乳杆菌、海参肠自溶酶解液的质量比为0.5:0.5:100,酿酒酵母≥1
×
106cfu/g,干酪乳杆菌≥1
×
106cfu/g,固液分离得第二次海参肠发酵原汁,将第二次海参肠发酵原汁冷冻干燥得海参肠提取物冻干粉b;d. 将海参海参肠提取物冻干粉b、蓝莓干粉、覆盆子干粉及桑葚干粉加水制成混合培养液,各组分的质量百分比为海参肠提取物冻干粉b 5%、蓝莓干粉10%、覆盆子干粉10%、桑葚干粉10%,再加入混合培养液质量6%的益生菌粉在37℃密封静置发酵24h,所述益生菌粉是由保加利亚乳酸菌、青春双歧杆菌、干酪乳杆菌、嗜酸乳杆菌等质量组成,所述保加利亚乳酸菌≥1
×
106cfu/g、青春双歧杆菌≥1
×
106cfu/g、干酪乳杆菌≥1
×
106cfu/g、嗜酸乳杆菌≥1
×
106cfu/g;e. 将发酵液转移到后储罐中进行发酵后熟,发酵至ph为4.00,总酸达到5g/l,得海参肠提取物益生菌饮品。
11.实验例1:
将本发明实施例1所得海参肠提取物益生菌饮品冻干粉与对照组进行肽、皂苷、锌、硒、钒含量测定。对照组是以粉碎后的新鲜海参肠桨冻干粉代替本发明实施例1所得海参肠提取物冻干粉b,按照本发明实施例1的步骤d、e制备出的饮品的冻干粉。按照gb/t22492
‑
2008规定的方法进行肽含量测定;按照《保健食品检验与评价技术规范》2003年版测定总皂苷含量;参照gb5009.268
‑
2016测定钒、锌、硒含量;结果如表2。
12.表2结果表明:本发明实施例1的海参肠提取物益生菌饮品冻干粉中的肽、皂苷、锌、硒、钒含量分别是对照组中的肽、皂苷、锌、硒、钒含量的1.64、1.56、1.84、1.83以及2倍,即本发明可将海参肠中的有效成分充分提取出来。
13.实验例2:取18~22g雄性icr小鼠50只,随机分成5组:空白组、阴性对照组、阳性对照组、对照组、本发明实施例1组。除空白组皮下注射生理盐水(25mg/kg
•
d)外,每组小鼠皮下注射等量(25mg/kg
•
d)的氢化可的松,连续7d构建肾阳虚小鼠模型。建模之后连续灌胃24d:空白组和阴性对照组灌胃生理盐水(25ml/kg
•
d),阳性对照组注射丙酸睾酮(5mg/kg
•
d),对照组(0.5g/kg
•
d)灌胃样品同实验例1,本发明组(0.5g/kg
•
d)灌胃本发明实施例1所得饮品的冻干粉;最后一次灌胃结束后24h,将小鼠放入水温为6
±
2℃的水箱中,记录小鼠游泳时间,以小鼠不能游动为截止时间。待小鼠游泳结束后,以颈椎脱臼处死小鼠,检测睾丸组织中睾酮水平、精囊腺中精液乳酸脱氢酶(ldh)水平及精子活动率。结果如表3所示:表3
表3中与空白组相比,极显著**(p<0.01),显著*(p<0.05);与对照组相比,极显著##(p<0.01),显著#(p<0.05)。
14.结果表明,从阳虚小鼠低温游泳时间、睾酮水平、精囊腺中精液乳酸脱氢酶(ldh)水平及精子活动率等指标看出,本发明组明显高于对照组、阴性对照组及阳性对照组,说明本发明组可显著增强强肾健体效果。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1