2-O-α-D-葡糖基-L-抗坏血酸的钾盐晶体及其制备方法与流程
2
‑
o
‑
α
‑
d
‑
葡糖基
‑
l
‑
抗坏血酸的钾盐晶体及其制备方法
技术领域
1.本发明涉及新的2
‑
o
‑
α
‑
d
‑
葡糖基
‑
l
‑
抗坏血酸的钾盐晶体及其制备方法。
背景技术:
[0002]2‑
o
‑
α
‑
d
‑
葡糖基
‑
l
‑
抗坏血酸(以下,在本说明书中简称为“抗坏血酸2
‑
葡糖苷”)是在l
‑
抗坏血酸(维生素c)分子的2位羟基上经由α
‑
糖苷键与1分子的d
‑
葡糖键合而得到的化合物。抗坏血酸2
‑
葡糖苷与l
‑
抗坏血酸不同,是非还原性的,稳定性优异,因此也称为“稳定型维生素c”。另外,抗坏血酸2
‑
葡糖苷在生物体内容易被酶水解成l
‑
抗坏血酸和d
‑
葡萄糖,发挥l
‑
抗坏血酸固有的生理活性。
[0003]
抗坏血酸2
‑
葡糖苷是通过使含有淀粉质和l
‑
抗坏血酸的溶液与环麦芽糊精
‑
葡糖基转移酶(以下,在本说明书中简称为“cgtase”)作用、再与葡糖淀粉酶作用而以工业规模制造(例如,参照专利文献1~3等)。含有高纯度的抗坏血酸2
‑
葡糖苷的无水晶体的粉末由本技术人以商品名“aa2g”(注册商标)在化妆品、医药部外品((quasi drug)准药品)领域销售,主要作为美白成分等在化妆品、医药部外品等领域广泛使用。另外,面向食品和饮料的含有抗坏血酸2
‑
葡糖苷的无水晶体的粉末同样由本技术人以商品名
“アスコフレッシュ”
(注册商标)销售(例如,参照专利文献4~7等)。
[0004]
关于抗坏血酸2
‑
葡糖苷,还报道了各种上述无水晶体以外的其他晶体形态。例如,在专利文献8中公开了抗坏血酸2
‑
葡糖苷的含水晶体。另外,在专利文献9中,作为抗坏血酸2
‑
葡糖苷的金属盐的结晶,公开了抗坏血酸2
‑
葡糖苷的铝盐的2种结晶性粉末和抗坏血酸2
‑
葡糖苷的锌盐的结晶性粉末。进而,在专利文献10中公开了抗坏血酸2
‑
葡糖苷的钠盐的含水晶体和无水晶体。但是,除此以外的抗坏血酸2
‑
葡糖苷的晶体没有被报道,如果能够提供抗坏血酸2
‑
葡糖苷或其盐的新晶体,在扩大抗坏血酸2
‑
葡糖苷在各个领域中的使用选择的意义上是非常有用的。现有技术文献
[0005]
专利文献专利文献1:日本特开平3
‑
139288号公报专利文献2:日本特开平3
‑
135992号公报专利文献3:日本特开平3
‑
183492号公报专利文献4:日本特开平4
‑
046112号公报专利文献5:日本特开平4
‑
182412号公报专利文献6:日本特开平4
‑
182413号公报专利文献7:日本特开平4
‑
182419号公报专利文献8:日本专利第5856963号专利文献9:日本专利第3290490号专利文献10:日本专利第6307444号
技术实现要素:
发明要解决的课题
[0006]
本发明的课题在于提供一种新的抗坏血酸2
‑
葡糖苷的盐的晶体及其制备方法。解决课题的手段
[0007]
本发明人等为了解决上述课题,在对抗坏血酸2
‑
葡糖苷的结晶化条件进行各种研究的过程中,发现将抗坏血酸2
‑
葡糖苷溶解在特定浓度的氢氧化钾水溶液中,添加醇静置,结果,析出结晶。将获得的该结晶供于hplc分析,结果,仅确认抗坏血酸2
‑
葡糖苷的峰,供于粉末x射线衍射法,结果显示出,与以往公知的抗坏血酸2
‑
葡糖苷的晶体不同的粉末x射线衍射图,因此判明为新的抗坏血酸2
‑
葡糖苷的晶体。进而,由于该晶体含有特定量的钾和水,因此判明是钾盐的含水晶体。而且,本发明人等明确了该新的抗坏血酸2
‑
葡糖苷的钾盐晶体的物性,同时确立了其制备方法,从而完成了本发明。
[0008]
即,本发明通过提供新的抗坏血酸2
‑
葡糖苷的钾盐晶体及其制备方法来解决上述课题。发明效果
[0009]
根据本发明,能够供给新的抗坏血酸2
‑
葡糖苷的钾盐晶体。在将本发明的抗坏血酸2
‑
葡糖苷钾盐的晶体与抗坏血酸2
‑
葡糖苷无水晶体并用而制成混合物的形态的情况下,通过适当调整两者的混合比,能够在不使用碱来中和显示强酸性的抗坏血酸2
‑
葡糖苷的情况下,将该混合物的水溶液调整至期望的ph范围,因此能够有利地用于饮食品、化妆品、医药部外品、药品、工业用品等的制造。
附图说明
[0010]
图1是在抗坏血酸2
‑
葡糖苷的氢氧化钾水溶液中添加甲醇而获得的晶体的光学显微镜照片(倍率125倍)。图2是在抗坏血酸2
‑
葡糖苷的氢氧化钾水溶液中添加甲醇而获得的晶体的粉末x射线衍射图。图3是将图2所示的晶体的粉末x射线衍射图与抗坏血酸2
‑
葡糖苷的无水晶体、含水晶体和钠盐晶体(含水晶体)的粉末x射线衍射图进行对比的图。图4是通过单晶x射线结构解析得到的抗坏血酸2
‑
葡糖苷钾盐的含水晶体的ortep图。
具体实施方式
[0011]
本发明涉及一种抗坏血酸2
‑
葡糖苷的钾盐晶体。本发明的抗坏血酸2
‑
葡糖苷的钾盐晶体只要是本发明人等独自发现的、全新的抗坏血酸2
‑
葡糖苷的盐的晶体,只要是抗坏血酸2
‑
葡糖苷钾盐的晶体,另外,只要显示出作为本说明书中公开的抗坏血酸2
‑
葡糖苷钾盐晶体的物性和特征,则不限于通过特定制备方法制备的物质。
[0012]
本发明的抗坏血酸2
‑
葡糖苷的钾盐晶体如后述的实验项所示,其特征在于,在供于使用cukα射线作为x射线源的粉末x射线衍射法得到的粉末x射线衍射图中,至少在衍射角(2θ)8.27
°
、8.81
°
、16.05
°
、18.88
°
和25.64
°
处显示出特征衍射峰。该粉末x射线衍射图与以往公知的抗坏血酸2
‑
葡糖苷的无水晶体、含水晶体、钠盐晶体的粉末x射线衍射图均不
同,因此本发明中获得的晶体是指与上述以往公知的抗坏血酸2
‑
葡糖苷的晶体不同的抗坏血酸2
‑
葡糖苷的晶体。
[0013]
另外,本发明的抗坏血酸2
‑
葡糖苷的钾盐晶体如后述的实验项中所示,在利用常规方法的卡尔
‑
费歇尔法测定时,通常显示12.5~14.8质量%的水分含量。由此可知,本发明的抗坏血酸2
‑
葡糖苷的钾盐晶体为含水晶体的形态。
[0014]
本发明的抗坏血酸2
‑
葡糖苷的钾盐晶体通过后述的实验项中的离子色谱法测定时,通常含有14.1~14.6质量%的钾。由该结果可确认,本发明的抗坏血酸2
‑
葡糖苷的晶体为钾盐晶体。
[0015]
顺便说一下,本发明人等还成功地获得了具有能够分析关于抗坏血酸2
‑
葡糖苷钾盐的含水晶体的单晶x射线晶体结构的尺寸的单晶,该单晶如后述的实验项所示,根据x射线晶体结构分析可知,该含水晶体属于斜方晶系,是空间群显示p212121、晶格常数显示、晶格常数显示的晶体。
[0016]
另外,本发明是提供新的抗坏血酸2
‑
葡糖苷的钾盐晶体的制备方法的发明。本发明的抗坏血酸2
‑
葡糖苷钾盐的含水晶体的制备方法包括:将作为原料的抗坏血酸2
‑
葡糖苷溶解于特定浓度的氢氧化钾水溶液,然后添加特定量的醇,在低温下静置,由此析出结晶,接着,使用离心分离等固液分离法回收结晶,由此能够制造抗坏血酸2
‑
葡糖苷钾盐的含水晶体。
[0017]
在抗坏血酸2
‑
葡糖苷钾盐的含水晶体的制造中,无论作为原料的抗坏血酸2
‑
葡糖苷的来源如何,都可以通过有机合成而得到,但通常适宜使用以往公知的用于饮食品和化妆品的抗坏血酸2
‑
葡糖苷的制备方法,即,使淀粉质和l
‑
抗坏血酸与cgtase作用,再与葡糖淀粉酶作用的方法而得到的含有抗坏血酸2
‑
葡糖苷的溶液或由此制备的、医药部外品(准药品)级的含有抗坏血酸2
‑
葡糖苷无水晶体的粉末(商品名“aa2g”(注册商标)、抗坏血酸2
‑
葡糖苷纯度98质量%以上,株式会社林原销售)、或食品级的含有抗坏血酸2
‑
葡糖苷无水晶体的粉末(商品名
“アスコフレッシュ”
(注册商标)、抗坏血酸2
‑
葡糖苷纯度98质量%以上,株式会社林原销售)。
[0018]
在以抗坏血酸2
‑
葡糖苷为原料制造抗坏血酸2
‑
葡糖苷的钾盐晶体的情况下,例如,相对于抗坏血酸2
‑
葡糖苷无水晶体的质量1,以液量2的比率添加并溶解浓度为4~8当量(n)的氢氧化钾水溶液,接着,以液量3以上的比率添加醇并混合,然后在低温下静置,则抗坏血酸2
‑
葡糖苷钾盐的含水晶体析出。具体而言,例如在使用抗坏血酸2
‑
葡糖苷无水晶体1g时,向其中添加并溶解浓度为4~8当量(n)的氢氧化钾水溶液2ml,接着,添加并混合3ml以上的醇,在低温下静置即可。氢氧化钾相对于抗坏血酸2
‑
葡糖苷的摩尔比通常适宜为2.7~5.4,更优选为3.4~4.1的范围。另外,在使晶体析出的操作中添加的醇没有特别限定,可适宜使用该领域中通用的甲醇、乙醇。晶析时的醇浓度以终浓度计优选为50体积%左右。予以说明,析出的晶体可以通过过滤、离心分离等通常的固液分离法回收。
[0019]
通过晶析操作得到的抗坏血酸2
‑
葡糖苷钾盐的含水晶体通过用酒精水溶液清洗,可制成更高纯度的含水晶体。得到的含水晶体根据需要粉碎、干燥,由此可以制成含有抗坏血酸2
‑
葡糖苷钾盐的含水晶体的粉末。另外,也可以将通过添加醇使晶体析出而得到的糖膏喷雾干燥,由此得到含有抗坏血酸2
‑
葡糖苷钾盐的含水晶体的粉末。
[0020]
作为本发明的抗坏血酸2
‑
葡糖苷钾盐的含水晶体的特征之一,可举出:在溶解于水的情况下,得到的水溶液显示碱性,在这一点上,与公知的抗坏血酸2
‑
葡糖苷的钠盐的晶体是同样的。与性质对照的是,在抗坏血酸2
‑
葡糖苷无水晶体溶解于水的情况下,得到的水溶液显示较强的酸性。因此,本发明人等创制出的新的抗坏血酸2
‑
葡糖苷的钾盐的含水晶体即使是在对于以往的抗坏血酸2
‑
葡糖苷无水晶体来说由于水溶液显示较强的酸性而使用量、使用形式以及使用本身受限的用途中也能够适宜地使用。例如,在用于要求弱碱性的肥皂系的皮肤外用组合物、例如肥皂、洗发水、洗面奶、沐浴露等的情况下,在使用以往的含有抗坏血酸2
‑
葡糖苷无水晶体的粉末时,需要预先用碱中和溶解于水性介质的抗坏血酸2
‑
葡糖苷的酸性溶液的操作和添加用于调整ph的缓冲剂,但溶解抗坏血酸2
‑
葡糖苷钾盐的含水晶体而得到的水溶液通常显示碱性,因此在配合于该皮肤外用组合物时,不需要使用碱中和抗坏血酸2
‑
葡糖苷的操作、也不需要并用缓冲剂的情况较多。
[0021]
进而,在将抗坏血酸2
‑
葡糖苷钾盐的含水晶体与抗坏血酸2
‑
葡糖苷无水晶体并用时,通过调整两者的配合比,可得到以下优点:能够得到溶解于水性介质时的ph在预定范围内、例如弱碱性至弱酸性的范围内的抗坏血酸2
‑
葡糖苷的水溶液。因此,将抗坏血酸2
‑
葡糖苷钾盐的含水晶体与抗坏血酸2
‑
葡糖苷无水晶体并用时,可得到以下优点:无需另外使用抗坏血酸2
‑
葡糖苷钾盐的含水晶体以外的碱来中和抗坏血酸2
‑
葡糖苷,就能够制造出包含皮肤外用组合物、基础化妆品在内的整体的ph优选成为弱碱性至弱酸性的范围内的各种组合物。予以说明,在并用两者时,在制造各种组合物时,将抗坏血酸2
‑
葡糖苷无水晶体与抗坏血酸2
‑
葡糖苷钾盐的含水晶体仅计量根据各自的配比的量使用即可,但根据目标组合物所需的ph,预先制成以规定的质量比配合抗坏血酸2
‑
葡糖苷无水晶体与抗坏血酸2
‑
葡糖苷钾盐的含水晶体而得到的组合物是便利的。此时,其质量比可以根据期望的ph任意设定,但为了使其成为化妆品用途等所通用的弱酸性至中性的范围,通常适宜以质量比70∶30~45∶55、优选50∶50~45∶55的范围配合。
[0022]
本发明的抗坏血酸2
‑
葡糖苷钾盐的晶体是抗坏血酸2
‑
葡糖苷的新的晶体形态,在其水溶液的ph显示碱性方面,与公知的抗坏血酸2
‑
葡糖苷钠盐的晶体是相同的。本发明的抗坏血酸2
‑
葡糖苷钾盐的晶体也与以往公知的抗坏血酸2
‑
葡糖苷的无水晶体、含水晶体、钠盐晶体等同样地,可有利地用于配合有抗坏血酸2
‑
葡糖苷的饮食品、化妆品、医药部外品、药品或工业用品的制造。
[0023]
以下,通过实验详细说明本发明。
[0024]
<实验1:抗坏血酸2
‑
葡糖苷的新晶体的制备>将市售的含有抗坏血酸2
‑
葡糖苷无水晶体的粉末(商品名
“アスコフレッシュ”
(注册商标),株式会社林原销售)12g溶解在5n的氢氧化钾水溶液24ml中,然后在该水溶液中进一步加入甲醇36ml并搅拌,在4℃下静置4天,结果发现白浊,显微镜观察的结果,确认晶体的析出。使用桐山漏斗(使用东洋滤纸no.5)过滤晶体悬浮液,由此回收晶体,用去离子水清洗后,在30℃下真空干燥5小时,得到约15.4g的晶体粉末。所述水溶液中的氢氧化钾相对于抗坏血酸2
‑
葡糖苷的摩尔比为3.4。
[0025]
<实验2:抗坏血酸2
‑
葡糖苷的新晶体的各种分析>对实验1中获得的晶体,显微镜观察晶体形状,并且进行hplc分析、水溶液的ph、uv吸收光谱的测定、粉末x射线衍射图、水分含量和钾含量的各种测定。
[0026]
<实验2
‑
1:晶体的形状>对实验1中获得的晶体,使用光学显微镜(bx
‑
50型,奥林巴斯公司制)观察晶体的形状,结果,实验1中获得的晶体为10~100μm
×
1000μm的大小,其形状为柱状,透明。拍摄所得晶体中被认为典型的晶体的显微镜照片(倍率125倍),示于图1。另外,图1右下方所示的比例尺长度为200μm。
[0027]
<实验2
‑
2:hplc分析>将实验1中获得的晶体溶解在去离子水中至最终浓度为1质量%,在下述条件下进行hplc分析。作为对照,使用食品级的含有抗坏血酸2
‑
葡糖苷无水晶体的粉末(商品名
“アスコフレッシュ”
(注册商标),株式会社林原销售),在相同条件下进行分析。<hplc分析条件>柱:wakopak wakobeads t
‑
330,(内径10mm
×
长度300mm)h型28901(和光纯药工业株式会社销售)洗脱液:0.0001n硝酸水溶液流速:0.4ml/分钟温度:室温检测器:差示折射计
[0028]
在溶解有晶体的待测样品液的hplc色谱图中,与用作对照的含有抗坏血酸2
‑
葡糖苷的无水晶体的粉末的情况同样地,基本上仅检测出抗坏血酸2
‑
葡糖苷的峰,因此确认实验1中获得的晶体为抗坏血酸2
‑
葡糖苷的晶体。
[0029]
<实验2
‑
3:溶解有晶体的水溶液的ph和uv吸收光谱>将实验1中获得的晶体制成1质量%水溶液来测定其ph,结果ph显示12.7和碱性。另外,将该水溶液稀释300倍,测定uv吸收光谱,结果显示与抗坏血酸2
‑
葡糖苷相同的uv吸收光谱(λmax 260nm)。
[0030]
<实验2
‑
4:粉末x射线衍射图>将实验1中获得的晶体使用粉末x射线衍射装置(“x
‘
pert pro mpd”,使用cukα射线,spectris公司制)进行粉末x射线衍射分析。将约50mg晶体样品放置于硅制无反射板上,一边旋转一边在下述条件下照射cukα射线,通过反射法求出粉末x射线衍射图。将得到的粉末x射线衍射图示于图2。<cukα射线照射条件>x射线管电流:40max射线管电压:45kv波长:
[0031]
另外,将新获得的晶体的粉末x射线衍射图与公知的抗坏血酸2
‑
葡糖苷的晶体的粉末x射线衍射图一并记载于图3。在图3中,分别用符号a、b、c和d表示实验1中获得的晶体的粉末x射线衍射图、抗坏血酸2
‑
葡糖苷的钠盐晶体(含水晶体,株式会社林原制品)的粉末x射线衍射图、抗坏血酸2
‑
葡糖苷的含水晶体(株式会社林原制品)的粉末x射线衍射图、以及抗坏血酸2
‑
葡糖苷的无水晶体(商品名
“アスコフレッシュ”
(注册商标),株式会社林原销售)的粉末x射线衍射图。
[0032]
如图2所示,新获得的晶体在粉末x射线衍射图中显示出在衍射角(2θ)8.27
°
、
8.81
°
、16.05
°
、18.88
°
和25.64
°
处具有特征衍射峰(图2的符号a、b、c、d和e),除此以外,由图3可知,其粉末x射线衍射图与以往公知的抗坏血酸2
‑
葡糖苷无水晶体、含水晶体和钠盐晶体(含水晶体)的任一种的粉末x射线衍射图完全不同。由该结果可知,实验1中获得的晶体是新的抗坏血酸2
‑
葡糖苷的晶体。
[0033]
<实验2
‑
5:水分含量的测定>对实验1中获得的晶体使用卡尔
‑
费歇尔水分测定装置(商品名“aq
‑
2200”,平沼产业株式会社制)测定水分含量,结果为14.8质量%。由该结果可知,实验1中获得的抗坏血酸2
‑
葡糖苷的新晶体为含水晶体的形态。
[0034]
<实验2
‑
6:钾含量的测定>称取150mg实验1中获得的晶体,溶解在100ml去离子水中,进一步用去离子水稀释50倍而作为测定样品。使用离子色谱仪(“dionex ics
‑
5000+”,thermo fisher scientific公司制)在下述条件下测定样品中的钾量。<测定条件>柱:dionex ionpac cs16(5
×
250mm)(thermo fisher scientific公司制)保护柱:dionex ionpac cs16 guard(5
×
50mm)(thermo fisher scientific公司制)洗脱液:30mm甲磺酸流速:1.0ml/分钟柱温:40℃检测器:电导率检测器抑制器:电场再生型cers
‑
500电流:89ma检测室温度:20℃样品注入量:25μl标准液:阳离子混合标准液ii(6种)ic用no.07197
‑
96(关东化学株式会社制)
[0035]
基于离子色谱法的结果计算出的晶体的钾含量为14.2质量%。由该结果可确认,实验1中获得的抗坏血酸2
‑
葡糖苷的晶体为钾盐晶体。
[0036]
顺便说一下,该晶体中假设钾作为氢氧化钾(koh)存在时计算出的晶体的组成(质量%)示于表1。进而,计算出此时的抗坏血酸2
‑
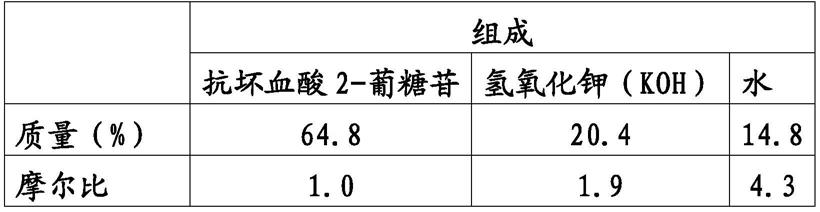
葡糖苷与氢氧化钾的摩尔比的结果也一并记载于表1。
[0037]
[表1]
[0038]
予以说明,如上所述,抗坏血酸2
‑
葡糖苷钾盐的含水晶体中的钾含量约为14.2质量%,假设钾全部以氢氧化钾(koh)的形态存在时,计算出氢氧化钾的含量为20.4质量%。
此时,当从晶体质量100质量%中减去水的质量14.8质量%和氢氧化钾的质量20.4质量%时,抗坏血酸2
‑
葡糖苷所占的量为64.8质量%。根据该数值计算出抗坏血酸2
‑
葡糖苷与氢氧化钾的摩尔比,如表1所示,为1.0:1.90,因此,当假设钾全部以氢氧化钾的形态存在时,该抗坏血酸2
‑
葡糖苷钾盐的含水晶体被推定为相对于1分子的抗坏血酸2
‑
葡糖苷含有约2分子的氢氧化钾。
[0039]
另外,同样地,抗坏血酸2
‑
葡糖苷钾盐的含水晶体中的水分含量约为14.8质量%,抗坏血酸2
‑
葡糖苷与水分子的摩尔比约为1.0:4.3,因此推测该抗坏血酸2
‑
葡糖苷钾盐的含水晶体相对于1分子的抗坏血酸2
‑
葡糖苷含有4分子的结晶水。
[0040]
由实验2
‑
1至2
‑
6的结果判断,实验1中获得的抗坏血酸2
‑
葡糖苷的新的晶体为抗坏血酸2
‑
葡糖苷钾盐的含水晶体。
[0041]
<实验3:抗坏血酸2
‑
葡糖苷的钾盐晶体的生成条件的研究>相对于1g含有抗坏血酸2
‑
葡糖苷无水晶体的粉末(商品名
“アスコフレッシュ”
(注册商标),株式会社林原销售),添加2ml下表2所示的1~10n的氢氧化钾水溶液,溶解后添加3ml甲醇,混合,将混合液在4℃下放置24小时,目测观察晶体的析出程度。晶体析出程度分以下四个等级判定,结果示于表2。
“‑”
:晶体未析出“+”:晶体少量析出“++”:晶体析出混合液容量的一半左右“+++”:晶体全部析出而固化
[0043]
如表2所示,将抗坏血酸2
‑
葡糖苷无水晶体的粉末溶解在4n、5n、6n和8n的各浓度的氢氧化钾水溶液中,从添加有甲醇的氢氧化钾水溶液中分别观察到抗坏血酸2
‑
葡糖苷的
钾盐晶体的析出。若讨论氢氧化钾相对于抗坏血酸2
‑
葡糖苷的摩尔比,在该摩尔比为2.7~5.4的范围观察到晶体的析出。另一方面,若讨论氢氧化钾浓度为3n以下、氢氧化钾相对于抗坏血酸2
‑
葡糖苷的摩尔比,则当该摩尔比为2.0以下时,完全没有发现晶体的析出。另外,若讨论氢氧化钾浓度为10n以上、氢氧化钾相对于抗坏血酸2
‑
葡糖苷的摩尔比,则该摩尔比为6.8以上时,完全看不到晶体的析出,样品着色。
[0044]
另外,专利文献10中公开了一种抗坏血酸2
‑
葡糖苷的钠盐晶体的制备方法,根据该制备方法,氢氧化钠相对于抗坏血酸2
‑
葡糖苷的摩尔比为1.7以上、且相对于1g抗坏血酸2
‑
葡糖苷的甲醇量为1ml时,观察到晶体的析出。本发明人等在制造抗坏血酸2
‑
葡糖苷的钾盐的晶体时,首先将氢氧化钠替换为氢氧化钾,除此以外,在与专利文献10公开的钠盐晶体的情况相同的析出条件下进行了尝试,但无法得到钾盐的晶体。即,相对于10g含有抗坏血酸2
‑
葡糖苷无水晶体的粉末(商品名“aa2g”(注册商标),株式会社林原销售),添加8n氢氧化钾水溶液10ml,溶解后添加甲醇10ml并混合,在4℃静置24小时,但无法得到钾盐的晶体。在此反复试错的结果,意外地通过将添加的甲醇的量增加至3倍,成功地析出抗坏血酸2
‑
葡糖苷的钾盐的晶体。综上,本发明的抗坏血酸2
‑
葡糖苷的钾盐晶体是通过与钠盐晶体的情况完全不同的条件得到的。
[0045]
<实验4:抗坏血酸2
‑
葡糖苷钾盐晶体与抗坏血酸2
‑
葡糖苷无水晶体的配合物的ph>将市售的含有抗坏血酸2
‑
葡糖苷无水晶体的粉末(商品名
“アスコフレッシュ”
(注册商标),株式会社林原销售)和实验1的方法得到的抗坏血酸2
‑
葡糖苷钾盐的含水晶体以下表3所示的100:0~0:100的质量比配合而得到的各配合物分别溶解在去离子水中至浓度为1质量%,测定得到的水溶液的ph。结果示于表3。
[0046]
[表3]
[0047]
如表3所示,单独(100质量%)溶解含有抗坏血酸2
‑
葡糖苷无水晶体的粉末,浓度为1质量%的水溶液的ph为2.2,与此相比,单独(100质量%)溶解抗坏血酸2
‑
葡糖苷钾盐的含水晶体,浓度为1质量%的水溶液的ph为12.7。另外,将含有抗坏血酸2
‑
葡糖苷无水晶体的粉末与抗坏血酸2
‑
葡糖苷钾盐的含水晶体的相对配比在90∶10~10∶90的范围内变化,浓度为1质量%的水溶液的ph显示2.5~12.6的范围。由这些结果可知,通过将含有抗坏血酸2
‑
葡糖苷无水晶体的粉末与抗坏血酸2
‑
葡糖苷钾盐的含水晶体以适当的质量比配合而制成水溶液时,可以在酸性至碱性的宽范围内得到期望的ph,特别是在以70∶30~45∶55的质量比配合时,可以在ph3.0~7.0的范围,更优选以50∶50~45∶55的质量比配合时,可以在ph4.4~7.0的弱酸性至中性的范围调节ph。
[0048]
<实验5:抗坏血酸2
‑
葡糖苷钾盐的含水晶体的吸湿性>对实验1的方法得到的抗坏血酸2
‑
葡糖苷钾盐的含水晶体、和上述专利文献10所述的方法得到的抗坏血酸2
‑
葡糖苷钠盐的含水晶体,进行比较两者吸湿性的实验。即,分别称取各0.5g抗坏血酸2
‑
葡糖苷钾盐的含水晶体和抗坏血酸2
‑
葡糖苷钠盐的含水晶体,在室温下在用饱和生理盐水溶液调湿至相对湿度(rh)为75.2%的干燥器内保存24小时后,测定各自的质量,求出因吸湿而增加的质量,求出质量增加率{(因保存而增加的质量/保存开始时的质量)
×
100}(质量%)。结果示于表4。
[0049]
[表4]待测样品质量增加率
*
(质量%)抗坏血酸2
‑
葡糖苷钾盐的含水晶体9.1抗坏血酸2
‑
葡糖苷钠盐的含水晶体15.8*:相对湿度75.2%、室温、24小时保存后
[0050]
如表4所示,抗坏血酸2
‑
葡糖苷钾盐的含水晶体和抗坏血酸2
‑
葡糖苷钠盐的含水晶体在本试验中的质量增加率分别显示为9.1质量%和15.8质量%,判定其均在相对湿度(rh)75.2%的条件下吸湿。抗坏血酸2
‑
葡糖苷钾盐的含水晶体的质量增加率为抗坏血酸2
‑
葡糖苷钠盐的含水晶体的质量增加率的不到60%,结果可知,抗坏血酸2
‑
葡糖苷钾盐的含水晶体的吸湿性比抗坏血酸2
‑
葡糖苷钠盐的含水晶体的吸湿性低。
[0051]
<实验6:抗坏血酸2
‑
葡糖苷钾盐的含水晶体的单晶x射线晶体结构分析>为了得到可用于单晶x射线晶体结构分析的比较大的晶体,在比通常晶体更难以析出的条件下花时间进行结晶化。即,将1g含有抗坏血酸2
‑
葡糖苷无水晶体的粉末(商品名
“アスコフレッシュ”
(注册商标),株式会社林原销售)溶解在浓度比通常的结晶化更低的4n氢氧化钾水溶液2ml中,然后添加3ml甲醇进行混合,用4天晶析,使抗坏血酸2
‑
葡糖苷钾盐的含水晶体析出。从得到的晶体中选择适当大小的晶体(0.30
×
0.09
×
0.07mm),使用x射线衍射装置(“rigaku varimax with saturn 724”,株式会社
リガク
制),在下述条件下测定x射线衍射图。分析软件使用“crystal clear”(株式会社
リガク
制)。<测定条件>入射x射线:mokα射线(波长)输出:50kv,24ma检测器:成像板测定温度:约
‑
173℃(氮气吹拂法)
[0052]
在成像板上的x射线衍射图中,观察到许多衍射斑点(spot),确认该晶体为单晶。将通过单晶x射线晶体结构分析得到的抗坏血酸2
‑
葡糖苷钾盐的含水晶体的晶体学参数汇总于表5。
[0053]
[表5]
[0054]
根据得到的x射线衍射强度数据,如表5所示,确定:抗坏血酸2
‑
葡糖苷钾盐的含水晶体属于斜方晶系,空间群为p212121,晶格常数为,晶格常数为
[0055]
另外,根据得到的x射线衍射强度数据,认为抗坏血酸2
‑
葡糖苷的钾盐的含水晶体的分子式为c
12
h
24
k2o
15
、结构式为c
12
h
17
o
11
‑
·
2k
+
·
oh
‑
·
3h2o,分子量为486.51。如图4所示,推定该晶体是包含以下成分的晶体:从l
‑
抗坏血酸的3位羟基解离出氢而得到的抗坏血酸2
‑
葡糖苷1分子、钾离子2个、氢氧根离子1个、和水3分子。实施例
[0056]
以下,通过实施例更详细地说明本发明。但是,本发明不限定于这些实施例。
实施例1
[0057]
<抗坏血酸2
‑
葡糖苷钾盐的含水晶体>向2l的5n氢氧化钾水溶液中加入市售的含有抗坏血酸2
‑
葡糖苷无水晶体的粉末(商品名“aa2g”(注册商标),纯度98质量%以上,株式会社林原销售)1kg,通过搅拌使其完全溶解。向该水溶液中添加3l甲醇并混合,添加预先用实验1的方法制备的抗坏血酸2
‑
葡糖苷钾盐的含水晶体10g作为晶种,搅拌混合后,在5℃下放置3天,由此使晶体析出。接着,将得到的晶体过滤而回收,用60体积%的甲醇水溶液洗涤,在30℃下干燥,由此制造约1.1kg的抗坏血酸2
‑
葡糖苷钾盐的含水晶体。通过实验2
‑
2记载的hplc法测定本晶体中的抗坏血酸2
‑
葡糖苷纯度,结果为99.2质量%,另外,通过卡尔
‑
费歇尔法测定水分含量,结果为12.5质量%,基于离子色谱法的结果计算出的晶体的钾含量为14.1质量%。
[0058]
本品为流动性良好的抗坏血酸2
‑
葡糖苷钾盐的含水晶体制品,可广泛地利用于饮食物、化妆品、医药部外品(准药品)、药品等各种组合物。实施例2
[0059]
<含有抗坏血酸2
‑
葡糖苷钾盐的含水晶体的粉末>向25质量份的水中加入7质量份的木薯淀粉,加入市售的液化酶,加热溶解后,加入l
‑
抗坏血酸3质量份,将ph调整为5.5,制成基质溶液。向其中加入每1g木薯淀粉固体物质100单位的来自嗜热脂肪芽孢杆菌(geobacillus stearothermophilus)的cgtase酶剂,在55℃下反应50小时,生成抗坏血酸2
‑
葡糖苷和抗坏血酸2
‑
糖苷。
[0060]
加热该反应液,使酶失活后,将ph调节至4.5,向其中加入每1g淀粉固体物质50单位的葡糖淀粉酶(商品名
“グルコチーム
#20000”,20,000单位/g,
ナガセケムテックス
株式会社销售),在55℃下反应24小时,将抗坏血酸2
‑
糖苷分解成抗坏血酸2
‑
葡糖苷,另外,将混合的糖质分解成葡萄糖。本反应液中的抗坏血酸2
‑
葡糖苷的含量按无水物换算约为30.5质量%。
[0061]
加热本反应液,使酶失活后,用活性炭脱色过滤,将滤液用阳离子交换树脂(h
+
型)脱盐,接着,使l
‑
抗坏血酸和抗坏血酸2
‑
葡糖苷吸附于阴离子交换树脂(oh
‑
型),水洗除去大部分葡萄糖后,用0.5n盐酸溶液洗脱,浓缩后,再供于使用强酸性阳离子交换树脂(商品名
“ダウエツクス
50wx4”,ca
2+
型,道化学公司制)的凝胶渗透色谱,回收高含量抗坏血酸2
‑
葡糖苷级分。回收的含有抗坏血酸2
‑
葡糖苷的溶液的组成按无水物换算,抗坏血酸2
‑
葡糖苷为95.3质量%,l
‑
抗坏血酸为1.2质量%,葡萄糖为2.5质量%,其他为1.0质量%。
[0062]
减压浓缩该含有抗坏血酸2
‑
葡糖苷的溶液,使固体物质浓度约为60质量%,添加氢氧化钾至最终浓度为5n,使之溶解,再添加乙醇至最终浓度为60体积%。将其采集到助晶罐中,将温度冷却至5℃,相对于抗坏血酸2
‑
葡糖苷的固体物质质量,加入2质量%的实验1的方法得到的抗坏血酸2
‑
葡糖苷钾盐的含水晶体粉末作为晶种,温和地搅拌,晶析3日,得到抗坏血酸2
‑
葡糖苷钾盐的含水晶体析出的糖膏。将该糖膏通过常规方法以篮式离心分离机回收晶体,通过喷雾少量的75体积%乙醇水溶液来清洗晶体,然后粉碎、干燥,得到含有抗坏血酸2
‑
葡糖苷钾盐的含水晶体的粉末。本品的抗坏血酸2
‑
葡糖苷的纯度按无水物换算为98.6质量%,另外,通过卡尔
‑
费歇尔法测定水分含量,结果为14.3质量%,基于离子色谱法的结果计算出的晶体的钾含量为14.1质量%。
[0063]
本品为流动性良好的抗坏血酸2
‑
葡糖苷钾盐的含水晶体的粉末制品,可广泛利用
于饮食物、化妆品、医药部外品、药品等各种组合物。实施例3
[0064]
<抗坏血酸2
‑
葡糖苷钾盐的含水晶体和抗坏血酸2
‑
葡糖苷无水晶体的配合物>向实施例1的方法得到的抗坏血酸2
‑
葡糖苷钾盐的含水晶体50质量份中均匀混合含有抗坏血酸2
‑
葡糖苷无水晶体的粉末(商品名“aa2g”(注册商标),株式会社林原销售)50质量份,粉碎、干燥,得到粉末状的配合物。
[0065]
本品是抗坏血酸2
‑
葡糖苷钾盐的含水晶体与通用的抗坏血酸2
‑
葡糖苷无水晶体的配合物,与以往的含有抗坏血酸2
‑
葡糖苷无水晶体的粉末同样地,可有利地用作化妆品原料,另外,也可以有利地用作医药部外品、药品、食品等的原料。另外,由于本品的水溶液显示弱酸性,因此与使用以往的含有抗坏血酸2
‑
葡糖苷无水晶体的粉末的情况相比,可容易地调整为期望的ph。实施例4
[0066]
<化妆水>(配方)
[0067]
将上述配方的成分(1)至(4)溶解在精制水(9)中后,缓慢添加混合成分(5)至(8)的混合物并混合,由此制备化妆水。本品是配合有抗坏血酸2
‑
葡糖苷的化妆水,用作不仅抗皱作用、抗细纹作用、而且美白作用、以及抗斑、抗松弛作用、皮肤屏障功能及玻尿酸产生的维持或亢进作用也优异的抗衰用化妆水。另外,由于配合了1,2
‑
戊二醇,因此是防腐效果和保湿性优异、对皮肤的刺激性低、而且稳定性优异的化妆水。实施例5
[0068]
<美容液>(配方)
[0069]
按照上述配方,通过常规方法将配合成分混合,制备美容液。本品是配合有抗坏血酸2
‑
葡糖苷的美容液,用作发挥稳定的抗皱作用、抗细纹作用,并且美白作用优异、使用感也优异的抗衰用美容液。实施例6
[0070]
<健康辅助食品>将1质量份的实施例3的方法得到的配合物和99质量份的海藻糖(商品名
“トレハ”
(商品名“treha”)(注册商标),株式会社林原销售)均匀混合后,制成每50g填充在玻璃瓶中的制品。本品用作强化维生素c(富含维生素c)的健康辅助食品。实施例7
[0071]
<健康食品>将脱脂乳85质量份、脱脂奶粉3质量份、海藻糖(商品名
“トレハ”
(商品名“treha”)(注册商标),株式会社林原销售)6质量份、琼脂0.1质量份、实施例3的方法得到的配合物3质量份、粉末糖转移橙皮苷4质量份和精制水2质量份放入调和罐中,一边搅拌一边加热至55℃,完全溶解。接着,按照常规方法将混合物均质化,通过杀菌冷却器杀菌,接种3质量%的发酵剂,填充到塑料容器中后,在37℃下发酵5小时,得到酸奶型健康食品。本品是强化维生素c(富含维生素c)的酸奶型健康食品。实施例8
[0072]
<维生素c粉末制剂>使用实施例3的方法得到的配合物作为粉末状食品材料,向其中加入蔗糖70质量份、糊精10质量份、适量的香料,使用混合机搅拌混合,制造维生素c粉末制剂。抗坏血酸2
‑
葡糖苷的晶体粉末与其他粉末可使用混合机容易地均匀混合,在制造步骤上可毫无障碍地制造。
[0073]
本品是可易于与其他饮食品材料混合、即使长时间保存也不易发生褐变或凝固的维生素c粉末制剂。本品和配合有本品的组合物具有维生素c的生理功能,因此可口服以保持皮肤和粘膜的健康、以及美白。实施例9
[0074]
<软膏>将三水合乙酸钠1质量份、dl
‑
乳酸钙4质量份与甘油10质量份混合均匀,将该混合物加入到凡士林50质量份、木蜡10质量份、羊毛脂10质量份、芝麻油14.5质量份、实施例3的方法得到的配合物1质量份和薄荷油0.5质量份的混合物中,进一步均匀混合,制造软膏。
[0075]
本品可有利地用作防晒剂、美肤剂、美白剂等,还可以有利地用作外伤(创伤)和烧伤(烫伤)的愈合促进剂等。产业实用性
[0076]
本发明的抗坏血酸2
‑
葡糖苷钾盐的含水晶体是迄今为止未知的抗坏血酸2
‑
葡糖苷的新晶型。当本发明的抗坏血酸2
‑
葡糖苷钾盐的含水晶体与抗坏血酸2
‑
葡糖苷无水晶体组合使用时,通过适当调节两者的配比,能够在不使用碱来中和抗坏血酸2
‑
葡糖苷的情况下将制品的ph调整至期望的范围,因此可具有以下优点:能够以更少的步骤更容易地制造饮食品、化妆品、医药部外品、药品、工业用品等。本发明具有如此优异的优点,具有很大的产业实用性。附图标记说明
[0077]
在图2中,
↓
:晶体的粉末x射线衍射图中的5个特征衍射峰a:衍射角(2θ)为8.27
°
的衍射峰b:衍射角(2θ)为8.81
°
的衍射峰c:衍射角(2θ)为16.05
°
的衍射峰d:衍射角(2θ)为18.88
°
的衍射峰e:衍射角(2θ)为25.64
°
的衍射峰在图3中,a:新获得的晶体的粉末x射线衍射图b:抗坏血酸2
‑
葡糖苷钠盐(含水晶体)的粉末x射线衍射图c:抗坏血酸2
‑
葡糖苷的含水晶体(1/2含水)的粉末x射线衍射图d:抗坏血酸2
‑
葡糖苷无水晶体的粉末x射线衍射图
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1