一种益生菌微囊及其制备方法和应用与流程
1.本发明属于功能食品技术领域,具体涉及一种益生菌微囊及其制备方法和应用。
背景技术:
2.近年来,随着科学的不断研究,肠道菌群与肥胖之间的关系也慢慢被揭示。jeffrey gordon教授将具有特征性丰度比例的胖小鼠的肠道菌以及另一种瘦小鼠的肠道菌移植到无菌鼠的肠道中,两周后令人惊讶的发现,移植了胖鼠肠道菌的无菌鼠比移植了瘦鼠肠道菌的无菌鼠体内脂肪重量增加了20%。人们开始意识到肠道益生菌在体重管理上的重要作用,体重管理市场的益生菌产品不断增长。
3.益生菌对环境敏感,经常通过包埋技术来提高其到达肠道内的菌株存活率。而由于包埋配方和工艺的局限性,往往无法达到理想的存活效果。且很多包埋益生菌的材料在肠道内,对于肠道菌群影响较小甚至有可能产生副作用。
4.cn 109464425 a公开了一种益生菌包埋颗粒及其制备方法,所述益生菌包埋颗粒包括益生菌核芯以及益生菌核芯外的三个包埋层,所述包埋层从内到外依次为:淀粉保护层、薄膜包衣隔离层和肠溶包衣层。最终包埋后活菌存活率仅为39~49%。
5.cn 113230280 a公开了一种结肠靶向的益生菌多层包埋微胶囊及其制备方法与应用,属于生物医学工程领域。本发明以海藻酸钠/益生元/益生菌为核层,海藻酸钠/果胶为壳层壁材,大豆分离蛋白为最外层壁材,通过同轴静电喷涂装置制备得到负载活性物质的多层微胶囊。所得微胶囊实现益生菌结肠靶向释放,但所述的益生元选用低聚果糖,无法起到定向调节特定肠道菌群的作用,而且容易引起肠道内产气细菌的增长。
6.因此,为了解决这一问题,有必要研究一种包埋效果好,高存活率,且能够定向有益调节肠道菌群的产品。
技术实现要素:
7.本发明的目的在于提供一种益生菌微囊,克服现有技术中存在的上述技术问题。
8.本发明的另一个目的在于提供一种益生菌微囊的制备方法,通过二次包埋方法得到益生菌微囊,包埋效果好,存活率高。
9.本发明的另一个目的在于提供一种益生菌微囊在制备减重产品中的应用,能够定向有益调节肠道菌群,减重效果良好。
10.为此,本发明提供的技术方案如下:一种益生菌微囊,包括活菌粉、蛋白壁材、复合益生元和水溶性多糖壁材,所述活菌粉与蛋白壁材形成一级包埋粉,所述益生菌微囊通过一级包埋粉与水溶性多糖壁材、复合益生元混合分散、均质进行二次包埋喷雾干燥后得到;所述蛋白壁材质量为活菌粉的4-6倍,所述一级包埋粉与水溶性多糖壁材的质量比为1:2-2:1,所述复合益生元和一级包埋粉的质量比为 1:2-2:1。
11.所述复合益生元为低聚甘露糖和水苏糖,两者的质量比为1:3-3:1。
12.所述活菌粉是动物双歧杆菌b420、乳双歧杆菌b420、嗜酸乳杆菌dds-1和副干酪乳杆菌lpc-37的一种或几种经过发酵培养后再处理得到。
13.所述蛋白壁材为明胶、阿拉伯胶、酪蛋白、大豆分离蛋白和玉米醇溶蛋白中的一种或几种。
14.所述水溶性多糖壁材为变形淀粉、葡甘聚糖、海藻酸钠、纤维素、壳聚糖中的一种或几种。
15.一种益生菌微囊的制备方法,包括以下步骤:步骤1)制备活菌粉;步骤2)对活菌粉进行第一次包埋,得到一级包埋粉;步骤3)将一级包埋粉、水溶性变性淀粉、复合益生元混合,之后分散均质、喷雾干燥得到两层包埋菌粉,即得。
16.步骤1)制备活菌粉的具体过程为:将一种或几种益生菌进行发酵培养,发酵条件37℃,发酵液活菌浓度达到 10
10-15
10
cfu/g时终止发酵 ;随后发酵液离心,无菌水洗涤,获得益生菌湿菌体;将湿菌体与冻干保护剂按质量比1:1混合,乳化 30 分钟,-55℃预冻 8h,-80℃冷冻干燥得到活菌粉。
17.步骤2)中的一级包埋粉制备方法为:将活菌粉与蛋白壁材混合,加入0.01-0.03g tg 酶,乳化搅拌均匀后,进行交联反应 40mins 后,得到一级包埋粉。
18.一种益生菌微囊在制备减重产品中的应用。
19.所述减重产品包括固体饮料、片剂和乳制品。
20.本发明的有益效果是:本发明提供的这种益生菌微囊,将活菌粉为芯材,同时将特定增殖肠道的瘦子菌的复合益生元作为包埋壁材,具有良好减重效果;采用二次包埋方法提高存活率,使益生菌和益生元均能到达肠道,定向调节肠道瘦子菌比例。
21.下面将结合附图做进一步详细说明。
附图说明
22.图1是模拟胃酸条件下菌株存活率曲线;图2是模拟胆盐溶液条件下菌株存活率曲线。
具体实施方式
23.以下由特定的具体实施例说明本发明的实施方式,本领域技术人员可由本说明书所揭示的内容轻易地了解本发明的其他优点及功效。
24.现介绍本发明的示例性实施方式,然而,本发明可以用许多不同的形式来实施,并且不局限于此处描述的实施例,提供这些实施例是为了详尽地且完全地公开本发明,并且向所属技术领域的技术人员充分传达本发明的范围。对于表示在附图中的示例性实施方式中的术语并不是对本发明的限定。
25.除非另有说明,此处使用的术语(包括科技术语)对所属技术领域的技术人员具有通常的理解含义。另外,可以理解的是,以通常使用的词典限定的术语,应当被理解为与其相关领域的语境具有一致的含义,而不应该被理解为理想化的或过于正式的意义。
26.实施例1:本实施例提供了一种益生菌微囊,包括活菌粉、蛋白壁材、复合益生元和水溶性多糖壁材,所述活菌粉与蛋白壁材形成一级包埋粉,所述益生菌微囊通过一级包埋粉与水溶性多糖壁材、复合益生元混合分散、均质进行二次包埋喷雾干燥后得到;所述蛋白壁材质量为活菌粉的4-6倍,所述一级包埋粉与水溶性多糖壁材的质量比为1:2-2:1,所述复合益生元和一级包埋粉的质量比为 1:2-2:1。
27.其中,复合益生元为低聚甘露糖和水苏糖,两者的质量比为1:3-3:1。
28.活菌粉是动物双歧杆菌b420、乳双歧杆菌b420、嗜酸乳杆菌dds-1和副干酪乳杆菌lpc-37的一种或几种经过发酵培养后再处理得到。
29.所述蛋白壁材为明胶、阿拉伯胶、酪蛋白、大豆分离蛋白和玉米醇溶蛋白中的一种或几种。
30.所述水溶性多糖壁材为变形淀粉、葡甘聚糖、海藻酸钠、纤维素、壳聚糖中的一种或几种。
31.本发明提供的这种益生菌微囊,将活菌粉为芯材,同时将特定增殖肠道的瘦子菌的复合益生元作为包埋壁材,具有良好减重效果;采用二次包埋方法提高存活率,使益生菌和益生元均能到达肠道,定向调节肠道瘦子菌比例。
32.实施例2:在实施例1的基础上,本实施例提供了一种益生菌微囊,包括活菌粉、蛋白壁材、复合益生元和水溶性多糖壁材,蛋白壁材质量为活菌粉的4倍,所述一级包埋粉与水溶性多糖壁材的质量比为2:1,所述复合益生元和一级包埋粉的质量比为 2:1。
33.益生菌微囊的制备方法,包括以下步骤:步骤1)制备活菌粉:将40g益生菌动物双歧杆菌b420接种于3000ml三角瓶中,37℃培养 60h 后,扩大发酵培养,当其发酵液活菌浓度达到 10
10
cfu/g,且镜检无杂菌,益生菌形态正常,终止发酵;将发酵液分别离心,用50ml无菌水洗涤两次后,获得益生菌湿菌体;将湿菌体动物双歧杆菌b420 22g与 22g 冻干保护剂混合,乳化 30 分钟,-55℃预冻 8h,-80℃冷冻干燥得到活菌粉;其中,冻干保护剂由以下质量百分比的物质组成:可溶性淀粉30%,vc 钠盐6%, 脱脂乳粉 26%,低聚木糖 38%.步骤2)对活菌粉进行第一次包埋,具体为:取菌粉 10g 与40g蛋白壁材混合,加入 0.020g tg 酶,乳化搅拌均匀后,于 45℃培养箱中交联反应 40mins 后取出,完成第一层包埋,得到一级包埋粉;步骤3)将一级包埋粉32g与16g水溶性多糖壁材、48g复合益生元混合,将所得混合物15000rpm 分散 5 分钟,60mpa 均质两次;喷雾干燥,其中进风温度 170℃,出风温度 90℃,流量 360ml/min,得到两层包埋菌粉即得。
34.在本实施例中,复合益生元中低聚甘露糖和水苏糖的重量比为1:3。蛋白壁材为明胶,水溶性多糖壁材为水溶性变性淀粉。
35.实施例3:在实施例1的基础上,本实施例提供了一种益生菌微囊,包括活菌粉、蛋白壁材、复合益生元和水溶变形淀粉,蛋白壁材质量为活菌粉的5倍,所述一级包埋粉与水溶性多糖壁材的质量比为1:1,所述复合益生元和一级包埋粉的质量比为 1:1。
36.益生菌微囊的制备方法,包括以下步骤:步骤1)制备活菌粉:将益生菌动物双歧杆菌b420、乳双歧杆菌b420各 20g 分别接种于 3000ml 三角瓶中,37℃培养 60h 后,扩大发酵培养,当其发酵液活菌浓度达到 12
10
cfu/g,且镜检无杂菌,益生菌形态正常,终止发酵;将两种发酵液分别离心,用无菌水 50ml 洗涤两次后,获得两种益生菌湿菌体;将湿菌体动物双歧杆菌b420 8.2g、13.8g乳双歧杆菌b420与 22g 冻干保护剂混合,乳化 30 分钟,-55℃预冻 8h,-80℃冷冻干燥得到活菌粉;步骤2)对活菌粉进行第一次包埋,具体为:菌粉 10g 与50g 蛋白壁材混合,加入 0.020g tg 酶,乳化搅拌均匀后,于45℃培养箱中交联反应 40mins 后取出,完成第一层包埋,得到一级包埋粉;步骤3)将一级包埋粉32g与32g水溶性多糖壁材、32g复合益生元混合,将所得混合物15000rpm分散 5 分钟,60mpa 均质两次;喷雾干燥,其中进风温度 170℃,出风温度 90℃,流量 360ml/min,得到两层包埋菌粉即得。
37.在本实施例中,复合益生元中低聚甘露糖和水苏糖的重量比为1:1;蛋白壁材为阿拉伯胶和酪蛋白的混合物,质量比为1:1;水溶性多糖壁材为水溶性葡甘露糖和海藻酸钠的复合物,质量比为1:1。
38.实施例4:在实施例1的基础上,本实施例提供了一种益生菌微囊,包括活菌粉、蛋白壁材、复合益生元和水溶变形淀粉,蛋白壁材质量为活菌粉的6倍,所述一级包埋粉与水溶性多糖壁材的质量比为2:1,所述复合益生元和一级包埋粉的质量比为 2:1。
39.益生菌微囊的制备方法,包括以下步骤:步骤1)制备活菌粉:将益生菌动物双歧杆菌b420、乳双歧杆菌b420、嗜酸乳杆菌dds-1和副干酪乳杆菌lpc-37各 10g 分别接种于3000ml三角瓶中,37℃培养 60h 后,扩大发酵培养,当其发酵液活菌浓度达到15
10
cfu/g,且镜检无杂菌,益生菌形态正常,终止发酵;将四种发酵液分别离心,用无菌水 50ml 洗涤两次后,获得四种益生菌湿菌体;将湿菌体动物双歧杆菌b420 8.2g、乳双歧杆菌b420 7.6g、嗜酸乳杆菌dds-1 3.7g和副干酪乳杆菌lpc-37 2.5g与 22g 冻干保护剂混合,乳化 30 分钟,-55℃预冻 8h,-80℃冷冻干燥得到活菌粉;步骤2)对活菌粉进行第一次包埋,具体为:活菌粉10g 与蛋白壁材46g 混合,加入 0.020g tg 酶,乳化搅拌均匀后,于45℃培养箱中交联反应 40mins 后取出,完成第一层包埋,得到一级包埋粉;步骤3)将一级包埋粉32g与64g水溶性多糖壁材、16g复合益生元混合,将所得混合物 15000rpm 分散 5 分钟,60mpa 均质两次;喷雾干燥,其中进风温度 170℃,出风温度 90℃,流量360ml/min,得到两层包埋菌粉即得。
40.在本实施例中,复合益生元中低聚甘露糖和水苏糖的重量比为3:1;蛋白壁材为明胶 、大豆分离蛋白和玉米醇溶蛋白复合物,质量比为2:1:1;水溶性多糖壁材为水海藻酸钠、纤维素和壳聚糖的复合物,质量比为2:1:1。
41.为了对本发明的技术效果做进一步说明,以下对实施例2-4制备的益生菌微囊与对比例进行效果对比。
42.、包埋率包埋率测定:称取0.5g 本发明实施例2-4制备的益生菌微胶囊,加入到4.5ml 模拟肠液( 用naoh 溶液将以重量计0.8%-0.85% nacl 溶液的ph 值调节到8.0 后,加入0.1%胰蛋白酶,用0.22μm的膜进行过滤灭菌) 中,在温度37℃下震荡培养120min,使菌体完全释放,然后取样梯度稀释,采用平板计数法进行活菌计数,按照下式进行计算。
43.包埋率(% ) =微胶囊中活菌数量/ 初始活菌数量
×
100%其结果表明,测定实施例2-4的包埋率分别为:97.2%、97.6%和98.1%,未添加复合益生元的空白包埋组(复合益生元部分用麦芽糊精代替)包埋率仅为74.6%。
44.、耐胃酸试验将实施例2-4制备的益生菌微囊与普通冻干菌粉及未添加复合益生元的包埋益生菌微囊分别进行耐酸性试验。
45.试验方法:用盐酸,加水稀释配制ph值为2的盐酸溶液,并加入1%的胃蛋白酶,混匀,即得模拟胃酸。然后将益生菌包埋颗粒或益生菌粉加入到模拟胃酸里,37℃水浴处理2h,进行活菌数的检测,计算存活率,存活率指经过模拟胃酸处理后活菌数的检测值与起始值之比,用百分比表示,具体结果见图1。
46.由图1可知,实施例2、3、4在模拟胃酸条件下菌株存活率均大于80%,优于未添加益生元的包埋菌株和普通冻干菌粉。
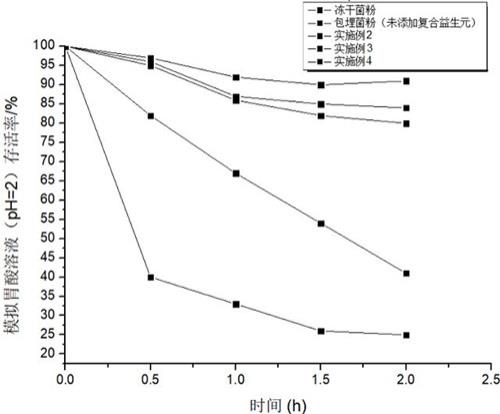
47.、耐胆盐试验将实施例2-4制备的益生菌微囊与普通冻干菌粉及未添加复合益生元的包埋益生菌微囊进行耐酸性试验。试验方法:将300mg胆盐加入到100ml生理盐水(0.85%,w/v)中,调节溶液ph为6.8后灭菌;在该100ml无菌胆盐溶液中加入100mg胰蛋白酶得到模拟小肠液。然后将益生菌包埋颗粒或益生菌粉加入到模拟小肠液里,37℃水浴处理2h,进行活菌数的检测,计算存活率,存活率指经过模拟小肠溶液处理后活菌数的检测值与起始值之比,测试结果见图2。
48.由图2可知,实施例2、3、4在模拟胆盐溶液中下菌株存活率在85%,优于未添加益生元的包埋菌株和普通冻干菌粉。
49.、功效评价试验(动物)领取36只5周龄雄性c57bl/6j小鼠,进行为期一周的适应性饲养,期间给予充足的水和正常饮食。一周后,所有小鼠随机分成3组,一组喂食含45%脂肪的高脂饮食记为hfd/(-)组,另外两组的45%脂肪高脂饮食鼠粮中分别加入5g益生菌微囊(未添加复合益生元)、5g 实施例2益生菌微囊记为hfd/(实施例2)组。三组小鼠均可接触无限制的水和食物。喂养12周后,喂养期间监控小鼠体重变化,见表1。
50.表1小鼠的体重影响
如表1所示,12周后,hfd/(实施例2)、hfd/(实施例3)和hfd/(实施例4)与小鼠相比hfd/(-)组空白组相比均具有显著差异,其中实施例4降低减重效果最为明显,相比于空白组hfd/(-)降低36.48%左右,减重效果明显。
51.、功效评价试验(人体)hfd/(-)组:人员20名、分别为男性10人、女性10人,正常饮食;实验组:共40人,分为2组,每组20人(男性10人、女性10人)。正常饮食外,每日午餐前,两组分别服用5g实施例1和5g益生菌微囊(未添加复合益生元)。实验天数:30天;30天后测定其减重率和减脂率,测定数据如表2所示。
52.表2人体内减重、减脂效果试验由表2可知,相同摄食量,hfd/(实施例2)、hfd/(实施例3)和hfd/(实施例4)与小鼠相比hfd/(-)组空白组相比均有明显减重效果,其中“hfd/(实施例4)”组减重效果最优,减重率在3.5%左右、减脂率在2.5%左右,在人体内具有较好的减重、减脂效果。
53.以上例举仅仅是对本发明的举例说明,并不构成对本发明的保护范围的限制,凡是与本发明相同或相似的设计均属于本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1