一种药食同源的富硒复合固体饮料及其制备方法与流程
1.本发明属于饮料技术领域,具体涉及一种药食同源的富硒复合固体饮料及其制备方法。
背景技术:
2.硒是人体内最重要的微量元素之一,人体中的硒通常以硒蛋白的形式发挥生物学功能,不同的硒蛋白具有不同的生理功能,它们在消炎镇痛、免疫调节、清除自由基、防癌抗癌、延缓机体衰老、拮抗重金属等方面发挥重要作用,同时硒元素还具有抗氧化、抗衰老、提高人体免疫力等预防保健作用,享有“生命的火种”、“长寿元素”等美誉,科学研究表明,癌症、衰老或其它疾病大都与过量自由基的产生有关联,氧化应激是机体或细胞内氧化与抗氧化的平衡失调的病理状态,在多种疾病的发生发展中起着重要作用。抗氧化是预防衰老的重要步骤,机体产生的自由基或氧化剂会将细胞和组织分解,影响代谢功能,并会引起不同的健康问题。如果能够消除过多的氧化自由基,就能预防许多由自由基引起的相关的疾病。如常见的癌症、动脉硬化、糖尿病、白内障、心血管病、老年痴呆、关节炎等,这些疾病都被认为与自由基相关。抗氧化物质能有效抑制自由基的氧化反应,在临床和医疗界广泛应用。
3.然而,人工合成的抗氧化剂如果长期用于人体治疗的话,带给人们的毒副作用会极大影响人们的身体健康,这与当前人们所倡导的养生、保健等观念相冲突,人体的抗氧化物质有自身合成的,也有由食物供给的,长期缺硒会造成人体免疫力降低,使得一些病毒及病菌入侵机体而诱发克山病、大骨节病等。依据who推荐成年人硒的摄入量为55μg
·
d-1
,低于40μg
·
d-1
即被判定为硒摄入不足。根据我国13省份普查结果显示,超过7亿人均存在硒摄入不足的情况。
4.食物是人们摄入硒的重要来源。因此,开发富硒产品,通过日常饮食提高硒摄入量,对提高缺硒地区的居民群体健康水平具有重要意义。随着社会经济的发展和人们健康意识的增强,作为功能性食品代表的富硒产品越来越受到人们的欢迎,硒资源的开发利用迎来了前所未有的热潮。
技术实现要素:
5.针对上述的不足,本发明的目的是提供一种药食同源的富硒复合固体饮料及其制备方法,以七种药食同源的原料制备的到具有抗氧化、消炎镇痛功效的富硒复合固体饮料,制备工艺简单、食用方便、毒副作用小。
6.为实现上述目的,本发明采取以下技术方案:
7.一种药食同源的富硒复合固体饮料,所述富硒复合固体饮料按照重量份数包括有以下原料:
8.富硒苦瓜6~15份、富硒黄精6~15份、富硒葛根6~15份、富硒木瓜15~25份、富硒甘蓝6~15份、富硒西兰花6~15份、绿茶10~20份。
9.进一步地,所述富硒复合固体饮料按照重量份数包括有以下原料:
10.富硒苦瓜6份、富硒黄精8份、富硒葛根10份、富硒木瓜10份、富硒甘蓝10份、富硒西兰花15份、绿茶20份。
11.进一步地,所述的药食同源的富硒复合固体饮料的制备方法,其特征在于,具体步骤如下:
12.1)称重:按照重量份数称取洗净烘干的富硒苦瓜、富硒黄精、富硒葛根、富硒木瓜、富硒甘蓝、富硒西兰花、绿茶;
13.2)原料粉碎:在无菌室中,将步骤1)中称取的富硒苦瓜、富硒黄精、富硒葛根、富硒木瓜、富硒甘蓝、富硒西兰花、绿茶分别粉碎成小粉粒,过100-200目筛,得到各原料的混合粉末;
14.3)提取:在步骤2)的混合粉末中加入95%食用乙醇浸泡提取8h,提取三次后合并滤液,用100目的滤袋装离心机过滤,得到滤液ⅰ;
15.4)脱色:将步骤3)中的滤液ⅰ用活性碳柱进行脱色处理,得到滤液ⅱ;
16.5)浓缩:将步骤4)中的滤液ⅱ抽真空浓缩至相对密度为1.08~1.22,然后放置室温无菌状态下冷却,得到提取物干膏;
17.6)干膏粉碎:将步骤5)中的提取物干膏粉碎,过100目筛,得到固体粉末,即为富硒复合固体饮料。
18.进一步地,步骤3)中所述95%食用乙醇的用量为95%食用乙醇质量:混合粉末质量=12:1;
19.步骤5)中所述真空浓缩的条件为温度70℃,真空度-0.06mpa。
20.本发明所述的药食同源的富硒复合固体饮料,配方搭配科学,各成分之间具有协同增效的作用,下面结合配方成分对本发明的技术方案做进一步的说明:
21.本发明中包括的富硒苦瓜、富硒黄精、富硒葛根、富硒木瓜、富硒甘蓝、富硒西兰花、绿茶等药食同源成分,具有抗氧化、消炎和等作用。
22.富硒苦瓜:性甘味苦寒凉,活性成分包括三萜类、生物碱类、甾体类化合物和有机酸类等。
23.富硒黄精:从育苗到采收生产周期为七年,性味甘平,黄精富含甾体皂苷、黄精多糖和黄精低聚糖,能补气养阴,健脾润肺,具有增强免疫功能、抗衰老、耐缺氧、抗疲劳等功用。
24.富硒葛根:从育苗到采收生产周期为三年,是我国传统的大宗中药材和药食两用植物资源,富含淀粉及异黄酮类物质,异黄酮类物质能够降低血管阻力、改善脑及冠脉循环,降低心肌耗氧等,因此具有解肌退热、生津、透疹、升阳止咳等功效。
25.富硒木瓜:从育苗到采收生产周期为五年,性温味酸,平肝和胃,具有很强的抗氧化能力,帮助机体修复组织,消除有毒物质,增强人体免疫力。
26.富硒甘蓝:具有丰富的抗氧化成分,可增强体内酵素系统的解毒能力,中和毒素对dna产生的伤害,也可预防癌细胞转移。
27.富硒西兰花:富含维生素c,为强抗氧化成分,能识别并清除体内的自由基,保证人体健康和延缓衰老,具有美容养颜、抗衰老、降压、增强机体免疫力等作用。
28.绿茶:含有多酚类物质以及儿茶素的氧化聚合成分不仅能够增加该复合物的抗氧
化作用,还能调和香气。
29.采用以上方案,本发明具有如下优点:
30.1、本发明依据药食同源理论,将富硒苦瓜、富硒黄精、富硒葛根、富硒木瓜、富硒甘蓝、富硒西兰花和绿茶这七味药食同源物品进行配伍组方,同时结合现代制备工艺,经提取、过滤、脱色、浓缩、粉碎和包装制得固体粉末即富硒复合固体饮料,本发明得到的固体粉末外观呈淡黄色,形态疏松,无结块,在70℃以上热水中可迅速溶解分散,液体呈淡黄色,静置后无沉淀和分层,保留了原料的香气,味甜、微酸,无防腐剂、添加剂,食用安全,产品质量符合国家标准,且体积小,携带方便,符合现代人群的快节奏生活需求。此外,本技术中的富硒复合固体饮料制备工艺简单,原料来源广泛、设备要求相对较低,便于大规模工业化生产。
31.2、本发明中富硒复合固体饮料在制备过程中通过食用乙醇浸提,能够使组方中有效成分充分释放,提高生物活性,使该固体粉末具有更好的抗氧化、消炎镇痛的效果。
32.3、本发明中的七种药食同源物品,均是含糖量低的物品,适应市场对产品的低糖需求,均含有丰富的抗氧化活性物质。通过体外实验评价,本发明工艺制备的富硒复合固体饮料具有明显的抗氧化、消炎镇痛活性。
33.4、本发明中富硒复合固体饮料每袋装量为10g,开袋倒入水杯中,加入70℃热水200ml,搅拌待完全溶解,即可饮用,携带和食用方便。
34.本发明的其他优点、目标和特征在某种程度上将在随后的说明书中进行阐述,并且在某种程度上,基于对下文的考察研究对本领域技术人员而言将是显而易见的,或者可以从本发明的实践中得到教导。本发明的目标和其他优点可以通过下面的说明书来实现和获得。
35.说明书附图
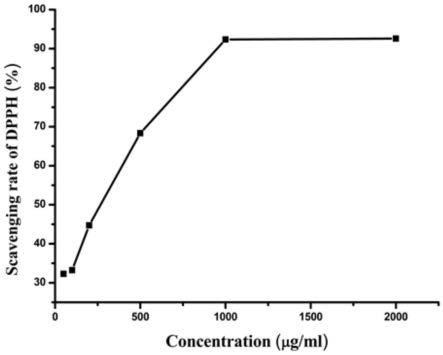
36.图1为富硒复合固体饮料的dpph自由基清除能力图。
37.图2为富硒复合固体饮料对h2o2诱导的lo2细胞形态图。
38.图3为富硒复合固体饮料的活性氧荧光强度测定图。
39.图4为富硒复方固体饮料复合物的醋酸扭体作用图。
具体实施方式
40.下面结合附图和实施例对本发明的进行详细的描述,但实施例并不对本发明作任何形式的限定,除非特别说明,本发明所涉及的试剂、方法和设备为本技术领域常规试剂、方法和设备。
41.实施例1:一种药食同源的富硒复合固体饮料的制备
42.具体步骤如下:
43.1)称重:按照重量份数称取洗净烘干原料,即富硒苦瓜6份、富硒黄精10份、富硒葛根10份、富硒木瓜15份、富硒甘蓝8份、富硒西兰花8份、绿茶15份;
44.2)原料粉碎:在无菌室中,将步骤1)中称取的原料分别粉碎成小粉粒,过100-200目筛,得到各原料的混合粉末,保持无菌及洁净状态;
45.3)提取:在步骤2)的混合粉末中加入95%食用乙醇浸泡提取8h,乙醇的用量为95%食用乙醇质量:混合粉末质量=12:1,提取三次后合并滤液,用100目的滤袋装离心机
过滤,得到滤液ⅰ;
46.4)脱色:将步骤3)中的滤液ⅰ用活性碳柱进行脱色处理,进一步过滤,得到滤液ⅱ;
47.5)浓缩:将步骤4)中的滤液ⅱ抽真空浓缩至相对密度为1.12,浓缩的条件为,温度70℃,真空度-0.06mpa,然后放置室温无菌状态下冷却,得到提取物干膏;
48.6)干膏粉碎:将步骤5)中的提取物干膏粉碎,过100目筛,得到固体粉末,即为富硒复合固体饮料;
49.7)包装:用食用级塑料,在真空条件下将步骤6)中的固体粉末进行分包装,每袋包装为10g。
50.实施例2:一种药食同源的富硒复合固体饮料的制备
51.具体步骤如下:
52.1)称重:按照重量份数称取洗净烘干原料,即富硒苦瓜6份、富硒黄精8份、富硒葛根10份、富硒木瓜10份、富硒甘蓝10份、富硒西兰花15份、绿茶20份;
53.2)原料粉碎:在无菌室中,将步骤1)中称取的原料分别粉碎成小粉粒,过100-200目筛,得到各原料的混合粉末,保持无菌及洁净状态;
54.3)提取:在步骤2)的混合粉末中加入95%食用乙醇浸泡提取8h,乙醇的用量为95%食用乙醇质量:混合粉末质量=12:1,提取三次后合并滤液,用100目的滤袋装离心机过滤,得到滤液ⅰ;
55.4)脱色:将步骤3)中的滤液ⅰ用活性碳柱进行脱色处理,进一步过滤,得到滤液ⅱ;
56.5)浓缩:将步骤4)中的滤液ⅱ抽真空浓缩至相对密度为1.12,浓缩的条件为,温度70℃,真空度-0.06mpa,然后放置室温无菌状态下冷却,得到提取物干膏;
57.6)干膏粉碎:将步骤5)中的提取物干膏粉碎,过100目筛,得到固体粉末,即为富硒复合固体饮料;
58.7)包装:用食用级塑料,在真空条件下将步骤6)中的固体粉末进行分包装,每袋包装为10g。
59.实施例3:富硒复合固体饮料的质量评价
60.1、实验材料
61.以实施例2的条件下制得的富硒复合固体饮料。
62.2、实验方法
63.外观评价:取实施例2中的富硒复合固体饮料肉眼观察;
64.溶化性的测定:取实施例2中的富硒复合固体饮料粉末10g,加入70℃热水200ml,用玻璃棒搅拌3min,立即观察,可溶粉末应全部溶解或者轻微浑浊;
65.溶解时间的测定:取实施例2中的富硒复合固体饮料粉末10g,加入水温为25℃的100ml水中,用玻璃棒轻轻搅拌,记录完全溶解所需要的时间。
66.3、实验结果
67.富硒复合固体饮料外观呈淡黄色,形态疏松,无结块现象,粉末粗细均匀,粒度适宜,色泽良好,总体观感良好;
68.在测定溶化性时,在70℃以上热水中可迅速的全部溶解分散,测定的溶解时间应小于40s,溶液颜色呈浅黄至黄色,静置后无沉淀、分层现象,具有原料的香气,味甜、微酸,食用安全。
69.实施例4:富硒复合固体饮料的细菌检测
70.1、实验材料
71.以实施例2的条件下制得的富硒复合固体饮料。
72.2、实验方法
73.参考国标gb 47889.2-2010菌落总数测定法测定,平板培养法。取10g实施例2的条件下制得的富硒复合固体饮料装入有100ml生理盐水的无菌均质袋中,制成1:10的样品溶液,取1:10的样品溶液1ml,沿管壁缓慢注入装有9ml生理盐水的无菌试管中,注意吸管不要触碰稀释液面,振摇试管混合均匀,制成1:10的样品溶液,取1:100的样品溶液1ml,沿管壁缓慢注入装有9ml生理盐水的无菌试管中,振摇试管混合均匀,制成1:1000的样品溶液。根据每个活的细菌能长出一个菌落的原理设计,分别吸取1ml的1:10、1:100、1:1000的样品溶液于无菌平板中,每个浓度平行做3个平板。同时,吸取1ml的空白稀释液加入3个无菌平板中作为空白对照,吸取1ml混合标准菌液加入3个无菌平板中作为阳性对照。加入琼脂培养基,并混合均匀,在37℃下培养48h,根据培养出的菌落数,计算活菌数。
74.3、实验结果
75.富硒复合固体饮料的菌落总数(cfu/g)≤1000,大肠菌群(mpn/g)≤0.4,霉菌(cfu/g)≤25,酵母菌(cfu/g)≤25,沙门氏菌、志贺氏菌、金黄色葡萄球菌均末检出。
76.实施例5:富硒复合固体饮料的dpph自由基清除力的测定
77.1、实验材料
78.以实施例2的条件下制得的富硒复合固体饮料。
79.2、实验方法
80.精密称取富硒复合固体饮料粉末样品,用无水乙醇配置成浓度梯度为50μg/ml、100μg/ml、200μg/ml、500μg/ml、1000μg/ml、2000μg/ml的溶液,取100μl一定浓度的样品溶液,加入100μl 0.2m dpph溶液、立即混匀,室温避光放置30min,波长517nm处测定吸光度值。光值越小,表明自由基清除能力越强。使用无水乙醇代替样品溶液为空白组,用维生素c作阳性对照,每个样品三个重复,按如下公式计算清除率:
81.清除率(%)=[1-(a
s-a
sb
)/ab]
×
100
[0082]ab
为空白吸光度,as为dpph溶液加入样品后的吸光度,a
sb
为样品本身的吸光度(不加dpph溶液)。
[0083]
3、实验结果
[0084]
经实验统计,本发明中的复合固体饮料的各剂量组dpph自由基清除能力见表1。结果表明,阳性对照维生素c在浓度为2.5μg/ml时,dpph清除率已达90%以上。复合固体饮料的样品在50μg/ml时的dpph清除率为32.28%,在50~1000μg/ml时,dpph清除率随着样品浓度的升高而升高。在1000~2000μg/ml间,dpph清除率稳定在90%以上。表明富硒复合固体饮料有一定的dpph自由基清除能力,并呈现一定的量效关系,说明本发明的富硒复合固体饮料有很好的抗氧化作用。
[0085]
表1复合固体饮料的各剂量组dpph自由基清除率表
[0086][0087]
实施例6:富硒复合固体饮料对h2o2诱导lo2细胞形态的影响
[0088]
1、实验材料
[0089]
以实施例2的条件下制得的富硒复合固体饮料。
[0090]
2、实验方法
[0091]
实验分组情况:空白对照组、h2o2造模组、nac阳性对照组、待测定样品组。待测定样品浓度为50μg/ml、30μg/ml、20μg/ml、15μg/ml、10μg/ml、5μg/ml;
[0092]
取处于对数生长期且生长状态良好的lo2细胞,消化计数后接种到24孔板中,每孔中的细胞个数为0.4
×
105个,加rpmi-1640细胞完全培养基至500μl,放置于细胞培养箱中培养24h;
[0093]
用培养基稀释样品储备液至待测定样品的浓度(50、30、20、15、10和5μg/ml),每孔加入500μl样品,24孔板继续放置在细胞培养箱中培养24h(空白对照组、h2o2造模组只加培养基;nac阳性对照组加4mm nac);
[0094]
去除药物和nac,pbs洗两遍,所有组加h2o2作用30min,弃掉h2o2,pbs洗两遍,每孔加10μm dcfh-da染色30min,室温下避光,每孔用300μl pbs洗2次,吸去pbs后在荧光显微镜下拍照(放大200倍)。
[0095]
3、实验结果
[0096]
结果如图2所示,细胞用过h2o2(1mm)造模时处理30min,h2o2造模组的荧光强度明显强于空白对照组,说明造模成功。各个待测定样品组的荧光强度均明显低于造模组,而且与空白对照组和nac阳性对照组的荧光强度接近,说明50μg/ml、30μg/ml、20μg/ml、15μg/ml、10μg/ml、5μg/ml的富硒复合固体饮料具有明显的抗氧化活性。
[0097]
实施例7:富硒复合固体饮料对h2o2诱导lo2细胞内活性氧的影响
[0098]
1、实验材料
[0099]
以实施例2的条件下制得的富硒复合固体饮料
[0100]
2、实验方法
[0101]
实验分组情况:空白对照组、h2o2造模组、nac阳性对照组、待测定样品组。待测定样
品浓度为20μg/ml、15μg/ml、10μg/ml、5μg/ml;
[0102]
荧光酶标仪检测细胞内活性氧荧光强度:
[0103]
取处于对数生长期且生长状态良好的lo2细胞,消化计数后接种到24孔板中,每孔中的细胞个数为0.4
×
105个,培养24h;
[0104]
用培养基稀释样品储备液至待测定样品的浓度,每孔加入500μl样品,24孔板继续放置在细胞培养箱中培养24h(空白对照组、h2o2造模组只加培养基;nac阳性对照组加4mm nac);
[0105]
去除药物及nac,pbs洗两遍,用dcfh-da染料(终浓度10μm)染色30min后,pbs洗2次;
[0106]
24孔板中每孔加入400μl裂解液(dmso:pbs=9:1),室温下避光摇床孵育10min;
[0107]
将24孔板中的裂解液分别加入至黑框透明底的96孔板的3个孔中的,每孔100μl;
[0108]
采用荧光酶标仪测定荧光强度,条件为激发光波长488nm,发射光波长520nm。
[0109]
3、实验结果
[0110]
结果如图3所示,细胞用过h2o2(1mm)造模时处理30min,h2o2造模组的荧光强度明显强于空白对照组,说明造模成功。各个待测定样品组的荧光强度均明显低于造模组,而且与空白对照组和nac阳性对照组的荧光强度接近,说明20μg/ml、15μg/ml、10μg/ml、5μg/ml的富硒复合固体饮料能逆转h2o2诱导lo2细胞内ros升高,具有明显的抗氧化活性
[0111]
实施例8:富硒复合固体饮料的抗炎镇痛活性
[0112]
1、实验材料
[0113]
以实施例1和2的条件下制得的富硒复合固体饮料。
[0114]
2、实验方法
[0115]
实验动物:
[0116]
km小鼠,雌雄各半,清洁级标准,共100只,体重约18-22g,随机分成十组,每组10只。设空白对照组(0.9% nacl溶液),阳性对照组(吗啡溶液)和复合固体饮料的高中低三个剂量组。上述实施例1和2中所得的复合固体饮料的三个的剂量组分别标记为a1、a2、a3、b1、b2和b3;
[0117]
样品来源与配制:
[0118]
高剂量组(a1和b1):复方固体饮料颗粒,加生理盐水稀释,相当于生药含量25mg/ml,给药剂量相当于250mg/kg。
[0119]
中剂量组(a2和b2):复方固体饮料颗粒,加生理盐水稀释,相当于生药含量5mg/ml,给药剂量相当于50mg/kg。
[0120]
低剂量组(a3和b3):复方固体饮料颗粒,加生理盐水稀释,相当于生药含量1mg/ml,给药剂量相当于10mg/kg。
[0121]
阳性对照组(m1~m4):阳性药为盐酸吗啡溶液,设置浓度梯度分别为5mg/kg、1mg/kg、0.2mg/kg和0.04mg/kg。
[0122]
醋酸诱导的小鼠扭体实验:
[0123]
实验前小鼠禁食不禁水12h,然后各组小鼠按0.7ml/20g体重灌胃给药,其中模型对照组给等体积蒸馏水。给药后30min,腹腔注射0.6%醋酸溶液0.2ml,观察记录30min内扭体次数,并计算镇痛率。
[0124]
小鼠在疼痛模型下会表现出比较明显的扭体反应,而具有镇痛效果的活性成分则会减少扭体次数。小鼠出现腹部内凹,躯干与后肢伸张,臀部高起等行为,称为一次完整的扭体反应。
[0125]
空白对照组为0.9%nacl溶液,阳性药组为吗啡溶液。将每只小鼠单独放在铁网笼里独立观察,腹腔注射不同剂量的待测定样品溶液30分钟后,腹腔注射0.8%v/v的醋酸溶液(0.1ml/10g),记录30分钟内小鼠的扭体次数,每一组实验采用10只随机的小鼠进行重复性实验。
[0126]
镇痛率=[(空白对照组扭体次数-给药组扭体次数)/空白对照组扭体次数]
×
100%
[0127]
3、实验结果
[0128]
结果如图4和表2所示,用graphpad prism统计各实验组数据,在醋酸诱导的小鼠扭体实验中,与正常模型组相比较,实施例1和实施例2中得到的富硒复方固体饮料各剂量组均具有明显的镇痛作用。其中该复方固体的高剂量组的效果与阳性对照组吗啡的效果相当,实施例1的高剂量组镇痛抑制率为92.3%,实施例2的高剂量组镇痛抑制率为97.7%,说明该富硒复合固体饮料具有明显的消炎镇痛作用。
[0129]
表1各实验组镇痛实验的结果表(x
±
s,n=10)
[0130]
组别给药剂量扭体次数抑制率模型组0.1ml/10g43.1
±
1.5-阳性对照组m15mg/kg0***100%阳性对照组m21mg/kg9.4
±
1.6***78.2%阳性对照组m30.2mg/kg13.8
±
1.9***68.1%阳性对照组m40.04mg/kg19.8
±
2.2***54.1%复方高剂量组a1250mg/kg3.3
±
2.1***92.3%复方中剂量组a250mg/kg10.5
±
0.7**75.6%复方低剂量组a310mg/kg14.0
±
2.2***67.5%复方高剂量组b1250mg/kg1.0
±
0.0***97.7%复方中剂量组b250mg/kg6.4
±
0.9***85.2%复方低剂量组b310mg/kg11.5
±
3.6**73.3%
[0131]
与模型组比较,***p《0.001,**p《0.01。
[0132]
最后用说明的是:以上所述仅为本发明的优选实施例而已,并不用于限制本发明,尽管参照前述实施例对本发明进行了详细的说明,对于本领域的技术人员来说,其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行同等替换。凡在本发明的精神和原则之内,所作的任何修改、同等替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1