咖啡酸及其酯的用途的制作方法与工艺
本发明涉及药物化学领域,具体而言,涉及咖啡酸及其酯的用途。
背景技术:
流感是一类集传播性、致病性、变异性较强,波及范围较广的流行性疾病,由不同亚型病毒株感染引起,主要分为A型、B型和C型三大类,尤以A型为主。该类病毒RNA聚合酶PA亚基的N端蛋白(PAN)在参与稳定PA结构、核酸内切酶活性、帽状结构结合、启动子结合等功能方面起关键作用,同时因其在A型、B型、C型毒株RNA序列中的高度保守性,目前已成为研发广谱型流感病毒抑制剂的一个重要靶点。其中A型H1N1、H5N1威胁较大,H1N1可感染宿主范围较广,H5N1虽不能由禽类直接传播至人类,但其危害性最为严重。近几年来,由H5N1亚型禽流感病毒引起的疫情广泛传播,对人类的健康造成重大威胁。流感病毒基因组含有8个RNA片段,已知可以编码11种病毒蛋白质。其中,由PA、PB1和PB2等3个亚基组成的聚合酶复合体是负责病毒基因组RNA复制以及病毒mRNA转录的主要组分和维持病毒生命周期的至关重要的分子机器,使之成为抗流感病毒药物设计潜在的重要靶点。PAN蛋白是流感病毒聚合酶其中一个亚基PA的N端,是有256个氨基酸残基构成的。流感病毒聚合酶是高度保守的,根据已有的大量报导,PA亚基被发现不但参与病毒复制过程,而且还参与病毒RNA转录、核酸内切酶的活性、具有蛋白酶活性以及参与病毒粒子组装等多种病毒活动过程。饶子和在CN101792745A中公开一种流感病毒聚合酶亚基PA氨基端PAN的晶体三维结构,还提供对流感病毒聚合酶亚基PA氨基端PAN的表达、纯化和结晶的方法;以及PAN的晶体结构及晶体结构在药物筛选及药物设计方面的应用。由于病毒的不断变异,开发新型抗流感药物成为各国极为迫切的重大任务。通过与流感病毒密切相关的蛋白质的抑制剂的发掘,对开发抗流感病毒药物具有重要价值。PAN作为一个全新的、热门的研究广谱型流感病毒抑制剂的靶点,目前针对该靶点的抑制剂较少,且无成品上市药物。已报道的天然产物源抑制剂也是屈指可数的。现有的一些抗流感复方药物作用靶点不明确,作用成分复杂繁多。而现有用于治疗流感的药物如金刚脘胺类,达菲等,目前在临床应用中也存在一定的耐药性。天然产物又称次级代谢产物(SecondaryMetabolites),具有结构的多样性和生物活性的多样性。天然产物及其衍生物在以往的疾病治疗中发挥了无可限量的作用,也是当今药物研发过程中最具潜力的资源之一。现在对中药等传统药物、海洋生物以及微生物代谢过程中的天然产物研究方兴未艾,每年都会有大量结构新颖的化合物被发现提供出来,这些新颖化合物是合成方法所无法实现的药物和药物先导化合物的重要源泉,在新药和先导化合物的发现中起着重要作用。对于天然产物尤其是来源于中药等的天然产物的研究是很有必要的,因为中药在我国已有数千年应用的历史,是一个宝贵的天然产物化合物库,因此从中药来源的天然产物中进行重要病毒或重要疾病相关靶蛋白抑制剂的筛选是很有必要的。天然产物及其衍生物被用于治疗各种疾病由来已久。与合成药物相比而言,天然产物具有结构多样性,功能多样性,副作用低等优点,其中传统中药更是历经几千年医疗验证,因此从中筛选结构新颖,作用方式独特的PAN抑制剂具有很大意义。咖啡酸(CaffeicAcid)是一种从中药中提取的天然产物,它是5-脂氧酶(5-1ipoxygenase,5-LO)非竞争性抑制剂,通过选择性抑制5-LO活性从而减少白三烯的生物合成,具有抗氧化和抗炎症等活性。它是植物代谢过程中是一个重要的合成子,参与糖、糖苷等的衍生化过程,从而产生许多天然的咖啡酸衍生物,例如天然产物乌金苷、1,3-二咖啡酰基奎宁酸、连翘酯苷A、连翘酯苷B等。咖啡酸衍生物具有广泛的生物活性。连晓媛在CN101543488中公开含有咖啡酸3,4-二羟基苯乙酯的药物可用于抗肿瘤、增效减毒、抗肿瘤放化疗的毒性反应及肿瘤辅助治疗,亦用于原发性血小板减少性紫癜及继发性血小板减少性紫癜,并可用于治疗常见细菌性感染。又在CN101502506中公开咖啡酸3,4-二羟基苯乙酯可用来制备抗肿瘤药物,对消化系统肿瘤,肺癌,乳腺癌,卵巢癌,前列腺癌,中枢神经系统肿瘤,黑色素瘤、白血病、胃癌,结肠癌,肝癌或者胰腺癌均有效。B·B·阿加尔瓦尔在CN1495254中公开咖啡酸苯乙酯的两种类似物可阻断NF-κB的活化。张艺在CN101966172A中公开咖啡酸及其衍生物在制备脑神经保护剂的药物中的用途。咖啡酸为原料结构修饰的咖啡酸甲酯、咖啡酸乙酯、3,4-二乙酰基咖啡酸均有明显脑神经保护活性,且咖啡酸甲酯和3,4-二乙酰基咖啡酸均可透过血脑屏障,直接到达靶器官,是较理想的脑神经保护剂候选药物。唐于平在CN101585770A中公开咖啡酸双酯类化合物比咖啡酸和乙酰水杨酸都具有更好的抑制血小板聚集的作用,咖啡酸和乙酰水杨酸缩合后得到的咖啡酸双酯类化合物能起到协同增效的作用,临床用量可更低,小量反应降低。此外,钟慧等在CN102050849A中公开连翘酯苷A具有清热解毒、预防急慢性肝损伤作用。玄振玉在CN101757006A中公开连翘酯苷A在制备治疗乙型肝炎药物中的用途,体外实验表明连翘酯苷A能有效抑制乙肝抗原和乙肝病毒。陆伟根等在CN101919869A中公开一种连翘酯苷A药物组合物,发明了一种含质量比0.05∶10~0.5∶10的连翘酯苷A,与油性基质和/或含油性基质的植物提取物,该组合物在胃肠道中吸收较好,血药浓度较高,口服生物利用度较高。张立伟等在CN101816667A中公开连翘酯苷A在制备防治心脑血管疾病中的应用,指出通过连翘酯苷A对ADP诱导大鼠体外血小板凝集的影响,对大鼠血浆凝血酶原时间(PT)的影响以及大鼠血浆凝血酶时间(TT)的影响证明连翘酯苷A具有抑制血小板凝集作用,同时也具有抗凝血作用,因此可用于制备防治心脑血管疾病的药物和作为食品添加剂用于制备防治心脑血管疾病的功能性食品。蒋王林等则在CN101496809A中公开连翘酯苷B在治疗或预防肝病的药物中的应用,指出连翘酯苷B具有抗急、慢性肝损伤及肝纤维化作用。他们又在CN101919868A中公开连翘酯苷B能显著降低急性心肌缺血大鼠肢体导联心电图J点的升高,减少缺血面积,可用于制备治疗或预防冠心病、心绞痛或心肌梗塞的药物。虽然咖啡酸及其天然源衍生物包括乌金苷、1,3-二咖啡酰基奎宁酸、连翘酯苷A、连翘酯苷B等在抗炎、抗肿瘤、抗肝损伤、保护脑神经及抗血栓等方面有较强药理作用,但在作为流感PAN抑制剂方面的研究尚无报道。
技术实现要素:
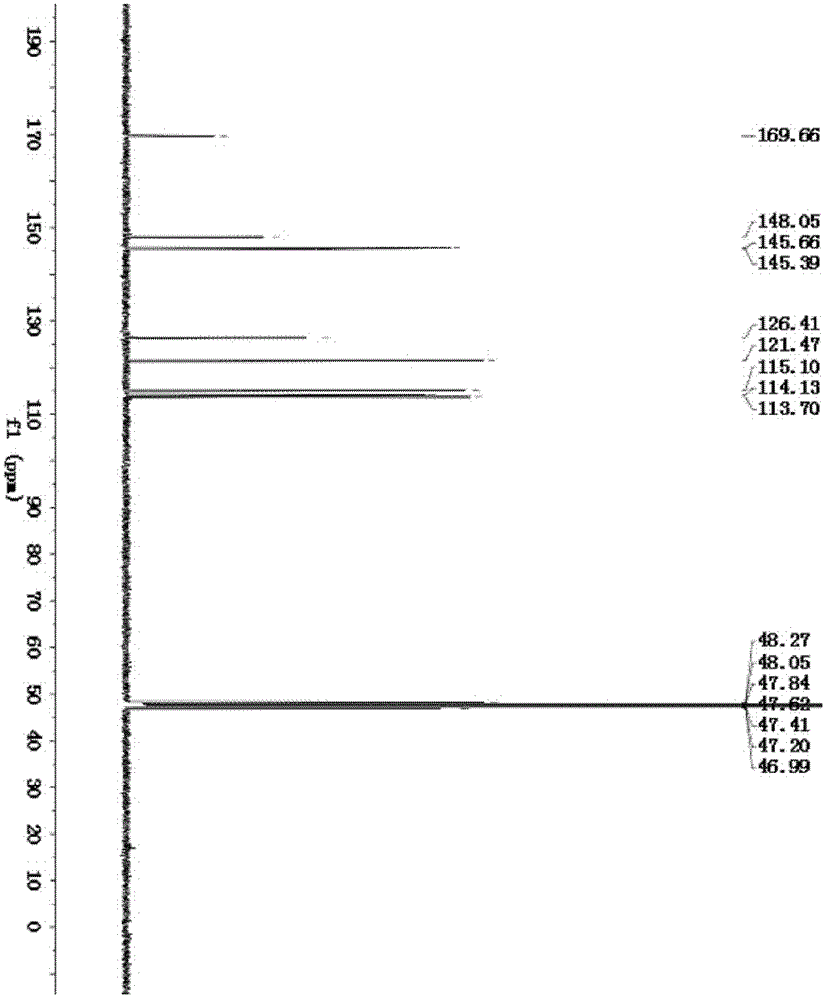
本发明选取流感病毒H5N1亚型PA亚基N端核酸序列所表达的蛋白(PAN)作为靶标蛋白,采用体外酶活筛选评价方法对咖啡酸及其酯进行抗H5N1病毒活性测试,从而提供了咖啡酸及其酯在制备抑制流感病毒的药物方面的新用途,即在制药中的新应用。具体而言,本发明涉及咖啡酸及其酯在制备抑制H5N1流感病毒的药物方面的用途。涉及咖啡酸及其酯在制备抑制H5N1流感病毒RNA聚合酶的药物方面的用途。涉及咖啡酸及其酯在制备抑制H5N1流感病毒RNA聚合酶亚基PA的药物方面的用途。还涉及咖啡酸及其酯在制备抑制H5N1流感病毒RNA聚合酶亚基PA的N端PAN蛋白的药物方面的用途。其中咖啡酸的酯是咖啡酸与多元醇形成的羧酸酯,优选咖啡酸的糖苷酯,特别优选咖啡酸的六元糖苷酯。其中所述咖啡酸及其酯优选咖啡酸、乌金苷、1,3-二咖啡酰基奎宁酸、连翘酯苷A、连翘酯苷B等化合物。本发明提供的咖啡酸及其酯类化合物对流感PAN有很好的抑制活性,其中咖啡酸、乌金苷、1,3-二咖啡酰基奎宁酸、连翘酯苷A和连翘酯苷B的IC50值分别为69.6μM、136μM、81.9μM、388μM和352μM。附图说明图1示出咖啡酸的1HNMR图。图2示出咖啡酸的13CNMR图。图3示出连翘酯苷A的1HNMR图。图4示出连翘酯苷A的13CNMR图。图5示出连翘酯苷A的DEPT图。图6示出连翘酯苷A的HMBC图。图7示出连翘酯苷B的1HNMR图。图8示出连翘酯苷B的13CNMR图。图9示出连翘酯苷B的DEPT图。图10示出咖啡酸的IC50曲线图。具体实施方式下面将详细描述本发明的具体实施方式,这仅用于解释本发明,而不能解释为对本发明的限制。实施例1咖啡酸、连翘酯苷A、连翘酯苷B的制备方法咖啡酸、连翘酯苷A、连翘酯苷B从连翘成熟果实(Forsythiasuspensa(Thunb.)vahl)中分离纯化得到,HPLC分析含量>95.0%。咖啡酸、连翘酯苷A、连翘酯苷B的提取分离方法:1)原药材的预处理:本发明选取中药连翘成熟果实(Forsythiasuspensa(Thunb.)vahl)为实验材料,原药材总重20Kg,其中2Kg留样,将剩余部分用95%乙醇进行回流提取,料药比例为5∶1(L/Kg),每次提取4h,共计提取三次。将提取液经粗纱布过滤后减压蒸干得浸膏,取其中1Kg用于后续分离纯化活性评价等方面的实验研究。向浸膏中加入适量双蒸水并用超声波将其充分溶解,利用有机溶剂对其水溶液进行萃取。按极性由小到大依次利用石油醚、乙酸乙酯、正丁醇进行萃取。2)目标成分分离本方案是依据活性筛选结果而制定。活性筛选结果显示活性部位主要集中在乙酸乙酯相,所采取的分离方案为传统色谱纯化方法。将乙酸乙酯相浸膏用少许无水乙醇溶解后加适量200~300目硅胶进行拌样,常温下晾干并研磨成粉末状。湿法装柱干法上样,洗脱体系为二氯甲烷/甲醇,薄层色谱(TLC)检视后对流份合并,得8个组分即A、B、C、D、E、F、G、H。进一步活性检测结果显示活性部位为D、G、H。D部分:少许无水甲醇溶解后,用200~300目硅胶按质量比1∶1进行拌样。湿法装柱干法上样,洗脱体系为石油醚/乙酸乙酯/醋酸,TLC(石油醚∶乙酸乙酯∶醋酸=40∶10∶1)检视后合并流份,得4个组分即D1、D2、D3、D4。其中D3为纯净物,土黄色粉末。经H-NMR、13C-NMR鉴定为咖啡酸。G部分:少许无水甲醇溶解后,用200~300目硅胶按质量比1∶1进行拌样。湿法装柱干法上样,洗脱体系为二氯甲烷/甲醇/醋酸,TLC(氯仿∶甲醇∶醋酸=20∶5∶1)检视后合并流份,得5个组分即G1、G2、G3、G4、G5。其中G4活性最强。组分G4:红褐色粘稠状。少许无水甲醇溶解后,用200~300目硅胶按质量比1∶1进行拌样。湿法装柱干法上样,洗脱体系为氯仿/甲醇/醋酸,TLC(氯仿∶甲醇∶醋酸=20∶5∶1)检视后合并流份,得6个组分即G1、G2、G3、G4、G5、G6。其中G6为纯净物,糖浆状。经H-NMR、13C-NMR、HMBC和ESI-MS鉴定为连翘酯苷A。体外酶活测试发现该成分活性良好。H部分:红褐色粘稠状。少许无水甲醇溶解后,用200~300目硅胶按质量比1∶1进行拌样。湿法装柱干法上样,洗脱体系为氯仿/甲醇/醋酸,TLC(氯仿∶甲醇∶醋酸=15∶5∶1)检视后合并流份,得3个组分即H1、H2、H3。其中组分H2活性较强。组分H2经凝胶SephadexLH-20(甲醇)反复纯化后得一纯净物,褐色糖浆状。经H-NMR、13C-NMR、DEPT鉴定为连翘酯苷B。咖啡酸的核磁数据如下:1HNMR:(CD3OD,400MHz):δ7.55(1H,d,J=16.0Hz,H-7),7.06(1H,d,J=2.0Hz,H-2),6.95(1H,dd,J=8.0Hz,2.0Hz,H-6),6.80(1H,d,J=8.0Hz,H-5),6.24(1H,d,J=16.0Hz,H-8);咖啡酸的1HNMR谱图见附图1。13CNMR(CD3OD,100MHz):δ169.66(C-9),148.05(C-4),145.66(C-3),145.39(C-7),126.41(C-1),121.47(C-6),115.10(C-5),114.12(C-8),113.70(C-2)。咖啡酸的13CNMR谱图见附图2。所获核磁数据与文献(高燕,蔡丽等,甘肃醉鱼草化学成分研究(II),中药材,2007,6,667-668)报道一致。连翘酯苷A的核磁数据如下:1HNMR:(CD3OD,400MHz):δ7.61(1H,d,J=16Hz,H-7″′),7.08(1H,d,J=1.6Hz,H-2″′),6.97(1H,dd,J=8.0Hz,1.6Hz,H-6),6.80(1H,d,J=8.0Hz,H-5″′),6.71(1H,s,H-2),6.70(1H,d,J=8.0Hz,H-5),6.58(1H,dd,J=8.0Hz,1.6Hz,H-6″′),6.35(1H,d,J=15.6Hz,H-8″′),5.07(1H,t,J=9.2Hz,H-4′),4.78(1H,s,H-1″),4.43(1H,d,J=8.0Hz,H-1′),4.01(1H,m,H-8),3.72(1H,m,H-7b),4.01(1H,m,H-7a),3.72(1H,m,H-7b),3.88(1H,d,J=1.6Hz,H-2′),3.73(1H,d,J=13.0Hz,H-6′a),3.42(1H,dd,J=13.0Hz,7.5Hz,H-6′b),2.81(2H,m,H-7),1.29(3H,d,J=6.4Hz,H-6″)。翘酯苷A的1HNMR谱图见附图3。13CNMR(CD3OD,100MHz):δ130.1(C-1),115.7(C-2),130.0(C-3),143.3(C-4),121.6(C-5),115.5(C-6),35.5(C-7),70.9(C-8),103.0(C-1′),72.2(C-2′),77.5(C-3′),68.6(C-4′),66.4(C-6′),100.8(C-1″),70.9(C-2″),68.6(C-3″),68.4(C-4″),72.6(C-5″),16.68(C-6″),148.1(C-1″′),113.8(C-2″′),145.6(C-3″′),144.7(C-4″′),119.9(C-5″′),126.5(C-6″′),145.4(C-7″′),114.0(C-8″′),167.7(C-9″′)。连翘酯苷A的13CNMR谱图见附图4,DEPT、HMBC谱图见附图5、附图6。核磁数据与文献(Endo,K.;Takahashi,K.;Abe,T.;Hikino,H.StructureofforsythosideB,anantibacterialprincipleofForsythiakoreanastems.Heterocycles1982,19,261-264)报道一致。连翘酯苷B的核磁数据如下:1HNMR:(CD3OD,400MHz):δ7.61(1H,d,J=15.6Hz,H-7″″),7.08(1H,d,J=2.0Hz,H-2″″),6.98(1H,dd,J=8.0Hz,2.0Hz,H-6″″),6.80(1H,d,J=8.4Hz,H-5″′),6.71(1H,d,J=2.0Hz,H-2),6.70(1H,d,J=8.0Hz,H-5),6.59(1H,dd,J=8.0Hz,2.0Hz),6.30(1H,d,J=16.0Hz,H-8″″),5.20(1H,d,J=1.2Hz,H-1′),4.96(1H,t,J=9.6Hz,H-4′),4.93(1H,d,J=2.4Hz,H-1″′),4.39(1H,d,J=8.0Hz,H-1″),3.3~3.55,3.65~4.1(15H,saccharide-H-2′,5′,6′,2″,3″,4″,5″,2″′,4″′,5″′,H2-8)3.63(1H,d,J=7.2Hz,H-3′),2.81(2H,m,H2-7),1.11(3H,d,J=6.4Hz,H-6″)。连翘酯苷B的1HNMR谱图见附图7。13CNMR(CD3OD,100MHz):δ166.75(C-9″″),148.40(C-4″″),146.65(C-7″″),145.44(C-3″″),144.72(C-3),143.29(C-4),130.05(C-1),126.27(C-1″″),121.85(C-6″″),119.90(C-6),115.72(C-5″″),115.12(C-2″″),114.94(C-8″″),113.85(C-2),113.37(C-5),109.65(C-1″′),102.85(C-1′),101.65(C-1″),80.21(C-3′),79.22(C-3″′),76.70(C-2″′),74.77(C-5′),73.70(C-4″′),73.22(C-5″),72.37(C-2″),70.99(C-8),70.95(C-4″),70.66(C-3″),69.48(C-2′),69.04(C-4′),67.06(C-6′),64.27(C-5′),35.23(C-7),16.97(C-6″)。连翘酯苷B的13CNMR谱图见附图8,DEPT谱图见附图9。核磁数据与文献(FuNanWang,ZhiQiangMaetc.NewPhenylethanoidGlycosidesfromtheFruitsofForsythiaSuspense(Thunb.)Vahl.Molecules2009,14,1324-1331)报道一致。实施例2体外酶活实验和IC50值的测定标准溶液的配制:配制方法为将5.00mg待测样品完全溶解于100微升的95%DMSO(含5%的双蒸水)溶液中,浓度为50.0mg/mL。酶活测定:本发明采用以下体外酶活评价体系,该体系由表1所列组分组成:表1体外酶活评价体系的组成其中,PAN蛋白为禽流感病毒A/goose/Guangdong/1/1996(H1N5)毒株RNA聚合酶PA亚基1-256位氨基酸残基(制备方法参见:PuweiYuan,MarkBartlam,ZhiyongLou,eta1.,CrystalstructureofanavianinfluenzapolymerasePANrevealsanendonucleaseactivesite,Nature,2009,458,909-913),PAN蛋白储存溶液为:20mMTrispH8.0,150mMNaCl,pH=8.0,最终PAN蛋白浓度为1mg/mL;底物为5′FAM--AA--3′BHQ1(购于上海生工生物工程有限公司),溶于缓冲液(20mMTrispH8.0,150mMNaCl,pH=8.0)中,浓度为50μM;EDTA的浓度为200mM,取14.97克EDTA溶于150毫升双蒸水中,然后定容至200毫升。评价体系设定阴阳对照。阳性对照组为向体系中加入1.00L200mMEDTA溶液,阴性对照组为向体系中加入1.00L200mMTris(pH=8.0)溶液。实验组为向体系中加入1.00L不同浓度的所测样品溶液。将表1所述体系在37℃下孵育10分钟后,利用酶标仪(FluoroskanAscent,ThermoScientific公司,滤光片为机器自带),测定所采用的激发光和发射光分别为494nm和526nm,每隔30秒记录一次荧光强度数值,共记录200次。根据所获荧光强度数值绘制酶活曲线,并计算PAN蛋白的剩余活性,平行重复3次,取平均值。PAN蛋白剩余活性(RA)的计算方法:在酶活曲线中,取阴性对照曲线斜率最大处值为V0,药物曲线斜率最大处为V1,则PAN蛋白的剩余活性RA=V1/V0。取10μL的标准溶液用95%的DMSO进行成2倍量递增的梯度稀释,共稀释成18个不同浓度的待测溶液。用上述测定方法记录荧光强度数值,并计算PAN蛋白的剩余活性,平行重复3次。将稀释的化合物浓度除以相应化合物的分子量并取以10为底的对数值作为X轴,对应的剩余活性值为Y轴,用GraphPadPrism5作图并计算出相应的IC50值。实施例3咖啡酸、乌金苷、1,3-二咖啡酰基奎宁酸、连翘酯苷A和连翘酯苷B的IC50值测定根据实施例2的方法测试咖啡酸的IC50值,咖啡酸的活性测试结果如表2所示,咖啡酸的IC50曲线图如附图10所示,通过拟合计算可得咖啡酸的IC50=69.6μM,IC50曲线拟合的线性相关系数R2=0.9946。表2咖啡酸的活性测试结果根据与测定咖啡酸IC50值相同的方法分别测定乌金苷、1,3-二咖啡酰基奎宁酸、连翘酯苷A和连翘酯苷B的IC50值,结果如表3所示。表3咖啡酸及其酯的结构式与IC50值本发明选取的乌金苷、1,3-二咖啡酰基奎宁酸购于成都曼斯特对照品有限公司的标准品,HPLC分析含量>98.0%;咖啡酸、连翘酯苷A、连翘酯苷B分离自连翘成熟果实(Forsythiasuspensa(Thunb.)vahl),HPLC分析含量>95.0%。尽管已经示出和描述了本发明的实施例,对于本领域的普通技术人员而言,可以理解在不脱离本发明的原理和精神的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由所附权利要求及其等同物限定。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1