一种装载胰岛素/丝素微球的丝素多孔材料及其制备方法与流程
本发明涉及一种装载胰岛素/丝素微球的丝素多孔材料及其制备方法,该材料可用于创伤、烧伤等皮肤缺损和慢性皮肤溃疡的治疗,属生物医用材料技术领域。
背景技术:
皮肤是人体的最大器官,它既是机体的外部屏障又是机体与外界沟通的桥梁。我国每年有大量的皮肤缺损患者,主要有创伤、烧伤或因糖尿病等疾病引起的慢性皮肤溃疡。近年来,随着糖尿病患者数量的迅速增长,糖尿病性并发难愈创面问题成为亟待解决的临床问题。因此,开发针对难愈创面的生物敷料是临床中的迫切需求。胰岛素作为一种“生长因子样”激素,能够显著加速创面愈合,改善创面愈合质量,给难愈创面提供了有效的促愈手段。但胰岛素在血液中易被蛋白酶水解或失活,并且过高浓度的胰岛素会对人体健康产生威胁。因此,建立合适的胰岛素控释系统,对慢性难愈创面的临床治疗至关重要。丝素蛋白是由绢丝腺内壁上的内皮细胞合成、分泌并储存于绢丝腺内的天然高纯度蛋白质,不含细胞器等生物杂质。再生丝素蛋白因具有优良的生物相容性、可生物降解性等而被广泛研究用作药物释放材料、抗凝血材料、功能性细胞培养基质、生物传感器、人工韧带、人工肌腱、隐形眼镜、人工角膜、人工骨及人工皮肤等。丝素蛋白内的RGD、VITTDSDGNE、NIDNFDED等生物活性序列能促进细胞对其特异性识别和粘附,有利于作为药物载体时达到药物向特定细胞靶向传输的目的,并且丝素蛋白易加工成多种形态的载体材料,有利于保持蛋白质及多肽等敏感性药物的活性。本发明之前,公开号为CN101972481A的中国发明专利“一种丝素蛋白微载体及其制备方法”中,通过同轴高压静电技术和冷冻干燥法制备芯壳结构的微载体,可用于细胞培养和药物缓释领域。该方法工艺过程简单,以水为溶剂,不会引起丝素蛋白生物相容性的降低。公开号为CN103083723A的中国发明专利“胶原/纳米纤维素皮肤再生材料及其制备方法与应用”中,采用乳化法制备明胶微球微球,然后将微球浸泡在生长因子溶液中得到负载生长因子的明胶微球溶液,通过冷冻干燥的方法制备胶原/纳米纤维素多孔支架,再采用戊二醛交联的方法将微球与支架复合以促进创面血管化。该方法制备的微球具有良好的缓释效果,但在制备的过程中引入有机溶剂,存在潜在的毒副作用。公开号为CN103100109A的中国发明专利“负载万古霉素/明胶微球的丝素蛋白复合支架及其制备方法”中,用万古霉素浸泡明胶微球,通过冷冻干燥法使其吸附在微球内,然后采用共混的方法将微球装载到丝素支架内。该方法制备的载药微球突释现象明显,且微球分布在支架的底部,部分微球会因结合不牢靠而脱落。“Alginate-PEGSpongeArchitectureandRoleintheDesignofInsulinReleaseDressings”[Biomacromolecules,2012,13(5):1478-1485]一文中,采用乳化法制备装载胰岛素的PLGA微球,然后通过共混法和冷冻干燥法制备载微球的藻朊酸盐-PEG多孔材料用于创面敷料。结果表明,该材料可有效地持续释放胰岛素21天,且释放出的胰岛素能够促进角质细胞的迁移,但在微球的制备过程中引入了有机溶剂,存在潜在的细胞毒副作用。
技术实现要素:
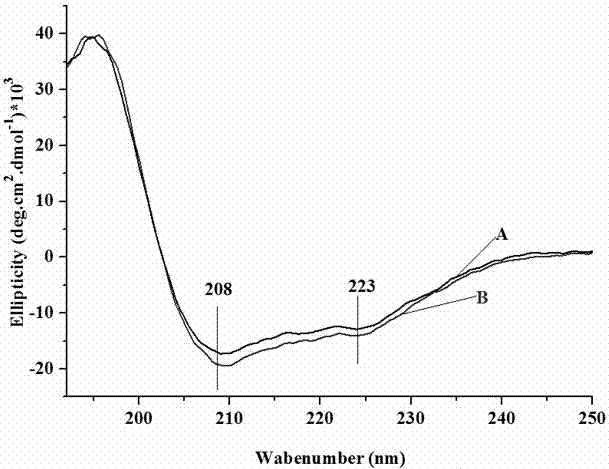
本发明的目的是针对现有技术制备载药微球引入有机溶剂所存在的不足,提供一种能释放生物活性、采用层层组装得到的装载胰岛素/丝素微球的丝素多孔材料及其制备方法。为实现上述发明目的,本发明采用的技术方案是:一种装载胰岛素/丝素微球的丝素多孔材料的制备方法,将蚕丝进行脱胶、溶解、透析处理后得到再生丝素蛋白溶液,再进行如下步骤的加工:1、将甘油加入到浓度为1~5wt%的丝素溶液中搅拌均匀,甘油为丝素质量的3~50%,得到外层溶液;将胰岛素溶于0.01M的HCl溶液中,配置成浓度为1~20mg/mL的溶液,用NaOH溶液调节pH值为6.5~7.2,得到芯层溶液;2、采用同轴静电纺丝工艺在液氮浴中得到微球,经冷冻干燥,再在20~25℃,60%~65%RH的恒温恒湿条件下平衡处理,得到不溶于水的载胰岛素的丝素微球;3、将浓度为1~10wt%的丝素溶液置于冰浴中,加入交联剂反应30~60min,得到丝素蛋白激活液;4、将丝素蛋白激活液按60~90μL/cm2铺于铝盘中,在温度为-20℃~-80℃的条件下冷冻处理30~50min,再在冷冻后的丝素激活液上均匀铺展0.5~5mg/cm2载胰岛素的丝素微球,在温度为-20℃~-80℃的条件下冷冻处理10~20min;5、在步骤4得到的冷冻体上表面,按40~60μL/cm2铺展丝素蛋白激活液,在温度为-20℃~-80℃的条件下冷冻处理30~50min后,按0.5~5mg/cm2均匀铺展载胰岛素的丝素微球,按60~90μL/cm2铺展丝素蛋白激活液,在温度为-20℃~-80℃的条件下冷冻处理24~48h,再经冷冻干燥得到装载胰岛素/丝素微球的丝素多孔材料。本发明技术方案中,所述的交联剂包括一水吗啉乙磺酸、N-羟基琥珀酰亚胺和1-(3-二甲氨基丙基)-3-乙基碳二亚胺,按与丝素的质量百分比分别为20~25%、10~15%和20~25%。所述的交联剂为京尼平,其与丝素的质量百分比为10~15%。本发明提供的制备方法中的一个优选方案是同轴静电纺丝工艺条件为电源电压8~15kV;芯层胰岛素溶液的推注速度为0.1~1mL/h,壳层丝素溶液的推注速度为0.1~3mL/h;外喷针的内径为1~2mm,内喷针的外径为0.45~1.6mm,内喷针的内径为0.1~1.2mm;收集距离为8~15cm。本发明技术方案还包括按上述制备方法得到的一种装载胰岛素/丝素微球的丝素多孔材料,其孔隙率为70%~95%,孔径为50~200μm。。一个优选的方案是:按质量计,丝素多孔材料中胰岛素的含量为1~50%。本发明具有以下明显优点:1、丝素蛋白内的RGD、VITTDSDGNE、NIDNFDED等生物活性序列能促进细胞对其特异性识别和粘附,有利于达到药物向特定细胞靶向传输的目的,并且丝素蛋白易加工成多种形态的载体材料,有利于保持蛋白质及多肽等敏感性药物的活性。2、胰岛素不仅能够治疗糖尿病,而且能够显著加速创面愈合速度,改善创面愈合质量,将胰岛素应用于创面修复是一种有效的促愈手段。3、利用同轴高压静电技术和冷冻干燥法,可以得到粒径分布均匀并且尺寸可控的装载胰岛素的丝素微球。该法工艺过程简单、设备简易、微球产量较高、不引进有机溶剂避免毒副作用。4、采用层层组装和冷冻干燥法,可制备装载胰岛素/丝素微球的丝素多孔材料,该多孔材料内微球分布均匀,且与材料结合牢固,该材料能够持续释放胰岛素,且释放出的胰岛素具有生物活性,可刺激表皮细胞和内皮细胞迁移,以促进创面愈合速度,改善创面愈合质量,为创伤、烧伤等皮肤缺损和慢性皮肤溃疡的治疗提供了性能良好的创面敷料。附图说明图1是本发明实施例提供的载胰岛素的丝素微球的电子显微镜照片;图2是本发明实施例提供的释放胰岛素溶液的圆二色光谱图;图3是本发明实施例提供的载胰岛素/丝素微球的丝素多孔材料的纵截面电子显微镜照片图;图4是本发明实施例提供的装载胰岛素/丝素微球的丝素多孔材料中胰岛素的释放曲线图。具体实施方式下面结合实施例和附图对本发明技术方案作进一步描述。实施例一:(1)将150g家蚕生丝放入6L质量浓度为0.05%的Na2CO3水溶液中,于98~100oC处理30min,重复3次,使蚕丝脱胶,充分洗涤干燥后得到纯丝素纤维。将纯丝素纤维加入三元溶液(氯化钙:水:乙醇的摩尔比为1:8:2)中,在72oC搅拌溶解成丝素蛋白混合溶液。将所得到的丝素混合溶液装入透析袋中,用去离子水透析4天,得到纯化的丝素蛋白溶液。(2)将丝素溶液的浓度调至1wt.%,加入占丝素质量30%的甘油,搅拌均匀作为外层溶液;将胰岛素溶于0.01M的HCl溶液中配置成浓度为1mg/mL的溶液,用0.1M的NaOH溶液调节其pH值至6.5作为芯层溶液。采用同轴静电纺丝技术制备微球,电源电压为8kV,芯层胰岛素溶液的推注速度为0.1mL/h,壳层丝素溶液的推注速度为0.3mL/h,收集距离为8cm,纺制的微球由于电场力作用落入液氮浴中,经冷冻干燥机干燥48h,然后在恒温恒湿(25℃,60%RH...
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1