一种中性pH下自组装成水凝胶的多肽材料及其应用的制作方法与工艺
本发明属于材料制备领域,更具体地,涉及一种中性pH下自组装成水凝胶的多肽材料及其应用。
背景技术:
三维多孔纳米支架能够模仿天然细胞外基质结构,为细胞生长提供支持,广泛应用于生物医学、组织工程学等研究领域。几乎所有的组织细胞在体内都是在三维条件下生长,细胞被包裹在由胶原纤维作为主要成分组成的纳米纤维水凝胶之中,此外,细胞外基质中还含有大量的不溶性基质蛋白和可溶性生长因子。但目前研究中细胞培养技术中所采用的大多都是二维培养,即细胞在培养板或者培养皿上进行培养,这与体内生长环境相差较大,影响细胞生长,甚至会引起细胞基因或者功能变化。如何体外构建具有模仿天然细胞外基质结构和功能的人工支架材料,为细胞提供三维生长环境一直是生物、医学以及材料工程领域基础研究和产品开发的热点。自组装短肽RADA16-I是4个重复的精氨酸-丙氨酸-天冬氨酸-丙氨酸序列,即(精氨酸-丙氨酸-天冬氨酸-丙氨酸)4,当其水溶液调节至pH=7时会形成由纳米纤维网络构成的水凝胶,与天然细胞外基质结构很相似,作为组织工程支架、药物载体和止血材料在生物医学工程领域有广泛的应用,是自组装短肽水凝胶材料的典型代表。但是一个显著的缺点是该材料水溶液具有明显的酸性(pH=3~4),不能与细胞悬液和活性分子直接混合原位成凝胶,即很难实现细胞包埋在RADA16-I水凝胶中进行三维生长。目前关于细胞培养的报道仍是采用先制备水凝胶然后在其表面种植细胞的二维培养模式,不能实现真正的三维细胞培养。而将该材料直接注射体内修复损伤和用于止血时较低的pH会对宿主组织造成损害。自1993年首次报道该材料以来,人们对RADA16-I进行了大量的研究,但是对于其酸性的缺点仍不能有效解决。
技术实现要素:
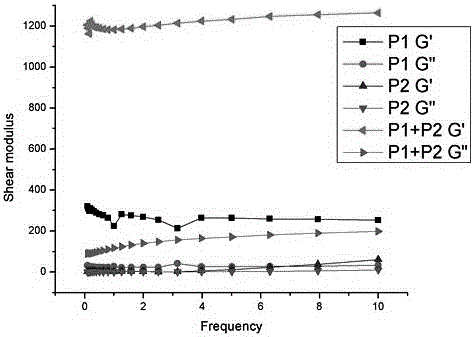
本发明根据目前自组装水凝胶材料中的不足,提供了一种中性pH下自组装成水凝胶的多肽材料。本发明的另一目的在于提供上述多肽材料的制备方法和应用。本发明的技术目的通过以下技术方案实现:本发明提供了一种中性pH下自组装成水凝胶的多肽材料,包括在RADA16-I序列上分别连接多个酸性氨基酸和多个碱性氨基酸,以此形成两种带相反电荷的短肽,混合后自组装形成所述水凝胶的多肽材料。本发明是以低分子量自组装短肽为基础的水凝胶,为细胞三维生长提供空间,用于构建组织工程支架。本材料可在常温中性pH条件下形成纳米纤维水凝胶,模仿了天然细胞外基质结构,具有良好的理化性能和生物相容性,支持细胞三维生长,满足组织工程支架的要求,而且可负载活性分子药物,例如生长因子、短肽药物。可广泛应用于软骨、血管、神经、皮肤等人工器官的再生和损伤的修复。优选地,所述两种带相反电荷的短肽序列分别为序列1:(精氨酸-丙氨酸-天冬氨酸-丙氨酸)4-精氨酸-异亮氨酸-赖氨酸-缬氨酸-丙氨酸-缬氨酸;序列2:(精氨酸-丙氨酸-天冬氨酸-丙氨酸)4-谷氨酸-谷氨酸-酪氨酸-异亮氨酸-甘氨酸-丝氨酸-精氨酸。优选地,所述两种带相反电荷的短肽序列分别为序列3:(精氨酸-丙氨酸-天冬氨酸-丙氨酸)4-(赖氨酸)n;序列4:(精氨酸-丙氨酸-天冬氨酸-丙氨酸)4-谷氨酸-谷氨酸-天冬氨酸-天冬氨酸-天冬氨酸;其中,n为1~10内任意一个自然数。申请人发现,在(精氨酸-丙氨酸-天冬氨酸-丙氨酸)4上接枝赖氨酸,并且与序列4进行混合,赖氨酸的接枝数量可以为1~10中任意一个自然数,这样形成的两对短肽混合后均可以实现中性pH下自组装的能力。优选地,将所述两种带相反电荷的短肽分别配置成5~15mg/mL的水溶液,按照1:1的体积比混合,调节pH至中性,即得所述多肽材料。本发明采用的技术方案是:在短肽(精氨酸-丙氨酸-天冬氨酸-丙氨酸)4序列上通过化学共价键连接多个酸性氨基酸为主的序列,例如如天冬氨酸和谷氨酸,或者连接多个碱性氨基酸为主的序列,例如赖氨酸、精氨酸和组氨酸。最终得到在中性pH条件下分别带有净正电荷和净负电荷的两条短肽序列,溶于水后调整其pH至7,两者混合后形成三维纳米多孔水凝胶。该水凝胶保持中性pH值,三维结构稳定。本发明两对短肽序列的合成是采用了现有的接枝方向获得,由于目前未有成型的理论支持何种改性(即接枝序列和接枝位置)能够获得真正在中性条件下合成的自组装多肽水凝胶,不同的序列排列方式不同,电荷分布也不同,同时结构内部自组装方式均会影响最终的接枝效果,因此,上述接枝物的具体接枝位点和接枝序列排布,对最终效果影响非常大。与现有多肽自组装水凝胶相比,本发明在生理条件下(pH为7-7.4)即可形成三维多孔水凝胶,由直径约20nm的纳米纤维网络构成,凝胶网络结构稳定,可为细胞三维培养提供支撑作用。将含有功能性氨基酸序列引入,能够促进细胞生长、粘附,同时也可负载活性分子药物,如生长因子、短肽药物,获得控制释放。也可注射使用,操作简便,是非常理想的生物材料。本发明所述的中性pH下自组装成水凝胶的多肽材料,并且使用过程都是中性的,不会对细胞核宿主组织产生危害,能够用于真正的三维培养细胞,方法为将细胞悬液分别与所述两种带相反电荷的短肽进行混合,然后将两者混合,得到包埋细胞的水凝胶/细胞复合体,并加入培养基进行培养。进一步地,所述的中性pH下自组装成水凝胶的多肽材料在运用于软骨、血管、神经或皮肤的再生和损伤修复中,具有极大的应用前景。与现有技术相比,本发明具有以下有益效果:本发明提供了一种可在常温中性pH条件,即在人体生理条件自组装形成三维多孔纳米纤维水凝胶。利用本发明技术制备的材料具有更好的生物相容性,可实现原位负载细胞/活性分子以及体内原位注射,在细胞三维培养、组织工程生物支架材料和药物载体领域具有非常广阔的应用前景和临床应用价值。附图说明图1为两种修饰改性后的短肽(P1、P2),混合后形成的水凝胶材料(P1+P2),向水凝胶扩散的细胞培养基未改变颜色,说明形成的水凝胶呈中性pH;原子力显微镜显示纳米纤维形貌,说明所形成的水凝胶是由纳米纤维构成的网络。图2为三种材料的流变性能对比图,P1,P2为改性短肽,P1+P2为两者混合物。G’为储能模量,G”为损耗模量。P1和P2混合后G’大大升高,说明形成了稳定的水凝胶。图3为神经干细胞球在不同纳米纤维水凝胶中三维生长形貌。A为本发明专利制备的纳米纤维水凝胶;B为RADA16-I纳米纤维水凝胶;从图中可以看出神经干细胞球在本发明专利制备的纳米纤维水凝胶中可以三维生长,并长出较长的轴突,而在RADA16-I水凝胶中则没有任何轴突长出。图4为利用活死细胞检测试剂盒检测神经干细胞在不同三维支架中的存活,绿色代表活细胞,红色代表死细胞。A为本发明专利制备的纳米纤维水凝胶;B为RADA16-I纳米纤维水凝胶;从图中可以看出神经干细胞在本发明专利制备的纳米纤维水凝胶中大量存活,存活率达到100%,并可以三维生长,并长出较长的轴突,而在RADA16-I水凝胶中则大量死亡,层圆球状,没有任何轴突长出。具体实施方式下面通过实施例对本发明进行具体描述,有必要在此指出的是本实施例只用于对本发明进行进一步说明,但不能理解为对本发明保护范围的限制,该领域的技术熟练人员可以根据上述本发明的内容作出一些非本质的改进和调整。除非特别说明,本发明采用的试剂、方法和设备为本技术领域常规试剂、方法和设备。实施例1:水凝胶的多肽材料制备:序列1(P1):(精氨酸-丙氨酸-天冬氨酸-丙氨酸)4-精氨酸-异亮氨酸-赖氨酸-缬氨酸-丙氨酸-缬氨酸溶于超纯水后,配置成浓度为5~15ml/mL的溶液,用NaOH调节其pH值至7,可得到带正电荷的短肽水溶液。序列2(P2):(精氨酸-丙氨酸-天冬氨酸-丙氨酸)4-谷氨酸-谷氨酸-酪氨酸-异亮氨酸-甘氨酸-丝氨酸-精氨酸溶于超纯水后,,配置成浓度为5~15ml/mL的溶液,用NaOH调节其pH值至7,可得到带负电荷的短肽水溶液。之后将两者溶液以1:1的体积比混合,静置后迅速形成凝胶,形状稳定后即可投入使用(见图1)。如图1所示,两者混合后形成水凝胶,流动性失去。原子力显微镜显示纳米纤维形貌,由直径约20nm的纳米纤维网络构成,说明所形成的水凝胶是由纳米纤维构成的网络,且凝胶网络结构稳定,可为细胞三维培养提供支撑作用。实施例2:水凝胶的多肽材料制备:制备方法同实施例1,序列3(P1’):(精氨酸-丙氨酸-天冬氨酸-丙氨酸)4-(赖氨酸)1-10;n为1~10内任意一个自然数均可。序列4(P2’):(精氨酸-丙氨酸-天冬氨酸-丙氨酸)4-谷氨酸-谷氨酸-天冬氨酸-天冬氨酸-天冬氨酸。实施例3:三维细胞培养以超纯水为溶剂,配成浓度为5-15mg/mL的P1及P2溶液,将细胞悬液分别与调整至中性pH的P1和P2混合,得到均匀的细胞/短肽混合物,用NaOH溶液调节其pH至中性,之后以1:1混合得到包埋有细胞的三维水凝胶,静置后迅速形成凝胶,加入细胞培养基进行培养。实施例3中包埋细胞为神经干细胞球,如图3和4所示,可以看出神经干细胞球在本发明专利制备的纳米纤维水凝胶中可以三维生长,达到了100%的存活率,并长出较长的轴突,而在RADA16-I水凝胶中则没有任何轴突长出。实施例4:三维细胞培养以超纯水为溶剂,配成浓度为5-15mg/mL的P1’及P2’溶液,将细胞悬液分别与调整至中性pH的P1和P2混合,得到均匀的细胞/短肽混合物,用NaOH溶液调节其pH至中性,之后以1:1混合得到包埋有细胞的三维水凝胶,静置后迅速形成凝胶,加入细胞培养基进行培养。实施例4包埋细胞为为神经干细胞球,其检测后的现象同实施例3的结果相同,与RADA16-I水凝胶相比,本发明提供的纳米纤维水凝胶中可以三维生长,达到了100%的存活率,并长出较长的轴突,而在RADA16-I水凝胶中则没有任何轴突长出。实施例:5:体内原位注射成凝胶在体内缺损部位依次注射P1和P2,即可形成凝胶。凝胶成中性,不会对周围组织造成伤害。在体内缺损部位依次注射P1’和P2’,即可形成凝胶。凝胶成中性,不会对周围组织造成伤害。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1