用于治疗肿瘤的含糖脂组合物的制作方法
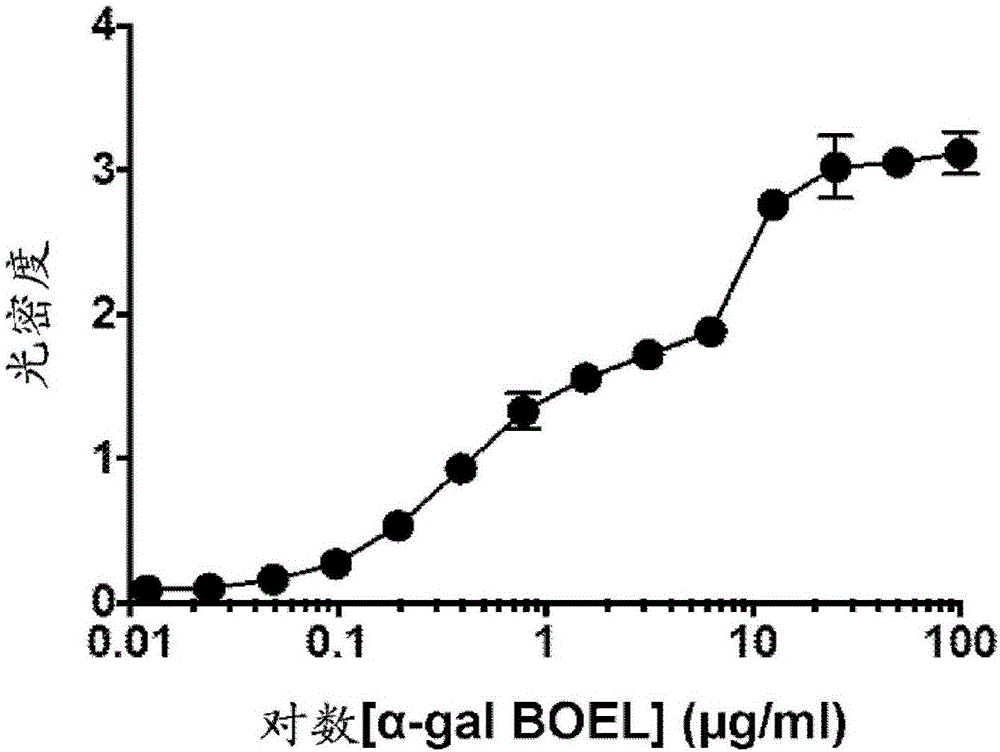
本发明涉及用于治疗肿瘤的包含α-Gal糖脂(9Z,9’Z)-(2R)-3-(((2-(6-((3-(((2R,3R,4R,5S,6R)-3-乙酰胺基-5-(((2S,3R,4S,5S,6R)-3,5-二羟基-6-(羟甲基)-4-(((2R,3R,4S,5R,6R)-3,4,5-三羟基-6-(羟甲基)四氢-2H-吡喃-2-基)氧基)四氢-2H-吡喃-2-基)氧基)-4-羟基-6-(羟甲基)四氢-2H-吡喃-2-基)氧基)丙基)氨基)-6-氧代己酰胺基)乙氧基)(羟基)磷酰基)氧基)丙烷-1,2-二基双(十八-9-烯酸酯)(α-GalBOEL)的药物组合物。本发明还涉及使用所述组合物治疗肿瘤的方法。发明背景患有实体肿瘤的癌症患者中死亡的主要原因是手术后癌症复发,因为多发性转移是不可切除和/或任何治疗难治的。这些患者中的大多数被认为患有末期癌症疾病。由于没有可用治疗,许多这些患者在检测到转移性肿瘤病变之后数周或数月内死亡。肿瘤在癌症患者中发展,因为免疫系统不能检测到作为应该被破坏的细胞的肿瘤细胞。肿瘤细胞在大部分癌症患者中表达自体肿瘤抗原。这些自体肿瘤抗原可引发保护性抗肿瘤免疫应答。肿瘤细胞或肿瘤细胞膜必须通过抗原呈递细胞内化,以便诱导抗肿瘤免疫应答的发展。然而,癌症患者中的免疫系统展示针对肿瘤抗原的与以“隐身”方式进行的肿瘤早期发展相关的“无知”,因此其对于抗原呈递细胞是“不可见的”(PardollDM.Clin.Immunol.2000;95:S44-49;及DunnGP等人NatImmunol2002;3:991-8)。此外,肿瘤微环境和局部细胞因子环境通常是针对免疫功能抑制性的,并且能够主动诱导免疫细胞无反应性和死亡(MalmbergKJ.CancerImmunol.Immunother.2004;53∶879-92;LugadeAA等人J.Immunol.2005;174:7516-23)。这种转移性肿瘤病变的有效治疗需要两个组成部分:1.破坏足够大至通过视觉或通过成像技术检测到的病变,以及2.诱导针对肿瘤抗原的保护性抗肿瘤免疫应答。这种免疫应答产生不能通过视觉检测到且不能通过成像检测到的微转移的免疫介导的检测、消退和/或破坏。保护性抗肿瘤免疫应答的诱导需要通过抗原呈递细胞摄取肿瘤细胞或细胞膜并将其转运至引流淋巴结,其中所述抗原呈递细胞加工肿瘤抗原分子。这些肿瘤抗原中的大多数是对个体患者特异性的。免疫原性肿瘤抗原肽通过与分别用于活化肿瘤特异性CD8+和CD4+T细胞的I类或II类MHC分子缔合的抗原呈递细胞呈递。只有在这些T细胞通过加工的和呈递的肿瘤抗原肽活化后,这些淋巴细胞才能增殖、离开淋巴结、在体内循环、寻找且破坏表达肿瘤抗原的转移性肿瘤细胞。此外,虽然只有在它们被活化后,辅助T细胞才能够帮助B细胞产生针对肿瘤抗原的抗体。然而,由于肿瘤细胞自然进化为对抗原呈递细胞“不可见”,因此发展中肿瘤转移通常被免疫系统忽略至转移性肿瘤细胞甚至能够在淋巴结内增殖的程度。因此,引发有效抗肿瘤免疫应答需要肿瘤细胞有效靶向抗原呈递细胞。所需要的是在使得化合物将插入肿瘤细胞膜中并且天然存在的抗体将与引入的化合物相互作用的条件下将化合物引入肿瘤中(如通过非手术方法或手术方法)的组合物和方法。据信这种相互作用将诱导局部炎症以用于消退和/或破坏肿瘤且使肿瘤细胞和/或肿瘤细胞膜靶向抗原呈递细胞。此过程将在宿主中引发针对在微转移中表达肿瘤抗原的肿瘤细胞的保护性免疫应答,所述微转移不能通过视觉或通过成像检测到且因此不能通过切除术去除。US2006/251661描述了向肿瘤病变施用天然糖脂化合物的方法,所述肿瘤病变诱导肿瘤内与天然抗Gal抗体相互作用的α-Gal表位的局部表达。因此,需要提供一种将α-Gal分子并入肿瘤以便活化针对肿瘤的抗Gal介导的免疫应答的改进方法,还需要有助于所述方法的新型药物组合物。发明简述根据本发明的第一方面,提供一种用于治疗肿瘤的药物组合物,其包含(9Z,9’Z)-(2R)-3-(((2-(6-((3-(((2R,3R,4R,5S,6R)-3-乙酰胺基-5-(((2S,3R,4S,5S,6R)-3,5-二羟基-6-(羟甲基)-4-(((2R,3R,4S,5R,6R)-3,4,5-三羟基-6-(羟甲基)四氢-2H-吡喃-2-基)氧基)四氢-2H-吡喃-2-基)氧基)-4-羟基-6-(羟甲基)四氢-2H-吡喃-2-基)氧基)丙基)氨基)-6-氧代己酰胺基)乙氧基)(羟基)磷酰基)氧基)丙烷-1,2-二-基双(十八-9-烯酸酯)(α-GalBOEL)。根据本发明的另一方面,提供一种包含α-GalBOEL与一种或多种另外的治疗剂的组合的药物组合物。根据本发明的另一方面,提供一种治疗受试者的肿瘤的方法,所述方法包括:a)提供:i)包括至少一种肿瘤的受试者,所述肿瘤包含具有细胞表面的多个癌细胞;以及ii)如本文定义的药物组合物;以及b)将所述药物组合物引入所述肿瘤中。α-GalBOEL的治疗用途先前尚未在本领域中描述,用于治疗肿瘤的特定用途也尚未在本领域中描述。先前认为为了诱导免疫应答,具有复杂且冗长碳水化合物链的α-Gal糖脂是必要的(例如,如在US2006/251661的实施例和Galili等人,TheJournalofImmunology,2007,178:4676-4687中所描述)。源自兔红细胞的天然来源的这些复合碳水化合物包含α-Gal糖脂的未分级混合物,这些糖脂各自含有α-Gal表位。由聚糖生物合成产生的微观不均一性与由提取产生的化合物的不可分离混合物相结合使得衡量材料复杂且困难(Galili等人(2007),同上)。然而,本发明人出人意料地发现含具有短碳水化合物链的α-Gal糖脂(如α-GalBOEL的短碳水化合物“功能性”基团)的单分子在治疗肿瘤中是有效的,并且具有易于生产、储存和施用的附加益处。还据信α-GalBOEL具有提高的水溶性,从而有利于注射液的形成。不受理论束缚,认为α-GalBOEL的间隔区组分提高了分子的溶解性。本文呈现了证明α-GalBOEL在治疗肿瘤中的用途的许多有益特性的数据。例如,α-GalBOEL展示与抗Gal抗体的有效结合(参见实施例1和图2)。此外,α-GalBOEL展示了通过诱导补体介导的癌细胞细胞溶解带来的有效特性(参见实施例2和图3),并且在不存在补体的情况下细胞的存活力不受影响(参见实施例2和图4),且α-GalBOEL能够有效地并入肿瘤细胞中(参见实施例2和图5)。此外,并入α-GalBOEL导致补体蛋白沉积到肿瘤细胞上(实施例3和图6)。此外,α-GalBOEL展示在体内功效模型中诱导针对远端转移的发展的保护性抗肿瘤免疫应答。这种作用取决于在所治疗的受试者中抗Gal的存在。在不存在抗Gal的情况下,没有观察到显著保护性抗肿瘤免疫应答(参见实施例4以及图7和8)。此外,α-GalBOEL和抗PD-1抗体组合显示优于单独抗PD-1抗体的优异体内活性(参见实施例5和图9)。附图简述图1:α-GalBOEL的结构。图2:用于证明α-GalBOEL结合抗Gal抗体的数据。图3:用于证明α-GalBOEL诱导补体介导的癌细胞细胞溶解的数据。图4:用于证明并入α-GalBOEL在补体不存在下不会引起对细胞的明显细胞毒性的数据。图5:用于证明α-GalBOEL并入肿瘤细胞中的数据。图6:用于证明并入α-GalBOEL导致来自人血清的补体蛋白C3b和MAC沉积到肿瘤细胞上的数据。图7:使用α-GalBOEL的剂量滴定实验。将产生抗Gal的GTKO小鼠在其右侧腹上注射1×106个B16-F10黑素瘤细胞以用于原发性肿瘤生长并且在相对侧腹上注射1×104个B16-F10细胞以用于继发性/远端肿瘤注射。5天之后,将主要肿瘤用PBS(空心圆圈)或0.1mgα-GalBOEL(空心三角形)或0.5mgα-GalBOEL(实心三角形)或1mgα-GalBOEL(实心圆圈)肿瘤内治疗。追踪作为转移发展的模型的可见远端肿瘤的发展多达32天。将无可见远端肿瘤的小鼠的百分比绘制在图中。通过对数秩检验来确定所述组之间的统计差异。图8:产生抗Gal的小鼠(即,用猪肾膜免疫的小鼠)或缺乏抗Gal的小鼠(即,非免疫的小鼠)中的α-GalBOEL活性。将超免疫的或非免疫的GTKO小鼠在其右侧腹上注射1×106个B16-F10细胞以用于原发性肿瘤生长并且在相对侧腹上注射1×104个B16-F10细胞以用于继发性/远端肿瘤注射。4天之后,将主要肿瘤在超免疫的小鼠(空心圆圈)中用PBS肿瘤内治疗或用1mgα-GalBOEL(对于超免疫的小鼠,实心圆圈;对于非免疫的小鼠,空心正方形)肿瘤内治疗。追踪作为转移发展的模型的可见远端肿瘤的发展多达28天。将无可见远端肿瘤的小鼠的百分比绘制在图中。通过对数秩检验来确定所述组之间的统计差异。图9:α-GalBOEL与抗PD-1的组合显示在B16-F10黑素瘤模型中的优异活性。将产生抗Gal的GTKO小鼠在其右侧腹上注射1×106个B16-F10细胞以用于原发性肿瘤生长并且在相对侧腹上注射1×104个B16-F10细胞以用于继发性/远端肿瘤注射。5天之后,将主要肿瘤用100μLPBS或含0.1和0.25mgα-GalBOEL的100μLPBS肿瘤内(i.t.)治疗。在第8天或第10天,将小鼠用200μLPBS或含250μg抗PD-1的200μLPBS腹膜内(i.p.)治疗。以三至四天时间间隔重复腹膜内治疗3次。追踪作为转移发展的模型的可见继发性/远端肿瘤的发展多达32天。将无可见远端肿瘤的小鼠的百分比绘制在图中。通过对数秩检验来确定所述治疗组之间的统计差异。α-GalBOEL肿瘤内/抗PD-1腹膜内的组合(实心菱形)显示优于α-GalBOEL肿瘤内/PBS腹膜内(实心圆圈;*,p<0.05)以及优于PBS肿瘤内/抗PD-1腹膜内(实心三角形;***,p=0.0003)以及优于PBS肿瘤内/PBS腹膜内(空心圆圈;***,p<0.0001)的统计上显著的优异活性。对于所述图,合并两个独立实验的结果。发明详述本文描述的发明提供一种使α-Gal糖脂(即α-GalBOEL)能插入至所治疗的肿瘤内的肿瘤细胞的细胞膜中的组合物和方法。据信肿瘤病变中α-Gal糖脂的存在通过由受试者中存在的天然抗Gal抗体与α-GalBOEL的α-Gal表位之间的相互作用诱导的免疫介导的炎症过程产生肿瘤的破坏或消退。此外,这种治疗将所治疗的肿瘤转化成引发全身性保护性抗肿瘤免疫应答的疫苗,所述免疫应答通过转移性肿瘤细胞的免疫破坏而预防远端转移的发展。本文描述的发明包括一种疗法治疗模式,其包括但不限于被称为α-GalBOEL的特异性糖脂的肿瘤内递送,所述糖脂携带α-Gal表位且因此可被称为“α-Gal糖脂”。α-Gal糖脂插入所治疗病变内的肿瘤细胞的细胞膜的外小叶中。肿瘤病变中α-Gal糖脂的存在实现两个目的:1.通过在肿瘤病变内由天然抗Gal抗体与插入肿瘤细胞膜中的α-Gal糖脂的α-Gal表位之间的相互作用诱导的炎症过程进行的肿瘤病变的免疫介导的破坏;以及2.通过肿瘤细胞和具有插入的α-Gal糖脂且因此表达结合原位抗Gal抗体的α-Gal表位的肿瘤细胞膜的抗原呈递细胞有效摄取,从而将所治疗的肿瘤病变转化成自体肿瘤疫苗。虽然不必理解本发明的机制,但据信这种摄取产生针对存在于表达α-Gal表位的肿瘤细胞之上或之内的肿瘤抗原的有效免疫应答。进一步据信这种免疫应答可产生不表达α-Gal表位、但表达肿瘤抗原的转移性肿瘤细胞的免疫介导的破坏。本发明涵盖通过注射或任何其他方式将化合物施用至肿瘤中,所述化合物诱导所治疗肿瘤内的细胞上的α-Gal表位的表达。α-Gal糖脂的这种施用实现以下目的:1.天然抗Gal抗体与α-Gal糖脂的α-Gal表位的结合可产生局部补体活化,从而产生趋化因子,包括但不限于C5a和C3a。这些趋化因子诱导抗原呈递细胞如但不限于树突细胞和巨噬细胞广泛迁移至肿瘤组织中。2.α-Gal糖脂的脂质尾将自发地插入所治疗病变内的肿瘤细胞膜中,从而产生肿瘤细胞上α-Gal表位的表达。抗Gal与这些表位的结合据信诱导包含肿瘤细胞的肿瘤的消退和/或破坏。3.通过抗Gal产生的肿瘤细胞膜的调理作用使所述肿瘤细胞膜靶向通过迁移至肿瘤中的抗原呈递细胞有效摄取。这些抗原呈递细胞的迁移通过在抗Gal与所治疗肿瘤内的α-Gal糖脂结合之后产生的趋化补体裂解肽指导。不受任何特定机制束缚,据信肿瘤细胞膜结合的抗GalIgG分子的Fc部分结合抗原呈递细胞上的Fc-γ受体(FcγR)并且诱导所述抗原呈递细胞摄取肿瘤细胞。摄取的类似诱导可由于结合抗Gal的肿瘤细胞上的补体沉积的C3b补体与抗原呈递细胞上的C3b受体之间的相互作用而发生。这种抗Gal介导的肿瘤膜靶向抗原呈递细胞实现自体肿瘤抗原有效转运至引流淋巴结,以及由所述淋巴结内的抗原呈递细胞进行的免疫原性肿瘤抗原肽的加工和呈递。因此,α-Gal糖脂的肿瘤内注射将所治疗的肿瘤病变转化成原位自体肿瘤疫苗,所述疫苗向免疫系统提供肿瘤抗原,从而引发保护性抗肿瘤免疫应答。这种免疫应答能够诱导肿瘤消退,所述肿瘤消退包括单个肿瘤细胞或肿瘤细胞的小聚集体(即,例如微转移)的破坏。这些微转移通常是通过视觉或通过成像不可检测到的且通过常规手术或放射疗法技术不可及的(即,它们由于其较小大小而是不可切除的)。因此,本发明方法具有以下附加优点:它能够治疗通常通过视觉或通过成像不可检测到且通过常规手术和放射疗法技术不可及的微转移。定义本文提及的术语“α-GalBOEL”是指α-Gal糖脂的具体实例,如α-Gal桥联的双十八烯酸酯脂质,其具有图1中所示的结构和以下完整化学名称(根据IUPAC惯例):(9Z,9’Z)-(2R)-3-(((2-(6-((3-(((2R,3R,4R,5S,6R)-3-乙酰胺基-5-(((2S,3R,4S,5S,6R)-3,5-二羟基-6-(羟甲基)-4-(((2R,3R,4S,5R,6R)-3,4,5-三羟基-6-(羟甲基)四氢-2H-吡喃-2-基)氧基)四氢-2H-吡喃-2-基)氧基)-4-羟基-6-(羟甲基)四氢-2H-吡喃-2-基)氧基)丙基)氨基)-6-氧代己酰胺基)乙氧基)(羟基)磷酰基)氧基)丙烷-1,2-二基双(十八-9-烯酸酯)。α-GalBOEL可自Sigma-Aldrich在产品名称“FSL-Galili(tri)TM”(目录号F9432)下商购。此构建体由功能性(F)、间隔区(S)和脂质(L)组分组成且可用于插入细胞膜中,以使得细胞将在其表面上展示功能性(F)组分。α-GalBOEL的功能性组分是以下的三糖基团:Gal-α1-3-Gal-β1-4GlcNAc(即α-Gal表位)。间隔区组分是O(CH2)3NH基团且脂质组分是二油酰磷脂酰乙醇胺(DOPE)的己二酸酯衍生物(即OOC(CH2)4COO,己二酸的离子化形式)。如本文所用的术语“α-Gal表位”是指任何分子或分子的一部分,其具有包含Galα1-3Galβ1-4GlcNAc-R、Galα1-3Galβ1-3GlcNAc-R或在非还原端具有末端Galα1-3Gal的任何碳水化合物链的末端结构。α-半乳糖基(还称为“alpha-Gal”或“α-Gal”)表位,即,半乳糖基-α-1,3-半乳糖基-β-1,4-N-乙酰基葡糖胺描述于Galili,U.和Avila,J.L.,Alpha-GalandAnti-Gal,SubcellularBiochemistry,第32卷,1999中。异种移植研究已确定人发动对α-半乳糖基表位的免疫应答,所述表位本身通常不在人中发现,但在其他动物和许多微生物中发现。如本文所用,术语“糖脂”是指具有连接至神经酰胺、脂肪酸链或任何其他脂质的至少一个碳水化合物链的任何分子。或者,糖脂可被称为鞘糖脂。在一个实施方案中,糖脂是二油酰磷脂酰乙醇胺(DOPE)的己二酸酯衍生物。如本文所用的术语“抗Gal”是指结合α-Gal表位的天然存在的抗体。如本文所用的术语“α-1,3-半乳糖基转移酶”是指能够合成α-Gal表位的任何酶。如本文所用的术语“抗Gal结合表位”是指能够在体内或体外结合天然抗Gal抗体的任何分子或分子的一部分。如本文所用的术语“不可切除的”是指器官或身体结构的不能通过手术去除的任何部分。例如,“不可切除的肿瘤”可以是通过常规手术技术身体上不可达到的肿瘤,其中其去除不会改善患者的总体癌症疾病或健康的肿瘤,或其中其去除可能对重要器官有害的肿瘤。如本文所用的术语“膜结合的”是指稳定地连接至磷脂双层或包埋在磷脂双层内的任何分子。这种连接或包埋可涉及包括但不限于离子键、共价键、疏水作用力或范德华力等的力。例如,包含疏水性氨基酸区域的蛋白质本身可插入磷脂双层膜中,或包含脂质尾的分子本身可插入细胞的磷脂双层中且变得包埋。α-GalBOEL的脂质组分用于插入肿瘤的细胞膜中以产生在其细胞表面上展示α-Gal表位的肿瘤。如本文所用的术语“亚群”是指在数目上小于整个群体的专化群体。例如,患者可呈现多个不可切除的实体肿瘤。在此多个中,一个亚群可以是通过非手术技术可及的,而另一亚群可能不可通过非手术技术可及。如本文所用的术语“可及的”是指通过非手术技术治疗实体肿瘤的任何能力。此类技术可包括但不限于注射至皮肤中或经由内窥镜检查、支气管镜检查、膀胱镜检查、结肠镜检查、腹腔镜检查、导管插入术注射或通过洗剂、软膏或粉末局部应用。例如,卵巢实体肿瘤可以是通过腹腔镜检查可及的。在另一实例中,结肠实体肿瘤可以是通过结肠镜检查可及的。如本文所用的术语“引入”是指将化合物转移至组织中且随后转移至所述组织内的细胞中的任何方法。所述引入方法可包括但不限于病毒载体、逆转录病毒载体、腺病毒载体、基因枪法(biobalistics)、脂质转染以及本领域中已知的许多可商购的DNA载体。或者,化合物可邻近细胞放置以使得所述化合物通过生理机制(即,例如疏水相互作用或主动转运)并入细胞中。一种引入方法包括注射,其中化合物被直接放置到所注射组织内的细胞间空间中。这种注射在器官部分、生长(即,例如实体肿瘤)或体腔为“可及”时可以是可能的。如本文所用的术语“至……中”是指分子成功渗透穿过细胞膜或在细胞内。例如,病毒载体可在使得肿瘤细胞被转染的条件下引入实体肿瘤细胞中。在另一实例中,糖脂可在使得糖脂变得插入至细胞的磷脂双层膜中的条件下引入肿瘤细胞中。如本文所用的术语“消退”是在大小上至少部分缩减,或“减少”是指身体生长、例如像实体肿瘤的缩减。这种缩减可通过所测量的参数如但不限于直径、质量(即,重量)或体积的减少来测定。缩减决不指示大小完全减少,仅指示所测量参数在数量上小于先前测定。如本文所用的术语“破坏”是指身体生长、例如像实体肿瘤的完全细胞分解。这种破坏可涉及细胞内细胞凋亡、T细胞介导的细胞杀伤、补体介导的细胞溶解和/或巨噬细胞吞噬作用,以使得身体生长被完全消化且从身体消除。术语“肿瘤的破坏”是指肿瘤减少至其不再可通过诊断方式检测到的这样一种程度。全部在本文使用的术语“治疗(treating)”、“治疗(treatment)”“治疗(treat)”意图指产生身体生长、例如像实体肿瘤的大小的至少部分缩减或大小减少的程序。如本文所用的术语“少于全部”是指群体的亚群。在本发明的一个实施方案的背景下,涵盖患者的少于全部肿瘤的治疗。换言之,在一个实施方案中,不必通过引入α-Gal表位(例如通过引入α-GalBOEL)治疗每一肿瘤;而是引入至亚群产生所有肿瘤(包括不直接治疗的那些肿瘤)的免疫应答。以此方式,能够实现多个身体生长、例如像实体肿瘤转移的集体缩减。这种缩减可通过所测量的参数如但不限于数目的减少来测定。缩减决不指示参数减少至零,仅指示所测量参数在数量上小于先前测定。如本文所用的术语“生长”是指包括被认为表示异常增殖的细胞团块的任何组织或器官。此类生长可以是癌性的、非癌性的、恶性的或非恶性的。如果生长包括癌症,则它可以是肿瘤。如本文所用的术语“肿瘤”是指由细胞的异常生长或分裂产生的异常组织团块。此类肿瘤可以是实体的(即特定器官、组织或腺体中的细胞团块,如在腹膜、肝、胰腺、肺、膀胱、前列腺、子宫、子宫颈、阴道、乳腺、皮肤、脑、淋巴结、头和颈、胃、肠、结肠或卵巢上)或非实体的(即在血液中发展的液体肿瘤,如白血病)。如本文所用的术语“受试者”是指能够发展肿瘤的任何生物体。此类生物体包括但不限于哺乳动物、人、非灵长类哺乳动物、原猴亚目以及新大陆猴等。如本文所用的术语“分子”是指组合物的最小颗粒,所述最小颗粒保留所述组合物的所有性质且由一个或多个原子组成。这一个或多个原子排列为使得所述分子可与其他分子相互作用(即,离子、共价、非共价等)以形成连接和/或缔合。例如,分子可具有一个或多个被排列为提供与抗Gal抗体相互作用的能力的原子。天然抗Gal抗体、α-Gal表位以及异种移植排斥抗Gal据信为可存在于所有人中、构成血清免疫球蛋白的0.1%-2%的天然抗体(BovinN.V.,Biochemistry(Moscow),2013;78(7):786-797;Galili等人J.Exp.Med.1984;160:1519-31以及HamadehRM等人Clin.Diagnos.Lab.Immunol.1995;2:125-31)。研究已经呈现了指示抗Gal抗体可能与细胞表面或游离糖脂和糖蛋白上的α-Gal表位特异性相互作用的数据。(GaliliU等人J.Exp.Med.1985,162:573-82和GaliliU.SpringerSeminImmunopathol.1993;15:155-171)。进一步报道抗Gal抗体可由于胃肠菌群的细菌的抗原刺激而在整个生命期间产生(GaliliU等人Infect.Immun.1988;56:1730-37)。α-Gal表位可通过非灵长类哺乳动物、原猴亚目和新大陆猴的细胞的高尔基体内的糖基化酶α1,3半乳糖基转移酶在磷脂和糖蛋白上大量生物合成(GaliliU等人Biol.Chem.1988;263;17755-62)。相比之下,人、猿和旧大陆猴缺乏α-Gal表位,但以极大量产生天然抗Gal抗体(GaliliU等人Proc.Natl.Acad.Sci.USA1987,84:1369-73)。基于猴和猿中的α1,3半乳糖基转移酶假基因的序列,据估计α1,3半乳糖基转移酶基因在大约2千万年前在祖先旧大陆灵长类动物中失活(GaliliU,SwansonK.Proc.Natl.Acad.Sci.USA1991;88:7401-04)。表明此演化事件与旧大陆(即当前欧洲、亚洲和非洲)所特有的感染性微生物剂的出现相关,所述感染性微生物剂对灵长类动物有害且表达α-Gal表位。灵长类动物能够产生抗Gal作为针对这种推定有害剂的保护性抗体,仅在它们在选择性压力下演化以用于使α1,3半乳糖基转移酶基因失活且因此丧失对α-Gal表位的免疫耐受性(GaliliU,AndrewsP.J.HumanEvolution29:433-42,1995)。天然抗Gal抗体的强保护活性一直是在人和猴中进化上保守的。这可从使用表达α-Gal表位的猪器官的异种移植研究来推断。因为各种哺乳动物(包括猪)的细胞表达α-Gal表位,所以在人或旧大陆猴中移植的来自猪的器官由于抗Gal抗体与猪细胞上的这些表位的体内结合而被排斥(Galili,U.Immunol.Today1993,14:480-82)。猪组织移植至人或旧大陆猴中导致与体内移植物上的α-Gal表位的有效抗Gal结合以及异种移植物排斥的随后诱导。血管化异种移植物(例如猪心)通常在猴中在30-60分钟内经历快速排斥(称为超级性排斥),这是由于抗Gal抗体分子与猪内皮细胞上的α-Gal表位的结合、补体的活化、内皮细胞的溶解以及血管床的坍塌(CollinsBH等人J.Immunol.1995;154:5500-10)。此外,血管外区域中的异种移植物细胞的许多破坏是由抗GalIgG与各种细胞上的α-Gal表位的结合介导的。在抗GalIgG的Fc部分与粒细胞、巨噬细胞和NK细胞上的细胞结合的Fcγ受体的结合之后,这种结合导致抗体依赖性细胞介导的细胞溶解(ADCC)。抗Gal介导的异种移植物的破坏可用移植至恒河猴(即,天然产生抗Gal抗体的猴)中的猪软骨(无血管异种移植物组织)监测。研究指示抗Gal与猪组织中的α-Gal表位的结合导致诱导广泛炎症反应,所述炎症反应导致在2个月内组织的逐渐破坏(StoneKR等人Transplantation1998,65:1577-83)。抗Gal与软骨细胞和细胞外基质糖蛋白上的α-Gal表位的结合进一步调理它们(即,与它们形成免疫复合物)且因此通过免疫复合的抗Gal的Fc部分与抗原呈递细胞上的Fcγ受体的结合使它们靶向抗原呈递细胞。抗原呈递细胞进而将这些猪糖蛋白转运至引流淋巴结,其中它们活化对多种猪异种肽具有特异性的许多T细胞。这些活化的T细胞随后迁移至软骨异种移植物植入物中且包含大约80%的浸润单核细胞。这种炎症应答主要通过抗Gal与α-Gal表位的相互作用介导可从监测对猪软骨异种移植物的免疫应答来推断,从所述异种移植物通过酶处理去除α-Gal表位(例如,使用重组α-半乳糖苷酶)。α-半乳糖苷酶通过裂解(水解)末端α-半乳糖基单元破坏软骨糖蛋白上的α-Gal表位。在猪软骨糖蛋白上的α-Gal表位不存在下,不存在与异种移植物的抗Gal结合且因此未发生异种糖蛋白的有效抗原呈递细胞介导的转运。这通过异种移植物中的显著T细胞浸润的缺乏指示。本发明涵盖利用在猪软骨异种移植物排斥中显示的天然抗Gal抗体的免疫潜力用于消退和/或破坏进行治疗以展示α-Gal表位的肿瘤病变并且用于通过抗Gal抗体使肿瘤细胞膜靶向抗原呈递细胞。据信这种治疗将使肿瘤病变转化成原位自体肿瘤疫苗,所述疫苗通过与在猴中猪软骨的排斥中观察到的那些机制类似的机制引发针对转移性肿瘤的全身性保护性免疫应答。进一步据信抗GalIgG分子与表达α-Gal表位的肿瘤细胞的结合将使肿瘤细胞膜靶向抗原呈递细胞以用于引发针对在所治疗病变中的肿瘤细胞上表达且还在转移性肿瘤细胞上表达的自体肿瘤抗原的保护性抗肿瘤免疫应答。药物组合物根据本发明的另一方面,提供一种用于治疗肿瘤的包含α-GalBOEL的药物组合物。在一个实施方案中,所述肿瘤是实体肿瘤、骨髓瘤或淋巴瘤。在另一实施方案中,所述肿瘤是实体肿瘤。在替代实施方案中,所述肿瘤是非实体肿瘤。在一个实施方案中,所述肿瘤是来源于选自以下各项的器官的肿瘤:腹膜、肝、胰腺、肺、膀胱、前列腺、子宫、子宫颈、阴道、骨髓、乳腺、皮肤、脑、淋巴结、头和颈、胃、肠、结肠、肾、睾丸以及卵巢。在另一实施方案中,所述肿瘤是来源于选自以下各项的器官的肿瘤:腹膜、肝、胰腺、肺、膀胱、前列腺、子宫、子宫颈、阴道、乳腺、皮肤、脑、淋巴结、头和颈、胃、肠、结肠以及卵巢。在一个实施方案中,所述肿瘤包括原发性肿瘤和/或转移。在另一实施方案中,所述肿瘤包括原发性肿瘤。在替代实施方案中,所述肿瘤包括继发性肿瘤。在一个实施方案中,所述肿瘤包括黑素瘤、肉瘤、神经胶质瘤或癌细胞。在另一实施方案中,所述肿瘤包括黑素瘤或癌细胞或转移。所述组合物可被制备为包含α-GalBOEL的水性糖脂制剂,其中所述制剂包含糖脂胶束。在一个实施方案中,所述组合物另外包含一种或多种药学上可接受的载体、稀释剂和/或赋形剂。载体、稀释剂和/或赋形剂在可与组合物的其他成分相容以及不对其接受者有害的意义上必须是“药学上可接受的”。本领域的技术人员将了解例如在Remington:TheScienceandPracticeofPharmacy;PharmaceuticalPress;第22版;Allen,LoydV.Ed.2012,London,UK中例示的药物制剂的方面。本发明的组合物可根据本领域中熟知的常规程序通过组合α-GalBOEL与标准药物载体或赋形剂来制备。这些程序可涉及混合、制粒和压缩或溶解如对于所需制剂而言适当的所述成分。在一个实施方案中,所述药物组合物还可包含脱氧胆酸酯,或可增加糖脂渗透至细胞膜中的其他温和洗涤剂本发明的药物组合物可被配制用于通过任何途径施用,并且包括呈适于口服、局部或胃肠外施用至哺乳动物(包括人)的形式的那些。因此,在一个实施方案中,所述组合物用于通过注射施用。在替代实施方案中,所述组合物是局部施加,如局部软膏、局部洗剂或局部溶液。在一个实施方案中,所述组合物以一个剂量或多个剂量(如多个剂量)施用。在另一实施方案中,所述多个剂量同时施用(即一次的情况)。在另一替代实施方案中,顺序施用多个剂量(即,两次或更多次分开的情况,如在分开治疗期间)。当施用是顺序(即在分开的情况)时,所述组合物可在适合时间已在施用之间经过(例如3天、5天、1周、2周、1个月、2个月、3个月、6个月或12个月)时施用。对于胃肠外施用,利用组合物和无菌媒介物如水来制备流体单位剂型。在制备溶液中,所述组合物可溶解于注射用水中且在填充至适合小瓶或安瓿且密封之前无菌过滤。所述组合物可呈片剂、胶囊、粉末、颗粒、锭剂、乳膏或脂质制剂,如口服或无菌胃肠外溶液或悬浮液的形式。本发明的局部制剂可呈现为例如软膏、乳膏或洗剂、眼软膏和眼或耳滴剂、浸透敷料以及气雾剂,并且可包含适当常规添加剂,如软膏和乳膏中的防腐剂和软化剂。所述制剂也可包含相容性常规载体,如乳膏或软膏基质以及用于洗剂的乙醇或油醇。组合将了解本发明的化合物可作为唯一治疗剂施用或其可以与一种或多种其他化合物(或疗法)的组合疗法施用以用于治疗肿瘤。因此,根据本发明的另一方面,提供一种包含α-GalBOEL与一种或多种另外的治疗剂的组合的药物组合物。对于肿瘤的治疗,本发明的化合物可有利地与一种或多种其他药剂,更具体地与癌症疗法中的一种或多种抗癌剂或佐剂(疗法中的支持剂)组合来应用。可与本发明的化合物一起施用(无论是同时还是以不同时间间隔)的其他治疗剂或治疗的实例包括但不限于:·拓扑异构酶I抑制剂;·抗代谢药;·微管蛋白靶向剂;·DNA结合剂和拓扑异构酶II抑制剂;·烷化剂;·单克隆抗体;·抗激素剂;·信号转导抑制剂;·蛋白酶体抑制剂;·DNA甲基转移酶;·细胞因子和类视黄醇;·染色质靶向疗法;·放射疗法;以及·其他治疗剂或预防剂。抗癌药剂或佐剂(或其盐)的具体实例包括但不限于选自组(i)-(xlvi)以及任选组(xlvii)的任何药剂:(i)铂化合物,例如顺铂(任选与氨磷汀组合)、卡铂或奥沙利铂;(ii)紫杉烷化合物,例如紫杉醇、紫杉醇蛋白结合颗粒(AbraxaneTM)、多西他赛、卡巴他赛或拉罗他赛(larotaxel);(iii)拓扑异构酶I抑制剂,例如喜树碱化合物,例如喜树碱、伊立替康(CPT11)、SN-38或拓扑替康;(iv)拓扑异构酶II抑制剂,例如抗肿瘤表鬼臼毒素或足叶草毒素衍生物,例如依托泊苷或替尼泊苷;(v)长春花生物碱,例如长春花碱、长春新碱、脂质体长春新碱(Onco-TCS)、长春瑞滨、长春地辛、长春氟宁或vinvesir;(vi)核苷衍生物,例如5-氟尿嘧啶(5-FU,任选与亚叶酸组合)、吉西他滨、卡培他滨、替加氟、UFT、S1、克拉屈滨、阿糖胞苷(Ara-C,胞嘧啶阿拉伯糖苷)、氟达拉滨、氯法拉滨或奈拉滨;(vii)抗代谢药,例如氯法拉滨、氨基蝶呤或甲氨蝶呤、阿扎胞苷、阿糖胞苷、氟尿苷、喷司他丁、硫鸟嘌呤、硫嘌呤、6-巯基嘌呤或羟基脲(羟基尿素);(viii)烷化剂,如氮芥或亚硝基脲,例如环磷酰胺、苯丁酸氮芥、卡氮芥(BCNU)、苯达莫司汀、噻替派、美法仑、苏消安、洛莫司汀(CCNU)、六甲蜜胺、白消安、达卡巴嗪、雌莫司汀、福莫司汀、异环磷酰胺(任选与美司钠组合)、哌泊溴烷、丙卡巴肼、链佐星、替莫唑胺、尿嘧啶、二氯甲基二乙胺、甲基环己基氯乙基亚硝基脲或尼莫司汀(ACNU);(ix)蒽环类、蒽醌类以及相关药物,例如柔红霉素、阿霉素(任选与右雷佐生组合)、阿霉素的脂质体制剂(例如,CaelyxTM、MyocetTM、DoxilTM)、伊达比星、米托蒽醌、表柔比星、安吖啶或戊柔比星;(x)埃博霉素,例如伊沙匹隆、帕土匹龙(patupilone)、BMS-310705、KOS-862和ZK-EPO、埃博霉素A、埃博霉素B、脱氧埃博霉素B(也称为埃博霉素D或KOS-862)、氮杂埃博霉素B(也称为BMS-247550)、aulimalide、isolaulimalide或luetherobin;(xi)DNA甲基转移酶抑制剂,例如替莫唑胺、氮胞苷或地西他滨;(xii)抗叶酸剂,例如甲氨蝶呤、培美曲塞二钠或雷替曲塞;(xiii)细胞毒性抗生素,例如放线菌素D、博来霉素、丝裂霉素C、更生霉素、洋红霉素、柔红霉素、左旋咪唑、普卡霉素或光辉霉素;(xiv)微管蛋白结合剂,例如考布他丁(combrestatin)、秋水仙碱或诺考达唑;(xv)信号转导抑制剂,如激酶抑制剂(例如,EGFR(表皮生长因子受体)抑制剂、VEGFR(血管内皮生长因子受体)抑制剂、PDGFR(血小板源生长因子受体)抑制剂、MTKI(多靶标激酶抑制剂)、Raf抑制剂、mTOR抑制剂,例如甲磺酸伊马替尼、埃罗替尼、吉非替尼、达沙替尼、拉帕替尼、多韦替尼(dovotinib)、阿西替尼、尼罗替尼、凡德他尼、瓦他拉尼(vatalinib)、帕唑帕尼、索拉非尼、舒尼替尼、坦罗莫司、依维莫司(RAD001)或维罗非尼(PLX4032/RG7204);(xvi)极光激酶抑制剂,例如AT9283、巴拉塞替(barasertib)(AZD1152)、TAK-901、MK0457(VX680)、塞尼色替(cenisertib)(R-763)、达鲁色替(danusertib)(PHA-739358)、阿利色替(alisertib)(MLN-8237)或MP-470;(xvii)CDK抑制剂,例如AT7519、roscovitine、seliciclib、阿伏西地(alvocidib)(夫拉平度(flavopiridol))、dinaciclib(SCH-727965)、7-羟基-星孢菌素(UCN-01)、JNJ-7706621、BMS-387032(亦称为SNS-032)、PHA533533、PD332991、ZK-304709或AZD-5438;(xviii)PKA/B抑制剂和PKB(akt)路径抑制剂,例如ATl3148、AZ-5363、Semaphore、SF1126和MTOR抑制剂如雷帕霉素类似物、AP23841和AP23573、钙调蛋白抑制剂(叉头易位抑制剂)、API-2/TCN(曲西瑞宾)、RX-0201、盐酸恩斯他瑞(enzastaurinHCl)(LY317615)、NL-71-101、SR-13668、PX-316或KRX-0401(哌立福辛/NSC639966);(xix)Hsp90抑制剂,例如AT13387、除莠霉素、格尔德霉素(GA)、17-烯丙基氨基-17-脱甲氧基格尔德霉素(17-AAG)(例如NSC-330507、Kos-953和CNF-1010)、盐酸17-二甲基氨基乙氨基-17-脱甲氧基格尔德霉素(17-DMAG)(例如,NSC-707545和Kos-1022)、NVP-AUY922(VER-52296)、NVP-BEP800、CNF-2024(BIIB-021,口服嘌呤)、ganetespib(STA-9090)、SNX-5422(SC-102112)或IPI-504;(xx)单克隆抗体(未缀合或者与放射性同位素、毒素或其他药剂缀合)、抗体衍生物和相关药剂,如抗-CD、抗-VEGFR、抗-HER2或抗-EGFR抗体,例如利妥昔单抗(CD20)、奥法木单抗(CD20)、替伊莫单抗(CD20)、GA101(CD20)、托西莫单抗(CD20)、依帕珠单抗(CD22)、林妥珠单抗(CD33)、吉妥单抗(CD33)、阿仑单抗(CD52)、加利昔单抗(CD80)、曲妥珠单抗(HER2抗体)、帕妥珠单抗(HER2)、曲妥珠单抗-DM1(HER2)、厄妥索单抗(HER2和CD3)、西妥昔单抗(EGFR)、帕尼单抗(EGFR)、雷莫芦单抗(necitumumab)(EGFR)、尼妥珠单抗(EGFR)、贝伐单抗(VEGF)、伊匹单抗(CTLA4)、卡妥索单抗(catumaxumab)(EpCAM和CD3)、阿巴伏单抗(CA125)、法利珠单抗(farletuzumab)(叶酸受体)、依洛珠单抗(elotuzumab)(CS1)、地诺单抗(RANK配体)、芬妥木单抗(figitumumab)(IGFlR)、CP751,871(IGF1R)、马帕木单抗(mapatumumab)(TRAIL受体)、metMAB(met)、米妥莫单抗(GD3神经节苷脂)、他那莫单抗(naptumomabestafenatox)(5T4)或司妥昔单抗(IL6);(xxi)雌激素受体拮抗剂或选择性雌激素受体调节剂(SERM)或雌激素合成抑制剂,例如他莫昔芬、氟维司群、托瑞米芬、屈洛昔芬、法洛德(faslodex)或雷洛昔芬;(xxii)芳香酶抑制剂和相关药物,如依西美坦、阿那曲唑、来曲唑、睾内酯氨鲁米特、米托坦或伏罗唑;(xxiii)抗雄激素物质(即,雄激素受体拮抗剂)和相关药剂,例如比卡鲁胺、尼鲁米特、氟他胺、环丙孕酮或酮康唑;(xxiv)激素及其类似物,如甲羟孕酮、乙烯雌酚(亦称为已烯雌酚)或奥曲肽;(xxv)类固醇,例如丙酸屈他雄酮、醋酸甲地孕酮、诺龙(癸酸酯、苯丙酸酯)、氟甲睾酮或棉子酚,(xxvi)类固醇细胞色素P45017α-羟化酶-17,20-裂解酶抑制剂(CYP17),例如阿比特龙;(xxvii)促性腺激素释放激素激动剂或拮抗剂(GnRA),例如阿巴瑞克、乙酸戈舍瑞林、乙酸组氨瑞林、乙酸亮丙瑞林、曲普瑞林、布舍瑞林或地洛瑞林;(xxviii)糖皮质激素,例如泼尼松、泼尼松龙、地塞米松;(xxix)分化剂如类视黄醇、rexinoid、维生素D或视黄酸以及视黄酸代谢阻断剂(RAMBA)例如异维甲酸、阿利维A酸、贝沙罗汀或维甲酸;(xxx)法尼基转移酶抑制剂,例如替吡法尼;(xxxi)染色质靶向疗法,如组蛋白脱乙酰酶(HDAC)抑制剂,例如丁酸钠、辛二酰苯胺羟基酰胺酸(SAHA)、缩酚肽(FR901228)、达西司特(NVP-LAQ824)、R306465/JNJ-16241199、JNJ-26481585、曲古抑菌素A、伏立诺他、克林霉素(chlamydocin)、A-173、JNJ-MGCD-0103、PXD-101或阿匹西定(apicidin);(xxxii)蛋白酶体抑制剂,例如硼替佐米、卡非佐米、CEP-18770、MLN-9708或ONX-0912;(xxxiii)光动力学药物,例如卟吩姆钠或替莫卟吩;(xxxiv)海洋生物来源的抗癌剂,如曲贝替定(trabectidin);(xxxv)用于放射性免疫疗法的放射性标记的药物,例如使用β粒子发射性同位素(例如,碘-131、钇-90)或α粒子发射性同位素(例如,铋-213或锕-225)的放射性标记的药物,例如替伊莫单抗或碘托西莫单抗;(xxxvi)端粒酶抑制剂,例如特洛他汀(telomestatin);(xxxvii)基质金属蛋白酶抑制剂,例如巴马司他、马立马司他、普林如果司他(prinostat)或美司他(metastat);(xxxviii)重组干扰素(如干扰素-γ和干扰素α)和白介素(例如,白介素2),例如阿地白介素、地尼白介素、干扰素α2a、干扰素α2b或聚乙二醇干扰素α2b;(xxxix)选择性免疫应答调节剂,例如沙利度胺或雷利度胺;(x1)治疗性疫苗,如西普鲁塞(sipuleucel)-T(普罗文奇)或OncoVex;(xli)细胞因子活化剂,包括毕西巴尼(Picibanil)、罗莫肽、西佐喃、维鲁利秦或胸腺素;(xlii)三氧化二砷;(xliii)G-蛋白偶联受体(GPCR)抑制剂,例如阿曲生坦;(xliv)酶,如L-天冬酰胺酶、培门冬酶、拉布立酶或培加酶;(xlv)DNA修复抑制剂,如PARP抑制剂,例如奥拉帕尼、维利帕尼(velaparib)、iniparib、INO-1001、AG-014699或ONO-2231;(xlvi)死亡受体的激动剂(例如,TNF-相关的细胞凋亡诱导配体(TRAIL)受体),如马帕木单抗(原来的HGS-ETR1)、可那木单抗(conatumumab)(原来的AMG655)、PRO95780、来沙木单抗、杜拉乐明、CS-1008、阿普单抗或者重组TRAIL配体如重组人TRAIL/Apo2配体;(xlvii)预防剂(佐剂);即,减少或减轻一些与化学治疗剂相关的副作用的药剂,例如-抗呕剂;-预防或减少化学治疗剂相关的嗜中性粒细胞减少症的持续时间并且预防由血小板、红血细胞或白血细胞水平降低所引起的并发症的药剂,例如白介素-11(例如,奥普瑞白介素)、红细胞生成素(EPO)及其类似物(例如,阿法达伯汀(darbepoetinalfa))、集落刺激因子类似物如粒细胞巨噬细胞集落刺激因子(GM-CSF)(例如,沙格司亭)以及粒细胞集落刺激因子(G-CSF)及其类似物(例如,非格司亭、聚乙二醇非格司亭);-抑制骨吸收的药剂,如德尼单抗或二磷酸盐,例如唑来磷酸盐、唑来磷酸、帕米膦酸盐以及伊班膦酸盐;-抑制炎症反应的药剂,如地塞米松、泼尼松和泼尼松龙;-用于在患有肢端肥大症或其他罕见激素产生肿瘤的患者中降低生长激素和IGF-I(以及其他激素)的血液水平的药剂,如合成形式的激素生长激素抑制素,例如乙酸奥曲肽;-降低叶酸水平的药物的解毒剂,如亚叶酸或叶酸;-用于疼痛的药剂,例如鸦片剂,如吗啡、二乙酰吗啡和芬太尼;-非类固醇抗炎药(NSAID),如COX-2抑制剂,例如塞来昔布、依托昔布和罗美昔布;-用于粘膜炎的药剂,例如帕利夫明;-用于治疗副作用(包括厌食、恶病质、水肿或血栓栓塞发作)的药剂,如乙酸甲地孕酮。在一个具体实施方案中,所述药物组合物另外包含免疫系统下调的一种或多种系统抑制剂。免疫系统下调的适合系统性抑制剂的实例描述于US2012/263677中并且包括抗CTLA-4、PD-1和PD-L1抗体。在另一实施方案中,免疫系统下调的一种或多种系统抑制剂选自抗PD-1抗体。数据在本文中在实施例5和图9中呈现,所述数据证明相较于单独α-GalBOEL和抗PD-1,本发明的化合物(α-GalBOEL)与抗PD-1抗体的组合关于预防转移生长的协同特性。在另一实施方案中,所述药物组合物另外包含免疫系统上调的一种或多种增强剂。免疫系统上调的适合增强剂的实例描述于US2012/263677中并且包括适合非特异性细胞因子,如白介素-1、-2或-6(IL-1、IL-2或IL-6)和阿地白介素;干扰素-α或γ(IFN-α和IFN-γ)、干扰素α-2b和聚乙二醇化干扰素(包括聚乙二醇化干扰素α-2a和聚乙二醇化干扰素α-2b);粒细胞巨噬细胞集落刺激因子(GM-CSF,莫拉司亭或沙格司亭);树突细胞疫苗和其他同种异体或自体治疗性癌症疫苗,包括含有编码GM-CSF的溶瘤疱疹病毒或被设计为表达同种异体MHCI类抗原的编码人白细胞抗原-B7和β-2微球蛋白剂的质粒的病变内疫苗;以及针对特异性肿瘤抗原的抗体。在另一实施方案中,免疫系统上调的一种或多种增强剂选自IL-2和干扰素-γ。存在于本发明的组合中的每种化合物可以单独变化的剂量方案并且经由不同的路径给予。例如,本发明的α-GalBOEL意图直接施用至肿瘤,而免疫系统下调的系统抑制剂如抗PD-1抗体通常将全身递送,即通过静脉内注射。如此,两种或更多种药剂中的每种的剂量学可不同:各自可在相同时间或在不同时间施用。本领域的技术人员将通过他或她的公知常识知道待使用的给药方案和组合疗法。例如,本发明的化合物可与根据其现有组合方案施用的一种或多种其他药剂组合使用。治疗方法根据本发明的另一方面,提供一种治疗受试者的肿瘤的方法,所述方法包括:a)提供:i)包括至少一种肿瘤的受试者,所述肿瘤包含具有细胞表面的多个癌细胞;以及ii)如本文定义的药物组合物;以及b)将所述药物组合物引入所述肿瘤中。在一个实施方案中,所述药物组合物诱导针对肿瘤的免疫应答,从而治疗所述肿瘤。在一个实施方案中,本发明提供一种用于诱导针对受试者的肿瘤的免疫应答的方法,所述方法包括:a)向包括至少一种肿瘤的受试者施用有效量的包含α-GalBOEL的药物组合物以诱导针对所述至少一种肿瘤的免疫应答。在一个实施方案中,本发明提供一种用于治疗受试者的肿瘤的方法,所述方法包括:a)向包括至少一种肿瘤的受试者施用有效量的包含α-GalBOEL的药物组合物以诱导针对所述至少一种肿瘤的免疫应答,其中诱导针对所述肿瘤的免疫应答产生肿瘤的减少,从而治疗所述受试者的肿瘤。在一个实施方案中,所述组合物还包含免疫系统下调的至少一种系统抑制剂。在一个实施方案中,免疫系统下调的至少一种系统抑制剂选自抗CTLA-4、PD-1和PD-L1抗体。在一个实施方案中,将所述方法重复1-5次直到肿瘤大小减小。在一个实施方案中,将所述方法重复1-5次直到肿瘤不可检测。在一个实施方案中,所述药物组合物被注射至原发性肿瘤中并且诱导在治疗由原发性肿瘤产生的至少一种继发性肿瘤方面有效的免疫应答。在一个实施方案中,所述药物组合物被注射至原发性肿瘤中并且诱导在减小由原发性肿瘤产生的至少一种继发性肿瘤的大小方面有效的免疫应答。在一个实施方案中,所述方法还包括在诱导针对肿瘤的免疫应答之后手术去除肿瘤。在一个实施方案中,所述方法还包括在施用所述药物组合物之后手术去除肿瘤。在一个实施方案中,肿瘤的手术去除在施用所述药物组合物之后约1-21天之间发生。在一个实施方案中,肿瘤的手术去除在施用所述药物组合物之后约1-14天之间发生。在一个实施方案中,肿瘤的手术去除在施用所述药物组合物之后约1-7天之间发生。在一个实施方案中,肿瘤的手术去除在施用所述药物组合物之后约7-14天之间发生。在一个实施方案中,肿瘤的手术去除在施用所述药物组合物之后约14-21天之间发生。本发明的方法允许施用α-GalBOEL以便在癌细胞的细胞表面上展示α-Gal表位。在一个实施方案中,所述方法还包括在所述肿瘤细胞上展示膜结合α-Gal表位。在一个实施方案中,本发明涵盖一种治疗受试者的方法,所述方法包括:a)提供:i)具有内源性抗Gal抗体和多个不可切除肿瘤的受试者,其中所述肿瘤的至少一个亚群经由选自由以下各项组成的组的程序可及:直接注射、通过内窥镜检查、支气管镜检查、膀胱镜检查、结肠镜检查、腹腔镜检查以及导管插入术注射,ii)如本文定义的药物组合物;以及b)使用所述程序肿瘤内注射所述组合物。在一个实施方案中,α-GalBOEL的α-Gal表位变得经调理。在一个实施方案中,调理的α-Gal表位通过使肿瘤细胞和细胞膜靶向抗原呈递细胞来诱导针对所述肿瘤的自体疫苗的产生。在一个实施方案中,受试者为人或小鼠。在一个实施方案中,受试者是人。在一个替代实施方案中,受试者是小鼠。根据本发明的另一方面,提供一种将α-GalBOEL引入小鼠中的肿瘤中的方法,所述方法包括:a)提供:i)小鼠,其(1)缺乏α1,3半乳糖基转移酶基因,(2)具有抗Gal抗体,以及(3)包括包含具有细胞表面的多个癌细胞的至少一种肿瘤;以及ii)α-GalBOEL;以及b)将α-GalBOEL引入至少一种所述肿瘤中以在癌细胞的细胞表面上展示α-Gal表位。自体肿瘤疫苗抗Gal靶向抗原呈递细胞已表明α-Gal表位可通过用α-Gal糖脂孵育肿瘤细胞来体外插入肿瘤细胞膜中。肿瘤细胞或肿瘤细胞膜与此类α-Gal糖脂的共孵育导致其自发体外插入肿瘤细胞膜中以及在这些细胞膜上表达α-Gal表位。通过各种分子生物学方法使用α1,3半乳糖基转移酶基因工程化为表达α-Gal表位的肿瘤细胞作为自体肿瘤疫苗进行研究。在其皮内注射之后,天然抗GalIgG抗体在疫苗接种部位处原位结合疫苗接种肿瘤细胞膜上的α-Gal表位并且使疫苗靶向抗原呈递细胞。虽然不必理解发明机制,但据信复合抗Gal的Fc部分与抗原呈递细胞上的Fcγ受体的结合诱导调理的疫苗接种肿瘤细胞膜有效摄取至抗原呈递细胞中。因此,自体肿瘤的未表征的肿瘤抗原也内化至抗原呈递细胞中。在将疫苗接种自体肿瘤细胞膜转运至引流淋巴结之后,抗原呈递细胞加工且呈递肿瘤抗原肽以用于活化肿瘤特异性细胞毒性T细胞和辅助T细胞(即,分别CD8+T细胞和CD4+T细胞)。表达α-Gal表位的肿瘤疫苗的功效的原理的证据在用表达α-Gal表位的黑素瘤细胞免疫且用相同、但缺乏α-Gal表位的黑素瘤细胞激发的小鼠实验模型中的研究中实现(LaTempleDC等人CancerRes.1999,59:3417-23和DeriyL等人CancerGeneTherapy2005;12:528-39)。在那些研究中使用的小鼠是针对α1,3半乳糖基转移酶基因的敲除小鼠(即,这些小鼠缺乏α-Gal表位且能够产生抗Gal抗体)。用工程化为表达α-Gal表位的黑素瘤细胞免疫的小鼠展示针对用相同但缺乏α-Gal表位的肿瘤细胞激发的有效免疫保护。相比之下,用缺乏α-Gal表位的肿瘤细胞免疫的小鼠未展示针对用缺乏α-Gal表位的活肿瘤细胞激发的保护性免疫应答。肿瘤疗法中的α-Gal糖脂本发明涵盖治疗具有实体肿瘤团块的患者。本发明的具体实施方案涵盖癌症患者的新型免疫疗法治疗,所述治疗目的在于通过将个体患者的自身肿瘤转化成自体肿瘤疫苗来使所述患者针对他或她的自身肿瘤病变进行免疫(参见以引用的方式并入本文的美国专利号5,879,675)。例如,′675专利教导肿瘤细胞和/或细胞膜的体外加工。在将这些细胞注射至患者中之后,通过抗Gal抗体使疫苗靶向APC并且引发针对自体肿瘤抗原的保护性免疫应答。然而,与本发明不同,′675专利未教导:i)用于通过天然抗Gal抗体诱导肿瘤的炎症、消退和/或破坏的体内肿瘤内治疗;或ii)在癌症患者内肿瘤内注射α-Gal糖脂之后在肿瘤细胞上体内展示α-Gal表位。在本发明的一个实施方案中,α-Gal糖脂可通过非手术肿瘤内注射(即,例如通过内窥镜检查、导管插入术等)或通过任何其他方法递送至包括肿瘤细胞的肿瘤病变中以用于将α-Gal糖脂或各种分子上的抗Gal结合表位体内引入至肿瘤中。化学疗法难治性转移的手术后复发据信是患有实体肿瘤的患者中死亡的最常见原因。这种复发性转移的高发病率(80%)已在患有胰腺癌和卵巢癌的患者中报道且在其他实体肿瘤如黑素瘤和结肠直肠癌、肺癌和乳腺癌中至稍微较低程度。许多这些复发性患者被认为具有终末期疾病,因为没有治疗可用于他们,并且他们在检测到转移之后的数周或数月内死亡。在一个实施方案中,本发明涵盖一种用于通过利用所有人天然产生作为其免疫球蛋白的大约1%的抗Gal抗体的事实消退和/或破坏肿瘤转移的治疗方法。所述抗Gal抗体的免疫潜力可用于消退和/或破坏任何肿瘤病变且通过肿瘤内注射携带α-Gal表位的糖脂(即α-GalBOEL)将所述肿瘤病变转化成原位自体肿瘤疫苗。因此,本文描述的发明可诱导所治疗肿瘤病变的消退和/或破坏。因此,在一个实施方案中,所治疗的肿瘤经历消退。在一个替代实施方案中,所治疗的肿瘤被破坏。在另一实施方案中,肿瘤(即,其展示α-Gal表位)经历消退,其中所述肿瘤选自黑素瘤或器官转移,如肝转移。在另一替代实施方案中,肿瘤(即,其展示α-Gal表位)被破坏,其中所述肿瘤选自黑素瘤或器官转移,如肝转移。在一个实施方案中,引入步骤由于将所治疗肿瘤转化成自体肿瘤疫苗而引起受试者的第二肿瘤的消退。在另一实施方案中,所述第二肿瘤选自黑素瘤或肝转移。在一个实施方案中,引入步骤引起受试者的第二肿瘤的破坏。在另一实施方案中,所述第二肿瘤选自黑素瘤或肝转移。许多α-Gal糖脂将自发地插入肿瘤细胞膜中,因为相较于水围绕的胶束核心,当包埋于细胞膜的脂质双层的外小叶中时α-Gal糖脂的疏水性(即,亲脂性)脂质尾处于更稳定的高能形式。先前已证明了称为神经节苷酯的其他类型的糖脂自发插入(并入)细胞膜中(KandaS等人JBiochem.(Tokyo).1982;91:1707-18和SpiegelS等人J.CellBiol.1985;100:721-26)。α-Gal糖脂插入肿瘤细胞膜中预期产生所述细胞膜表面上α-Gal表位的从头展示。α-Gal表位表达可通过包括但不限于补体介导的细胞溶解(CDC)和抗体依赖性细胞介导的细胞溶解(ADCC)的这类机制有助于抗Gal抗体介导的肿瘤细胞的消退和/或破坏,并且还可导致肿瘤坏死。抗Gal调理的肿瘤细胞膜然后将被抗原呈递细胞有效靶向,从而将所治疗的肿瘤病变转化成自体肿瘤疫苗。这种自体疫苗然后将刺激免疫系统来针对肿瘤抗原反应,从而产生所治疗患者的其他肿瘤病变和/或微转移内的表达这些抗原的肿瘤细胞的进一步消退和/或破坏。在一个实施方案中,受试者先前进行了治疗以手术去除肿瘤。在一个替代实施方案中,受试者先前未进行治疗来手术去除肿瘤,即本文描述的方法可在切除原发性肿瘤之前数周作为新辅助疗法进行。在一个实施方案中,α-GalBOEL的肿瘤内注射减小肿瘤的大小并且将所治疗肿瘤转化成自体肿瘤疫苗。虽然这种肿瘤将最终被切除,但据信在其切除之前,所治疗的肿瘤将引发针对展示相同肿瘤抗原的微转移的免疫应答。抗Gal抗体肿瘤消退和/或破坏的机制虽然不必理解发明机制,但据信通过所注射的α-Gal糖脂进行的肿瘤病变消退和/或破坏可包括生物化学和生理学基础。在一个实施方案中,所述方法进一步包括诱导肿瘤内炎症。肿瘤内注射可产生肿瘤相关毛细管的局部破裂,从而提供天然抗GalIgM和抗GalIgG抗体分子可及肿瘤内部。抗Gal抗体然后将能够与α-Gal糖脂胶束或单独α-Gal糖脂分子上的α-Gal表位相互作用,从而诱导补体的局部活化和补体裂解趋化因子C5a和C3a的产生。此外,C3b共价沉积至靶细胞上。补体活化然后起始局部炎症过程,所述炎症过程有助于通过所治疗肿瘤病变内的从头产生的C5a和C3a趋化因子指导的肿瘤内粒细胞、单核细胞、巨噬细胞和树突细胞迁移。炎症过程可由于α-Gal糖脂插入细胞膜中而进一步增强,从而引起内皮细胞的抗Gal活化(PalmetshoferA等人Transplantation.1998;65:844-53;PalmetshoferA等人Transplantation.1998;65:971-8)。内皮细胞活化和总体肿瘤细胞损伤可导致另外促炎性细胞因子和趋化因子的局部产生。这些局部分泌的细胞因子和趋化因子诱导巨噬细胞、树突细胞的另外迁移,以及淋巴细胞随后迁移至注射有α-Gal糖脂的病变中。这种细胞迁移由抗原呈递细胞和淋巴细胞上的促炎性细胞因子和趋化因子的受体介导(CravensPD和LipskyPEImmunol.CellBiol.2002;80:497-505)。炎症应答的初始诱导使免疫系统能够克服其检测发展中肿瘤病变的“隐身性质”的能力的普遍缺乏。这种炎症还使免疫系统能够克服实体肿瘤病变内由局部细胞因子环境诱导且通常防止淋巴细胞渗透至肿瘤中的免疫抑制微环境(MalmbergKJ.CancerImmunol.Immunother.2004;53:879-92;LugadeAA等人J.Immunol.2005;174:7516-23)。肿瘤细胞的破坏通过抗Gal结合至插入细胞膜中的α-Gal糖脂而发生。注射至肿瘤中的α-Gal糖脂可自发地插入肿瘤细胞膜的磷脂双层的外小叶中。抗GalIgM和/或抗GalIgG与所插入α-Gal糖脂上的α-Gal表位的随后结合经由补体依赖性细胞溶解(CDC)诱导所治疗肿瘤的消退和/或破坏。抗GalIgG分子与这些α-Gal表位的结合也有助于肿瘤细胞的抗体依赖性细胞溶解(ADCC)。在一个实施方案中,肿瘤经由补体依赖性细胞溶解(CDC)经历消退和/或破坏。在一个实施方案中,肿瘤经由抗体依赖性细胞溶解(ADCC)经历消退和/或破坏。在补体依赖性细胞溶解中,据信抗GalIgG和/或IgM分子与表达α-Gal表位的肿瘤细胞的结合(由于α-Gal糖脂插入)活化补体系统。随后,补体C5b-9膜攻击复合物由于这种补体活化而形成,然后在肿瘤细胞膜上“刺”孔,从而产生肿瘤细胞溶解。这种补体依赖性细胞溶解在猪内皮细胞溶解时类似地发现,从而导致异种移植物的超急性排斥(CollinsBH等人J.Immunol.1995;154:5500-10,)。在ADCC中,效应细胞是粒细胞、巨噬细胞和NK细胞。这些细胞由于抗Gal诱导的炎症过程而被吸引至病变。它们经由其Fcγ受体(FcγR)结合至抗GalIgG分子的Fc部分,所述抗GalIgG分子分子结合至插入肿瘤细胞膜中的α-Gal糖脂。一旦附着至肿瘤细胞,这些效应细胞就将其颗粒酶囊泡分泌至膜接触区域中,从而在肿瘤细胞膜中产生孔,由此诱导这些肿瘤细胞的破坏。证明了抗GalIgG在诱导表达α-Gal表位的细胞的ADCC破坏方面的功效,其中异种移植物猪细胞经由其α-Gal表位结合抗Gal(Galili,U.Immunol.Today1993,14:480-82)。类似的抗Gal介导的ADCC过程在肿瘤细胞经由在其细胞表面膜上表达的α-Gal表位结合抗Gal时发生(TanemuraM等人J.Clin.Invest.2000;105:301-10)。通过抗原呈递细胞摄取肿瘤细胞膜可产生针对自体肿瘤抗原的保护性免疫应答的诱导以便消退和/或破坏化学疗法难治性微转移。经由抗Gal依赖性补体活化结合至靶细胞上沉积的膜插入的α-Gal糖脂或C3b上的α-Gal表位的抗GalIgG抗体刺激抗原呈递细胞内化表达肿瘤抗原(即,例如,肿瘤相关抗原,TAA)的细胞膜。内化的肿瘤抗原然后可通过抗原呈递细胞从所治疗的肿瘤病变转运至引流淋巴结。这些肿瘤抗原然后进一步通过抗原呈递细胞加工且呈递为活化肿瘤特异性T细胞的免疫源性肿瘤肽。此过程产生全身性保护性抗肿瘤免疫应答(即,例如,自体肿瘤疫苗)的诱导。因此,注射有α-Gal糖脂的肿瘤病变最终转化成原位自体肿瘤疫苗,所述疫苗引发针对表达肿瘤抗原(如在所治疗的肿瘤病变中的那些肿瘤抗原)的微转移的免疫应答。作为临床治疗模式,α-Gal糖脂可通过各种方法施用至癌症病变,所述方法包括但不限于皮内注射(即,例如注射至黑素瘤肿瘤中);内镜注射(即,例如注射至结肠直肠肠道转移中);腹腔镜注射(即,例如注射至腹部卵巢、结肠、胃、肝或胰腺癌转移中(例如,注射在腹膜上或在肝中));经皮成像引导的针注射(即,例如注射至肺肿瘤中);支气管镜注射(即,例如注射至肺肿瘤中);结肠镜注射;或膀胱镜注射(即,例如注射至膀胱癌中)。因此,在一个实施方案中,引入包括以下程序,所述程序包括但不限于注射、成像引导的注射、内窥镜检查、支气管镜检查、膀胱镜检查、结肠镜检查、腹腔镜检查以及导管插入术。在一个实施方案中,引入包括非手术肿瘤内注射。例如,引入包括选自以下各项的程序:皮内注射、经皮成像引导的注射、内镜注射、支气管镜注射、膀胱镜注射、结肠镜注射以及腹腔镜注射。在一个实施方案中,将α-Gal糖脂(即α-GalBOEL)注射在选自下组的药学上可接受的溶液(即无菌溶液)中,所述组包括但不限于磷酸盐缓冲盐水(PBS)、盐水、公认安全(GRAS)的其他水溶液或其他赋形剂。在一个实施方案中,α-Gal糖脂的溶液还可包含脱氧胆酸酯,或可增加糖脂渗透至细胞膜中的其他温和洗涤剂。在一个实施方案中,本发明涵盖将α-Gal糖脂(即α-GalBOEL)肿瘤内注射至原发性肿瘤中作为在肿瘤切除手术之前提供的新辅助疗法。在一个实施方案中,通过α-Gal糖脂的手术前注射诱导的快速炎症应答导致减小肿瘤病变大小,以及将所述肿瘤病变转化成原位自体肿瘤疫苗。虽然不必理解发明机制,但据信所治疗肿瘤的免疫应答可最终帮助诱导在原发性肿瘤的手术切除时不可检测到的微转移的免疫破坏。进一步据信手术前施用可帮助预防疾病的复发,这是由于对常规辅助疗法(即,例如化学疗法和辐射)具有抗性且如原发性肿瘤一样表达肿瘤抗原的微转移的免疫破坏。这种新辅助疗法可施用至任何实体肿瘤或淋巴瘤,所述施用可以是直接注射或通过引导成像或任何其他已知的方法注射。根据本发明的另一方面,提供一种试剂盒,所述试剂盒包括如本文定义的药物组合物以及任选地根据如本文定义的方法来使用所述试剂盒的说明书。在一个实施方案中,所述试剂盒另外包括递送装置,如肿瘤内递送装置。在本说明书中引用的所有出版物和专利均以引用的方式并入本文,所述引用的程度就如同具体地且个别地指示将各个别公布或专利以引用的方式并入,并且以引用的方式并入本文以公开和描述与所述公布引用的内容相关的方法和/或材料。引用任何出版物都是因为它的公开内容在提交日期之前,而不应解释为认可本公开由于先前公开而无权先于所述公布。以下实施例意图仅作为本发明的实施方案的说明性实施例。所述实施例不应被视为限制本发明。合成在下文所描述的合成方法的描述中以及在所引用的用于制备起始材料的合成方法中,应理解,所有建议的反应条件,包括溶剂的选择、反应氛围、反应温度、实验的持续时间以及后处理(workup)程序可由本领域的技术人员选择。有机合成领域的技术人员了解,分子的不同部分上存在的官能度必须与所使用的试剂和条件相容。必要起始材料可通过有机化学的标准方法获得,并且可通过与其之内说明和/或引用的那些程序类似的程序获得。使用商业试剂(Acros,Aldrich和Fluka)进行反应;根据标准程序纯化无水溶剂。在硅胶600.040-0.063mm(Merck)上进行柱色谱法,在SephadexLH-20(GEHealthcare)柱上进行凝胶过滤。在真空中在30℃-40℃下去除溶剂。在硅胶60F254铝衬板(Merck)上进行薄层色谱法(TLC)。通过将TLC板浸入H3PO4(8%)的溶液中且随后加热(>150℃)来可视化化合物的斑点。1HNMR谱在30℃下记录在BrukerBioSpinGmbH(700MHz)光谱仪上;化学位移(δ,ppm)被称为内部D2O(δ4.750)、CDCl3(δ7.270)或CD3OD(δ3.500)的峰;偶联常数(J)以Hz测量。1HNMR的信号。糖类的NMR谱中的单糖残基的符号:I-β-GlcNAc(还原端)、II-β-Gal、III-α-Gal。MALDITOFMS谱被记录在BrukerDaltonicsUltraflexMALDITOF/TOF质谱仪(Germany)上。下文描述的合成方法可由本领域的技术人员用于制备(9Z,9Z)-(2R)-3-(((2-(6-((3-(((2R,3R,4R,5S,6R)-3-乙酰胺基-5-(((2S,3R,4S,5S,6R)-3,5-二羟基-6-(羟甲基)-4-(((2R,3R,4S,5R,6R)-3,4,5-三羟基-6-(羟甲基)四氢-2H-吡喃-2-基)氧基)四氢-2H-吡喃-2-基)氧基)-4-羟基-6-(羟甲基)四氢-2H-吡喃-2-基)氧基)丙基)氨基)-6-氧代己酰胺基)乙氧基)(羟基)磷酰基)氧基)丙烷-1,2-二-基双(十八-9-烯酸酯)(a-GalBOEL)。合成方案:(9Z,9′Z)-(2R)-3-(((2-(6-((3-(((2R,3R,4R,5S,6R)-3-乙酰胺基-5-(((2S,3R,4S,5S,6R)-3,5-二羟基-6-(羟甲基)-4-(((2R,3R,4S,5R,6R)-3,4,5-三羟基-6-(羟甲基)四氢-2H-吡喃-2-基)氧基)四氢-2H-吡喃-2-基)氧基)-4-羟基-6-(羟甲基)四氢-2H-吡喃-2-基)氧基)丙基)氨基)-6-氧代己酰胺基)乙氧基)(羟基)磷酰基)氧基)丙烷-1,2-二基双(十八-9-烯酸酯)的制备。向4-O-[3-O-(α-D-吡喃半乳糖基)-β-D-吡喃半乳糖基]-2-乙酰胺基-2-脱氧-β-D-吡喃葡萄糖苷β-氨基丙酯(II)(MendeleevCommunications,2002,(143-145)或Tetrahedron,61,(2005),4313-4321;52mg,0.086mmol)于无水DMF(2mL)中的溶液添加15μL的Et3N,接着添加DOPE-Ad-ONSu(III)(US8,013,131B2,100.6mg,1.00mmol)于CH2Cl2(2mL)中的溶液。将反应在室温下搅拌2小时,接着连续柱色谱法(第一在SephadexLH-20上,且第二在硅胶上,用CH2Cl2-EtOH-H2O;6∶5∶1洗脱)以得到标题化合物(I)(105.6mg,84%)。Rf0.5(CH2Cl2-EtOH-H2O;6∶5∶1)1HNMR(700MHz,CDCl3-CD3OD1∶1,30℃),δ,ppm,选择的:5.45-5.54(m,4H,2×-CH=CH-),5.34-5.43(m,1H,-OCH2-CHO-CH2O-),5.18(d,1H,J1,22.52,H-1III),4.61(d,1H,J1,27.57,H-1II),4.60(dd,1H,J2.87,J12.00,C(O)OCHHCHOCH2O-),4.56(d,1H,J1,28.39,H-1I),4.36(dd,1H,J6.8,J12.00,-C(O)OCHHCHOCH2O-),4.19(d,1H,J3,42.48,H-4II),4.13-4.18(m,2H,-CHO-CH2OP-),3.52-3.62(m,3H,PO-CH2-CH2-NH,-CH2-CHH-NH),3.29-3.35(m,1H,-CH2-CHH-NH),2.45-2.52(m,4H,2×-CH2-CO),2.36-2.45(m,4H,2×-CH2-CO),2.14-2.22(m,11H,2×(-CH2-CH=CH-CH2-),NHC(O)CH3),1.85-1.96(m,2H,O-CH2CH2CH2-NH),1.73-1.84(m,8H,COCH2CH2CH2CH2CO以及2×(COCH2CH2-),1.36-1.55(m,40H,20CH2),1.05(t,6H,J6.98,2CH3)。C70H126N3O26P;MALDIMS:m/z1480(MNa+H);1496(MK+H);1502(MNa+Na),1518(MNa+K)实施例1:用于证明与抗Gal抗体结合的ELISA将96孔板首先用α-GalBOEL(作为FSL-Galili(tri)TM获自Sigma,目录号F9432)涂覆。将50μLPBS添加至各孔。将α-GalBOEL在PBS中再悬浮至2mg/ml的浓度且将50μL添加至孔。通过将50μL跨板转移至孔中来进行连续稀释,从而确保每个孔在转移之前充分混合。将板静置过夜至干燥。这产生α-GalBOEL与所述孔通过所述分子的L(脂质)部分的强粘附。将150μL封闭缓冲液(1XPBS/1%BSA)添加至干燥孔。将板覆盖且在37℃下孵育2小时。将孔内容物丢弃且用PBS洗涤所述孔。将50μL第一抗Gal抗体(在此实施例中单克隆小鼠抗GalIgM,M86杂交瘤上清液)添加至各孔。将板在室温下孵育2小时。将板用200μL洗涤缓冲液(1XPBS,0.05%Tween)洗涤3次。将50μL第二山羊抗小鼠IgM-HRP溶液(AccurateChemical;目录号JGM035020)添加至各孔。将板覆盖且在室温下孵育1小时,并且然后用200μL洗涤缓冲液洗涤3次。将100μL标准OPD(邻苯二胺盐酸盐)溶液(例如Sigma;目录号P8287)添加至各孔,孵育5分钟且然后添加50μL终止溶液(1M硫酸)。立即在492nm(A492)下读取孔吸光度(参见图2)。图2示出当跨ELISA板增加α-GalBOEL的量时A492的增加。结合至ELISA孔的α-GalBOEL的量增加与单克隆抗Gal抗体与这些ELISA孔的结合增加之间的直接关联指示所述抗体结合至在所述孔中干燥的α-GalBOEL分子上的α-Gal表位。实施例2:补体依赖性细胞毒性和并入测定下文的测定定量插入细胞质膜中的α-GalBOEL的量和α-GalBOEL插入在刺激抗Gal介导的补体依赖性细胞毒性(CDC)中的功能影响两者。将α-GalBOEL滴定且与CHO-K1细胞一起孵育。将这些细胞固定且用于全细胞ELISA测定中以测定α-Gal并入至膜中,或与抗Gal抗体和人血清一起孵育以测量CDC(或在来自人血清的补体不存在下一般细胞毒性)。α-GalBOEL滴定和CHO-K1细胞制备如下滴定α-GalBOEL。将α-GalBOEL(2mg/ml(作为FSL-Galili(tri)TM获自Sigma,目录号F9432))的一个40μl等分部分解冻且超声处理30秒。将40μl磷酸盐缓冲盐水(PBS)添加至管且涡旋10秒。将25μl的此混合物添加至55μl的PBS且充分混合。重复这些稀释以得到处于所需浓度范围中的α-GalBOEL的完全滴定。将缺乏α-Gal表位的CHO-K1细胞在37℃下再悬浮于杜尔贝科氏PBS(DPBS)中并且在1000rpm下离心5分钟。吸出上清液且将细胞沉淀在450μlDPBS(37℃)中再悬浮至1×107个细胞/ml。再次洗涤细胞沉淀以去除所有痕量血清。CHO-K1细胞与α-GalBOEL的孵育将细胞悬浮液的等分部分(45μl)转移至α-GalBOEL的所有管且通过倒置轻轻混合并且在37℃下孵育30分钟。将细胞充分洗涤以去除过量未并入的α-GalBOEL。将所述管在200xg下离心5分钟且将细胞沉淀用900μl温热DPBS洗涤,在200xg下再次离心5分钟且再悬浮于250μl温热培养基中。将细胞悬浮液(25μl)转移至测定板(用于发光读出的标准白色96孔板(可自Corning获得))以进行CDC测定(A)或将50μl转移至用于细胞中ELISA的聚-d-赖氨酸涂覆的板(可自Sigma获得)(B)以测量并入至细胞膜中。补体依赖性细胞毒性/细胞溶解(CDC)测定将抗Gal抗体(来自一系列来源,在此实施例中含有小鼠抗Gal的血浆)添加(25μl/孔)至CDC测定板(A)且然后在37℃下孵育30分钟。将测定板在加热的离心管区块中在37℃下孵育另外30分钟。将人血清(含有活性补体)稀释于温热培养基中(至在测定中通过滴定获得的预定水平)并且将50μl添加至各孔。将板在37℃下下孵育30分钟。将板从孵育箱中去除并且使其在室温下平衡15分钟。将100μlCellTiterGlo试剂(Promega,G7572)添加至所述板的各孔。这种试剂发光与从溶解的细胞释放的ATP的量成比例。将所述板用箔覆盖且在板振荡器(400rpm)上孵育2分钟。使用标准96孔板阅读器测量发光输出(参见图3)。通过按照以上CDC测定程序,但用预先温热的培养基置换人血清来测量一般细胞毒性。通过以与用于以上CDC测定完全相同的方式添加100μlCellTitreGlo试剂至各孔来测量细胞死亡水平(参见图4)。图3示出通过增加α-GalBOEL的剂量来抑制补体依赖性细胞溶解。随着α-GalBOEL的剂量增加,如通过CellTitreGlo测量的细胞存活力由于阻断补体组分结合至细胞且溶解所述补体组分而增加。这种阻断通过以下方式来介导:α-GalBOEL胶束结合溶液中的抗Gal并且活化溶液中的补体级联,引起补体消耗,从而抑制表达α-Gal表位的细胞的补体介导的溶解。如果补体失活,则不发生细胞死亡。在人血清不存在下,直至500μg/ml,α-GalBOEL对细胞存活力也没有影响(图4)。表1描述在4个独立实验内α-GalBOEL对CDC的抑制的EC50值(α-GalBOEL的给出半最大反应的浓度)。平均EC50值是1.35μg/ml+/-1.48。直至500μg/ml也未观察到明显细胞毒性。表1:来自CDC测定的结果实验测试日期EC50(μg/ml)106/02/20141.36206/02/20141.24319/03/20141.38422/04/20141.43几何平均值1.35用于测量α-GalBOEL并入细胞中的细胞中ELISA为了测量α-GalBOEL并入CHO-K1细胞中,将50μl含有α-GalBOEL的CHO-K1细胞悬浮液转移至聚-D-赖氨酸涂覆的透明96孔板(B)。将板在1,000rpm下离心5分钟。为了固定细胞,将培养基去除,并且将100μL4%甲醛添加至各孔。将板在室温下在通风橱中孵育15分钟。将甲醛去除且将板用100μL/孔的1XTris缓冲盐水(TBS)洗涤两次。细胞中ELISA试剂盒(细胞中ELISA比色测定试剂盒,62200PierceLtd)用于测量α-GalBOEL的并入水平。将TBS去除并且添加100μL/孔的淬灭溶液且在室温下孵育20分钟。将淬灭溶液去除且将板用100μL/孔的1XTBS洗涤一次。添加100μL/孔的封闭缓冲液且在室温下孵育30分钟。去除封闭缓冲液且添加50μL/孔的稀释第一抗体(在此实施例中M86杂交瘤上清液,滴定以找到最佳浓度)。施加板密封剂且将板在4℃下孵育过夜。将第一抗体溶液去除且将板用100μL/孔的1X洗涤缓冲液洗涤三次。添加100μL/孔的HRP缀合的山羊抗人(或小鼠)IgG+IgM+IgA第二抗体。将板在室温下孵育30分钟。将板用200μL/孔的1X洗涤缓冲液洗涤三次。添加100μL/孔的TMB底物,且将板在室温下孵育,避光。通过在15分钟内(或在已经实现所需蓝色颜色时)添加100μl/孔的TMB终止溶液来终止反应。在终止反应的30分钟内测量在450nm下的吸光度(参见图5)。可从图5中看出,在如上所述孵育之后,可在CHO-K1细胞的表面上检测到α-GalBOEL。实施例3:补体沉积测定从生长培养物收获1×106个B16-F10细胞和CHO-K1细胞并且与500μg/mlαGalBOEL在PBS中在37℃下孵育1小时,在其之后将所述细胞用PBS洗涤3次。在洗涤之后,将CHO-K1细胞与2.5%正常(NHS)或热灭活的(HINHS)人血清一起在37℃下孵育10分钟。将B16-F10细胞与来自正常GT-/-小鼠(NMS)的2.5%血清或来自猪肾匀浆免疫的小鼠(INMS)的2.5%血清一起在37℃下孵育10分钟。将所述细胞放置在冰上且用冰冷细胞染色缓冲液(PBS+0.1%BSA)洗涤两次。将所述细胞与抗C3b(C3b,PierceMAI-70054,在细胞染色缓冲液中1∶1000稀释)或抗SC5b-9(MAC,QuidelA239,在细胞染色缓冲液中1∶100稀释)一起在冰上孵育30分钟。将所述细胞用冰冷细胞染色缓冲液洗涤两次且与FITC山羊抗小鼠IgG(Abcamab97022,在细胞染色缓冲液中1∶2000稀释)一起在冰上孵育30分钟。在用冰冷细胞染色缓冲液洗涤另外2次之后,将所述细胞再悬浮于冰冷细胞染色缓冲液加7-AAD(Biolegend420403)中。使用BeckmanCoulterCytomicsFC500流式细胞仪对细胞进行分析,其中数据捕获在FL-1通道中。所呈现的直方图上的数据在活细胞上门控。图6证明并入α-GalBOEL导致来自人或小鼠血清的补体蛋白C3b和MAC沉积至CHOK1(A&B)和B16小鼠黑素瘤细胞(C&D)的表面上。实施例4:α-GalBOEL在α1,3-半乳糖基转移酶敲除(GTKO)小鼠黑素瘤模型中的体内活性进行体内药效动力学实验以评定α-GalBOEL在具有B16-F10黑素瘤细胞的GTKO小鼠黑素瘤模型中的作用。选择GTKO小鼠品系,因为如同人一样,它不表达α-Gal抗原。因此,可将GTKO小鼠用猪肾膜匀浆免疫以产生类似于在人中天然观察到的那些的IgG和IgM抗Gal抗体的滴度。诱导了这种免疫应答,因为猪肾膜在细胞膜上和细胞间基质中包含高浓度的a-Gal表位。使用B16-F10细胞,因为它们是唯一已知的不表达α-Gal表位的鼠细胞。在B16-F10黑素瘤模型中,将小鼠在两侧腹上注射培养的B16-F10细胞,在一侧上将它们注射1×106个黑素瘤细胞以产生原发性肿瘤,并且在相对侧腹注射减少的细胞数目(1×104个黑素瘤细胞)以产生还被称为继发性肿瘤的“远端转移”的模型。当达到预定肿瘤直径时,将原发性肿瘤肿瘤内注射α-GalBOEL或媒介物对照。所记录的关键终点是“远端”肿瘤的生长,这用于测量药剂在整个体内引发有效保护性抗肿瘤免疫应答的能力。测试了0.1-2.5mg的α-GalBOEL的剂量。当100μL媒介物中的0.1-mg至1-mgα-GalBOEL剂量在B16-F10模型中并行测试时,观察到α-GalBOEL的剂量依赖性活性应答。如在图7中所例示,与0.1-mg和0.5-mg剂量相比,1mgα-GalBOEL一致地赋予更高保护程度。还已显示,用猪肾膜匀浆免疫GTKO小鼠诱导抗GalIgG和IgM抗体的产生,所述抗体对于在B16-F10黑素瘤模型中赋予α-GalBOEL介导的保护免于远端肿瘤发展来说是必要的。如可在图8中看出,1mgα-GalBOEL保护80%的产生抗Gal的GTKO小鼠免于继发性肿瘤发展。相比之下,1mgα-GalBOEL在非免疫GTKO小鼠(即,缺乏抗Gal的小鼠)中缺乏保护活性。这些观察结果指示α-GalBOEL介导的针对发展远端转移的保护性抗肿瘤免疫应答的诱导依赖于所治疗受试者中抗Gal的存在。在不存在抗Gal的情况下,没有观察到显著保护性抗肿瘤免疫应答。实施例5:α-GalBOEL和抗PD-1抗体组合显示优于单独抗PD-1抗体的优异体内活性若干证据表明T细胞上的两种受体PD-1和CTLA-4充当负调控抗肿瘤免疫应答的检查点。同时,靶向的PD-1和CTLA-4的保健抗体药物的标准在临床试验中显示用于治疗晚期黑素瘤的前景。测试在上述GTKO小鼠黑素瘤模型中,合成糖脂α-GalBOEL的抗肿瘤作用是否可以与免疫检查点抑制剂即PD-1单克隆抗体(mAb)的组合增强。假定由呈递加工的肿瘤抗原肽的抗原呈递细胞诱导的肿瘤特异性T细胞的初始增殖可通过免疫检查点如抗PD1单克隆抗体的抑制增强。因此,预期用α-GalBOEL和抗PD1抗体两者组合治疗携带肿瘤的受试者将比仅用这两种治疗中的一种治疗受试者更有效。为了研究这种假设,将小鼠在一侧腹用106个B16-F10肿瘤细胞激发以产生原发性肿瘤且在相对侧腹用104个B16-F10细胞激发以诱导转移样继发性肿瘤。在肿瘤细胞注射之后五天,将原发性肿瘤仅用0.1和0.25mgα-GalBOEL(代替图7中的实验中的1.0mg)或PBS(=媒介物对照)肿瘤内治疗。在第8天或第10天之后,将小鼠用250μg抗PD-1单克隆抗体RMP1-14(Biolegend(目录号114102))或用PBS腹膜内治疗。值得注意,克隆RMP1-14在若干研究中用于研究在肿瘤模型中的抗PD-1作用。用PD-1或媒介物治疗在每个实验中重复三次(小鼠接受总计四个250-μg剂量)。如可在图9中看出,相较于单独α-GalBOEL和抗PD-1,α-GalBOEL与抗PD-1抗体的组合在预防远端转移的生长方面具有优异活性。这指示抗PD-1与α-GalBOEL在引发比在使用单独α-GalBOEL和抗PD-1抗体的治疗中所观察到的更有效的保护性抗肿瘤免疫应答方面协同作用。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1