带式换能器超声治疗的制作方法
本申请要求于2014年4月18日提交的美国临时申请61/981660的优先权的权益,其全部内容通过引用方式并入本文中。
技术领域
本发明的几个实施方案总体涉及实现美容和/或医疗效果的非侵入性、半侵入性和/或侵入性的基于能量的治疗。例如,一些实施方案总体涉及具有用于安全且有效地执行各种治疗过程的线性、弯曲、平面和/或三维的超声治疗聚焦区的装置、系统和方法。治疗系统的不同的实施方案可以通过减少治疗时间和/或降低治疗能量来改善美容效果和患者结果,减少治疗时间和/或降低治疗能量可以提高舒适度和美容效果。在不同的实施方案中,超声换能器具有呈一个或多个线、条、带和/或平面的形式的治疗聚焦区。
背景技术:
许多美容过程涉及可能需要侵入性手术的侵入性过程,其可能对生物相容性和无菌性提出更多要求。患者不仅必须忍受数周的恢复时间,而且还经常需要经受危险的麻醉程序以进行美容治疗。涉及刺穿或切割皮肤表面以进入皮肤表面下的靶组织的传统美容过程往往涉及对生物相容性和无菌性的更高要求。例如利用射频(RF)和激光治疗的某些传统的基于能量的治疗必须加热或治疗从皮肤表面开始的组织,这影响了在皮肤表面和皮肤表面下一定深度处的靶组织之间的所有中间组织。
技术实现要素:
尽管已经披露了用于美容和医疗目的的基于能量的治疗,但除了申请人自己的工作之外,申请人不知道有什么程序能通过用带形治疗聚焦区技术扩大在特定的靶区域治疗的组织的面积和体积,利用定靶的和精确的超声波经由热途径带来可见且有效的美容效果来成功地实现美感的组织加热和/或治疗效果。治疗可以包括加热、凝固和/或消融(包括例如热疗,热剂量测定,细胞凋亡和细胞溶解)。在不同的实施方案中,与透热疗法或一般的整体加热技术相比,带式治疗给组织提供了改善的热加热和治疗。在不同的实施方案中,带式治疗提供了在特定深度范围加热和/或治疗组织而不影响邻近组织的能力。一般而言,透热疗法和整体加热技术通常涉及加热皮肤表面并通过皮肤表面和所有下面的组织传导热量以使热量到达皮肤表面下方的靶深度处的组织。在不同的实施方案中,带式治疗在皮肤表面下方的特定的规定深度范围提供定靶的加热和治疗,而不加热皮肤表面和/或在皮肤表面和靶组织之间的中间组织。这种偏移的带式治疗减少了皮肤表面的损伤和相关的疼痛,并且仅在规定的、定靶的组织深度处治疗组织。因此,本发明的实施方案可用于治疗皮肤表面下方的特定深度范围中的组织,而不加热皮肤表面。在一些实施方案中,通过将靶组织预热至升高的温度,带式治疗也可以用于预备好靶深度处的组织以便二次超声治疗,因此可以进行二次治疗,但时间和/或能量减少,舒适性增加。
根据不同的实施方案,美容超声治疗系统和/或方法可以非侵入性地产生单个或多个美容治疗区和/或热治疗点、线、带、条、平面、区域、体积和/或形状,其中超声波聚焦在皮肤表面下的一个或多个深度处的组织内的治疗区域中的一个或多个位置中。一些系统和方法在组织中的不同位置处提供美容治疗,其中治疗区域处于各种深度、高度、宽度和/或位置。在一个实施方案中,方法和系统包括换能器系统,其配置为用于向多于一个的感兴趣区域,例如在至少两个感兴趣的治疗位置和/或区域之间,提供超声治疗。在一个实施方案中,方法和系统包括换能器系统,其配置为用于向多于一个的感兴趣区域,例如在组织内的感兴趣区域中的不同位置(例如,处于固定的或可变的深度、高度、宽度、方向等等)中的至少两条线之间,提供超声治疗。在不同的实施方案中,线可以是直的、弯曲的、连续的和/或非连续的。在一些实施方案中,能量束被分裂以在用于美容治疗区和/或用于组织中感兴趣区域中的成像的两个、三个、四个或更多聚焦区(例如,多个焦线,多焦线)处聚焦。聚焦区的位置可以轴向地、横向地或以其它方式定位在组织内。一些实施方案可以配置为用于空间控制,例如通过聚焦线的定位,改变换能器和可选运动机构之间的距离或角度,和/或改变聚焦到或未聚焦到感兴趣区域的能量的角度,和/或配置为用于时间控制,例如通过控制换能器的频率、驱动幅度和定时的变化。在一些实施方案中,多个治疗区域的位置可以通过极化、相极化、双相极化和/或多相极化来实现。结果,治疗区域的位置、感兴趣区域中的治疗区域、加热区域和/或损伤的数量、形状、尺寸和/或体积的变化以及热条件可以随时间被动态地控制。关于极化和调整的额外细节在2014年2月28日提交的美国专利申请14/193234中披露,其美国公开号为2014-0257145,其通过引用的方式全部并入本文中。
在一个实施方案中,美学成像和治疗系统包括具有壳体的手持式探头,壳体包围超声换能器,超声换能器配置为向聚焦区的组织应用超声治疗。在一个实施方案中,聚焦区是线。在一个实施方案中,聚焦区是二维区域或平面。在一个实施方案中,聚焦区是体积。在不同的实施方案中,聚焦区治疗的治疗区域是线性的、弯曲的、矩形的和/或平面的。在不同的实施方案中,治疗区域的尺寸取决于换能器的尺寸。治疗可以在线和/或平面中进行。在不同的实施方案中,治疗聚焦区的宽度为5-50mm,5-30mm,5-25mm,10-25mm,10mm-15mm,15mm-20mm,10mm,15mm,20mm,25mm,或其中的任何范围(包括但不限于12mm-22mm)。在不同的实施方案中,可以移动聚焦区以扫掠第一位置和第二位置之间的体积。在不同的实施方案中,一个或多个聚焦区位置可以以基本上线性的顺序位于美容治疗区内。在不同的实施方案中,一个或多个聚焦区位置利用一个、两个或更多个运动机构定位以形成美容治疗区内的治疗区域的任何形状。在一个实施方案中,第一组位置位于第一美容治疗区内,第二组位置位于第二美容治疗区内,所述第一区不同于所述第二区。在一个实施方案中,第一美容治疗区包括基本上线性顺序的第一组位置,第二美容治疗区包括基本上线性顺序的第二组位置。在一些非限制性实施方案中,换能器可以配置为用于皮肤表面以下1.5mm、3mm、4.5mm、6mm、小于3mm、1.5mm至3mm之间、1.5mm至4.5mm之间、大于4.5mm、大于6mm,以及在0.1mm-3mm、0.1mm-4.5mm、3mm-7mm、3mm-9mm、0.1mm-25mm、0.1mm-100mm的范围内的任何地方,以及其中任何深度(包括例如4.5mm-6mm、1mm-20mm、1mm-15mm、1mm-10mm、5mm-25mm,以及其中任何深度)的组织深度处的治疗区。在一个实施方案中,美容治疗区是连续的。在一个实施方案中,美容治疗区没有间隔。在一个实施方案中,一系列单独的美容治疗区具有的治疗间隔在从约0.05mm至约25mm的范围内(例如,0.05-0.1mm,0.05-1mm,0.2-0.5mm,0.5-2mm,1-10mm,0.5-3mm,5-12mm)。在不同的实施方案中,治疗间隔具有恒定的间距、可变的间距、重叠的间距和/或不重叠的间距。
在一个实施方案中,超声换能器配置为在换能器表面上提供在约1W/cm2至100W/cm2之间的范围内的治疗强度(例如,1-50,10-90,25-75,10-40,50-80W/cm2及其中的任何范围和值)。在一个实施方案中,超声换能器配置为提供在约1W至约100W之间的范围内的超声治疗的声功率以及约1MHz至约10MHz的频率,以热地加热组织。在不同的实施方案中,换能器模块配置为提供在约1W至约100W之间的范围内的超声治疗的声功率(例如5-40W,10-50W,25-35W,35-60W,35W,40W,50W,60W)以及约1MHz至约10MHz的频率,以热地加热组织。在一个实施方案中,声功率的范围可以是从1W到约100W,频率范围从约1MHz至约12MHz(例如,3.5MHz,4MHz,4.5MHz,7MHz,10MHz,3-5MHz),或声功率的范围从约10W至约50W,频率范围从约3MHz至约8MHz。在一个实施方案中,声功率和频率是约40W和约4.3MHz,以及约30W和约7.5MHz。在不同的实施方案中,换能器模块配置为在没有间距或具有0.1-2mm(例如,0.4,0.5,0.6,0.7,0.8,0.9,1.0,1.1,1.2,1.5mm)的间距的情况下输送能量。在不同的实施方案中,间距是恒定的或可变的。在不同的实施方案中,换能器模块配置为以10-500ms的接通时间来输送能量(例如,30-100,90-200,32,35,40,50,60,64,75,90,100,112,200,300,400ms和其中的任何范围)。在不同的实施方案中,换能器模块配置为以1-200ms(例如,4,10,22,45,60,90,100,150ms以及其中的任何范围)的停歇时间来输送能量。在一个实施方案中,由该声功率产生的声能可以在约0.01焦耳(“J”)至约10J之间或约2J至约5J之间。在一个实施方案中,声能处于小于约3J的范围内。在不同的实施方案中,在单次剂量通过中由该声功率产生的声能可以在约1至500J之间(例如,20-310,70,100,120,140,150,160,200,250,300,350,400,450J和其中的任何范围)。在不同的实施方案中,治疗可以涉及1、2、3、4、5、10次或更多次剂量通过。
在本文披露的几个实施方案中,非侵入性超声被用于实现以下效果中的一个或多个:组织加热,组织预加热,面部除皱,眉提升,下巴提升,眼部治疗,祛皱,祛疤,烧伤治疗,纹身移除,静脉移除,静脉减少,对汗腺的治疗,多汗症的治疗,减肥或减脂和/或减脂肪团,晒斑去除,痤疮治疗,丘疹减少。在几个实施方案中提供了皮肤皱纹的治疗。在另一个实施方案中,系统、装置和/或方法可以应用于生殖器区域(例如,阴道复原和/或阴道收紧,例如用于收紧阴道的支持组织)。在本文中描述的几个实施方案中,该过程完全是美容行为,而不是医学行为。例如,在一个实施方案中,本文中描述的方法不必由医生执行,而是在水疗中心或其他美学机构中执行。在一些实施方案中,系统可用于皮肤的非侵入性美容治疗。
在一个实施方案中,减少圆柱形超声换能器的焦点增益差异的方法包括提供包括凸表面和凹表面的圆柱形换能元件,其中所述表面之一(例如,凹表面)包括多个电极(或例如电导体或电气材料),该方法还包括随后向电极施加电流,由此将超声能量引导到焦点深度处的线性聚焦区。超声能量在线性聚焦区产生减小的焦点增益差异。凹表面可以镀银。凸表面可以包括无覆层区域和多个有覆层区域。多个有覆层区域可以包括烧制的银以形成多个电极。凸表面上的特征可以改为在凹表面上。
在一个实施方案中,边缘噪声的减少有利于组织的有效且一致的治疗,其中圆柱形换能元件配置为向焦点深度处的线性组织热治疗区应用超声治疗。
在一个实施方案中,边缘噪声的减少有利于材料的有效且一致的加热,其中材料是由化合物、粘合剂和食物组成的组中的任何一种。
在一个实施方案中,用于减少焦线处的边缘噪声的超声换能系统包括圆柱形换能元件和配置为驱动圆柱形换能元件的电源。圆柱形换能元件配置为将超声能量施加到焦点深度处的线性聚焦区。圆柱形换能元件包括凸表面和凹表面。凹表面镀有电导体,例如银。凸表面包括无覆层区域和一个或多个有覆层区域,其中所述一个或多个有覆层区域包括银以形成电极。电源与电极电连通。有覆层区域配置为减小焦点深度处的线性聚焦区处的焦点增益差异。
在一个实施方案中,用于减小焦线处的边缘噪声的超声换能系统包括圆柱形换能元件和配置为驱动圆柱形换能元件的电源。圆柱形换能元件配置为将超声能量施加到焦点深度处的线性聚焦区。圆柱形换能元件包括凸表面和凹表面。凸表面镀银。凹表面包括无覆层区域和一个或多个有覆层区域,其中一个或多个有覆层区域包括银以形成电极。电源与电极电连通。有覆层区域配置为减小焦点深度处的线性聚焦区处的焦点增益差异。
在一个实施方案中,用于减小聚焦区处的焦点增益差异的有覆层的换能器包括圆柱形换能元件,其包括凸表面和凹表面。凹表面镀银。凸表面包括无覆层区域和多个有覆层区域。多个有覆层区域包括形成多个电极的银。圆柱形换能元件配置为向焦点深度处的线性聚焦区应用超声治疗。有覆层区域配置为减少在线性聚焦区处的焦点增益差异。
在一个实施方案中,用于减小聚焦区处的焦点增益差异的有覆层的换能器包括圆柱形换能元件,其包括凸表面和凹表面。在一个实施方案中,凸表面被电镀。在一个实施方案中,凹表面被电镀。在一个实施方案中,凹表面包括无覆层区域和多个有覆层区域。在一个实施方案中,凸表面包括无覆层区域和多个有覆层区域。多个有覆层区域包括形成多个电极的导体。圆柱形换能元件配置为向焦点深度处的线性聚焦区应用超声治疗。有覆层区域配置为减小线性聚焦区处的焦点增益差异。
在一个实施方案中,美学治疗系统包括圆柱形换能元件,其包括凸表面和凹表面。在一个实施方案中,凹表面镀有银以形成电极。在一个实施方案中,凸表面镀有银以形成电极。在一个实施方案中,凸表面包括无覆层区域和一个或多个有覆层区域,其中一个或多个有覆层区域包括银以形成电极。在一个实施方案中,凹表面包括无覆层区域和一个或多个有覆层区域,其中一个或多个有覆层区域包括银以形成电极。圆柱形换能元件配置为向焦点深度处的线性组织热治疗区应用超声治疗。有覆层区域配置为减小热治疗区处的焦点增益差异。圆柱形换能元件容纳在超声手持探头内。在一个实施方案中,超声探头包括壳体、圆柱形换能元件和运动机构。超声换能器可在壳体内移动。运动机构附连到超声换能器并且配置为使超声换能器在壳体内沿着线性路径移动。
在一个实施方案中,美学成像和治疗系统包括超声探头,超声探头包括壳体、有覆层的超声换能器和运动机构。超声换能器可在壳体内移动,超声换能器包括圆柱形换能元件和成像元件。圆柱形换能元件配置为向焦点深度处的线性组织热治疗区应用超声治疗。圆柱形换能元件具有构造为用于放置成像元件的开口。圆柱形换能元件包括凸表面和凹表面。在一个实施方案中,整个凹表面镀有银。在一个实施方案中,整个凸表面镀有银。在一个实施方案中,凸表面包括无覆层部分和一个或多个有覆层区域。在一个实施方案中,凹表面包括无覆层部分和一个或多个有覆层区域。有覆层区域包括银以形成电极。有覆层区域配置为减小热治疗区处的焦点增益差异。运动机构附连到超声换能器并且配置为使超声换能器在壳体内沿着线性路径移动。
如本文中提供的,换能元件的表面之一(凸表面或凹表面)被导电材料(包括但不限于银或别的金属或合金)完全覆盖(或至少覆盖90%),另一个表面(凸表面或凹表面)具有有覆层和无覆层部分的多个区域(或图案或拼接部分),其涂覆有导电材料(包括但不限于银或别的金属或合金)。这在几个实施方案中可能是有利的,因为它有利于均匀加热(例如,降低温度尖峰或波动)。在一些实施方案中,两个表面(凸表面和凹表面)包含有覆层和无覆层部分的多个区域(或图案或拼接部分)。虽然本文中描述了凸表面和凹表面,但是在一些实施方案中,这些表面之一或两者可以是平面的。此外,如本文中所述的凸表面或凹表面可以是多面的(例如,具有多个凸面和/或凹面),并且还包括具有曲率(例如,一个或多个小于180度的角度)的表面。在几个实施方案中,有覆层和无覆层区域的图案可以包括,一个、两个或更多个有覆层区域和一个、两个或更多个无覆层区域,其中有覆层区域覆盖表面的至少60%、70%、80%或90%。此外,无覆层区域可以被认为是在这样一种程度上未涂覆的,即它没有导电覆层——在某些实施方案中,无覆层区域可以具有其他类型的表面覆层。
在不同的实施方案中,超声系统包括具有换能元件(例如,扁平的,球形的,圆形的,圆柱形的,环形的,具有环的,凹的,凸的,波状外形的或其他形状的换能元件)的换能器。
在不同的实施方案中,超声换能系统包括换能元件(例如,圆柱形换能元件)和配置为驱动换能元件的电源,其中换能元件配置为向焦点深度处的线性聚焦区施加超声能量,其中换能元件包括第一表面和第二表面,其中第一表面包括导电覆层,其中第二表面包括至少一个导电的有覆层区域和至少一个没有涂覆导电覆层的无覆层区域,其中第二表面上的所述至少一个有覆层区域包括当所述电源与所述至少一个有覆层区域电连通时形成电极的导电材料,其中第二表面上的所述至少一个有覆层区域配置为减小在焦点深度处的线性聚焦区处的边缘噪声。
在不同的实施方案中,超声换能系统包括圆柱形换能元件和配置为驱动圆柱形换能元件的电源,其中圆柱形换能元件配置为向焦点深度处的线性聚焦区施加超声能量。在一些实施方案中,圆柱形换能元件包括第一表面和第二表面,其中第一表面包括覆层,其中第二表面包括至少一个有覆层区域和至少一个无覆层区域,其中第二表面上的所述至少一个有覆层区域包括当电源与所述至少一个有覆层区域电连通时形成电极的导电材料,其中第二表面上的所述至少一个有覆层区域配置为减小在焦点深度处的线性聚焦区处的边缘噪声。
在一实施方案中,无覆层区域不包括导电材料。在一实施方案中,导电材料是金属(例如,银、金、铂、汞和/或铜,或合金)。在一实施方案中,第一表面是凹表面,第二表面是凸表面。在一实施方案中,第一表面是凸表面,第二表面是凹表面。在一实施方案中,圆柱形换能元件容纳在超声手持探头内,其中超声探头包括壳体、圆柱形换能元件和运动机构,其中超声换能器可在壳体内移动,其中运动机构附连到超声换能器并且配置为使超声换能器在壳体内沿着线性路径移动。在一实施方案中,运动机构自动地移动圆柱形换能元件,以将焦点深度处的治疗区域加热到40-65摄氏度之间的范围内的(例如,40-45,40-50,40-55,45-60,45-55,45-50摄氏度,和其中的任何值)温度。在一实施方案中,边缘噪声的减少有利于在治疗区域中产生均匀(例如,完全均匀,基本上均匀,大约大致均匀)的温度。在一实施方案中,边缘噪声的减少有利于组织的有效和一致的治疗,其中圆柱形换能元件配置为对组织中的焦点深度处的治疗区应用超声治疗。在一实施方案中,边缘噪声的减少降低了峰值,从而使焦点深度周围的差异减小了75-200%(例如,75-100,80-150,100-150,95-175%,和其中的任何值)。在一实施方案中,边缘噪声的减少降低了峰值,从而使焦点深度周围的强度的差异为5mm或更小(例如,4.5,4,3.5,3,2.5,2,1.5,1,0.5或更小)。在一实施方案中,边缘噪声的减少将焦点增益差异减小在到0.01-10(例如,1-5,2-8,0.5-3,和其中的任何值)的范围内。在一实施方案中,电源配置为驱动圆柱形换能元件以在焦点深度处的组织中产生在42-55摄氏度范围内的温度(例如,43-48,45-53,45-50摄氏度,和其中的任何值)。在一实施方案中,温度传感器位于壳体上邻近壳体中的声窗,其配置为测量皮肤表面处的温度。在一实施方案中,系统包括一个或多个成像元件,其中圆柱形换能元件具有开口,其配置为用于放置一个或多个成像元件。在一实施方案中,成像元件配置为确认系统和皮肤表面之间的声耦合的水平。在一实施方案中,成像元件配置为通过由下列方式构成的组中的任一个来确认系统和皮肤表面之间的声耦合的水平:散焦成像和电压驻波比(VSWR)。在一实施方案中,成像元件配置为测量皮肤表面下面的焦点深度处的靶组织处的温度。在一实施方案中,成像元件配置为利用由声辐射力脉冲(ARFI)、剪切波弹性成像(SWEI)和衰减测量所构成的组中的任一个来测量皮肤表面下面的焦点深度处的靶组织处的温度。
在几个实施方案中,用圆柱形超声换能器加热组织的方法包括提供圆柱形换能元件,圆柱形换能元件包括第一表面、第二表面、有覆层区域和无覆层区域。在一些实施方案中,有覆层区域包括电导体。在一些实施方案中,无覆层区域不包括电导体。在一些实施方案中,第一表面包括至少一个有覆层区域,其中第二表面包括无覆层区域和多个有覆层区域,向有覆层区域施加电流,从而将超声能量引导到焦点深度处的线性聚焦区,其中超声能量在线性聚焦区产生焦点增益的减小。
在几个实施方案中,美容方法利用加热源(例如,圆柱形超声换能器)非侵入性地和非消融地加热组织以将患者皮肤下的区域加热5-25摄氏度,同时使得皮肤表面处的温度保持相同或增加至不引起不适的温度(例如,增加1-5,1-10,1-15摄氏度)。这种差别有利于患者的舒适度。在一个实施方案中,加热在5-120分钟的周期上以递增的方式进行,其中温度分级地或逐渐地增加。加热可以由本文所述的圆柱形超声换能器系统执行。可选地,可以随后通过将温度增加另一个5-25摄氏度来施加消融或凝固能量。初始的预热步骤或整体加热是有利的,因为其允许施加较少的能量以获得凝固/消融状态。在一个实施方案中,用不同于超声换能器的加热源执行初始预热步骤。例如,代替超声波或者除超声波之外,可以使用射频、微波、光、对流、转换和/或导电热源。
在几个实施方案中,加热组织的非侵入性的美容方法包括将美容加热系统应用于皮肤表面,其中美容加热系统包括手持式探头。在一些实施方案中,手持式探头包括壳体,壳体包围超声换能器,超声换能器配置为将皮肤表面下的组织加热到处于40-50摄氏度范围内的组织温度(例如,44-47,41-49,45-50摄氏度,和其中的任何值)。在一些实施方案中,超声换能器包括圆柱形换能元件,其包括第一表面、第二表面、有覆层区域和无覆层区域,其中有覆层区域包括电导体,其中第一表面包括至少一个有覆层区域,其中第二表面包括无覆层区域和多个有覆层区域。在一些实施方案中,该方法包括将电流施加到多个有覆层区域,从而将超声能量引导到焦点深度处的线性聚焦区,其中超声能量在线性聚焦区产生焦点增益的减小,从而将在线性聚焦区中的处于焦点深度处的组织加热到处于40-50摄氏度范围内的组织温度,以便进行持续时间小于1小时(例如,1-55,10-30,5-45,15-35,20-40分钟和其中的任何值)的美容治疗,从而减少组织中脂肪组织的体积。
在一实施方案中,焦点增益的减小有利于组织的有效且一致的治疗,其中圆柱形换能元件配置为向焦点深度处的热治疗区应用超声治疗。在一实施方案中,焦点增益的减小降低了峰值,使得焦点深度周围的差异减小25-100%(例如,30-50,45-75,50-90%,以及其中的任何值)。在一实施方案中,焦点增益的减小降低了峰值,从而使焦点深度周围的强度的差异为5mm或更小(例如,1,2,3,4mm或更小)。在一实施方案中,焦点增益的减小将焦点增益差异减小在0.01-10的范围内(例如,0.06,3,4.5,8或其中的任何值)。在一实施方案中,电导体是金属。在一实施方案中,第一表面是凹表面,第二表面是凸表面。在一实施方案中,第一表面是凸表面,第二表面是凹表面。在一实施方案中,圆柱形换能元件容纳在超声手持探头内,其中所述超声探头包括壳体、圆柱形换能元件和运动机构,其中超声换能器可在壳体内移动,其中运动机构附连到超声换能器并且配置为使超声换能器在壳体内沿着线性路径移动。在一实施方案中,运动机构自动地移动圆柱形换能元件,以将焦点深度处的治疗区域加热到在40-65摄氏度之间的范围内的温度。在一实施方案中,圆柱形换能元件在焦点深度处的组织中产生42-55摄氏度范围内的温度。在一实施方案中,该方法还包括用一个或多个成像元件对组织进行成像,其中圆柱形换能元件具有开口,其配置为用于放置一个或多个成像元件。在一实施方案中,该方法还包括用来自成像元件的图像确认系统和皮肤表面之间的声耦合的水平。在一实施方案中,该方法还包括用成像元件确认系统和皮肤表面之间的声耦合的水平,所述成像元件使用了由下列方式构成的组中的任一种方式:散焦成像和电压驻波比(VSWR)。在一实施方案中,该方法还包括利用成像元件测量皮肤表面下的焦点深度处的靶组织处的温度。在一实施方案中,该方法还包括利用成像元件测量皮肤表面下的焦点深度处的靶组织处的温度,所述成像元件利用了由声辐射力脉冲(ARFI)、剪切波弹性成像(SWEI)和衰减测量所构成的组中的任一个。
以上总结和在下面进一步详细阐述的方法描述了从业者采取的某些动作;然而,应当理解,它们还可以包括由别的人群发出的那些动作的指令。因此,诸如“施加超声能量”的动作包括“指示施加超声能量”。
此外,根据本文提供的描述,适用的领域将变得显而易见。应当理解,描述和具体实例仅仅是为了说明的目的,并不打算限制本文中披露的实施方案的范围。
附图说明
本文所描述的附图仅用于说明的目的,并不打算以任何方式限制本发明的范围。根据详细描述和附图,本发明的实施方案将被更充分地理解,其中:
图1是根据本发明的不同实施方案的超声系统的示意图。
图2是根据本发明的不同实施方案的耦合到感兴趣区域的超声系统的示意图。
图3表示根据一实施方案的美容治疗系统中的圆柱形换能器的示意性侧视横截面图。尽管这里示出了圆柱形的换能器,但换能器不必是圆柱形的。在几个实施方案中,换能器具有一个或多个形状或构造,其引起边缘效应,如超声波的传送的差异、尖峰或其它不一致。例如,换能器可以具有一个或多个非线性(例如,弯曲)部分。
图4表示图3的被切开的圆柱形换能器的示意性等距侧视图。
图5A-5B表示根据一实施方案的美容治疗系统中的通过运动机构移动的圆柱形换能器的示意性等距侧视图,其中热治疗区(TTZ)扫过治疗区域。
图6表示根据一实施方案的美容治疗系统中的圆柱形换能元件的示意性分解等距视图。
图7表示根据一实施方案的美容治疗系统中的具有运动机构的图6的圆柱形换能元件的示意性等距视图。
图8表示根据一实施方案的美容治疗系统的探头壳体中的具有图7的运动机构的圆柱形换能元件的示意性等距视图。
图9是根据本发明的不同实施方案的换能器的一部分的示意性局部剖视图。
图10是根据本发明的不同实施方案的超声系统的局部侧视剖视图。
图11A-11B是示意图和图表,示出了根据包括圆柱形换能元件的换能器的实施方案的在20mm深度处的标准压强分布。
图12A-12B是示意图和图表,示出了根据图11A-11B的包括圆柱形换能元件的换能器的实施方案的在15mm深度处的标准压强分布。
图13A-13B是示意图和图表,示出了根据图11A-11B的包括圆柱形换能元件的换能器的实施方案的在13mm深度处的标准压强分布。
图14A-14B是示意性图表,示出了根据包括圆柱形换能元件的换能器的实施方案的在20mm深度处的标准压强分布。
图15A-15B是示意性图表,示出了根据图11A-11B的包括圆柱形换能元件的换能器的实施方案的在15mm深度处的标准压强分布。
图16A-16B是示意性图表,示出了根据图11A-11B的包括圆柱形换能元件的换能器的实施方案的在13mm深度处的标准压强分布。
图17是图表,示出了包括圆柱形换能元件的换能器的实施方案在不同的功率水平下,随着时间的经过,猪的肌肉的温度。
图18是在实验性的治疗之后的猪肌肉的照片,其证实了利用包括圆柱形换能元件的换能器的实施方案加热的已确认的线和平面。
图19是穿过图18中的猪肌肉的横截面,示出了线性热治疗区。
图20是穿过图19中的猪肌肉的正交横截面,示出了平面热治疗区。
图21是根据本发明一实施方案的组合式成像和圆柱形治疗换能器的横截面图。
图22是根据图21的组合式成像和圆柱形治疗换能器的侧视图。
图23是图表,示出了具有成像元件的圆柱形元件的实施方案的横跨方位的谐波压力。
图24是图表,示出了具有成像元件的有覆层圆柱形元件的实施方案的横跨方位的谐波压力。
图25是图表,示出了与具有成像元件的有覆层圆柱形元件的实施方案相比,具有成像元件的圆柱形元件的实施方案的横跨方位的谐波压力。
图26是根据本发明一实施方案的有覆层换能器的侧视图,其包括具有一个或多个有覆层区域的圆柱形换能元件。
图27是图表,示出了圆柱形换能元件的两个实施方案的横跨方位的焦点增益。
图28是示意性图表,示出了根据有覆层换能器的实施方案的在聚焦区远侧大约5mm的深度处的标准压强分布,其中所述有覆层换能器包括具有一个或多个有覆层区域的圆柱形换能元件。
图29是示意性图表,示出了根据图28的有覆层换能器的实施方案的在焦点深度处的标准压强分布。
图30是示意性图表,示出了根据图28的有覆层换能器的实施方案的在焦点深度近侧大约2mm的深度处的标准压强分布。
图31是根据本发明一实施方案的有覆层换能器的侧视图。
图32是根据本发明一实施方案的有覆层换能器的侧视图。
图33是根据本发明一实施方案的有覆层换能器的侧视图。
图34是根据本发明一实施方案的有覆层换能器的侧视图。
图35是根据本发明一实施方案的有覆层换能器的侧视图。
图36是根据本发明一实施方案的有覆层换能器的侧视图。
图37是根据本发明一实施方案的有覆层换能器的侧视图。
图38是根据本发明一实施方案的有覆层换能器的侧视图。
图39表示根据本发明一实施方案的与时间和温度相关的用于获得各种理论细胞杀死比例的图表。
图40表示根据本发明一实施方案的与时间和温度相关的用于获得各种理论细胞杀死比例的图表。
图41是根据本发明一实施方案的表格,其列出了在理论上实现组织中1%存活比例的等效剂量,列出了温度和时间。
图42是根据本发明一实施方案的适用于细胞存活比例的等效剂量的与时间和温度相关的图表。
图43表示根据本发明一实施方案的圆柱形换能器输出的模拟,其示出了多个脉冲的线性叠加。
图44是根据本发明一实施方案的变迹换能器的俯视图。
图45表示根据图44的实施方案的具有变迹换能器的声压概图。
图46是图表,示出了根据本发明一实施方案的来自活体内的猪模型治疗剂量研究的实施方案的温度曲线。
图47是根据本发明一实施方案的用于等效剂量研究的设置的图表。
图48表示根据本发明一实施方案的与治疗研究的时间、温度和遍数计数相关的累积剂量。
图49是根据本发明一实施方案的用于治疗研究的具有目标温度和时间的表格。
图50是根据本发明一实施方案的用于等效热剂量治疗研究的换能器治疗设置的不同实施方案的表格。
图51是根据本发明一实施方案的由换能器导致的热过度剂量部位的图像。
图52是根据本发明一实施方案的将时间和温度与靶目标温度相关联的图表。
图53是根据本发明一实施方案的换能器和治疗区域的等距侧视图。
图54是表示根据本发明一实施方案的沿着轴的速度和位置的图表。
图55是表示根据本发明一实施方案的沿着轴的速度和位置的图表。
图56是表示根据本发明一实施方案的沿着轴的幅度和位置的图表。
图57是表示根据本发明一实施方案的沿着轴的速度和位置的图表。
图58是表示根据本发明一实施方案的沿着轴的速度和位置的图表。
图59表示根据本发明一实施方案的不重叠的治疗。
图60表示根据本发明一实施方案的部分重叠和部分不重叠的治疗。
图61表示根据本发明的不同实施方案的治疗区域。
图62是表示根据本发明一实施方案的强度和深度的图表。
图63是根据本发明一实施方案的换能器和具有多个热治疗区的治疗区域的等距侧视图。
图64是根据本发明一实施方案的在运动机构上包括多个超声元件的系统的示意性侧视图。
具体实施方式
以下描述阐述了实施方案的示例,其不是用于限制本发明或其教导、应用或其用途。应当理解,在全部附图中,相应的附图标记表示相同或相应的部件和特征。在本发明的不同实施方案中提出的具体示例的描述仅是为了说明的目的,并且不是用于限制本文所披露的本发明的范围。此外,具有所陈述的特征的多个实施方案的复述不是用于排除具有附加特征的其他实施方案或包含所陈述特征的不同组合的其它实施方案。此外,一个实施方案中的特征(例如在一个附图中)可以与其他实施方案的描述(和附图)组合。
在不同的实施方案中,用于组织的超声治疗的系统和方法配置为提供美容治疗。本发明的不同实施方案解决了由施用超声治疗所带来的潜在挑战。在不同的实施方案中,减少了为了在靶组织处进行所需的临床方法的所需美容的和/或治疗学的治疗而创建热治疗区(本文中也称为“TTZ”)的时间和/或能量的量。在不同的实施方案中,利用超声能量对皮肤表面下或皮肤表面处的组织,如表皮、真皮、颈阔肌、淋巴结、神经、筋膜、肌肉、脂肪和/或表浅肌肉腱膜系统(“SMAS”),进行非侵入性治疗。在不同的实施方案中,不治疗皮肤表面下或皮肤表面处的组织,例如表皮、真皮、颈阔肌、淋巴结、神经、筋膜、肌肉、脂肪和/或SMAS。超声能量可以聚焦在一个或多个治疗区,可以是未聚焦的和/或散焦的,并且可以应用于感兴趣的区域以实现美容和/或治疗效果。在不同的实施方案中,系统和/或方法通过加热、热治疗、凝固、消融和/或组织紧缩(包括例如热疗,热剂量测定,细胞凋亡和溶解)向组织提供非侵入性皮肤病治疗。在一个实施方案中,皮肤组织体积增加。在一个实施方案中,脂肪组织体积减小或减少。
在不同的实施方案中,靶组织是,但不限于,皮肤、眼睑、眼睫毛、眼眉、泪阜、鱼尾纹、皱纹、眼、鼻、口、舌、牙齿、牙龈、耳朵、脑、胸部、背部、臀部、腿部、手臂、手、腋窝、心脏、肺、肋、腹、胃、肝、肾、子宫、乳房、阴道、阴茎、前列腺、睾丸、腺、甲状腺、内脏器官、毛发、肌肉、骨、韧带、软骨、脂肪、脂肪小叶、脂肪组织、脂肪团、皮下组织、植入组织、植入器官、淋巴、肿瘤、囊肿、脓肿或一部分神经中的任一种,或其任意组合。在本文披露的几个实施方案中,非侵入性超声用于实现以下效果中的一种或多种:面部除皱,眉提升,下巴提升,眼部治疗,祛皱,祛疤,减脂,脂肪团外观的减少,皮肤皱纹治疗,烧伤治疗,纹身移除,静脉减少,对汗腺的治疗,多汗症的治疗,晒斑去除,痤疮治疗和丘疹去除。在一些实施方案中,在相同的治疗期间实现两种、三种或更多种有益效果,并且可以同时实现。
本发明的不同实施方案涉及控制能量向组织的传递的装置或方法。在不同的实施方案中,不同形式的能量可以包括声、超声、光、激光、射频(RF)、微波、电磁、辐射、热、低温、电子束、基于光子的、磁、磁共振和/其他能量形式。本发明的不同的实施方案涉及将超声能量束分开成多个束的装置或方法。在不同的实施方案中,装置或方法可用于在任何程序中改变超声声能的传递,例如但不限于,治疗性超声、诊断超声、使用超声的非破坏性测试(NDT)、超声波焊接、涉及将机械波耦合到物体的任何应用,以及其他过程。一般而言,对于治疗性超声,通过利用基于孔径的聚焦技术集中声能来实现组织效应。在一些情况下,高强度聚焦超声(HIFU)以这种方式用于治疗目的。在一个实施方案中,通过在特定位置(例如,深度,宽度)应用治疗性超声而创建的组织效应可以被称为热治疗区的创建。通过在特定位置创建热治疗区,可以非侵入性地或远程地从皮肤表面偏移地进行组织的热和/或机械加热、凝固和/或消融。
系统概述
在公开号为2011-0112405的美国专利申请中描述了超声治疗和/或成像装置的不同的实施方案,其是来自国际公开WO2009/149390的国家阶段的公开,其均通过引用的方式全部并入本文中。
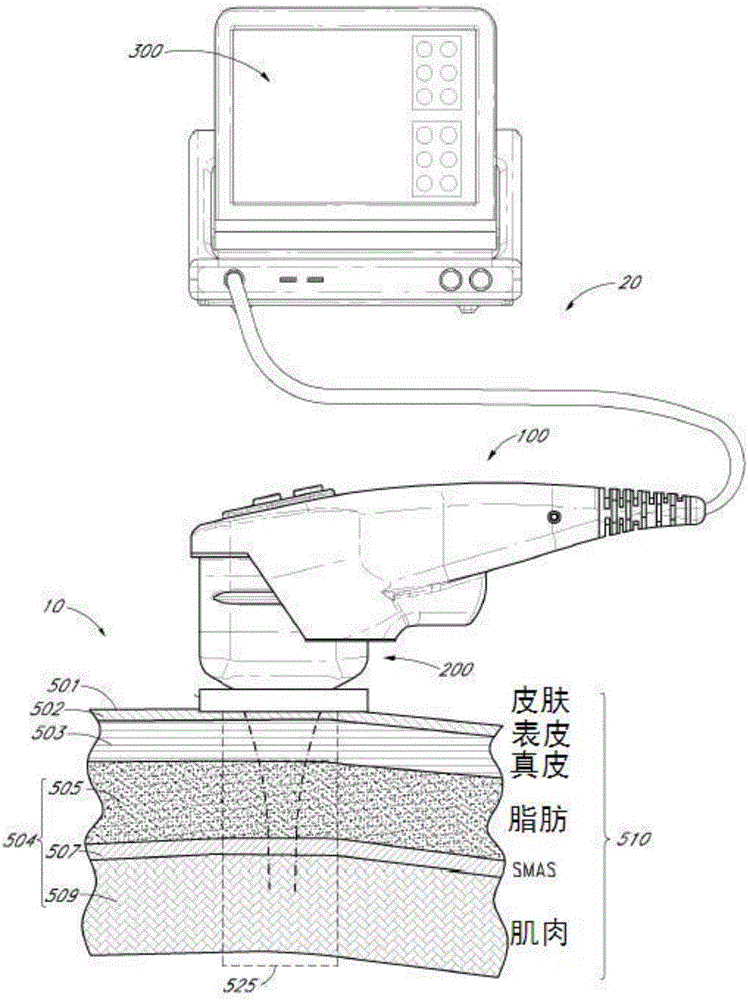
参考图1中的图示,超声系统20的实施方案包括手柄100,模块200和控制器300。手柄100可以通过接口130耦合到控制器300,接口130可以是有线或无线接口。接口130可以通过连接器145耦合到手柄100,接口130的远端可以连接到电路345上的控制器连接器。在一个实施方案中,接口130可以从控制器300向手柄100传输可控电力。在不同的实施方案中,控制器300可以配置为用于与手柄100和模块200一起操作,以及操作整个超声系统20的功能。在不同的实施方案中,控制器300配置为用于与具有一个或多个可移除模块200、200'、200”等的手柄100一起操作。控制器300可以包括交互式图形显示器310,其可以包括触摸屏监视器和允许用户与超声系统20交互的图形用户界面(GUI)。如图所示,图形显示器315包括触摸屏界面315。在不同的实施方案中,显示器310设置和显示操作条件,操作条件包括设备激活状态、治疗参数、系统消息和提示以及超声图像。在不同的实施方案中,控制器300可以配置为例如包括具有软件和输入/输出设备的微处理器,用于控制电子和/或机械扫描和/或换能器的多路传输和/或换能器模块的多路传输的系统和装置,用于电力输送的系统,用于监测的系统,用于感测探头和/或换能器的空间位置和/或换能器模块的多路传输的系统,和/或用于处理用户输入和记录治疗结果的系统等。在不同的实施方案中,控制器300可以包括系统处理器和各种模拟和/或数字控制逻辑,诸如微控制器、微处理器、现场可编程门阵列、计算板和相关组件中的一个或多个,所述相关组件包括固件和控制软件,其能与用户控制和接口电路以及用于通信、显示、接口连接、存储、文件整理和其他有用功能的输入/输出电路和系统连接。在系统程序上运行的系统软件可以配置为控制所有初始化、计时、水平设置、监视、安全监视以及用于实现用户定义的治疗目的的所有其他超声系统功能。此外,控制器300可以包括各种输入/输出模块,例如开关、按钮等,其也可适当地配置以控制超声系统20的操作。在一个实施方案中,控制器300可以包括一个或多个数据端口390。在不同的实施方案中,数据端口390可以是USB端口,蓝牙端口,红外数据端口,并行端口,串行端口等等。数据端口390可以位于控制器300的前部、侧部和/或后部,并且可以用于访问存储装置、打印装置、计算装置等。超声系统20可以包括锁395。在一个实施方案中,为了操作超声系统20,锁395应被解锁以使得可以激活电源开关393。在一个实施方案中,锁395可以经由数据端口390(例如,USB端口)连接到控制器300。可以通过将访问密钥(例如,USB访问密钥)、硬件加密狗等插入到数据端口390中来解锁锁395。控制器300可以包括紧急停止按钮392,其可以容易地接近以紧急停用。
如图1中所示,在一个实施方案中,手柄100包括一个或多个手指激活的控制器或开关,例如150和160。在一个实施方案中,手柄100可以包括可拆卸的模块200。在其他实施方案中,模块200可以是不可拆卸的。模块200可以利用闩锁件或耦合器140机械地耦合到手柄100。接口引导件235可以用于帮助将模块200耦合到手柄100。模块200可以包括一个或多个超声换能器280。在一些实施方案中,超声换能器280包括一个或多个超声元件281。模块200可以包括一个或多个超声元件281。元件281可以是治疗元件和/或成像元件。手柄100可以包括只进行成像的模块200,只进行治疗的模块200,成像和治疗模块200等。在一个实施方案中,通过手柄100提供成像。在一个实施方案中,控制模块300可以经由接口130耦合到手柄100,并且图形用户界面310可以配置为控制所述模块200。在一个实施方案中,控制模块300可以向手柄100提供电力。在一个实施方案中,手柄100可以包括电源。在一个实施方案中,开关150可以配置为用于控制组织成像功能,并且开关160可以配置为用于控制组织治疗功能。
在一个实施方案中,模块200可以耦合到手柄100。模块200可以发射和接收能量,例如超声能量。模块200可以电耦合到手柄100,并且这种耦合可以包括与控制器300通信的接口。在一个实施方案中,接口引导件235可以配置为在模块200和手柄100之间提供电子通信。模块200可以包括各种探头和/或换能器构造。例如,模块200可以配置为组合式的双模式成像/治疗换能器,耦合的或共同封装的成像/治疗换能器,分开的治疗和成像探头等。在一个实施方案中,当模块200插入或连接到手柄100时,控制器300自动检测它并更新交互式图形显示器310。
在不同的实施方案中,用超声能量对皮肤表面下的或甚至在皮肤表面处的组织(例如表皮、真皮、皮下组织、筋膜和SMAS和/或肌肉)进行非侵入性治疗。组织还可以包括血管和/或神经。超声能量可以是聚焦的、未聚焦的或散焦的,并且应用于感兴趣区域以实现治疗效果,所述感兴趣区域包括表皮、真皮、皮下组织、筋膜和SMAS中的至少一个。图2是例如利用声学凝胶耦合到感兴趣区域10的超声系统20的示意图。参考图2中的图示,超声系统20的实施方案包括手柄100、模块200和控制器300。在不同的实施方案中,感兴趣区域10的组织层可以在患者的身体的任何部分。在不同的实施方案中,组织层在患者的头部、面部、颈部和/或身体区域中。感兴趣区域10的组织的横截面部分包括皮肤表面501,表皮层502,真皮层503,脂肪层505,SMAS 507和肌肉层509。组织还可以包括下皮504,其可以包括真皮层503下面的任何组织。这些层的组合总体上可以称为皮下组织510。图2中还示出了治疗区525,其是表面501下面的主动治疗区域。在一个实施方案中,表面501可以是患者500的皮肤的表面。虽然在本文中可以用针对组织层的治疗的实施方案作为示例,但系统可以应用于身体中的任何组织。在不同的实施方案中,系统和/或方法可以用在面部、颈部、头部、手臂、腿部或身体中任何其他位置的肌肉(或其他组织)上。在不同的实施方案中,治疗可以应用于面部、头部、颈部、颏下区域、肩膀、手臂、背部、胸部、臀部、腹部、胃部、腰部、侧腹、腿部、大腿或身体内或身体上的任何其他位置。
使用圆柱形换能器的带式治疗
在不同的实施方案中,换能器280可以包括一个或多个治疗元件281,其可具有对应于各种聚焦区几何形状的各种形状。在一个实施方案中,换能器280包括单个治疗元件281。在一个实施方案中,换能器280不具有多个元件。在一个实施方案中,换能器280不具有元件的阵列。在几个实施方案中,本文所述的换能器280和/或治疗元件281可以是扁平的,球形的,圆形的,圆柱形的,环形的,具有环的,凹的,凸的,波状外形的和/或具有任何形状。在一些实施方案中,本文所述的换能器280和/或治疗元件281不是扁平的,球形的,圆形的,圆柱形的,环形的,具有环的,凹的,凸的,和/或波状外形的。在一个实施方案中,换能器280和/或治疗元件281具有机械聚焦。在一个实施方案中,换能器280和/或治疗元件281不具有机械聚焦。在一个实施方案中,换能器280和/或治疗元件281具有电聚焦。在一个实施方案中,换能器280和/或治疗元件281不具有电聚焦。尽管这里讨论了圆柱形换能器和/或圆柱形元件,但是换能器和/或元件不必是圆柱形的。在几个实施方案中,换能器和/或元件具有一个或多个形状或构造,其引起边缘效应,如超声波的传送的差异、尖峰或其它不一致。例如,换能器和/或元件可以具有一个或多个非线性(例如,弯曲)部分。换能器可以以聚焦的、平面的或未聚焦的单元件、多元件或阵列换能器(包括1维,2维和环形阵列;线性、曲线、扇形或球形阵列;球形地、圆柱形地和/或电子地聚焦的、散焦的和/或有透镜的源)的任意组合的形式由一个或多个单独的换能器和/或元件构成。在一个实施方案中,换能器不是多元件换能器。在一个实施方案中,换能器280可以包括具有直径的球形碗状件和一个或多个凹表面(具有各自的半径或直径),所述凹表面几何学上地聚焦到组织表面(例如皮肤表面501)下的焦点深度278处的单个点TTZ 550。在一个实施方案中,换能器280可以在三维上径向对称。例如,在一个实施方案中,换能器280可以是径向对称的碗状件,其配置为在空间中的单个点上产生焦点。在一些实施方案中,换能器不是球形的。在一些实施方案中,元件不是球形的。
在不同的实施方案中,增加用于超声程序的聚焦区位置的尺寸(例如宽度,深度,面积)和/或数量可能是有利的,因为其允许在各种各样的组织宽度、高度和/或深度对患者进行治疗,即使换能器280的焦点深度278是固定的。这可以提供协同的结果和使单个治疗期的临床结果最大化。例如,在单个表面区域下的较大治疗区域处的治疗允许组织治疗的较大的总体积,其可以加热较大的组织体积,并且其可以导致胶原的形成和收紧得到增强。另外,例如在不同深度的较大治疗区域影响不同类型的组织,从而产生不同的临床效果,它们一起提供增强的整体美容结果。例如,表面治疗可以降低皱纹的可见性,而较深的治疗可以诱导皮肤收紧和/或胶原生长。同样,在相同或不同深度的各个位置处的治疗可以改善治疗。在不同的实施方案中,可以使用具有较大聚焦区(例如,与点聚焦区相比的线性聚焦区)的换能器来实现较大的治疗面积。
在一个实施方案中,如图3和4中所示,换能器280包括圆柱形换能元件281。在图4中,具有凹表面282和凸表面283的圆柱形换能元件281的视图被剖开以示出从凹表面至线性TTZ 550的能量发射。圆柱形换能元件281沿其纵向轴线(X轴,方位)线性地延伸,沿Y轴(高程(elevation))具有弯曲的横截面。在一个实施方案中,圆柱形表面在圆柱形表面的曲率中心的焦点深度(z轴)处具有半径,以使得TTZ 550聚焦在半径的中心。例如,在一个实施方案中,圆柱形换能元件281具有像圆柱体一样延伸的凹表面,其产生沿着线(例如治疗线)延伸的聚焦区,例如TTZ 550。聚焦区TTZ 550沿着圆柱形换能元件281的宽度(沿着X轴,方位)在与圆柱形换能元件281的纵向轴线平行的线上延伸。如图3中所示,TTZ 550是在页面中和/或页面外延伸的线。在圆柱形换能元件281的不同的实施方案中,凹表面将超声能量引导到线性TTZ 550。圆柱形换能元件281不必是圆柱形的;在一些实施方案中,元件281是具有一个或多个弯曲或非线性部分的换能元件。
在不同的实施方案中,换能器280可以包括一个或多个换能元件281。换能元件281可以包括压电活性材料,例如锆钛酸铅(PZT)或任何其它压电活性材料,例如压电陶瓷,晶体,塑料,和/或复合材料,以及铌酸锂,钛酸铅,钛酸钡和/或偏铌酸铅。在不同的实施方案中,除了压电活性材料之外或代替压电活性材料,换能器可以包括配置为用于产生辐射和/或声能的任何其它材料。在一个实施方案中,当圆柱形换能元件281包括由电刺激激发的压电陶瓷材料时,材料可以膨胀或收缩。膨胀或收缩的量与陶瓷中的边界条件以及在陶瓷中产生的电场的大小有关。在常规的高强度聚焦超声(HIFU)设计的一些实施方案中,前表面(例如患者侧)耦合到水,并且换能器280的后表面耦合到通常为空气的低阻抗介质。在一些实施方案中,尽管陶瓷在后分界面处自由膨胀,但是由于显著的声阻抗差异,基本上没有机械能量从陶瓷耦合到空气。这导致在陶瓷背面处的这个能量反射并离开前(或患者侧)表面。如图3-5B的实施方案中所示,通过将陶瓷形成、铸造和/或机械加工成正确的曲率半径来产生焦点。在一个实施方案中,扁平的换能器材料被弯曲以形成圆柱形换能器。在不同的实施方案中,换能器280和/或治疗元件281可以配置为以不同的频率和治疗深度操作。换能器性质可以由焦距(FL)确定,焦距有时被称为焦点深度278。焦点深度278是从凹入的圆柱形表面至聚焦区TTZ 550的距离。在不同的实施方案中,焦点深度278是当探头的壳体抵靠皮肤表面放置时,离开距离270和治疗深度279之和。在一个实施方案中,离开距离270或偏移距离270是换能器280和探头壳体上的透声部件230的表面之间的距离。治疗深度279是皮肤表面501下面至靶组织的组织深度279。在一个实施方案中,在弯曲尺寸中的孔径的高度增大或最大化,以对与加热组织的能力相关的总焦点增益具有直接影响。例如,在一个实施方案中,对于6mm或更小的治疗深度,使在弯曲尺寸中的孔径的高度最大化。在一个实施方案中,当孔径增大时(例如,减小光圈),实际的加热区域变得更靠近表面。
在一个实施方案中,换能器可以配置为具有6mm、2-12mm、3-10mm、4-8mm、5-7mm的焦点深度278。在其他实施方案中,可以使用焦点深度278的其他合适的值,例如小于约15mm,大于约15mm,5-25mm,10-20mm等的焦点深度278。换能器模块可以配置为在不同的靶组织深度施加超声能量。在一个实施方案中,治疗为20mm或更小(例如,0.1mm-20mm,5-17mm,10-15mm)。在一个实施方案中,达到6mm或更小的装置具有13.6mm的曲率半径(ROC),治疗深度与ROC的比率为大约44%。在一个实施方案中,元件的高度为22mm。在一个实施方案中,使用20mm的治疗深度的纵横比,孔径高度将为74.5mm,ROC为45mm。
如图5A-5B、7、9和10中所示,在几个实施方案中,系统可以包括移动机构285,其配置为在一个、两个、三个或更多方向上移动包括圆柱形换能元件281的换能器280。在一个实施方案中,移动机构285可以在由标记为290的箭头所表示的线性方向上(一个或两个方向)移动,以便使TTZ 550移动通过组织。在不同的实施方案中,移动机构285可以在一个、两个和/或三个线性维度上和/或在一个、两个和/或三个旋转维度上移动换能器。在一个实施方案中,移动机构285可以在多达六个自由度上移动。TTZ550的移动可以伴随着换能器连续地传递能量以产生治疗区域552。在一个实施方案中,移动机构285可以自动地使圆柱形换能元件281移动越过治疗区域的表面,以使得TTZ550可以形成治疗区域552。
如图6、7和8中所示,圆柱形换能元件281可以连接到运动机构285并放置在模块200或探头内部。在不同的实施方案中,移动机构285或运动机构285移动换能器280和/或治疗元件281,以使得相应的TTZ 550移动以治疗更大的治疗区域552。在不同的实施方案中,移动机构285配置为使换能器在模块或探头内移动。在一个实施方案中,换能器由换能器保持器保持。在一个实施方案中,换能器保持器包括沿着运动约束轴承移动的套筒,运动约束轴承例如为线性轴承,即杆(或轴),以确保换能器的可重复的线性运动。在一个实施方案中,套筒是防止绕花键轴旋转的花键轴套,但是任何保持运动路径的导向件都是合适的。在一个实施方案中,换能器保持器由运动机构285驱动,运动机构285可位于手柄中或模块中或探头中。在一个实施方案中,运动机构285包括止转棒轭、运动构件和磁耦合中的任何一个或多个。在一个实施方案中,磁耦合帮助移动换能器。运动机构285的一个好处是其为成像和/或治疗目的提供了超声换能器的更有效、精确和准确的使用。相对于固定在壳体内的空间中的多个换能器的常规固定阵列,这种类型的运动机构的一个优点是固定阵列是分开固定距离的。通过在控制器的控制下将换能器放置在轨道(例如,线性轨道)上,系统和装置的实施方案除了效率、精度和准确度之外还提供了适应性和灵活性。可以通过运动机构285沿着受控运动对成像和治疗定位进行实时和接近实时的调节。除了基于可能通过运动机构285进行的增量调节来选择几乎任何分辨率的能力之外,如果成像检测到异常或有利于治疗间隔和靶向的变化的条件,也可以进行调节。在一个实施方案中,在模块中可以包括一个或多个传感器。在一个实施方案中,在模块中可以包括一个或多个传感器以确保移动构件和换能器保持器之间的机械耦合确实被耦合。在一个实施方案中,编码器可以位于换能器保持器的顶部上,传感器可以位于模块的一部分中,或反之亦然(交换)。在不同的实施方案中,传感器是磁传感器,例如巨磁阻效应(GMR)或霍尔效应传感器,编码器是磁体、磁体集合或多极磁条。传感器可以被定位为换能器模块初始位置。在一个实施方案中,传感器是接触压力传感器。在一个实施方案中,传感器是装置表面上的接触压力换能器,以感测装置或换能器在患者身上的位置。在不同的实施方案中,传感器可以用于在一个、二个或三个维度上映射装置或装置中的部件的位置。在一个实施方案中,传感器配置为感测装置(或其中的部件)和患者之间的位置、角度、倾斜、取向、布置、高程或其他关系。在一个实施方案中,传感器包括光学传感器。在一个实施方案中,传感器包括滚珠传感器。在一个实施方案中,传感器配置为在一个、二个和/或三个维度上映射位置以计算患者身上的皮肤或组织上的治疗区域或线之间的距离。
在不同的实施方案中,运动机构285可以是可被发现对于换能器的移动有用的任何机构。在一个实施方案中,运动机构285包括步进电机。在一个实施方案中,运动机构285包括蜗轮。在不同的实施方案中,运动机构285位于模块200中。在不同的实施方案中,运动机构285位于手柄100中。在不同的实施方案中,运动机构285可以提供线性、旋转、多维的运动或致动,并且运动可以包括空间中的点、线和/或取向的任何集合。根据几个实施方案,可以使用用于运动的不同的实施方案,包括但不限于,直线、圆形、椭圆形、弧形、螺旋形、空间中的一个或多个点的集合,或任何其它1维、2维或3维位置和姿态的运动的实施方案。运动机构285的速度可以是固定的或者可以由用户可调节地控制。在一个实施方案中,用于图像序列的运动机构285的速度可以不同于用于治疗序列的运动机构的速度。在一个实施方案中,运动机构285的速度可由控制器控制。
在一些实施方案中,从换能器传递的能量被打开和关闭,形成非连续治疗区域552,以使得TTZ 550在各个TTZ 550位置之间以治疗间隔地移动。例如,治疗间隔可以是约1mm、1.5mm、2mm、5mm、10mm等等。在几个实施方案中,探头可以进一步包括移动机构,其配置为按序列引导超声治疗,以使得以线性或基本上线性的序列形成多个TTZ 550。例如,换能器模块可以配置为沿着第一线性序列和第二线性序列形成多个TTZ550,所述第二线性序列以大约2mm和3mm之间的治疗间隔与第一线性序列分开。在一个实施方案中,用户可以手动地移动换能器模块使其越过治疗区域的表面,从而创建多个TTZ的相邻线性序列。
在一个实施方案中,TTZ可以从第一位置扫掠到第二位置。在一个实施方案中,TTZ可以重复地从第一位置扫掠到第二位置。在一个实施方案中,TTZ可以从第一位置扫掠到第二位置,并且返回到第一位置。在一个实施方案中,TTZ可以从第一位置扫掠到第二位置,并且返回到第一位置,并且重复。在一个实施方案中,可以在治疗区域中创建TTZ的多个序列。例如,多个TTZ可以沿着第一线性序列和与第一线性序列间隔开治疗距离的第二线性序列形成。
在一个实施方案中,可以以线性或基本上线性的区或序列创建TTZ,其中每个单独的TTZ通过治疗间隔与相邻的TTZ分开,如图9中所示。图9示出了超声系统20的实施方案,其换能器280配置为治疗焦点深度278处的组织。在一个实施方案中,焦点深度278是换能器280和治疗的靶组织之间的距离。在一个实施方案中,对于给定的换能器280,焦点深度278是固定的。在一个实施方案中,对于给定的换能器280,焦点深度278是可变的。如图9中所示,在不同的实施方案中,通过控制系统300的受控操作,由模块200提供在合适的焦点深度278、分布、定时和能量水平下的发射能量50的传输,以实现受控热损伤的期望治疗效果,从而治疗表皮层502、真皮层503、脂肪层505、SMAS层507、肌肉层509和/或下皮504中的至少一个。图9示出了对应于用于治疗肌肉的深度的深度实施方案。在不同的实施方案中,深度可以对应于任何组织、组织层、皮肤、表皮、真皮、下皮、脂肪、SMAS、肌肉、血管、神经或其他组织。在操作期间,模块200和/或换能器280也可以沿着表面501机械地和/或电子地扫描以治疗扩展区域。在超声能量50传递到表皮层502、真皮层503、下皮504、脂肪层505、SMAS层507和/或肌肉层509中的至少一个之前,期间和之后,可以对治疗区域和周围结构进行监视以计划和评估结果和/或经由图形界面310向控制器300和用户提供反馈。在一个实施方案中,超声系统20产生超声能量,该超声能量被引导至并聚焦在表面501下面。该受控的和聚焦的超声能量50产生热治疗区(TTZ)550。在一个实施方案中,TTZ 550是线。在一个实施方案中,TTZ 550是点。在一个实施方案中,TTZ 550是二维区域或平面。在一个实施方案中,TTZ 550是体积。在一个实施方案中,超声能量50热治疗皮下组织510。在不同的实施方案中,发射的能量50以表面501下的组织作为目标,其加热、切割、消融、凝固、微消融、推拿表面501下面的组织部分10和/或引起表面501下面的组织部分10的损伤。在一个实施方案中,在治疗序列期间,换能器280在由标记为290的箭头所表示的方向上移动,以移动TTZ 550。
在不同的实施方案中,可以使起作用的TTZ(连续地或非连续地)移动通过组织以形成治疗区域552,如图10中所示。参考图10中的图示,模块200可以包括能通过透声部件230发射能量的换能器280。在不同的实施方案中,深度可以指焦点深度278。在一个实施方案中,换能器280可以具有偏移距离270,其是换能器280和透声部件230表面之间的距离。在一个实施方案中,换能器280的焦点深度278距离换能器固定的距离。在一个实施方案中,换能器280可以具有从换能器至透声部件230的固定的偏移距离270。在一个实施方案中,透声部件230配置在模块200或超声系统20上的一位置处用于接触皮肤表面501。在不同的实施方案中,焦点深度278超过偏移距离270一个量,以对应于位于皮肤表面501下的组织深度279处的靶区域处的治疗。在不同的实施方案中,当超声系统20放置成与皮肤表面501物理接触时,组织深度279是透声部件230和靶区域之间的距离,其被测量为从手柄100或模块200表面接触皮肤的部分(有或没有声耦合凝胶,介质等)至组织中从该皮肤表面接触点到靶区域的深度的距离。在一个实施方案中,除了皮肤表面501下面至靶区域的组织深度279之外,焦点深度278可以对应于偏移距离270(其被测量至与耦合介质和/或皮肤501接触的透声部件230的表面)与该组织深度之和。在不同的实施方案中,不使用透声部件230。
在不同的实施方案中,通过使用被配置为将能量传递到扩展的TTZ的换能器,治疗性的治疗可以有利地以更快的速率和以提高的精度提供。这又可以减少治疗时间并减小患者经历的疼痛。在几个实施方案中,通过产生TTZ并使TTZ扫掠过单个换能器治疗的面积或体积,减少了治疗时间。在一些实施方案中,期望减少患者经历的治疗时间和相应的疼痛和/或不适的风险。通过形成较大的TTZ 550,同时、几乎同时或顺序地形成多个TTZ,和/或移动TTZ 550以形成较大的治疗区域552,可以通过在给定时间内治疗更大的面积来减少治疗时间。在一个实施方案中,通过用多个TTZ治疗给定面积或体积,减少了装置的总移动量,而减少治疗时间。在一些实施方案中,通过由一系列的单独的TTZ创建连续的治疗区域552或离散的、分段的治疗区域552,总治疗时间可以减少10%,20%,25%,30%,35%,40%,4%,50%,55%,60%,65%,70%,75%,80%或更多。在不同的实施方案中,治疗时间可以减少10-25%,30-50%,40-80%,50-90%或约40%,50%,60%,70%和/或80%。虽然在一个治疗期中在不同位置对患者的治疗在一些实施方案中可能是有利的,但是在其它实施方案中,随时间经过而进行顺序的治疗可能是有益的。例如,可以在相同的表面区域下在时间一在一个深度,在时间二在第二深度等等对患者进行治疗。在不同的实施方案中,时间可以是纳秒级、微秒级、毫秒级、秒级、分钟级、小时级、天级、周级、月级、或其他时间长度级别的。例如,在一些实施方案中,换能器模块配置为以10ms-100分钟的工作时间传递能量(例如,100ms,1秒,1-60秒,1分钟-10分钟,1分钟-60分钟,以及其中的任何范围)。通过第一次治疗产生的新胶原对随后的治疗可能更敏感,这对于一些适应症可能是期望的。备选地,在单个治疗期中在同一表面区域下的多深度治疗可能是有利的,因为在一个深度的治疗可以协同地增强或补充另一个深度的治疗(例如由于增强的血流,生长因子的刺激,激素刺激,等等。)。在几个实施方案中,不同的换能器模块在不同的深度提供治疗。在一个实施方案中,可以针对各种各样的深度调节或控制单个换能器模块。
在一个实施方案中,美容治疗系统包括具有可移除模块的超声探头,可移除模块包括超声换能器,其配置为向聚焦区处的组织应用超声治疗。在一个实施方案中,聚焦区是点。在一个实施方案中,聚焦区是线。在一个实施方案中,聚焦区是二维区域或平面。在一个实施方案中,聚焦区是体积。在不同的实施方案中,聚焦区可以移动以扫掠第一位置和第二位置之间的体积。在不同的实施方案中,一个或多个聚焦区位置以基本上线性的顺序位于美容治疗区内。在一个实施方案中,第一组位置位于第一美容治疗区内,而第二组位置位于第二美容治疗区内,第一区不同于第二区。在一个实施方案中,第一美容治疗区包括第一组位置的基本上线性的序列,第二美容治疗区包括第二组位置的基本上线性的序列。
在一个实施方案中,换能器模块280可以提供在大约1W或更小,大约1W至大约100W之间,和大于大约100W的范围内的声功率。在一个实施方案中,换能器模块280可以提供频率为大约1MHz或更小,大约1MHz至大约10MHz之间,和大于大约10MHz的声功率。在一个实施方案中,模块200具有的用于治疗的在皮肤表面501下面约4.5mm的组织深度279处的焦点深度278。换能器280或模块200的一些非限制性的实施方案可以配置为用于在3mm,4.5mm,6mm,小于3mm,3mm和4.5mm之间,4.5mm和6mm之间,大于4.5mm,大于6mm等的组织深度处,以及在0.1~3mm,0.1~4.5mm,0.1~6mm,0.1~25mm,0.1~100mm等的范围内的任何地方,以及其中的任何深度,传递超声能量。在一个实施方案中,超声系统20设置有两个或更多个可移除的换能器模块280。在一个实施方案中,换能器280可以在组织深度(例如,约6mm)处施加治疗。例如,第一换能器模块可以在第一组织深度(例如,约4.5mm)处施加治疗,第二换能器模块可以在第二组织深度(例如,约3mm)处施加治疗,第三换能器模块可以在第三组织深度(例如,约1.5-2mm)处施加治疗。在一个实施方案中,至少一些或所有换能器模块可以配置为在基本相同的深度施加治疗。在不同的实施方案中,组织深度可以是1.5mm,2mm,3mm,4.5mm,7mm,10mm,12mm,14mm,15mm,17mm,18mm和/或20mm,或其中的任何范围(包括但不限于12-20mm,或更高)。
在一个实施方案中,换能器模块允许皮肤表面处或皮肤表面下方的固定深度处的治疗序列。在一个实施方案中,换能器模块允许在皮肤表面下面的深度范围的治疗序列。在几个实施方案中,换能器模块包括移动机构,其配置为在TTZ移动超声治疗。在一个实施方案中,各个TTZ的线性序列具有的治疗间隔在从约0.01mm至约25mm的范围内。例如,间隔可以为1.1mm或更小,1.5mm或更大,在约1.1mm和约1.5mm之间等等。在一个实施方案中,各个TTZ是离散的。在一个实施方案中,各个TTZ是重叠的。在一个实施方案中,移动机构配置为被编程以在各个TTZ之间提供可变的间隔。在几个实施方案中,换能器模块包括移动机构,其配置为按序列引导超声治疗,以使得TTZ形成在以治疗距离分开的线性或基本上线性的序列中。例如,换能器模块可以配置为沿着第一线性序列和与第一线性序列分开一治疗距离的第二线性序列形成TTZ。在一个实施方案中,各个TTZ的相邻线性序列之间的治疗距离在从约0.01mm至约25mm的范围内。例如,治疗距离可以为2mm或更小,3mm或更大,在约2mm和约3mm之间等等。在几个实施方案中,换能器模块可以包括一个或多个移动机构,其配置为按序列引导超声治疗,以使得TTZ形成为与其它线性序列分开一治疗距离的各个热病损的线性或基本上线性的序列。在一个实施方案中,分开线性或基本上线性的TTZ序列的治疗距离是相同的或基本上相同的。在一个实施方案中,分开线性或基本上线性的TTZ序列的治疗距离对于各个相邻的线性TTZ序列对是不同的或基本上不同的。
使用具有成像元件的圆柱形换能器的带式治疗
在不同的实施方案中,包括成像换能器或具有圆柱形换能元件281的成像元件可以用于改善治疗的安全性和/或功效。在一个实施方案中,成像元件可以用于确认超声治疗换能器之间的可接受的耦合和/或识别皮肤表面下的靶组织。如图21和22所示,在不同的实施方案中,换能器280包括圆柱形换能元件281和一个或多个成像元件284。成像元件284配置为对任何合适的组织深度279处的感兴趣区域进行成像。在一个实施方案中,成像元件以治疗元件为中心。在一个实施方案中,成像元件与治疗元件是轴对称的。在一个实施方案中,成像元件与治疗元件不是轴对称的。在一个实施方案中,成像轴线可以指向完全不同的方向并且从治疗束轴线平移。在一个实施方案中,孔径中的成像元件的数量可以大于一。例如,在一个实施方案中,成像元件可以位于笔直指向前和/或在中间的圆柱的每个角上。在一个实施方案中,组合式成像和圆柱形治疗换能器280包括圆柱形换能元件281和一个或多个成像元件284。在一个实施方案中,组合式成像和圆柱形治疗换能器280包括具有开口285的圆柱形换能元件281,一个成像元件284配置为穿过开口285操作。在一个实施方案中,开口284是在圆柱形换能元件281的X轴(方位)和Y轴(高程)的中心处穿过圆柱形换能元件281的壁厚的圆形孔。在一个实施方案中,成像元件284的横截面是圆形的并且成像元件284配合在开口284中。
在一个实施方案中,提供了第一和第二可拆除的换能器模块。在一个实施方案中,第一和第二换能器模块均配置为用于超声成像和超声治疗。在一个实施方案中,换能器模块配置为仅用于治疗。在一个实施方案中,成像换能器可以附连到探头的把手或手柄上。第一和第二换能器模块配置为可互换地耦合到手柄。第一换能器模块配置为向第一治疗区域施加超声治疗,而第二换能器模块配置为向第二治疗区域施加超声治疗。第二治疗区域的深度、宽度、高度、位置和/或取向可以不同于第一治疗区域。
使用被配置为减小边缘效应的有覆层换能器的带式治疗
在不同的实施方案中,有利地可以以改进的精度提供治疗。此外,如果差异在治疗区域中减小,则可以提高效率、舒适度和安全性。这又可以减少治疗时间并减少患者经历的疼痛。在某些情况下,在聚焦区的不均匀加热可能由换能器的几何方面引起。压力或温度分布的不一致可归因于边缘效应,边缘效应可导致换能器的聚焦区周围的压力或温度的尖峰。因此,在有边缘效应的情况下,不是实现均匀的加热线段,而是将该线段分成许多独立的热点,这可能不能满足在聚焦区的更均匀热分布的目标。在与升高的声压相关的高加热速率下,这种现象进一步加重。这是由于产生了非线性谐波,其特别是在高压区域中被引起。处于谐波频率的能量比处于基频的能量更容易吸收。在一个实施方案中,能量吸收由下列公式控制:
H=2*α*f*p2/Z (1)
其中α是以奈培/兆赫兹·厘米为单位的吸收常数,f是以兆赫兹为单位的频率,p是该频率下的压力,Z是组织的声阻抗,H是以瓦特/立方厘米为单位的加热速率。在一个实施方案中,产生的谐波的量与强度成比例。图23示出了具有成像元件的圆柱形元件的一个实施方案的在焦点深度处横越方位的标准谐波压力。图23示出了在该深度处谐波压力的快速摆动,其导致热点和不均匀加热。
在一个实施方案中,对抗由边缘效应导致的这些热点和冷点的方法是减小焦点深度处的平均强度和/或增加加热时间。这两个方法可以减少非线性加热的量,以及允许将热量从热点传导到冷区域。当加热时间增加时,组织的热传导有效地充当声强度分布的低通滤波器。虽然这些方法可能减少不均匀加热的问题,但是它们也可能降低加热区的定位并且还可能增加治疗时间。因此,超声治疗的三个性能领域(例如功效、舒适性和治疗时间)受到不利的影响。在一个实施方案中,更标准的压力分布导致更一致的治疗,以使得通过加热、凝固和/或消融实现的温度增加是更可预测的,并且可以更好地确保在TTZ 550中获得期望的或目标的温度曲线。在不同的实施方案中,利用在特定区域中被涂覆的换能器来实现边缘效应的变迹。
在一个实施方案中,覆层或遮挡物的使用可以帮助规避这些问题,以使得功效,舒适度和治疗时间得到优化。图24示出了具有成像换能器的被遮蔽的孔径或有覆层元件的实施方案的谐波压力分布。在一个实施方案中,有覆层元件是具有成像元件的有覆层圆柱形元件。在整个治疗线上的谐波压力的变化的变化量小于1.5dB,最高强度位于中心和-10mm与+10mm的尖锐边缘附近。在一个实施方案中,有覆层元件设计不需要将热量传导远离热点,因为沿着焦线的组织在吸收期间具有均匀的温度增加。因此,可以增加焦点处的强度量以定位加热区并减少治疗时间。
在一个实施方案中,有覆层元件是被遮蔽的治疗圆柱体。在一个实施方案中,有覆层元件还在预期加热区之外具有好处。在一个实施方案中,当与无覆层元件相比时,被加热和未被加热的接合部之间的边界得到极大地改善。图25示出了与在该边界处有覆层的圆柱形元件600的实施方案相比,圆柱形元件280的实施方案的横跨方位的谐波压力的比较。图25示出了在一个实施方案中,对于具有有覆层的圆柱形元件600的被遮蔽的孔径,可能的谐波压力约低20dB,这帮助限制加热区并使舒适度最大化。在一个实施方案中,电镀或未电镀的区域最初用于限定压电材料将被极化或不极化的区域。有镀层的区域限定将被极化或实际上机械振动的区域。在一个实施方案中,圆柱形元件280可以是无覆层的。此外,无覆层区域可以被认为是在这样一种程度上未涂覆的,即它没有导电覆层——在某些实施方案中,无覆层区域可以具有其他类型的表面覆层。在一个实施方案中,圆柱形元件被完全涂覆。例如,在一个实施方案中,第一换能器280包括用镀层完全覆盖了圆柱形换能元件的凹表面282的第一有覆层区域287和用镀层完全覆盖了圆柱形换能元件的凸表面283的第二有覆层区域287。第二有覆层换能器600包括用镀层完全覆盖了圆柱形换能元件的凹表面282的第一有覆层区域287和用镀层部分覆盖了圆柱形换能元件的凸表面283的至少一第二有覆层区域287。如图27中所示,被完全涂覆的第一换能器281证明了由于边缘效应引起的焦点增益的尖峰。
参考图11A-13B,在一个实施方案中,基于在整个凹表面282和整个凸表面283上涂覆有覆层的圆柱形换能元件281的理论和实验性能绘制换能器治疗图。在一个实施方案中,覆层是金属。在一个实施方案中,覆层是导电金属。在一个实施方案中,覆层是电导体。在不同的实施方案中,覆层镀有银、金、铂、汞、铜或其它材料中的任何一种或多种。在一个实施方案中,覆层包括烧制的银。在一个实施方案中,表面被完全涂覆。在一个实施方案中,表面是完全未涂覆的。在一个实施方案中,表面部分涂覆并部分未涂覆。标准压力与指定深度处的热加热测量结果成比例。不连续的尖峰(在图的顶部的尖的区域)图指出了由于圆柱形换能元件281的几何形状的几何边缘效应而发生的压力和/或温度峰值。在不同的实施方案中,可以用包括一个或多个有覆层区域287的有覆层换能器600来减小尖峰或峰值。在一个实施方案中,有覆层区域287仅部分地涂覆换能器表面。在一个实施方案中,有覆层区域287没有完全涂覆换能器表面。
如图26中所示,在不同的实施方案中,有覆层换能器600包括具有一个或多个有覆层区域287的圆柱形换能元件281。在不同的实施方案中,有覆层区域287涂覆换能器600的表面的局部、一部分和/或全部。在不同的实施方案中,有覆层区域287涂覆圆柱形换能元件281的部分或全部表面。在不同的实施方案中,有覆层换能器600包括一个或多个成像元件284。在一些实施方案中,一个、两个、三个或更多个成像元件被放置在覆层/遮蔽部的“未使用区域”中以用于成像。
由于开口285的附加的边缘,由包括圆柱形换能元件281的组合式成像和圆柱形治疗换能器的一个实施方案的几何形状所引起的边缘效应是更加明显的,其中所述圆柱形换能元件281具有通过其的开口285。图27是图表,示出了具有不同覆层的组合式成像和圆柱形治疗换能器的两个实施方案的横跨所述方位的焦点增益。第一换能器280包括用镀层完全覆盖了圆柱形换能元件的凹表面282的第一有覆层区域287和用镀层完全覆盖了圆柱形换能元件的凸表面283的第二有覆层区域287。第一换能器280的第一和第二有覆层区域287都镀有银。第二有覆层换能器600包括用镀层完全覆盖了圆柱形换能元件的凹表面282的第一有覆层区域287和用镀层部分覆盖了圆柱形换能元件的凸表面283的至少第二有覆层区域287。第二换能器600的第一和第二有覆层区域287都镀有银。如图27中所示,被完全涂覆的第一换能器281表明了由边缘效应引起的焦点增益的尖峰。被部分涂覆的第二换能器600具有更一致的、标准的性能输出,其中尖峰基本上被减少和/或去除。在不同的实施方案中,有覆层换能器600减小了峰值,以使得在焦点深度周围的差异减小1-50%,25-100%,75-200%和/或10-20%,20-40%和60-80%。在不同的实施方案中,有覆层换能器600减小峰值,以使得围绕焦点深度的位置中的强度的差异为+/-0.01至5mm,5mm或更小,4mm或更小,3mm或更小,2mm或更小,1mm或更小,0.5mm或更小,0.25mm或更小,0.1mm或更小,0.05mm或更小,或其中的任何范围。在不同的实施方案中,有覆层换能器600减小焦点增益的峰值,以使得焦点增益的差异为0.01-0.1,0.01-1.0,0.01-5,0.01-10,1-10,1-5,10,9,8,7,6,5,4,3,2,1或更小,或其中的任何范围。
如下面在例2中所述,图28、29和30示出了图27中被部分涂覆的第二换能器600在不同深度处的性能的实施方案。在所示的实施方案中,被部分涂覆的第二换能器600具有15mm的焦点深度。在不同的实施方案中,焦点深度可以在任何深度。在不同的实施方案中,焦点深度在7,8,9,10,12,13,13.6,14,15,16,17,18或其中的任何深度。
在一个实施方案中,有覆层区域287是电镀的。在一个实施方案中,有覆层区域287是导电材料。在一个实施方案中,有覆层区域287是半导电材料。在一个实施方案中,有覆层区域287是绝缘体材料。在不同的实施方案中,有覆层区域287是银、铜、金、铂、镍、铬和/或将与压电材料的表面粘接的任何导电材料,或其任何组合。在一个实施方案中,有覆层区域287是镀银的。
在不同的实施方案中,圆柱形换能元件281具有在1-50mm,5-40mm,10-20mm,15-25mm范围内的和/或15mm,16mm,17mm,18mm,19mm,20mm,21mm,22mm,23mm,24mm和25mm的方位(x轴)尺寸。在不同的实施方案中,圆柱形换能元件281具有在1-50mm,5-40mm,10-20mm,15-25mm范围内的和/或15mm,16mm,17mm,18mm,19mm,20mm,21mm,22mm,23mm,24mm和25mm的高程(y轴)尺寸。在不同的实施方案中,圆柱形换能元件281具有在1-50mm,5-40mm,10-20mm,15-25mm,12-17mm,13-15mm范围内的和/或10mm,11mm,12mm,13mm,13.6mm,14mm,15mm,16mm,17mm,18mm,19mm,20mm,21mm,22mm,23mm,24mm和25mm的焦点深度(z轴)尺寸。在一些非限制性的实施方案中,换能器可以配置为用于在皮肤表面以下1.5mm,3mm,4.5mm,6mm,小于3mm,1.5mm和3mm之间,1.5mm和4.5mm之间,大于4.5mm,大于6mm,以及在0.1mm-3mm,0.1mm-4.5mm,3mm-7mm,3mm-9mm,0.1mm-25mm,0.1mm-100mm的范围内的任何地方以及其中的任何深度的组织深度处的治疗区。
在不同的实施方案中,包括圆柱形换能元件281的有覆层换能器600具有一个、两个、三个、四个或更多个有覆层区域287。在一个实施方案中,有覆层区域287覆盖元件的整个表面。在一个实施方案中,有覆层区域287覆盖元件的一部分表面。在不同的实施方案中,有覆层区域287包括导电镀层。在一个实施方案中,有覆层区域287包括镀银以形成电极。当电信号施加到有覆层区域287处的电极时,有覆层区域287使圆柱形换能元件281的相应部分膨胀和/或收缩。在不同的实施方案中,有覆层区域287具有完全或部分的点、边缘、线、曲线、半径、圆形、椭圆形、抛物线形、星形、三角形、正方形、矩形、五边形、多边形、其组合的形状或其它形状的形状或边界。在不同的实施方案中,有覆层换能器600还可以包括开口285。
在图31所示的一个实施方案中,包括圆柱形换能元件281的局部有覆层的换能器600在凸表面283上具有一个、两个、三个、四个或更多个具有一个或多个形状的有覆层区域287。在一个实施方案中,包括圆柱形换能元件281的局部有覆层的换能器600在凹表面282上具有一个、两个、三个、四个或更多个具有一个或多个形状的有覆层区域287。在不同的实施方案中,有覆层区域287具有侧缘293、侧边290和中间边缘291。各种边缘可以是直的、弯曲的和/或具有半径,并且尺寸可以修改以得到各种性能曲线。
在图32所示的一个实施方案中,包括圆柱形换能元件281的局部有覆层的换能器600具有一个、两个、三个、四个或更多个圆形的、球形的、弯曲的和/或椭圆形的有覆层区域287。在不同的实施方案中,有覆层区域287具有侧缘293、侧边290和中间边缘291。各个边缘可以是直的、弯曲的和/或具有半径,并且尺寸可以修改以得到各种性能曲线。
在图33所示的一个实施方案中,包括圆柱形换能元件281的局部有覆层的换能器600具有一个、两个、三个、四个或更多个三角形的有覆层区域287。在不同的实施方案中,有覆层区域287具有侧缘293、侧边290和中间边缘291。各个边缘可以是直的、弯曲的和/或具有半径,并且尺寸可以修改以得到各种性能曲线。
在图34所示的一个实施方案中,包括圆柱形换能元件281的局部有覆层的换能器600具有一个、两个或更多个正方形、矩形和/或多边形的有覆层区域287。在不同的实施方案中,有覆层区域287具有侧缘293、侧边290和中间边缘291。各个边缘和/或尺寸可以修改以得到各种性能曲线。
在图35所示的一个实施方案中,包括圆柱形换能元件281的局部有覆层的换能器600具有一个、两个或更多个组合形状和/或混合形状的有覆层区域287。在图35所示的一个实施方案中,局部有覆层的换能器600是组合式成像和圆柱形治疗换能器,其包括具有用于成像元件284的开口285的圆柱形换能元件281。在一个实施方案中,有覆层换能器600包括完全地镀有烧制银的凹表面282,并且具有凸表面283,其具有两个有覆层区域287,所述两个有覆层区域287镀有烧制银以形成电极。当电信号施加到有覆层区域287处的电极时,有覆层区域287使圆柱形换能元件281的对应部分膨胀和/或收缩。在一些实施方案中,可以在极化过程之前或之后施加形状,因为在电极所处的位置会发生振动。在不同的实施方案中,可以在极化之前或之后限定电极。在不同的实施方案中,覆层图案可以在凹表面或凸表面上。在一个实施方案中,有覆层区域287具有侧缘293,第一和第二侧边290以及具有中心边缘297的中间边缘291。各个边缘可以是直的,弯曲的和/或具有半径。可以修改各个尺寸294,295,296和各个边缘以得到各种性能曲线。在一个实施方案中,沿着弯曲尺寸(高程)的中间边缘291是椭圆的一部分。在一个实施方案中,沿着弯曲尺寸(高程)的中间边缘291是抛物线的一部分。在一个实施方案中,沿着未弯曲尺寸(方位)的第一和第二侧边290是抛物线的一部分。在一个实施方案中,沿着未弯曲尺寸(方位)的第一和第二侧边290是椭圆的一部分。
在图36所示的实施方案中,包括圆柱形换能元件281的局部有覆层的换能器600具有一个、两个、三个、四个或更多个菱形、斜方形和/或其它多边形的有覆层区域287。在不同的实施方案中,有覆层区域287具有侧缘293、侧边290和中间边缘291。各个边缘和/或尺寸可以修改以得到各种性能曲线。
在图37和38所示的实施方案中,包括圆柱形换能元件281的局部有覆层的换能器600具有一个、两个、三个、四个或更多个有覆层区域287。在不同的实施方案中,有覆层区域287具有侧缘293、侧边290和中间边缘291。在一些实施方案中,有覆层区域287配置为通过极化、相极化、双相极化和/或多相极化来定位一个、两个、三个、四个或更多个(例如多个)热治疗区。在2014年2月28日提交的美国专利申请14/193,234中描述了具有通过极化、相极化、双相极化和/或多相极化实现的多个治疗区的超声治疗和/或成像装置的各种实施方案,该专利申请通过引用的方式全部并入本文中。
具有减小的边缘效应的有覆层圆柱形换能器的非治疗用途
在不同的实施方案中,包括一个或多个有覆层区域287的有覆层圆柱形换能器600配置为用于非治疗用途。
在一个实施方案中,包括一个或多个有覆层区域287的有覆层圆柱形换能器600配置为用于材料加工。在一个实施方案中,包括一个或多个有覆层区域287的有覆层圆柱形换能器600配置为用于超声冲击处理,以增强材料(如金属、化合物、聚合物、粘合剂、液体、浆料、工业材料)的性质。
在一个实施方案中,包括一个或多个有覆层区域287的有覆层圆柱形换能器600配置为用于材料加热。在不同的实施方案中,圆柱形换能器600配置为用于烹饪、加热和/或加温材料、食品、粘合剂或其它产品。
加热组织和用于超声波带式治疗的热剂量的量化
如上所述,在不同的实施方案中,系统和/或方法通过加热、热疗、热剂量测定、热治疗、凝固、消融、细胞凋亡、细胞溶解、增加组织体积、减少或减小组织体积和/或组织收紧来向组织提供非侵入性皮肤病治疗。在一个实施方案中,增加皮肤组织体积。在一个实施方案中,减少或减小脂肪组织体积。
在不同的实施方案中,带式治疗包括用热量量化脂肪细胞死亡的量的度量标准。例如,在一个实施方案中,热治疗中的热剂量将时间-温度曲线回复为与单一参考温度相关,例如T=43摄氏度,使用阿伦尼乌斯方程。在一个实施方案中,在如下关系下配置带式治疗,即在高于体温的范围内,组织温度每升高1摄氏度,细胞死亡率加倍。然后可以通过将热剂量与来自文献的经验数据进行比较来确定理论存活比例。
在不同的实施方案中,与透热疗法或一般的整体加热技术相比,带式治疗给组织提供了改善的热性加热和治疗。通常,正常体温趋向于在约33-37摄氏度之间的范围内。在不同的实施方案中,当组织在约37-43摄氏度的范围内被加热时,可能发生生理学的热疗,并且暴露于该温度范围(例如大约几小时)可能导致正常组织代谢的增大和/或正常组织血流量增大,并且在一些实施方案中,加速了正常组织修复。当组织中的温度达到高于43摄氏度的范围和/或组织经受更长时间(例如2小时,3小时或更长时间)的温度,组织会经历剧烈的组织代谢和/或剧烈的组织血流,并且在一些实施方案中,加速了正常组织修复。在一个实施方案中,将组织加热(例如,整体加热)至约42-55摄氏度的范围。在不同的实施方案中,将组织加热至约43-50摄氏度会被认为是辅助协同热疗,并且暴露于这个温度范围例如大约几分钟可能导致立即或延迟的细胞死亡、细胞凋亡、肿瘤代谢减少、组织含氧量增加、组织损伤增加、对治疗的敏感性增加、血管状态、DNA损伤、细胞增殖失败和/或细胞破坏。在不同的实施方案中,将组织加热至约50-100摄氏度可以被认为是手术热疗,并且暴露于该温度范围例如大约几秒钟或几分之一秒就可导致凝固、消融、气化和立即的细胞破坏。
在本发明的一些实施方案中,组织治疗部位(例如,脂肪细胞)的温度被升高到38-43摄氏度,并且根据一个实施方案,由此提高组织代谢和灌注并加速组织修复机制。在其它实施方案中,组织治疗部位(例如,脂肪细胞)的温度被升高到43-50摄氏度,在一个实施方案中,其可以增大细胞损伤起点并导致细胞立即死亡,特别是当温度保持升高状态大约几分钟至一小时(或更长)时。在其它实施方案中,组织治疗部位(例如,脂肪细胞)的温度升高到50摄氏度以上,这在一个实施方案中在大约数秒和更短时间内导致蛋白质凝固,并且可以导致细胞立即死亡和消融。在不同的实施方案中,组织治疗部位的温度被加热至40,41,42,43,44,45,46,47,48,49,50,51,52,53,54,55,56,57,58,59,60,61,62,63,64,65,70,75,80,90或100摄氏度,和/或其中的任何范围。在不同的实施方案中,治疗区域具有均匀的温度,1%,2%,3%,4%,5%,6%,7%,8%,9%,10%,12%,15%20%,25%,30%,40%,50%或更多的差异。在不同的实施方案中,治疗区域具有+/-0,1,2,3,4,5,6,7,8,9,10,12,15,20,25摄氏度或更大的差异。
在几个实施方案中,本发明包括将组织治疗部位(例如,脂肪细胞)的温度升高到38-50摄氏度持续1-120分钟之间的时间段,然后任选地在一个、两个、三个、四个、五个或更多个增长过程中将温度升高10-50%。作为使用三个增长过程的示例,可以如下增加目标温度:(i)将温度升高到约40-42摄氏度持续10-30分钟,(ii)然后可选地将温度升高约20%以将温度升高到约48-51摄氏度持续1-10分钟,和(iii)然后可选地增加约10-50%持续更短的时间范围。作为另一个实例,可以如下增加目标温度:(i)将温度升高至约50摄氏度持续30秒至5分钟(例如,大约1分钟)以破坏超过90%、95%或99%的靶(例如,脂肪)细胞,其中具有可选的在温度升高至50℃之前将温度升高至38-49摄氏度持续10-120分钟时间的预热步骤。作为又一个实例,在一些实施方案中,一种加热组织的非侵入式美容方法包括将美容加热系统应用于皮肤表面,其中美容加热系统包括手持式探头,其中手持式探头包括包围超声换能器的壳体,超声换能器配置为将皮肤表面下的组织加热至40-50摄氏度范围内的组织温度,其中超声换能器包括圆柱形换能元件,圆柱形换能元件包括第一表面、第二表面、有覆层区域和无覆层区域,其中有覆层区域包括电导体,其中第一表面包括至少一个有覆层区域,其中第二表面包括无覆层区域和多个有覆层区域,向所述多个有覆层区域施加电流,从而将超声能量引导到焦点深度处的线性聚焦区,其中超声能量产生线性聚焦区处的焦点增益的减小,由此将在线性聚焦区中处于焦点深度处的组织加热到40-50摄氏度范围内的组织温度,持续小于1小时的美容治疗持续时间,从而减少组织中的脂肪组织的体积。
在一个实施方案中,带式治疗系统使用细胞死亡和时间-温度剂量之间的关系,如使用阿伦尼乌斯方程量化的。阿伦尼乌斯方程表明在细胞死亡与暴露时间和温度之间存在指数关系。在某一破坏温度以上,通过温度杀死的细胞率的增加是相对恒定的。在几种类型的组织中实现等效剂量的时间-温度关系似乎在多种细胞类型上在体外和体内都是守恒的。
在一些实施方案中,临床情况包括当接近和保持稳态温度时的温度升高、冷却和波动。在不同的实施方案中,不同的热曲线可以产生相同的热剂量。为了根据时变热曲线估计热剂量,将温度曲线离散化为小的时间步长,并计算每个时间步长期间的平均温度。然后根据方程式(2)对这些温度进行积分,将热剂量计算为破坏温度(43摄氏度)下的等效暴露时间:
方程式(2)表明,随温度的杀灭率的增加是相对恒定的。在一些实施方案中,在断裂点之上升高1摄氏度会导致细胞死亡率加倍。图39和40示出了取决于组织温度的随时间的理论细胞死亡比例,其中在较高的温度和/或较大的时间段具有较高的理论细胞杀死比例。杀死比例越高(如通过99%,80%,50%,40%和20%的杀死比例所示的),在治疗的实施方案中使用越高的温度和/或时间。
一旦计算出热剂量,就可以根据经验数据估计剂量存活响应。在一个实施方案中,43摄氏度持续100分钟的等效剂量理论上产生1%的细胞存活比例。根据本发明的实施方案,基于阿伦尼乌斯关系,可以利用44摄氏度持续50分钟的等效剂量或者45摄氏度下持续25分钟等获得类似的存活比例,如图41的表中列出的,该表列出了理论上实现1%存活比例的等效剂量。
在不同的实施方案中,使用与组织和热方程之间的关系相关联的圆柱形换能器源条件的带式治疗的不同实施方案的模拟表明了连续治疗脉冲遵循线性叠加,这允许简化热传递物理学,从而使加热速率可被描述为温度上升/时间(摄氏度/秒)和被描述为温度上升/遍(摄氏度/按钮按压)。
通过超声带式治疗加热组织
在不同的实施方案中,带式治疗系统配置为用于治疗组织。例如,在一个实施方案中,带式治疗配置为用于治疗颈阔肌上的颏下脂肪。在一个实施方案中,脂肪的治疗包括在不引起任何主要的皮肤表面效应的情况下,在约2.5-6.0mm的深度选择性地引起热量的热冲击,随后导致脂肪层的细胞凋亡。在一个实施方案中,治疗包括在皮肤表面上不超过41摄氏度的情况下,将脂肪暴露于具有42-55摄氏度的温度持续时间的整体加热治疗1-5分钟,其具有生理/生物效应(例如,凝固、细胞凋亡、脂肪细胞溶解等中的一种或多种)。在不同的实施方案中,使用带式换能器的治疗利用等效剂量治疗组织,如图42的图表中所示,该图表示出了各种水平的理论细胞杀死比例。
在不同的实施方案中,使用Khokhlov-Zabolotskaya-Kuznetsov(KZK)方程堆叠多个治疗脉冲的效果的理论回顾利用圆柱形源声学几何结构实现,其与生物热方程相关联(例如,在一个实施方案中,使用阿伦尼乌斯方程)。图43表示圆柱形换能器输出的KZK模拟的结果,其示出了多个脉冲的线性叠加;当用0.45J的3个脉冲或1.35J的1个脉冲(3*0.45J)治疗时,达到近似相同的温度。如图43中所示的带式治疗系统的一个实施方案的理论实验的结果间接表明,对于能量,非线性声音不是最终温度的主要贡献者,并且间接表明身体组织充当线性非时变系统,这允许简化热传递物理学,并且用相对少的参数描述加热和冷却速率。在不同的实施方案中,具有手柄100的治疗系统包括具有一个或多个超声换能器280的模块200。在一些实施方案中,超声换能器280包括一个或多个圆柱形超声元件281,如图5A-8中所示。圆柱形换能元件281配置为用于沿着轴线利用其线性聚焦进行整体加热治疗,导致可以利用自动运动机构移动以治疗矩形平面的连续的线。在一个实施方案中,治疗线在单个方向上垂直于电机运动的方向安置。单“遍”治疗产生的治疗线数量等于{长度}/{间隔}。
在不同的实施方案中,从第一构造(4.5MHz-12mm宽度,深度为4.5mm和6.0mm)测试各种圆柱形几何形状;然而,声学罐测试在治疗线的每个边缘处显示了较高的声压(和因而的加热速率)。在一个实施方案中,陶瓷换能器被变迹以产生平坦的热曲线,如图44和45中所示。在不同的实施方案中,建立了基于两个操作频率、两个治疗宽度和两个治疗深度的不同的圆柱几何形状:(1)3.5MHz-22mm宽度-4.5mm深度;(2)3.5MHz-22mm宽度-6.0mm深度;(3)4.5MHz-22mm宽度-4.5mm深度;(4)4.5MHz-22mm宽度-6.0mm深度;(5)3.5MHz-12mm宽度-4.5mm深度;(6)4.5MHz-12mm宽度-4.5mm深度;(7)3.5MHz-12mm宽度-6.0mm深度;和(8)4.5MHz-12mm宽度-6.0mm深度。在不同的实施方案中,组织温度测量系统包括红外热成像、温度条和电阻温度检测器(RTD)和热电偶中的一个或多个。红外热成像可用于读取皮肤表面温度,温度条能够提供达到的峰值温度,RTD护套具有大的热质量并且可具有缓慢的响应时间。在不同的实施方案中,热电偶具有小于1秒的响应时间,这有利于测量单次治疗的加热和冷却阶段。热电偶还具有足够小的优点,以使得它们可以通过大的孔针定位到期望的组织深度。在一个实施方案中,经由加热阶段连接特定的等效剂量,随后是维持阶段,其中系统或操作者以一定间隔进行脉冲治疗以维持稳态温度。在该阶段期间感兴趣的参数是维持稳态温度所需的平均脉冲周期。
通过超声带式治疗进行的体形塑造
在不同的实施方案中,带式治疗系统配置为用于体形塑造。在一个实施方案中,体形塑造治疗包括与细胞凋亡同时发生的和/或继之以细胞凋亡的热量热冲击。在一个实施方案中,体形塑造治疗包括将脂肪暴露于42-55摄氏度下持续1-5分钟以引起延迟的细胞凋亡。在一个实施方案中,体形塑造治疗包括将脂肪暴露在皮肤表面下至少13mm的焦点深度处。
温度和剂量控制
在不同的实施方案中,在模块200或系统20中可以包括一个或多个传感器以测量温度。在一个实施方案中,提供温度和/或剂量控制的方法。在一个实施方案中,测量温度以控制为组织治疗提供的能量的剂量。在不同的实施方案中,用温度传感器测量组织温度以增加、减少和/或维持施加于组织的能量,以便达到目标温度或目标温度范围。在一些实施方案中,温度传感器用于安全设备以,例如,如果达到阈值或最大目标温度,则减小或停止施加能量。在一个实施方案中,如果达到某一温度,则可以采用冷却装置或系统来冷却组织温度。在一些实施方案中,温度传感器用于例如通过幅度、功率、频率、脉冲、速度或其他因素的调节、终止来调节能量剂量。
在一个实施方案中,温度传感器用于测量皮肤表面温度。在一个实施方案中,温度传感器可以位于换能器保持器之上,并且传感器可以位于模块的一部分中,或反之亦然(交换)。在不同的实施方案中,温度传感器位于系统或模块壳体上,例如在一个实施方案中,位于声窗(如透声部件230)附近或之上。在一个实施方案中,一个或多个温度传感器位于透声部件230周围或附近。在一个实施方案中,一个或多个温度传感器位于透声部件230中或上。在一个实施方案中,可以使用来自皮肤表面的温度传感器测量结果来计算在能量应用的焦点深度处的组织中的温度。在不同的实施方案中,可以计算目标组织温度和/或将其与组织中的深度、组织类型(例如表皮,真皮,脂肪等等)以及皮肤表面和焦点深度之间的组织的相对厚度相关。在一些实施方案中,温度传感器以信号方式向控制系统提供温度测量结果。在一些实施方案中,温度传感器以视觉和/或听觉反馈的方式向系统操作者提供温度测量结果,例如文本、颜色、闪光、声音、哔哔声、警告、警报或温度状态的其他感应指示。
在一些实施方案中,成像可用于控制能量剂量。在一个实施方案中,热透镜效应可用于解决散斑移位和/或特征移位,以指示靶位置处(例如皮肤表面下的组织中的焦点深度处)的组织温度。在一个实施方案中,使用声辐射力脉冲(ARFI)成像来计算组织温度。在一个实施方案中,使用剪切波弹性成像(SWEI)来计算组织温度。在一个实施方案中,用衰减来计算组织温度。
在不同的实施方案中,用可变剂量输送技术来获得组织中的目标温度并维持该目标温度。组织中一深度处的体温围绕热治疗区(TTZ)。在一个实施方案中,为了克服体温,治疗将能量以第一速率聚焦于TTZ,以使TTZ中的组织温度达到目标温度。一旦达到目标温度,可以减小或停止第二速率以将组织维持在目标温度。
在一些实施方案中,能量被聚焦在TTZ的组织中的深度或位置处,以使得聚焦区中的温度增加。然而,在聚焦区的边缘(例如,端部,顶部,底部,侧部等),体温的边界条件可导致治疗区域552的边界处的温度波动。在不同的实施方案中,TTZ 550的移动可能伴随着换能器传递能量以产生治疗区域552。在一个实施方案中,移动机构285可以自动地使圆柱形换能元件281移动横跨治疗区域的表面,以使得TTZ 550可以形成治疗区域552。在图53中,治疗区域552在边缘处被体温包围或近似被体温包围。在一些实施方案中,治疗区域552中沿着边缘/边界的温度低于期望的目标温度。
在不同的实施方案中,用机械速度调节来获得治疗区域552中的特定热分布。在一个实施方案中,为了在治疗区域552中获得更均匀的温度,提高在边缘/边界处施加的温度以抵消周围的体温差。图54示出了机械速度调节的实施方案,其中通过在边界附近减速,导致在边界处(在一个实施方案中,例如沿着25mm的行进距离的开始和停止位置)的温度升高,来改变使换能器沿着方向290(沿着高程方向)移动的运动机构的自动运动的速率或速度,以在治疗区域552中提供更均匀的温度。在中部附近增加的速度传递比降低的速度更低的温度。
在不同的实施方案中,使用幅度调节来获得治疗区域552中的特定热分布。在一个实施方案中,为了在治疗区域552中获得更均匀的温度,提高在边缘/边界处施加的温度以抵消周围的体温差。图55示出了幅度调节的实施方案,其中通过增加边界附近的幅度,导致在边界处(在一个实施方案中,例如沿着25mm的行进距离的开始和停止位置)的温度升高,来改变当运动机构的自动运动沿着方向290(沿着高程方向)移动时由换能器传递的能量的幅度(与功率相关),以在治疗区域552中提供更均匀的温度。在中部附近的较低幅度传递比边界附近的较高幅度更低的温度。
在不同的实施方案中,使用孔径变迹来获得治疗区域552中的特定热分布。在一个实施方案中,使用沿着非聚焦维度(例如沿着TTZ 550和/或方位方向)的孔径变迹,以便在治疗区域552中获得更均匀的温度。增加沿着边缘/边界在端点处施加的温度,以抵消周围的体温差。图56示出了孔径变迹的实施方案,其中通过增大在边界附近的端点附近的幅度,导致边界处的温度升高(其中L作为聚焦线TTZ 550的长度,从中心开始的L/2为端点),来改变由换能器沿着TTZ 550传递的能量的幅度,以在治疗区域552中提供更均匀的温度。在中部附近的较低幅度传递比边界附近的较高幅度更低的温度。在不同的实施方案中,可以利用有覆层换能元件600的实施方案沿着TTZ产生温度分布,如图31-38中所示。
在不同的实施方案中,控制脉冲和/或占空比以获得治疗区域552中的特定热分布。在图57,在不同的实施方案中,治疗图案可以具有一致或恒定的脉冲或占空比。在图58,在不同的实施方案中,治疗图案可具有可变的脉冲或可变的占空比,其具有峰值振幅、施加间隔、施加持续时间中的任一者的变化。如图58中所示,能量的施加更长并且覆盖治疗区域552的边界附近的更大区域,而对于内部区域中相应的较低温度的施加,内部区域施加的功率较小。
在不同的实施方案中,治疗图案用于获得治疗区域552中的特定热分布。在一些实施方案中,TTZ 550具有尺寸(例如,宽度,高度,厚度等)。在一些实施方案中,TTZ550的脉冲施加是不重叠的,如图59中所示。在一些实施方案中,TTZ550的脉冲施加是重叠的,如图60中的边界附近所示,其中重叠量可以是恒定的或变化的。如图60中的实施方案所示,重叠量变化并且包括非重叠部分。在不同的实施方案中,使用交叉影线图案,其中系统机头旋转约90度或正交,并且运动机构在与先前那遍治疗正交的方向上在靶组织区域上面操作额外的一遍或多遍。
在不同的实施方案中,治疗区域552中的特定热分布包括用37-50摄氏度的组织温度进行治疗持续数分钟至数小时以引起目标百分比的细胞死亡(例如脂肪细胞死亡),其关系可以通过阿伦尼乌斯方程来确定,例如图61的左侧所示。在不同的实施方案中,治疗区域552中的特定热分布包括用超过60摄氏度的组织温度进行治疗持续几秒至几分之一秒(或接近瞬时)以在高温下引起凝固、消融和/或细胞死亡(例如脂肪细胞死亡),如图62的右侧所示。在不同的实施方案中,治疗可以是顺序和/或同时治疗中的一种或两者都有。
在一些实施方案中,可以使用机械速度调节、幅度调节、孔径变迹、脉冲占空比和/或在不同温度下的治疗中的一个、两个、三个、四个或更多个来实现整个治疗区域552上的期望温度分布。在不同的实施方案中,使用机械速度调节、幅度调节、孔径变迹、脉冲占空比和/或在不同温度下的治疗中的一个或多个来创建温度分布,其中温度分布可以包括用于升高的、降低的和/或均匀的温度的区域。在一些实施方案中,一种、两种或更多种类型的治疗应用在一个、两个或三个维度上(沿着方位、高程和/或深度方向中的任一个),并且配置为用于在一个、两个、或三个维度的任一者中进行治疗以创建一维、二维或三维温度分布。
在一些实施方案中,复合透镜系统产生各种峰值强度和不同的深度。在不同的实施方案中,机械和/或电子聚焦透镜可以用于方位、高程和/或深度方向中的任何一个或多个上。如图62和图63中所示,复合透镜系统可以创建两条或更多条焦线550和550a。
在不同的实施方案中,超声系统20包括配置为用于移动多个超声换能器280和/或多个超声元件281的运动机构285。在一些实施方案中,如图64的实施方案中所示,运动机构285配置为通过在传送系统上提供所述多个元件281来将被治疗的组织中的热波动减到最小并减少治疗时间,所述传送系统例如具有可以使所述多个元件281以速度v移动的皮带和/或皮带轮系统。在不同的实施方案中,速度可以是恒定的,可变的,零(例如,停止),可逆的(例如向前和向后,左和右,第一方向和第二方向等等)和/或具有在0-100RPM、1RPM-50RPM范围内的值或其它速度。在不同的实施方案中,速度为1-1000厘米/秒中的任何值(例如,10,20,50,100,200,500,1000厘米/秒,以及其中的任何其它值)。在不同的实施方案中,运动机构285移动一个、两个、三个、四个、五个、六个、七个、八个或更多个超声元件281。在不同的实施方案中,超声元件281相连或间隔开0.01-10厘米的距离(例如,0.1,0.5,1,2,5厘米和其中的任何值),以使得一个、两个或更多个超声元件281配置为治疗治疗区域。
在一些实施方案中,使用成像来确认治疗装置和皮肤之间的声耦合的质量。在一个实施方案中,沿着治疗区域、线或点的超声图像的清晰度被用于确定装置声耦合到皮肤表面的程度。在一个实施方案中,使用来自后向散射的散焦成像和/或电压驻波比(VSWR)来检查用于治疗的声耦合。
在一些实施方案中,治疗是自动的。在一个实施方案中,通过将系统声耦合到皮肤表面来建立治疗,并且移动机构和治疗自动操作以起作用。在不同的实施方案中,系统经由吸力耦合到皮肤表面。在不同的实施方案中,系统操作者将系统耦合到皮肤表面,启动系统,并且可以让系统自动执行治疗或治疗的一部分。在一个实施方案中,系统利用吸力和/或真空压力来将探头或系统的一部分保持到皮肤表面,这允许系统使用者开始治疗并让系统自动执行治疗或治疗的一部分并持续一段时间。在一些实施方案中,治疗系统包括TENS刺激装置以减少皮肤治疗部位的疼痛。
用圆柱形换能器进行的理论和实验治疗
以下的实例说明各种非限制性的实施方案。
实例1
以下实例是本发明的非限制性实施方案。
如图11A-20所示,实验证实,应用于模拟靶组织、人造组织和猪组织样品的包括圆柱形换能元件281的换能器280的实施方案在靶向聚焦区域552中形成局部的、线性的热治疗区(TTZ 550)。在实验中,单个圆柱形换能元件281被构造为具有15mm的半径和焦点深度。圆柱形换能元件281的尺寸为20mm(方位)乘以17mm(高程)。可以用更大的孔径实现额外的焦点增益。深度受频率和焦点增益的限制,并且被设置至模拟的组织表面以下6mm。
在图11A-13B中,基于用圆柱形换能元件281实现的理论和实验性能绘制治疗曲线。标准压力与指定深度处的热加热测量结果成正比例。尖峰(在图顶部的尖锐区域)图示表示由于圆柱形换能元件281的几何形状的几何边缘效应而出现的压力峰值。尖峰在理论和实验的性能结果中都可以见到。软件模拟实验在图11A、12A、13A、14A、15A和16A中反映了15mm圆柱形换能元件281的理论性能。进行和测量模拟组织中的物理实验,结果在图11B、12B、13B、14B、15B和16B中。
在图11A-11B和14A-14B中,深度为20mm,其中标准压力在大约0.15的值处达到峰值。如图14A-14B中所示,标准压力是不可见的。在图12A-12B和15A-15B中,深度是设计出的最佳的15mm,其中标准压力在大约0.8的值处达到峰值。如图15A-15B中所示,标准压力是清楚可见的,峰值标准压力在大约0.9-1.0。圆柱形换能元件281的尺寸为20mm(方位)乘以17mm(高程)。在15mm深度处的TTZ 550的尺寸为约0.5mm厚(沿着方位)乘以17mm宽度(沿着高程)。在图13A-13B和16A-16B中,深度为13mm,其中标准压力在大约0.25的值处达到峰值。如图16A-16B中所示,标准压力几乎不可见。如通过理论和实验数据所示,在线性TTZ 550的情况下,用于15mm焦点深度的圆柱形换能元件281的对应于TTZ 550的标准压力为15mm深度。
如图17-20所示,实验证实,应用于猪组织样本(肌肉组织)的包括圆柱形换能元件281的换能器280的实施方案在靶向聚焦区域552中形成局部的、线性的热治疗区(TTZ 550)。在实验中,包括圆柱形换能元件281的换能器280的实施方案在20秒内经过猪肌肉组织三遍,其在4.5MHz和6mm的组织深度下操作。如图17中所示,所述三遍(用温度中的三个尖峰示出)增加了猪肌肉的温度。显示了两个功率水平。40W时,猪肌肉开始于30摄氏度,并且在圆柱形换能元件281在靶组织区域上方通过三遍的20秒的加热过程(在20和40秒的标记之间)中,温度达到约55摄氏度的最大值,然后在治疗开始后的100秒逐渐冷却至约32摄氏度。60W时,猪肌肉开始于约24摄氏度,并且在圆柱形换能元件281在靶组织区域上方通过三遍的20秒的加热过程(在40和60秒的标记之间)中,温度达到约59摄氏度的最大值,然后在治疗开始后的80秒逐渐冷却至约40摄氏度。
图18是治疗后的猪肌肉的照片,其证实了线和平面加热。在一个实施方案中,凝固取决于线之间的空余时间、各遍之间的空余时间和遍数。温度升高比热凝固点慢。图19是穿过图18中的猪肌肉的横截面,其示出了线性热治疗区。图20是穿过图19中的猪肌肉的正交横截面,其示出了平面热治疗区。
实例2
以下实例是本发明的非限制性实施方案。
如图28-30所示,实验证实,应用于模拟靶组织的包括圆柱形换能元件281的局部有覆层的换能器600的实施方案在靶向聚焦区域552中形成局部的、线性的热治疗区(TTZ 550)。局部有覆层的换能器600包括用镀层完全覆盖圆柱形换能元件的凹表面282的第一有覆层区域287和用镀层部分覆盖圆柱形换能元件的凸表面283的至少一第二有覆层区域287。局部有覆层的换能器600的第一和第二有覆层区域287都镀有银。在实验中,单个圆柱形换能元件281被构造为具有15mm的半径和焦点深度。圆柱形换能元件281的尺寸为20mm(方位)乘以17mm(高程)。圆柱形换能元件281在中心具有直径为4mm的开口285。
在图28、29和30中,基于用圆柱形换能元件281实现的理论性能绘制治疗概图。理论性能与指定深度处的热加热成正比例。软件模拟实验反映了15mm局部有覆层的换能器600的理论性能,其显示了在15mm深度处的一致的线性热治疗区550。
实例3
以下实例是本发明的非限制性实施方案。
实施多次猪的体内研究和多次尸体研究以评价硬件的不同实施方案以进行整体加热治疗。早期研究集中于指定和改进测量皮下温度所需的仪器。在一些实施方案中,通过使热电偶蛇形穿过皮肤中用针钻出的孔并通过西门子s2000超声装置验证深度,将绝缘线热电偶放置在焦点和亚焦点深度。使用高采样DAQ卡收集温度曲线。一旦确定测量设置,就在猪体内模型中进行复制的3-因子3水平的实验设计以确定能够安全地达到等效剂量而不引起皮肤表面损伤的能量设置。在一个实施方案中,在~1.2摄氏度/遍的平均焦点加热速率的情况下,观察到10摄氏度的平均温差。安全加热速率在整个换能器上似乎是相似的。
在确定安全加热速率后,在猪体内模型中进行热剂量研究。研究表明,该系统的实施方案能够达到等效剂量,例如47摄氏度持续3分钟,48摄氏度持续1分钟,和50摄氏度持续1分钟,而在皮肤表面上不超过41摄氏度。在一些实施方案中,使用温度较高、暴露时间较短的治疗可具有超过目标温度的可能性并且可能使皮肤表面过热。在不同的实施方案中,执行等效剂量花费的时间越长,向周围组织的热扩散就越多,并且治疗随着深度变得选择性越少。此外,等效暴露时间越长,从操作者和人机工程学角度来看,治疗变得越不切实际。由于这些原因,在一些实施方案中,优选使用较高的等效温度和较短的暴露时间。
进行猪体内测试以确定用于颏下的候选治疗设置是否会引起不利的表面皮肤效应。为这些研究获得的动物是浅皮肤的、120-140磅的阉割的雄性尤卡坦微型猪,由于其皮肤特性与人类组织的特性相似而选择它。通过在治疗后监测动物的皮肤表面上的红斑、水肿和挫伤的证据来评价皮肤表面数据。在治疗之前和之后拍摄每个治疗区域的照片(Cannon G9和Cannon VIXIA HF 510)。在一个实施方案中,使用圆柱形元件换能器的热剂量研究在猪体内模型上进行。在几个实施方案中,测试部位能够在焦点组织部位和皮肤表面之间实现显著的温差,而不引起对皮肤表面的损害。图46示出了来自猪体内模型治疗的实施方案的温度曲线,其中温度曲线达到50摄氏度持续了几秒钟,而皮肤表面不超过41摄氏度,并且显示了在焦点组织部位和皮肤表面之间的多达15摄氏度的温差。由单遍治疗产生的温度变化十分小(大约0.9摄氏度/遍或0.13摄氏度/秒)以执行校正行为并将目标温度保持在+/-1摄氏度内。在猪体内模型中进行改进的3-因子3-水平的实验设计以确定能够安全达到图42中所示的等效剂量温度的能量设置的范围。根据不同的实施方案,该设置在图47的表中列出。实验设计(DOE)测试的声功率范围为10-20W,曝光时间为20-40ms,间隔范围为0.1-0.3mm。图48示出了能够在焦点处实现相对高的热剂量而在皮肤表面处具有很少至没有剂量或温度增加的治疗设置的实施方案。焦点在第24遍时在T=43摄氏度实现了100当量分钟的热剂量(红色虚线),其对应于根据图42的1%的理论存活比例。在不同的实施方案中,在用于不引起显著皮肤表面损伤的治疗的换能器的各种实施方案中,在焦点和表面处实现了类似的温度升高和加热速率。在~1.2摄氏度/遍的平均焦点加热速率的情况下,观察到10摄氏度的平均温度差。在焦点和皮肤之间的最大温差由3.5MHz,22mm宽度,6.0深度的设计获得,其在治疗中具有12摄氏度的平均差异。由于产生很少至没有的表面效应的加热速率在换能器上是相似的,因此选择3.5MHz,22mm宽度,6.0mm深度的换能器以在热剂量研究中进行评估。
在不同的实施方案中,对猪体内和尸体模型进行热剂量研究,以通过组织学评价来确定安全的等效剂量和脂肪细胞死亡的几何形态。图49的表列出了为了实现不同水平的脂肪细胞死亡而暴露的目标时间-温度。根据图42中的经验数据,部位2和5应达到很少的或没有脂肪细胞死亡。部位3、6和7应达到高度的脂肪细胞死亡。部位1和4在过渡区域内,应达到中等量的脂肪细胞死亡。图50的表列出了用于利用3.5MHz,22mm宽度,6.0mm深度的换能器接近每个等效剂量的能量设置。在不同的实施方案中,治疗持续进行2-3分钟,脉冲为20-30,以1摄氏度/遍的斜度且然后总是维持脉冲3-5秒的方式达到目标温度。几个测试部位在治疗当天显示了轻微的表面效应,仅当损伤上升到皮肤表面时变得更明显。图51示出了一个部位,出于使用于组织学对照的组织凝固的目的而通过过量剂量对该部位进行侵略性的治疗。在图51的实施方案中,损伤的尺寸代表热能的扩展的示例,在皮肤表面上测量为12.6×19.9mm,从皮肤表面可以检测到的水肿深度达12mm。在图52中示出了在图49的表中列出的时间-温度目标的可视表示(三角形标记),其中在实验室中获得的六个等效剂量被示于图52上(正方形标记)。这些等效剂量中的两个落入凝固区域,两个落入过渡区域,两个落入热疗区域。
本申请中描述的一些实施方案和实例是示例性的,并且在描述这些发明(多个)的组合和方法的全部范围时并非限制性的。在本申请的实施方案的范围内可以做出一些实施方案、材料、组成和方法的等效改变、修改和变化。在不同的实施方案中,装置或方法可以组合本申请中披露的任何实施方案的特征或特性。
虽然本发明容许各种修改和替代形式,但是其具体实例已经在附图中示出并且在本申请中详细描述。然而,应当理解,本发明不限于所披露的特定形式或方法,而是相反,本发明覆盖落入所描述的不同实施方案和所附权利要求的精神和范围内的所有变型、等价方案和替代方案。本申请中披露的任何方法不必以记载的顺序执行。本申请中披露的方法包括从业者采取的某些行为;然而,他们也可以明确地或暗示地包括那些行为的任何第三方指令。例如,诸如“将超声探头耦合到皮肤表面”的行为包括“指示将超声探头耦合到皮肤表面”。本申请中披露的范围还包括其任何和所有重叠、子范围和组合。诸如“多达”,“至少”,“大于”,“小于”,“在……之间”等语言包括所列举的数字。前面有术语诸如“约”或“大约”的数字包括列举的数字。例如,“约25mm”包括“25mm”。当用于本申请中时,术语“大约”、“约”和“基本上”代表接近所声称的量或特性的量或特性,其仍然执行期望的功能或达到期望的结果。例如,术语“约”,“大约”和“基本上”可以指在比所声明的量或特征小10%,小5%,小1%,小0.1%,和小0.01%内的量。
- 还没有人留言评论。精彩留言会获得点赞!