提供与药剂输送相关的基于温度的反馈的制作方法
本说明书涉及一种向用户提供与药剂输送相关的反馈。具体地,但不排他地,本说明书涉及一种反馈设备,该反馈设备向用户施加与药剂输送相关的基于温度的反馈。
背景技术:
用于向患者输送药剂的可穿戴装置有时由患者穿戴相当长的时间,以允许以期望的速率或在期望的时间段内输送药剂。这种类型的可穿戴装置的示例是推注注射器,其通常像贴片一样被穿戴在皮肤上。推注注射器通常对患者进行相对大体积的液体药剂的自动皮下输送,例如至少1ml。药剂输送可持续几分钟或数小时。这种高容量推注注射器装置可以称为大体积装置(LVD)。
在完成药剂输送之后,患者必须在稍后的时间从他或她的身体移除该装置。
技术实现要素:
根据本发明的方面,提供一种被构造为通过注射将药剂输送给用户的装置,包括注射反馈设备,该注射反馈设备被构造为向用户施加与药剂输送相关的基于温度的反馈。
基于温度的反馈可以以谨慎的且可由可穿戴装置的用户直观地理解的方式提供关于注射的反馈。
反馈设备可以被构造为通过使热能被施加于用户皮肤组织或从用户皮肤组织去除来将基于温度的反馈施加于用户皮肤组织。
将基于温度的反馈施加于用户皮肤组织可以允许以直接和谨慎的方式(例如在用户的衣服下)输送反馈。
反馈设备可以被构造为通过改变患者接口元件的温度来加热或冷却皮肤组织。
患者接口元件可以帮助以舒适和/或热有效的方式(例如,通过与皮肤组织接触)提供反馈。
反馈设备可以被构造为将患者接口元件的温度改变预定量。
接口元件的温度所改变的预定量可以是适当的,以允许用户容易地感知温度的变化,从而知道反馈。如果该变化是温度的增加,则可不足以使用户皮肤组织变性。预定量的实例是+/-5℃。最大温度可以为约42℃。
反馈设备可以被构造为在预定时间段内改变患者接口元件的温度。
可以选择周期的长度以允许患者容易地感知变化。一个示例是不到一分钟。
反馈设备可以被构造为响应于与药剂输送相关联的触发事件而提供基于温度的反馈。
这可以允许反馈设备向用户指示特定事件,诸如完成一剂药剂的注射。这可以增加用户的反馈的质量。
反馈设备可以被构造为响应于不同的触发事件而将不同的温度施加于皮肤组织。
这可以允许反馈设备例如通过对皮肤组织施加不同的温度向用户提供多种类型的信息。这可能是有利的,因为可以增加给予用户的反馈的范围。
触发事件可以是完成从装置注射药剂。
这可以允许该设备通知用户能够安全地从身体移除该设备。
反馈设备可以包括珀耳帖元件,该珀耳帖元件被构造为控制用户皮肤组织的局部区域的温度以提供基于温度的反馈。
珀耳帖元件可以允许皮肤组织的精确温度控制,并且因此允许用户的高质量且可区分的反馈。
反馈设备可以包括电阻加热元件或红外加热元件,以导致对用户皮肤组织的加热。
这可以允许设备引起皮肤组织的快速加热,并且因此使得设备能够响应于触发事件快速地提供反馈。
反馈设备可以被构造成启动吸热或放热化学反应,以导致用户皮肤组织的冷却或加热。
这可以允许装置引起对皮肤组织的快速加热或冷却,并且因此使得设备能够响应于触发事件而快速地提供反馈。
该装置可以包括靠着用户的皮肤穿戴的接触区域,并且反馈设备可以被布置成将基于温度的反馈施加于接触区域下面的皮肤组织。
将反馈施加于接触区域下面的皮肤区域可以使得用户更容易将反馈与装置相关联,并且因此使注射更容易。
该装置可以被构造为响应于患者启动的触发器而自动地施加反馈以输送药剂。
以这种方式,可以响应于设备的首次启动或一些其他触发而启动反馈过程,并且此后可以在没有来自用户的任何单独输入的情况下自动进行反馈过程。这可以增加设备的可用性。
该装置可以是推注注射器装置。
该装置可以是可穿戴的。
反馈设备可以被构造为启动气体的压缩或膨胀,以导致对用户皮肤组织的冷却或加热。
这可以允许装置导致对皮肤组织的快速加热或冷却,并且因此使得设备能够响应于触发事件而快速地提供反馈。
该装置可以包括定时元件以触发对用户施加基于温度的反馈。
这可以允许反馈设备在不受诸如微控制器的控制器控制的情况下运转。这可以降低生产装置的成本。
该装置可以被构造为通过所述反馈设备允许所述用户皮肤组织在加热一段时间之后自然冷却来施加所述基于温度的反馈。。
装置的这个方面可以允许用户以自然的方式感知反馈。
根据本发明的方面,提供一种包括上述装置的系统,其还包括通过注射输送到用户中的药剂的贮存器。
根据本发明的方面,提供了一种向被构造为通过注射向用户输送药剂的装置的用户提供反馈的方法,该方法包括向用户施加基于温度的反馈。
附图说明
仅出于示例的目的,下面参照附图描述实施例,其中:
图1是用于通过注射向用户输送药剂并且对用户施加关于注射的基于温度的反馈的可穿戴装置的示意图;
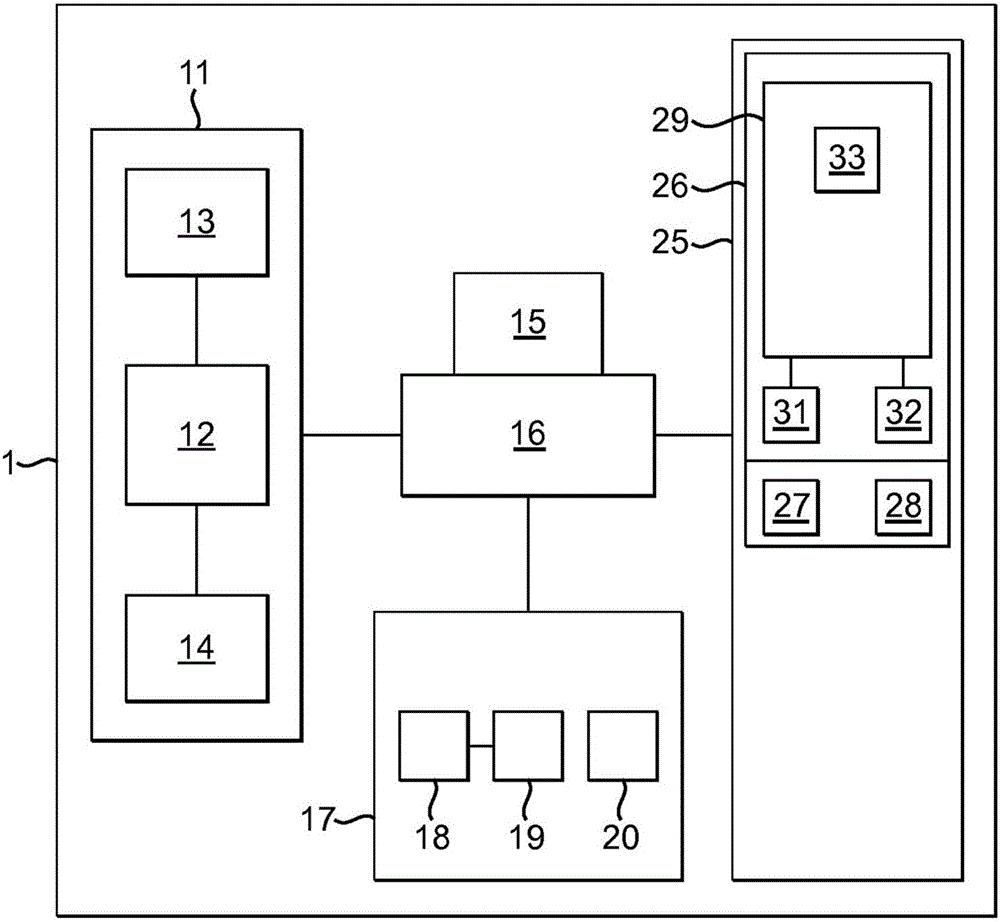
图2是用于通过注射向用户输送药剂并且对用户施加关于注射的基于温度的反馈的可穿戴装置的框图;
图3是用于通过注射将药剂输送给用户并且对用户施加关于注射的基于温度的反馈的可穿戴装置的患者接触区域的示意图;以及
图4是向用于通过注射输送药剂的可穿戴装置的用户提供基于温度的反馈的方法的流程图。
具体实施方式
下面描述了用于将流体药剂输送到患者的可穿戴流体输送装置。该装置包括用于储存一定量的药剂的贮存器和用于将药剂输送到患者的分配接口。该装置被构造成通过注射从分配接口输送药剂并且对患者施加关于注射的基于温度的反馈。例如,可以通过基于温度的反馈通知患者何时移除装置,或何时由于另一个原因而注意装置。在靠着患者的皮肤穿戴装置时提供注射和反馈。
下面在推注注射器的背景下描述该装置,但是应当理解,该装置可以替代地是另一种类型的大体积装置(LVD)。参照图1所示的示例性实施例,装置1包括保护性壳体2,其中药剂贮存器3和分配接口4与装置1的其它部件一起定位。壳体2由模制塑料或另一种合适的材料形成。药剂贮存器3设置在胶囊5中,胶囊5可以包含单剂量的药剂。胶囊5由诸如玻璃的惰性材料形成,并且被固定在壳体2的内部空腔内部。胶囊5可以是可更换的,以允许重新使用装置1。或者,胶囊5在装置1中可以是不可更换的,使得一旦胶囊5的内容物已经耗尽,装置1就不能再用于输送药剂并且必须被丢弃。装置1的这种一次性使用特性促进了简易操作并且通过确保患者不能错误地安装不正确的替换胶囊来提高安全性。
分配接口4包括用于将药剂从装置1注射到患者体内的注射元件。下面在套管6的背景下解释注射元件,如图1所示,但是应当理解,可以替代地使用其他类型的注射元件。下面进一步讨论替代注射元件的示例。
套管6包括远端7,该远端7在使用期间穿过装置1的壳体2突出到患者的身体组织中。套管6还包括近端8,该近端8布置成从上述贮存器3接收药剂。例如,胶囊5中的呈出口端口形式的开口9可以通过导管10连接到套管6的近端8,使得流体药剂可以从胶囊5流入到套管6中。
套管6可以可控地延伸和/或缩回穿过壳体2的外部,以便允许其在不使用时安全地收纳在壳体2中。装置1可以包含用户可操作的致动器11以促进这一点。致动器11被构造为使套管6相对于装置1的壳体2移动,以便使套管6延伸和/或缩回。一个示例是致动器11,其包括弹力元件12和用于释放弹力元件12的开关13。在通过开关13释放时,弹力元件12可以构造成自动延伸并且由此将套管6部分地驱动出壳体2进入注射位置中。致动器11可以是电动的。例如,用于释放上述弹力元件12的开关13可以是电动的。电功率还可以用于将弹力元件12缩回到其初始的非伸展位置,从而也抽出套管6。为此,致动器11可以包括马达14和联接到弹力元件12的适当的驱动机构。电功率可以由装置1中的电池15或其他电源提供,所述电池15或其他电源可以是可再充电的。
特别地,如果装置1的构造使得药剂的胶囊5是可更换的,则电池15可以是可再充电的。在这种类型的构造中,装置1包括灭菌部分和非灭菌部分。装置1的灭菌部分是可更换的,并且包括可更换的胶囊5。装置1的非灭菌部分是可重复使用的,并且包括装置1的可重复使用的元件。非灭菌部分中的元件可以包括例如可充电电池15。通常,非灭菌部分包括对于装置1的安全操作不需要无菌的元件,并且可以安全地重复使用。然而,应当理解,对不需要无菌的元件不作要求仅限制于装置1的非灭菌部分。例如,电池15可以与装置1的灭菌部分中的其它可更换元件一起被包括。在该构造中,电池15是不可再充电的,因为每次更换胶囊5时更换电池。
如下面将更详细地解释的,装置1可以包括电子控制器16,该电子控制器16被构造为控制致动器11和/或装置1的其他元件的操作。电子控制器16包括处理器和存储器,并且可以例如包括使用系统总线(未示出)通信地耦合到致动器11和/或装置1的其它元件的电子微控制器。开关13、马达14、电池15和控制器16在图2中的装置1的框图中示出,但在图1中未示出。
套管6的远端7可以被削尖以便于将其插入到患者的身体组织中。或者,分配接口4还可以包括用于帮助将套管6的远端7插入身体组织中的单独的针(未示出)。在这种情况下,套管和针可以一起形成套管针。针可以以与上述套管6类似的方式从装置1的壳体2可控地延伸和/或缩回。针被构造成刺破患者的皮肤,以便允许套管6移动到身体组织中。针可以例如被布置成延伸穿过套管6的中心。一旦皮肤被刺破,装置1被构造为在输送药剂之前将针回缩到壳体2中。在装置1包括上述类型的单独的针的情况下,装置1可以包括类似于先前相对于套管6所讨论的致动器的致动器,以便于针的伸出和缩回。
另一种替代方案是药剂通过针自身输送。在这种情况下,针具有类似于常规注射针的特性。针的近端以与上述套管6相似的方式连接到药剂贮存器3,使得流体药剂可以经针流入患者的身体组织中。如果以这种方式构造装置1,则可以从分配接口4省略套管6。
药剂流入套管6或其它注射元件中由流动控制设备17控制。如图1所示,流动控制设备17可以包括活塞18,该活塞18可通过胶囊5从一端移动到另一端以将药剂从胶囊5经上述开口9驱出。合适的驱动机构(未示出)机械地联接到活塞18,并且可操作以使活塞18移动经过胶囊5。活塞18的移动可以是电动的。例如,马达19可以连接到驱动机构。马达19由装置1中的电源(诸如,先前提及的电池15)供电。
附加地或替代地,流动控制装置17可以包括密封件20,该密封件20位于胶囊5中的开口9处,以防止药剂在期望药剂从胶囊5流出之前从胶囊5流出。密封件20是易破裂的或以某种其它方式可打开的,以允许药剂经由前述的导管10从胶囊5移入到套管6或其它注射元件中。装置1被构造为响应于患者启动的触发器,例如通过破坏密封件20和/或移动活塞18来操作流动控制装置17,如下所述。
参照图3,壳体2的接触区域21布置成在使用装置1期间靠着患者的皮肤穿戴。接触区域21可以例如位于壳体2的底面上。接触区域21具有几何和触觉性质,其被选择为当被穿戴在患者皮肤上时是舒适的。通过壳体2的接触区域21,套管6或其它注射元件在药剂的输送期间突出到患者的身体组织中。接触区域21可以例如包括孔22,套管6在使用装置1期间通过该孔22突出。孔22足够大以容纳上述套管6和/或单独的针,包括在先前描述的扩展和缩回操作期间。
在使用装置1期间,接触区域21通过紧固件保持靠着患者的皮肤。紧固件适于将接触区域21保持在靠着皮肤的稳定位置中持续相当长的时间,例如几个小时,以确保在使用装置1期间注射元件相对于患者的身体始终保持在固定位置。接触区域21可以是大致平面的或大致弓形的,并且可以延伸穿过装置1的表面的至少一部分。如图1和图3所示,合适的紧固件是用于将接触区域21临时粘附到患者皮肤的粘合层23。粘合层23可以包括标准的生物相容的胶,如在普通的胶粘绷带中所使用的。为了保护粘合层23免于损坏并且为了防止粘合层23在附接到患者的皮肤上之前粘附到不期望的物体上,装置1的接触区域21还包括覆在粘合层23上的保护性覆盖物(未示出)。该保护覆盖物可选择性地从接触区域21移除,以便在使用装置1之前例如通过将覆盖物从粘合层23上剥离而暴露粘合层23。
装置1还包括用于向患者提供与药剂输送相关的反馈的反馈设备25。反馈设备25被构造为以患者身体组织的局部加热或冷却的形式向患者身体施加反馈。加热或冷却的程度足以使其容易被患者察觉,如下所述。接触区域21和输送接口4可以通过成形和定尺寸以帮助在该反馈过程中促进热能在反馈设备25和患者身体之间的高效传递。
反馈设备25包括温度控制设备26,该温度控制设备26被构造成在患者穿戴装置1时使热能传入到患者体内或从患者的身体传出。由温度控制设备26引起的热能的传递可以响应于与将药剂输送到患者中相关联的事件而进行。在这些事件中的一个或多个之后使热能传入到患者体内或从患者的身体传出的速率可以相对较快,使得反馈设备25可以向患者提供事件的尖锐指示。反馈设备25可以例如被构造为通过引起患者皮肤温度的相对快速的增加或减少来指示事件。在反馈设备25使皮肤温度(分别)升高或降低不久之后使皮肤温度升高或降低的意义上,温度升高或降低可以以温度峰值的形式提供。
患者皮肤温度变化可由反馈设备25以主动方式或被动方式引起。例如,如下所述,反馈设备25可以被构造为通过使用温度控制设备26主动加热或冷却皮肤来主动地改变患者的皮肤温度。或者,反馈设备25可以被构造为通过停止主动加热或冷却皮肤来改变患者的皮肤温度。这通过允许皮肤温度以自然的方式与其周围环境平衡而引起温度变化。
可以由反馈设备25实现的温度变化的示例是患者皮肤温度在大约2℃和大约5℃之间的变化。该变化可以在短于1分钟,例如短于30秒,或短于10秒的时间内进行。患者皮肤可被加热的最高温度为42℃。这防止反馈设备25使患者的皮肤变性。
可以触发反馈设备25以引起患者可感知的患者皮肤组织的温度变化的事件的示例是药剂注射过程的完成。特别地,装置1可以被构造为检测药剂的剂量何时已经通过套管6或其他注射元件完全注射到患者体内。反馈设备25包括一个或多个适当的传感器,用于检测该信号并且将指示信号馈送回先前提到的电子控制器16。
例如,反馈设备25可以包括活塞位置传感器27,该活塞位置传感器27被构造为检测上述活塞18何时沿胶囊5移动了预定距离。传感器27可以是光学传感器,但是可以使用任何合适的传感器。预定距离表示已经从胶囊5通过开口9被推出到导管10中的药剂的一个剂量。如果胶囊5最初包含多个剂量的药剂,则预定距离对应于胶囊5的部分长度。如果胶囊5仅包含单剂量的药剂,则预定距离可以对应于胶囊5的全长。在感测到活塞18已经行进了预定距离时,活塞位置传感器27被构造为产生指示已经从胶囊5排出一定剂量的药剂的信号。
另外地或替代地,反馈设备25可以包括传感器28,该传感器28被构造为检测预定体积的药剂已经通过前面提到的开口9穿出胶囊5。传感器28可以例如位于开口9或与开口9连接的导管10中。合适的传感器28是药剂流量传感器。传感器28可以通过检测通过导管10进入套管6的药剂的流动已经停止,从而指示预定剂量的药剂已经通过活塞18从胶囊5排出而操作。在感测到一定剂量的药剂已经经过导管10之后,流量传感器28被构造为产生指示一定剂量的药剂已经从胶囊5排出到套管6中的信号。
应当理解,来自传感器27、28的信号指示输送装置1的状态,并且特别地,指示药剂注射到患者的身体组织中的进展。输送装置1的状态不仅可以从上述传感器确定,而且可以从检测指示输送装置1的状态的事件的其他类型的传感器(未示出)确定。这种传感器的示例是位置传感器,其构造成监测套管6或其他注射元件的位置。该传感器构造成当套管6或其它注射元件从壳体2延伸或缩回到壳体2中时向控制器16报告,并且这样做指示药剂输送到患者体内的开始和结束。
由反馈设备25中的上述传感器27、28产生的信号经由通信连接器被转发到装置1的控制器16,通信连接器可以包括之前提到的系统总线。控制器16使用信号来确定与药剂输送相关联的事件,例如当药剂的剂量的输送已经由分配接口4完成时。例如,控制器16可以被构造为根据指示套管6或其他注射元件缩回到壳体2中的信号来判定药剂输送过程的结束。
控制器16可以通过分析来自上述传感器的信号以及存储在其内置存储器中的信息来做出对事件的判定。例如,控制器16可以包含预先存储的数据,该预先存储的数据指示在来自反馈设备25的指示一定剂量的药剂已经从胶囊5排出之后该一定剂量的药剂通过套管6输送所花的时长。控制器16使用该信息来计算药剂输送将何时完成。
另一种选择是反馈设备25使用诸如机械定时器的定时元件来判定与药剂输送相关联的事件。定时元件可以是倒计时定时器。定时元件的倒计数时段的流逝可以指示事件已经发生。例如,反馈设备25可以包括定时器(未示出),该定时器被构造为响应于患者对装置1的初始启动或响应于套管6或其他注射元件从壳体2的延伸而对固定时间段倒计时。倒计数时段的持续时间被预先设置为指示事件。
例如,倒计数时段的持续时间可以设置为等于在患者启动装置1之后将一剂药剂完全输送到患者体内所花费的已知的时长。装置1可以例如通过在装置的外部按下开关34来启动,如下面进一步描述的。在经过倒计数时段之后,定时器和温度控制设备26之间的连接使得温度控制设备26提供与由定时器指示的事件相关的基于温度的反馈。定时器和温度控制设备26之间的连接可以是机械的或电气的。如果装置1不包括上述的中央控制器16,则这种类型的基于定时器的构造可能是特别适用的。
温度控制设备26位于装置1的壳体2的靠近患者的皮肤组织的区域中。例如,如图1所示,温度控制设备26可以位于上述接触区域21中,使得其被定位成在温度控制设备26和患者的皮肤组织之间实现热能的快速传递。
参照图1,温度控制设备26的示例包括一个或多个热电加热或冷却元件,所述一个或多个热电加热或冷却元件可以作为热电加热或冷却装置29的一部分提供。热电加热或冷却装置的具体示例是珀尔帖装置,其包括一个或多个珀耳帖元件。热电装置29包括患者接口材料30,该患者接口材料30被构造为将热能传递到患者的皮肤组织中或从患者的皮肤组织传出。这可以通过与患者皮肤组织的热传导接触或通过适当的中间传热介质的热对流或传导而发生,如图1所示。患者接口材料30是导电和导热材料,其电连接到在装置1的相对侧上的不同的导电和导热材料31。热电装置29被构造为使电流流过材料30、31之间的接合处,以由于珀尔帖效应在材料30、31之间产生温度差。使用该效应,热电装置29被构造为通过监测接口材料30的温度并且在材料30、31之间的结上施加适当的电压来高度精确地控制患者接口材料30的温度。
参照图2,患者接口材料30的温度由温度传感器32检测,温度传感器32例如以热敏电阻的形式,其紧邻材料30的表面定位。使用来自该温度传感器32的信号,热电装置29调节施加在不同材料30、31之间的接合处的电压,从而调节患者接口材料30的温度,以在传感器32处获得期望的值。基于预先存储的值和由反馈设备25中的传感器27、28馈送到控制器16的信息,患者接口材料的期望温度30可在任何给定时间由控制器16传送到热电装置29。以这种方式,控制器16被构造为通过使热电装置29改变患者接口材料30的温度来响应诸如注射完成的事件。
患者接口表面30的温度变化由患者通过患者接口表面30和患者身体围绕注射部位的局部区域之间的热能的流动来感知。这告知患者最近已经发生了与药剂注射相关的事件。取决于热电装置29的构造,患者可能经历加热或冷却感觉。通过适当地控制患者接口材料30的表面的温度,任一种感觉同样是可能的。例如,控制器16可以被构造为通过使热电装置29将患者接口材料30的表面冷却至显着低于患者的体温的温度来响应于与药剂输送相关联的事件。一个示例是比患者的体温低5摄氏度。相反,控制器16可以被构造为通过使热电装置29将患者接口材料30的表面加热到明显高于患者的体温的温度来响应于与药剂输送相关联的另一事件。一个示例是比患者体温高5摄氏度。
如果热电装置29被构造为通过降低患者接口材料30的温度来常规地冷却患者身体的局部区域,则热电装置29可以包括散热器33,该散热器33被布置成将从患者接口材料30提取的热能从热电装置29转移出去。
作为热电装置的补充或替代,温度控制设备26可以包括其他加热或冷却元件或装置。一个示例是被构造成通过在反应模块中产生放热或吸热化学反应来加热或冷却其周围环境的元件或装置。另一个示例是被构造成通过气体(诸如,热泵)的压缩和/或膨胀来加热或冷却其周围环境的元件或装置。另一个示例是被构造为输出红外能量的元件或装置,例如红外加热元件。另一个示例是包括电阻加热元件的元件或装置。这些元件和装置可以响应于来自控制器16的信号以与热电装置类似的方式开始加热或冷却患者身体的局部区域。然而,应当理解,这些替代的加热元件和装置可以可选地由前述类型的相对简单的机械或电气定时器触发。
在所有情况下,温度控制设备26包括接口元件,通过该接口元件将反馈施加于患者的皮肤。这通常是温度控制设备26的温度可控元件,温度控制设备26在将药剂输送到患者期间与患者的皮肤接触或靠得很近。反馈设备25可以被构造为响应于不同的触发事件而将不同的温度施加于皮肤组织,以便允许患者容易地区分不同类型的事件。
装置1被构造为响应于用户启动的触发开始将药剂输送到患者。例如,如图1所示,装置1可以包括用户可致动元件,该用户可致动元件位于壳体2的外部,并且用户可以操作该用户可致动元件以使装置1开始输送药剂。下面在电气开关34的背景下描述可致动元件。开关34可以相对简单地操作,以便改善装置1对患者的可用性。示例是按钮开关或类似物。
下面参照图4描述药剂注射和基于温度的反馈过程的示例。在第一步骤S1中,患者将装置1的接触区域21紧固到他或她身体上的注射部位。患者可以例如将保护性覆盖物从粘合层23上剥离并且将粘合层23压靠在他或她的皮肤上以将装置1附接到注射部位。
在第二步骤S2中,患者致动开关34以开始输送药剂。响应于开关34被致动,装置1被构造为使注射元件延伸穿过壳体2中的孔22并且进入患者的身体组织。例如,控制器16可以被构造成接收开关34已经被致动的指示,并且作为响应,使致动器11以前述方式将套管6移动经过壳体2中的孔22进入患者的皮下组织。装置1可以可选地包括传感器(未示出),该传感器被构造为检测套管6何时已经完全延伸通过壳体2中的孔22并且处于将药剂注射到身体组织内的位置并且向控制器16报告。
在第三步骤S3中,响应于套管6完全延伸到患者体内,控制器16触发药剂流经胶囊5中的开口7并且进入套管6的近端8。例如,控制器16可以使功率从电池15供应到联接到胶囊5中的活塞18的电马达19。电马达19驱动活塞18通过胶囊5的运动,以通过胶囊5的远端中的孔9排出一定剂量的药剂。如果流动控制装置17在胶囊5的开口9处包括密封件20,则该密封件20被破坏以允许流体药剂被释放到导管10中。密封件20可能由于活塞18的移动引起胶囊5中的流体压力而破裂,或者可能被诸如致动器(未示出)的一些其它装置破坏,所述其它装置响应于来自控制器16的信号而移动以刺穿密封件20。
装置1被构造为以预设的方式和速率输送药剂剂量。例如,可以以预设速率以连续方式向患者施用剂量。或者,可以通过活塞18的适当移动在预设时间段内或以任何其它方式以多个离散部分向患者给送剂量。输送的方式和速率可以由控制器16指示。
在第四步骤S4中,反馈设备25向患者的身体施加基于温度的反馈,以指示与药剂输送相关联的事件。由反馈设备25施加的基于温度的反馈的优点是以高度谨慎的方式向患者提供反馈。除患者之外的任何人都不会察觉到反馈。因此,患者可以穿戴装置1并且在没有任何其他人意识到的情况下被告知注射的进展。基于温度的反馈的另一个优点是患者能够以直观的方式理解反馈。温度变化是接收反馈的非常自然的方式,因此反馈设备25提供了改善装置1对患者的使用方便性的益处。人类本能地对其皮肤上的热和冷感觉做出反应。通过适当地控制皮肤温度,装置1可以向患者提供反馈,而患者不需要首先需要了解装置1将如何给出反馈。例如,装置1可以被构造为在注射期间向皮肤输送温热感觉,以指示所有注射都正常进行。这之后可以是皮肤温度的增加或降低,以指示诸如注射结束的事件。温度的变化对于患者可能略微不舒服,使得其被清楚地感知为指示事件。
在第五步骤S5中,控制器16被构造为使致动器11将套管6缩回到患者的身体组织外部,以结束药剂输送过程。
在第六步骤S6中,反馈设备25将进一步的基于温度的反馈施加于患者的身体,以指示药剂输送过程已经完成,并且因此患者可以将装置1从他或她的身体解开。
应当理解,所描述的替代方案可以单独使用或组合使用。
尽管装置1已经被描述为包括自动延伸/缩回的注射元件,但是应当理解,注射元件可以是固定的,使得其永久地突出穿过壳体。在这些情况下,注射元件可以由可移除的保护装置保护,以最小化在使用装置之前元件被损坏或意外损坏其它东西的任何危险。还应当理解,在这些情况下,当将装置靠着患者的皮肤放置时,而不是在如上所述的随后的步骤中,注射元件通常被引入到患者的身体组织中。注射元件可包括上述套管6或可以包括针。如上所述,在一个示例中,注射元件包括具有套管布置的套管针(其不具有孔),该套管针在药剂输送期间在用户组织中留下柔性管,但不将针留在用户中。
装置1在上文描述为被构造为皮下输送药剂。然而,它可以替代地被构造用于皮内注射,例如使用微针,或者以某种其它方式注射。
推注注射器装置可以是称为大体积装置(LVD)的类型。LVD注射装置被构造为分配相对大剂量的药剂,特别是至少1ml,通常高达2.5ml,但可能高达10ml。
推注注射器装置被构造成输送大剂量相应药剂,以在预定时间内使一定体积的药剂进入患者体内。然而,注射速率可能不是关键的,即,可能不需要严格的控制。然而,对于输送速率可能存在(生理)上限,以便避免损害输送部位周围的组织。输送大剂量药剂所需的时间可能在几分钟和若干小时之间,这取决于许多因素,包括药剂的量(体积)、药剂的粘度和意图使用注射装置的注射部位的性质。
从用户或健康护理专业人员的角度来看,期望注射装置被构造为最低限度地影响患者的生活方式和日程安排,从而为患者在注射之间提供关于他或她的疾病的最少提醒。治疗的治疗例程通常是间歇的,即,可以是每周一次注射,每隔一周一次注射或每月一次注射。因此,患者在处理他或她的疾病方面通常没有例行程序,因此在执行所需的注射中具有最少的例行程序/经验。因此,非常期望简化患者对其操作的注射装置的构造。
因为其旨在用于快速推注操作,所以与旨在用于基础操作的注射装置相比,该注射装置的构造是非常不同的。此外,它的使用是完全不同的。例如,基础型胰岛素泵通常是相对昂贵的,因为其包括许多复杂的糖尿病特异性特征,例如可编程输送速率曲线,推注计算器等。此外,经由输注套件到身体的连接在治疗正在进行的同时允许患者在他/她的视野中处理和操纵泵。此外,糖尿病患者在设置输注套件、连接和操作泵以及针对像淋浴以使泵不暴露于水的事件等暂时断开泵方面具有例行程序。相比之下,上述的推注注射器装置可以是相对简单且廉价的装置。它们可以被提供为单次使用装置,其不能用药剂进行再填充,这进一步降低了复杂性和成本。
上述致动器可以包括机械致动器,例如包括一个或多个弹力元件。致动器可以可选地包括螺线管、压电致动器、磁致动器或其它机构。
药剂流经装置可以由一个或多个阀(未示出)控制,特别是如果药剂的贮存器在胶囊5中被加压的话。
本文中使用的术语“药物”(drug)或“药剂”(medicament)意指含有至少一种药学活性化合物的药物配制剂。在一些实施例中,所述药学活性化合物能够具有多至1500Da的分子量或可以包括肽、蛋白质、多糖、疫苗、DNA分子、RNA分子、酶、抗体或其片段、激素或寡核苷酸,或是上述药学活性化合物的混合物。还考虑了化合物的各种类型或亚型。例如,RNA可以包括RNAi、siRNA或miRNA。在其它实施例中,所述药学活性化合物对于治疗和/或预防糖尿病或与糖尿病有关的并发症,诸如糖尿病性视网膜病(diabetic retinopathy)、血栓栓塞病症(thromboembolism disorders)诸如深静脉或肺血栓栓塞、急性冠状动脉综合征(acute coronary syndrome,ACS)、心绞痛、心肌梗死、癌症、黄斑变性(macular degeneration)、炎症、枯草热、动脉粥样硬化和/或类风湿关节炎是会是有用的。在一些实施例中,所述药学活性化合物能够包括至少一种用于治疗和/或预防糖尿病或与糖尿病有关的并发症(诸如糖尿病性视网膜病)的肽。所述药学活性化合物还可包括至少一种人胰岛素或人胰岛素类似物或衍生物、胰高血糖素样肽(glucagon-like peptide,GLP-1)或其类似物或衍生物、或毒蜥外泌肽-3(exedin-3)或毒蜥外泌肽-4(exedin-4)或毒蜥外泌肽-3或毒蜥外泌肽-4的类似物或衍生物或其药学可接受盐或溶剂化物。
胰岛素类似物可包括例如Gly(A21)、Arg(B31)、Arg(B32)人胰岛素;Lys(B3)、Glu(B29)人胰岛素;Lys(B28)、Pro(B29)人胰岛素;Asp(B28)人胰岛素;人胰岛素,其中B28位的脯氨酸被替换为Asp、Lys、Leu、Val或Ala且其中B29位的Lys可以替换为Pro;Ala(B26)人胰岛素;Des(B28-B30)人胰岛素;Des(B27)人胰岛素;和Des(B30)人胰岛素。
胰岛素衍生物可包括例如B29-N-肉豆蔻酰基-des(B30)人胰岛素;B29-N-棕榈酰基-des(B30)人胰岛素;B29-N-肉豆蔻酰基人胰岛素;B29-N-棕榈酰基人胰岛素;B28-N-肉豆蔻酰基LysB28ProB29人胰岛素;B28-N-棕榈酰基-LysB28ProB29人胰岛素;B30-N-肉豆蔻酰基-ThrB29LysB30人胰岛素;B30-N-棕榈酰基-ThrB29LysB30人胰岛素;B29-N-(N-棕榈酰基-Υ-谷氨酰)-des(B30)人胰岛素;B29-N-(N-石胆酰基-Υ-谷氨酰基)-des(B30)人胰岛素;B29-N-(ω-羧基十七酰基)-des(B30)人胰岛素和B29-N-(ω-羧基十七酰基)人胰岛素。
毒蜥外泌肽-4可包括例如毒蜥外泌肽-4(1-39)。
激素可包括例如垂体激素(hypophysis hormones)或下丘脑激素(hypothalamus hormones)或调节性活性肽(regulatory active peptides)和它们的拮抗剂,诸如促性腺激素(促滤泡素(Follitropin)、促黄体激素(Lutropin)、绒毛膜促性腺激素(Choriongonadotropin)、绝经促性素(Menotropin))、生长激素((Somatropin))、去氨加压素(Desmopressin)、特利加压素(Terlipressin)、戈那瑞林(Gonadorelin)、曲普瑞林(Triptorelin)、亮丙瑞林(Leuprorelin)、布舍瑞林(Buserelin)、那法瑞林(Nafarelin)或戈舍瑞林(Goserelin)。
多糖可包括例如葡糖胺聚糖(glucosaminoglycane)、透明质酸(hyaluronic acid)、肝素、低分子量肝素或超低分子量肝素或其衍生物,或前述多糖的硫酸化,例如多硫酸化的形式,和/或其药学可接受的盐。多硫酸化低分子量肝素的药学可接受盐的一个示例是依诺肝素钠(enoxaparin sodium)。
抗体可包括大体球状血浆蛋白质(~150kDa),也称为免疫球蛋白,其共有一种基础结构。因为它们可具有添加至氨基酸残基的糖链,所以它们也可以被归类为糖蛋白。每个抗体的基础功能单元是免疫球蛋白(Ig)单体(仅含有一个Ig单元);分泌的抗体也可以是具有两个Ig单元的二聚体如IgA、具有四个Ig单元的四聚体如硬骨鱼(teleost fish)的IgM、或具有五个Ig单元的五聚体如哺乳动物的IgM。
Ig单体是“Y”形分子,其可包括四条多肽链组成;两条相同的重链和两条相同的轻链,它们通过半胱氨酸残基之间的二硫键连接。每条重链可长约440个氨基酸;每条轻链可长约220个氨基酸。每条重链和轻链可均含有链内二硫键,链内二硫键稳定它们的折叠。每条链都由称为Ig域的结构域构成。这些域代表性地含有约70-110个氨基酸,并根据它们的大小和功能分类被归入不同的范畴(例如,可变或V、恒定或C)。它们具有特征性的免疫球蛋白折叠,其中两个β片层创建一种“三明治”形状,该形状由保守的半胱氨酸和其它带电荷的氨基酸之间的相互作用而保持在一起。
哺乳动物Ig重链有五种类型,表示为α、δ、ε、γ、和μ。存在的重链的类型决定抗体的同种型;这些链分别可以在IgA、IgD、IgE、IgG、和IgM抗体中找到。
不同的重链的大小和组成是不同的;α和γ含有大约450个氨基酸,δ含有大约500个氨基酸,而μ和ε具有大约550个氨基酸。每条重链具有两个区,即恒定区(CH)和可变区(VH)。在一个物种中,恒定区在同一同种型的所有抗体中是基本上相同的,但是在不同同种型的抗体中是不同的。重链γ、α和δ具有包含三个串联Ig域的恒定区,和用于增加柔性的绞链区;重链μ和ε具有包含四个免疫球蛋白域的恒定区。重链的可变区在由不同B细胞生成的抗体中是不同的,但其对于由单个B细胞或单个B细胞克隆生成的所有抗体而言是相同的。每条重链的可变区为大约110氨基酸长并包含单个Ig域。
在哺乳动物中,有两种类型的免疫球蛋白轻链,表示为λ和κ。轻链具有两个连续的域:一个恒定域(CL)和一个可变域(VL)。轻链长大约211到217个氨基酸。每个抗体含有两条轻链,它们总是相同的;在哺乳动物中每个抗体仅存在一种类型的轻链,或是κ或是λ。
如上文详述的,虽然所有抗体的大体结构可非常相似,但是给定抗体的独特性质是由可变(V)区决定的。更具体地说,可变环——其常常在各轻链(VL)上有三个和在重链(VH)上有三个——负责结合抗原,即抗原特异性。这些环被称为互补决定区(Complementarity Determining Regions,CDRs)。因为来自VH和VL域的CDR都对抗原结合位点有贡献,所以它通常是重链和轻链的组合,而不是其中单独一个,决定最终的抗原特异性。
“抗体片段”含有如上定义的至少一个抗原结合片段,并呈现与衍生抗体片段的完整抗体基本上相同的功能和特异性。以木瓜蛋白酶(papain)限制性的蛋白水解消化将Ig原型裂解为三个片段。两个相同的氨基末端片段是抗原结合片段(Fab),每个片段含有一个完整L链和大约一半H链。第三个片段是可结晶片段(Fc),其大小相似但包含的是两条重链的羧基末端的那一半,并具备链间二硫键。Fc含有糖、补体结合位点、和FcR结合位点。限制性的胃蛋白酶(pepsin)消化产生含有两条Fab片和铰链区的单一F(ab')2片段,其包括H-H链间二硫键。F(ab')2对于抗原结合而言是二价的。F(ab')2的二硫键可以裂解以获得Fab'。此外,可将重链和轻链的可变区融合到一起以形成单链可变片段(scFv)。
药学可接受盐例如酸加成盐和碱性盐。酸加成盐例如HCl或HBr盐。碱性盐例如具有选自碱或碱土的阳离子,例如Na+、或K+、或Ca2+、或铵离子。药学可接受溶剂合物例如水合物。
在一些实施例中,可以注射具有各种粘度的药剂。例如,粘度可以在从约3cP至约50cP的范围内。在其它实施例中,粘度可以小于约3cP或大于约50cP。注射还可以包括将药剂输送到患者体内的皮下,肌肉内或透皮位置。药剂可以是以液体、凝胶、浆液、悬浮液、颗粒、粉末或其它类型的形式。
典型的注射体积可以在从约1mL至约10mL的范围内。注射速率可以是约0.5mL/min,约0.2mL/min或约0.1mL/min。这样的注射分布可以在流速上大致恒定,在持续时间上大致连续,或大致恒定并且大致连续。这些注射也可以在单个给送步骤中发生。这种注射分布可以称为推注注射。
使用这种药剂起作用的输送装置可以利用针、套管或被构造成将药剂输送给患者的其它注射元件,如前所述。这种注射元件可以例如具有27G或更小的外部尺寸或直径。此外,注射元件可以是刚性的,挠性的,并且使用一系列的一种或多种材料形成。并且在一些实施例中,注射元件可以包括两个或更多个部件。例如,刚性套管针可以如前所述结合柔性套管一起操作。最初,套管针和套管可以一起移动以刺穿皮肤。然后,可以缩回套管针,同时套管至少部分地保留在目标组织内。稍后,套管可以单独地缩回到输送装置中。
用于插入插入元件的插入机构可以采取任何合适的形式。如上所述,其可以是基于机械弹簧的机构。或者,插入元件机构可以例如包括电马达和齿轮机构,该齿轮机构导致将插入元件插入用户体内。或者,插入机构可以是气体或流体压力操作机构,在这种情况下,针驱动能量源是加压气体的贮存器或化学系统,在该化学系统中,两种或更多种化学品混合在一起以产生气体或流体压力。
- 还没有人留言评论。精彩留言会获得点赞!