用于放射治疗的图像导引的制作方法
优先权要求
本专利申请要求(1)moreau于2014年10月27日提交的题目为“核磁共振成像直线加速器实时图像导引技术”的序列号为62/069,145的美国临时专利申请以及(2)lachaine等人于2014年12月9日提交的题目为“磁共振成像靶定位”的序列号为62/089,482的美国临时专利申请的优先权,其各自的全部内容通过引用并入文中。
本公开总体涉及放射治疗或放射疗法。更具体地,本公开涉及用于使放射疗法治疗计划适应性改变以补偿放射治疗的递送期间的靶肿瘤位置的变化的系统和方法。
背景技术:
放射治疗或“放射疗法”可用于治疗哺乳动物(例如,人和动物)组织中的癌症或其它疾病。一种这样的放射疗法技术是伽马刀,通过伽玛刀,患者被以高强度和高精度汇聚到靶(例如,肿瘤)处的大量低强度γ射线照射。在另一个实施例中,使用直线加速器提供放射疗法,由此肿瘤被高能粒子(例如,电子、质子、离子、高能光子等)照射。放射束的放置和剂量必须被精确控制以确保肿瘤接收到规定的放射,并且射束应当被放置成诸如对周围健康组织(常常称为危及器官(oar))的损害最小化。放射被称为“规定的”,因为医师为肿瘤和周围的器官开了类似于药物处方的预定义的放射量。
通常,准直射束形式的电离放射从外部放射源指向患者。
指定或可选择的射束能量可以用于诸如递送诊断能级范围或治疗能级范围。放射束的调制可由一个或更多衰减器或准直器(例如,多叶准直器)提供。放射束的强度和形状可以通过准直来调节,通过使投射的射束适形于靶向组织的轮廓来避免损害邻近靶向组织的健康组织(例如,危及器官)。
治疗计划程序可以包括使用患者的三维图像来识别靶区(例如,肿瘤)并识别肿瘤附近的关键器官。制定治疗计划可能是一个耗时的过程,其中计划者试图遵守各种治疗目的或约束(例如,剂量体积直方图(dvh)目的)),考虑它们的个体重要性(例如,权重)以产生临床可接受的治疗计划。这个任务可能是被各种危及器官(oar)复杂化的耗时的试错过程,因为随着oar的数量增大(例如,对头颈部治疗达到十三处),该过程的复杂性也增大。远离肿瘤的oar可以容易地免于放射,而靠近靶肿瘤或与靶肿瘤重叠的oar可能难以免于放射。
传统来说,对于每个患者,可以以“离线”的方式产生初始治疗计划。治疗计划可以在放射治疗被递送之前诸如使用一种或更多种医学成像技术很好地改进。成像信息可以包括例如来自x射线、计算机断层摄影(ct)、核磁共振(mr)、正电子发射断层摄影(pet)、单光子发射计算机断层摄影(spect)或超声的图像。诸如医师的医护人员可以使用指示患者解剖结构的三维成像信息来识别一个或更多靶肿瘤连同在肿瘤附近的危及器官。医护人员可以使用手动技术来勾画要接收规定的放射剂量的靶肿瘤,并且医护人员可以类似地勾画附近的有受到放射治疗的损害的风险的诸如器官的组织。可替代地或另外地,可以使用自动化工具(例如,由瑞典的医科达公司提供的abas)来辅助识别或勾画靶肿瘤和危及器官。然后可以使用基于临床和剂量测定目标和约束(例如,对肿瘤和关键器官的最大、最小和平均放射剂量)的优化技术来制定放射疗法治疗计划(“治疗计划”)。
治疗计划过程可以包括使用患者的三维图像来识别靶区(例如,肿瘤)并识别肿瘤附近的关键器官。制定治疗计划可能是一个耗时的过程,其中计划者试图遵守各种治疗目标或约束(例如,剂量体积直方图(dvh)目标)),考虑它们的个体重要性(例如,权重)以产生临床可接受的治疗计划。这个任务可能是被各种危及器官(oar)复杂化的耗时的试错过程,因为随着oar的数量增大(例如,对头颈部治疗达到十三处),该过程的复杂性也增大。远离肿瘤的oar可以容易地免于放射,而靠近靶肿瘤或与靶肿瘤重叠的oar可能难以免于放射。
然后可以通过定位患者并递送规定的放射治疗来在后来进行治疗计划。放射疗法治疗计划可以包括剂量“分份”,由此在预定时间段提供放射治疗递送的序列(例如,45份),其中每个治疗递送包括总规定剂量的指定分份。然而,在治疗期间,为了确保靶肿瘤而不是健康的组织被照射,相对于治疗机(例如,直线加速器“linac”)的患者的位置和靶肿瘤的位置是非常重要的。
技术实现要素:
本发明人认识到了,可以以自适应的方式同时调整放射疗法治疗计划,以补偿向肿瘤递送放射治疗期间的靶肿瘤的位置的变化。例如,诸如肿瘤的期望的靶可以位置偏移到这种程度,使得:如果使用专门的“离线”方式来实现治疗计划,在治疗之前拍摄的医学图像所指示的肿瘤的位置可能与放射疗法治疗期间的肿瘤靶的位置明显不同。例如,与治疗计划中指示的预期或期望的位置相比,肿瘤可能缩小、可能移动或可能未对准。靶的运动可以由一个或更多源引起,诸如心脏运动、呼吸活动、诸如咳嗽的反射或其他活动引起。因此,基于治疗前拍摄的图像应当递送放射治疗的位置会与放射治疗最终被递送时的期望的靶明显未对准。在下文中,“靶部位”是靶的诸如在治疗之前的位置,并且“治疗部位”是治疗期间放射治疗被递送的位置(并且理想地与靶在放射治疗递送时的实际位置对准)。
在一种方案中,可以在放射治疗的递送同时执行成像,诸如在疗程期间在开始放射治疗递送之前立即执行成像采集;或者,在放射治疗递送疗程期间,使用相应的治疗递送的序列,随后立即采集肿瘤的一个或更多图像。这样的成像可以提供有助于识别靶的位置或有助于识别靶的运动的信息。这样的同时成像可以被统称为“实时”的,但是通常在图像的采集与放射治疗的递送之间存在延迟或延时,其通常为大约100到500毫秒(ms)的数量级。
如果三维体积成像信息的采集延迟或成像采集速率是不可接受的(例如,成像采集太慢而不允许治疗导引或控制,诸如,对于呼吸的靶大于约500ms),则会存在问题。本文描述的主题可以诸如通过促进更快速地采集成像切片(包括较早成像的体积区域的一维轮廓、二维切片或包括子体积或子区域在内的三维体积中的一个或更多)来解决这样的问题,所述促进更快速地采集成像切片包括将从一个或更多成像切片快速获取的指示靶部位的部分的信息与从较早采集的体积参考图像获取的信息进行比较。
在一个示例中,自适应图像导引治疗递送系统可以接收包括体积图像的成像信息,并且可以接收对应于包括靶的不同部分的一个或更多成像切片的成像信息,所述体积图像包括放射治疗患者体内的靶,所述成像切片在采集体积图像之后的不同时刻采集。
根据各个示例,所述系统可以空间配准来自较早采集的至少一个成像切片的指示靶的部分的信息,以及空间配准来自较晚时采集的至少一个成像切片的靶的部分。然后,所述系统然后可以确定由空间配准的信息指示的靶的位置与由较早采集的体积图像指示的靶的较早位置之间的差。然后,所述系统可以基于所确定的靶的位置的差来生成更新的治疗方案以控制治疗射束的递送。
在另一示例中,体积参考图像的一部分或全部可以与一个或更多成像切片空间配准,诸如以确定体积参考图像与一个或更多成像切片之间的最佳移动。例如,体积参考图像可以包括三维成像信息(例如,对应于体素的灰度或对比度值),并且所述三维成像信息可以被平移或旋转以实现与一个或更多成像切片(例如,二维成像信息)的最佳配准。移动或旋转后的三维体积成像信息与一个或更多成像切片之间的拟合优度可以包括在不需要分割靶的情况下使用一个或更多度量。
可以以自适应方式生成更新的治疗方案,以将由治疗射束构建的治疗部位与更新的靶部位对准,或者门控所述射束,使得当治疗部位经过靶部位时递送治疗。作为说明性示例,更新治疗方案可以包括以下中的一个或更多:(a)对联接到诸如支撑治疗受检者的椅或台的可移动平台的致动器的调节,(b)对配置成准直或定形治疗射束的一个或更多孔径的调节,(c)对配置成定位治疗输出部以构建指定的治疗射束方向的一个或更多致动器的调节,或者(d)诸如使用从其他传感器获取的成像或信息对治疗递送的门控。
本概述旨在提供对本专利申请的主题的概述。而不是旨在提供本发明的排他或详尽的说明。具体实施方式被包含以提供有关本专利申请的进一步信息。
附图说明
图1a大体示出了可以包括被配置为提供治疗射束的放射治疗输出部的放射治疗系统的示例。
图1b大体示出了放射治疗系统的另一示例。
图1c大体示出了可以包括放射治疗系统和成像系统的组合(诸如可以包括计算机断层摄影(ct)成像系统)的系统的示例。
图1d大体示出了可以包括放射治疗系统和成像系统的组合(诸如可以包括核磁共振(mr)成像系统)的系统的示例的部分剖视图。
图2大体示出了诸如可以用于对放射治疗射束进行成形、定向或调强中的一个或更多种的准直器配置的示例。
图3大体示出了诸如可以包括放射治疗装置和成像采集装置的放射治疗系统的示例。
图4大体示出了可以用于成像采集、图像分割、靶预测、治疗控制或治疗调节中的一个或更多种的系统的示例。
图5大体示出了诸如可以包括具有成像输入部的放射治疗控制器、放射治疗发生器和放射治疗输出部的系统的示例。
图6大体示出了诸如可以使用体积成像技术获取的诸如肿瘤区域的靶部位的视图。
图7a和图7b示出了对应于第一成像平面取向的成像采集平面(图7a中)和相应的采集的成像切片(图7b中)的视图。
图7c和图7d示出了对应于第二成像平面取向(诸如可以与上述关于图7a和图7b的第一成像平面取向正交)的成像采集平面(图7c中)和相应的采集的成像切片(图7d中)的视图。
图7e和图7f示出了对应于第三成像平面取向(诸如可以与上述的关于图7a、图7b、图7c和图7d的第一和第二成像平面取向中的一个或更多正交)的成像采集平面(图7e中)和相应的采集的成像切片(图7f中)的视图。
图8a大体示出了诸如可以随着靶部位从一个成像采集场合(instance)向另一个移动所获取的一系列成像采集平面。
图8b大体示出了诸如可以包括弯曲形状的一系列成像采集区域。
图8c大体示出了诸如可以包括不需要彼此均正交的不同取向的一系列成像采集平面。
图9a大体示出了诸如包括在第一和第二成像切片之间移位的靶部位的一系列两个成像切片。
图9b大体示出了诸如在一个或更多成像切片中调整了分割的靶部位的部分之后的一系列两个空间配准的成像切片。
图10大体示出了可以包括空间配准所分割的靶部位的部分的技术。
图11a大体示出了诸如在不同时间采集的靶部位的部分的空间配准之后靶部位的复合体分割表示。
图11b大体示出了用于确定根据采集的空间配准的成像信息的靶部位的位置与诸如较早采集的体积成像信息所表示的靶部位的较早位置相比的差的技术。
图11c大体示出了用于更新治疗方案以诸如将治疗部位移动到新位置的技术。
图12示出了可以包括使对应于先前采集的成像切片的成像信息的处理与成像采集交错诸如以提高本文所描述的其它技术的效率的技术。
图13大体示出了可以包括接收诸如参考图像的体积成像信息和接收成像切片的诸如方法的技术,包括确定靶部位的位置的差。
附图不一定按比例绘制,在附图中,相同的标号在不同的视图中可以描述相似的部件。具有不同字母后缀的相同的标号可以表示类似部件的不同情形。附图总体通过举例而不是限制的方式示出了本文档中论述的各种实施例。
具体实施方式
图1a大体示出了可以包括被配置为提供治疗射束108的放射治疗输出部104的放射治疗系统102的示例。放射治疗输出部104可以包括一个或更多衰减器或准直器,诸如图2的说明性示例中所描述的多叶准直器(mlc)。回顾图1a,患者可以位于诸如平台116(例如,台或椅)上的区域112中,以根据放射疗法治疗计划接收放射治疗剂量。放射治疗输出部104可以位于台架106或其他机械支撑件上,诸如围绕轴线(“a”)旋转治疗输出部104。平台116或放射治疗输出部104中的一个或更多可以可移动到其他位置,例如可在横向方向(“t”)或侧向方向(“l”)上移动。其他自由度是可以的,例如围绕一个或更多其它轴线的旋转,诸如围绕横向轴线(表示为“r”)的旋转。
图1a所示的坐标系(包括轴线a、轴线t和轴线l)可以具有位于等中心110处的原点。该等中心可以被定义为放射治疗射束108与坐标轴的原点相交的位置,诸如以将规定的放射剂量递送到患者身上或患者体内的位置。例如,等中心110可以被定义为对于由台架106围绕轴线a定位的放射治疗输出部104的各种旋转位置而言放射治疗射束108都与患者相交的位置。
在一个示例中,检测器114可以位于治疗射束108的场内,诸如可以包括平板检测器(例如,直接检测器或基于闪烁的检测器)。检测器114可以与放射治疗输出部104相对地安装在台架106上,诸如以随着台架106旋转而保持与治疗射束108对准。以这种方式,检测器114可以用于监测治疗射束108,或者检测器114可以用于诸如射野成像的成像。
在说明性示例中,平台116、治疗输出部104或台架106中的一个或更多可以自动定位,并且治疗输出部104可以根据针对具体治疗递送情形的指定剂量来构建治疗射束108。可以诸如使用台架106、平台116或治疗输出部104的一个或更多不同取向或位置根据放射治疗计划来指定一系列治疗递送。治疗递送可以相继地发生,但可以在患者身上或患者体内的诸如在等中心110处的期望的治疗部位中相交。因此,可以将规定的累积剂量的放射治疗递送到治疗部位,同时减少或避免了对治疗部位附近的组织的损伤。
如关于文中其他示例所述,放射治疗系统102可以包括或可以联接到成像采集系统,诸如以提供核磁共振(mr)成像、诸如可以包括计算机断层摄影(ct)成像的x射线成像、或超声成像中的一个或更多种。在一个示例中,可以使用mr成像信息或其他成像信息来生成等同于ct成像的成像信息或可视化,而不需要实际的ct成像。这样的成像可以被称为“伪ct”成像。
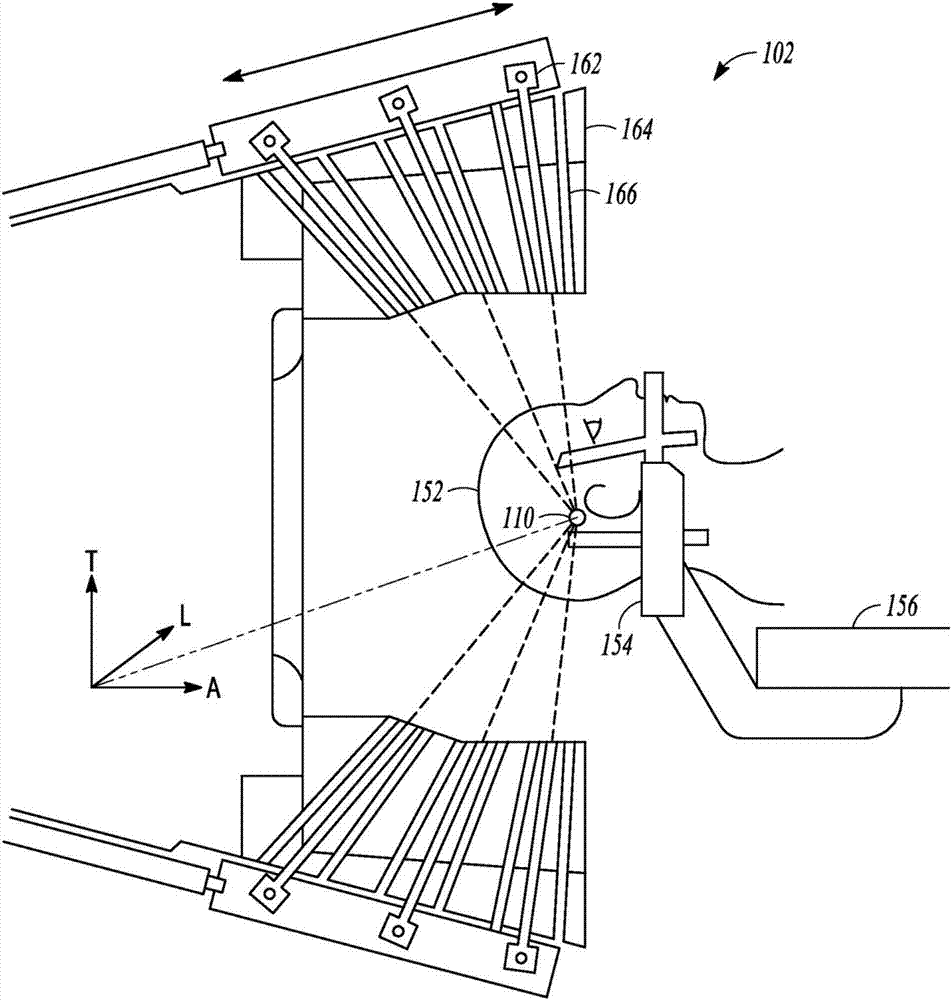
图1b大体示出了根据本公开的一些实施例的放射治疗系统102(例如,由瑞典斯德哥尔摩的医科达公司制造的leksell伽马刀)的另一示例。如图1b所示,在放射治疗疗程中,患者152可以佩戴坐标架154以稳定患者解剖结构(例如,头部)的经历手术或放射治疗的部分。坐标架154和患者定位系统156可以构建可以在对患者进行成像的同时或在放射手术期间使用的空间坐标系。
放射治疗装置102可以包括保护壳体164以封闭多个放射源162。放射源162可以通过射束通道166产生多个放射束(例如,小射束)。多个放射束可以被配置为从不同方向聚焦在等中心158上。虽然每个单个的放射束可以具有相对低的强度,但是当来自不同放射束的多剂量聚集在等中心158处时,等中心158可以接收到相对高水平的放射。在某些实施例中,等中心158可以对应于在进行手术或治疗的诸如肿瘤的靶。
图1c大体示出了可以包括放射治疗系统102和成像系统(诸如可以包括计算机断层摄影(ct)成像系统)的组合的系统的示例。ct成像系统可以包括诸如提供千电子伏特(kev)能量范围的x射线能量的成像x射线源118。成像x射线源118提供指向诸如平板检测器的成像检测器122的一个或更多扇形或锥形射束120。放射治疗系统102可以类似于关于图1a描述的系统102,诸如包括放射治疗输出部104、台架106、平台116和另一平板检测器114。如在图1a、图1b以及图1d的示例中,放射治疗系统102可以联接到或者可以包括被配置为提供治疗放射束的高能量加速器。x射线源118可以提供用于成像的较低能量的x射线诊断射束。
在图1c的说明性示例中,放射治疗输出部104和x射线源118可以安装在相同的旋转台架106上,彼此旋转地分开90度。在另一示例中,可以沿着台架106的圆周安装两个以上的x射线源,诸如每个x射线源自带检测器布置,以同时地提供多个角度的诊断成像。类似地,可以提供多个放射治疗输出部104。
图1d大体示出了可以包括放射治疗系统102和成像系统(诸如可以包括核磁共振(mr)成像系统130)的组合的系统的示例的部分剖视图。mr成像系统130可以布置成限定围绕轴线(“a”)的“孔”,并且放射治疗系统可以包括放射治疗输出部104,诸如以沿着轴线a提供指向该孔内的等中心110的放射治疗射束108。放射治疗输出部104可以包括准直器124,诸如以控制、定形或调制放射治疗射束108中的一种或多种,以将射束108指向到与患者体内期望的靶部位对准的治疗部位。患者可以由平台支撑,诸如由可沿着轴向方向a、侧向方向l或横向方向t中的一个或更多而定位的平台支撑。放射治疗系统102的一个或更多部分可以安装在台架106上,诸如以使放射治疗输出部104围绕轴线a旋转。
图1a、图1b、图1c和图1d大体示出了包括其中治疗输出部可以围绕中心轴线(例如,轴线“a”)旋转的配置的示例。还可以使用其他放射治疗输出部配置。例如,放射治疗输出部可以安装在诸如具有多个自由度的机器人臂或操纵器上。在又一示例中,治疗输出部可以被固定,诸如被定位在与患者侧向分离的区域中,并且可以使用支撑患者的平台来将放射治疗等中心与患者体内的指定的靶部位对准。
图2大体示出了诸如可用于定形、指向或调制放射治疗射束的强度中的一种或多种的多叶准直器(mlc)132的示例。在图2中,叶片132a至132j可以被自动定位以限定近似于肿瘤140横截面或投影的孔径。根据放射治疗计划,在孔径之外的区域中,叶片132a至132j可以由指定用于衰减或阻挡放射束的材料制成。例如,叶片132a至132j可以包括诸如包括钨在内的金属板,其中板的纵轴线垂直于射束方向而定向,并且具有平行于射束方向而定向的端部(如图2的图示的平面所示)。mlc132的“状态”可以在放射治疗的过程中自适应地调节,诸如以与使用静态准直器配置相比或者与使用专门使用“离线”治疗计划技术而确定的mlc132配置相比构建了更好地近似肿瘤140或其他靶部位的形状或位置的治疗射束。包括使用mlc132产生对肿瘤或肿瘤内的特定区域的指定放射剂量分布的放射治疗技术可以被称为强度调制放射治疗(imrt)。
图3大体示出了诸如可以包括放射治疗装置330和成像采集装置的放射治疗系统300的示例。放射治疗系统300可以包括训练模块312、预测模块314、训练数据库322、测试数据库324、放射治疗装置330和图像采集装置350。放射治疗系统300还可以连接到治疗计划系统(tps)342和可以提供患者信息的肿瘤信息系统(ois)344。另外,放射治疗系统300可以包括显示装置和用户界面。
图4大体示出了可用于成像采集、图像分割、目标预测、治疗控制或治疗调节中的一个或更多的系统400的示例。根据一些实施例,系统400可以是与所公开的实施例相符的能够识别、分析、维护、生成或提供大量数据的一个或更多高性能计算装置。系统400可以是单独的,或者它可以是子系统的一部分,子系统又可以是更大的系统的一部分。例如,系统400可以表示远程定位并通过诸如因特网或诸如局域网(lan)或广域网(wan)的专用网络的网络进行通信的分布式高性能服务器。在一些实施例中,系统400可以包括嵌入式系统、成像扫描仪(例如,核磁共振(mr)扫描仪或诸如计算机断层摄影(ct)扫描仪的其他扫描仪)和/或与一个或更多远程定位的高性能计算装置通信的触摸屏显示装置。
在一个实施例中,系统400可以包括一个或更多处理器414、一个或更多存储器410以及一个或更多通信接口415。处理器414可以是包括诸如微处理器、中央处理单元(cpu)、图形处理单元(gpu)等的一个或更多通用处理装置的处理器电路。更具体地,处理器414可以是复杂指令集计算(cisc)微处理器、精简指令集计算(risc)微处理器、超长指令字(vliw)微处理器、实现其他指令集的处理器、或实现指令集的组合的处理器。
处理器414还可以是一个或更多专用处理装置,诸如专用集成电路(asic)、现场可编程门阵列(fpga)、数字信号处理器(dsp)、片上系统(soc)等。如本领域技术人员将领会的,在一些实施例中,处理器装置414可以是专用处理器,而不是通用处理器。处理器414可以包括一个或更多已知的处理装置,诸如由inteltm制造的pentiumtm或xeontm系列的微处理器、由amdtm制造的turiontm系列的微处理器、或由其他供应商诸如oracletm制造的任何各种处理器(例如,sparctm架构处理器)。处理器414还可以包括由nvidiatm制造的图形处理单元。所公开的实施例不限于与所公开的实施例相符的以其他方式被配置为满足识别、分析、维护、生成和/或提供大量成像数据或任何其他类型的数据的计算需求的任何类型的(一个或数个)处理器。
存储器410可以包括被配置为存储由处理器414使用的计算机可执行指令的一个或更多存储设备,以执行与所公开的实施例相关的功能。例如,存储器410可以存储用于治疗计划软件411、操作系统软件412以及训练/预测软件413的计算机可执行软件指令。处理器414可以通信地联接到存储器/存储设备410,并且处理器414可以被配置为执行存储在其中的计算机可执行指令,以执行根据所公开的实施例的一个或更多操作。例如,处理器414可以执行训练/预测软件413以实现训练模块312和预测模块314的功能。此外,处理器装置414可以执行可以与训练/预测软件413交互的治疗计划软件411(例如,诸如由医科达提供的
所公开的实施例不限于分离的程序或被配置为执行专用任务的计算机。例如,存储器410可以包括执行系统400的功能的单个程序或多个程序(例如,治疗计划软件411和/或训练/预测软件413)。此外,处理器414可以执行距系统400远程定位的一个或更多程序,诸如存储在数据库420中的程序,这样的远程程序可以包括肿瘤信息系统软件或治疗计划软件。存储器410还可以以系统可用来执行与所公开的实施例相符的操作的任何格式来存储图像数据或任何其他类型的数据/信息。
通信接口415可以是被配置为允许由系统400接收和/或发送数据的一个或更多装置。通信接口415可以包括允许系统400与其他机器和装置通信的一个或更多数字和/或模拟通信装置,诸如系统400的远程定位组件、数据库420或医院数据库430。例如,处理器414可以通过通信接口415与(一个或数个)数据库420或(一个或数个)医院数据库430通信地连接。例如,通信接口415可以是诸如因特网、或者诸如lan或wan的专用网络的计算机网络。可替代地,通信接口415可以是允许处理器414向(一个或数个)数据库420、430发送数据或者从(一个或数个)数据库420、430接收数据的卫星通信线路或任何形式的数字或模拟通信线路。
(一个或数个)数据库420和(一个或数个)医院数据库430可以包括存储信息并通过系统400访问和管理的一个或更多存储器装置。以示例的方式,(一个或数个)数据库420、(一个或数个)医院数据库530或两者可以包括诸如oracletm数据库、sybasetm数据库或其他数据库的关系数据库,并且可以包括诸如hadoop序列文件、hbase、cassandra或其他数据库的非关系数据库。数据库或其他文件例如可以包括诸如用于训练或提供参考图像、mr特征向量、ct值、降维特征矢量、(一个或数个)伪ct预测模型、(一个或数个)伪ct值、伪ct图像、dicom数据等的与成像对象相关联的来自mr扫描或ct扫描的一个或更多原始数据。然而,所公开的实施例的系统和方法不限于分离的数据库。在一个方案中,系统400可以包括(一个或数个)数据库420或(一个或数个)医院数据库430。可替代地,(一个或数个)数据库420和/或(一个或数个)医院数据库430可以距系统400远程定位。(一个或数个)数据库420和(一个或数个)医院数据库430可以包括被配置为接收和处理针对存储在(一个或数个)数据库420或(一个或数个)医院数据库430的存储器装置中的数据的请求并提供来自(一个或数个)数据库420或(一个或数个)医院数据库430的数据的计算组件(例如,数据库管理系统、数据库服务器等)。
系统400可以通过网络(未示出)与其他装置或系统400的组件进行通信。该网络可以是提供通信、交换信息或促进信息的交换并实现通过网络(未示出)在其他装置和/或系统400的组件之间发送和接收信息的任何类型的网络(包括基础设施在内)。在其他实施例中,系统400的一个或更多组件可以通过诸如系统400与(一个或数个)数据库420和(一个或数个)医院数据库430之间的链路(例如,硬布线链路、无线链路、或卫星链路、或者其他通信链路)的(一个或数个)专用通信线路直接地通信。
为了便于描述,文中已经定义了系统400的功能构建模块的配置和边界。只要适当地执行指定的功能和关系,就可以定义其他可替代的边界。基于文中所包含的教导,替代方案(包括文中所述的那些方案的等同形式、扩展形式、变化形式、偏离形式等在内)对于相关领域的技术人员来说将是显而易见的。这样的替代方案落入所公开的实施例的范围之内。
图5大体示出了诸如可以包括具有成像输入部560的放射治疗控制器系统554、放射治疗发生器556和放射治疗输出部504的系统500的示例。治疗发生器556可以包括诸如直线加速器的加速器,或另一放射源,并且治疗输出部504可以联接到治疗发生器556以处理由治疗发生器556提供的能量光子或粒子的射束。例如,治疗输出部504可以包括或可以联接到输出致动器566以旋转或平移治疗输出部504中的一种或多种以提供具有指向期望的靶部位的治疗部位的放射治疗射束。治疗输出部504可以包括准直器564,诸如上文关于图2所述的多叶准直器。回顾图5,治疗控制器系统554可以被配置为使用如文中其他示例中所述的自适应放射治疗技术来控制治疗发生器556、治疗输出部504或患者位置致动器516(诸如包括椅或台的可移动平台)的一个或更多。
治疗控制器系统554可以诸如使用传感器输入部562联接到一个或更多传感器。例如,患者传感器558可以向治疗控制器系统提供生理信息,诸如指示呼吸运动(例如,使用体积描记传感器)、患者心脏机械或电活动、外周循环活动、患者位置或患者运动中的一个或更多的信息。这样的信息可以提供与待由治疗输出部504靶向的一个或更多器官或其他区域的运动相关的替代信号,并且这样的信息可以用于控制治疗(例如,用于治疗门控)。
成像输入部560可以联接到成像系统550(作为说明性示例,诸如可以包括计算机断层摄影成像系统、核磁共振(mr)成像系统或超声成像系统)。可替代地,或另外地,治疗控制器系统554可以从诸如集中式成像数据库或成像服务器的成像数据存储部552接收成像信息。治疗控制器系统554或成像系统550中的一个或更多可以包括关于图4所示的系统400所示出和描述的元件。
图6大体示出了诸如待使用放射治疗来治疗的肿瘤区域的靶部位616的视图。可以使用体积成像技术来获取指示靶部位616的信息。图6中的表示被示出为具有矩形小平面仅仅是为了说明的目的,并且实际的靶部位616可以包括弯曲或不规则的表面。关注区域612可以诸如使用mr成像、ct成像、伪ct图像可视化、射野成像、超声成像或其它技术中的一个或更多来成像。诸如可以使用自动化、手动或半自动图像分割技术来识别靶部位616。例如,指定的标记可以赋予体素(例如,体素620)以识别构成放射治疗靶的体素的部位或组。作为说明性示例,可以将体素620的对比度值与相邻的体素进行比较,并且诸如使用对比度信息可以识别肿瘤或其它区域的边缘。还可以识别其他区域,诸如附近的器官或其他特征的位置。
可以确定靶部位的各种特征,诸如一个或更多边缘位置(例如,使用边缘检测或边缘识别技术)。例如,可以通过确定靶部位616的空间质心608来识别靶部位616的位置。将质心608用作提取特征是说明性的,并且诸如手动识别或自动确定的靶部位616的点、表面或边缘的位置的其它特征也可用于追踪靶部位616运动。在又一示例中,可以使用可植入或外部种子基准,诸如在获取的成像信息中提供标记。
靶部位616和诸如质心608的一个或更多对应的特征可以在治疗计划成像期间被识别,诸如份间地(例如,在各次放射递送之间)或恰好在开始一次放射治疗递送之前被识别。包括靶部位616的体积成像信息可以被称为“参考图像”。如上所述,因为图像采集和处理延迟可能妨碍在放射治疗期间对体积成像信息的“实时”采集,所以可能存在挑战。相应地,每份内的图像采集(诸如在一次放射治疗中的放射治疗递送期间或之间)可以包括更快速地采集成像切片(包括一维轮廓、二维切片或包括较早成像的体积区域的子体积或子区域的三维体积中的一个或更多)。可以将指示从一个或更多成像切片快速获取的靶部位的部分的信息与从较早采集的体积参考图像获取的信息进行比较,以更新治疗方案,诸如由于靶部位的移动而调节治疗。用于获取或产生体积参考图像的成像模式不必与用于份内的成像的成像模式相同。
在另一示例中,靶部位616不需要在体积参考图像中被分割或以其他方式识别。短语“靶部位”的使用仅仅是说明关注区域内的靶,例如待治疗的肿瘤的一部分或全部或该肿瘤附近的诸如器官的其它解剖结构。除了对靶部位616的分割之外,或者代替对靶部位616的分割,还可以执行如本文所述的各种技术,诸如包括诸如使用包括对比度或灰度值的体素值将体积参考图像的一部分(例如,指定的关注区域)或体积参考图像的整体与其他成像信息空间配准。例如,这种空间配准可以包括与一个或更多二维成像切片的三维(例如,体积)配准(例如,3d到2d配准)或其他技术。
图7a和图7b示出了对应于沿着线706a与靶部位716相交的第一成像平面取向的靶部位716的成像采集平面712a(图7a中)以及相应的采集的成像切片714a(图7b中)的视图。作为说明性示例,图7a可以表示图像采集平面712a和对应的切片714a的矢状取向。成像“切片”可以包括二维像素成像信息或三维成像信息,诸如具有如图7b所示的小的有限厚度。诸如再次使用分割技术(例如使用离散动态轮廓、snake分割算法或水平集或基于配准的技术)可以识别成像切片714a中的靶部位的部分718a。
可以获取诸如包括如图7c、图7d、图7e和图7f所示的不同成像采集平面取向的一系列成像切片。例如,图7c和图7d示出了对应于(诸如可以与上述关于图7a和图7b所述的第一成像平面取向正交的)第二成像平面取向的沿着线706b与靶部位716相交的成像采集平面712b(图7c中)以及相应的采集的包括靶部位716的不同部分718b的成像切片714b(图7d中)的视图。作为说明,图7c和图7d可以对应于冠状平面。图7e和图7f示出了对应于(诸如可以与上文关于图7a、图7b、图7c和图7d所述的第一和第二成像平面取向中的一个或更多正交的)第三成像平面取向的沿线706c与靶部位716相交的成像采集平面712c(图7e中)以及相应的采集的包括靶部位716的又一不同部分718c的成像切片714c(图7f中)的视图。作为说明,图7e和图7f可以对应于轴状成像平面。图7a、图7b、图7c、图7d、图7e和图7f的成像切片被示出为彼此正交的二维平面。然而,如关于文中其他示例所述,切片既不需要是平面的也不需要是正交的。可以处理每个采集的成像切片,包括与采集成像切片并行来处理一个或更多切片。例如,这样的处理可以包括来自体积参考图像的诸如对应于所采集的成像切片的平面或区域的采样信息。
在一个方案中,从一个或更多成像切片714a、714b或714c提取的特征可以与从体积参考图像提取的成像信息进行比较。例如,来自体积参考图像的分割的靶部位616的部分或者封装靶部位和周围组织的区域可以与对应的成像切片714a、714b或714c进行空间配准,以确定靶部位是否已经移动。然而,将从单个二维成像切片提取的特征与来自体积参考图像的对应的特征进行比较可能存在挑战。例如,图8a大体示出了诸如可以随着靶部位816从一个成像采集情形移动到另一个而获取的一系列成像采集平面812a、812b和812c。在时刻ti-2,成像采集平面与靶部位816相交的线806a大致居中,在时刻ti-1,线806b移动,而在时刻ti,线806c进一步移动。在时刻ti、ti-1、ti-2、...获取的成像切片通常可标记为si,、si-1、si-2、...。
如果靶部位的运动是平面外的,则即使靶部位显著移动,或者靶部位可能呈现出变形,质心或其他特征位置随着图像变化可能仍然不会呈现明显地移动,使得对运动的解析变得困难。然而,诸如通过如下的一种或更多种:改变连续采集的成像切片的取向(例如,如图8c和其他地方所示),或者针对成像采集区域的非平面形状进行改变或补偿使得该成像切片在三维意义上未被表示为完全平坦的(例如,如图8b所示),可以适当地追踪这种平面外的运动,。图8b大体示出了诸如可以包括弯曲形状的一系列成像切片813a、813b和813c。通常,即使当参考图像采集“平面”时,本文所描述的技术仍然可以与诸如图8b的弯曲切片的其他切片几何形状一起使用。作为说明性示例,mr成像信息可以得到用作平面切片,并且可以对平面切片施加变换以获取在三维意义上弯曲的表面,诸如帮助捕获或校正整个成像场上的失真,诸如以补偿已构建的磁场的不均匀性。作为另一说明性示例,图8c大体示出了诸如可以包括不必各自正交的不同取向的一系列成像采集平面815a、815b和815c。
如上所述,如果在时间上相继地采集了成像切片,则靶部位可能在连续的图像采集之间移动。图9a大体示出了诸如包括在第一和第二成像切片之间移位的靶部位的一系列的两个成像切片。两个相继采集的成像切片的示例是说明性的。本文描述的技术还通常适用于两个以上的成像切片的序列(或者甚至是关于参考体积成像信息的一部分或全部所分析的单个成像切片)。
成像切片914a(例如,si)可以包括靶部位的部分918a,并且第二成像切片914b(诸如在时间上较早采集的si-1)可以包括第二部分918b。第二部分918b呈现出相对于第一部分918a移动了位移920。由于位移920通常是未知值或向量,所以可以使用各种技术,诸如以将第一部分918a和第二部分918b空间配准。如图9b所示,空间配准的切片914c可以包括靶部位的部分918c的调节后的位置。符号上,一组或一系列采集的成像切片可以被标记为si、si-1、si-2、...、si-n,其中si对应于最近采集的用于处理的切片,si-n对应于最早采集的用于处理的切片。一系列空间配准的成像切片可以被标记为si、s'i-1、s'i-2、...s'i-n。
图10大体示出了可以包括将从两个(或多于两个)成像切片si、si-1、si-2、...、si-n分割的靶部位的部分空间配准的技术。在一个方案中,可以定义量化靶部位1018a和1018b的两个部分对准的程度(或更一般地,两个成像切片或成像体积对准的程度)的度量,诸如沿着接合第一部分1018a和移动后的第二部分1018b的相交线1022的像素之间的相似度。这种度量的示例包括一维归一化互相关度或互信息。可以执行自动优化技术来找到提供度量的最佳值的第二部分1018b的平移。可以使用掩膜将计算限制为仅最相关的像素,诸如接近关注靶的像素。该第一方案通常依赖于具有公共相交线的平面。
另一种方案可以包括创建诸如具有第一图像和第二切片取向的第二图像的三维(3d)体素图像,第一图像对应于第一切片取向,包括对应于切片内的靶部位的部分的填充体素和切片外的零值体素,第二图像包括对应于第二图像中的靶部位的部分的其自身的填充体素。作为说明性示例,mr成像切片通常具有诸如对应于约5毫米的有限的厚度。可以通过使用从mr成像切片提取的二维(2d)像素信息在实际切片厚度内向体素赋予切片信息来考虑有限的切片厚度。可以使用3d配准技术找到两个3d图像之间的最佳平移,并且可以使用掩膜来排除不包含切片信息的体素。3d配准方案也通常依赖于具有公共的相交线。图11a中说明性地示出了三维配准的成像切片的说明性示例。
在又一方案中,可以将预测技术应用于先前的成像切片,以找到靶部位的部分对于先前的成像切片取向但是具有与当前或更近期采集的成像切片相同的时间戳的最可能位置。可以使用诸如内核密度估计、神经网络或模板匹配技术的各种技术用于这样的预测。如果靶部位的运动本质上是高度周期性的,诸如是与呼吸运动相关的,则预测可以是特别有效的。尽管使用预测仅仅是一种近似,但是其还可以与上文和本文其他地方描述的基于图像的方法结合来使用。基于预测的方案不依赖于具有公共相交线的图像采集平面,由此当采集平行的切片时可以使用预测技术。
在另一方案中,当采集到快速垂直mr成像切片时,暗线在当前图像中可能出现在先前图像被激发并且尚未完全松弛到平衡的位置。因为来自先前切片的激发的磁偶极子跟随移动的解剖结构,所以先前激发的可见区域(例如,激发线)可以用作将先前的切片与较晚采集的成像信息对准的锚定物。这可以隐式地与上述的其他技术一起考虑,因为诸如像素或体素特征这样的变暗区域可能影响配准,或者诸如通过识别或显式地确定这些变暗区域在所采集的成像切片中的位置来显式地考虑。例如,可以使用峰值检测技术来找到沿着变暗区域的中心的点,并且可以找到一条提供对这些点的最优拟合的线(直线或曲线)。本文档中描述的各个示例是指图像之间的配准,诸如包括分割的第一图像的部分与第二图像(或一系列图像)的分割的部分或其他识别出的特征的配准。通常,两个图像之间的配准可以包括运动图像和固定图像。目的可以是确定运动图像的位置或变换,使其与固定图像最优拟合。例如,“运动”可以意味着在一个或更多维度上空间地移动(仅平移)运动图像,移动和旋转运动图像,或者甚至使运动图像变形。可用于移动运动图像的自由度可以被称为“优化参数”,作为说明性示例,“优化参数”在仅关于两个2d图像的移动情况下可以包括两个自由度,或者针对3d图像可以包括移动加旋转的6个自由度。尽管通常我们可能是指3d图像配准,但是在不失去通用性的情况下“优化参数”仍然可以通常被称为“移动值”。
对于给定的一组优化参数,度量可以定义运动图像与固定图像之间确定的重叠的“优良度”。各个示例可以包括确定归一化互相关度或互信息(诸如将体素或像素值用作输入值),并且这样的技术可以当图像完美匹配时提供对最佳的度量值的指示。底层成像技术的属性可以有助于确立使用哪个度量。例如,互信息技术可以用于使用诸如正电子发射断层摄影(pet)和ct成像的不同模式所获取的图像。
可以使用优化技术来找到优化运动图像与固定图像之间的度量的移动值,诸如以识别给出两个图像之间的最优匹配的移动值。可以使用的不同的优化工具可以包括梯度下降、模拟退火、信任区域梯度下降、或者一个或更多其他技术。在一些情况下,图像之间可能会出现变形,但并不总是需要优化变形矢量场并考虑这些因素,因为变形信息的优化可能导致一个或更多不期望的延迟或者可能削弱优化技术的稳定性。度量的计算可以限于诸如被称为“掩膜”的指定的关注区域。例如,假设在关注区域中存在可忽略的变形,则可以使用没有变形的一个或更多平移或旋转来确定在指定的关注区域中局部最佳的移动值。
通常,如果一个或更多2d成像切片可用,则可以在当前2d切片(诸如mr成像切片)与初始3d体积(例如,参考体积图像)之间确定放射治疗靶的运动。作为说明性示例,3d体积还可以对应于特定的呼吸相以减少呼吸运动模糊,这可以通过门控成像或触发成像(例如,触发成像)或者通过在特定阶段从四维成像信息中提取3d体积图像(例如,从诸如使用mr成像获取的4d成像信息的4d成像序列中提取3d体积快照)来完成。
在一个方案中,靶自身可以在成像切片中被识别。然而,虽然在本文其他地方提到了分割,但是在不执行分割或其他特征提取的情况下,本文描述的技术也是适用的。作为说明性示例,可以在一个或更多较晚采集的成像切片与较早采集的参考3d图像之间确定灰度值的最优拟合。靶不需要实际在图像中,而是可以指定关注区域,诸如可以包括靶的部分、或者靶加扩边(margin)、或者仅仅是没有靶的任意关注区域。
在一个方案中,可以执行2d/3d配准以找到当前成像切片与参考体积之间的相对移动。关于配准技术,3d图像可以表示“运动图像”,并且2d切片可以表示“固定图像”。通常,可以在3d图像中识别靶的位置,并且,诸如在三维坐标系内,将相对移动应用于较早的靶位置可以提供对靶的更新位置的估计。这样的估计可以在不需要确定变形的情况下执行,并且甚至可以在不使用旋转参数的情况下执行,诸如以增大优化技术的执行效率。诸如当将3d参考图像配准到一个或更多2d成像切片时,可以应用这种简化假设。
例如,(尽管关注区域不需要包括靶或靶的整体),可以使用指定的关注区域来限定围绕靶加扩边的掩膜。可能存在变形,但是作为说明性示例,如果扩边是小的,则变形也会是很小的(例如,可忽略的),并且可以使用忽略变形的配准技术来确定目标自身的移动。以这种方式,单平面技术(例如,成像切片是固定图像的技术)仍然可以提供指示三维移动的信息。当图像中有足够的特征来“锁定”三维的配准时这种技术是稳健的---配准收敛到良好定义的优化---尽管不需要提取或分割特征。
在一个方案中,由于这样的技术趋于匹配图像边缘,并且会因图像不同而不同的灰度绝对值较不敏感,因此可以将图像的梯度的归一化互相关度用作配准度量。在一些情况下,单成像切片或平面可能不够足够稳健来确立具有清楚最佳值的移动(通俗而言,“锁定”)。相应地,作为说明性示例,诸如使用当前的矢状切片的和先前采集的冠状切片(反之亦然),附加的切片可以用于帮助在所有方向上锁定。由于用于配准的切片的计数增加,因此无论是平行的平面、正交的平面、还是在非平行的平面和非正交的平面中,更多的信息可用于执行参考体积图像与较晚采集的成像切片之间的配准,这提高了所得到的移动参数确定的稳健性。
配准可以包括在一个或更多成像切片上扫描3d体积,或者如本文其他地方所述,可以将切片插入到3d体积中,在这种情况下,可以使用3d到3d配准技术(诸如抑制或忽略对未填充体素的配准)。诸如如果快速连续地采集切片,例如,对应于采集的切片的时刻之间小于约50ms,则多切片技术效果良好。如果在成像切片采集之间发生了较长的持续时间,则较旧的切片可能变得“过时”。然而,这样的切片仍然可以使用以下方式在时间上重新对准:a)诸如靶运动是周期性属性的情况下使用预测技术;b)例如,如本文其他地方所述,通过拟合线经过由成像模式提供的激发线(例如,从mr成像采集可见的激发线)来对准该激发线;或者c)通过使用沿着相交线计算出的度量来将过时的成像切片空间配准,使得其与当前的切片适配。
图11a总体示出了诸如对应于空间配准的成像切片1114a和1114b的在不同时间采集的分割的靶部位的部分的空间配准之后靶部位的复合体1118表示。在来自两个以上的成像切片的靶部位的部分已经被空间配准之后,可以诸如从复合体1118提取特征。例如,可以确定复合体1118的质心位置1108或其他特征,诸如提供对靶部位的质心位置的估计用于更新放射治疗方案。在另一示例中,可以使用第一成像切片1114a和第二成像切片1114b中的靶部位的部分之间的所确定的空间位移来更新放射治疗方案。
图11b大体示出了用于根据采集的空间配准的成像信息的靶部位的复合体1118的较晚估计或预测的位置与诸如由先前采集的体积成像信息所表示的靶部位616的较早位置相比的差的技术。可以使用一个或更多特征的位移来估计当前或将来的靶部位位置。例如,可以在从参考成像信息提取的较早确定的质心608与稍后确定的质心1108之间确定位移。在另一示例中,可以在不需要提取或确定诸如质心的特征的情况下,使用来自成像配准的移动参数来提供更新的靶部位。通常,可以使用各种其他技术,诸如来提取指示在利用空间配准的成像切片的情况下靶部位616的运动或位移的信息。
例如,一旦先前的成像切片集合对准到当前的切片而形成了切片集合si、s'i-1、s'i-2、...s'i-n,就可以找到该切片集合(或从这样的切片集合产生的复合体1108)与三维参考体积之间(诸如对应于如图11b所示的靶部位616的参考体积)的最佳配准。作为说明性示例,可以在冠状切片采集之后进行矢状切片采集。可以识别出使冠状切片处于与矢状切片相同的时间点的空间平移,以使冠状切片与矢状切片空间配准。然后,可以在3d体素坐标空间内构建两个切片。这可以通过将切片作为无穷小的薄片插入或者使用已知的切片厚度(诸如在图11a和图11b的复合体1118所示)将切片作为有限的切片插入来完成。
来自每个切片的未被靶部位的部分填充的体素可以保持未填充。然后可以在3d参考图像(例如,对应于靶部位616)与3d“切片填充图像”(对应于复合体1118)之间确定3d到3d配准。可以使用掩膜来滤掉未填充的体素。在另一示例中,可以诸如使用多个2d切片而不是单个复合体来执行3d到2d配准。例如,可以评估3d参考图像的移动参数(例如,诸如质心的一个或更多特征的位移或指定关注区域的平移或旋转的移动值集合),诸如使用如上所述的配准和优化技术将移动后的3d体积参考图像的体素与多个2d成像切片的各个切片进行比较的相似性度量的优化值。以这种方式,可以执行3d到2d配准,诸如以识别最佳的移动值集合。可以使用从移动值获取的信息来更新靶的位置。3d到3d配准技术、2d到2d配准技术、或3d到2d配准技术不需要进行图像分割(例如,靶部位自身不需要被分割),并且这种配准不需要识别诸如质心或边缘位置的成像特征。而是,诸如在通常如在本文其他地方所述的特定的关注区域上,可以使用灰度或对比度成像信息(或其他的提取值)执行配准。
图11c大体示出了用于更新治疗方案诸如以将治疗部位移动到新位置的的技术。可以构建较早的放射治疗靶区1110a,诸如与从体积参考图像提取的或根据其他治疗或剂量测定目标而构建的靶部位相对应。这样的治疗靶区1110a可以至少部分地使用定位放射治疗输出部、调制治疗射束(包括调制强度或射束形状中的一个或更多)、或者使用诸如可移动治疗椅或台的致动器来移动患者中的一个或更多种来构建。可以从治疗靶区提取诸如质心1108a的一个或更多特征。可以诸如使用本文所述的其它技术来确定所估计或所预测的靶部位(例如,待治疗的肿瘤或其他结构)的位移。
可以调节治疗靶区1110a来提供更新的治疗靶区1110b。例如,如果靶部位由于患者运动而平移,则可以将类似的位移应用于较早的质心1110a以提供更新的治疗靶区1110b质心1108b。类似地,如果提取了其他特征,则可以使用诸如旋转或缩放的其他技术来调节治疗靶区1110a。在另一个示例中,代替调整治疗靶区1110a或除了调整治疗靶区1110a之外,还可以使用其他技术来控制治疗,诸如对治疗进行门控以抑制放射治疗的递送直到更新的治疗靶区1110b落入指定区内。在又一示例中,诸如从传感器输出得到的替代信号可用于门控治疗。例如,传感器输出可以与在成像切片被空间配准之后从成像切片提取的特征的位置相关联,诸如与靶部位在成像切片内的质心位置相关联。可以以同步方式对治疗递送进行门控,诸如响应于传感器输出而被触发(例如,诸如在诸如呼吸的周期性运动期间的一定时间递送治疗)。
上述的技术可以以串行方式执行,诸如包括采集图像和处理这样的图像,然后采集另一序列的图像,并且处理后续采集的图像集合。在另一方案中,本文描述的技术的一个或更多部分可以以并行方式或以交错方式执行,诸如提供位移或其它信息的持续产生用于以适应性方式更新治疗方案。例如,图12示出了可以包括对应于先前采集的成像切片的成像信息与成像采集的交错处理的技术,诸如以增强本文所描述的其它技术的效率。如图12说明性示出的,成像采集系统可以采集成像切片,诸如对应于采集时刻ti、ti-1、ti-2、ti-3、...的切片si、si-1、si-2、si-3、...。在时刻t,可以采集切片si,并且在采集成像切片si期间,可以将诸如切片si-1和si-2的一个或更多先前采集的切片彼此空间配准或以其它方式处理。
作为说明性示例,成像切片被示出为彼此正交的二维平面。然而,如关于本文其他示例所述,切片不需要是平面的也不需要是正交的。可以处理每个采集的成像切片,包括与成像切片采集并行的对一个或更多切片的处理。例如,这样的处理可以包括来自体积参考图像的诸如对应于所采集的成像切片的平面或区域的采样信息。可以从体积参考图像中的一个或更多分割的结构提取靶部位(例如,可以用作用于自适应指向放射治疗的界标的肿瘤或其他解剖结构)的范围。
可以将扩边添加到靶部位的该范围上,诸如来限定区域,在该区域内,靶部位必须位于后续采集的成像切片中。可以基于诸如图像采集率的因子进行调节该扩边(采集率越低,肿瘤或其他靶在图像采集之间行进越远,并且扩边可以相应地扩大)。可以在采集的成像切片中分割肿瘤或其他靶。从一个或更多成像切片提取的分割的靶的信息可以与在计划图像中识别的靶部位空间配准。如本文其他实施例中所述,这种配准可用于确定更新的靶部位,或以其他方式控制或使治疗适应性调整。例如,作为说明性示例,更新的靶部位可以用于对治疗进行门控,诸如在更新的靶部位指示靶部位部分地或全部地在指定的空间门控窗口之外的同时暂停治疗,或者更新的靶部位可以用于使射束孔径形状适应于追踪肿瘤。
在执行这样的处理的同时,可以重新使用先前采集的成像切片,诸如以更高的速率进行门控或追踪更新,如图12中说明性示出的。可以使用诸如提取的特征位置(例如,质心位置)的关于更新的靶部位的信息来调节将来采集的成像切片的位置或取向,诸如以回到中点或以其他方式保持靶部位的期望部分处于成像场之内。
图13大体示出了可以包括在1302接收诸如参考图像的体积成像信息、在1304接收成像切片并且包括在1308确定靶部位的位置的差的诸如方法的技术1300。可以诸如使用如图1a、图1b、图1c、图1d、图2、图3、图4或图5所示的系统或其他元件来执行技术1300(或本文描述的其它技术)的部分或者整体。
在1302,可以接收诸如对应于计划或参考图像的体积成像信息。体积成像信息可以包括靶部位,诸如包括待利用放射治疗靶向的体素的区域。如本文其他地方所述,成像采集延迟可能妨碍以诸如份内(intra-fractionally)的实时方式获取靶部位的全体积成像。相应地,在1304,可以接收诸如包括一个或更多成像切片的成像信息。例如,可以诸如在采集了在1302接收到的体积图像之后的不同时间段不同的时刻来采集两个成像切片。如果两个成像切片在不同时刻采集,则靶部位的部分在各个成像切片中的位置可能是不同的(并且这样的成像切片可以被称为“在时间上未对准”)。
在1306,如果成像切片在时间上未对准,则来自至少两个成像切片中较早采集的一个成像切片的信息(诸如指示靶部位的信息)可以与至少两个成像切片中较晚采集的一个成像切片的至少一部分的空间配准。在1308,可以在由空间配准的信息指示的靶部位的位置与由在1302接收到的体积图像所指示的靶部位的较早位置之间确定差。例如,可以如上所述使用配准技术,诸如以在不需要分割或特征提取的情况下确定诸如靶部位的质心的特征的移动或靶的移动。所确定的移动值可以提供指示靶或其他关注区域的更新位置的信息。
可选地,在1310,可以使用关于在1308确定的靶的更新的位置的信息来更新治疗部位(例如,由放射治疗射束靶向的区域或体积)。另外地,或者替代地,可选地,在1312,可以对治疗射束操作进行门控,诸如当治疗与更新的或估计的靶位置适当地对准时允许治疗递送。以这种方式,可以使用成像切片和较早采集的体积参考图像来自适应地控制放射治疗。
各种注释和示例
本文献中描述的每个非限制性示例可以独立地存在,或者可以以各种排列或组合与一个或更多其他示例结合。
上述的具体说明包括对作为具体说明的一部分的附图的参照。附图通过说明的方式示出了可以实施本发明的具体实施例。这些实施例在本文中也称为“示例”。这样的示例可以包括除了所示出或所描述的那些之外的元件。然而,本发明人还考虑了仅提供所示出或所描述的那些元件的示例。此外,或者关于特定示例(或其一个或更多方案),或者关于其它示例(或其一个或更多方案),本发明人还考虑了使用所示出或所描述的那些元件的任何组合或组合的示例(或其一个或更多方案)。
在本文献与通过引用而并入的任何文献之间的用法不一致的情况下,以则本文献中的用法为准。
在本文献中,不定冠词“a”或“an”如在专利文档中通常方式使用,以包括一个或多于一个,而独立于“至少一个”或“一个或更多”的任何其他情形或使用。术语“或”用于指非排他性的“或”,从而除非另有说明,否则“a或b”包括“有a没有b”、“有b没有a”、以及“a和b”。在此文档中,术语“包括”和“其中(inwhich)”用作各个术语“包含”和“其中(wherein)”的通俗易懂的等效。此外,在以下权利要求中,术语“包括”是开放式的,也就是说,包括除了在权利要求中的这样的术语之后列出的那些元件之外的元件的系统、装置、物件,构成、公式或过程仍被认为落入该权利要求的范围之内。此外,在下面的权利要求中,术语“第一”,“第二”和“第三”等仅用作标记,并不意图对其对象施加数值要求。
本文描述的方法示例至少部分可以是机器或计算机实现的。一些示例可以包括编码有指令的计算机可读介质或机器可读介质,该指令可经操作以配置电子装置来执行如上述示例中所描述的方法。这种方法的实现可以包括诸如微代码、汇编语言代码、较高级语言代码等的代码。这种代码可以包括用于执行各种方法的计算机可读指令。这种代码可以形成计算机程序产品的一部分。此外,在一个示例中,例如在运行期间或在其它时间,代码可以有形地存储在一个或更多易失性、非暂时性或非易失性有形计算机可读介质上。这些有形的计算机可读介质的示例可以包括但不限于硬盘、可移动磁盘、可移动光盘(例如,压缩光盘和数字视频盘)、磁带、存储卡或存储棒、随机存取存储器(ram)、只读存储器(rom)等。
以上描述旨在是说明性的而不是限制性的。例如,上述示例(或其一个或更多方案)可以彼此结合来使用。诸如本领域普通技术人员在阅读上述描述时可以使用其它实施例。提供摘要以符合美国专利法实施细则(37c.f.r.)第1.72(b)节,以允许读者快速确定技术公开的实质。提交时应该理解是,它不会用于解释或限制权利要求的范围或含义。另外,在上述具体实施方式中,各种特征可以被分组在一起以简化本公开。这不应该被理解为一种使不要求保护的公开的特征对于任一权利要求都是必要的意图。相反,本发明的主题可以少于公开的特定实施例的全部特征。因而,以下权利要求书作为示例或实施例被并入具体实施方式中,其中每个权利要求独立地作为分离的实施例,并且认为这些实施例可以以各种组合或排列来彼此结合。本发明的范围应参照所附权利要求以及这些权利要求赋权的等同形式的全部范围来确定。
- 还没有人留言评论。精彩留言会获得点赞!