合成肽的制作方法
本申请要求于2014年11月21日提交的美国临时申请序列号62/082,902的优先权,该申请以全文引用的方式并入本文中。
领域
本文提供包含合成的脂酶刺激肽的组合物,以及用其治疗高甘油三酯血症以及其他病状和疾病的方法。具体地说,提供展现出apoa-v的脂酶刺激活性或使其增强的合成肽(av-肽)和拟肽物(av-拟肽物),以及其使用方法。
背景
在主要药物市场上超过35000万人受高甘油三酯血症(htg)(tg水平>150mg/dl;100mg/dl为正常)的影响,甘油三酯血症为包括心血管疾病、胰腺炎、糖尿病以及肝性脂肪变性的若干疾病的重要危险因素。所述群体中约1-2%具有基因遗传性原发性htg(>500mg/dltg),其可为与严重临床罹病率和死亡率结果相关的单基因或多基因病症。当前对htg的治疗具有许多脱靶效应并且不足够满足患者所建议的目标。
概述
本文提供包含合成的脂酶刺激肽的组合物,以及用其治疗高甘油三酯血症以及其他病状和疾病的方法。具体地说,提供展现出apoa-v的脂酶刺激活性或使其增强的合成肽(av-肽)和拟肽物(av-拟肽物),以及其使用方法。
本文提供包含肽或多肽的组合物,所述肽或多肽与seqidno:1(全长apoa-v)具有低于100%的序列同一性,涵盖与seqidno:8(av199-224)具有至少50%的序列同一性(例如>50%、>60%、>70%、>75%、>80%、>85%、>90%、>95%)的部分,并且展现出脂酶刺激活性。在一些实施方案中,肽或多肽包含与seqidno:8具有至少80%的序列相似性(例如>80%、>90%、>95%)的部分。在一些实施方案中,肽或多肽与seqidno:3(av199-237)具有低于100%的序列同一性但超过50%的序列同一性(例如>50%、>60%、>70%、>75%、>80%、>85%、>90%、>95%)。在一些实施方案中,肽或多肽与seqidno:3具有至少80%的序列相似性。在一些实施方案中,肽或多肽与seqidno:5(av199-232)具有低于100%的序列同一性但超过50%的序列同一性(例如>50%、>60%、>70%、>75%、>80%、>85%、>90%、>95%)。在一些实施方案中,肽或多肽与天然apoa-v序列(例如seqidno:1或其部分(例如seqidno:5))具有低于100%的序列同一性,但与seqidno:5(av199-232)、seqidno:12(av-h/k)、seqidno:23(av-h/k-2f)、seqidno:26(av-h/k-c6s)、seqidno:27(av-h/k-ac/nh2)以及/或者seqidno:28(av-h/k-2f/har)具有50%或更高的序列同一性(例如>50%、>60%、>70%、>75%、>80%、>85%、>90%、>95%)。
在一些实施方案中,组合物包含与seqidno:5(av199-232)具有低于100%的序列同一性但超过50%的序列同一性(例如<100%,但>50%、>60%、>70%、>75%、>80%、>85%、>90%、>95%)的肽。在一些实施方案中,肽与seqidno:5具有至少50%的序列相似性(例如>50%、>55%、>60%、>65%、>70%、>75%、>80%、>85%、>90%、>95%)。在一些实施方案中,肽与seqidno:10具有低于100%的序列同一性但超过50%的序列同一性(例如<100%,但>50%、>60%、>70%、>75%、>80%、>85%、>90%、>95%)。在一些实施方案中,肽与seqidno:10具有至少80%的序列相似性(例如>80%、>85%、>90%、>95%、100%)。在一些实施方案中,肽或多肽具有与seqidno:10具有100%序列同一性的部分。在一些实施方案中,肽为seqidno:10。在一些实施方案中,肽与seqidno:11具有低于100%的序列同一性但超过50%的序列同一性(例如<100%,但>50%、>60%、>70%、>75%、>80%、>85%、>90%、>95%)。在一些实施方案中,肽与seqidno:11具有至少80%的序列相似性(例如>80%、>85%、>90%、>95%、100%)。在一些实施方案中,肽或多肽具有与seqidno:11具有100%序列同一性的部分。在一些实施方案中,肽为seqidno:11。在一些实施方案中,肽与seqidno:12具有低于100%的序列同一性但超过50%的序列同一性(例如<100%,但>50%、>60%、>70%、>75%、>80%、>85%、>90%、>95%)。在一些实施方案中,肽与seqidno:12具有至少80%的序列相似性(例如>80%、>85%、>90%、>95%、100%)。在一些实施方案中,肽或多肽具有与seqidno:12具有100%序列同一性的部分。在一些实施方案中,肽为seqidno:12。
在一些实施方案中,合成av-肽的长度为10-50个氨基酸(例如10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50以及其中的任何范围(例如20-48、22-46、24-44、26-42、28-40、30-38、32-36))。在一些实施方案中,合成av-肽相对于野生型或天然apoa-v序列在肽的长度上包含至少1个突变(例如1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34或更多以及其中的任何范围)。在一些实施方案中,合成av-肽相对于野生型或天然apoa-v序列在肽的长度上包含至少1个非保守突变(例如1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34或更多以及其中的任何范围)。在一些实施方案中,av-肽相对于野生型或天然apoa-v序列在肽的长度上包含至少1个保守突变(例如1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34或更多以及其中的任何范围)。在一些实施方案中,av-肽相对于野生型或天然apoa-v序列在肽的长度上包含至少1个半保守突变(例如1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34或更多以及其中的任何范围)。在一些实施方案中,提供包含合成av-肽序列的肽或多肽。
在一些实施方案中,肽与apoa-v中长度至少为5个氨基酸(例如5、10、15、20、25、30、35、40、45、50以及其中的任何范围)的部分(例如seqidno:5)具有低于100%但高于50%(例如55%、60%、70%、80%、90%、95%以及其中的任何范围)的序列同一性。在一些实施方案中,肽与apoa-v中长度至少为10、12、14、16、18、20、22、24、26、28、30、32或34个氨基酸的部分(例seqidno:5)具有低于100%但高于50%(例如55%、60%、70%、80%、90%、95%以及其中的任何范围)的序列同一性。
在一些实施方案中,提供包含肽和/或多肽的组合物,例如在分别阐述于实施例1、图3a-c的描述、图4a-d的描述以及图8的描述中的一种或多种分析中,所述肽和/或多肽相对于seqidno:1(全长apoa-v)展现出增强的脂酶刺激活性。在一些实施方案中,肽和/或多肽相对于seqidno:1展现出增加>10%、增加>20%、增加>30%、增加>40%、增加>50%、增加>60%、增加>70%、增加>80%、增加>90%、>2倍、>3倍、>4倍、>5倍、>6倍、>8倍、>10倍或>20倍的脂酶刺激活性。在一些实施方案中,提供包含肽和/或多肽的组合物,所述肽和/或多肽相对于seqidno:5(av199-232)展现出增强的脂酶刺激活性。在一些实施方案中,例如在分别阐述于实施例1、图3a-c的描述、图4a-d的描述以及图的描述中的一种或多种分析中,肽和/或多肽相对于seqidno:5中的一者或两者展现出增加>10%、增加>20%、增加>30%、增加>40%、增加>50%、增加>60%、增加>70%、增加>80%、增加>90%、>2倍、>3倍、>4倍、>5倍、>6倍、>8倍、>10倍或>20倍的脂酶刺激活性。在一些实施方案中,肽展现出α-螺旋特性。在一些实施方案中,二级结构预测技术确定所述肽大体上或完全为α螺旋的。
在一些实施方案中,本文中的肽和/或多肽包含两亲性α-螺旋。在一些实施方案中,本文中的两亲性α-螺旋展现出av-199-232肽的结构域构造(参见例如图11)。在展开本文中的实施方案期间所进行的3d结构模型化、生物信息和生物化学以及生物物理学实验表明,av199-232肽和其活性变体(以及包含此类肽的多肽)包含四个结构域,所述四个结构是根据氨基酸类别和α螺旋上的周围位置(例如在α螺旋的螺旋轮表示中的空间位置)而非根据一级序列加以定义。av-199-232以及相关肽和多肽的结构域为:结构域1:a1、r5、r12、l16、k19、23a、30d以及34e;结构域2:r2、c6、k13、k17、a20、r24以及q31;结构域h:s4、t15、h22以及r33;以及结构域l:l3、v7、l10、s11、l14、a18、l21、i25、n28、l29以及l32。在展开本文中的实施方案期间进行的实验以及结构域内残基的身份与以下相符合:结构域1和h(以及结构域2)在刺激脂酶活性中起作用,结构域l在脂质结合或相互作用中起作用,并且结构域2在肝素结合中起作用;然而,本文中的实施方案不限于任何特定作用机制并且实践此类实施方案无需理解所述作用机制。在一些实施方案中,本文提供包含合成肽或多肽的组合物,所述合成肽或多肽包含具有一定氨基酸序列的大体上α螺旋区域,所述氨基酸序列中至少24个氨基酸(例如24、25、26、27、28、29、30、31、32以及其间的任何范围)并且不超过33个氨基酸与seqidno:5同一或为在其情况下的保守或半保守取代。在一些实施方案中,肽或多肽能够结合于脂蛋白脂酶(lpl)和/或刺激lpl的脂酶活性。在一些实施方案中,至少24个氨基酸(例如24、25、26、27、28、29、30、31、32以及其间的任何范围)与seqidno:5同一或为在其情况下的保守取代。在一些实施方案中,至少24个氨基酸(例如24、25、26、27、28、29、30、31、32以及其间的任何范围)与seqidno:5同一。在一些实施方案中,肽或多肽能够在体外结合于和/或刺激lpl。在一些实施方案中,肽或多肽能够在体内结合于和/或刺激lpl。在一些实施方案中,肽或多肽能够结合肝素。
在一些实施方案中,肽或多肽中对应于seqidno:5中的位置的氨基酸:(i)与seqidno:5中的对应位置同一,(ii)为相对于seqidno:5中对应位置的保守取代,(iii)为相对于seqidno:5中的对应位置的半保守取代,以及/或者(iv)为相对于seqidno:5中的对应位置的非保守取代。在一些实施方案中,肽或多肽中对应于seqidno:5中的位置的氨基酸:(i)与seqidno:5中的对应位置同一,(ii)为相对于seqidno:5中的对应位置的保守取代,以及/或者(iii)为相对于seqidno:5中的对应位置的半保守取代。在一些实施方案中,肽或多肽中对应于seqidno:5中的位置的氨基酸:(i)与seqidno:5中的对应位置同一,以及/或者(ii)为相对于seqidno:5中的对应位置的保守取代。在一些实施方案中,肽或多肽中对应于seqidno:5中的位置的氨基酸:(i)与seqidno:5中的对应位置同一。在一些实施方案中,肽或多肽中对应于seqidno:5中的位置的不与seqidno:5中的对应位置同一并且除非另外说明否则不为特定氨基酸或选自一组氨基酸的任何氨基酸为相对于seqidno:5中的对应位置的保守取代或半保守取代。在一些实施方案中,肽或多肽中对应于seqidno:5中的位置的不与seqidno:5中的对应位置同一并且除非另外说明否则不为特定氨基酸或选自一组氨基酸的任何氨基酸为相对于seqidno:5中的对应位置的保守取代。
在一些实施方案中,本文提供包含本文所描述的合成肽或多肽的组合物,所述合成肽或多肽包含具有成组残基的结构域(结构域2)并且包含对应于seqidno:5的位置2、6、13、17、20、24以及31的残基。在一些实施方案中,结构域2能够结合于肝素。在一些实施方案中,肽或多肽中对应于seqidno:5的位置6的残基不为半胱氨酸残基。在一些实施方案中,对应于seqidno:5的位置6的残基为结构域2中仅有的不与seqidno:5中的对应位置同一的残基。在一些实施方案中,肽或多肽中对应于seqidno:5的位置6的残基选自由以下组成的群组:s、t、n以及q。在一些实施方案中,肽或多肽中对应于seqidno:5的位置6的残基为s。在一些实施方案中,肽或多肽中对应于seqidno:5的位置6的残基为t。在一些实施方案中,肽或多肽中对应于seqidno:5的位置6的残基选自由y和h组成的群组。在一些实施方案中,肽或多肽中对应于seqidno:5的位置13和17的一个或两个残基选自由以下组成的群组:高赖氨酸(hlys)、r、高精氨酸(harg)以及鸟氨酸。在一些实施方案中,肽或多肽中对应于seqidno:5的位置17的残基选自由以下组成的群组:q、n以及s。
在一些实施方案中,本文提供包含本文所描述的合成肽或多肽的组合物,所述合成肽或多肽包含具有成组残基的结构域(结构域h),所述结构域包含对应于seqidno:5的位置4、15、22以及33的残基。在一些实施方案中,肽或多肽中对应于seqidno:5的位置22的残基不为组氨酸残基。在一些实施方案中,肽或多肽中对应于seqidno:5的位置22的残基选自由以下组成的群组:k、hlys、r、harg以及鸟氨酸。在一些实施方案中,对应于seqidno:5的位置22的残基为k。在一些实施方案中,对应于seqidno:5的位置22的残基为hlys。在一些实施方案中,肽或多肽中对应于seqidno:5的位置4的残基为s。在一些实施方案中,肽或多肽中对应于seqidno:5的位置4的残基选自由以下组成的群组:t、n以及g。在一些实施方案中,肽或多肽中对应于seqidno:5的位置15和33的残基分别为t和r。
在一些实施方案中,本文提供包含本文所描述的合成肽或多肽的组合物,所述合成肽或多肽包含具有成组残基的疏水性结构域(结构域l),所述结构域包含对应于seqidno:5的位置3、7、10、11、14、18、21、25、28、29以及32的残基。在一些实施方案中,疏水性结构域的一个或多个残基不与seqidno:5的对应位置同一。在一些实施方案中,将疏水性结构域中对应于seqidno:5的非极性脂族残基的一个或多个残基用选自由以下组成的群组的非极性芳族残基取代:f、y以及w。在一些实施方案中,肽或多肽中对应于seqidno:5的位置10的残基为非极性芳族残基。在一些实施方案中,肽或多肽中对应于seqidno:5的位置10的残基为f。在一些实施方案中,肽或多肽中对应于seqidno:5的位置29的残基为非极性芳族残基。在一些实施方案中,肽或多肽中对应于seqidno:5的位置29的残基为f。在一些实施方案中,肽或多肽在疏水性结构域中对应于seqidno:5中的位置包含不与在seqidno:5中的对应位置的残基同一的一个或多个残基。在一些实施方案中,疏水性结构域中的非同一位置中的至少一者为y。在一些实施方案中,疏水性结构域中的非同一位置中的至少两者为y。在一些实施方案中,疏水性结构域中的非同一位置中的至少两者选自由以下组成的群组:f、y以及w。在一些实施方案中,疏水性结构域中的非同一位置中的至少一者为f。在一些实施方案中,疏水性结构域中的非同一位置中的至少两者为f。在一些实施方案中,疏水性结构域中的非同一位置中的两者为l10f和l29f。在一些实施方案中,疏水性结构域中的非同一位置中的至少一者为w。在一些实施方案中,疏水性结构域中的非同一位置中的至少两者为w。在一些实施方案中,将疏水性结构域中的非同一氨基酸中的至少三者为将非极性脂族氯基酸用选自由以下组成的群组的非极性芳族氨基酸取代:f、y以及w。在一些实施方案中,疏水性结构域中的非同一氨基酸中的至少一者为将非极性脂族氨基酸用不同的非极性脂族氨基酸取代。
在一些实施方案中,本文提供包含本文所描述的合成肽或多肽的组合物,所述合成肽或多肽包含具有成组残基的结构域(结构域1),所述结构域包含对应于seqidno:5的位置1、5、12、16、19、23、30以及34的残基。在一些实施方案中,将结构域1内的对应于seqidno:5的赖氨酸残基的一个或多个残基用选自由以下组成的群组的残基取代:r、harg以及hlys。在一些实施方案中,将结构域1内的对应于seqidno:5的精氨酸残基的一个或多个残基用选自由以下组成的群组的残基取代:k、hakg以及hlys。在一些实施方案中,结构域1中的所有残基与seqidno:5中的对应残基同一,将除了seqidno:5的一个或多个精氨酸或赖氨酸残基用选自由以下组成的群组的残基取代:r、k、harg以及hlys。在一些实施方案中,非同一氨基酸中的至少一者为精氨酸以harg或hlys取代。
在一些实施方案中,本文提供包含一定序列的肽和多肽,所述序列相对于以下序列具有10个或更少(例如10、9、8、7、6、5、4、3、2、1、0或其间的范围)个取代(例如保守取代、半保守取代、非保守取代):ar(l/f/y/w)(s/t/n/g)(r/k/hlys/harg)(c/s/t/n/q/y/h)(v/f/y/w)qv(l/f/y/w)s(r/k/hlys/harg)(k/r/harg/hlys/orn)(l/f/y/w)tl(k/r/harg/hlys/orn)(a/f/y/w)(r/k/hlys/harg)a(l/f/y/w)(h/k/hlys/r/harg/orn)ar(i/f/y/w)qqn(l/f/y/w)dq(l/f/y/w)re(seqidno:29),但与seqidno:5具有低于100%的序列同一性。在一些实施方案中,本文提供包含一定序列的肽和多肽,所述序列相对于以下序列具有10个或更少(例如10、9、8、7、6、5、4、3、2、1、0或其间的范围)个取代(例如保守取代、半保守取代、非保守取代):arx3x4x5x6x7qvx10sx12x13x14tlx17x18x19ax21x22arx25qqnx29dqx32re,其中:x3为l、f、y或w;x4为s、t、n或g;x5为r、k、hlys或harg;x6为c、s、t、n、q、y或h;x7为v、f、y或w;x10为l、f、y或w;x12为r、k、hlys或harg;x13为k、r、harg、hlys或orn;x14为l、f、y或w;x17为k、r、harg、hlys或orn;x18为a、f、y或w;x19为r、k、hlys或harg;x21为l、f、y或w;x22为h、k、hlys、r、harg或orn;x25为i、f、y或w;x29为l、f、y或w;并且x32为l、f、y或w(seqidno:29),但与seqidno:5具有低于100%的序列同一性。在一些实施方案中,本文提供包含一定序列的肽和多肽,所述序列与seqidno:29具有100%序列同一性,但与seqidno:5具有低于100%的序列同一性。
在一些实施方案中,本文提供包含本文所描述的合成肽或多肽的组合物,所述合成肽或多肽包含选自由以下组成的群组的n端修饰:脱氨基、n-低碳烷基、n-二低碳烷基、受约束烷基以及n-酰基修饰。在一些实施方案中,肽或多肽的c端包含选自由以下组成的群组的修饰:酰胺、低碳烷基酰胺、受约束烷基、二烷基酰胺以及低碳烷基酯修饰。
在一些实施方案中,本文提供药物制剂,其包含:(a)本文(例如在前述段落中)所描述的av-肽或多肽;以及(b)生理学上可接受的缓冲液或载体。在一些实施方案中,药物制剂进一步包含额外的治疗剂(例如用于治疗htg、关节硬化、胆固醇升高、心脏病等)。
在一些实施方案中,本文提供融合肽或多肽,其包含:(a)本文(例如在前述段落中)所描述的av-肽或多肽,以及(b)官能性肽或多肽片段。在一些实施方案中,官能性肽或多肽片段包含信号传导部分、治疗性部分、定位部分(例如细胞引入信号、核定位信号等)、可检测部分(例如荧光部分、对比剂)或分离/纯化部分(例如链霉亲和素、his6等)。
在一些实施方案中,本文提供编码本文(例如在前述段落中)所描述的av-肽或多肽的聚核苷酸。在一些实施方案中,本文提供核酸载体(例如质粒、杆粒、病毒载体(例如aav)),所述核酸载体包含编码本文(例如在前述段落中)所描述的av-肽或多肽的聚核苷酸。在一些实施方案中,载体进一步包含启动子和/或一个或多个表达元件(例如转录增强子、翻译起始位点、内部核糖体进入位点等)。在一些实施方案中,提供以下方法,其包括向受试者或样品施用本文所描述的聚核苷酸或载体(例如用于治疗高甘油三酯血症、用于降低甘油三酯的浓度等)。
在一些实施方案中,本文提供治疗高甘油三酯血症或相关病状或疾病(例如动脉粥样硬化、心脏病、急性胰腺炎等)的方法,所述方法包括向罹患高甘油三酯血症或所述相关病状或疾病的受试者施用本文(例如在前述段落中)所描述的av-肽或多肽。
在一些实施方案中,本文提供预防高甘油三酯血症或相关病状或疾病(例如动脉粥样硬化、心脏病、急性胰腺炎等)的方法,所述方法包括向(例如家族史、遗传易感性、升高的甘油三酯、生活方式、年龄、性别等)处于高甘油三酯血症或所述相关病状或疾病风险中的受试者施用本文(例如在前述段落中)所描述的av-肽或多肽。
在一些实施方案中,本文提供治疗或预防受试者的动脉粥样硬化和/或心血管疾病的方法,所述方法包括向受试者施用本文(例如在前述段落中)所描述的av-肽或多肽。在一些实施方案中,施用包括共施用:(a)所述肽或多肽,以及(b)用于治疗和/或预防动脉粥样硬化和/或心血管疾病的治疗和/或治疗剂。在一些实施方案中,同时和/或以单一药物制剂的形式施用(a)和(b)。在一些实施方案中,并行和/或以分开的药物制剂的形式施用(a)和(b)。
在一些实施方案中,本文提供降低样品中的甘油三酯浓度的方法,所述方法包括:(a)向包含(i)甘油三酯和(ii)甘油三酯水解脂酶的样品施用本文(例如在前述段落中)所描述的av-肽或多肽;或(b)向包含甘油三酯的样品施用:(i)本文(例如在前述段落中)所描述的av-肽或多肽,以及(ii)甘油三酯水解脂酶。在一些实施方案中,甘油三酯水解脂酶选自由以下组成的群组:脂蛋白脂酶(lpl)、内皮脂酶(el)以及肝脂酶(hl)。
在一些实施方案中,本文提供本文所描述的av-肽或多肽的用途,其用于治疗高甘油三酯血症或相关病状或疾病(例如动脉粥样硬化、心脏病、急性胰腺炎等)。在一些实施方案中,本文提供用于用作药剂的本文所描述的av-肽或多肽。在一些实施方案中,本文提供用于治疗高甘油三酯血症或相关病状或疾病(例如动脉粥样硬化、心脏病、急性胰腺炎等)的av-肽或多肽。在一些实施方案中,本文提供本文所描述的av-肽或多肽的用途,其用于制造用于治疗高甘油三酯血症或相关病状或疾病(例如动脉粥样硬化、心脏病、急性胰腺炎等)的药剂。
图式简单说明
图1a-d.(a)人类apoa-v蛋白质序列(成熟蛋白;uniprot/q6q788;seqidno:1),突出显示缺失以及在各种群体中已确定并且与高甘油三酯血症(htg)相关的若干突变;(b)残基199-259内的apoa-v功能丧失型突变/缺失簇,其表明此区域可具有潜在lpl刺激结构域。绘制apoa-v的在残基199-259内成簇的与高甘油三酯血症和/或cad有关的所有已知序列变体,突变竖线和星号表示先前被报导为降低apoa-v的lpl刺激活性的突变;(c)apoa-v的3d模型(phyre2)预示结构富含α-螺旋;并且(d)测试肽av199-237含有推定亮氨酸拉链基序(seqidno:20)。
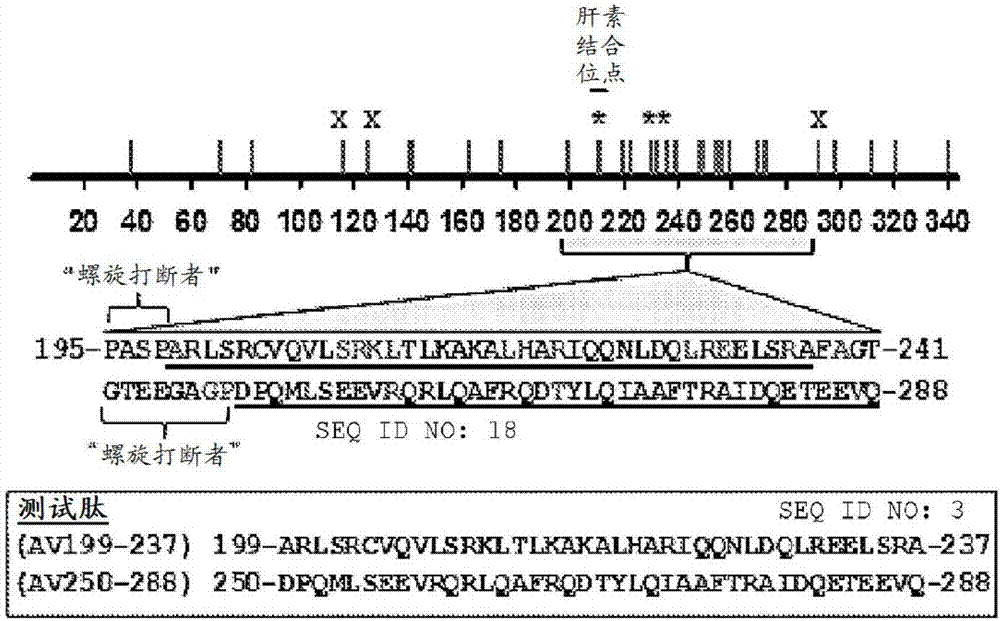
图2a-b.通过phyre2预测的apoa-v3d结构,突出显示(ser232_leu235)del和leu253prosnps的位置(a)。由富含作为已知蛋白质结构破坏者(α-螺旋打断者)的p和a的序列围住的所示蛋白质序列(seqidno:2)(b)。通过视觉检验来选择合成肽av199-237(seqidno:3)的范本。基于成熟蛋白(信号肽得以移除)来进行肽编号。
图3a-c.使用荧光tg类似物enzchek(invitrogen)进行的脂蛋白脂酶(lpl)活性分析。酶反应混合物由增加浓度的含于100μltris缓冲生理盐水(tbs)中的lpl、1%bsa(ph7.8)、0.015%zwittergent3-14以及1μmenzchek底物组成。通过荧光(λex=482nm,λem=515nm)监测反应,并且针对时间绘制相对荧光单位(rfu)(a)。使用bodipy标记的脂肪酸(bodipy-fa)来确定在脂酶情况下产生的产物浓度(b)。购自invitrogeninc.的enzchek底物(e33955)的结构(c)。
图4.在肝细胞(hepg2)和单核细胞(raw267.4)细胞系中的脂酶活性分析。在hepg2培养物中,反应依赖于tg-底物的细胞表面接触。从细胞中移除反应介质使产物的进一步产生停止,并且使其返回细胞中使反应再起始(a)。用已知从细胞表面移除脂酶的肝素预洗涤hepg2细胞也降低tg-底物的水解速率(b)。细胞(c)与纯lpl(d)均对不同脂蛋白(vldl、ldl以及hdl)的脱辅基蛋白含量敏感。
图5.av199-237肽刺激lpl活性,但仅在富tg脂蛋白存在下如此。添加至lpl中的肽(10μm)不增加酶活性(图片a),除非首先将肽与vldl或ldl一起孵育(b)。添加vldl或ldl归因于apoc-iii含量而引起lpl活性降低。将av199-237lpl刺激活性与lpl的另一活化剂apoc-ii肽(c-ii50-79)相比较(c)。虽然av199-237肽在vldl存在下刺激lpl活性,但av250-288并不如此(d、e)。
图6.av199-237肽有效刺激培养物中活肝细胞中的肝脂酶(hl)的活性(a)。向细胞中添加av199-237(10μm)使hl活性增加约2.8倍,并且在监测反应的整个75min时间段中得以持续(b)。
图7.针对脂酶刺激活性对av残基199-288进行筛选以确定为刺激lpl活性所必需的最小肽序列。相对活性以++、+以及-指示。
图8.确定具有完全脂酶刺激活性(b、d)的最小肽序列(a)。将av199-237缩短5个残基成为av199-232产生活性增强,同时减小长度另外对活性具有副作用。通过添加10μm肽至体外lpl分析物(b)或肝细胞(hepg2)细胞培养物(d)中来进行分析。在24孔组织培养板中,将细胞在37℃下在200μltbs、1.5%bsa、0.2%zwittergent3-14、1μmenzchek底物中孵育1h。av199-232还在已知表达lpl的活thp-1巨噬细胞的培养物中具活性(c)。
图9.av199-232通过改善lpl对底物的亲和力来刺激lpl活性。以不同底物浓度(0-25μm)进行脂酶反应(a、c、d),以确定在+/-vldl(10μg/ml)和+/-av199-232(2.5μm)情况下的lpl酶活性的动力学参数。(b)添加vldl将酶对底物的亲和力降低5.3倍,这与由apoc-iii产生的抑制一致。av199-232在v最大和km方面仅显示边际变化。av199-232+vldl使lpl的明显底物亲和力增加7.8倍。使用graphpadprism软件米氏酶动力学方程(michaelis-mentenenzymekineticequation)曲线拟合来确定动力学参数。
图10.av199-232为结合肝素的α-螺旋肽。通过圆二色性光谱学以实验方式分析肽折叠和构象(a)并且经过计算为约42%α-螺旋,其在结合肝素后增加至约76%。使用phyre2经由计算机模拟的3d模型化也指示肽可积极地折叠成α-螺旋(b)。
图11.av199-232的结构表示:(a)3d结构模型,经过预测为>88%α-螺旋状(predictprotein.org),其与圆二色性分析一致;(b)使用heliquest2从由软件产生的螺旋轮表示揭示四个不同的结构域(1、2、h以及l);以及(c)av199-232的一级序列,突出显示在各个单个的结构域中的一些所关注的关键残基。
图12.为研究结构域的重要性,合成具有所选残基取代的肽以单个地“敲出”结构域。
图13.在结构域1和结构域2中具有敲出取代的av199-232肽的脂酶刺激(a)和肝素结合(b)潜能。脂酶活性似乎高度依赖于结构域1与结构域2,同时肝素结合需要结构域2。
图14.将结构域-h中的h残基用k(av-h/k)取代大体上改善av199-232的脂酶刺激潜能。在不存在vldl的情况下,av-h/k刺激lpl活性达1.6倍(a/c)。当在添加至lpl之前与vldl一起孵育时,av-h/k刺激lpl活性达8倍,相对于av199-232增加44%(b/d)。所有肽均在10μm浓度下进行比较。
图15.av199-232结合vldl(a)并且肽-脂蛋白复合物刺激lpl活性(b)。
图16.调整脂质-结合面改善脂酶刺激性能。
图17.对进行脂酶刺激活性测试的示例性av-肽的概述。序列被显示对脂酶活性具有相对影响。
图18.用于评估av-199-232(seqidno:5)残基对脂酶刺激活性的相对影响的丙氨酸扫描。
图19.通过使用phyre2的基于同源性的模型化继之以在galaxyweb进行的分子改进来产生lpl和av-199-232的3d结构。
图20.使用cluspro2.0进行的apoc-iii与lpl的分子对接(b)。
图21.使用cluspro2.0进行的av199-232与lpl的分子对接。
图22.对稳定lpl:av199-232相互作用的接触残基的分子模型化预测。
图23.(a-c)白细胞-lpl活性为可检测的并且对av199-232肽刺激有反应。(d)在正常和脂代谢异常血浆存在下,av199-232刺激lpl活性。
定义
如本文所用,除非另外明确陈述,否则将以下术语定义为具有以下含义。
术语“氨基酸”是指天然氨基酸、非天然氨基酸以及氨基酸类似物,除非另外指出,否则所有均呈其d和l立体异构体形式(如果其结构允许此类立体异构形式)。
天然氨基酸包括丙氨酸(ala或a)、精氨酸(arg或r)、天冬酰胺(asn或n)、天冬氨酸(asp或d)、半胱氨酸(cys或c)、谷酰胺(gln或q)、谷氨酸(glu或e)、甘氨酸(gly或g)、组氨酸(his或h)、异亮氨酸(ile或i)、亮氨酸(leu或l)、赖氨酸(lys或k)、甲硫氨酸(met或m)、苯基丙氨酸(phe或f)、脯氨酸(pro或p)、丝氨酸(ser或s)、苏氨酸(thr或t)、色氨酸(trp或w)、酪氨酸(tyr或y)以及缬氨酸(val或v)。
非天然氨基酸包括但不限于吖丁啶羧酸、2-氨基己二酸、3-氨基己二酸、β-丙氨酸、萘基丙氨酸(“naph”)、氨基丙酸、2-氨基丁酸、4-氨基丁酸、6-氨基己酸、2-氨基庚酸、2-氨基异丁酸、3-氨基异丁酸、2-氨基庚二酸,叔丁基甘氨酸(“tbug”)、2,4-二氨基异丁酸、锁链素(desmosine)、2,2'-二氨基庚二酸、2,3-二氨基丙酸、n-乙基甘氨酸、n-乙基天冬酰胺、高脯氨酸(“hpro”或“homop”)、羟基赖氨酸、别羟基赖氨酸、3-羟基脯氨酸(”3hyp”)、4-羟基脯氨酸(“4hyp”)、异锁链素、别异亮氨酸、n-甲基丙氨酸(“meala”或“nime”)、n-烷基甘氨酸(“nag”)(包括n-甲基甘氨酸、n-甲基异亮氨酸)、n-烷基戊基甘氨酸(“napg”)(包括n-甲基戊基甘氨酸)、n-甲基缬氨酸、萘基丙氨酸、正缬氨酸(“norval”)、正亮氨酸(“norleu”)、辛基甘氨酸(“octg”)、鸟氨酸(“orn”)、戊基甘氨酸(“pg”或“pgly”)、哌啶酸、硫代脯氨酸(“thiop”或“tpro”)、高赖氨酸(“hlys”)以及高精氨酸(“harg”)。
术语“氨基酸类似物”是指其中c端羧基、n端氨基以及侧链官能团中的一者或多者已被可逆或不可逆化学阻断或以其他方式加以修饰成为另一官能团的天然或非天然氨基酸。举例来说,天冬氨酸-(β-甲酯)为天冬氨酸的氨基酸类似物;n-乙基甘氨酸为甘氨酸的氨基酸类似物;或丙氨酸甲酰胺为丙氨酸的氨基酸类似物。其他氨基酸类似物包括甲硫氨酸亚砜、甲硫氨酸砜、s-(羧甲基)-半胱氨酸、s-(羧甲基)-半胱氨酸亚砜以及s-(羧甲基)-半胱氨酸砜。
如本文所用,术语“肽”涉及通过肽键键联在一起的氨基酸的短聚合物。与其他氨基酸聚合物(例如蛋白质、多肽等)相比之下,肽的长度为约50个氨基酸或更短。肽可包含天然氨基酸、非天然氨基酸、氨基酸类似物以及/或者修饰过的氨基酸。肽可为天然存在的蛋白质的子序列或非天然(合成)序列。
如本文所用,术语“突变肽”是指肽的变体,所述肽的变体具有不同于自然界中存在的称为“野生型”序列的大多数常见变体的氨基酸序列。突变肽可为突变蛋白质或多肽的子序列(例如天然存在的蛋白质的不为自然界中的最常见序列的子序列),或可为不为天然存在的蛋白质或多肽的子序列的肽。举例来说,“突变apoa-v肽”可为apoa-v的突变型式的子序列或可为在天然存在的apoa-v蛋白中未发现的不同序列。
如本文所用,术语“合成肽”是指具有与在天然肽和/或蛋白质中所发现的氨基酸序列不同的氨基酸序列的肽。合成蛋白不为天然存在的蛋白质的子序列,既非野生型(即最丰富者)也非其突变型式。举例来说,“合成apo-v肽”(“sav肽”)不为天然存在的apoa-v的子序列。可通过任何适合的方法(例如重组表达、化学合成、酶促合成等)来制备或合成如本文所用的“合成肽”。
术语“肽拟似物”或“拟肽物”是指仿效衍生自蛋白质或肽的序列的肽样分子。肽拟似物或拟肽物可含有氨基酸和/或非氨基酸组分。拟肽物的实例包括化学修饰肽、类肽(侧链附加至肽主链的氮原子,而非α-碳)、β-肽(氨基键合至β碳,而非α碳)等。
如本文所用,“保守”氨基酸取代是指将肽或多肽中的氨基酸用具有类似化学性质(诸如尺寸或电荷)的另一氨基酸取代。出于本公开的目的,以下八种基团各自含有彼此保守取代的氨基酸:
1)丙氨酸(a)与甘氨酸(g);
2)天冬氨酸(d)与谷氨酸(e);
3)天冬酰胺(n)与谷酰胺(q);
4)精氨酸(r)与赖氨酸(k);
5)异亮氨酸(i)、亮氨酸(l)、甲硫氨酸(m)以及缬氨酸(v);
6)苯基丙氨酸(f)、酪氨酸(y)以及色氨酸(w);
7)丝氨酸(s)与苏氨酸(t);以及
8)半胱氨酸(c)与甲硫氨酸(m)。
天然存在的残基可基于共同侧链性质划分成多个类别,例如:正极性(组氨酸(h)、赖氨酸(k)以及精氨酸(r));负极性(天冬氨酸(d)、谷氨酸(e));中性极性(丝氨酸(s)、苏氨酸(t)、天冬酰胺(n)、谷酰胺(q));非极性脂族(丙氨酸(a)、缬氨酸(v)、亮氨酸(l)、异亮氨酸(i)、甲硫氨酸(m));非极性芳族(苯基丙氨酸(f)、酪氨酸(y)、色氨酸(w));脯氨酸和甘氨酸;以及半胱氨酸。如本文所用,“半保守”氨基酸取代是指将肽或多肽中的氨基酸用同一类别内的另一氨基酸取代。
在一些实施方案中,除非另作说明,否则保守或半保守氨基酸取代还可涵盖具有与天然残基类似的化学性质的非天然存在的氨基酸残基。典型地通过化学肽合成而非通过在生物系统中合成来合并这些非天然残基。这些包括但不限于拟肽物和其他反向或颠倒形式的氨基酸部分。在一些实施方案中,本文中的实施方案可限于天然氨基酸、非天然氨基酸以及/或者氨基酸类似物。
非保守取代可涉及一个类别的成员换成另一类别的成员。
如本文所用,术语“序列同一性”是指两个聚合物序列(例如肽、多肽、核酸等)具有单体相同的连续亚单位组合物所达到的程度。术语“序列相似性”是指两个聚合物序列(例如肽、多肽、核酸等)仅因保守和/或半保守氨基酸取代而不同的程度。如下计算“序列同一性百分比”(或“序列相似性百分比”):(1)在比较视窗(例如较长序列的长度、较短序列的长度、指定视窗等)上比较两个最佳比对序列,(2)确定含有同一(或相似)的单体(例如在两个序列中出现相同氨基酸、在两个序列出现相似氨基酸)的位置的数目以产生匹配位置的数目,(3)将匹配位置的数目除以比较视窗(例如较长序列的长度、较短序列的长度、指定视窗)中的位置的总数目,并且(4)将结果乘以100以产生序列同一性百分比或序列相似性百分比。举例来说,如果肽a与b的长度均为20个氨基酸并且在除1处以外的所有位置具有同一的氨基酸,那么肽a与肽b具有95%序列同一性。如果在非同一位置的氨基酸共有相同生物物理特性(例如两者均为酸性),那么肽a与肽b将具有100%序列相似性。作为另一实例,如果肽c的长度为20个氨基酸并且肽d的长度为15个氨基酸,并且肽d中的15个氨基酸中有14个与肽c的一部分的那些氨基酸同一,那么肽c与d具有70%序列同一性,但肽d与最佳比较窗口的肽c具有93.3%序列同一性。出于本文中计算“序列同一性百分比”(或“序列相似性百分比”)的目的,将比对序列中的任何空位视为在所述位置处失配。
如本文所用,术语“成组残基”是指肽、多肽或蛋白质内在三维空间中物理地安置在一起的一组氨基酸。成组残基在肽、多肽或蛋白质的一级序列中可能为或可能不为连续的。残基可在球形结构域中成组,可存在于相同表面上,或可存在于肽、多肽或蛋白质内的二级结构(例如α螺旋)或三级结构的相同末端或侧。在一些实施方案中,除物理地安置在一起之外,成组残基还在残基特性(例如尺寸、极性电荷等)方面展现出一定程度的相似性。
如本文所用,术语“受试者”泛指任何动物,包括但不限于人类和非人类动物(例如犬、猫、牛、马、羊、家禽、鱼、甲壳动物等)。如本文所用,术语“患者”典型地指正进行疾病或病状治疗的受试者。
如本文所用,术语“有效量”是指组合物(例如合成肽)足以实现有益或所需结果的量。可以一次或多次施用、施加或剂量施用有效量并且不旨在限于特定配制品或施用途径。
如本文所用,术语“施用(administration/administering)”是指向受试者或体内、体外或离体细胞、组织以及器官给予药物、前药或其他药剂或治疗性治疗(例如合成肽)的动作。示例性人体施用途径可为通过在脑或脊髓的蛛网膜下的间隙(鞘内)、眼睛(眼部)、口腔(经口)、皮肤(局部或经皮)、鼻(鼻内)、肺(吸入)、口腔粘膜(颊内)、耳、直肠、阴道;通过注射(例如静脉内、皮下、瘤内、腹膜内等)等。
如本文所用,术语“共施用(co-administration/co-administering)”是指向受试者施用至少两种药剂(例如多种合成肽或合成肽与另一治疗剂)或治疗。在一些实施方案中,两种或更多种药剂或治疗的共施用为并行的。在其他实施方案中,第一药剂/治疗是在第二药剂/治疗之前施用。本领域技术人员了解,所用的各种药剂或治疗的配制品和/或施用途径可变化。用于共施用的适当剂量可由本领域技术人员容易地确定。在一些实施方案中,当共施用药剂或治疗时,以低于适合其单独施用的剂量施用相应药剂或治疗。因此,在共施用药剂或治疗使潜在有害(例如毒性)药剂的必需剂量降低的实施方案中,以及/或者当共施用两种或更多种药剂使得受试者对所述药剂中的一者经由共施用另一药剂而得到的有益作用敏感时,尤其需要共施用。
如本文所用,术语“治疗”意谓获得有益或预期临床结果的方法。有益或预期临床结果可包括症状减轻、疾病严重程度降低、抑制疾病或病状的潜在病因、使处于非晚期状态的疾病稳定、延迟疾病进展以及/或者改善或减轻疾病病状。
如本文所用,术语“药物组合物”是指活性剂(例如合成av肽)与惰性或活性载体的组合,所述组合使得组合物尤其适合用于体外、体内或离体诊断或治疗用途。
如本文所用的术语“药学上可接受”或“药理学上可接受”是指组合物当向受试者施用时不大体上产生有害反应,例如毒性、过敏或免疫反应。
如本文所用,术语“药学上可接受的载体”是指标准药物载体中的任一者,包括但不限于磷酸盐缓冲盐水溶液、水、乳液(例如诸如油/水或水/油乳液)以及各种类型的润湿剂、任何和所有溶剂、分散介质、包衣、月桂基硫酸钠、等渗和吸收延迟剂、崩解剂(例如马铃薯淀粉或淀粉羟乙酸钠)等。组合物还可包括稳定剂和防腐剂。关于载体、稳定剂以及助剂的实例,参见例如martin,remington'spharmaceuticalsciences,第15版,mackpubl.co.,easton,pa.(1975),该文献以全文引用的方式并入本文中。
如本文所用,术语“受约束烷基”是指分枝链、环状、稠合烷基以及金刚烷基。
如本文所用,术语“低碳烷基”是指c1至c4烷基(例如甲基、乙基、丙基以及丁基)。
本文中的许多实施方案是使用开放性“包含”措辞加以描述。此类实施方案涵盖多个封闭性的“由……组成”和/或“基本上由……组成”实施方案,这些实施方案可替代地使用此类措辞来进行要求或描述。
详细说明
本文提供包含合成的脂酶刺激肽的组合物,以及用其治疗高甘油三酯血症以及其他病状和疾病的方法。具体地说,提供展现出apoa-v的脂酶刺激活性或使其增强的合成肽(av-肽)和拟肽物(av-拟肽物),以及其使用方法。
本文提供合成肽(apoa-v肽或同义词av-肽),在本文所描述的分析中的一者或多者中,所述合成肽刺激包括以下各项的脂酶子集的甘油三酯(tg)水解活性:脂蛋白脂酶(lpl)、内皮脂酶(el)以及肝脂酶(hl)(例如相对于seqidno:1、seqidno:3、seqidno:5等达到至少2倍(例如>2倍、>3倍、>4倍、>5倍、>6倍、>7倍、>8倍、>9倍、>10倍或更多倍,或其中的范围))。这些脂酶为细胞表面酶,其例如降低血浆中的循环tg的浓度。这些脂酶(例如lpl、el、hl等)对酶活性的刺激使得血浆tg水平降低并且为称为高甘油三酯血症(htg)的临床上升高的tg提供高度特异性治疗性治疗。
甘油三酯(也为三酰甘油,tg)为由通过酯键键联的甘油和3-脂肪酸组成的一类脂质。tg为植物油和动物脂肪的主要成分,并且在所有大量营养素中脂肪酸的能量密度最大,与碳水化合物(例如葡萄糖和糖原)相比含有约2.2倍多的卡路里能量。在人类中,血浆tg浓度通常维持在约100-150mg/dl。然而,在最近30年以来,tg水平已稳定上升,并且目前据估计在工业化世界中约三分之一的人口具有长期升高的血浆tg(>150mg/dl)。这种称为高甘油三酯血症(htg)的病状可具有许多病因,包括生活方式/饮食、药物以及遗传,并且它是以下疾病的被认可的危险因子:冠状动脉疾病(cad)(包括缺血性中风、心脏病)、代谢综合征以及胰腺炎(>500mg/dl)(do,r.等人,(2013)nat.genet.45,1345-1352;该文献以全文引用的方式并入本文中)。还充分表明高甘油三酯血症(htg)为发展以下疾病的危险因子:胰岛素抗性和糖尿病、非酒精性脂肪肝疾病(nafld)以及癌症。虽然不清楚确切机制,但高甘油三酯血症(htg)与ldl-胆固醇增加和hdl-胆固醇降低有关,这还促成促粥样硬化血脂异常并且可能是归因于削弱的脂蛋白加工。可将htg患者划分成具有不同严重程度的类别,并且在许多临床研究中已估计了所述群体中归入这些类别中的百分比(do,r.等人,(2013)nat.genet.45,1345-1352;ford等人(2009)arch.intern.med.169,572-578;christian等人(2011)am.j.cardiol.107,891-897;这些文献以全文引用的方式并入本文中)。
tg主要是通过脂酶家族(脂蛋白脂酶(lpl)、内皮脂酶(el)以及肝脂酶(hl))的酶促作用从循环中清除,所述脂酶是通过与硫酸乙酰肝素的高亲和力相互作用而拴系至细胞表面。这些脂酶又在循环中结合富tg脂蛋白(乳糜微粒、vldl、ldl以及hdl)并且将其tg水解成游离脂肪酸和单酰基甘油,这些物质容易由细胞吸收并代谢。脂酶活性受许多与脂蛋白缔合的可交换脱辅基脂蛋白(apo)的影响。或许最佳表征者为apoc-ii和apoc-iii,apoc-ii和apoc-iii分别刺激和抑制脂酶活性。
在一些实施方案中,本文提供用于治疗或预防以下中的一者或多者的组合物、试剂盒、系统以及/或者方法:高甘油三酯血症、甘油三酯水平增加、心血管疾病、关节硬化、急性胰腺炎、糖尿病、肝性脂肪变性以及/或者相关疾病和病状。在一些实施方案中,通过本文所描述的组合物和方法来活化甘油三酯的水解。在一些实施方案中,通过本文所描述的组合物和方法来活化甘油三酯水解蛋白(例如脂蛋白脂酶(lpl)、内皮脂酶(el)以及肝脂酶(hl))以及/或者通道。在一些实施方案中,组合物和方法是用于治疗和/或预防:高甘油三酯血症、甘油三酯水平增加、心血管疾病、关节硬化、急性胰腺炎、糖尿病、肝性脂肪变性以及/或者相关疾病和病状。在一些实施方案中,组合物和方法是用于筛选适合用于治疗和/或预防以下疾病的肽和多肽:高甘油三酯血症、甘油三酯水平增加、心血管疾病、关节硬化、急性胰腺炎、糖尿病、肝性脂肪变性以及/或者相关疾病和病状。
在一些实施方案中,本文提供用于治疗或预防高甘油三酯血症、甘油三酯水平增加以及/或者相关疾病和病状的药物组合物、肽、蛋白质、多肽、编码肽的核酸、蛋白质和多肽、前述物质的分子复合物等。在一些实施方案中,本文提供av-肽和多肽(例如包含低于100%序列同一性的全长apoa-v(seqidno:1),或全长apoa-v的片段(例如seqidno:2、seqidno:3、seqidno:4、seqidno:5、seqidno:6、seqidno:7、seqidno:8或其截短型式)等)。在一些实施方案中,肽为合成肽。在一些实施方案中,通过本领域一般技术人员已知的方法来制备本文所描述的多肽或肽。举例来说,可使用固相多肽合成技术(例如fmoc或boc化学)来合成肽或多肽。或者,可使用重组dna技术(例如使用细菌或真核表达系统)来制备肽或多肽。另外,肽或多肽可在受试者内(例如在施用适当载体之后)得到表达。因此,为促进此类方法,本文提供包含编码多肽的序列的遗传载体(例如质粒、病毒载体(例如aav)等),以及包含此类载体的宿主细胞。此外,本文提供经由此类方法制备的肽和多肽。
在一些实施方案中,提供基于apoa-v的肽和多肽以及与其相关的组合物(例如基于apoa-v的肽和多肽的拟似物、编码基于apoa-v的肽和多肽的核酸等)的施用。在一些实施方案中,本文提供肽和多肽的施用,所述肽和多肽增强三酰甘油降解(例如水解等)或为本文中另外所描述。此类肽和多肽的实例包括选自由以下组成的群组的那些:seqidno.2-seqidno.29。在一些实施方案中,提供包含以下序列或由其组成的肽或多肽:seqidno:2、seqidno:3、seqidno:4、seqidno:5、seqidno:6、seqidno:7、seqidno:8、seqidno:9、seqidno:10、seqidno:11、seqidno:12、seqidno:13、seqidno:14、seqidno:15、seqidno:16、seqidno:17、seqidno:18、seqidno:19、seqidno:20、seqidno:21、seqidno:22、seqidno:23、seqidno:24、seqidno:25、seqidno:26、seqidno:27、seqidno:28、seqidno:29。在一些实施方案中,提供与以下中的一者具有至少50%的序列同一性(例如至少60%的序列同一性、至少70%的序列同一性、至少80%的序列同一性、至少90%的序列同一性、至少95%的序列同一性等)的肽或多肽:seqidno:1、seqidno:2、seqidno:3、seqidno:4、seqidno:5、seqidno:6、seqidno:7、seqidno:8、seqidno:9、seqidno:10、seqidno:11、seqidno:12、seqidno:13、seqidno:14、seqidno:15、seqidno:16、seqidno:17、seqidno:18、seqidno:19、seqidno:20、seqidno:21、seqidno:22、seqidno:23、seqidno:24、seqidno:25、seqidno:26、seqidno:27、seqidno:28、seqidno:29。在一些实施方案中,肽和多肽相对于野生型序列(例如seqidno:1-seqidno:8)包含至少一种突变。在一些实施方案中,肽或多肽包含:arlsrcvqvlsr(x1)ltl(x2)akal(x3)ariqqnldqlre,其中x1、x2以及x3独立地为任何氨基酸(seqidno:15);arlsrcvqvlsr(b1)ltl(b2)akal(b3)ariqqnldqlre,其中b1、b2以及b3独立地为任何酸性和/或带电荷氨基酸(seqidno:16);arlsrcvqvlsr(k/q)ltl(k/q)akal(h/k/q)ariqqnldqlre,(seqidno:17)。在一些实施方案中,本文提供如下方法,所述方法包括施用(例如向受试者、向细胞、向样品等)以上所提到的apoa-v肽或多肽中的一者或多者。
在展开本文中的实施方案期间所进行的实验证实av199-232(seqidno:5)为用于最佳诱导lpl活性的apoa-v的最小部分(seqidno:1)。包括生物化学突变分析、计算机研究、分子模型化以及丙氨酸扫描的实验指示av199-232的(1)与脂酶刺激最低程度相关、(2)与脂酶刺激适度相关以及(3)与脂酶刺激高度相关的各种残基。实验还指示其中相对于天然av199-232序列的取代提供(或可提供)av-肽的一个或多个特性(例如lpl活化、溶解度、脂质结合、肝素结合等)的增强的某些残基。在一些实施方案中,提供包含具有一个或多个非天然取代的av199-232序列(例如seqidno:5)的av-肽。
在一些实施方案中,av-肽相对于seqidno:5在本文中的数据指示与脂酶活性刺激最低程度相关的位置包含保守、半保守以及/或者非保守取代。在一些实施方案中,av-肽相对于seqidno:5在本文中的数据指示与脂酶活性刺激最低程度相关的位置包含保守和/或半保守取代。在一些实施方案中,av-肽相对于seqidno:5在本文中的数据指示与脂酶活性刺激最低程度相关的位置包含保守取代。
在一些实施方案中,av-肽相对于seqidno:5在本文中的数据指示与脂酶活性刺激适度相关的位置包含保守、半保守以及/或者某些非保守取代。在一些实施方案中,av-肽相对于seqidno:5在本文中的数据指示与脂酶活性刺激适度相关的位置包含保守和/或半保守取代。在一些实施方案中,av-肽相对于seqidno:5在本文中的数据指示与脂酶活性刺激适度相关的位置包含保守取代。
在一些实施方案中,av-肽相对于seqidno:5在本文中的数据指示与脂酶活性刺激高度相关的位置包含保守、半保守取代以及/或者不包含取代。在一些实施方案中,av-肽相对于seqidno:5在本文中的数据指示与脂酶活性刺激高度相关的位置包含保守取代以及/或者不包含取代。在一些实施方案中,av-肽相对于seqidno:5在本文中的数据指示与脂酶活性刺激高度相关的位置不包含取代。
在一些实施方案中,在展开本文中的实施方案期间所进行的各种实验指示对特定残基或残基类别的取代(例如保守、半保守、非保守)增强对脂酶活性的刺激的残基(例如与脂酶活性刺激最低限度、适度或高度相关)。由本文所描述的实验和数据来看,av199-232肽内的各种此类位置为显而易见的。由以下seqidno:29来看可尤其有益的某些取代为显而易见的:
ar(l/f/y/w)(s/t/n/g)(r/k/hlys/harg)(c/s/t/n/q/y/h)(v/f/y/w)qv(l/f/y/w)s(r/k/hlys/harg)(k/r/harg/hlys/orn)(l/f/y/w)tl(k/r/harg/hlys/orn)(a/f/y/w)(r/k/hlys/harg)a(l/f/y/w)(h/k/hlys/r/harg/orn)ar(i/f/y/w)qqn(l/f/y/w)dq(l/f/y/w)re;或
arx3x4x5x6x7qvx10sx12x13x14tlx17x18x19ax21x22arx25qqnx29dqx32re,其中:x3为l、f、y或w;x4为s、t、n或g;x5为r、k、hlys或harg;x6为c、s、t、n、q、y或h;x7为v、f、y或w;x10为l、f、y或w;x12为r、k、hlys或harg;x13为k、r、harg、hlys或orn;x14为l、f、y或w;x17为k、r、harg、hlys或orn;x18为a、f、y或w;x19为r、k、hlys或harg;x21为l、f、y或w;x22为h、k、hlys、r、harg或orn;x25为i、f、y或w;x29为l、f、y或w;并且x32为l、f、y或w。
在一些实施方案中,本文所描述的实验和分析表明seqidno:29中允许进行的各种取代增强或不显著削弱肽的脂酶刺激活性。本文所描述的数据还可指示其他取代,并且它们在本文的实施方案的范围内。
在一些实施方案中,表1(实施例8)提供在本文的实施方案范围内的相对于seqidno:5的取代。
实施方案不受本文所描述的特定取代的限制。在一些实施方案中,满足本文所描述的限制(例如脂族螺旋、lpl刺激、类似结构域构造等)并且具有未明确描述的取代的肽在此处的实施方案范围内。在一些实施方案中,对本文所描述的肽进行进一步修饰(例如取代、缺失或添加标准氨基酸;化学修饰;等)。本领域中所理解的修饰包括n端修饰、c端修饰(其使肽不发生蛋白降解)、酰胺基的烷基化、烃“钉合(stapling)”(例如用于稳定α-螺旋构象)。在一些实施方案中,可通过例如带电荷残基的保守残基取代(k至r、r至k、d至e以及e至d)对本文所描述的肽进行修饰。在一些实施方案中,此类保守取代提供例如脂酶和肝素结合位点的微小变化,目标为改善特异性和/或脂酶刺激性能。举例来说,富含r残基的肽倾向于以比富含k的肽高的亲和力结合肝素。未端羧基的修饰包括但不限于酰胺、低碳烷基酰胺、受约束烷基(例如分枝链、环状、稠合、金刚烷基)烷基、二烷基酰胺以及低碳烷基酯修饰。低碳烷基为c1-c4烷基。此外,一或多个侧基或末端基团可受到一般熟练的肽化学工作者已知的保护基的保护。氨基酸的α-碳可为单甲基化或双甲基化的。
在一些实施方案中,在肽内引入一个或多个肽内二硫键(例如在两个半胱氨酸(例如c6与被取代的半胱氨酸、两个被取代的半胱氨酸、在av肽序列外部的一个或两个半胱氨酸等之间)。在一些实施方案中,肽内二硫键的存在使肽稳定。
在一些实施方案中,本文所描述的任何实施方案可包含对应于本文所描述的av-肽的av-拟肽物,其具有本领域中了解的各种修饰。在一些实施方案中,可将本文所描述的肽序列中的残基用具有类似特性(例如疏水性至疏水性、中性至中性等)或具有其他所需特性(例如更酸、更疏水、更不庞大、更庞大等)的氨基酸取代。在一些实施方案中,将非天然氨基酸(或除20种标准氨基酸以外的天然存在的氨基酸)加以取代以实现所需性质。
在一些实施方案中,将具有在生理条件下带正电荷的侧链的残基或需要带正电荷的侧链的残基用包括但不限于以下的残基取代:赖氨酸、高赖氨酸、δ-羟基赖氨酸、高精氨酸、2,4-二氨基丁酸、3-高精氨酸、d-精氨酸、精胺醛(精氨酸中的-cooh由-cho置换)、2-氨基-3-胍基丙酸、硝基精氨酸(n(g)-硝基精氨酸)、亚硝基精氨酸(n(g)-亚硝基精氨酸)、甲基精氨酸(n-甲基-精氨酸)、ε-n-甲基赖氨酸、别羟基赖氨酸、2,3-二氨基丙酸、2,2'-二氨基庚二酸、鸟氨酸、对称二甲基精氨酸、不对称二甲基精氨酸、2,6-二氨基已炔酸、对氨基苯甲酸和3-氨基酪氨酸以及组氨酸、1-甲基组氨酸和3-甲基组氨酸。
中性残基为具有在生理条件下不带电荷的侧链的残基。极性残基优选在侧链中具有至少一个极性基团。在一些实施方案中,极性基团选自羟基、硫氢基、胺、酰胺以及酯基或允许形成氢桥的其他基团。
在一些实施方案中,将具有在生理条件下为中性/极性的侧链的残基或需要中性侧链的残基用包括但不限于以下的残基取代:天冬酰胺、半胱氨酸、谷酰胺、丝氨酸、苏氨酸、酪氨酸、瓜氨酸、n-甲基丝氨酸、高丝氨酸、别苏氨酸和3,5-二硝基-酪氨酸以及β-高丝氨酸。
具有非极性、疏水性侧链的残基为在生理条件下不带电荷的残基,优选具有超过0、尤其超过3的亲水性指数。在一些实施方案中,非极性、疏水性侧链选自具有1至10个、优选2至6个碳原子的烷基、亚烷基、烷氧基、烯氧基、烷基磺酰基以及链烯基磺酰基残基,或具有5至12个碳原子的芳基。在一些实施方案中,将具有非极性、疏水性侧链的残基或需要非极性、疏水性侧链的残基用包括但不限于以下的残基取代:亮氨酸、异亮氨酸、缬氨酸、甲硫氨酸、丙氨酸、苯基丙氨酸、n-甲基亮氨酸、叔丁基甘氨酸、辛基甘氨酸、环己基丙氨酸、β-丙氨酸、1-氨基环己基羧酸、n-甲基异亮氨酸、正亮氨酸、正缬氨酸以及n-甲基缬氨酸。
在一些实施方案中,将肽和多肽分离并且/或者纯化(或大体上分离并且/或者大体上纯化)。因此,在此类实施方案中,以大体上分离形式提供肽和/或多肽。在一些实施方案中,肽和/或多肽是由于例如固相肽合成而与其他肽和/或多肽分离。或者,可在重组制备的细胞溶解之后从其他蛋白质大体上分离肽和/或多肽。可使用蛋白质纯化的标准方法(例如hplc)来大体上纯化肽和/或多肽。在一些实施方案中,本发明提供一种肽和/或多肽的制剂,所述肽和/或多肽的制剂视所需用途而定呈许多配制品形式。举例来说,在将多肽大体上分离(或甚至与其他蛋白质几乎完全分离)的情况下,可将它在适合用于储存(例如在冷藏条件下或在冷冻条件下)的介质溶液中进行配制。此类制剂可含有防护剂(诸如缓冲液)、防腐剂、低温防护剂(例如糖,诸如海藻糖)等。此类制剂的形式可为溶液、凝胶等。在一些实施方案中,将apoa-v肽和/或多肽制备成冻干形式。此外,此类制剂可包括其他所需药剂,诸如小分子或其他肽、多肽或蛋白质。实际上,可提供包含在此所描述的肽和/或多肽的不同实施方案的混合物的此类制剂。
在一些实施方案中,本文提供本文所描述的肽序列的拟肽物型式或其变体。在一些实施方案中,拟肽物的特征在于实体保留其肽等效物的极性(或无极性、疏水性等)、三维尺寸以及官能性(生物活性),但其中所有或一部分肽键已被置换(例如由更稳定的键联置换)。在一些实施方案中,‘稳定’是指对化学降解或由水解酶进行酶促降解更具抵抗力。在一些实施方案中,置换酰胺键(例如酰胺键代用物)的键保留酰胺键的一些性质(例如构象、空间体积、静电特性、氢键合能力等)。“drugdesignanddevelopment”,krogsgaard,larsen,liljefors以及madsen(编)1996,horwoodacad.publishers的第14章提供对设计和合成拟肽物的技术的一般论述并且以全文引用的方式并入本文中。适合的酰胺键代用物包括但不限于:n-烷基化(schmidt,r.等人,int.j.peptideproteinres.,1995,46,47;该文献以全文引用的方式并入本文中)、逆翻转酰胺(chorev,m.和goodman,m.,acc.chem.res,1993,26,266;该文献以全文引用的方式并入本文中)、硫酰胺(shermand.b.和spatola,a.f.j.am.chem.soc.,1990,112,433;该文献以全文引用的方式并入本文中)、硫酯、膦酸酯、酮基亚甲基(hoffman,r.v.和kim,h.o.j.org.chem.,1995,60,5107;该文献以全文引用的方式并入本文中)、羟基亚甲基、氟乙烯基(allmendinger,t.等人,tetrahydronlett.,1990,31,7297;该文献以全文引用的方式并入本文中),乙烯基、亚甲基胺(sasaki,y和abe,j.chem.pharm.bull.199745,13;该文献以全文引用的方式并入本文中)、亚甲基硫基(spatola,a.f.,methodsneurosci,1993,13,19;该文献以全文引用的方式并入本文中)、链烷(lavielle,s.等人,int.j.peptideproteinres.,1993,42,270;该文献以全文引用的方式并入本文中)以及磺酰胺基(luisi,g.等人tetrahedronlett.1993,34,2391;该文献以全文引用的方式并入本文中)。
像酰胺键的置换一样,拟肽物可涉及用二拟肽或三拟肽结构置换较大结构部分,并且在此情况下,可以二肽置换形式使用涉及肽键的拟似物部分(诸如唑衍生的拟似物)。适合的拟肽物包括还原肽,其中已通过用还原剂(例如硼烷或氢化物试剂,诸如氢化锂铝)处理将酰胺键还原为亚甲基胺;此类还原具有增加的优点,即增加分子的总阳离子度。
其他拟肽物包括例如通过分步合成酰胺官能化聚甘氨酸形成的类肽。一些拟肽物主链将可轻易获自其肽前体,诸如已全甲基化的肽,适合的的方法由ostresh,j.m.等人描述于proc.natl.acad.sci.usa(1994)91,11138-11142中;该文献以全文引用的方式并入本文中。
在一些实施方案中,在使用之前将肽加以处理或调节。举例来说,可将apoa-v肽与极低密度脂蛋白(vldl)一起孵育。在一些实施方案中,可将av-肽与肝素、合成脂蛋白、脂质体或患者自己的脂蛋白一起孵育以增强生物可用性和治疗功效。
在一些实施方案中,以与其他肽或多肽融合的形式提供本文所描述的肽。此类融合物可由编码apoa-v肽和额外的肽/多肽的重组dna表达或可通过化学合成来形成。举例来说,融合物可包含apoa-v肽和所关注的酶、荧光素酶、核糖核酸酶抑制剂(rnasin)或核糖核酸酶和/或通道蛋白(例如离子通道蛋白)、受体、膜蛋白、胞质蛋白、核蛋白、结构蛋白、磷蛋白、激酶、信号传导蛋白、代谢蛋白、线粒体蛋白、受体相关蛋白、荧光蛋白、酶底物、转录因子、可选标记蛋白、核酸结合蛋白、细胞外基质蛋白、所分泌蛋白质、受体配体、血清蛋白、具有反应性半胱氨酸的蛋白质、转运蛋白、靶向序列(例如肉豆蔻基化序列)、线粒体定位序列或核定位序列。可将额外的肽/多肽融合至apoa-v肽的n端和/或c端。在一个实施方案中,融合蛋白包含位于apoa-v肽的n端的第一肽/多肽以及位于c端的另一(不同)肽/多肽。任选地,融合物中的元件由连接序列隔开,所述连接序列为例如优选具有至少2个氨基酸残基的连接序列,诸如具有13个并且多达40或50个氨基酸残基的连接序列。在本发明的融合蛋白中存在连接序列并不相对于每个单个元件的功能大体上改变融合物中的任一元件(例如apoa-v肽)的功能,这可能归因于连接序列为融合物中的每个元件提供可挠性(自主性)。在某些实施方案中,连接序列为由酶识别的序列或为可光裂解的。举例来说,连接序列可包括蛋白酶识别位点。
在一些实施方案中,本文提供包含本文所描述的一种或多种av-肽和多肽(例如与seqidno:5具有低于100%的序列同一性、展现出增强的甘油三酯水解脂酶活化等)以及药学上可接受的载体的药物组合物。可供应活性肽或多肽(例如在不破坏载体内的肽或多肽的情况下)的任何载体均为适合的载体,并且此类载体为本领域中熟知的。在一些实施方案中,将组合物配制成用于通过包括但不限于以下的任何适合的途径进行施用:经口(例如诸如以片剂、胶囊、颗粒或粉末形式)、舌下、经颊、肠胃外(诸如通过皮下、静脉内、肌肉内、真皮内或胸骨内注射或输注(例如以无菌可注射水溶液或非水溶液或悬浮液等形式))、经鼻(包括向鼻膜施用,诸如通过吸入喷雾)、表面(诸如以乳膏或软膏形式)、经皮(诸如通过经皮贴片)、经直肠(诸如以栓剂形式)等。
在一些实施方案中,本文提供用于治疗罹患高甘油三酯血症(或处于其风险中)和/或需要治疗(或预防性治疗)的患者的方法。在一些实施方案中,以足以治疗病状的量并且在足以治疗病状的位置向此类患者递送包含至少一种本文所描述的av-肽或多肽的药物组合物。在一些实施方案中,可将肽和/或多肽(或包含此类物质的药物组合物)全身或局部递送至患者,并且确定用于治疗的最适当递送途径、时程以及剂量将在治疗此类患者的医疗专业人员的一般技术之内。应了解,治疗患者的施用方法最优选大体上缓解或甚至消除此类症状;然而,如许多医学治疗一般,如果在本发明方法期间、在其之后或以其他方式作为其结果,患者的疾病或病症的症状减退至可查明的程度,那么认为本发明方法的应用为成功的。
可以与药学上可接受的载体和任选的赋形剂、助剂等一起根据良好药物实践加以配制的形式来施用药物组合物。基于av-肽的药物组合物可呈诸如以下的固体、半固体或液体剂型形式:粉末、溶液、酏剂、糖浆、悬浮液、乳膏、滴剂、糊剂以及喷雾。如本领域技术人员将认识到,视所选施用途径(例如丸剂、注射等)而定,确定组合物形式。一般来说,为实现容易并且准确的活性药物肽或多肽施用,优选使用单位剂型。一般来说,治疗有效性药物化合物以在以总组合物的重量计约0.5%至约99%范围内的浓度水平(例如以足以提供所需单位剂量的量)存在于此类剂型中。在一些实施方案中,可以单剂量或多剂量施用药物组合物。技术人员将按照所要治疗的个体的病状以及所述受试者对治疗的反应来确定特定施用途径和给药方案。在一些实施方案中,以用于向受试者施用的单位剂型形式提供基于av-肽的药物组合物,包含av-肽或多肽(例如与seqidno:2的部分具有低于100%的序列同一性等)以及一种或多种无毒的药学上可接受的载体、助剂或媒介物。可与此类物质组合以制备单一剂型的活性成分的量将视如以上所指出的各种因素而不同。如在药物技术中可用,在本发明的组合物中可使用多种材料作为载体、助剂以及媒介物。可按需要使用适合的分散或润湿剂以及悬浮剂将可注射制剂(诸如油性溶液、悬浮液或乳液)配制成本领域中已知的形式。无菌可注射制剂可使用无毒的肠胃外可接受的稀释剂或溶剂,诸如无菌无热原水或1,3-丁二醇。在其他可接受的媒介物和溶剂之中,可使用的是5%葡萄糖注射液、林格氏注射液(ringer'sinjection)以及等渗氯化钠注射液(如usp/nf中所描述)。此外,常规地可使用无菌、固定油作为溶剂或悬浮介质。出于此目的,可使用任何温和的固定油,包括合成的甘油单酯、甘油二酯或甘油三酯。在可注射组合物的制备中还可使用脂肪酸,诸如油酸。
可进一步通过诸如以下化学变化来衍生出本文所公开的涵盖大体上α螺旋肽区域的肽和多肽:酰胺化、糖基化、酰化、硫酸盐化、磷酰化、乙酰基化以及环化。可通过化学或生物化学方法以及通过体内方法或其任何组合来获得此类化学变化。
在某些实施方案中,通过修饰末端氨基来衍生出本文所描述的肽和多肽。此类修饰包括但不限于脱氨基、n-低碳烷基、n-二低碳烷基、受约束烷基(例如分枝链、环状、稠合、金刚烷基)以及n-酰基修饰,其中酰基部分为c6-c20烷基。
在某些实施方案中,通过修饰末端羧基来衍生出本文所描述的肽和多肽。此类修饰包括但不限于酰胺、低碳烷基酰胺、受约束烷基(例如分枝链、环状、稠合、金刚烷基)烷基、二烷基酰胺以及低碳烷基酯修饰,其中低碳烷基为c1-c4烷基。此外,一个或多个侧基或末端基团可受到一般熟练的肽化学工作者已知的保护基的保护。氨基酸的α-碳可为单甲基化或双甲基化的。
在各个实施方案中,通过缀合至一种或多种聚合物或小分子取代基来衍生出本文所公开的肽和多肽。
在这些实施方案中的某些中,通过偶联至聚乙二醇(peg)来衍生出本文所描述的合成肽和多肽。可使用已知方法进行偶联。参见int.j.hematology,68:1(1998);bioconjugatechem.,6:150(1995);以及crit.rev.therap.drugcarriersys.,9:249(1992),所述文献全部以全文引用的方式并入本文中。因此,本领域技术人员将能够利用此类熟知用于使一种或多种聚乙二醇聚合物键联至本文所描述的肽和多肽的技术。典型地可商购获得或可通过本领域技术人员熟知的技术来制备适合的聚乙二醇聚合物。聚乙二醇聚合物优选具有500与20,000之间的分子量并且可为分枝链或直链聚合物。
可通过偶联至氨基、羧基或硫醇基来实现peg附接至本文所描述的肽或多肽。这些基团将典型地为n端和c端以及如赖氨酸、天冬氨酸、谷氨酸以及半胱氨酸一般位于此类天然存在的氨基酸的侧链上。因为可通过固相肽化学技术来制备本公开的肽和多肽,所以可引入含有具有正交保护基的二氨基和二羧基的多个部分以与peg缀合。
本公开还提供本文所描述的肽和多肽与一种或多种不为聚乙二醇的聚合物的缀合。
在一些实施方案中,通过缀合或键联至聚氨基酸(例如聚his、聚arg、聚lys等)和/或各种长度的脂肪酸链或将聚氨基酸和/或各种长度的脂肪酸链附接至n端或c端或氨基酸残基侧链来衍生出本文所描述的肽和多肽。在某些实施方案中,如以全文引用的方式并入本文中的美国专利号6,552,167中所描述,通过添加精确长度的聚酰胺链、尤其聚酰胺链来衍生出本文所描述的肽和多肽。在其他实施方案中,如以全文引用的方式并入本文中的美国专利号5,359,030和5,681,811中所描述,通过添加烷基peg部分来修饰肽和多肽。
在所选实施方案中,通过结合至包括白蛋白和明胶的聚合物来衍生出本文所公开的肽和多肽。参见gombotzandpettit,bioconjugatechem.,6:332-351,1995,该文献以全文引用的方式并入本文中。
在其他实施方案中,使本文所公开的肽和多肽缀合或融合至免疫球蛋白或免疫球蛋白片段,诸如抗体fc区。
在各个实施方案中,通过附接小分子取代基来衍生出本文所描述的肽和多肽,所述小分子取代基包括短链烷基和受约束烷基(例如分枝链、环状、稠合、金刚烷基)以及芳族基。
在某些实施方案中,本文所描述的肽和多肽包含含有c5-c9直链或分枝链烷基侧链的烷基甘氨酸氨基酸类似物或环烷基。在一个实施方案中,肽或多肽包含烷基甘氨酸,所述烷基甘氨酸包含c6-c8直链或分枝链烷基侧链。在另一实施方案中,多肽包含辛基甘氨酸,所述辛基甘氨酸包含c8直链烷基侧链(辛基-甘氨酸)。
可用各种无机和有机酸以及碱将本文所描述的肽和多肽制备成盐。此类盐包括用有机和无机酸,例如用hcl、hbr、h2so4、h3po4、三氟乙酸、乙酸、甲酸、甲磺酸、甲苯磺酸、顺丁烯二酸、反丁烯二酸以及樟脑磺酸制备的盐。用碱制备的盐包括铵盐、碱金属盐(例如钠盐和钾盐)、碱土盐(例如钙盐和镁盐)以及锌盐。可通过常规手段来形成所述盐,诸如通过使产物的游离酸或碱形式与适当的碱或酸的一种或多种等效物在不溶解盐的溶剂或介质中或在随后在真空下或通过冷冻干燥移除的溶剂(诸如水)中反应,或通过在适合的离子交换树脂上将现有盐的离子交换为另一离子。
可将本文所描述的肽和多肽配制成药学上可接受的盐和/或其复合物的形式。药学上可接受的盐包括酸加成盐,诸如那些含有以下物质的酸加成盐:硫酸盐、盐酸盐、磷酸盐、氨基磺酸盐、乙酸盐、柠檬酸盐、乳酸盐、酒石酸盐、丁二酸盐、草酸盐、甲烷磺酸盐、乙烷磺酸盐、苯磺酸盐、对甲苯磺酸盐、环己基氨基磺酸盐以及奎尼酸盐(quinate)。药学上可接受的盐可从酸获得,诸如盐酸、硫酸、磷酸、氨基磺酸、乙酸、柠檬酸、乳酸、酒石酸、丙二酸、甲磺酸、乙磺酸、苯磺酸、对甲苯磺酸、环己基氨基磺酸以及奎尼酸。可如下制备此类盐,例如通过使产物的游离酸或碱形式与适当的碱或酸的一种或多种等效物在不溶解盐的溶剂或介质中或在随后在真空下或通过冷冻干燥移除的溶剂(诸如水)中反应,或通过在适合的离子交换树脂上将现有盐的离子交换为另一离子。
可将本文所描述的肽和多肽配制成用于结合本公开的方法使用的药物组合物的形式。可适宜地以适合用于包括以下的肠胃外施用的配制品的形式提供本文所公开的组合物:皮下、肌肉内以及静脉内施用、鼻内施用、经肺施用或经口施用。标准配制品专著(例如e.w.martin的remington'spharmaceuticalsciences)中描述了肽和多肽的适合用于各种此类施用途径的配制品。还参见wang,y.j.和hanson,m.a.“parenteralformulationsofproteinsandpeptides:stabilityandstabilizers”,journalofparenteralscienceandtechnology,technicalreport第10期,增刊42:2s(1988)。
某些本文所描述的肽和多肽可大体上不溶于水且微溶于大多数药学上可接受的质子溶剂和植物油。在某些实施方案中,可添加环糊精作为水溶性增强剂。环糊精包括α-环糊精、β-环糊精以及γ-环糊精的甲基、二甲基、羟丙基、羟乙基、葡糖基、麦芽糖基以及麦芽三糖基衍生物。示例性环糊精溶解度增强剂为羟丙基-β-环糊精(hpbcd),所述羟丙基-β-环糊精可被添加至以上所描述的组合物中的任一者中以进一步改善肽或多肽的水溶性特性。在一个实施方案中,组合物包含0.1%至20%hpbcd、1%至15%hpbcd或2.5%至10%hpbcd。所用溶解度增强剂的量将取决于组合物中本公开的肽或多肽的量。在某些实施方案中,可在诸如以下的非水性极性非质子溶剂中对肽加以配制:dmso、二甲基甲酰胺(dmf)或n-甲基吡咯烷酮(nmp)。
在一些情况下,提供呈单一组合物或溶液形式以便将一起施用的肽或多肽和另一活性剂将为适宜的。在其他情况下,将额外的药剂与所述多肽分开施用可为更有利的。
关于使用,可以单位剂型形式提供本文所描述的肽和多肽的药物组合物,所述单位剂型含有在单次施用中有效的量的肽或多肽。适合用于皮下施用的单位剂型包括预装填注射器和注入器。
在一些实施方案中,av-肽/多肽是以药物组合物形式提供和/或与一种或多种额外的治疗剂共施用(并行或串联)。此类额外的药剂可用于进一步降低甘油三酯水平或用于治疗相关问题(例如胆固醇水平升高、高血压等)病状或疾病。额外的药剂可包括但不限于:纤维酸衍生物、烟碱酸、ω-3脂肪酸、激素药物(例如美曲普汀(metreleptin)(myalept))、他汀(例如辛伐他汀(simvastatin)、阿伐他汀(atorvastatin),罗伐他汀(rosuvastatin)等)、抗血小板剂(例如阿司匹林(aspirin)、氯吡格雷(clopidogrel)、双嘧达莫(dipyridamole)、噻氯匹定(ticlopidine)等)、抗凝剂(例如杀鼠灵(warfarin)(coumadin)和肝素)、用于治疗糖尿病的药物(例如磺酰脲、双胍、美格替奈(meglitinide)、噻唑啶二酮、dpp-4抑制剂、sglt2抑制剂、α-葡糖苷酶抑制剂、胆汁酸钳合剂等)、胰岛素、glp-1肽(例如victoza)等。
在一些实施方案中,提供本文所描述的基于av-肽的组合物是作为试剂盒的一部分。在一些实施方案中,本发明的试剂盒包含一种或多种基于apoa-v的肽或多肽。在一些实施方案中,试剂盒包含被配置成与一种或多种额外的组合物(例如药物组合物)共施用的基于av-肽的组合物。在一些实施方案中,将一种或多种基于av-肽的组合物与用于使降低甘油三酯或治疗或预防高甘油三酯血症或相关疾病或病状有效增强的一种或多种其他药剂共施用。
在一些实施方案中,为降低甘油三酯浓度、增强降解(例如水解)和/或治疗或预防高甘油三酯血症、心血管疾病、关节硬化、急性胰腺炎、糖尿病、肝性脂肪变性和/或相关疾病和病状而提供基于av-肽的组合物。对所描述的特征和实施方案的各种修改、重组以及变化对本领域技术人员来说将为清楚的,而不会背离本发明的范围和精神。虽然已描述特定实施方案,但应了解如所要求的本发明不应过度受限于此类特定实施方案。实际上,对所描述的模式和实施方案的对相关领域的熟练人员来说明显的各种修改旨在在以下权利要求书的范围内。
如本文所陈述,在一些实施方案中,提供治疗高甘油三酯血症的方法。所述方法包括以足以降低血液甘油三酯水平的量、按足以实现此目的的时程向高甘油三酯血症患者施用如本文所描述的肽或多肽并且持续足以实现此目的的持续时间。
在某些实施方案中,患者具有极限高甘油三酯血症,极限高甘油三酯血症被定义为在本文所提供的治疗之前非空腹血浆甘油三酯(“tg”)水平≥885mg/dl。在一些实施方案中,患者具有严重高甘油三酯血症,严重高甘油三酯血症被定义为治疗前tg水平在500与885mg/dl之间。在一些实施方案中,在治疗之前患者具有难治性高甘油三酯血症,难治性高甘油三酯血症被定义为tg水平在200mg/dl与500mg/dl之间。在其他实施方案中,患者在治疗之前具有在150mg/dl与200mg/dl之间的边界高甘油三酯血症。在常规实施方案中,患者将具有高甘油三酯血症,不过在起始本文所提供的治疗之前已用一种或多种其他治疗剂进行了治疗。
在某些实施方案中,患者将具有乳糜微粒血症。在一些实施方案中,患者将具有超过正常值的ldl-c水平。在一些实施方案中,患者将具有低于正常水平的hdl-c。
在一些实施方案中,患者将具有胰腺炎。在一些实施方案中,患者将具有糖尿病。在某些实施方案中,患者将具有代谢综合征。一些患者将具有肝脾肿大。一些患者将具有非酒精性脂肪性肝炎(“nash”)。一些患者将具有脂肪代谢障碍(例如先天性、后天性、全身性、部分性等)。
在某些实施方案中,患者为成人。在其他实施方案中,患者为儿童。
在多个实施方案中,以足以使甘油三酯水平与即将起始治疗前的水平相比降低至少5%、10%、15%、20%或25%或更多的量、按足以实现此目的的时程施用多肽并且持续足以实现此目的的持续时间。在一些实施方案中,以足以使甘油三酯水平降低至少30%、35%、40%、45%或50%的量、按足以实现此目的的给药时程施用多肽并且持续足以实现此目的的持续时间。在特定实施方案中,以足以使甘油三酯水平降低至少55%、60%、65%、甚至至少约70%或更多的量、按足以实现此目的的时程施用多肽并且持续足以实现此目的的时间。
在某些实施方案中,以不管给药频率如何均表述为日等效剂量的量施用多肽,所述量为每天50微克(“mcg”)、每天60mcg、每天70mcg、每天75mcg、每天100mcg、每天150mcg、每天200mcg或每天250mcg。在一些实施方案中,以每天500mcg、每天750mcg或每天1毫克(“mg”)的量施用多肽。在其他实施方案中,以不管给药频率如何均表述为日等效剂量的量施用多肽,所述量为每天1-10mg,包括每天1mg、每天1.5mg、每天1.75mg、每天2mg、每天2.5mg、每天3mg、每天3.5mg、每天4mg、每天4.5mg、每天5mg、每天5.5mg、每天6mg、每天6.5mg、每天7mg、每天7.5mg、每天8mg、每天8.5mg、每天9mg、每天9.5mg或每天10mg。
在多个实施方案中,按每月给药时程施用多肽系。在其他实施方案中,每两周施用多肽。在其他实施方案中,每周施用多肽。在某些实施方案中,每天(“每天一次”)施用多肽。在所选实施方案中,一天施用两次(“每天两次”)多肽。
在典型实施方案中,施用多肽至少3个月、至少6个月、至少12个月或更久。在一些实施方案中,施用多肽至少18个月、2年、3年或更久。
在典型实施方案中,肠胃外施用多肽。在一些肠胃外实施方案中,皮下施用多肽。在一些肠胃外实施方案中,肌肉内施用多肽。在其他实施方案中,静脉内施用多肽。在某些实施方案中,通过皮下植入渗透性微型泵(intarcia)来施用多肽。
在其他实施方案中,鼻内施用多肽。在某些实施方案中,通过吸入施用多肽。在其他实施方案中,通过颊内施用或通过舌下施用而经口施用多肽。
在其他实施方案中,经皮施用多肽。
在某些优选实施方案中,通过皮下注射以0.5-5.0mg的量每天施用一次多肽,持续至少6个月。
在典型实施方案中,施用多肽作为设计成降低甘油三酯水平的膳食的辅助物。
在多个实施方案中,将多肽与至少一种额外的治疗剂组合施用。典型地,在此类实施方案中,以单独的组合物形式施用额外的治疗剂。在这些实施方案中的某些中,通过与本文所描述的多肽不同的施用途径和/或按不同的给药时程来施用额外的治疗剂。
在组合实施方案中的某些中,至少一种额外的药剂中的至少一者选自由以下组成的群组:烟碱酸、ω-3多不饱和脂肪酸;贝特(fibrate);米泊美生(mipomersen);以及阿利泼金(alipogenetiparvovec)。在特定实施方案中,ω-3多不饱和脂肪酸选自由以下组成的群组:乙基二十碳五烯酸(icosapentethyl);ω-3羧酸;以及ω-3-酸乙酯。在某些实施方案中,至少一种额外的药剂为他汀。在某些实施方案中,他汀选自由以下组成的群组:普伐他汀(pravastatin)、洛伐他汀(lovastatin)、辛伐他汀、阿伐他汀、氟伐他汀(fluvastatin),罗伐他汀、替伐他汀(tenivastatin)以及匹伐他汀(pitavastatin)。
实验
实施例1
apoa-v中的脂酶刺激结构域
apoa-v为343个氨基酸的相对大的蛋白质并且已被认为具有三种活性:脂质结合、肝素/受体结合以及脂酶活化(图1)。我们特别关注的是apoa-v中刺激脂酶活性的结构域,并且在人类群体中已确定的许多突变已帮助阐明其位置。近来由mendoza-barberá和同事进行的描绘在htg患者中的三种不相关apoa5突变的重要研究(sharma等人(2014)arterioscler.thromb.vasc.biol.34,2254-2260;该文献以全文引用的方式并入本文中)识别了显著削弱apoa-v的脂酶刺激活性的(ser232-leu235)del和leu253pro。此缺失对应于先前报导的富含带正电荷残基的42氨基酸序列,其具有强硫酸乙酰肝素结合潜能,并且被显示为细胞表面结合所必需的(nilsson等人(2007)biochemistry46,3896-3904;该文献以全文引用的方式并入本文中)。pro残基(在leu253pro中)当仅置换一个残基位置时被视为蛋白质结构破坏者,并且将可能在蛋白质构象中引入显著变化从而影响周围区域。此区域也与一项更早的报导一致,所述报导显示缺失残基192-238的重组apoa-v具有削弱的结合脂质和活化脂酶活性的能力(sun等人(2006)chem.phys.lipids143,22-28;该文献以全文引用的方式并入本文中)。
对apoa-v的与高甘油三酯血症和/或cad有关的所有已知序列变体进行映射揭示残基199-259内的突变簇(图1b)。用富含α-螺旋的结构推导出apoa-v的3d模型并且预示结构富含α-螺旋(图1c)。残基199-259似乎构造成由短环连接的两个分开的α-螺旋。部分基于构造(例如合成)和测试跨越残基199-237(av199-237)与残基250-288(av250-288)的两个肽来设计后续实验。
apoa-v的3d结构尚未得到解决,因此在展开本文所描述的实施方案期间所进行的实验中,使用基于网络的服务器(phyre2)来预测3d结构,此表明残基200-245似乎折叠成α-螺旋,而不是随机未折叠结构(图2)。对序列的检验揭示螺旋打断者残基(p、g)将此结构域与蛋白质序列的其余部分分开并且将α-螺旋的末端区别开。
为寻找脂酶刺激物,采用了脂酶分析,所述脂酶分析使用由molecularprobes供应的可商购获得的荧光-tg底物(enzchek)(图3)。所述方案是由basu等人(basu等人(2011)j.lipidres.52,826-832;该文献以全文引用的方式并入本文中)改变而来,其中在ph值和洗涤剂方面有微小的修改。对于体外分析,将lpl(sigma)在制备于96孔黑色微量滴定板中的20mmtris-hcl、150mmnacl、1%bsa、0.015%zwittergent3-14(ph7.8)、1μmenzchek底物中稀释至0.12μg/ml。对于一些分析,将板在37℃下孵育10min。在synergyh1多模式读数器中使用分别为482nm和515nm的激发/发射波长进行检测。分析表明分析物对nmol/llpl敏感并且在逐渐增加的酶浓度情况下的直线表明底物浓度不具限制性。此外,可使用bodipy-c12脂肪酸来定量所制备的产物以确定酶反应的摩尔速率。因为所述分析使用无毒底物和低量的中性洗涤剂,所以有可能在活细胞情况下使用此分析(图4)。所分析的脂酶活性对从肝细胞表面移除脂酶(hl)(通过肝素预洗涤)以及在分离的脂蛋白、vldl、ldl以及hdl制剂中存在脱辅基脂蛋白两者均敏感。
实施例2
合成肽
合成(图2b)并测试了对lpl活性的影响(图5a-b)的第一种肽为av199-237。起初,当将肽添加至lpl中时,未观测到活性变化;然而,在将肽与极低密度脂蛋白(vldl)一起孵育然后添加至lpl中后,水解活性增加约4倍。对于av250-288,在存在(图5e)或不存在(图5d)vldl的情况下,观测到极小刺激活性或未观测到刺激活性。然而,在活细胞分析中,av-肽的脂酶刺激活性不需要vldl,表明所述肽直接作用于脂酶(图6和8)。在av199-237情况下的此活性增加超过了先前被报导也增加lpl活性的apoc-ii肽(c-ii50-79)情况下所见的结果。还已报导在高浓度下apoc-ii抑制脂酶活性。
av199-237在细胞培养物中也极有效地刺激脂酶活性(图6)。肝脂酶(hl)增加约3倍并且所述作用为可饱和的,这与肽作用于特定且有限集合的脂酶一致。此观测结果也为独特的,因为lpl和hl为不同的脂酶,表明与未曾对hl有影响的apoc-ii不同,apoa-v和其拟肽物可刺激lpl与hl两者。还值得注意的是,在细胞培养物中对hl的刺激持续至少75min(分析停止)。
为确定脂酶刺激功能是否可定位至更短的肽序列,产生一系列缩短的肽以在脂酶分析中进行测试(图7b、7d)。在体外lpl与细胞培养物分析两者中进行的测试均揭示av199-237可缩短5个残基并且所得av199-232肽具有完全活性并且实际上稍微更有效(图8)。
实施例3
lpl酶动力学和av199-232
研究了av199-232对lpl活性的动力学参数(例如v最大和km)的影响(图9a-b)。观测到添加vldl使lpl对底物的亲和力降低(km增加)约5倍。这是归因于vldl的apoc-iii含量。然而,添加av199-232(2.5μm)使km大体上提高几乎8倍,表明av199-232可能结合于lpl并且以变构方式刺激其活性位点。在vldl中存在apoc-iii的情况下av199-232也具功能性。比较了不同脂蛋白对lpl动力学的影响(图9d)。hdl或ldl两者均对km无显著影响。
鉴于在av199-232的由交替的极性和非极性残基组成的序列中似乎存在周期性,研究了肽折叠成两亲性α-螺旋的可能性(图10)。通过圆二色性光谱学对av199-232与av199-237两者进行分析,并且发现av199-232含有α-螺旋结构,其螺旋性质在添加肝素后有所增加证实肝素结合活性。经由计算机模拟分析也预测到高α-螺旋含量。这些数据验证了av-肽的螺旋轮状呈现的用途,所述螺旋轮状表示是用于辅助脱辅基脂蛋白中的功能性结构域组织的可视化的常用工具。将av199-232呈现为螺旋轮形式揭示3或4个离散结构域(图11)。在极性残基和非极性残基(结构域-l)被组织到螺旋的相对侧的情况下,肽的两亲性质为明显的。结构域-l负责结合于vldl。在极性侧还确定了结构域-1、结构域-2以及结构域-h。
为研究这些结构域对于脂酶活化的潜在重要性,设计了一系列肽,其中将有限集合的带电荷残基用与α-螺旋结构相容的极性不带电荷残基置换(图12)。结构域1和结构域2与av199-232活性高度相关。dom1(dom1ko;r12q/d30s)和dom2(dom2ko;k13q/k17q)中的取代使得lpl刺激活性显著降低(图13)。dom1(e34k)不影响av199-232活性,表明e34不发挥功能性作用(图13a)。doml(domlko;l10q/l21q/l29q)内的取代使得活性适度降低(图13a)。通过将增加浓度的肽施加至肝素-琼脂糖4b柱(0.2ml)来比较av199-232、dom1ko以及dom2ko的肝素结合活性(图13b)。测试这些突变肽证实结构域-1为lpl活化所必需的,并且结构域-2具有肝素结合位点并且也与lpl的活化高度相关(图13)。
结构域-h也为所关注的,因为与其他氨基酸不同,它为仅有的可在接近于细胞表面锚定脂酶处可发现的微酸性ph值下自中性变成正电荷的残基。合成将h用k置换的av199-232肽(av-h/k)并且评估其对脂酶刺激的影响(图14)。av-h/k能够在不存在vldl的情况下使lpl活性增加约1.6倍并且在vldl存在下增加约8倍,这对应于相较于av199-232活性增强44%。
图17中列出了对已设计并且针对脂酶刺激进行了测试的主要肽的概述。cd分析与经由计算机模拟预测均有力地支持了本文所描述的av-肽的高度组织化的α-螺旋结构。此结构信息已允许确定先前在av199-232中未识别的4个结构域,这与在展开本文所描述的实施方案期间所进行的实验一致,所述结构域中的两个(结构域-1和结构域-h)对于直接刺激脂酶活性来说为重要的。此外,如由在包括vldl的情况下的活性改善所证实,脂质结合域-l对活性来说也为重要的。此后一观测结果具有许多关于研制av-肽作为治疗剂的积极暗示。首先,tg通常被包装并且在vldl和其他富tg脂蛋白中循环,并且我的数据表明av-肽与这些脂蛋白缔合。其次,此脂蛋白亲和力可显著改善其体内生物可用性。最后,av-肽能够克服vldl中的apoc-iii的抑制作用并且极接近于apoc-iii可能对此活性来说为关键的。av-肽也位于活细胞系统中,并且在存在不同脂酶家族成员(例如lpl和hl)的情况下起作用的能力还指示av-肽可具有强体内存在度,并且对htg具有治疗性影响。最后,在结构域-h中将h用k取代已大体上改善av199-232肽的性能。基于在展开本文所描述的实施方案期间所进行的实验,在本文所描述的范围内的其他修饰预期可具有类似改善的性能。
实施例4
在展开本文中的实施方案期间进行实验,以证实av199-232结合vldl并且肽-脂蛋白复合物刺激lpl活性。将vldl(100μg)与av199-232(50μg)一起孵育并且在琼脂糖cl-4b柱上通过凝胶过滤将复合物与游离肽分离(图15a)。含有vldl:av199-232复合物的空隙部分(vo)在刺激lpl活性方面为有效的(图15b)。
在展开本文中的实施方案期间进行实验以确定在av-h/k肽的结构域l中的突变关键残基的作用,并且结果表明调整本文中的av肽的脂质结合阶段的取代适合用于改善脂酶刺激性能。av-h/k中的l10f和l29f取代(seqidno:23)使得脂酶刺激活性提高约2倍,而l10q、l21q以及l29q取代(seqidno:22)降低脂酶刺激活性(图16a,b)。预期l结构域中的l至f以及l至q取代分别使得与vldl的结合增加和降低。将肽(80μg/ml)与vldl(20μg/ml)一起预孵育,然后添加lpl和底物。在室温下连续监测脂酶反应持续16min(a),或者在37℃下孵育10min(b)。
实施例5
av199-232的丙氨酸扫描
在展开本文中的实施方案期间进行实验以确定av199-232的单个的残基的侧链身份的相对重要性。为此,对av199-232肽进行丙氨酸扫描,将每个残基单个地以丙氨酸残基加以置换(除了位置1、18、20以及23,这些位置已为丙氨酸),并且评估所得肽的脂酶刺激活性(图18)。脂酶刺激活性显著降低确定一个位置对于直接结合于lpl来说为重要的或者在帮助正确安置av199-232中的lpl刺激残基中发挥间接结构性作用。基于这些数据,残基大致分为三个类别:(1)用丙氨酸置换产生av199-232的>75%脂酶刺激活性的残基,(2)用丙氨酸置换产生av199-232的25-75%脂酶刺激活性的残基,以及(3)用丙氨酸置换产生av199-232的<25%脂酶刺激活性的残基。丙氨酸扫描的结果表明归入这三个类别的残基的侧链(1)与脂酶刺激最低程度相关,(2)与脂酶刺激适度相关,以及(3)与脂酶刺激高度相关。在图18中将在av199-232序列中的大多数高度相关的残基加下划线。这些结果与本文所呈现的生物化学研究(实施例2和3)、分子模型化研究(实施例6)以及生物信息学(实施例8)数据一致。
实施例6
分子模型化和3d对接
通过使用phyre2的基于同源性的模型化继之以在galaxyweb进行的模型改进来产生lpl(左)和av199-232(右)的3d结构(图19)。以两种姿态示出lpl,突出显示不同功能区域。催化三元体(s132、d156、h241)位于具有充当覆盖催化袋的盖子的相关联22残基环的”袋”中,并且在底物识别中起作用(图19,左/上)。av199-232模型被示出具有结构域l(面向下的疏水性脂质结合域)(图19,右)。
使用cluspro2.0(cluspro.bu.edu/login.php)进行分子对接实验以评估apoc-iii与lpl的结合(图20)。以条带状视图示出lpl,并且apoc-iii被示出具有呈球形形式的侧链。对于apoc-iii(pdbid:2jq3),预测对接在脂酶催化位点附近,并且apoc-iii的n端序列连接至盖序列的近端边缘。
使用cluspro2.0(cluspro.bu.edu/login.php)进行分子对接实验以评估av199-232与lpl的结合。呈现排在顶部的姿态(最高成簇数(highestclusternumber))(图21和22),示出lpl(条带(图21)或主链(图22)):av199-232(侧链球)复合物(左侧图片)。相互作用可因侧链隔开约
实施例7
体内lpl活性刺激
在展开本文中的实施方案期间进行实验以证实av-肽在刺激人类血液样品中的lpl活性中具活性,并且因此预期在体内起刺激作用。图23a证实在从新鲜人类血液分离的活白细胞中的lpl对av199-232治疗作出反应。用肝素移除细胞表面lpl使活性降低。在人类血浆存在下av-h/k也刺激lpl(图23b)。
血浆含有具有作为lpl活性的已知抑制剂的apoc-iii和angpt4的脂蛋白。然而,av199-232刺激活白细胞中的lpl活性(图23c)。在正常和脂代谢异常血浆存在下,av199-232刺激lpl活性(图23d)。将av199-232与来自正常和糖尿病/脂代谢异常血浆的全血浆一起孵育,并且然后通过peg-8000沉淀分离富tg脂蛋白(lp),并且添加至lpl分析物中(30μg/ml)。实验证实av199-232与血浆中的lpl缔合并且将其活化。
实施例8
av199-232同源性分析
由国家生物技术信息中心(nationalcenterforbiotechnologyinformation,ncbi)蛋白质数据库进行同源性检索,以确定av199-232肽序列的直系同源物,并且确定在类似序列之间不变或可允许取代的残基。使用在ncbiblastp网站上的缺省参数。表1中对结果进行了整理,以确定一组对av199-232肽中的残基适合的氨基酸取代。
表1.
以下所列和/或本文提供的所有出版物和专利是以全文引用的方式并入本文中。所描述的本发明组合物和方法的各种修改和变化对本领域技术人员来说将显而易见,而不会背离本发明的范围和精神。虽然已结合特定优选实施方案描述了本发明,但应了解如所要求的本发明不应过度受限于此类特定实施方案。实际上,对所描述的用于进行本发明的模式所进行的对相关领域熟练人员来说明显的各种修改旨在在本发明范围内。
参考文献
以下参考文献(其中一些也在上文中通过名称和/或编号进行引用)是以全文引用的方式并入本文中。
1.do,r.,etal.,(2013)commonvariantsassociatedwithplasmatriglyceridesandriskforcoronaryarterydiseasenat.genet.45,1345-1352
2.ford,e.s.,li,c.,zhao,g.,pearson,w.s.,mokdad,a.h.(2009)hypertriglyceridemiaanditspharmacologictreatmentamongusadults.arch.intern.med.169,572-578
3.christian,j.b.,bourgeois,n.,snipes,r.,lowe,k.a.(2011)prevalenceofsevere(500to2,000mg/dl)hypertriglyceridemiainunitedstatesadults.am.j.cardiol.107,891-897
4.pennacchio,l.a.,olivier,m.,hubacek,j.a.,cohen,j.c.,cox,d.r.,fruchart,j.c.,krauss,r.m.,rubin,e.m.(2001)anapolipoproteininfluencingtriglyceridesinhumansandmicerevealedbycomparativesequencing.science294,169-173
5.vandervliet,h.n.,sammels,m.g.,leegwater,a.c.,levels,j.h.,reitsma,p.h.,boers,w.,chamuleau,r.a.(2001)apolipoproteina-v:anovelapolipoproteinassociatedwithanearlyphaseofliverregeneration.j.biol.chem.276,44512-44520
6.o′brien,p.j.,alborn,w.e.,sloan,j.h.,ulmer,m.,boodhoo,a.,knierman,m.d.,schultze,a.e.,konrad,r.j.(2005)thenovelapolipoproteina5ispresentinhumanserum,isassociatedwithvldl,hdl,andchylomicrons,andcirculatesatverylowconcentrationscomparedwithotherapolipoproteins.clin.chem.51,351-359
7.olofsson,s.o.(2005)apoa-v:theregulationofaregulatorofplasmatriglycerides.arterioscler.thromb.vasc.biol.25,1097-1099
8.fruchart-najib,j.,bauge,e.,niculescu,l.s.,pham,t.,thomas,b.,rommens,c.,majd,z.,brewer,b.,pennacchio,l.a.,fruchart,j.c.(2004)mechanismoftriglycerideloweringinmiceexpressinghumanapolipoproteina5.biochem.biophys.res.commun.319,397-404
9.schaap,f.g.,rensen,p.c.,voshol,p.j.,vrins,c.,vandervliet,h.n.,chamuleau,r.a.,havekes,l.m.,groen,a.k.,vandijk,k.w.(2004)apoavreducesplasmatriglyceridesbyinhibitingverylowdensitylipoprotein-triglyceride(vldl-tg)productionandstimulatinglipoproteinlipase-mediatedvldl-tghydrolysis.j.biol.chem.279,27941-27947
10.sarwar,n.,sandhu,m.s.,ricketts,s.l.,butterworth,a.s.,di,a.e.,boekholdt,s.m.,ouwehand,w.,watkins,h.,samani,n.j.,saleheen,d.,lawlor,d.,reilly,m.p.,hingorani,a.d.,talmud,p.j.,danesh,j.(2010)triglyceride-mediatedpathwaysandcoronarydisease:collaborativeanalysisof101studies.lancet375,1634-1639
11.nilsson,s.k.,heeren,j.,olivecrona,g.,merkel,m.(2011)apolipoproteina-v,apotenttriglyceridereducer.atherosclerosis219,15-21
12.pennacchio,l.a.,olivier,m.,hubacek,j.a.,krauss,r.m.,rubin,e.m.,cohen,j.c.(2002)twoindependentapolipoproteina5haplotypesinfluencehumanplasmatriglyceridelevels.hum.mol.genet.11,3031-3038
13.charriere,s.,bernard,s.,aqallal,m.,merlin,m.,billon,s.,perrot,l.,le,c.e.,sassolas,a.,moulin,p.,marcais,c.(2008)associationofapoa5-1131t>cands19wgenepolymorphismswithbothmildhypertriglyceridemiaandhyperchylomicronemiaintype2diabeticpatients.clin.chim.acta394,99-103
14.talmud,p.j.,martin,s.,taskinen,m.r.,frick,m.h.,nieminen,m.s.,kesaniemi,y.a.,pasternack,a.,humphries,s.e.,syvanne,m.(2004)apoa5genevariants,lipoproteinparticledistribution,andprogressionofcoronaryheartdisease:resultsfromthelocatstudy.j.lipidres.45,750-756
15.priore,o.c.,pisciotta,l.,li,v.g.,sambataro,m.p.,cantafora,a.,bellocchio,a.,catapano,a.,tarugi,p.,bertolini,s.,calandra,s.(2005)inheritedapolipoproteina-vdeficiencyinseverehypertriglyceridemia.arterioscler.thromb.vasc.biol.25,411-417
16.priore,o.c.,carubbi,f.,schaap,f.g.,bertolini,s.,calandra,s.(2008)hypertriglyceridaemiaandlowplasmahdlinapatientwithapolipoproteina-vdeficiencyduetoanovelmutationintheapoa5gene.j.intern.med.263,450-458
17.tang,y.,sun,p.,guo,d.,ferro,a.,ji,y.,chen,q.,fan,l.(2006)ageneticvariantc.553g>tintheapolipoproteina5geneisassociatedwithanincreasedriskofcoronaryarterydiseaseandalteredtriglyceridelevelsinachinesepopulation.atherosclerosis185,433-437
18.pullinger,c.r.,aouizerat,b.e.,movsesyan,i.,durlach,v.,sijbrands,e.j.,nakajima,k.,poon,a.,dallinga-thie,g.m.,hattori,h.,green,l.l.,kwok,p.y.,havel,r.j.,frost,p.h.,malloy,m.j.,kane,j.p.(2008)anapolipoproteina-vgenesnpisassociatedwithmarkedhypertriglyceridemiaamongasian-americanpatients.j.lipidres.49,1846-1854
19.sharma,v.,witkowski,a.,witkowska,h.e.,dykstra,a.,simonsen,j.b.,nelbach,l.,beckstead,j.a.,pullinger,c.r.,kane,j.p.,malloy,m.j.,watson,g.,forte,t.m.,ryan,r.o.(2014)aberranthetero-disulfidebondformationbythehypertriglyceridemia-associatedp.gly185cysapoa5variant(rs2075291).arterioscler.thromb.vasc.biol.34,2254-2260
20.nilsson,s.k.,lookene,a.,beckstead,j.a.,gliemann,j.,ryan,r.o.,olivecrona,g.(2007)apolipoproteina-vinteractionwithmembersofthelowdensitylipoproteinreceptorgenefamily.biochemistry46,3896-3904
21.sun,g.,bi,n.,li,g.,zhu,x.,zeng,w.,wu,g.,xue,h.,chen,b.(2006)identificationoflipidbindingandlipoproteinlipaseactivationdomainsofhumanapoav.chem.phys.lipids143,22-28
22.basu,d.,manjur,j.,jin,w.(2011)determinationoflipoproteinlipaseactivityusinganovelfluorescentlipaseassay.j.lipidres.52,826-832
序列表
<110>芝加哥大学
<120>合成肽
<130>uchi-34207/tw-1/ord
<150>us62/082,902
<151>2014-11-21
<160>29
<170>patentin版本3.5
<210>1
<211>343
<212>prt
<213>智人
<400>1
arglysglyphetrpasptyrpheserglnthrserglyasplysgly
151015
argvalgluglnilehisglnglnlysmetalaarggluproalathr
202530
leulysaspserleugluglnaspleuasnasnmetasnlyspheleu
354045
glulysleuargproleuserglyserglualaproargleuprogln
505560
aspprovalglymetargargglnleuglnglugluleuglugluval
65707580
lysalaargleuglnprotyrmetalaglualahisgluleuvalgly
859095
trpasnleugluglyleuargglnglnleulysprotyrthrmetasp
100105110
leumetgluglnvalalaleuargvalglngluleuglngluglnleu
115120125
argvalvalglygluaspthrlysalaglnleuleuglyglyvalasp
130135140
glualatrpalaleuleuglnglyleuglnserargvalvalhishis
145150155160
thrglyargphelysgluleuphehisprotyralagluserleuval
165170175
serglyileglyarghisvalglngluleuhisargservalalapro
180185190
hisalaproalaserproalaargleuserargcysvalglnvalleu
195200205
serarglysleuthrleulysalalysalaleuhisalaargilegln
210215220
glnasnleuaspglnleuargglugluleuserargalaphealagly
225230235240
thrglythrglugluglyalaglyproaspproglnmetleuserglu
245250255
gluvalargglnargleuglnalapheargglnaspthrtyrleugln
260265270
ilealaalaphethrargalaileaspglngluthrglugluvalgln
275280285
glnglnleualaproproproproglyhisseralaphealaproglu
290295300
pheglnglnthraspserglylysvalleuserlysleuglnalaarg
305310315320
leuaspaspleutrpgluaspilethrhisserleuhisaspglngly
325330335
hisserhisleuglyasppro
340
<210>2
<211>60
<212>prt
<213>智人
<400>2
prohisalaproalaserproalaargleuserargcysvalglnval
151015
leuserarglysleuthrleulysalalysalaleuhisalaargile
202530
glnglnasnleuaspglnleuargglugluleuserargalapheala
354045
glythrglythrglugluglyalaglyproasppro
505560
<210>3
<211>39
<212>prt
<213>智人
<400>3
alaargleuserargcysvalglnvalleuserarglysleuthrleu
151015
lysalalysalaleuhisalaargileglnglnasnleuaspglnleu
202530
argglugluleuserargala
35
<210>4
<211>29
<212>prt
<213>智人
<400>4
serarglysleuthrleulysalalysalaleuhisalaargilegln
151015
glnasnleuaspglnleuargglugluleuserargala
2025
<210>5
<211>34
<212>prt
<213>智人
<400>5
alaargleuserargcysvalglnvalleuserarglysleuthrleu
151015
lysalalysalaleuhisalaargileglnglnasnleuaspglnleu
202530
argglu
<210>6
<211>32
<212>prt
<213>智人
<400>6
leuserargcysvalglnvalleuserarglysleuthrleulysala
151015
lysalaleuhisalaargileglnglnasnleuaspglnleuargglu
202530
<210>7
<211>28
<212>prt
<213>智人
<400>7
valglnvalleuserarglysleuthrleulysalalysalaleuhis
151015
alaargileglnglnasnleuaspglnleuargglu
2025
<210>8
<211>26
<212>prt
<213>智人
<400>8
alaargleuserargcysvalglnvalleuserarglysleuthrleu
151015
lysalalysalaleuhisalaargilegln
2025
<210>9
<211>34
<212>prt
<213>人工序列
<220>
<223>突变野生型肽
<400>9
alaargleuserargcysvalglnvalleuserglnlysleuthrleu
151015
lysalalysalaleuhisalaargileglnglnasnleuserglnleu
202530
argglu
<210>10
<211>34
<212>prt
<213>人工序列
<220>
<223>突变野生型肽
<400>10
alaargleuserargcysvalglnvalleuserargglnleuthrleu
151015
glnalalysalaleuhisalaargileglnglnasnleuaspglnleu
202530
argglu
<210>11
<211>34
<212>prt
<213>人工序列
<220>
<223>突变野生型肽
<400>11
alaargleuserargcysvalglnvalleuserarglysleuthrleu
151015
lysalalysalaleuglnalaargileglnglnasnleuaspglnleu
202530
argglu
<210>12
<211>34
<212>prt
<213>人工序列
<220>
<223>突变野生型肽
<400>12
alaargleuserargcysvalglnvalleuserarglysleuthrleu
151015
lysalalysalaleulysalaargileglnglnasnleuaspglnleu
202530
argglu
<210>13
<211>34
<212>prt
<213>人工序列
<220>
<223>突变野生型肽
<400>13
alaargleuserargalavalglnvalleuserarglysleuthrleu
151015
lysalalysalaleulysalaargileglnglnasnleuaspglnleu
202530
argglu
<210>14
<211>34
<212>prt
<213>人工序列
<220>
<223>突变野生型肽
<400>14
alaargleuserargalavalglnvalleuserargargleuthrleu
151015
glnalalysalaleuhisalalysileglngluasnleuaspaspleu
202530
argglu
<210>15
<211>34
<212>prt
<213>人工序列
<220>
<223>突变野生型肽
<220>
<221>杂项特征
<222>(13)..(13)
<223>xaa=任何氨基酸
<220>
<221>杂项特征
<222>(17)..(17)
<223>xaa=任何氨基酸
<220>
<221>杂项特征
<222>(22)..(22)
<223>xaa=任何氨基酸
<400>15
alaargleuserargcysvalglnvalleuserargxaaleuthrleu
151015
xaaalalysalaleuxaaalaargileglnglnasnleuaspglnleu
202530
argglu
<210>16
<211>34
<212>prt
<213>人工序列
<220>
<223>突变野生型肽
<220>
<221>杂项特征
<222>(13)..(13)
<223>xaa=任何氨基酸
<220>
<221>杂项特征
<222>(17)..(17)
<223>xaa=任何氨基酸
<220>
<221>杂项特征
<222>(22)..(22)
<223>xaa=任何氨基酸
<400>16
alaargleuserargcysvalglnvalleuserargxaaleuthrleu
151015
xaaalalysalaleuxaaalaargileglnglnasnleuaspglnleu
202530
argglu
<210>17
<211>34
<212>prt
<213>人工序列
<220>
<223>突变野生型肽
<220>
<221>杂项特征
<222>(13)..(13)
<223>xaa=k或q
<220>
<221>杂项特征
<222>(17)..(17)
<223>xaa=k或q
<220>
<221>杂项特征
<222>(22)..(22)
<223>xaa=h、k或q
<400>17
alaargleuserargcysvalglnvalleuserargxaaleuthrleu
151015
xaaalalysalaleuxaaalaargileglnglnasnleuaspglnleu
202530
argglu
<210>18
<211>93
<212>prt
<213>智人
<400>18
proalaserproalaargleuserargcysvalglnvalleuserarg
151015
lysleuthrleulysalalysalaleuhisalaargileglnglnasn
202530
leuaspglnleuargglugluleuserargalaphealaglythrgly
354045
thrglugluglyalaglyproaspproglnmetleuserglugluval
505560
argglnargleuglnalapheargglnthrtyrleuglnilealaala
65707580
phethrargalaileaspglngluthrglugluvalgln
8590
<210>19
<211>39
<212>prt
<213>智人
<400>19
aspproglnmetleuserglugluvalargglnargleuglnalaphe
151015
argglnaspthrtyrleuglnilealaalaphethrargalaileasp
202530
glngluthrglugluvalgln
35
<210>20
<211>32
<212>prt
<213>智人
<400>20
alaargleuserargcysvalglnvalleuserarglysleuthrleu
151015
lysalalysalaleuhisalaargileglnglnasnleuaspglnleu
202530
<210>21
<211>34
<212>prt
<213>人工序列
<220>
<223>突变野生型肽
<400>21
valglnhisalacyslysargleuasplysserargalaleuserarg
151015
leuleuleuthrleuargglngluleuarglysglnalaasnvalgln
202530
alaile
<210>22
<211>34
<212>prt
<213>人工序列
<220>
<223>突变野生型肽
<400>22
alaargleuserargcysvalglnvalglnserarglysleuthrgln
151015
lysalalysalaleulysalaargileglnglnasnglnaspglnleu
202530
argglu
<210>23
<211>34
<212>prt
<213>人工序列
<220>
<223>突变野生型肽
<400>23
alaargleuserargcysvalglnvalpheserarglysleuthrleu
151015
lysalalysalaleulysalaargileglnglnasnpheaspglnleu
202530
argglu
<210>24
<211>34
<212>prt
<213>人工序列
<220>
<223>突变野生型肽
<400>24
alaargleuserargcysvalglnvalleuserarglysleuthrleu
151015
lysalalysalaleuhisalaargileglnglnasnleuaspglnleu
202530
arglys
<210>25
<211>34
<212>prt
<213>人工序列
<220>
<223>突变野生型肽
<400>25
alaargleuserargcysvalglnvalglnserarglysleuthrleu
151015
lysalalysalaglnhisalaargileglnglnasnglnaspglnleu
202530
argglu
<210>26
<211>34
<212>prt
<213>人工序列
<220>
<223>突变野生型肽
<400>26
alaargleuserargservalglnvalpheserarglysleuthrleu
151015
lysalalysalaleulysalaargileglnglnasnpheaspglnleu
202530
argglu
<210>27
<211>34
<212>prt
<213>人工序列
<220>
<223>突变野生型肽
<400>27
alaargleuserargcysvalglnvalpheserarglysleuthrleu
151015
lysalalysalaleulysalaargileglnglnasnpheaspglnleu
202530
argglu
<210>28
<211>34
<212>prt
<213>人工序列
<220>
<223>突变野生型肽
<220>
<221>杂项特征
<222>(12)..(12)
<223>xaa=高精氨酸
<400>28
alaargleuserargcysvalglnvalpheserxaalysleuthrleu
151015
lysalalysalaleulysalaargileglnglnasnpheaspglnleu
202530
argglu
<210>29
<211>34
<212>prt
<213>人工序列
<220>
<223>突变野生型肽
<220>
<221>杂项特征
<222>(3)..(3)
<223>xaa=l、f、y或w
<220>
<221>杂项特征
<222>(4)..(4)
<223>xaa=s、t、n或g
<220>
<221>杂项特征
<222>(5)..(5)
<223>xaa=r、k、高赖氨酸或高精氨酸
<220>
<221>杂项特征
<222>(6)..(6)
<223>xaa=c、s、t、n、q、y或h
<220>
<221>杂项特征
<222>(7)..(7)
<223>xaa=v、f、y或w
<220>
<221>杂项特征
<222>(10)..(10)
<223>xaa=l、f、y或w
<220>
<221>杂项特征
<222>(12)..(12)
<223>xaa=r、k、hlys或harg
<220>
<221>杂项特征
<222>(13)..(13)
<223>xaa=k、r、harg、hlys或orn
<220>
<221>杂项特征
<222>(14)..(14)
<223>xaa=l、f、y或w
<220>
<221>杂项特征
<222>(17)..(17)
<223>xaa=k、r、harg、hlys或orn
<220>
<221>杂项特征
<222>(18)..(18)
<223>xaa=a、f、y或w
<220>
<221>杂项特征
<222>(19)..(19)
<223>xaa=r、k、hlys或harg
<220>
<221>杂项特征
<222>(21)..(21)
<223>xaa=l、f、y或w
<220>
<221>杂项特征
<222>(22)..(22)
<223>xaa=h、k、hlys、r、harg或orn
<220>
<221>杂项特征
<222>(25)..(25)
<223>xaa=i、f、y或w
<220>
<221>杂项特征
<222>(29)..(29)
<223>xaa=l、f、y或w
<220>
<221>杂项特征
<222>(32)..(32)
<223>xaa=l、f、y或w
<400>29
alaargxaaxaaxaaxaaxaaglnvalxaaserxaaxaaxaathrleu
151015
xaaxaaxaaalaxaaxaaalaargxaaglnglnasnxaaaspglnxaa
202530
argglu
- 还没有人留言评论。精彩留言会获得点赞!