用于有效的生育三烯酚递送的制剂的制作方法
本发明总体上涉及用于脂溶性物质的制剂。更具体地,本发明涉及一种用于改善生育三烯酚异构体的递送的自乳化药物递送制剂。
背景技术:
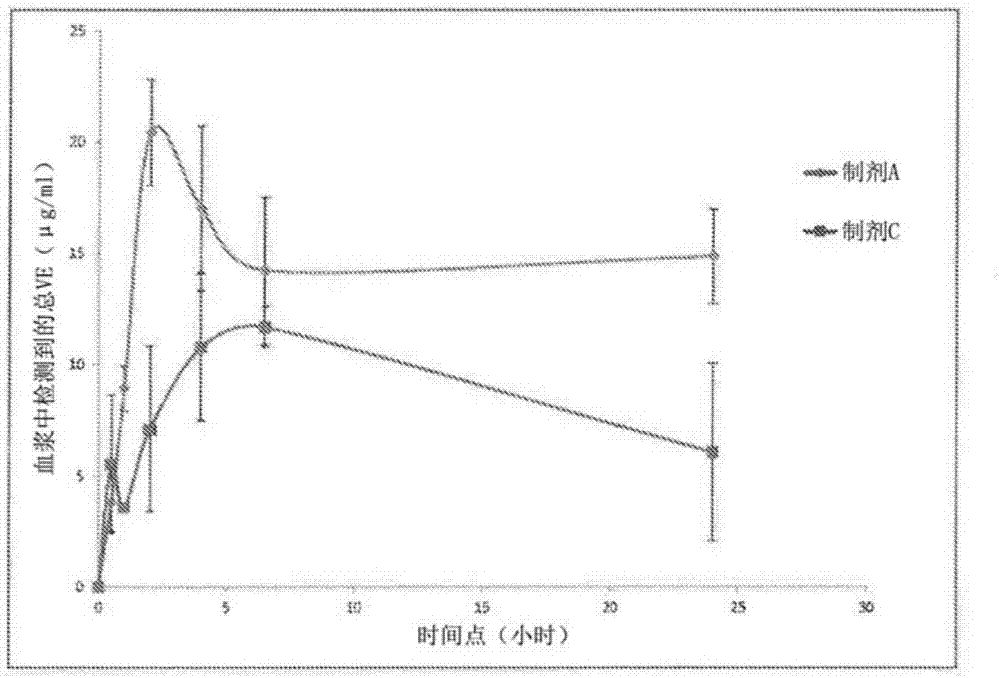
:维生素e是通常在植物和种子中发现的具有独特的抗氧化活性的八种相关脂溶性化合物(即生育酚的四种异构体和生育三烯酚的四种异构体)的家族的统称。生育酚和生育三烯酚亚家族各自由具有不同水平的生物活性的α、β、γ和δ组成。研究表明,抗氧化剂保护细胞免受自由基的破坏作用,该自由基是含有未配对电子的分子,并且已知有助于癌症和心血管疾病的发展。因此,维生素e成为一种在人体内起到抗氧化剂作用以预防疾病和促进健康的重要的脂溶性营养素。以前,α-生育酚一直被认为是最活性的形式。但是,近年来的科学研究清楚地表明,生育三烯酚不同于通常使用的维生素e形式(即α-生育酚),并赋予其更强且经常相对生育酚独特的特性。生育三烯酚通过血流分布在整个人体中,其中在口服给药后在包括脑、心脏、皮肤、心肌、肝脏和脂肪组织的多种身体组织中发现特定累积。因此,近来的进展表明,由于具有强大的神经保护作用、肿瘤抑制效果和降低胆固醇特性,天然维生素e的生育三烯酚亚家族是比生育酚亚家族更好的抗氧化剂。人体通过胆盐和胆汁酸的分泌将脂肪和油增溶成胶束,随后通过脂肪酶消化而在胃肠系统中吸收脂肪和油。在这种吸收过程存在高的个体间差异,从而导致不同人之间的不同剂量。此外,胆盐和胆汁酸的分泌是依赖性的并且由脂肪饮食刺激,其可以在所消耗的不同餐食之间很大地不同。像所有的脂溶性营养素和膳食脂类一样,生育三烯酚的口服吸收是低的、高度可变的并取决于制剂参数。为了规避这种可变因素和实现包括维生素e生育三烯酚的基于脂肪的维生素和药物的持续不变的高量吸收,使用不同类型的表面活性剂和油载体已经开发了自乳化药物递送系统(sedds)。富含生育三烯酚的棕榈来源的维生素e的现有sedds发明能够主要递送维生素e的α-生育酚异构体。此外,这种递送是以生育三烯酚异构体为代价的,生育三烯酚异构体的抗氧化活性可以达到生育酚的抗氧化活性的40倍至60倍。因此,存在提供一种具有相对于α-生育酚优先增加生育三烯酚异构体的口服生物利用度的有效制剂的自乳化递送系统的需要。本发明的自乳化制剂提供了一种具有持续不变且增强的生育三烯酚异构体水平的有用的给药方式,在与膳食脂肪不相关的口服摄取时,其在体内被吸收。技术实现要素:本发明公开了一种以自乳化药物递送制剂形式的制剂,其示出在口服摄取时增强的生育三烯酚异构体的生物利用度。本发明的制剂包含脂溶性化合物、有效量的乳化剂组合和油载体。本发明的上述方面和其他方面、优点以及新颖特征将从本发明的以下详细描述变得明显。附图说明图1示出了在口服给药具有不同乳化剂的自乳化制剂a和制剂b后所获得的血浆浓度随时间的变化曲线;图2例示了在口服给药具有不同油载体的自乳化制剂a和制剂c后所获得的血浆浓度随时间的变化曲线;图3示出了在口服给药具有不同油载体的自乳化制剂a和制剂d后所获得的血浆浓度随时间的变化曲线;以及图4a至4d是示出了制剂a和制剂e的多种维生素e(ve)异构体的口服生物利用度的曲线图。具体实施方式本发明描述了一种用于脂溶性药物的自乳化药物递送系统(sedds)的制剂,其具有生育三烯酚的增强的口服生物利用度和持续不变的高量吸收。当与水性环境接触或体内给药时该制剂自发地形成乳状液。自乳化药物递送系统(sedds)是油和表面活性剂的混合物,并且已被广泛地用于包括维生素e生育三烯酚的基于脂肪的制剂。sedds在暴露于具有温和搅拌(诸如胃或小肠的活动)的胃肠液时将形成水包油乳状液。因此,sedds可以有效地提供在吸收和口服生物利用度方面的改善。为了实现持续不变地高水平的维生素e生育三烯酚,油载体和乳化剂的正确组合的选择对于sedds的制剂是重要且关键的要素,这是因为在多种油和乳化剂以及乳化剂比例中确定了来自sedds的基于脂肪的维生素和药物化合物的溶解性和口服吸收效率。乳化剂和油载体对于提供自乳化制剂是有用的赋形剂。在脂质体系中难溶性药物的溶解度可以通过将维生素e与可接受的油载体混合而大大提高,并且维生素e和油载体的混合物可以用乳化剂(诸如非离子表面活性剂)容易地乳化。一种或多种非离子表面活性剂对于在水性环境中立即形成水包油液滴和提供自乳化过程是必需的。表面活性剂包括疏水性组分(油溶性)和亲水性组分(水溶性),并且由它们的亲水-亲油平衡值(hlb)来表征。在水与油混合的情况下,它们通过吸附在油和水之间的界面处而降低油和水之间的界面张力。当将该表面活性剂与水性流体接触时该表面活性剂能够形成稳定的乳状液。各种药学上可接受的表面活性剂都适合于在本发明中使用。通常,适用于本发明的表面活性剂是非离子表面活性剂,例如,聚乙氧基化蓖麻油(polyoxylatedcastoroil)(商品名为克列莫佛(聚氧乙烯蓖麻油,cremophor))、脂肪酸的聚乙氧基化甘油酯(polyoxylatedglyceridesoffatteracid)、聚氧乙烯山梨糖醇酐脂肪酸酯(聚氧乙烯失水山梨醇脂肪酸酯,polyoxyethylenesorbitanfattyacidester)、山梨糖醇酐脂肪酸酯、蔗糖脂肪酸酯(sucrosefattyacidester)、卵磷脂、皂角苷等或者它们的混合物。聚氧乙烯山梨糖醇酐脂肪酸酯可包括聚山梨醇酯(polysorbate),例如,聚山梨醇酯20、聚山梨醇酯40、聚山梨醇酯60和聚山梨醇酯80。山梨糖醇酐脂肪酸酯或山梨糖醇酐酯(sorbitanester)可以包括山梨糖醇酐单月桂酸酯(sorbitanmonolaurate)(司盘20)、山梨糖醇酐单棕榈酸酯(司盘40)、山梨糖醇酐单硬脂酸酯(司盘60)和山梨糖醇酐单油酸酯(司盘80)。本文中使用的卵磷脂由磷酸、胆碱、脂肪酸、甘油、糖脂(glycolipid)、甘油三酯和磷脂(例如,磷脂酰胆碱(phosphatidylcholine)、磷脂酰乙醇胺和磷脂酰肌醇)组成。本文所用的蔗糖脂肪酸酯由作为亲水基团的蔗糖和作为亲脂性基团的脂肪酸组成,并且通常被称为糖酯(sugarester)。由于蔗糖具有总共8个羟基,所以可以产生从蔗糖单脂肪酸酯变化至蔗糖八脂肪酸酯的化合物。皂角苷是一类在多种植物种类中特别大量发现的化学化合物。更具体地,它们是在现象上通过在水性溶液中振荡时它们产生的皂样泡沫以及在结构上通过具有一个或多个与亲脂性三萜衍生物组合的亲水糖苷部分来分组的两亲糖苷(amphipathicglycoside)。脂肪酸阻止了该制剂的成分之间的相分离。合适的脂肪酸的实例包括,但不限于,油酸、棕榈酸、硬脂酸等或它们的混合物。脂肪酸的加入提高了该制剂的溶解度。在优选的实施方式中,该制剂可以通过将富含生育三烯酚的维生素e的脂溶性化合物、乳化剂和油载体组合来实现,以获得改善的制剂。进行检验以比较在口服给药具有不同的乳化剂和油载体的自乳化制剂后维生素e的生物利用度。如下所示,在表1中描述了制剂a、b、c、d和e,其总结了所检验的每种制剂的组成。表1本发明的制剂a典型地包含按重量计约5%至60%的维生素e、按重量计约10%至60%的乳化剂和按重量计约0%至70%的油载体。在优选的实施方式中,制剂a包含按重量计约10%至约50%的维生素e、按重量计约15%至约45%的山梨糖醇酐单月桂酸酯(司盘20)与聚氧乙烯山梨糖醇酐20单油酸酯或聚山梨醇酯80(吐温80)的乳化剂组合,以及约6%至约56%(重量)的甘油酯油载体,所述甘油酯油载体为三油酸甘油酯(甘油三油酸酯,glyceroltrioleate)(gto)油。gto油中主要甘油三酸酯(tg),三油精(triolein)(ooo,c18:1)的水平是显著高的,其含量是gto油的重量的大约55%至约99%。在优选的实施方式中,gto油以gto油重量的约65%至85%的量含有三油精(ooo,c18:1)。类似地,司盘-20与吐温80的比是可变的,并且通常包含约1:1至约1:20。制剂a的司盘-20与吐温80的优选的最佳比为约1:2至约1:8。表2示出了多种制剂的维生素e(ve)异构体的分解(breakdown)百分比w/w。基本上,维生素e的分布在多种制剂之间是相似的。表2中的标号a和e表示如上在表1中所描述的制剂。表2制剂α-tp(%)α-t3(%)γ-t3(%)δ-t3(%)总ve(%)a5.44.56.93.220e4.75.36.53.520以每千克大鼠体重300mg维生素e的方式,一组大鼠用制剂a口服给药,而另一组大鼠用制剂b给药。制剂之间的差异是在制剂a中存在乳化剂的共混物而在制剂b中不存在。在给药后0.5小时、1小时、2小时、4小时、6.5小时和24小时从大鼠抽取血液样品。从血液样品提取血浆并且进行分析。在图1中示出了制剂a和制剂b的血浆中所检测的总ve随时间的变化曲线。该数据示出,来自用具有司盘-20和吐温80的乳化剂组合的制剂a给药的大鼠组的血液样品的血浆中所检测的总ve显著高于制剂b,并且维持了更长的时间,因此提供了维生素e的持续不变的高量吸收。制剂a的曲线下面积(auc)是制剂b的曲线下面积的约1.8倍。然后,关于不同油对维生素e吸收的影响比较了三种不同的油载体。在该研究中,以每千克大鼠体重300mg维生素e的方式,一组大鼠用制剂a口服给药,而另一组大鼠物用制剂c或d给药。制剂之间的差异是在制剂a中使用的油载体是gto并且在制剂c中使用的油载体是橄榄油,而在制剂d中使用的油载体是大豆油。在给药后0.5小时、1小时、2小时、4小时、6.5小时和24小时从大鼠抽取血液样品。从血液样品提取血浆并分析。在图2中示出了制剂a和制剂c的血浆中所检测的总ve随时间的变化曲线,而在图3中示出了制剂a和制剂d的血浆中所检测的总ve随时间的变化曲线。该数据示出,来自用具有gto油载体的制剂a给药的大鼠组的血液样品的血浆中所检测的总ve高于制剂c和制剂d二者。因此,油载体在提高体内维生素e吸收方面起重要作用。制剂a的曲线下面积(auc)是制剂c和制剂d的曲线下面积的约1.6倍。制备另外的制剂以用于与制剂a比较,即描述为制剂e的市售软明胶胶囊(美国专利6,596,306)。制剂e是据称在提供体内较好的口服吸收的sedds中递送脂溶性药物(包括生育酚、生育三烯酚、维生素a、维生素d和β-胡萝卜素)的制剂。图4a至4d示出了分别用于制剂a和制剂e的α-生育酚、α-生育三烯酚、γ-生育三烯酚和δ-生育三烯酚的不同ve异构体的分解。该数据示出,与制剂e相比,制剂a在血浆中递送了水平高得多的生育三烯酚异构体(α、γ和δ)。当比较这两种制剂时,差异的范围从约3倍(γ-生育三烯酚)至约5倍(δ-生育三烯酚)的更高的吸收。总体而言,很显然的是,制剂a递送了水平高得多的生育三烯酚异构体,而制剂e递送了稍微更高水平的α-生育酚。该制剂可被制成粉末形式、片剂或被填充到胶囊或明胶胶囊(包括软壳胶囊和硬壳胶囊)中、食品和饮料、乳剂体系等。该制剂优选地被口服给药。然而,该制剂还可以以其他形式用于局部的、肠胃外的、直肠的、鞘内的、腹膜内的或静脉内的输注。生育三烯酚的优选来源是谷类(诸如稻、大麦、燕麦、小麦和黑麦),以及植物油(诸如棕榈油和米糠油)。虽然已经关于优选的实施方式具体示出和描述了所公开的制剂,但本领域技术人员应当理解的是,在不偏离本发明的范围的情况下,可以在形式和细节上进行各种修改。因此,本发明包括在关于所附的权利要求书中所列举的主题的所有修改和等同物。此外,除非在此另有说明或与上下文明显矛盾,否则在其所有可能变型中的上述要素的任何组合都被本发明所涵盖。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1