表面具有富银纳米多层膜修饰的椎间融合器及制备方法与流程
本发明属于医用材料领域,更具体地说,适用一种医用手术植入物,特别是一种表面具有富银纳米多层膜修饰的椎间融合器及制备方法。
背景技术:
作为脊柱外科的一项重要技术,椎体间融合术是在该领域尤其是退行性脊柱疾病的治疗中发挥了不可替代的作用。退行性脊椎疾病和外伤性椎体滑脱会导致的疼痛与节段性不稳等问题,脊椎疾病已成为骨科常见疾病,对于这类疾病:切除病变的椎间盘,植入椎间融合器的融合手术是最有效的临床解决方案。椎间融合器于1992年进行腰椎临床试验至今己在腰椎手术中广为应用,近年来,已开始在颈椎外科中的应用。开发初始稳定性好,可为骨性融合提供尽可能好的生物环境和生物力学条件,并减少使用融合器相关的不良反应的椎间融合器是研究的目标。当金属材料植入体内后,由于生理环境的腐烛会造成金属离子向周围组织扩散,以及植入材料自身性质的退变,可能会导致毒副作用以致植入假体的松动甚至失效;另外,椎间融合器植入体内后,必然会发生磨损,产生大量的微粒子,引起一系列不良反应,组织细胞吞嚼并消化释放出的粒子形成肉芽肿瘤或类似肉芽肿瘤的组织,在植入体和骨的结合处,由于骨特性的变化会引发骨溶现象,继而引起假体的松动甚至失效。基于以上问题,在保留金属原有优良性能的基础上,对金属表面进行纳米多层膜改性,以有效提高其表面的各种性能,如生物相容性、生物活性、耐磨性、耐腐烛性和抗菌性等,从而改善植入体的功效和使用寿命,特别是减少不良反应的发生,具有重要的临床意义。
纳米多层膜机械、力学以及与基底材料结合性能远高于单层膜引起了体内植入物开发者与临床的极大关注,这种结构可以有效地调整膜中的位错和缺陷及其运动,从而获得高硬度、高模量等性能。通常运用纳米多层镀技术得到的高硬薄膜大多用在工业切割、干磨设备中,该技术应用体内植入器械中的研究起步较晚,特别是在椎间融合器中的应用属于首次。
此外,就椎间融合器植入物而言,虽然全身使用抗生素足以预防术后感染的发生,但是对于植入物相关的感染,单纯地全身使用抗生素,对于细菌在植入物表面和周围组织的定植是不够的。如果细菌定植于假体表面,那么即使使用全身预防性抗生素,对于感染的形成仍是没有作用的。目前也没有好的措施来减轻细菌感染,而摘除植入体通常是解决这一问题唯一有效的方法。总起来讲,植入体/组织界面上生物膜的形成和损伤的免疫系统使得金属植入体更容易细菌的粘附和进一步的感染。因为不可能完全除去细菌污染,所以研发能够阻止植入体相关感染的有效防范措施迫在眉睫。在植入体表面对周围组织的感染过程中,细菌在生物材料界面的最初贴壁是关键的一步,因此对金属基生物材料进行改性使其自身带有灭菌消炎功能,防止植入体表面的最初细菌附着是一重要策略。
因此,现有金属制椎间隔合器使用过程中存在生物相容性、生物活性、耐磨性、耐腐烛性和抗菌性等问题,改善椎间融合器的功效和使用寿命,特别是减少不良反应的发生,具有重要的临床意义。
技术实现要素:
本发明的目的在于克服上述金属制椎间融合器的不足,而提供一种表面具有富银纳米多层膜修饰的椎间融合器以及它的制备方法。本发明采用纳米多层镀技术,在钛合金椎间隔合器表面沉积表面富银的纳米多层膜(TiN/Ag纳米多层膜或DLC/Ag纳米多层膜),从而提高椎间融合器表面的硬度,耐磨性,耐腐蚀性和生物相容性,以及降低椎间融合器表面与固定端骨骼的微动摩损磨损引起松动与表面涂层的脱落等风险。
本发明为解决上述问题提供了一种表面具有富银纳米多层膜修饰的椎间融合器。其特征在于所述椎间融合器是在钛合金材料的椎间融合器表面运用物理气相沉积技术与离子注入技术覆盖表面富银的纳米多层膜;所述富银的纳米多层膜为在钛合金材料的椎间融合器表面注入氮化钛/银(TiN/Ag)或者类金刚石/银(DLC/Ag)纳米多层膜,并再在多层膜的表面注入银离子;所述多层膜整体厚度为500~1000nm。
所述物理气相沉积技术包括:离子束辅助沉积、磁控溅射或离子镀技术;所述离子注入技术包括:金属蒸汽弧源或等离子浸没技术。
本发明的具有富银纳米多层膜修饰的椎间融合器是通过以下方法制备的:
(1)表面预处理:经过切割打磨的钛合金制椎间融合器,依次经过丙酮和乙醇超声清洗15分钟,吹干后立即送入真空沉积室中;
(2)离子溅射清洗:在沉积薄膜以前,先用束流4-10mA用Ar+对椎间融合器表面进行离子溅射清洗5-10min;
(3)沉积纳米多层膜:将高纯度(大于为99.95%)的Ti靶和Ag靶交替地旋转至沉积位置制备TiN/Ag纳米多层膜,或高纯度(大于为99.95%)石墨靶和Ag靶交替地旋转至沉积位置制备DLC/Ag纳米多层膜;沉积薄膜时,保持TiN/Ag或DLC/Ag每个亚层的厚度(即调制周期)在10~100nm之间,纳米多层膜的总厚度在500nm-1000nm之间;
(4)Ag离子注入纳米多层膜表面:经过TiN/Ag或DLC/Ag纳米多层膜表面修饰的椎间融合器的表面再运用金属蒸汽弧源离子注入机或等离子浸没离子注入机进行银离子注入,银离子注入设备的能量选择为20-120keV,银离子的注入剂量保持在5×1014~5×1018ions/cm2范围内。
本发明在钛合金制椎间融合器表面制备表面富银纳米多层膜的优点在于:
1.在金属制椎间融合器表面沉积TIN、DLC薄膜,使其具有较高的硬度,耐磨性、耐腐蚀性和生物相容性,对减少椎间融合器临床使用的不良反应具有重要作用;
2.除了提高耐磨作用之外,还在金属基体与人体体液之间起隔离作用,大大减少了有毒金属离子的渗出,提高了生物相容性,不仅减少由于摩擦磨损引起的假体松动导致骨融合失败的风险,而且还能减少体液中金属腐蚀引起的有毒离子释放,为骨性融合提供尽可能好的生物环境。物理气相沉积得到的多层膜在小纳米周期范围内发生了性能异常升高的现象,得到纳米多层膜比单层膜晶粒更小、质地更均匀、致密,因此其抗腐蚀性、耐磨性以及与基底材料的结合能力与单层膜相比得到明显提高,因此本发明中的含TiN/Ag、DLC/Ag纳米多层膜具有比单层膜更优异的理化性能;
3.制备针对椎间融合器Cage置入术后感染易植入失败的问题,本发明提出选用纳米多层镀技术与银抗菌相结合,即在钛合金制椎间融合器表面沉积表面富银的高性能纳米多层膜(TiN/Ag纳米多层膜和DLC/Ag纳米多层膜),将抗菌物质定植于椎间融合器植入物表面,使植入假体在植入后即刻释放活性抗菌物质达到防止细菌的附着。由于多层膜含有富银层,保证银离子的长效释放,达到长期的阻止细菌粘着于植入物表面,降低感染的风险。
【附图说明】
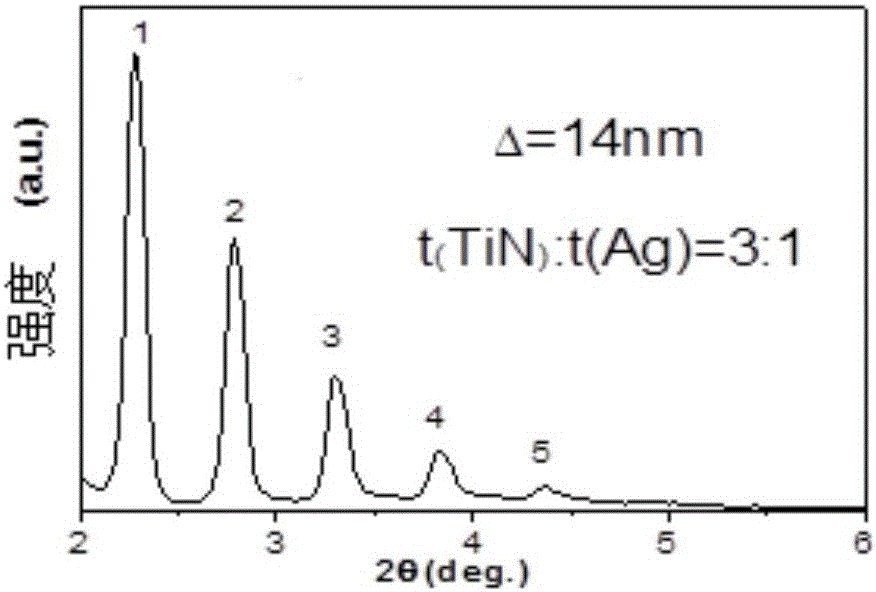
图1为钛合金基底偏压下沉积所得TiN/Ag薄膜的小角XRD图谱;
图2为沉积所得TiN薄膜的的表面SEM图;
图3为沉积所得TiN/Ag纳米多层膜薄膜的横断面SEM图;
图4为银离子随深度的分布图;
图5为注入剂量对大肠杆菌(Ecdi)和金黄色葡萄球菌(Saureus)的抑菌率曲线;
图6为不同注银剂量对大肠杆菌生长抑制情况观察;
图7为钛合金(a)、单层TiN(b)以及TiN-Ag纳米多层膜表面(c)的硬度对比;
图8大鼠间充质干细胞在钛合金表面(a)、TiN-Ag多层膜表面(b)的表面形貌;
图9大鼠间充质干细胞在钛合金表面、TiN-Ag多层膜表面(b)的细胞生长曲线。
以下将结合本发明的实施例参照附图进行详细叙述。
【具体实施方式】
本发明是在钛合金的椎间融合器表面运用物理气相沉积技术(包括:离子束辅助沉积、磁控溅射、磁过滤离子镀)合成TiN/Ag或DLC/Ag纳米级多层膜并在纳米多层膜上注入一定剂量的银离子,在椎间融合器表面形成表面富银的纳米多层膜,即将纳米多层镀技术与银抑菌相结合。具体如下:
经过切割打磨的钛合金制椎间融合器,依次经过丙酮、乙醇超声清洗15分钟,吹干后立即送入真空沉积室中。离子束辅助沉积、磁控溅射、磁过滤的离子镀等方法沉积薄膜时,在真空条件下用惰性气体离子(氮离子或氩离子)束轰击不同靶材,即将高纯度Ag靶和Ti靶交替地旋转至沉积位置制备TiN/Ag纳米多层膜,或将高纯度Ag靶和石墨靶交替地旋转至沉积位置运用氩离子轰击制备DLC/Ag纳米多层膜。并精确控制每个靶材的沉积时间,得到TiN/Ag或DLC/Ag多层薄膜。并在TiN/Ag或DLC/Ag多层薄膜表层(TiN或DLC)运用金属蒸汽弧源离子注入机或等离子浸没离子注入机进行银离子注入,离子注入能量为20-120keV,注入5×1014~5×1018ions/cm2范围剂量的银离子。
实施例1:
运用带磁过滤的离子镀和等离子浸没技术在钛合金椎间融合器表面制备表面富银的TiN/Ag多层膜:切割抛光的钛合金椎间融合器依次用丙酮、乙醇分别超声清洗15分钟,烘干后置于可转动的样品台上立即送入真空沉积室,用氩离子源轰击清洗铸件及表面活化,轰击束流5mA,时间为5min,通入氮气,将纯度为99.99%的Ti靶和Ag靶交替地放置在沉积位置(控制条件:偏压200eV,弧流80-85A,工作真空气压低于5.0×10-4Pa),精确控制沉积时间得到调制周期为14nm左右的TiN/Ag纳米多层膜。在制备好的TiN/Ag纳米多层膜表面运用氩离子溅射清洗5分钟,运用等离子浸没注入技术银离子注入,注入能量为50keV,银离子注入剂量5.0×1014至5.0×1018ions/cm2。
本发明对上述制备表面富银的TiN/Ag纳米多层膜进行了性能表征,具体如下:
(1)由图1可知,TiN/Ag纳米多层膜界面清晰,分支越多说明界面越平整,同时通过修正的布拉格公式计算可知调制周期约为14nm。
(2)图2显示的TiN/Ag多层膜的表面形貌和断面形貌,表面结构呈现出具有棱边的直角三棱锥的形貌,颗粒大小分布都很均分,且多层膜的厚度为546nm,如图3所示。
(3)如图4所示,不同剂量的银注入到多层膜的表面,银呈非对称高斯分布。因为注入和溅射是离子束与固体表面相互作用的两个物理过程,在大剂量的银的作用下,基底表面的钛原子被溅射,留下较多的银形成表面富银层。随着注入剂量的增加,表面的银浓度增加。
(4)图5和图6可以看到注入银离子的纳米多层膜对金黄色葡萄球菌和大肠杆菌具有明显的抗菌效果,并且抗菌率随着注入银离子剂量的增大而增大。在银离子注入剂量低于饱和剂量范围内,注银纳米多层膜的抗菌率随着注入剂量的增大而增大,当注入剂量达到一定时(5.56×1017ions/cm2),对金黄色葡萄球菌和大肠杆菌的抗菌率接近100%。
(5)从图7可以看出随着压入深度的增加,样品的硬度呈现增加然后慢慢的的降低并趋于一个平稳值。压痕得出钛合金的最高硬度在6.5GPa,而一层氮化钛的材料硬度明显提高,达到28.9pa,纳米多层膜的最高硬度值为56.4Pa,比钛合金提高了7倍之多。由此可见,纳米多层膜结构明显提高了钛合金表面的纳米硬度。
(6)耐腐蚀试验中测试了钛合金本身及镀膜样品的基本电化学参数,实验结果表明在Hanks模拟体液中,单层膜和纳米多层膜样品的稳定性高于钛合金基底材料,显示出很好的保护效果,有效地提高了钛合金椎间融合器表面的抗腐蚀性能。
(7)体外细胞培养的生物相容性评价中,在钛合金表面以及表面富银的TiN-Ag多层膜表面种植间充质干细胞,结果显示(如图8和图9所示):间充质干细胞在TiN-Ag多层膜表面都有良好的生长,但细胞在有氮化钛镀层的样品表面比无镀层的钛合金表面的生长程度更为旺盛,细胞形态也相对较好。
实施例2:运用离子束辅助沉积系统和金属蒸汽弧源离子注入技术在钛合金椎间融合器表面合成表面富银的TiN/Ag多层膜,具体方法如下:先依次用丙酮、乙醇超声清洗15分钟,烘干后置于可转动的样品台上立即送入沉积室中;在沉积薄膜以前,用低能Ar+对所有基底进行溅射清洗及活化,轰击束流5mA,时间为8min。真空室本底真空度为3×10-4Pa,工作气压为1.6×10-2Pa;两个离子源的Ar和N2为反应气体,沉积薄膜时,可将Ti(99.95%)和Ag(99.95%)靶交替地旋转至溅射位置并分别用氮离子和氩离子轰击,通过改变每个靶材的沉积时间可以得到不同调制周期10nm的多层膜,薄膜整体厚度为0.5um。运用金属蒸汽弧源(MEEVA)离子注入机进行银离子注入,考虑到低能注入对材料表面损伤小,银离子注入能量选择为30keV,注入银的剂量5×1017ions/cm2。扫描电镜(SEM)观察此方法可以得到界面清晰的多层膜结构;X射线光电子能谱分析(XPS)测试表明上述方法修饰的钛合金椎间融合器表面有一定量的单质银或AgO存在,且价态稳定;俄歇电子能谱(AES)分析测试表明,TiN/Ag多层膜样品周期性明显,在银离子注入后样品表面银的主要存在样品表面,当深度达到4nm左右时银的含量最高随着深度的增加,银的含量降低;内应力、硬度、弹性模量测试表明表面富银的TiN/Ag多层膜具有比较好的机械性能;细胞毒性检测结果表明富银表面的细胞毒性为0级,没有细胞毒性;抗菌和腐蚀实验结果表明:表面富银TiN/Ag多层膜样品具有很好抗菌性能和抗腐蚀性,样品表面对大肠杆菌和金黄色葡萄球菌的抗菌率达到97%以上,且抗腐蚀性能得到明显提高。在表面富银的TiN/Ag表面种植间胎鼠成骨细胞结果显示成骨细胞在富银多层膜表面都有良好的生长,与钛合金表面的生长情况相比细胞生长程度更为旺盛,细胞形态也相对较好。
实施例3:
采用磁控溅射的方法在钛合金椎间融合器表面进行表面富银的TiN/Ag纳米多层膜薄膜制备:切割抛光的钛合金椎间融合器依次用丙酮、乙醇超声清洗15分钟,烘干后置于可转动的样品台上立即送入真空沉积室中。在沉积薄膜以前,束流6mA Ar+对样品进行清洗5min。沉积薄膜时,可将高纯度Ti(99.95%)和Ag(99.95%)靶交替地旋转沉积位置,沉积薄膜时,可利用电脑程序设置精确控制靶材的溅射时间。用氮离子和氩离子分别交替轰击Ti和Ag靶,沉积得到TiN/Ag多层薄膜。制备工艺参数:磁控溅射的功率80W,镀膜时本底真空高于1.0×10-3Pa工作气压0.05Pa。上述方法制备TiN/Ag纳米多层薄膜整体厚度均控制在600nm。运用等离子浸没离子注入机进行银离子注入,银离子注入能量选择为40keV,银离子注入剂量分别为5×1016ions/cm2。扫描电镜(SEM)结果显示上述方法制备的薄膜界面清晰的调制周期为20nm左右多层膜结构,整体厚度为600nm;X射线光电子能谱分析(XPS)测试表明其表面有一定量的单质银或AgO存在,且价态稳定;俄歇电子能谱(AES)分析测试表明多层膜样品周期性明显,银离子注入表面银的主要存在样品表面(100nm之内);内应力、硬度、弹性模量测试表明表面富银的TiN/Ag多层膜具有较优的力学机械性能;细胞毒性检测结果表明富银表面的细胞毒性为0级;抗菌和腐蚀实验结果表明:表面富银TiN/Ag多层膜样品具有很好抗菌性能和抗腐蚀性,样品表面对大肠杆菌和金黄色葡萄球菌的抗菌率达到97%以上,且抗腐蚀性能较好。
实施例4:运用带磁过滤的离子镀和等离子浸没技术在钛合金椎间融合器表面制备表面富银的DLC/Ag多层膜:切割抛光的钛合金椎间融合器依次用丙酮、乙醇分别超声清洗15分钟,烘干后置于可转动的样品台上立即送入真空沉积室,用氩离子源轰击清洗铸件及表面活化,轰击束流5mA,时间为10min,通入氩气,将纯度为99.99%的石墨靶和Ag靶交替地放置在沉积位置(控制条件:偏压300eV,弧流100-120A,工作真空气压低于5.0×10-4Pa),精确控制沉积时间得到调制周期为20nm左右的TiN/Ag纳米多层膜。在制备好的DLC/Ag纳米多层膜表面运用氩离子溅射清洗5分钟,运用等离子浸没注入技术银离子注入,注入能量为50keV,银离子注入剂量5.0×1016ions/cm2。运用带磁过滤的离子镀和等离子浸没技术制备的表面富银的TiN/Ag纳米多层膜能有效的降低DLC薄膜在制备过程中产生的残余应力和增加膜基结合力,同时保持DLC薄膜高的硬度和优异的耐磨损性能。富银表面检测细胞毒性结果表明DLC/Ag纳米多层膜的细胞毒性为0级;抗菌和腐蚀实验结果表明:表面富银DLC/Ag多层膜样品具有很好抗菌性能和抗腐蚀性,样品表面对大肠杆菌和金黄色葡萄球菌的抗菌率达到97%以上,且抗腐蚀性能较好。
实施例5:运用离子束辅助沉积系统和金属蒸汽弧源离子注入技术在钛合金椎间融合器表面合成表面富银的DLC/Ag多层膜,具体方法如下:先依次用丙酮、乙醇超声清洗15分钟,烘干后置于可转动的样品台上立即送入沉积室中;在沉积薄膜以前,用低能Ar+对所有基底进行溅射清洗及活化,轰击束流5mA,时间为5min。真空室本底真空度为3×10-4Pa,工作气压为1.6×10-2Pa;离子源的Ar为反应气体,沉积薄膜时,可将石墨靶(纯度99.99%)和Ag(99.99%)靶交替地旋转至溅射位置氩离子轰击,通过改变每个靶材的沉积时间可以得到不同调制周期20nm的DLC/Ag多层膜,薄膜整体厚度为0.6um。运用金属蒸汽弧源(MEEVA)离子注入机进行银离子注入,考虑到低能注入对材料表面损伤小,银离子注入能量选择为40keV,注入银的剂量5×1016ions/cm2。扫描电镜(SEM)观察此方法可以得到界面清晰的多层膜结构;X射线光电子能谱分析(XPS)测试表明上述方法修饰的钛合金椎间融合器表面(1-100nm)含有单质银或AgO存在,且价态稳定;此方法制备的表面富银DLC/Ag多层膜的具有较低残余应力和较高膜基结合力,同时保持DLC薄膜高的硬度和优异的耐磨损性能;内应力、硬度、弹性模量测试表明表面富银的DLC/Ag多层膜具有比较好的机械性能;细胞毒性检测结果表明富银表面的细胞毒性为0级,没有细胞毒性;抗菌和腐蚀实验结果表明:表面富银DLC/Ag多层膜样品具有很好抗菌性能和抗腐蚀性,样品表面对大肠杆菌和金黄色葡萄球菌的抗菌率达到95%以上,且抗腐蚀性能得到明显提高。在表面富银的DLC/Ag表面种植大鼠间充质干细胞结果显示间充质干细胞在富银多层膜表面都有良好的生长,与钛合金表面的生长情况相比细胞生长程度更为旺盛,细胞形态也相对较好。
实施例6:采用磁控溅射技术和等离子浸没离子注入技术在钛合金椎间融合器表面进行表面富银的DLC/Ag纳米多层膜薄膜制备:切割抛光的钛合金椎间融合器依次用丙酮、乙醇超声清洗15分钟,烘干后置于可转动的样品台上立即送入真空沉积室中。在沉积薄膜以前,束流6mA Ar+对样品进行清洗8min。沉积薄膜时,可将高纯度石墨(99.99%)和Ag(99.99%)靶交替地旋转沉积位置,沉积薄膜时,可利用电脑程序设置精确控制靶材的溅射时间。用氩离子分别交替轰击Ti和Ag靶,沉积得到DLC/Ag多层薄膜。制备工艺参数:磁控溅射的功率100W,镀膜时本底真空高于1.0×10-3Pa工作气压0.05Pa。上述方法制备DLC/Ag纳米多层薄膜整体厚度均控制在600nm。运用等离子浸没离子注入机进行银离子注入,银离子注入能量选择为60keV,银离子注入剂量分别为5×1016ions/cm2。X射线光电子能谱分析(XPS)测试表明上述方法修饰的钛合金椎间融合器表面(1-100nm)含有单质银或AgO存在,且价态稳定;此方法制备的表面富银DLC/Ag多层膜的具有较低残余应力和较高膜基结合力,同时保持DLC薄膜高的硬度和优异的耐磨损性能;内应力、硬度、弹性模量测试表明表面富银的DLC/Ag多层膜具有比较好的机械性能;细胞毒性检测结果表明富银表面的细胞毒性为0级,没有细胞毒性;抗菌和腐蚀实验结果表明:表面富银DLC/Ag多层膜样品具有很好抗菌性能和抗腐蚀性,样品表面对大肠杆菌和金黄色葡萄球菌的抗菌率达到95%以上,且抗腐蚀性能得到明显提高。在表面富银的DLC/Ag表面种植间胎鼠成骨细胞结果显示成骨细胞在富银多层膜表面都有良好的生长,与钛合金表面的生长情况相比细胞生长程度更为旺盛,细胞形态也相对较好。
综上运用离子束辅助沉积、磁控溅射或离子镀技术以及金属蒸汽弧源或等离子浸没技术在钛合金椎间融合器表面制备的表面富银DLC/Ag或TiN/Ag纳米多层膜,使其表面结构和性能发生了明显的改变,椎间融合器表面具有较高的硬度和优异的耐磨损性能,在Hanks模拟体液中的抗腐蚀性能也显著提高,表面具有较为明显的抑菌的作用,体外细胞培养结果表明植入材料表面的细胞相容性有显著的改善。
以上对本发明的具体实施例进行了详细描述,但其只是作为范例,本发明并不限制于以上描述的具体实施例。对于本领域技术人员而言,任何对本发明进行的等同修改和替代也都在本发明的范畴之中。因此,在不脱离本发明的精神和范围下所作的均等变换和修改,都应涵盖在本发明的范围内。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种磁性纳米粒子与超滤膜结合处理废弃乳化液的方法与流程
- 一种多肽修饰纳米粒子在制备治疗急性肺损伤的药物中的应用的制作方法与工艺
- 一种金纳米花修饰的离子液体功能化石墨烯纸电极、其制备方法和应用与流程
- 一种新型的透明质酸修饰的多级纳米颗粒及其制备与应用的制作方法与工艺
- 一种核壳结构的磁性纳米粒子及其制备与应用的制作方法与工艺
- 一种室温固相反应制备的纳米铁修饰的铁基氨合成催化剂及其制备方法和应用与流程
- 一种丁氧基修饰的TiO2单晶空心四方纳米锥材料、制备方法及其应用与流程
- 一种改性粒子修饰的有机无机杂化聚合物涂料的制作方法与工艺
- 一种表面修饰片状纳米铜及含有该纳米铜的复合润滑油的制备方法与流程
- 一种用于简便修饰磁性纳米粒子的手性拆分添加剂的制备和应用的制作方法与工艺