艾滋病净化治疗仪的制作方法
本发明涉及生物医学领域中艾滋病净化治疗仪的制备及应用,主要用于艾滋病患者血细胞内、外艾滋病毒的清除,从而达到预防、控制和治疗艾滋病的目的。
背景技术:
艾滋病是由人类免疫缺陷病毒(Human Immunodeficiency Virus,HIV)引起的传染病,在全球广泛流行,根据世界卫生组织(WHO)和联合国艾滋病规划署的有关报告,自1981年美国发现首例艾滋病病例以来,至今全球有208个国家和地区受到了艾滋病的严重威胁,约有4000万人感染了艾滋病,死亡人数已超过2000万,每天约有6000人成为艾滋病感染者,同时每天约有300多人死于艾滋病。在中国HIV感染者正处于高速增长期,目前已远超过100万。艾滋病已经成为继肿瘤、心脑血管疾病、结核病、糖尿病后又一个人类面临的重大感染性疾病,已成为全球关注的严重的公共卫生和社会问题。
人类免疫缺陷病毒是一种感染人类免疫细胞的慢病毒(Lentivirus),属反转录病毒的一种,直径约120纳米,大致呈球形。病毒外膜是类脂包膜(来自宿主细胞),并嵌有病毒的蛋白gp120与gp41。gp41是跨膜蛋白,gp120位于表面,并与gp41通过非共价作用结合。向内是由蛋白p17形成的球形基质(Matrix),以及蛋白p24形成的半锥形衣壳(Capsid),衣壳在电镜下呈高电子密度,内含有病毒的RNA基因组、酶(逆转录酶、整合酶、蛋白酶)以及其他来自宿主细胞的成分。
HIV进入人体后,首先被巨噬细胞吞噬,但HIV很快改变了巨噬细胞内某些部位的酸性环境,创造了适合其生存的条件,不但不被杀灭反而在其内繁殖。因为CD4是HIV的受体,所以经巨噬细胞内繁殖的HIV通过其囊膜蛋白gp120并在gp41的辅助下(gp41起着桥的作用,利用自身的疏水作用介导病毒囊膜与细胞膜融合)进入CD4+细胞(细胞、单核巨噬细胞、树突状细胞等),在细胞内迅速增殖,每天产生109~1010病毒颗粒,并不断进入其他正常的和再生的CD4+细胞内复制,制造更多的病毒感染细胞,使外周血CD4+T细胞持续破坏、减少。HIV的gp120与CD4受体结合可直接激活受感染的细胞凋亡,甚至感染HIV的T细胞表达的囊膜抗原也可启动正常T细胞,通过细胞表面CD4分子交联间接地引起CD4+细胞的大量破坏,结果造成以CD4+T细胞缺损为中心的严重免疫缺陷,患者主要表现:外周淋巴细胞减少,T4/T8比例配置,对植物血凝素和某些抗原的反应消失,迟发型变态反应下降,NK细胞、巨噬细胞活性减弱,IL2、γ干扰素等细胞因子合成减少。CD4+T细胞是最重要的免疫细胞,感染者一旦失去了大量CD4+T细胞,整个免疫系统就会遭到致命的打击,对各种疾病的感染都失去抵抗力。HIV进入宿主CD4+细胞后也可以表现为长期潜伏而不表现出临床症状,其基因组RNA反转录成双链DNA,与病毒整合酶进入宿主细胞核内,在整合酶的作用下,双链DNA整合到宿主细胞基因组内,被整合的病毒DNA称为前病毒,可潜伏数月甚至多年不复制,造成AIDS数月至多年的潜伏期。在AIDS的潜伏期,HIV主要在淋巴结的巨噬细胞和树突状细胞内繁殖,这些细胞是体内的HIV贮存库,可释放至外周血或转染外周血中的CD4+T细胞,有丝分裂原、抗原、TNF、IL-2和淋巴素(LT)都能激发HIV前病毒基因在感染的CD4+T细胞内转录复制。经大量增殖后,HIV病毒颗粒不断从被破坏的感染细胞释放并游离于血液,然后再进入其他细胞继续感染过程。
HIV感染后可刺激机体生产囊膜蛋白(Gp120,Gp41)抗体和核心蛋白(P24)抗体。在HIV携带者、艾滋病病人血清中测出低水平的抗病毒中和抗体,其中艾滋病病人水平最低,HIV携带者最高,说明该抗体在体内有保护作用。但抗体不能与单核巨噬细胞内存留的病毒接触,且HIV囊膜蛋白易发生抗原性变异,原有抗体失去作用,使中和抗体不能发挥应有的作用。在潜伏感染阶段,HIV前病毒整合入宿主细胞基因组中,因此HIV不会被免疫系统所识别,所以仅依靠自身免疫功能无法将其清除。另外一个很重要的原因应该是,根据抗体杀灭、清除抗原的机理推测,免疫性抗体与抗原结合后,如果要产生免疫效应,要么通过激活补体,介导ADCC效应溶解细胞性抗原,但HIV不是细胞性抗原;要么通过趋化作用吸引吞噬细胞吞噬清除抗原,但HIV反而在吞噬细胞内被保护、增殖;要么抗体与抗原结合起中和作用,使之失去感染力,但HIV抗原结构多变,往往使抗体难以识别。
从目前已用于临床的艾滋病治疗方法看,效果不那么理想:(1)HIV逆转录酶抑制剂:仅能防止尚未感染HIV的易感细胞感染,对已感染的细胞没有治疗作用,且毒副作用较多,包括腺粒体毒性、骨髓抑制、红细胞性贫血、粒细胞和血小板减少、胰腺炎,加之交叉耐药性的产生,这类药已不单独使用,主要做联合用药,且易产生耐药变株,导致临床疗效下降或失效。(2)HIV蛋白酶抑制剂:易产生药物性肝损伤、脂质代谢紊乱等毒副作用及耐药性。(3)HIV整合酶抑制剂:通过抑制HIV病毒DNA与宿主细胞DNA整合而发挥作用,与HIV逆转录酶抑制剂和蛋白酶抑制剂联合同时使用对抗病毒有协同作用。(4)抑制HIV病毒进入抑制剂:包括阻断gp120与CD4结合、阻断HIV与辅助受体结合、作用于gp41膜亚单位及作用于T淋巴细胞表面CC趋化因子受体5(CCR5)来阻断HIV进入宿主细胞,但对肝和心脏有副作用。(5)细胞因子治疗:主要用于调节T细胞动态平衡。(6)HIV疫苗治疗:由于HIV的特殊性,如固有免疫不足以抵御HIV及其靶向破坏免疫系统,病毒突变迅速,导致至今尚未开发出真正安全有效的疫苗。(7)基因治疗:HIV基因治疗的研究从未间断,包括反义技术、RNA诱饵、RNA干扰、细胞内抗体、显性阴性突变体、自杀基因等,但进入II期临床试验阶段的基因疗法几乎没有。(8)单克隆抗体被动免疫疗法:通过下调CD4+T细胞表面CCR5来降低HIV的易感性、延缓艾滋病的进展和减少HIV的扩散,中和单克隆抗体2G12、2F5和4E10应用于HIV感染者具有良好的耐受性和安全性,能延缓但不能阻止病毒的反弹(9)过继性免疫细胞治疗:体外大量培养HIV自体的CD4+T细胞时会导致病毒大量扩增,增加病毒感染的CD4+T细胞数量,而回输CD4+T细胞可能会增加体内病毒复制的场所,导致病毒载量反弹,总体上看,过继性免疫细胞治疗无明显的毒副作用,也未取得满意的治疗效果。
CD4分子是HIV的受体,HIV易感于CD4+T细胞,CD4+T细胞是T淋巴细胞的一种,平均寿命一般为7天左右,但某些T细胞特别是经永生化成细胞系(株)后可长期存活、无限扩增。国外文献报道,猴肾病毒40(SV40)可以使某些人类细胞发生永生化。Poulin DL、Kung AL和Sullivan CS等研究表明,SV40T抗原基因的导入能加快转化细胞的生长速率,永生化细胞在体外多次传代后,仍具有相对稳定的增殖特性和功能状态,同时也能保留其原始细胞的许多分化表型。Reilly用猿猴病毒大T抗原基因转化来建立血管平滑肌细胞株,构建细胞模型以研究肝素对血管平滑肌的抑制作用机制。Su等利用经SV40转化的角化上皮细胞株,构建细胞模型来分析上皮细胞内蛋白质合成的调控作用。Miquel等用SV40转化的角化上皮细胞株,作为细胞模型研究层粘连蛋白5介导的细胞粘附作用。Webber等用经SV40转化的前列腺上皮细胞株作为细胞模型来研究前列腺上皮细胞的生理功能和分泌功能。Racusen等用经Ad12-SV40转化肾小管上皮细胞模型来研究近曲小管的损伤和疾病。Hougton等用SV40转化建立骨髓基质细胞株作为细胞模型以研究在一定培养条件下,细胞具有向脂肪细胞和成骨细胞的双向分化的潜能,进一步研究骨质疏松的机制。国外研究还表明,导入外源性人端粒酶逆转录酶(hTERT)可以使细胞保持正常表型及分化特征。近年来已利用hTERT成功建立了某些细胞的永生化细胞系,基本保持染色体稳定、分化正常、接触抑制、无致瘤性等相对正常的生长特征。在口腔医学领域,日本学者Kamata、Fujita和Fujii转染hTERT建立了永生化人牙龈成纤维细胞、牙周细胞、牙髓细胞系和牙囊细胞系,细胞群体倍增数达150次以上,细胞均表现原有的生物学特性,诱导培养后都可以表达来源细胞的相关蛋白。Kitagawa等转染hTERT建立了人成牙骨质细胞系,细胞倍增达200次以上,细胞分化标志物如碱性磷酸酶、I型胶原等表达稳定。因研究工作的需要,几乎每种疾病都有各自的细胞模型。如糖尿病细胞模型、癌细胞细胞模型、转基因细胞模型、绝经期综合症细胞模型、子宫内膜细胞模型、癫痫细胞模型、电子细胞模型、酒精性痴呆细胞模型、脑水肿细胞模型等。所以,可制备CD4+T细胞株,经大量培养后,用于制备治疗艾滋病的净化器,以CD4+T细胞吸附、清除血浆中的HIV,同时通过输给反应器中产生的CD4+T细胞的细胞因子,来治疗艾滋病患者。
人类的吞噬细胞有大、小两种,小吞噬细胞是外周血中的中性粒细胞,大吞噬细胞是血中的单核细胞和多种器官、组织中的巨噬细胞,两者构成单核吞噬细胞系统。单核细胞由骨髓中的单核细胞前体发育分化而成,约占血液中白细胞总数的3%一8%,其体积较淋巴细胞略大,单核细胞在血液中仅停留12-24小时,然后进入结缔组织或器官,发育成熟为巨噬细胞,巨噬细胞是单核吞噬细胞系统中高度分化、成熟的细胞类型,具有较强的吞噬功能,游走巨噬细胞大于单核细胞数倍,寿命较长,可在组织中存活几个月,定居的巨噬细胞有不同的名称,在肝中为枯否细胞、在脑中为小胶质细胞、在骨中为破骨细胞等,其表达Fc受体、C3b受体和CD14,在固有免疫中发挥防御功能,也是参与适应性免疫的专职抗原提呈细胞。巨噬细胞表达的CD4分子,是艾滋病毒(HIV)的受体,HIV进入人体后,首先遭到巨噬细胞的吞噬,但HIV很快改变了巨噬细胞内某些部位的酸性环境,创造了适合其生存的条件,不但不被杀灭反而在其内大量繁殖聚集,转而将HIV传递给CD4+T细胞。所以,可以常规杂交瘤细胞制备技术,制备巨噬细胞杂交瘤细胞,经大量扩增后用于制备治疗艾滋病的净化器,以巨噬细胞的吞噬功能来清除血浆中的HIV。
凝胶琼脂或琼脂糖是一种含有硫酸基的多糖体,高温时能溶于水,冷却后凝成凝胶,形成一种多孔的网状结构,可允许大分子物质(分子量可达百万以上)自由通过,其孔径的大小处决于琼脂浓度,浓度越大,孔径相对较小,浓度越小,孔径相对较大,1%琼脂凝胶的孔径约为85nm。由于琼脂或琼脂糖具有很好的化学稳定性,凝胶后含水量大,透明度好,来源方便,易处理,是一种很好的扩散介质,以琼脂凝胶为扩散介质的免疫扩散试验是用已知抗体检测相应未知抗原的常规实验诊断项目,也是《中国药典》2010版中规定用于流感病毒疫苗血凝素含量检测的标准方法。当一种溶液通过半固体凝胶时,其中的大分子溶质就被分子筛作用的凝胶孔阻留在凝胶中,当患者经体外循环分离出的血浆流经凝胶时,血浆中100~120nm的HIV能被孔径约为85nm的1%浓度的琼脂凝胶阻留在凝胶中,由此可清除血浆中的HIV。
总之,各种药物及生物制品无法有效杀灭体内的艾滋病毒,且价格贵,副作用大,至今尚无治疗艾滋病的有效方法,已成为久攻不克的世界性难题。
技术实现要素:
为了解决久攻不克的艾滋病治疗领域的世界性难题,本发明人提出了本发明。
本发明的目的是要提供艾滋病净化治疗仪;另一目的是要提供艾滋病净化治疗仪的制备及应用方法。
本发明的目的是这样实现的:制备能滤除多细胞结合而成的含有HIV的大体积细胞的血液分离器及能分离单个血细胞及血浆的血浆分离器;以外源基因转染的方法构建CD4+T细胞株和/或以CD4+T细胞表面特有分子抗体作为细胞生长刺激剂扩增;以杂交瘤技术制备既保留原巨噬细胞特性又能无限生长的杂交瘤巨噬细胞株并行扩增;取CD4+T细胞株和巨噬细胞株以高生物相容性材料包裹而制备能防止细胞及其碎片滤出并能为细胞株吞噬吸附HIV提供场所的血液净化器;取起载体作用的经100℃溶化后保温在39~41℃的0.7~1.1%梯度浓度的琼脂糖,按浓度从高至低依次加入血液净化器,待冷却至37℃成为半固体凝胶后再接着加下一次,使净化器中的凝胶从上到下形成从低到高的琼脂糖浓度的分层分布,有利于血浆灌流及分子筛和免疫清除的作用,其中CD4+T细胞株和巨噬细胞株均被固定在琼脂糖凝胶中,起吸附HIV的作用,所制备的艾滋病血液净化器进而与血液、血浆分离器组合并附加计算机调控程序而制备艾滋病净化治疗仪,体外循环中的血液被治疗仪中的血液分离器滤除大体积的多核血细胞,进而被血浆分离器分成血浆和单个血细胞,血浆经净化器滤除HIV后与单个血细胞汇合后回输。
本发明的技术核心由血液、血浆分离器和血浆净化器构成,其中血液分离器的孔径型号为150~250μm、50~150μm、15~40μm、8~15μm、5~8μm、3~5μm、1~2μm,能滤除血液中HIV感染细胞形成的多核巨细胞或多细胞聚合体;血浆分离器能分离中等体积的单个血细胞和血浆;血浆净化器中的净化剂由固定于琼脂凝胶的CD4+T细胞株和巨噬细胞株制成,因CD4+T细胞表面的CD4分子是HIV的受体而成为HIV的易感细胞,与HIV相遇时能吸附HIV,被吸附的HIV随CD4+T细胞被固定于琼脂凝胶,因杂交瘤巨噬细胞的天然吞噬特性,HIV与之相遇时能被吞噬而随之也被固定于琼脂凝胶,而且琼脂凝胶所形成的滤孔随着琼脂糖浓度的增高而减少,净化器进口处琼脂糖浓度低,滤孔就大,有利于血浆灌流及细胞与HIV的结合反应;而出口处浓度高,滤孔就小,易于阻留HIV或大分子结合物,净化器组合了多种特异和非特异的HIV清除成份,以免特种毒株因免疫差异所致的无效治疗。所以在艾滋病血液净化治疗的体外循环中,含有大量HIV的大体积细胞首先被血液分离器滤除,而血浆中游离的HIV被血浆净化器吸附清除,净化后的血浆与中等体积的单个血细胞汇合后回输,从而清除结合在细胞表面和/或细胞内的HIV以及游离于血浆的HIV。本发明以体外机械滤除HIV的方法替代长期以来无法有效杀灭HIV的常规体内抗逆转录药物治疗方法,实现了人工将HIV从体内机械清除的治疗新方法。
具体实施方式
图1是根据本发明提出的艾滋病净化治疗仪的应用示意图。
图2是根据本发明提出的血液分离器的内部结构示意图。
图3是根据本发明提出的血浆分离器的内部结构示意图。
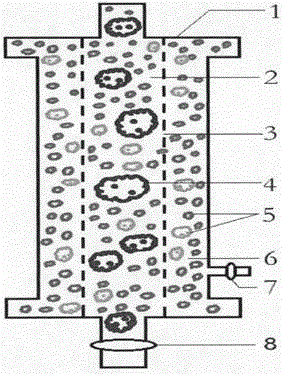
图4是根据本发明提出的净化器的内部结构示意图。
图1中,动脉血路管(1)的一端与动脉血管相连通,另一端经肝素和血液泵(2)与含有废液出口(5)的血液分离器(3)相连,血液分离器(3)经血液出口(4)、血液泵(6)、循环管路(7)与血浆分离器(8)相连,血浆分离器(8)的血浆出口经血浆泵(9)和血路管(10)与两个并联的净化器(11)和净化器(12)相连,两个净化器的出口管路(13)与血浆分离器(8)的血细胞出口管路(14)汇合后经静脉管路(15)汇流体循环。
图2表示图1中的血液分离器(3)的内部结构。图2中,分离器(1)的内腔(2)的管壁上有很多微孔(3),多核巨细胞(4)不能滤过微孔(3)而被阻留在内腔(2),从而可被清除,能通过微孔(3)的中、小体积的单个血细胞(5)进入外腔(6),然后经出口(7)流出,进而经图1所示的血浆分离器(8)分离出血细胞和血浆。
图3表示图1中的血浆分离器(8)的内部结构。图3中,1是血浆分离器,2是血浆分离器内腔,3是血浆分离器内腔管壁上的微孔,4是不能通过微孔(3)的单个血细胞,5是能通过微孔(3)的血浆化学成份,6是血浆分离器外腔,7是血浆流出口,8是具有可开关阀门的血细胞出口。
图4中,2、4分别为固定于琼脂凝胶(6)中的巨噬细胞株和CD4+T细胞株;1是游离的HIV;3、5分别为HIV与巨噬细胞株和CD4+T细胞株结合后而被阻留在琼脂凝胶(6)中的结合物,7为被琼脂凝胶(6)分子筛阻留的较大体积的HIV。
下面结合图1、图2、图3和图4,对本发明提出的艾滋病净化治疗仪的实施方案作详细的描述。
一、艾滋病血液净化剂的制备
(一)杂交瘤巨噬细胞株的制备
1、原代细胞来源
(1)单个核血液细胞:指以密度梯度离心法从血液中分离的淋巴细胞和单核巨噬细胞。具体方法是:购买血液中心的浓缩白细胞或为科研而保存的脐带血,取2mL标本,PBS液将血液稀释2~3倍,充分混匀后将6mL抗凝血用滴管沿管壁缓慢叠加于已加入4mL淋巴细胞分离液的10mL离心管中水平离心机中水平离心(400r/min,20℃)35min;离心后管内分为3层,上层为血浆和PBS液,下层主要为红细胞和粒细胞,中层为淋巴细胞分离液,在上、中层界面处有一以单个核细胞为主的白色云雾层狭窄带为PBMC,用毛细吸管插到云雾层,吸取PBMC置入另一50mL离心管中,加入5倍以上体积PBS离心(300r/min,20℃)10min,弃上清50mLPBS重悬细胞,离心(350r/min,20℃)15min,弃上清,加入Buffer(PBS+0.5%新生牛血清+2mmol/LEDTA,pH7.2)2mL重悬细胞,取15uL细胞悬液加入血球计数板上显微镜下计数4个大方格内的细胞(PBMC)总数。
(2)单个核组织细胞:由浙江大学组织工程研究平台提供。实质上属于来自脾脏的巨噬细胞,其制备方法是:①脾脏组织的获取和转运:在论理委员会批准和患者知情同意下,取手术切除的脾脏标本组织,立即剪碎成体积约1mm3的小组织块,移入装有预冷4℃的无菌密封瓶内,迅速转运至细胞培养室。②脾脏组织细胞混悬液的制备:将脾脏组织块移至无菌操作台,PBS洗涤3次,RPMI-1640洗涤2次,以清除组织内的血液并保证组织的无菌。机械研磨脾脏组织,这时便有大量的组织细胞悬混于RPMI-1640液中。用200目不锈钢滤网过滤悬混有组织细胞的RPMI-1640液,滤液为脾脏组织细胞混悬液(主要含红细胞、淋巴细胞、巨噬细胞等)。③脾脏组织细胞混悬液中红细胞的裂解:然后用RPMI-1640液洗涤离心(1000r/min,3min),以去除细胞碎屑,加入Tris-NH4Cl作用5min,裂解红细胞,迅速离心(1000r/min,3min),去除上清液内的裂解红细胞碎片,PBS洗涤离心3次,RPMI-1640洗涤离心1次,以清除混悬液中残存的Tris-NH4Cl,避免其影响细胞的存活,此时,混悬液中主要含脾脏组织巨噬细胞和淋巴细胞。④脾脏组织巨噬细胞的贴壁培养:将前述混悬液作为培养细胞原液,台盼蓝染色判定活力并计数,用RPMI-1640液调整细胞浓度为(3~5)×106/L,将调整好浓度的细胞悬液接种于玻璃培养瓶内,培养条件为37℃,50mL/LCO2,100%湿度,分别培养2~3h,相差显微镜下观察形态。贴壁脾脏组织巨噬细胞的消化:贴壁脾脏组织巨噬细胞的消化:吸去培养上清液,巨噬细胞贴壁,PBS反复吹打、消化,所得细胞悬液洗涤离心(1000r/min,3min),得到分离纯化的巨噬细胞。此外,还可以取治疗或手术后废弃的标本提取制备,如腹膜腔液、肺泡、肝脏、脾脏、腹膜组织、小肠黏膜等。
(3)羊水、绒毛细胞:浙江大学附属妇产科医院生殖遗传实验室备用。在论理委员会批准和患者知情同意下,取实验诊断报告后的剩余羊水、绒毛细胞,选择对数生长期细胞留用。
2、细胞培养及巨噬细胞贴壁初步分选
按常规细胞培养,但根据细胞性质的不同,适当调整培养时间,培养条件等,一般贴壁法将单个核血液细胞(PBMC)或单个核组织细胞(巨噬细胞)置于含有RPMI-1640培养基的培养皿中,于37℃,5%CO2的细胞培养箱(Themo electro corporation CLASS 100,美国)中孵育2h,待单个核细胞贴壁后,吸弃上层悬浮细胞(巨噬细胞以外的细胞不易贴壁而随上层液除去),PBs缓冲液轻轻洗涤3遍,加入少量RPMI一1640培养基,用细胞刮刀刮下贴壁细胞(主要为巨噬细胞,但还有少量其他贴壁细胞)。1 000r/min离心5min,弃上清。羊水细胞、绒毛细胞培养1~7天,出现细胞生长克隆、细胞生长汇合率达到60~80%的对数生长期细胞,以胰酶消化,PBS清洗,获取细胞悬液,配成合适细胞浓度。
3、CD4细胞分选
采用免疫磁珠法分选CD4细胞:①主要试剂和仪器:CD4免疫磁珠(德国美天旎生物技术有限公司);0.2%台盼蓝染色液(上海生工生物工程技术服务公司);新生牛血清(Hyclone公司);MiniMACS磁力分离系统(德国美天旎生物技术有限公司)。②CD4细胞免疫磁珠分选方法:细胞悬液均分至两个1.5mLEppendorf管,离心(300r/min,20℃)10min,弃去上清,重悬细胞每80uLBuffer含细胞数107个,每107个细胞加20uLCD4MicroBeads或CD8MicroBeads,充分混匀,在4~8℃孵化15min,用1mLBuffer洗涤细胞,离心(300r/min,20℃)10min,弃去上清500uLBuffer重悬细胞,将MS分离柱放置在MACS分离器的磁场中,以500uLBuffer漂洗,将500uL细胞悬液通过分离柱,用500uLBuffer冲洗分离柱重复操作3次,收集流出液,流出液中含非CD4细胞,自分离器中取出分离柱,用1000uLBuffer加压冲洗分离柱,收集流出液,此为CD4细胞(细胞活力检测:细胞纯化前后分别取15uL细胞悬液与等体积台盼蓝溶液混合,显微镜下观察不着色发亮者为活细胞,着色胀大者为死细胞,计算200个细胞中活细胞的百分比)。此时分选的细胞主要为巨噬细胞。
4、CD14细胞(巨噬细胞)分选
CD14为单核细胞和巨噬细胞特有的表面标志,理论上如果从单个核组织细胞、羊水细胞及绒毛细胞中分选,则所得细胞为巨噬细胞;如果从单个核血液细胞中分选,则所得细胞包括单核细胞和巨噬细胞;但因单核细胞寿命短、仅在外周血中存活1天且远不如巨噬细胞易于贴壁生长,所以在本发明的细胞贴壁培养中已基本除去,分选出来的细胞基本为巨噬细胞。
基本方法类同于CD4细胞,采用免疫磁珠法。①试剂:人CD14免疫磁珠试剂盒(Miltenyi Biotec,德国),RPMI-1640培养基(Hyclone,美国);②免疫磁珠法:(A)磁珠与特异性靶细胞一单核细胞结合:每1×108个PBMC加入200uL偶联CD14抗体的磁珠和800uL缓冲液(含有10%的牛血清白蛋白2.5mL和2mol/L EDTA0.5mL,4℃冰箱预冷),在15mL离心管中充分混匀,4℃孵育15min,中间可轻微振摇1次。15min后取出离心管,每1×107个细胞加入1~2mL预冷缓冲液,1 000r/min,离心8min,弃上清,加入0.5mL缓冲液并吹打成单细胞悬液。(B)收集磁珠标记的单核细胞:将细胞分离柱置于MACS磁力架上,加入1mL缓冲液平衡细胞分离柱,待无液体滴下,立即将上述细胞悬液加人细胞分离柱中,用0.5mL缓冲液冲洗细胞分离柱3次。待冲洗完毕后,加入1mL缓冲液,从磁力架中移出细胞分离柱,用针柱快速推动,冲出在分离柱中与CD14抗体一磁珠相结合的细胞,即为CD14+的巨噬细胞。
此外,还可采用以下2种方法分选,包括①贴壁法:将PBMC置于含有RPMI-1640培养基的培养皿中,于37℃,含5%C0:的细胞培养箱(Themo electro corporation CLASS 100,美国)中孵育2h。待单核细胞贴壁后,吸弃上层悬浮细胞,PBs缓冲液轻轻洗涤3遍,加入少量RPMI一1640培养基,用细胞刮刀刮下贴壁细胞。1 000r/min离心5min,弃上清。②流式细胞术法:CD14标记:取PBMC,用缓冲液(含有10%的牛血清白蛋白2.5mL和2mol/LEDTA 0.5mL)调整细胞密度为1×108/mL,在每毫升细胞悬液中加入CD14+-FITC抗体100uL,4℃避光标记18min,再向离心管中加入1mL流式缓冲液以终止染色,PBs洗涤3次,用含2%青链霉素的PBS调整细胞密度为2×107/mL。流式细胞仪分选:将制备的细胞在流式细胞仪(BD FAcsAriaII,美国)上分选,根据CD14抗体的荧光强度、细胞的相对大小以及细胞的相对颗粒性和内部结构的复杂性,收集CD14+的细胞。
5、CD14杂交瘤细胞株(杂交瘤巨噬细胞株)制备
(1)培养基及主要试剂:DMEM培养基、HAT、HT选择培养基购自Sigma公司,优级胎牛血清(FBS)购白天津市灏洋生物制品科技责任有限公司;DMSO(--甲基亚砜)为国产分析纯试剂。
(2)骨髓瘤细胞准备:融合前一周从液氮罐内取出一管冻存的骨髓瘤细胞(SP2/0),立即放入热水解冻(应用最多的是Sp2/0细胞株,该细胞株生长及融合效率均佳,本身不分泌任何免疫球蛋白重链或轻链,细胞的最高生长刻度为9×105/ml,倍增时间通常为10~15h;与人体相关的实际应用中考虑选择同源细胞株,如上海复祥生物科技有限公司向ATCC细胞库引进的NCI-H929人骨髓瘤细胞株)。融化后加入适量完全培养液,1000r/m离心3min;重复1次。将沉淀物移入细胞培养瓶中,加DMEM培养液,置CO2培养箱培养,3-4天进行一次传代或扩大培养,融合前24小时内调整细胞状态,保证融合前细胞形态良好、生长旺盛。加入适量基础培养基到离心管中,轻轻敲打混匀后1000r/m离心5-10min,重复洗涤细胞2次。
(3)待杂交CD14细胞(巨噬细胞)准备:本发明分选的单核巨噬细胞以基础培养基调整总细胞数到1×108~2×108用于细胞融合。以台盼兰染色用相差显微镜检查,活细胞数应高于80%为合格。
(4)细胞融合:将CD14细胞(单核巨噬细胞)与骨髓瘤细胞以10∶1-5∶1的比例加入离心管中,混和均匀,1000r/m离心5min,弃去上清,轻轻敲打管底至细胞无颗粒状沉淀,重复2次。在37℃水浴中轻轻旋转预热离心管,取出后无菌条件下将预热的1000μL的50%PEG3000在60s内沿管壁滴加到融合管中同时轻轻旋转离心管,之后将预热的25mL的基础培养基在3-5min内也沿管壁滴加到离心管中,在加入的过程中轻轻地旋转离心管,然后静置于37℃水浴10min,1000r/m离心5min,弃去上清,加入50mL HA T培养基。适当混匀后接种到96孔培养板中,置于37℃,5%的CO2培养箱中培养。
(5)具有吞噬功能的单核巨噬细胞株筛选:观察96孔培养板中细胞生长情况,7-10天后仅有杂交瘤细胞能够生长分裂,此时弃去HAT培养基,更换完全培养基。细胞克隆生长面积达到1/10个细胞孔时,去培养上清,选择有生长状态良好的杂交瘤细胞株的培养孔,显微镜下标记细胞株生长的位置、大小,使用无菌枪头在标注的位置吸取细胞克隆到新的有完全培养基的培养孔内,然后依次倍比稀释到后面数孔,37℃,5%CO2培养箱内培养一周左右,显微镜下观察细胞生长情况,待细胞克隆长满至孔底面积1/10以上时,取细胞或培养上清检测杂交瘤巨噬细胞(Mφ)株功能。
①杂交瘤巨噬细胞株吞噬细菌功能检测:将巨噬细胞与葡萄球菌或白色念珠菌悬液混合温育,涂片,固定,碱性亚甲兰液染色,在油镜下观察吞噬情况,计数吞噬细菌和未吞噬细菌的巨噬细胞数比例,以吞噬细菌功能强的巨噬细胞作为备选阳性克隆株。
②杂交瘤巨噬细胞株吞噬HIV功能检测:取疾控中心保存的艾滋病(AIDS)患者的血浆与杂交瘤巨噬细胞株混合培养后,分离细胞株,PBS清洗3次,测定经裂解的吞噬细胞株吞噬HIV的功能,具体根据HIV-1p24抗原检测试剂盒(酶联免疫法,上海启发生物科技有限公司)操作,以已知浓度0pg/ml、0.5pg/ml、1pg/ml、2.5pg/ml、5pg/ml、20pg/ml、40pg/ml、80pg/ml的p24抗原作为对照,最低检测限低于5pg/ml,测定范围0~400pg/ml,线性范围0.5pg/ml~80pg/ml,15min内450nm测定吸光度(OD),空白对照校准品吸光度值不高于0.050,0pg吸光度值不高于0.100,1000pg/ml吸光度不低于1.000,当吸光度>0.12时被认为是阳性。具体按试剂盒说明书操作。
③杂交瘤巨噬细胞株产生巨噬细胞因子检测:以人巨噬细胞移动抑制因子(MIF)ELISA检测试剂盒(上海百蕊生物科技有限公司)按说明书操作,检测范围为0~800pg/ml,敏感度为1.0pg/ml,可在白色背景下,直接用肉眼观察:反应孔内颜色越深,阳性越强,阴性反应为无色或极浅,依据所呈颜色的深浅,以“+”、“-”号表示。也可测OD值:在ELISA检测仪上,于450nm(若以ABTS显色,则410nm)处,以空白对照孔调零后测各孔OD值,若大于规定的阴性对照OD值的2.1倍,即为阳性,具体按试剂盒说明书操作。MIF是集细胞因子、生长因子、激素和酶特性于一身的多效能蛋白分子,作为固有免疫和炎症反应的调节因子发挥中枢性的作用,在各种感染和急慢性炎症性疾病中发挥多种免疫功能。
根据检测结果,挑选具有较强巨噬细胞功能的培养孔中的细胞克隆重复进行下一轮稀释培养,重复2-3轮,检测功能稳定后取出,转入培养瓶大量培养。
(6)杂交瘤巨噬细胞株的保存与复苏:保存前12小时调整细胞生长状态,取一瓶生长旺盛,形态良好的细胞,适当消化后制成细胞悬液,1000r/min离心5min,去上清液,轻弹管底使细胞松散,加入4℃保存的9份完全培养液和1份DMSO,分装细胞冻存管,1mL/管,-70℃冰箱过夜,取出后将冻存管放入液氮容器中保存备用。复苏前准备好40℃左右的热水,将冻存管从液氮中小心取出,迅速置于热水中均匀摇动使细胞解冻,解冻后在1000r/min离心5min,超净工作台内无菌条件下打开冻存管,将解冻后的细胞用完全培养液洗涤一次,然后在1000r/min离心5min,弃去上清,以备作扩大培养。
6、杂交瘤巨噬细胞株治疗细胞制备
即杂交瘤巨噬细胞株的扩增培养。将上述细胞沉淀使用完全培养液轻轻重悬后移入培养瓶内,置37℃,5%CO2培养箱中培养。反复传代扩增培养,直至所需的杂交瘤细胞株数量,每传代培养阳性杂交瘤细胞株10代,检测巨噬细胞杂交瘤细胞株的功能,观察是否稳定。继续在数瓶内进行大规模产业化制备,保存备用。
(二)CD4+T细胞株的制备
1、原代淋巴细胞的来源
有以下种途经:①用于科研保存的传染病实验室样本库中冻存的淋巴细胞株(经灭活HIV全病毒免疫但未感染HIV的淋巴细胞);②购买血站新鲜浓缩白细胞,然后进行过灭活HIV感染株免疫的淋巴细胞;③从商家直接购买的T淋巴细胞系(株);④用于科研保存的脐带血淋巴细胞(经灭活HIV免疫);⑤直接取自HIV-1感染者的外周血淋巴细胞(用于自身),采用Histopaque淋巴细胞分离液分离单个核细胞(PBMC)。
2、CD4+T细胞的制备
①主要试剂与仪器:CD4、CD8免疫磁珠(德国美天旎生物技术有限公司);异硫氰酸荧光素CD4-FITC、CD8-FITC、IgG1-FITC(Immunotech公司);淋巴细胞分离液(上海恒信生化试剂有限公司);乙二胺四乙酸(EDTA)、0.2%台盼蓝染色液(上海生工生物工程技术服务公司);新生牛血清(Hyclone公司);MiniMACS磁力分离系统(德国美天旎生物技术有限公司);EpicsXL型流式细胞仪(美国BeckmanCoulter公司)。②单个核细胞(PBMC)的分离(密度梯度离心法):无菌取20mL静脉血,并肝素钠(500IU/mL)2mL抗凝;PBS液将血液稀释2~3倍,充分混匀后将6mL抗凝静脉血用滴管沿管壁缓慢叠加于已加入4mL淋巴细胞分离液的10mL离心管中水平离心机中水平离心(400r/min,20℃)35min;离心后管内分为3层,上层为血浆和PBS液,下层主要为红细胞和粒细胞,中层为淋巴细胞分离液,在上、中层界面处有一以单个核细胞为主的白色云雾层狭窄带为PBMC,用毛细吸管插到云雾层,吸取PBMC置入另一50mL离心管中,加入5倍以上体积PBS离心(300r/min,20℃)10min,弃上清50mLPBS重悬细胞,离心(350r/min,20℃)15min,弃上清,加入Buffer(PBS+0.5%新生牛血清+2mmol/LEDTA,pH7.2)2mL重悬细胞,取15uL细胞悬液加入血球计数板上显微镜下计数4个大方格内的细胞(PBMC)总数。③CD4+T细胞和CD8+T细胞的分离纯化:PBMC细胞悬液均分至两个1.5mLEppendorf管,离心(300r/min,20℃)10min,弃去上清,重悬细胞每80uLBuffer含细胞数107个,每107个细胞加20uLCD4MicroBeads或CD8MicroBeads,充分混匀,在4~8℃孵化15min,用1mLBuffer洗涤细胞,离心(300r/min,20℃)10min,弃去上清500uLBuffer重悬细胞,将MS分离柱放置在MACS分离器的磁场中,以500uLBuffer漂洗,将500uL细胞悬液通过分离柱,用500uLBuffer冲洗分离柱重复操作3次,收集流出液,流出液中含非CD4+T淋巴细胞或非CD8+T淋巴细胞,自分离器中取出分离柱,用1000uLBuffer加压冲洗分离柱,收集流出液,此为CD4+T淋巴细胞或CD8+T淋巴细胞(细胞活力检测:细胞纯化前后分别取15uL细胞悬液与等体积台盼蓝溶液混合,显微镜下观察不着色发亮者为活细胞,着色胀大者为死细胞,计算200个细胞中活细胞的百分比)。
3、体外扩增CD4+T细胞
有文献报道利用T细胞表面CD3分子的单克隆抗体作为细胞生长的刺激剂,大量培养艾滋病患者分离的T细胞后,作为自身治疗性细胞回输。但HIV也随着HIV感染细胞的培养繁殖而在胞内增殖,增量T细胞的回输也导致了增量HIV的回输。本发明以SV40和/或hTERT永生化CD4+T细胞,并以CD3单克隆抗体为细胞生长刺激剂,大量扩增CD4+T细胞。
以CD3单克隆抗体为细胞生长刺激剂的方法是:将抗CD3单抗(CD4+T细胞同时含有CD3分子)包被到培养板上刺激单个核细胞(淋巴细胞)生长,称为抗CD3抗体包被法,可获得很好的扩增效果,应用这种方法扩增的淋巴细胞已用于肿瘤的二期临床治疗并取得了一定的疗效。国外文献报道[Shimizu等]亦用此方法培养了5例晚期艾滋病患者的淋巴细胞,培养4周就可获得1000倍的扩增,且扩增的细胞群中CD4+/CD8+T均可大量扩增(CD4+T细胞更明显)。另一种是抗CD3/CD28双抗交联法,即将抗CD3/CD28双抗交联于滋珠上作为刺激剂培养HIV感染者外周血单个核细胞(淋巴细胞),可以扩增大量的CD4+T细胞,并且扩增的CD4+T细胞具有对抗HIV感染的能力,其培养过程中病毒也低于检测水平,之后发现这可能与CD28提供了第二信号,选择性诱导分泌大量的Th1细胞因子和趋化因子有关,用此方法扩增的CD4+T细胞已用于HIV感染者的临床治疗回输,无风险但效果一般。
以hTERT永生化CD4+T细胞的方法是:以内切酶EcoR I和Xho I双酶切质粒pCIneo-hTERT和载体pLXSNneo,以Ligation Mix连接经PCR扩增、凝胶电泳分离的hTERT和pLXSNneo酶切产物,构建pLXSNneo-hTERT重组子,转化DH5a感受态细胞以扩增、纯化并挑取耐氨苄青霉素菌落抽提质粒,以脂质体转染法导入离体传代呈对数生长的T淋巴细胞,使重组子与细胞的DNA整合,并扩大培养经G418筛选的阳性重组子的克隆,筛选细胞形态、生长曲线、染色体核型、裸鼠致瘤试验、转染细胞端粒酶活性、hTERT mRNA表达产物、免疫组织化学染色、细胞增殖周期及细胞凋亡率符合永生化细胞特性并与原代细胞相同或相近者作为hTERT永生化的CD4+T细胞。
以SV40永生化CD4+T细胞的方法是:以T4DNA连接酶连接同时经BamHI酶切的pcDNA3.1(-)DNA和PCR扩增、琼脂糖凝胶电泳分离的SV40LTag DNA,构建SV40LTag-pcDNA3.1(-)重组质粒,转化DH5a大肠杆菌感受态细胞以扩增、纯化并挑取耐氨苄青霉素的菌落抽提质粒,以脂质体转染法导入体外培养的T淋巴细胞,使重组子与细胞的DNA整合,以G418筛选的含阳性重组子的细胞,作传代、扩大培养,筛选细胞形态、细胞生长曲线、染色体核型、裸鼠致瘤试验、转染细胞DNA中SV40大T基因检测、mRNA表达产物测定及DNA序列测定结果符合永生化细胞特性并与原代细胞相同或相近者作为SV40永生化的CD4+T细胞。
①以hTERT永生化CD4+T细胞的具体方法
(I)hTERT的提取:(i)酶切pClneo-hTERT:hTERT位于质粒pClneo-hTERT的EcoRI与SalI位点之间,pLXSNneo载体多克隆位点(MCS)含EcoRI与XhoI酶切位点。市售购买pCIneo-hTERT质粒,溶解于适量的超净H2O或TE缓冲液中,加2uL10×酶切缓冲液和18uL H2O,加限制性内切酶EcoR I和Xho I各0.5ul,37℃温育1h,75℃加热15min,灭活酶,加入5uL电泳加样缓冲液(也可通过加入0.5mol/L EDTA)终止反应,按常规PCR法扩增hTERT后,收取扩增物以备电泳。(ii)hTERT电泳:取电泳级琼脂糖以电泳缓冲液配成10%琼脂糖凝胶,倒入已封好的凝胶灌制平台上,插上样品梳,待胶凝固后从制胶平台上除去封带,拔出梳子,放入加有足够电泳缓冲液的电泳槽中,缓冲液高出凝胶表面大约1mm,用适量的10×加样缓冲液制备hTERT酶切样品,然后用移液器将样品加入样品孔中,并同时做合适的标准对照物,接通电极,使hTERT向阳极移动,然后在1-10V/cm(80V)凝胶的电压下电泳至足够分离hTERT片段的距离时(30min),关闭电源。(iii)hTERT纯化与回收:从琼脂糖中分离hTERT条带:在长波紫外光源下将含目标hTERT片段的凝胶条带切下装入透析袋中,向透析袋内加入2ml电泳缓冲液,使之浸没凝胶,并排空汽泡,将透析袋水平放入电泳槽(长度方向与电泳平行),加入适量缓冲液将透析袋浸没(约6-7mm),接通电源,150伏电洗,在紫外灯下观察待hTERT全部移出凝胶,改变电场方向继续通电1分钟,从透析袋中吸出缓冲液于1-5ml Eppendorf管中,加入1.5倍体积正丁醇,混匀抽提去EB,在台式离心机上最高速2分钟,吸去上层正丁醇溶液,如此重复二次,自下层hTERT的溶液中加入等体积酚氯仿(2个)抽提2次,上清转入另一Eppendorf管中加入1/10倍体积3M NaAc、2倍体积预冷无水乙醇,于20℃过夜,12000g,4℃下离心10分钟,得hTERT沉淀,弃上清,加入70%乙醇洗涤2次后弃干乙醇,加入50μl TE溶解hTERT。此外,还可用低熔点琼脂糖凝胶法、hTERT滤膜插片法等将目的hTERT片段从凝胶中分离、纯化出来。
(II)hTERT与pLXSNneo载体的连接:取9μl上述纯化的hTERT成份(0.1-5μg)、1μl10mmol/L ATP、10ul Ligation Mix或大肠杆菌DNA连接酶、2ul pLXSNneo空载体混合,15℃温育24h,构建pLXSNneo-hTERT重组子。
(III)pLXSNneo-hTERT重组子的纯化、扩增、鉴定:(i)大肠杆菌感受态的制备:其基本方法是用冰预冷的CaCl2或多种2价阳离子等处理细菌,使之进入感受态得以转化,用CaCl2制备新鲜或冷冻的大肠杆菌感受态细胞,常用于成批制备感受态细菌,本法适用于大多数大肠杆菌菌株,操作过程简述如下:从37℃培养16~20h的新鲜平板中挑取一个单菌落(如大肠杆菌DH52),或1ml新鲜的16~20h过夜培养物,转到一个含有100mlLB培养基的1L或500ml烧瓶中,于37℃剧烈振摇培养约2~3h(旋转摇床200~300r/min),每隔20~30min测量OD600值≈0.4,在无菌条件下将细菌转移到一个,用冰预冷的50ml聚丙烯离心管中,在冰上放置10~20min,于4℃用SorvallGS2转头(或与其离心管相配的转头)以4000r/min离心10min,以回收细胞,倒数培养液,将管倒置1min以使最后残留的痕量培养液流尽,以10ml用冰预冷的0.1mMCaCl2重悬每份沉淀,放于冰上,于4℃用SorvallGS3转头(或与其相应的转头)以4000r/min离心10min,以回收细胞,倒出培养液,将管倒置1min以使最后残留的痕量培养液流尽,每50ml初始培养物用2ml冰预冷的0.1M CaCl2重悬每份沉定,此时,可以迅速将细胞分装成小份,液氮中冰冻,-70℃贮存备用。(ii)以感受态大肠杆菌纯化、扩增pLXSNneo-hTERT重组子:用冷却的无菌吸头从每种感受态细胞悬液中各取200μl转移到无菌的微量离心管中,每管加DNA或连接反应混合物(体积≤10μl,DNA≤50ng),轻轻旋转以混匀内容物,在冰中放置30min,将离心管放到预加温到40℃的循环水浴中的试管架上,放置90s~2min,不要摇动试管,快速将管转移到冰浴中,使细胞冷却1~2min,每离心管加800μlSOC培养基,用水浴将培养基加温到37℃,然后将管转移到37℃摇床上,温育45min使细菌复苏,并且表达质粒编码的抗生素抗性标记基因,将适当体积(每90mm平板可达200μl)已转化的感受态细胞转移到含200mmol/LMgSO4和相应抗生素的SOB培养基上,将平板置于室温至液体被吸收,倒置平皿,于37℃培养,12~16h后可出现菌落。(iii)筛选、扩增重组子:用无菌牙签或灭菌接种针挑选单个菌落接种于5mL无菌的LB培养基或丰富培养基(如超级肉汤或TB超级肉汤培养基)中,培养过夜后,再加入到500mL含LB培养基(含有适当抗生素)的2L烧瓶中,再于37℃培养至饱和状态(OD600≈4,为提高产量,应采用表面积较大及带折流板的烧瓶以尽量增大通气度,振摇速度应大于400r/min),于4℃,6000g离心10min,用4mL GTL溶液重悬沉淀,并转移到一个容积≥20mL的高速离心管中(细菌沉淀可以在-20℃或-70℃无限期保存),加入1mL新配的含25mg/mL溶菌酶的GTE溶液,重悬沉淀,于室温放置10min,加入10mL新配NaOH/SDS溶液,并且轻轻混匀直至液体变得均一、清亮而粘稠,于冰上放置10min,加入7.5mL乙酸溶液,用吸管轻轻搅拌直至粘稠度下降并形成大的沉淀,于冰上放置10min,于4℃,20 000g离心10min,将上清轻轻倒入至另一个干净的离心管中,如果有可见的飘浮物可用数层纱布过滤,加入0.6倍体积的异丙醇,颠倒混匀,室温放置5~10min,于室温,1 500g离心10min,加入2mL 70%乙醇轻轻洗涤沉淀,然后短暂快速离心,吸去乙醇,真空干燥(沉淀可在4℃长期保存)。(iv)重组质粒的鉴定与扩增:挑取平皿上的单菌落,接种于3ml含100ug/ml氨苄青霉素LB培养基中,37℃,250r/min摇床中培养,14h后收集培养物,4℃、10000r/min离心5min,按试剂盒说明书小量提取并纯化重组质粒;以EcoRI和HindIII双酶切重组质粒反应体系:限制性内切酶各0.5ul、10×buffer 2ul、重组质粒10ul、加水补足至20ul,37℃酶切1h。酶切产物于80V电压条件下进行0.8%琼脂糖电泳,时间30min,凝胶成像系统拍照;按常规测定重组质粒的序列;重组质粒经酶切、测序鉴定准确后,将含有该质粒的细菌接种至LB培养液中,扩增培养,按大剂量质粒抽提试剂盒说明书进行大剂量质粒抽提纯化,紫外分光光度计测定质粒浓度及纯度后备用。
(IV)CD4+T细胞:从本发明“(2)CD4+T细胞的制备”取样制备。
(V)CD4+T细胞预培养:将上述细胞接种于含5~10nmol/L胰岛素、20%胎牛血清的RPMI1640液中,或接种于含20%胎牛血清、5~10nmol/L胰岛素的低糖DMEM细胞培养基中,一般接种于3ml新鲜配制的培养基(1.6%1M HEPES缓冲液;15%胎牛血清(FBS);1%青霉素和链霉素;PRMI 1640补足到100%),置于37℃,体积分数5%CO2培养箱内,培养1-2天,离心,去上清液,备用。
(VI)pLXSNneo-hTERT重组子导入T淋巴细胞及扩大培养:在1.5ml微量离心管中制备下列溶液:管A,将pLXSNneo-hTERT重组子溶于100μl无血清培养液中;管B,将20μl Lipofectamine溶于80μl无血清培养液中,将管A和管B混匀,室温下静置45min,用无血清培养液洗涤上述T淋巴细胞2次。在Lipofectamine-pLXSNneo-hTERT混合物中加入1ml无血清培养液,轻轻混匀,滴加至上述T淋巴细胞中,加入1ml无血清培养液(胎牛血清浓度为20ml/L),在CO2培养箱培养10h,吸出转染液,加4ml完全培养液(胎牛血清浓度为20%),继续培养20h,弃去培养液,更换浓度为400mg·L-1的G418培养液继续培养,8天后选择活细胞作扩大培养后,再加大G418浓度到800mg·L-1,将能在高浓度的G418环境中稳定生长的细胞继续进行扩增培养。培养9天左右镜下观察,可见淋巴细胞明显增大,出现聚集现象。如果细胞增长慢,或细胞密度低,或培养液pH值呈酸性,吸出半量培养液,进行等量换液。当总量达到14ml时转移到75ml培养瓶中,每2-3周加入5-10ml新鲜培养基。细胞培养至9-10周(约第75代),仍处于对数生长期,即细胞增加数量与培养时间呈倍增关系,死亡细胞少于10%(通过读取培养容器的刻度判断细胞数量的增加情况;通过台盼蓝染色法鉴别死细胞和活细胞。因为正常的活细胞,胞膜结构完整,能够排斥,使台盼蓝不能够进入胞内;而丧失活性的细胞,胞膜的通透性增加,可被台盼蓝染成蓝色,可判断为细胞已经死亡。方法是每周吸取一定量的细胞培养悬液,与台盼蓝染色剂混合后置室温5~10分钟,然后制成细胞薄片,在显微镜下计数1000个细胞总数,计算着色的死细胞和不着色的活细胞的百分比)。此后随着培养代数的增加和培养时间的延长,细胞数量的增加变慢、死亡细胞越来越多,直至细胞不再增加,甚至溶解、减少、全部死亡。当总量达到45ml时,置50ml离心管中,离心1500转,10分钟,弃上清后,加入3ml冻存培养基(5%二甲基亚枫(dimethyl sufoxide),95%FBS)混匀,成细胞悬浮液(细胞浓度约为105/ml)。冻存管分装,1ml/管,置-20℃2h,再置-70℃2h,然后冻存在-196℃液氮中(或立即置零下80度,1-2小时后移入液氮罐中)。
(VII)永生化CD4+T细胞生物学特性的鉴定:(i)观察细胞形态:可见淋巴细胞明显增大,出现聚集现象,具有淋巴母细胞化特征。(ii)观察细胞生长曲线:取生长较好的转染细胞,制成细胞悬液,经计数,分别取1.4×104细胞接种于30个含15FBS低糖DMEM培养基培养瓶。每天取2瓶细胞进行计数,计算均值,连续观察直至细胞数量明显下降,培养3天后每隔2天给未计数的细胞换液,采用同样方法观察转染细胞在hepato ZYME-SFM无血清培养基中的生长情况。结果以培养时间为横轴,细胞数量为纵轴(对数),描绘在半对数座标上制成曲线后即成该细胞的生长曲线,永生化细胞系呈典型的“S”特征或“穹隆”形成;(iii)检查染色体:通过分析染色体核型,如果染色体核型为二倍体“46,XX”或“46,XY”,则说明该细胞系没有发生恶性转化(同时可用流式细胞仪分析细胞系中是否出现异常的DNA群体,如果没有,也说明细胞系未出现瘤性特征)。染色体核型分析方法是:按5mL培养液中加入预热的250ug/ml秋水仙素100ul,混匀后置37℃培养箱4小时,经离心、去上清液、低渗、固定、制片、G显带后分析染色体核型;(iv)流式细胞术检测:检测第19代细胞系中合成、分裂的细胞比例,如果其增殖能力明显比未建系的正常细胞增强,说明是hTERT整合、表达的结果。(vii)DNA序列测定:按常规测序仪检测,显示hTERT基因序列。(v)转染细胞DNA中hTERT检测:如以免疫组织化学检测,hTERT转染的细胞核内染色可见大量棕色颗粒,表明hTERT已整合入细胞内;(vi)mRNA表达产物测定:取100μl体系的PCR扩增产物,用凝胶回收试剂盒(Takara,日本)回收产物,取2μl DNA溶液稀释100倍,测浓度,余下的DNA及上、下游引物各10μl进行测序。
(VIII)hTERT介导CD4+T细胞库:筛选并继续传代、扩大培养经上述鉴定后符合永生化细胞特性并与原代细胞相同或相近的细胞,取生长状态良好、处于对数生长期的不同世代的细胞,经离心分离(1 200r/min,6min),用含二甲亚砜的冻存液0.5~1ml重悬细胞,细胞密度为5×105个/ml,加入冻存管,经4℃,0.5h;-20℃,2h;-70℃,过夜,入-196℃液氮冻存,以此法构建生物学特性稳定的永生化CD4+T细胞库备用。
②以SV40永生化CD4+T细胞的具体方法
(I)SV40大T抗原DNA的提取:(i)SV40DNA酶切:从市售购买含有大T抗原基因的SV40冰冻干粉或SV40质粒,溶解于适量的H2O或TE缓冲液中,加2uL10×酶切缓冲液和18uL H2O,加限制性内切酶BamH I(1-5U/ugDNA),37℃温育1h,75℃加热15min,灭活酶,加入5uL电泳加样缓冲液(也可通过加入0.5mol/L EDTA)终止反应以备电泳。(ii)SV40DNA电泳:取电泳级琼脂糖以电泳缓冲液配成10%琼脂糖凝胶,倒入已封好的凝胶灌制平台上,插上样品梳,待胶凝固后从制胶平台上除去封带,拔出梳子,放入加有足够电泳缓冲液的电泳槽中,缓冲液高出凝胶表面约1mm,用适量的10×加样缓冲液制备DNA样品,然后用移液器将样品加入样品孔中,并同时做合适的DNA分子量标准对照物,接通电极,使DNA向阳极移动,在1-10V/cm凝胶的电压下电泳至足够分离DNA片段的距离时,关闭电源。(iii)从琼脂糖中分离约2600bp SV40大T抗原DNA:在300-360nm长波紫外光源下(使用长波紫外光源以防止DNA损伤)将含目标DNA片段的凝胶条带切下装入透析袋中,向透析袋内加入2ml电泳缓冲液,使之浸没凝胶,并排空汽泡,将透析袋水平放入电泳槽(长度方向与电泳平行),加入适量缓冲液将透析袋浸没(约6-7mm),接通电源,150伏电洗,在紫外灯下观察待DNA全部移出凝胶,改变电场方向继续通电1分钟,从透析袋中吸出缓冲液于1-5ml Eppendorf管中,加入1.5倍体积正丁醇,混匀抽提去EB,在台式离心机上最高速2分钟,吸去上层正丁醇溶液,如此重复二次,自下层言DNA的溶液中加入等体积酚氯仿(2个)抽提2次,上清转入另一Eppendorf管中加入1/10倍体积3M NaAc、2倍体积预冷无水乙醇,于20℃过夜,12000g,4℃下离心10分钟,得DNA沉淀,弃上清,加入70%乙醇洗涤2次后弃干乙醇,加入50μl TE溶解DNA。此外,还可用低熔点琼脂糖凝胶法、DNA滤膜插片法等将目的DNA片段从凝胶中分离、纯化出来。
(II)SV40大T抗原DNA与pcDNA3.1基因载体的连接:取9μl上述DNA成份(0.1-5μg)、10μl 2×连接缓冲液、1μl 10mmol/L ATP、T4DNA连接酶(20~500粘性末端单位)或大肠杆菌DNA连接酶、pcDNA3.1空载体混合,15℃温育24h,构建成SV40T/pcDNA3.1重组子。
(III)SV40T/pcDNA3.1重组子的扩增、分离与鉴定:(i)大肠杆菌感受态的制备:其基本方法是用冰预冷的CaCl2或多种2价阳离子等处理细菌,使之进入感受态得以转化,用CaCl2制备新鲜或冷冻的大肠杆菌感受态细胞,常用于成批制备感受态细菌,本法适用于大多数大肠杆菌菌株,操作过程简述如下:从37℃培养16~20h的新鲜平板中挑取一个单菌落(如大肠杆菌DH52),或1ml新鲜的16~20h过夜培养物,转到一个含有100mlLB培养基的1L或500ml烧瓶中,于37℃剧烈振摇培养约2~3h(旋转摇床200~300r/min),每隔20~30min测量OD600值≈0.4,在无菌条件下将细菌转移到一个,用冰预冷的50ml聚丙烯离心管中,在冰上放置10~20min,于4℃用SorvallGS2转头(或与其离心管相配的转头)以4000r/min离心10min,以回收细胞,倒数培养液,将管倒置1min以使最后残留的痕量培养液流尽,以10ml用冰预冷的0.1mMCaCl2重悬每份沉淀,放于冰上,于4℃用SorvallGS3转头(或与其相应的转头)以4000r/min离心10min,以回收细胞,倒出培养液,将管倒置1min以使最后残留的痕量培养液流尽,每50ml初始培养物用2ml冰预冷的0.1M CaCl2重悬每份沉定,此时,可以迅速将细胞分装成小份,液氮中冰冻,-70℃贮存备用,用冷却的无菌吸头从每种感受态细胞悬液中各取200μl转移到无菌的微量离心管中,应在每管中加DNA或连接反应混合物(体积≤10μl,DNA≤50ng),轻轻旋转以混匀内容物,在冰中放置30min,将离心管放到预加温到40℃的循环水浴中的试管架上,放置90s~2min,不要摇动试管,快速将管转移到冰浴中,使细胞冷却1~2min,每离心管加800μlSOC培养基,用水浴将培养基加温到37℃,然后将管转移到37℃摇床上,温育45min使细菌复苏,并且表达质粒编码的抗生素抗性标记基因,将适当体积(每个90mm平板可达200μl)已转化的感受态细胞转移到含200mmol/LMgSO4和相应抗生素的SOB培养基上,将平板置于室温至液体被吸收,倒置平皿,于37℃培养,12~16h后可出现菌落。(ii)重组子的筛选、扩增与提取:用无菌牙签或灭菌接种针挑选单个菌落接种于5mL无菌的LB培养基或丰富培养基(如超级肉汤或TB超级肉汤培养基)中,培养过夜后,再加入到500mL含LB培养基(含有适当抗生素)的2L烧瓶中,再于37℃培养至饱和状态(OD600≈4,为提高产量,应采用表面积较大及带折流板的烧瓶以尽量增大通气度,振摇速度应大于400r/min),于4℃,6000g离心10min,用4mL GTL溶液重悬沉淀,并转移到一个容积≥20mL的高速离心管中(细菌沉淀可以在-20℃或-70℃无限期保存),加入1mL新配的含25mg/mL溶菌酶的GTE溶液,重悬沉淀,于室温放置10min,加入10mL新配NaOH/SDS溶液,并且轻轻混匀直至液体变得均一、清亮而粘稠,于冰上放置10min,加入7.5mL乙酸溶液,用吸管轻轻搅拌直至粘稠度下降并形成大的沉淀,于冰上放置10min,于4℃,20 000g离心10min,将上清轻轻倒入至另一个干净的离心管中,如果有可见的飘浮物可用数层纱布过滤,加入0.6倍体积的异丙醇,颠倒混匀,室温放置5~10min,于室温,1 500g离心10min,加入2mL 70%乙醇轻轻洗涤沉淀,然后短暂快速离心,吸去乙醇,并真空干燥(沉淀可在4℃长期保存)。(iii)重组子的鉴定:上述从感受态大肠杆菌中提取的DNA(含重组子SV40T/pcDNA3.1),同上法用限制性内切酶BamH I进行酶切,10g/L琼脂糖凝胶电泳鉴定,获得大小约2600bp及5600bp的2条带,前者符合GenBank中SV40T片段的大小。
(IV)CD4+T细胞:从本发明“(2)CD4+T细胞的制备”取样制备。
(V)CD4+T细胞预培养:将上述细胞接种于含5~10nmol/L胰岛素、20%胎牛血清的RPMI1640液中,或接种于含20%胎牛血清、5~10nmol/L胰岛素的低糖DMEM细胞培养基中,一般接种于3ml新鲜配制的培养基(1.6%1M HEPES缓冲液;15%胎牛血清(FBS);1%青霉素和链霉素;PRMI 1640补足到100%),置于37℃,体积分数5%CO2培养箱内,培养1-2天,离心,去上清液,备用。
(VI)SV40T/pcDNA3.1的导入及扩大培养:在1.5ml微量离心管中制备下列溶液:管A,将SV40T/pcDNA3.1溶于100μl无血清培养液(胎牛血清浓度为20ml/L)中;管B,将20μl Lipofectamine溶于80μl无血清培养液中,将管A和管B混匀,室温下置45min。用无血清培养液洗涤上述T淋巴细胞2次。在Lipofectamine-SV40T/pcDNA3.1混合物中加入1ml无血清培养液,轻轻混匀,再滴加至上述T淋巴细胞中,然后加入1ml无血清培养液(胎牛血清浓度为20ml/L),在CO2培养箱培养10h,吸出转染液,加4ml完全培养液(胎牛血清浓度为20%),继续培养20h,弃去培养液,更换浓度为400mg·L-1的G418培养液继续培养,8天后选择活细胞作扩大培养后,再加大G418浓度到800mg·L-1,将能在高浓度的G418环境中稳定生长的细胞继续进行扩增培养。培养9天左右镜下观察,可见淋巴细胞明显增大,出现聚集现象。如果细胞增长慢,或细胞密度低,或培养液pH值呈酸性,吸出半量培养液,进行等量换液。当总量达到14ml时转移到75ml培养瓶中,每2-3周加入5-10ml新鲜培养基。细胞培养约6-8周(约第55代),仍处于对数生长,即培养时间与细胞增加数量呈倍增关系,死亡细胞少于10%(通过读取培养容器的刻度判断细胞数量的增加情况;通过台盼蓝染色法鉴别死细胞和活细胞。因为正常的活细胞,胞膜结构完整,能够排斥,使台盼蓝不能够进入胞内;而丧失活性的细胞,胞膜的通透性增加,可被台盼蓝染成蓝色,可判断为细胞已经死亡。方法是每周吸取一定量的细胞培养悬液,与台盼蓝染色剂混合后置室温5~10分钟,然后制成细胞薄片,在显微镜下计数1000个细胞总数,计算着色的死细胞和不着色的活细胞的百分比)。此后随着培养代数的增加和培养时间的延长,细胞数量的增加变慢、死亡细胞越来越多,直至细胞不再增加,甚至溶解、减少、全部死亡。当总量达到45ml时,置50ml离心管中,离心1500转,10分钟,弃上清,加入3ml冻存培养基(5%二甲基亚枫(dimethyl sufoxide),95%FBS)混匀,成细胞悬浮液(细胞浓度约为105/ml)。冻存管分装,1ml/管,置-20℃2h,再置-70℃2h,然后冻存在-196℃液氮中(或立即置零下80度,1-2小时后移入液氮罐中)。
(VII)永生化CD4+T细胞生物学特性的鉴定:(i)观察细胞形态:可见淋巴细胞明显增大,出现聚集现象,具有淋巴母细胞化特征。(ii)观察细胞生长曲线:取生长较好的转染细胞,制成细胞悬液,经计数,分别取1.4×104细胞接种于30个含15FBS低糖DMEM培养基培养瓶。每天取2瓶细胞进行计数,计算均值,连续观察直至细胞数量明显下降,培养3天后每隔2天给未计数的细胞换液,采用同样方法观察转染细胞在hepato ZYME-SFM无血清培养基中的生长情况。结果以培养时间为横轴,细胞数量为纵轴(对数),描绘在半对数座标上制成曲线后即成该细胞的生长曲线,永生化细胞系呈典型的“S”特征或“穹隆”形成;(iii)检查染色体:通过分析染色体核型,如果染色体核型为二倍体“46,XX”或“46,XY”,则说明该细胞系没有发生恶性转化(同时可用流式细胞仪分析细胞系中是否出现异常的DNA群体,如没有,说明细胞系未出现瘤性特征)。染色体核型分析方法是:按5mL培养液中加入预热的250ug/ml秋水仙素100ul,混匀后置37℃培养箱4小时,经离心、去上清液、低渗、固定、制片、G显带后分析染色体核型;(iv)流式细胞术检测:检测第19代细胞系中合成、分裂的细胞比例,如果其增殖能力明显比未建系的正常细胞增强,说明是SV40大T抗原整合、表达的结果。(viii)DNA序列测定:按常规测序仪检测,显示SV40大T抗原DNA序列。(v)转染细胞DNA中SV40大T基因检测:如以免疫组织化学检测,SV40转染的细胞核内染色可见大量棕色颗粒,表明SV40T抗原已整合入细胞内;也可用RT-PCR法检测T抗原在细胞中的表达,其中T抗原的引物:上游引物(A4239)5’-GTT ATG ATT ATA ACT GTT ATG-3’,下游引物(S4496)5’-GAA ATG CCA TCT AGT GAT-3’;扩增产物长度为268bp,扩增条件为94℃,5min,即:(94℃,1min;55℃,1min,-0.5℃/循环;72℃,1min)×30、(94℃,30S;40℃,30S,72℃,30S)×15,扩增体系为50μl:[Mg2+]2mmol/L、dNTPs 200μmol/L、引物浓度0.4μmol/L、Taq1U、模板5μl;实验组以第19代细胞的cDNA为模板(参照市售cDNA第一链合成试剂盒进行cDNA第一链合成,产物-20℃保存);阴性对照设两个,分别以无菌水、原代细胞的cDNA做模板,阳性对照以SV40DNA为模板(参照SDS-蛋白酶K法提取SV40DNA,因为SV40病毒无包膜,不使用SDS破膜,取5μl进行1.5%琼脂糖凝胶电泳检测,其余-20℃保存备用);(vi)mRNA表达产物测定:T抗原mRNA RT-PCR产物测序:取100μl体系的扩增产物,用凝胶回收试剂盒(Takara,日本)回收产物,取2μl DNA溶液稀释100倍,测浓度,余下的DNA及上、下游引物各10μl进行测序。
(VIII)SV40LT基因介导CD4+T细胞库:筛选并继续传代、扩大培养经上述鉴定后符合永生化细胞特性并与原代细胞相同或相近的细胞,取生长状态良好、处于对数生长期的不同世代的细胞,经离心分离(1 200r/min,6min),用含二甲亚砜的冻存液0.5~1ml重悬细胞,细胞密度为5×105个/ml,加入冻存管,经4℃,0.5h;-20℃,2h;-70℃,过夜,入-196℃液氮冻存,以此法构建生物学特性稳定的CD4+T细胞库备用。
(4)与CD4+T细胞相似功能颗粒的制备:可将CD4分子、基因重组的CD4分子及类似功能的分子通过常规化学偶联、交联、亲和吸附等固定于载体上制成包被有CD4分子的颗粒,或直接取用功能相似的颗粒替代CD4+细胞应用。本发明的CD4+T细胞代表其他CD4+细胞,包括用其他方法制备永生化CD4+T细胞。
二、艾滋病血液净化器的制备
1、净化剂的充填
以无菌生理盐水清洗所制杂交瘤巨噬细胞株和CD4+T细胞株,1000r/min离心,洗净后再次离心沉淀,直接取沉淀细胞,或按杂交瘤巨噬细胞株和CD4+T细胞株之比为1∶0.5~3的比例取沉淀细胞,装入丙烯酸酯之类高生物相容性材料制成的200ml圆柱形容器内,充填至4/5以上,制成血液净化细胞柱,封口备用。另取起载体作用的经100℃溶化后保温在39~41℃的0.7%、0.8%、0.9%、1.0%、1.1%的琼脂糖C1-4B生理盐水,按高浓度至低浓度依次取40ml琼脂糖加入细胞柱内,要求在先加入的琼脂糖冷却至37℃成为半固体后才接着加下一次,使细胞柱从上到下(从进口到出口)形成从低到高的琼脂糖浓度的分层分布,其中杂交瘤巨噬细胞和CD4+T细胞均被固定在凝胶中起吸附HIV的作用。琼脂凝胶所形成的滤孔随着琼脂糖浓度的增高而减少,净化器进口处琼脂糖浓度低,滤孔就大,有利于血浆灌流及细胞与HIV的结合反应;而出口处浓度高,滤孔就小,易于阻留HIV或大分子结合物,净化器组合了多种特异和非特异的HIV清除成份,以免特种毒株因免疫差异所致的无效治疗。
2、净化器的规格
上述制备的细胞柱即为净化器,为底径小、顶径大的圆柱形,或方形、漏斗形,容积为200~300ml,进出口均设有细胞筛网,进口处顶径筛网目数为800目;出口处底径筛网目数为2.0~5.0目(2.5~5.0目相当于0.1~0.2微米或100~200纳米),具体可制成2.0目、2.5目、3.0目、3.5目、4.0目、4.5目和5.0目的7种不同规格,用以阻挡120纳米的HIV病毒或更大的细菌;液体出口处设置目数为100目(相当于4微米)的细胞滤网,用以阻挡可能滤出的细胞;液体进出口与网筛之间设有缓冲区,有利于系统循环的稳定性。
3、净化器的材料
血液净化器选用丙烯酸酯之类的高分子材料,要求生物相容性好,几乎不激活补体、不引起炎症反应、不引起白细胞、血小板、血氧分压、补体C3a、C5a的改变。可通过共价、接枝、聚合等方法改进材料的结构、调节表面的不均匀性、亲水性、减少对凝血及氧化应激的影响、从而提高生物相容性、减少并发症的发生。将某些具有抗凝作用的物质固化在载体或净化器内表面的材料上,可抑制血液凝固,提高生物相容性,还可降低肝素用量,并有可能实现无肝素化。将肝素共价结合到聚醚砜表面,能提高净化器内表面的抗凝血性能。在醋酸纤维膜上共价固化亚油酸膜都可增加组织相容性和抗凝血效果。
三、分离器的制备
(一)血液分离器的制备
1、制备原理:①血细胞、细菌、病毒的分子大小:人体血液中有形成份(细胞)的大小为:正常红细胞大约为7微米(μm),是双凹圆盘状的细胞;白细胞分为5种,中性粒细胞约12μm,嗜酸性粒细胞略大些,嗜碱性粒细胞与中性粒细胞接近,小淋巴细胞6-8μm,与红细胞近似,单核细胞最大,约15-20μm。血小板为圆盘形,直径1~4微米到7~8微米不等,人的血小板平均直径为2-4微米,厚0.5~1.5微米。细菌的大小为:球菌的直径约在0.75-1.25μm之间,杆菌长度约在2-5μm,螺旋菌长约100-200μm。病毒的大小以纳米(nm)为单位[1cm=10mm,1mm=1000μm,1μm=1000nm],不同病毒间大小差异很大,最小的如植物的联体病毒(Geminiviruses)直径仅18-20nm,最大的动物痘病毒(Poxviruses)大小达300-450nm×170-260nm,最长的如丝状病毒科(Filoviridae)病毒粒子大小为80nm×790-14000nm,多数单个病毒粒子的直径在100nm左右,艾滋病毒为100-120nm(0.1-0.12μm)。②艾滋病患者血液中存在的相关成份:多核巨细胞(HIV感染细胞表面的gp120与CD4+细胞结合而成的大体积的HIV感染细胞)、gp120细胞(表面有gp120但以单个细胞存在的HIV感染细胞)、基因整合细胞(艾滋病感染初期或潜伏期,整合有HIV双链DNA,但细胞表面没有gp120的HIV感染细胞)、正常白细胞(未感染HIV的单个细胞存在的粒细胞、单核细胞、淋巴细胞)、红细胞、血小板、化学成份(蛋白质、糖类、脂类、电解质等)、游离的HIV、细菌及其他微生物。③多核巨细胞为天然的大体积细胞;gp120细胞和基因整合细胞可通过抗原和抗体的免疫反应使细胞凝集为大体积多细胞聚合体;游离的HIV可通过载体颗粒/免疫反应转变为大体积成份。④根据上述3点,可以制备能通过单个细胞但不能通过大体积细胞或颗粒的血液分离器。⑤选用具有选择性吸附功能的材料,经本发明的体外血液循环支路筛除血液中的HIV感染细胞。
2、血液分离器的材料与要求:同本发明的净化器,选用聚醋无纺布、醋酸纤维、脱脂棉等,要求生物相容性好,几乎不激活补体、不引起炎症反应和白细胞、血小板、血氧分压、C3a、C5a的改变。
3、血液分离器的型号与规格:血液分离器的外形制备成柱形结构(以醋酸纤维或脱脂棉等材料作滤芯)、扁平结构(以聚醋无纺布等材料作滤芯)等形状;孔径制备成150~250μm、50~150μm、15~40μm、8~15μm、5~8μm、3~5μm、1~2μm等型号。
4、血液分离器的应用原则:根据艾滋病患者的病情选用不同型号的分离器,原则上先选用大孔径型号做预筛滤,然后选用较小孔径的型号。重度艾滋病患者常发生严重的机会性感染,血液中含有不同大小的成份。如含有特大体积的真菌、螺旋菌、肿瘤细胞及其他异物,则选用孔径为150~250μm或50~150μm的分离器;如为筛滤HIV感染的单核巨噬细胞、多核巨细胞、多细胞聚合体及吸附有HIV的颗粒性物质,以及为了置换易受HIV感染的CD4+细胞,则选用15~40μm、8~15μm、5~8μm、3~5μm之类的型号。这几种型号近似或小于血液中单个红细胞、中性粒细胞、小淋巴细胞的体积,但红细胞、中性粒细胞及巨噬细胞具有变形运动的特性,能通过比自身体积更小的微孔。
(二)血浆分离器的制备
(1)制备原理:根据血细胞和血浆成份的分子大小制备。如人体血液中有形成份(血细胞)的大小为:正常红细胞大约为7微米(μm),是双凹圆盘状的细胞;白细胞分为5种,中性粒细胞约12μm,嗜酸性粒细胞略大些,嗜碱性粒细胞与中性粒细胞接近,小淋巴细胞6-8μm,与红细胞近似,单核细胞最大,约15-20μm。血小板为圆盘形,直径1~4微米到7~8微米不等,人的血小板平均直径为2-4微米,厚0.5~1.5微米。
(2)材料:可选用聚醋无纺布、醋酸纤维、脱脂棉等,要求生物相容性好,几乎不激活补体、不引起炎症反应、不引起白细胞、血小板、血氧分压、补体C3a、C5a的改变。可通过共价、接枝、聚合等方法改进材料的结构、调节表面的微观不均匀性、亲水性、减少对凝血及氧化应激的影响、从而提高筛滤充分性和生物相容性、减少并发症的发生。
(3)型号与规格:就分离器的外形来说,可以醋酸纤维或脱脂棉等材料作滤芯制备成柱形结构、以聚醋无纺布等材料作滤芯制备成扁平结构等形状;按待分离的血细胞和血浆成份的分子大小确定孔径。本发明所涉及的血浆分离器用性质稳定、生物相容性好、通透性高的高分子聚合物制成空心纤维型滤器,空心纤维膜直径为270~370μm,膜厚度为50μm,孔径为0.2~0.6μm,纤维长度为13.5~26μm。该孔仅准许血浆滤过,但能阻挡所有的细胞成分。
四、艾滋病净化治疗仪的构件
1、关键构件:(1)血液分离器:用于按体积大小筛除以多核巨细胞或多细胞聚合体状态存在的HIV感染细胞,即用于清除血细胞内的HIV;(2)血浆分离器:用于分离单个血细胞和血浆;(3)血浆净化器:用于吸附血浆中的HIV。
2、附加构件:包括血泵、肝素泵、动静脉压和空气监测、温度控制系统、除气系统、电导率监测系统、超滤监测和漏血监测等部分组成。(1)血泵(Blood Pump):用来推动血液循环以维持血液净化治疗的顺利进行,通常血泵部分往往具有转速检测功能,以监测病人的血流情况,因此血泵转轮与凹槽间距设定要精确,并需要经常调整,根据血路泵管的情况,一般将间距设定为3.2~3.3mm,不可太松,否则会造成血流检测不准;也不可太紧,否则会造成管路破裂。(2)肝素泵(Heparin Pump):肝素泵相当于临床上应用的微量注射泵,用以持续向筛滤管道(病人血液)中注射肝素,由于病人的血液在体外循环与空气接触,容易发生凝血现象,使用肝素泵可以防止凝血的发生。(3)动静脉压监测:动脉压监测主要用以动态监测血液分离器微孔的堵塞情况,另外用以监测体外循环血栓、凝固和压力的变化。当血流不足时,动脉压就会降低;当有凝血、血栓形成,特别是分离器微孔堵塞时,动脉压就会升高;静脉压监测用来监测管路血液回流的压力,当分离器微孔堵塞、凝血、血栓形成、血流不足以及静脉血回流针头脱落时,静脉压就会下降,如果血路回流管扭曲堵塞或回流针头发生堵塞时,静脉压就会升高。(4)空气监测(Air Detector):用来监测血液流路的空气气泡,一般用超声波探测的原理,为了避免病人发生空气栓塞而设置。当监测到有空气气泡时,检测系统会驱动动、静脉血路夹来阻断血流,防止危险的发生。
总之,在本发明关键构件和附加构件的基础上,引入计算机调控而制成操作的人性化、治疗的个性化、设计的安全性,以及模块化、自动监测及调控、液晶显示、自行判断警报原因及解除信号等微电脑处理的血液净化治疗仪。
五、艾滋病净化治疗仪的连接通路与使用方法
1、安装:如图1,以无菌操作连接各部件,包括血液分离器、血浆分离器、血浆净化器及各循环管路。
2、排气:以无菌生理盐水充液分离器、净化器及各循环管路,排除分离器、净化器及其循环管路内的气体、气泡,仔细检查,确认无气体、气泡后使用。
3、通液:将动脉血路管(1)接通艾滋病患者的动脉血管,在操作中再次仔细检查排气是否完全,液流是否通畅,并避免管内流液污染。
4、抗凝:从肝素泵(2)向液流中注射抗凝剂(肝素),初次为2500∪或20~30∪/kg。
5、启动:将动脉血路管(1)的一端与动脉血管相连通,将静脉管路(15)接通静脉血管,然后打开血液泵(2),血流量为100~150ml/min,如图1,当动脉血液经动脉血路管(1)、肝素和血液泵(2)进入血液分离器(3)时,因HIV感染而形成的大体积多核巨细胞被阻留在血液分离器(3)内,单个血细胞和血浆依次经血液出口(4)、血液泵(6)和循环管路(7)流入血浆分离器(8),分离的血浆依次经血浆泵(9)和血路管(10)流入此时开放的净化器(11),待充满血浆、约10分钟,开始放出血浆,经出口管路(13)流出,同步向净化器(12)灌注血浆,在净化器(11)内的血浆将近流完时,再次开始灌注血浆,此时净化器(12)开始放出血浆,两个并联的净化器(11)和(12)交替进行。如表示图1中的血液分离器(3)的内部结构的图2,血液分离器(1)的内腔(2)的管壁上有很多微孔(3),多核巨细胞(4)不能滤过微孔(3)而被阻留在内腔(2),从而可被清除,能通过微孔(3)的中、小体积的单个血细胞(5)及血浆进入外腔(6),然后经出口(7)流出,进而经图1所示的血浆分离器(8)分离出血细胞和血浆。如表示图1中的血浆分离器(8)的内部结构的图3,血浆分离器(1)的内腔(2)的管壁上有很多微孔(3),不能通过微孔(3)的单个血细胞(4)经具有可开关阀门的血细胞出口(8)流出,进入图1所示的血细胞出口管路(14);能通过微孔(3)的血浆及其化学成分(5)进入血浆分离器外腔(6),然后经血浆流出口(7)、图1所示的血浆泵(9)和血路管(10)进入净化器。如表示图1中净化器(11)和(12)内部结构的图4,当含有HIV(1)的血浆进入净化器时,其中的HIV(1)分别被固定在琼脂凝胶(6)中的巨噬细胞(2)、CD4+T细胞(4)结合成巨噬细胞吞噬体(3)、CD4+T细胞结合物(5),被结合后的HIV不再往下移动,另外未被结合的较大体积的HIV又被因浓度更高而微孔更小的下层琼脂凝胶分子筛微孔阻挡在(7)处。被吸附HIV后的净化血浆经图1所示的出口管路(13)与血浆分离器(8)分离的单个细胞在出口管路(14)汇合后经静脉管路(15)汇流。如此净化血液、清除HIV,直至事先设定的血浆循环量(通常为9L),治疗才宣告结束。整个治疗过程均由电脑控制,并可随时检测工作状态,使用方便、自动化和安全。
六、艾滋病净化治疗仪功效的验证
1、血液分离器滤除HIV感染细胞功效的验证
本发明人按照本发明的基本方法,做了如下的简易验证实验:取疾控中心和传染病实验室生物样本库保存的已确诊的艾滋病(AIDS)患者的抗凝全血若干份,分别取数份相同ABO血型的抗凝全血混合成为5例,使血液量足够大,然后委托浙江省医院中心血站按成份输血的血液成份分离方法,经血液成份分离系统分离出白细胞、红细胞、血浆,取白细胞成份按常规离心沉淀,吸弃上清液,以适量的生理盐水悬浮白细胞沉淀,然后加入合适比例的gp120抗体(上海广锐生物科技有限公司),混匀后置37℃反应5分钟,然后以孔径为20~30um的血液成份分离系统分离出大体积的白细胞(称为大白细胞),对滤过的白细胞滤液再进一步以孔径为15~25um的血液成份分离系统分离出中等体积的白细胞(称为中白细胞),滤液中的白细胞为小体积的白细胞(称为小白细胞),分别收集大、中、小白细胞分离悬液,常规离心沉淀,吸弃上清液,以定量移液器分别吸取等量的大、中、小白细胞沉淀,常规方法(机械或细胞裂解液)裂解细胞(如用同种裂解液,需加量相等),离心沉淀后取上清液,然后根据HIV-1p24抗原检测试剂盒(酶联免疫法,上海启发生物科技有限公司)操作,以已知浓度0pg/ml、0.5pg/ml、1pg/ml、2.5pg/ml、5pg/ml、20pg/ml、40pg/ml、80pg/ml的p24抗原作为对照,最低检测限低于5pg/ml,测定范围0~400pg/ml,线性范围0.5pg/ml~80pg/ml,15min内450nm测定吸光度(OD),空白对照校准品吸光度值不高于0.050,0pg吸光度值不高于0.100,1000pg/ml吸光度不低于1.000,当吸光度>0.12时被认为是阳性,检测结果(表1)说明,AIDS患者不同体积大小的白细胞中的HIV-p24含量不同,在大、中、小白细胞中HIV-p24的平均含量分别为275.0pg/ml、196.0pg/ml、126.4pg/ml,其中大、小白细胞中HIV-p24平均含量相差148.6pg/ml,减少了54.4%;在大、中、小白细胞中HIV-P24的总含量分别为1375.0pg/ml、979.9pg/ml、632.1pg/ml,其中大、小白细胞中HIV-p24总含量相差742.9pg/ml,减少了54.3%,经统计学检验,t=2.43,p<0.05。说明AIDS患者体内的大体积白细胞或经gp120抗体作用后而形成的大体积白细胞中含有较高含量的HIV,能通过实施本发明的技术方案被分离清除。
表1 AIDS患者外周血大、中、小白细胞中HIV-p24检测结果(p24:pg/ml)
2、血浆净化器(剂)清除HIV功效的验证
(1)CD4+T细胞株吸附清除HIV功效的验证
为了验证CD4+T细胞株吸附清除HIV的功效,本发明设计了简易的测试方法:取灭菌的2.5×300mm魏氏血沉管5支,分别吸取经离心(1000r/min,5min)沉淀的CD4+T细胞至200mm刻度,接着吸取经100℃溶化后保温在39~41℃备用的0.9%琼脂糖C1-4B,达到约10mm长刻度,置血沉架冷却后,琼脂糖成为半固体,能阻止血沉管内细胞流出但不会阻止小分子的水和化学成份之类的物质通过。另取疾控中心及传染病实验室样本库保存的艾滋病患者的5例血浆,各约10mL,各取9mLAIDS滤前血浆分批次注入血沉管上端空管,待流经血沉管下层的CD4+T细胞层并从血沉管内流出后,收集流出液,称为AIDS滤后血浆。取AIDS滤前血浆和滤后血浆,根据HIV-1p24抗原检测试剂盒(酶联免疫法,上海启发生物科技有限公司)操作,以已知浓度0pg/ml、0.5pg/ml、1pg/ml、2.5pg/ml、5pg/ml、20pg/ml、40pg/ml、80pg/ml的p24抗原作为对照,最低检测限低于5pg/ml,测定范围0~400pg/ml,线性范围0.5pg/ml~80pg/ml,15min内450nm测定吸光度(OD),空白对照校准品吸光度值不高于0.050,0pg吸光度值不高于0.100,1000pg/ml吸光度不低于1.000,当吸光度>0.12时被认为是阳性,检测结果(表1)说明,AIDS血浆滤过含CD4+T细胞的简易净化装置后,部分HIV已被CD4+T细胞吸附,经第1次滤过后,HIV总清除率为22.84%,经第2次滤过后,总清除率为35.31%,经第3次滤过后,总清除率为41.9%。说明随着滤过次数的增加,HIV会被不断地清除,从而达到治疗AIDS目的。
表1 AIDS血浆滤过含CD4+T细胞的简易净化装置前后p24检测结果(pg/ml)
(2)杂交瘤巨噬细胞株吸附清除HIV功效的验证
为了验证杂交瘤巨噬细胞株吸附清除HIV的功效,本发明设计了简易的测试方法:取灭菌的2.5×300mm魏氏血沉管5支,分别吸取经离心(1000r/min,5min)沉淀的巨噬细胞杂交瘤细胞株至200mm刻度,接着吸取经100℃溶化后保温在39~41℃备用的0.9%琼脂糖C1-4B,达到约10mm长刻度,置血沉管冷却后,琼脂糖成为半固体,能阻止血沉管内细胞流出但不会阻止小分子的水和化学成份之类的物质通过。另取疾控中心及传染病实验室样本库保存的艾滋病(AIDS)患者的5例血浆,各约10mL,各取9mLAIDS滤前血浆分批次注入血沉管(简易净化装置)上端空管,待流经血沉管下层的杂交瘤巨噬细胞株层并从血沉管内流出后,收集流出液,称为AIDS滤后血浆。取AIDS滤前血浆和滤后血浆,以人巨噬细胞移动抑制因子(MIF)ELISA检测试剂盒(上海百蕊生物科技有限公司)配对检测,按说明书操作,检测范围为0~800pg/ml,敏感度为1.0pg/ml,可在白色背景下,直接用肉眼观察:反应孔内颜色越深,阳性越强,阴性反应为无色或极浅,依据所呈颜色的深浅,以“+”、“-”号表示。也可测OD值:在ELISA检测仪上,于450nm(若以ABTS显色,则410nm)处,以空白对照孔调零后测各孔OD值,若大于规定的阴性对照OD值的2.1倍,即为阳性。结果如表1,滤前血浆中MIF检测结果均为阴性(或因含量低于检测灵敏度、血浆长期保存致降解等),而滤后血浆中检测结果均为阳性。说明巨噬细胞杂交瘤细胞株在此过程产生了MIF细胞因子。MIF是集细胞因子、生长因子、激素和酶特性于一身的多效能蛋白分子,作为固有免疫和炎症反应的调节因子发挥中枢性的作用,在各种感染和急慢性炎症性疾病中发挥多种免疫功能。在作AIDS血浆滤过简易净化器前后MIF配对检测的同时,本发明还做了HIV-1p24的配对检测,根据HIV-1p24抗原检测试剂盒(酶联免疫法,上海启发生物科技有限公司)操作,以已知浓度0pg/ml、0.5pg/ml、1pg/ml、2.5pg/ml、5pg/ml、20pg/ml、40pg/ml、80pg/ml的p24抗原作为对照,最低检测限低于5pg/ml,测定范围0~400pg/ml,线性范围0.5pg/ml~80pg/ml,15min内450nm测定吸光度(OD),空白对照校准品吸光度值不高于0.050,0pg吸光度值不高于0.100,1000pg/ml吸光度不低于1.000,当吸光度>0.12时被认为是阳性,结果(表2)说明AIDS血浆滤过简易净化装置后,部分HIV已被巨噬细胞杂交瘤细胞株吞噬吸附,滤过后的血浆HIV明显减少,经第1次滤过后,HIV清除率为20.55%,经第2次滤过后,HIV清除率为42.83%,p<0.01,具有明显的效果,说明随着滤过次数的增加HIV会被不断地清除,从而达到治疗AIDS目的。
表1 AIDS血浆滤过含杂交瘤巨噬细胞的简易净化装置前后MIF检测结果(定量:pg/ml)
表2 AIDS血浆滤过含杂交瘤巨噬细胞的简易净化装置前后p24检测结果(p24:pg/ml)
总之,上述简易验证实验表明,已被HIV感染的外周血白细胞易融合成大体积的多核巨细胞或多细胞聚合体,能被本发明的血液分离器分离清除;而血浆中游离的HIV,能被本发明的血液净化剂(杂交瘤巨噬细胞株、CD4+T细胞株、琼脂凝胶微孔)吸附清除。表明以血液分离器和血浆净化器(剂)为关键部件构成的艾滋病净化治疗仪具有显著的清除血液细胞内、外HIV病毒的治疗功效。
- 还没有人留言评论。精彩留言会获得点赞!