电刺激器及应用其的刺激方法及电刺激系统与流程
本发明提供一种电刺激器,尤其指一种对生物体的目标区域进行电刺激的电刺激器,以使其疼痛感降低而不会产生异常感觉。
背景技术:
人体神经主要是作为大脑所发出的指令(电流)的传导路径,其中人体神经具有阈值,而受损神经区域其阈值往往会降低,也因此人体在受损经神区域的部位特别容易感受到不舒适的酸痛感,长久下即形成慢性疼痛病。
临床上,一种连续射频刺激(continuous radiofrequency;简称CRF),也称为电烧,被应用于多种并发症,例如:颈源性头痛、枕神经痛、颈椎损伤、肋间神经痛等疼痛。而连续射频刺激方法,主要是将电烧针插入患部的相关神经组织附近,利用连续高频电刺激所产生的高温,将患部的神经组织烧死。由于此方法是将患部的神经组织烧死,由此使患部于手术后获得止痛效果。然而,因人体自我修复功能被激活时,被烧死的神经组织会自行修复,一旦神经组织自行修复,新增生的神经组织并不会照着原本的神经组织形状生长,乃会在已烧死的神经组织上任意生长而形成神经瘤,当神经瘤形成时,人体神经会更容易被压迫及伤害,进而造成患部疼痛并再覆发,甚至引发更严重的疼痛情形。
技术实现要素:
为达上述目的,依据本发明的一种电刺激器应用于电刺激生物体的目标区域,以使疼痛感降低而不会产生异常感觉。电刺激器包括至少一个电刺激单元。电刺激单元具有至少一个第一电极及至少一个第二电极。电刺激单元接收高频电刺激信号,使第一电极与第二电极产生电场。电场范围涵盖目标区域且电场强度的范围介于100V/m~1000V/m,其中,该高频电刺激信号的频率范围介于200KHz~1000KHz。
在一个实施例中,高频电刺激信号为脉冲式信号,其脉冲频率范围介于0~1KHz。
在一个实施例中,高频电刺激信号的频率范围介于200KHz~450KHz或550KHz~1000KHz。
在一个实施例中,高频电刺激信号的电压范围介于-10V~-1V或1V~10V。
在一个实施例中,高频电刺激信号的电流范围介于2mA~50mA。
在一个实施例中,第一电极与该第二电极之间的距离介于1~7毫米,且该第一电极及该第二电极与该目标区域之间的距离介于0~10毫米。
在一个实施例中,电刺激器以高频电刺激信号阻断目标区域的神经传导。
在一个实施例中,目标区域为脑、脊椎、背根神经节(dorsal root ganglion)和/或脊髓背角(Spinal dorsal horn)。
在一个实施例中,电刺激单元接收低频电刺激信号,低频电刺激信号的频率小于1KHz。
为达上述目的,依据本发明的一种刺激方法,其应用电刺激器以电刺激生物体的目标区域,以使疼痛感降低而不会产生异常感觉。电刺激器具有电刺激单元且电刺激单元具有至少一个第一电极及至少一个第二电极。刺激方法包括以下步骤:设置电刺激单元于目标区域;电刺激单元发出高频电刺激信号;第一电极与第二电极产生电场,电场范围涵盖目标区域且电场强度的范围介于100V/m~1000V/m;以及对目标区域进行电刺激,其中,该高频电刺激信号的频率范围介于200KHz~1000KHz。
在一个实施例中,高频电刺激信号为脉冲式信号,其脉冲频率范围介于0~1KHz。
在一个实施例中,高频电刺激信号的频率范围介于200KHz~450KHz或550KHz~1000KHz。
在一个实施例中,高频电刺激信号的电压范围介于-10V~-1V或1V~10V。
在一个实施例中,高频电刺激信号的电流范围系介于2mA~50mA。
在一个实施例中,电刺激器以高频电刺激信号阻断目标区域的神经传导。
在一个实施例中,目标区域为脑、脊椎、背根神经节(dorsal root ganglion)和/或脊髓背角(Spinal dorsal horn)。
为达上述目的,依据本发明的一种电刺激系统,包括控制器以及电刺激器。电刺激器包括至少一个电刺激单元。电刺激单元具有至少一个第一电极及至少一个第二电极。控制器指示电刺激单元发出高频电刺激信号,使第一电极与第二电极产生电场。电场范围涵盖目标区域且电场强度的范围介于100V/m~1000V/m,以对目标区域进行电刺激,其中,该高频电刺激信号的频率范围介于200KHz~1000KHz。
在一个实施例中,高频电刺激信号的频率范围介于200KHz~450KHz或550KHz~1000KHz。
在一个实施例中,高频电刺激信号的电压范围介于-10V~-1V或1V~10V。
在一个实施例中,高频电刺激信号的电流范围介于2mA~50mA。
附图说明
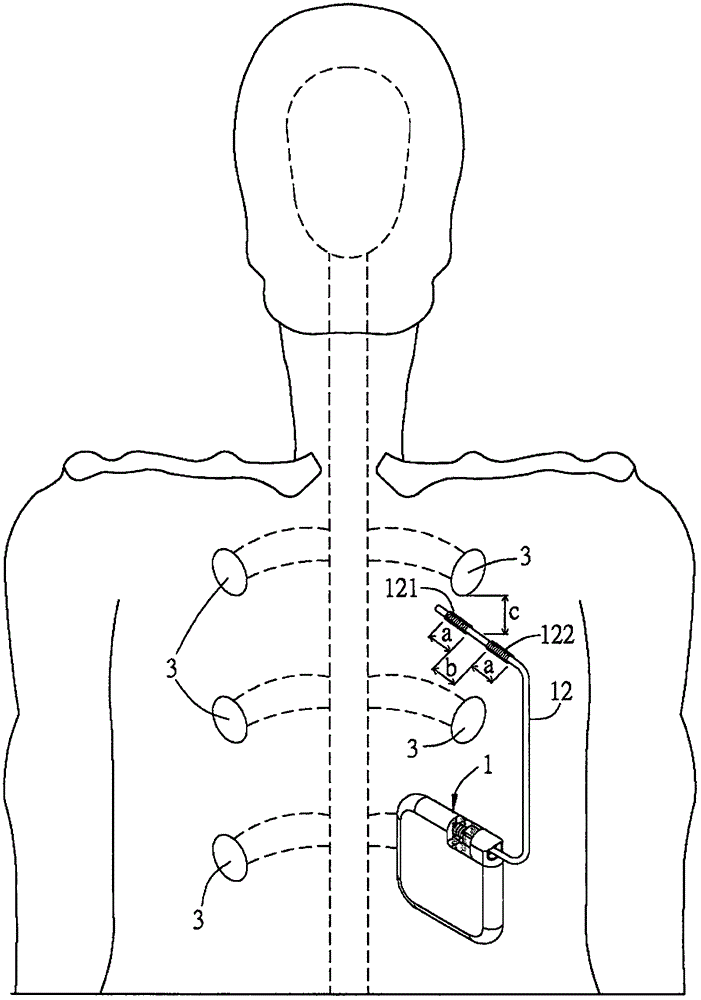
图1A为依据本发明第一实施例的电刺激器应用于背根神经节的实施示意图。
图1B为依据图1A的电刺激器及搭配的控制器的电路方块示意图。
图1C为图1A的电刺激器的电刺激信号为脉冲信号的示意图。
图2A及2B分别为图1A所示的电刺激单元的局部放大示意图。
图3A至图3E及图4A至图4E为本发明电刺激器的电场模拟示意图。
图5A及图5B为本发明电刺激器在不同电极间距及不同电刺激信号频率时,电场仿真示意图。
图6为图1A所示的电刺激器的另一个示意图。
图7及图8为依据本发明其他实施例的电刺激器的形态示意图。
图9~图14为依据本发明所示的电刺激器的其他形态示意图。
图15为依据本发明又一实施例的高频刺激器的应用示意图。
图16为本发明的大鼠足部的疼痛行为测试Von Frey(VF)测试结果。
图17A及图17B分别为本发明的神经电生理测试的控制组及实验组的结果。
具体实施方式
以下将参照相关附图,说明依本发明优选实施例的一种电刺激器及应用其的刺激方法及电刺激系统,其中相同的元件将以相同的参照符号加以说明。
图1A为依据本发明第一实施例的电刺激器应用于背根神经节的实施示意图。请先参考图1A所示,本实施例揭露一种电刺激器1,其应用于电刺激生物体的目标区域,本实施例的目标区域以生物体的背根神经节3为例说明。然于实际应用时,目标区域可例如但不限于应用于电刺激生物体的脑、脊椎、和/或脊髓背角(Spinal dorsal horn)。其中,上述的脊椎特别系指第九节胸椎神经(T9 vertebrae)及第十节胸椎神经(T10 vertebrae)。以下针对电刺激器的各元件组成及应用方式说明之。
为使本方法在实施时的各步骤的相关细节更为清楚明了,以下先清楚介绍电刺激器1及其配合的控制器2的电路结构及相互配合的方式,进而以此为基础,具体说明如何于利用本实施例的电刺激器1针对生物体的目标区域进行电刺激。但是特别需要提出的是,以下所举实施例中的内容仅为方便说明使用,并非用以限制本发明。
图1B为依据本发明第一实施例的电刺激器1及搭配的控制器2的电路方块示意图。请参考图1B所示,电刺激器1通过控制器2进行参数的设定及能量的供给,控制器2并不需要植入生物体,故也称为外部控制器2。以下分别就电刺激器1及控制器2的细部元件,以及其相互之间的关系进行说明。
在本实施例中,电刺激器1包括第一控制单元11以及电刺激单元12。电刺激单元12耦接第一控制单元11。控制器2则包括第二控制单元21、人机接口22以及电源供应单元23。人机接口22耦接第二控制单元21,而电源供应单元23同样耦接第二控制单元21并作为控制器2的电力来源。电源供应单元23可为电池或充电电池,或可为电源适配器,以连接市电提供电力。
在本实施例中,用户可通过控制器2的人机接口22进行操作。在开始前先将控制器2的系统设定值进行初始化,再接着通过人机接口22将所需设定的参数输入到第二控制单元21。本实施例的人机接口22可例如为触控按键、触控面板、实体按键或上述组合,在此并不加以限制。第二控制单元21则指示电源供应单元23供应直流电力给电刺激器1的各元件(特别是电刺激单元12)进行运作。
其中,所称第一控制单元11及第二控制单元21都可由数字电路例如集成电路(IC),或模拟电路来实现,其中集成电路可例如为微处理器(Micro-processor)、微控制器(MCU)、可程序逻辑门阵列(FPGA或CPLD)或特定应用集成电路(ASIC),而本实施例是以微控制器(MCU)为例进行说明,但本发明并不限制。
本实施例的电刺激器1是以其为一种植入式电刺激器为例说明,且所称“植入式”电刺激器指至少部分的电刺激器1的元件植入至个体体内(如:皮下)使用之。但本发明并不限制于实际应用时,电刺激器1可依据患者的症状及需求调整为经皮式电刺激器。在本实施例中,电刺激单元12是供植入至个体内使用,而第一控制单元11则可依设计的需求,而也是植入个体内或是设置于个体之外。当电刺激单元12植入一个体时,其优选植入于与患者疼痛相关的脊神经的背根神经节处。在此所谓的“个体”优选为生物体,其主要包括哺乳类动物,如老鼠、人类、兔、牛、羊、猪、猴、狗、猫等,优选为人类。
进一步针对电刺激单元12的细部结构说明,请参考图1A至图2B所示,电刺激单元12包含具有挠性的导线(lead),导线包括有至少一个第一电极121及至少一个第二电极122,而本实施例是以包括一对电极,即第一电极121为正极及第二电极122为负极作说明。当然,关于电刺激单元12所设置的电极数目,也可以为两组或三组以上,且平均分布设置在电刺激单元12这条导线上。而上述电极是以双极性的方式(bipolar mode)进行操作,以在第一电极121及第二电极122之间形成电场。在本实施例中,第一电极121与第二电极122的材质为金属,例如为铂、银、金或其他具有导电性的金属。第一电极121与第二电极122之间实际上为由与电极电性连接的同轴导线缠绕成线圈(coils or wires)的区域,具体而言,第一电极121及第二电极122设置在电刺激单元12的一端,而电刺激单元12的另一端则具有两个接点作为正极和负极,两个接点与第一控制单元11电性连接或电性耦合。第一电极121及第二电极122分别与致密缠绕的线圈连结,通过线圈而连结至接点,另外,电刺激单元12在第一电极121与第二电极122之外的线圈设有绝缘体120包覆。图2A中,电刺激单元12在电极之间的部分区域,取下绝缘体120,以示意设置在其中的线圈。
而各电极的个别长度a的范围依据实际使用需求而设置,电极长度a介于0.5~6毫米,优选为1~4毫米。其中,所称的第一电极121与第二电极122的个别“长度a”是指未植入时,水平延伸电刺激单元12,电极平行于电刺激单元12的导线长轴延伸方向上的长度尺寸。第一电极121与第二电极122之间的距离b介于1~7毫米,优选为1~4毫米。详细而言,相邻的第一电极121与第二电极122邻近的两端部的优选距离b介于1~4毫米。
而电刺激单元12的第一电极121及第二电极122与所述背根神经节3之间具有距离c,所述距离c的定义为相邻的第一电极121及第二电极122之间的中点与背根神经节3的最短距离。在本实施例中,距离c的范围介于0~10毫米,优选为0~5毫米。其中,当距离c为0毫米时,表示第一电极121及第二电极122之间的中点在投影方向上与背根神经节3相互重合。
请再参考图1C所示,本实施例的电刺激器1所输出的电刺激信号可为连续正弦波、连续三角波或高频脉冲电刺激信号,当为脉冲电刺激信号时,一个脉冲周期时间Tp(pulse cycle time)中包含多个脉冲信号以及至少一段休息的时间,而一个脉冲周期时间为脉冲重复频率(pulse repetition frequency)的倒数,脉冲重复频率(也可简称为脉冲频率)介于0~1KHz,优选介于1~100Hz,而本实施例的电刺激信号的脉冲重复频率为2Hz。另外,一个脉冲周期时间中多个脉冲的持续时间Td(duration time)介于1~250ms,优选介于为10~100ms,本实施例以25ms为例说明。
请再参考图1C所示,在本实施例中,电刺激单元12用于传输高频电刺激信号。该高频电刺激信号是例如由患者(或医护人员)以控制器2进行电刺激频率、刺激周期及刺激强度等参数的设定,再由控制器2输出参数及能量至电刺激器1,经由第一控制单元11指示电刺激单元1所发出之信号。在本实施例中,高频电刺激信号的频率为600KHz,换言之,其刺激周期时间Ts为约1.67μs。
实际应用时,电刺激器可选择使用定电压模式或定电流模式驱动,其中,定电压模式较为安全,然其强度会较为不稳定;定电流模式强度较稳定,但较不安全。模式的选用视电刺激的目标区域而定,例如当目标为背柱(dorsal column)时,选用定电流模式;当目标为背根神经节时,则选用定电压模式。当选用定电压模式驱动时,该高频电刺激信号的电压为固定值,该高频电刺激信号的电流随着第一电极121及第二电极122的位置及电阻改变;反之,当选用定电流模式驱动时,该高频电刺激信号的电流为固定值,该高频电刺激信号的电压随着该第一电极121及第二电极122的位置及电阻值改变。举例而言,在定电压模式时,高频电刺激信号的电压范围可介于-10V~-1V或1V~10V;优选的,本实施例以高频电刺激信号的电压范围为介于10V~-3V或3V~10V;在定电流模式时,高频电刺激信号的电流范围则可介于电流范围介于2mA~50mA,优选的范围则介于4~30mA。
此外,高频电刺激信号的频率范围则介于200kHZ~1000KHz,优选介于200KHz~250KHz、250KHz~350KHz、350KHz~450KHz、450KHz~550KHz、550KHz~650KHz、650KHz~750KHz、750KHz~800KHz、或800KHz~1000KHz。其中,当选用的频率范围介于200KHz~450KHz时,可于较低的频率操作,故所产生生物热的风险低,具有较安全的优势;反之,当选用的频率范围介于550KHz~1000KHz,则所形成的电场密度较大,其电刺激效果较好。另外,也可通过调整持续时间Td的长短,以调整电刺激量与生物热产生时的散热时间,例如当刺激强度较低时,可以增加持续时间Td以连续刺激,而若使用高频率与高强度进行电刺激时,则可以减少持续时间Td,以增加散热时间。
进一步而言,当电刺激单元12接收到高频电刺激信号,会进一步使电刺激单元12的第一电极121及第二电极122产生电场。配置第一电极121及第二电极12与背根神经节3之间的距离介于距离c的范围内,进而使得第一电极121及第二电极122所产生的电场涵盖背根神经节3,换言之,使该电场覆盖于背根神经节3的周围,以对目标的背根神经节3进行低强度、低温度之高频电刺激,以在不破坏背根神经节3其神经组织细胞情况下,抑制背根神经节3中产生生物分子,同时可降低该背根神经节3区域的阈值,进而降低此目标背根神经节3区域的神经传导能力,达到阻断神经传导的效果,并有效降低病患的神经疼痛感的功效。
此外,更重要的是,应用本实施例的电刺激器进行电刺激可有效地降低目标部位的疼痛感,而不会产生异常感觉,进而使长期受到疼痛困扰的患者可接受有效且不会产生过多不适感的电刺激疗法;优选地,通过本实施例的电刺激器进行电刺激,可维持约1周的效果,换言之,可阻断神经传导达约1周的功效,进而降低患者接受电刺激疗法的频率,使患者无须频繁地进行刺激,从而提升患者接受的意愿,此细节可参照后面实验例所揭露的,在此先不赘述。
请参考图3A至图3D所示,本发明可通过调整第一电极121与第二电极122的电极长度a、第一电极121与第二电极122之间的距离b,或第一电极121及第二电极122与背根神经节3之间的距离c,由此调整电场的场形。以电刺激信号的电压为5V、频率500KHz、距离c为5mm为例,令第一电极121与第二电极122的电极长度a及距离c都为固定(a=1mm;c=5mm),当第一电极121与第二电极122之间的距离b较小时(b=2mm),如图3A的电场模拟图所示,其电场只可涵盖在欲刺激的背根神经节3周围(电场强度为100V/m~1000V/m);当第一电极121与第二电极122之间的距离b较大时(b=4mm),则如图3B所示,其电场的场形空间分布也被拉大且可完全涵盖在欲刺激的背根神经节3周围(已画出的电场强度范围为100V/m~1000V/m);相对的,越接近第一电极121与第二电极122的电磁场其电场强度相对越强。如图3C所示,其为图3A的电场场形图中,再加上较高电场的场形分布图,使得电场强度分布成为100V/m~5000V/m,由图中可知,只要电极所设置的位置离待刺激的目标区域够近(距离c介于0~10mm),均可受到电场的影响,且愈高的电场强度分布愈靠近电极的表面。接着,请看图3D与图3E,图3D与图3C不同的地方在于第一电极121与第二电极122的电极长度a,图3D中电极长度a改为2mm,由图3D中则可看出电极变长,则电场场形的空间分布也有稍微变大;图3E与图3D不同的地方则在于,在固定了第一电极121与第二电极122的电极长度a(均为2mm)后,电极间的距离b则改为6mm,随着电极间的距离b变大,则电场场形的空间分布也是随着变大。
其次,再比较不同电压对于电场场形的空间分布的影响。请参照图4A至图4C所示,其以固定电刺激信号的频率为500KHz、第一电极121与第二电极122的电极长度a、及电极间距离b、与待刺激的目标区域距离c都为固定时(a=2mm;b=2mm;c=5mm),不同电压对于电场场形的空间分布的影响(图4A的电压为3V、图4B的电压为5V、图4C的电压为10V)。由图中可发现,随着电压的增强,电场场形的空间分布也随着增大。
接着请同时比较图4B及图4D、图4E,其以电刺激信号的电压(5V)、第一电极121与第二电极122的电极长度a、及电极间距离b、与待刺激的目标区域距离c都为固定时(a=2mm;b=2mm;c=5mm),不同电刺激信号的频率对于电场场形的空间分布的影响(图4D的电刺激信号频率为200KHz、图4B的电刺激信号频率为500KHz、图4E的电刺激信号频率为800KHz)。由图5B中可发现,由于弧长4mm附近是距离电刺激单元最近的点,所以具有最强的电场强度,且随着电刺激信号频率的增加,电场场形的空间分布也是随着增大。故由图3A至图4E可知,在本实施例中,所述电场强度的范围可介于100V/m~5000V/m,优选地400V/m~5000V/m。
请同时参考图5A及图5B所示,其以图2B中示意的待刺激目标物(圆形背根神经节3)的径长5mm,第一电极121与第二电极122的电极宽度a为1mm、距离c为5mm、输入电压为5V时,待刺激目标物面对电极侧上不同的弧长位置(横轴以圆形左侧的切线为弧长0mm的起点)的电场强度大小。图5A是进行不同频率的电刺激时(200KHz、600KHz以及1000KHz);图5B则比较不同电极间距b(b为2、3、4、5、6mm)时所对应的电场强度。由图5A中可看出,电刺激信号的频率愈高,则电场的强度也较高,电场场形分布就越大,举例来说,在电刺激信号频率1000KHz情况下,目标区域的电场强度最高可有400V/m;而在电刺激信号频率200KHz时,目标区域的电场强度最高却不到300V/m。由图5B则可看出,在电极间距b为4mm~6mm左右,电场有最大强度。
为使电刺激单元12在植入生物体后能够发挥其最佳的电刺激效果,本实施例的电刺激器1更具有低频模式以协助医师在进行植入手术后,可确认电极的位置是否不正确。详细而言,在低频模式下,电刺激单元12可发出低频电刺激信号,该低频电刺激信号的频率介于0.1Hz~1KHz,且此低频电刺激信号的脉冲宽度介于10μs~500μs。电刺激单元12通过发出低频电刺激信号,并侦测对应的肌肉是否有跳动情形,以确认所植入的电刺激单元是否有脱落或错位的情形产生。
请参考图2A及图6所示,在本实施例中,电刺激单元12呈直线状,然此非限制性的,关于电刺激单元12的形状也可如后面实施例所描述,而非本发明限制性的。
本实施例所应用的电刺激器1为主动式电刺激器,其第一控制单元11与电刺激单元12共同植入至生物体的目标区域,换言之,第一控制单元11与电刺激单元12都植入于生物体的皮下位置,或是第一控制单元11与电刺激单元12一体成型后,植入于皮下。通过第一控制单元11电性耦接于生物体外部的控制器2,可接收来自第二控制单元21的参数信号及电能,从而使电刺激单元12可针对生物体的目标区域进行电刺激。
然需说明的是,本发明所提供的电刺激器并不以上述的电刺激器1为限,在其他实施例中,主动式电刺激器也可实施为如图7的电刺激器形态。本实施例的电刺激器1a与前述实施例的电刺激器1具有实质上相同的元件,且第一控制单元11a与电刺激单元12a分别植入生物体表皮S之内(皮下)的位置。不同的地方在于,本实施例的电刺激器1a的第一控制单元11a为整合在电刺激单元的软性电路板,且同样可接收来自生物体外部的第二控制单元(图未示)的参数信号及电能,并发出电刺激信号从而使电刺激单元12a可针对生物体的背根神经节3进行电刺激。本实施例的电刺激器1a可缩小植入至皮下的装置的体积,降低生物体(患者)的负担。
或者,本发明的电刺激器也可选用如图8的形态。如图8所示,本实施例的电刺激器1b为被动式电刺激器,其与前述实施例之电刺激器1不同的地方在于,电刺激器1b的第一控制单元11b整合于设置在生物体表皮S之外(皮外)的控制器2b中,故植入的电刺激器1b并未具有控制单元。而电刺激单元(lead)11b的尾部有软性电路板且位于深度不深的皮下(例如深度小于5cm),以通过未植入于皮内的外部控制器2b发送电刺激信号给电刺激单元11b,从而使电刺激单元12b可针对生物体的背根神经节3进行电刺激。
关于本案的电刺激单元的形态,并不以上述的电刺激单元12为限。请参考图9、12、13所示的另一个实施例,本实施例的电刺激单元12c呈环状,且电刺激单元12c包括至少两个第一电极121及至少两个第二电极122。其中,第一电极121与第二电极122以间隔交错方式排列设置(如图12所示);另外,第一电极121与第二电极122也可以非交错方式依序排列(如图13所示)。由电刺激单元12的第一电极121及第二电极122所产生电磁场围绕涵盖在欲刺激的背根神经节3周围(如图14所示),以对欲刺激的背根神经节3进行低强度、低温度的高频电磁刺激;相对的,越接近第一电极121与第二电极122的电场强度相对越强。
请参考图10所示,所述的电刺激单元12d可呈螺旋状,且电刺激单元12d配置有至少两个第一电极121及至少两个第二电极122,而本实施例以电刺激单元12d包括两个第一电极121及两个第二电极122为例说明。本实施例并不限制第一电极121与第二电极122的排列,第一电极121与第二电极122以交错方式排列或非交错方式排列,且第一电极121与第二电极122以螺旋状围绕背根神经节3配置。由第一电极121及第二电极122所产生电场以螺旋状围绕并涵盖目标背根神经节3的周围,以对目标背根神经节3进行低强度、低温度的高频电刺激。
请参考图11所示,在本实施例中,电刺激单元12e呈弧状,且电刺激单元12e设有至少两个第一电极121及至少两个第二电极122,而本实施例以电刺激单元12e包括两个第一电极121及两个第二电极122为例说明。本实施例并不限制第一电极121与第二电极122的排列,第一电极121与第二电极122以交错方式排列或非交错方式排列,且第一电极121与第二电极122围绕背根神经节3配置。由第一电极121及第二电极13所产生电场围绕并涵盖目标背根神经节3的周围,以对目标背根神经节3进行低强度、低温度的高频电刺激。
请参考图15所示,本实施例的电刺激单元12f呈片状(平板状),且电刺激单元12f设有多个第一电极121及多个第二电极122,该些第一电极121与该些第二电极122以数组方式间隔排列。同样地,由第一电极121及第二电极122所产生电场围绕并涵盖目标背根神经节3的周围,以对目标背根神经节3进行低强度、低温度的高频电刺激。
接下来将以实验例代表说明本发明的电刺激器应用于刺激背根神经节的实际操作方式及效果。然需注意的是,以下的说明是用来详述本发明以使此熟习该项技术者能够据以实现,但并非用以限定本发明的范围。
实验例1:大鼠足部的疼痛行为测试-Von Frey(VF)测试
采用SD大鼠(Sprague-Dawley rats,BioLASCO,Taiwan co.,Ltd.;Taiwan),每只重约275至350克,提供自台湾新光医院中央实验室动物中心。将SD大鼠的第五腰椎神经进行神经结扎手术(Spinal nerve ligation,SNL),待疼痛行为发展稳定数日并符合临床疼痛发展模式后,植入本发明之电刺激单元,并开始进行高频电刺激。本实验例依据介入不同电刺激措施分成控制组(N=3)与实验组(N=7),实验组在手术后持续观察疼痛行为达7天,待疼痛行为稳定后进行每周一次、每次5分钟,共3次高频电刺激疗程,并观察其疼痛行为测试反应,其结果请参考图16所示。
如图16所示,在控制组疼痛行为在第3天趋于稳定直到第29天,Von Frey疼痛压力阈值测试都小于5g(介于1.72±0.39g~4.85±1.31g);而在实验组方面,接受高频电刺激(第7天,D7)以前其疼痛行为与控制组相当,同样约于第3天呈现疼痛稳定状态,但在接受第一次(D7)高频电刺激后对Von Frey疼痛压力阈值有提升的现象,尤其在D8(9.85±1.56g)、D10(9.0±1.68)都与控制组(D8:4.73±1.47g;D10:4.85±1.31g)有差异,且实验组压力阈值耐受度提高达约10g左右、疼痛压力阈值增加至约是控制组的2.08倍左右,而疼痛缓解效果会渐趋衰减直到第二次接受高频电刺激(实验组D14:4.53±1.08;控制组D14:2.98±1.44)。在第二次(D14)接受高频电刺激后的隔天(实验组D15:8.12±1.65;控制组D15:1.81±0.53,疼痛压力阈值差异约4.49倍),仍有同第一次接受高频电刺激的效果存在,第三次(D21)接受高频电刺激后隔天疼痛行为反应仍旧良好(实验组D22:9.17±1.93;控制组D22:2.73±0.57,疼痛压力阈值差异约3.36倍)。明显地,在每一次接受高频电刺激后其疼痛都能立即缓解、并与控制组有疼痛压力阈值上的差异,即证实在植入本发明的电刺激单元后,每周接受一次高频电刺激5分钟,能达到短时间疼痛缓解的效果。
实验例2:神经电生理测试
将SD大鼠分成实验组与控制组,实验组(图17B)接受5分钟的高频电刺激,而控制组(图17A)无接受任何电刺激,两组接受同样条件的坐骨神经大电流刺激(2.5T,C response threshold),以诱发同侧脊髓背角出现明显的A反应(对应A-fiber)和C反应(对应C-fiber)。在介入措施(高频电刺激5分钟或暂停纪录5分钟)之前,预先量测30分钟(18 samples,100 seconds interval)的基准值(Baseline)。当施与介入措施后,即每隔30分钟进行一次坐骨神经大电流刺激,并持续纪录达2个小时,两组分别产生五个实验波型。控制组及实验组的结果分别显示于图17A及图17B。
本实验于接受高频电刺激5分钟的大鼠,将每30分钟的神经反应平均值对准90ms点后,比较各组个别时间的差异。请参考图17A及图17B,将每30分钟为区间的平均线复合起来比较。其中,图17A所显示的控制组在个别时间的曲线并无明显的差异;相比控制组的结果,由图17B的实验组则可明显看出经过高频电刺激反应后C-component相比Baseline具有大幅度的缩减。
详细而言,本实验例利用大电流对周边坐骨神经的刺激,当成疼痛的出入源,其神经传导会将信号通过A-fiber跟C-fiber传导到被根神经节与脊髓的背根神经,通过神经传导的电生理量测,由此观察介入高频电刺激措施对神经的反应。由图17B的结果显示,诱发的C response在接受高频电刺激后,随着时间显著的下降,其C-component面积(强度)也随着时间显著的缩减,代表主司痛觉(由其是慢性、不易定位的痛觉)的C-fiber轴索在传导上有所改变,而高频电刺激阻断或抑制了某些fiber上神经元的信号传导,进而使疼痛能够缓解,甚至完全阻断。
但是,上述详细说明是针对本发明的可行实施例的具体说明,该实施例并非用以限制本发明,而凡未脱离本发明技艺精神所为之等效实施或变更,均应包含在本案的专利范围中。
- 还没有人留言评论。精彩留言会获得点赞!